糖基化是植物生长发育过程中次生代谢产物修饰的关键生化过程,通过引入糖基单元显著改变母体化合物的理化特性与生物功能,赋予其全新的药理特性[1]。植物源糖苷化合物在食品医药工业具有广泛的应用。例如,淫羊藿的主要活性被成分淫羊藿苷因其具有调节骨骼代谢和抗肿瘤等活性被广泛应用于保健品和医药行业[2];罗汉果甜苷作为具有多种药用价值的零卡路里甜味剂被广泛应用于食品领域[3];熊果苷因其具有调节糖代谢及抗炎等活性被广泛应用于食品和医药行业[4]。绝大多数植物次级代谢产物的糖基化反应是由尿苷二磷酸依赖型的糖基转移酶(uridine diphosphate-glycosyltransferase,UGT)催化的。近年来,随着基因组、转录组测序技术的快速发展,很多参与植物黄酮类[5]、苯乙醇苷类[6]、萜类[7]化合物合成的糖基转移酶功能得到验证,但是海量的糖基转移酶有待发掘鉴定,底物多样性和宽泛性的研究仍待拓展。
短管兔耳草(Lagotis brevituba Maxim),一种玄参科兔耳草属多年生植物,多分布于我国青海及西藏地区。兔耳草中富含多种黄酮糖苷类、苯乙醇苷类及环烯醚萜苷类化合物,具有抗衰老、抗菌、消炎及神经系统保护等多种生理活性,是民间的传统藏药[8-10]。
本研究基于短管兔耳草转录组数据,分析UGTs候选基因,通过逆转录-聚合酶链式反应(reverse transcription-polymerase chain reaction,RT-PCR)克隆,构建原核表达载体,在大肠杆菌中实现异源可溶表达,利用体外酶促反应测试对黄酮类、苯乙醇苷类和萜类等化合物的活性。本研究发现了一个新的糖基转移酶,UGT命名委员会命名为UGT74DU1,可以识别槲皮素、山奈酚、芦丁、异槲皮苷等复杂黄酮类化合物C-7-OH,反应生成系列黄酮-7-O-葡萄糖苷,进一步识别C-4′-OH生成相应的黄酮-4′,7-O-双葡萄糖苷;同时也可以催化苯乙醇苷类化合物毛蕊花糖苷C-3″-OH的糖基化,具有一定的底物宽泛性。因此,UGT74DU1可能是一种潜在的多功能糖基转移酶,可以催化芳香族化合物的糖基化,在功能性食品开发和创新药物研发中具有一定的应用价值。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株和质粒
大肠杆菌(Escherichia coli)DH5α 感受态及BL21(DE3)感受态购自南京诺维赞生物科技有限公司;质粒pET28a、pGro7由实验室保存。
1.1.2 培养基及常用溶液
蛋白纯化缓冲液A(50 mmol/L Tris-HCl pH值为7.5,20 mmol/L咪唑,100 mmol/L NaCl),蛋白纯化缓冲液B(50 mmol/L Tris-HCl pH值为7.5,500 mmol/L咪唑,100 mmol/L NaCl),蛋白纯化缓冲液 C(50 mmol/L Tris-HCl pH值为7.5,100 mmol/L NaCl),LB培养基(g/L):氯化钠10,酵母粉5,蛋白胨10。
1.1.3 实验试剂
一步克隆试剂盒,南京诺维赞生物科技有限公司;高保真DNA聚合酶及反转录试剂盒,北京全式金生物技术有限公司;质粒小量提取试剂盒及增强型胶回收试剂盒,北京天根生化科技有限公司;限制性内切酶,赛默飞世尔科技有限公司;4%~12%蛋白预制胶及缓冲液,常州天地人和生物技术有限公司;卡那霉素、氯霉素,Sigma公司;IPTG,北京索莱宝生物科技有限公司;兔耳草mRNA,实验室保存;山奈酚,上海阿拉丁生化科技股份有限公司;槲皮素标准品,天津百倍生物科技有限公司;异槲皮苷和芦丁标准品,上海吉至生化科技有限公司;毛蕊花糖苷、原人参二醇、熊果酸、薯蓣皂苷元和尿苷二磷酸葡萄糖(uridine diphosphate glucose,UDPG),上海源叶生物科技有限公司。
1.2 仪器与设备
GET3XG PCR仪、5810R冷冻离心机,Eppendorf生命科学公司;HWS-24电热恒温水浴锅,上海博迅实业有限公司;JY600C E6090核酸电泳仪、JY600C E6006垂直电泳仪,Bio-Rad公司;102112588超声细胞破碎仪,宁波新芝生物技术有限公司;UV-1800紫外分光光度计、LC-20AD高效液相色谱仪,岛津仪器有限公司;AKTA purifier10蛋白纯化仪,Cytiva公司;Bruker Metabolic Profiler高效液相色谱-质谱联用/核磁共振(nuclear magnetic resonance,NMR)仪,北京布鲁克科技有限公司。
1.3 实验方法
1.3.1 基因克隆及表达载体构建
以兔耳草总mRNA为模板,使用全式金反转录试剂盒,按操作说明书进行反转录合成cDNA第一链;使用Snapgene软件设计特异性引物(实验中所用引物如表1所示),以cDNA液为模板,PCR扩增目的基因,目的基因进行胶回收;将胶回收产物与pET28a载体同源重组;重组后的载体转入E.coli 感受态细胞DH5α 中。利用菌落PCR筛选阳性克隆,将筛选得到的正确的单菌落扩大培养提质粒;质粒交由金唯智公司测序验证。
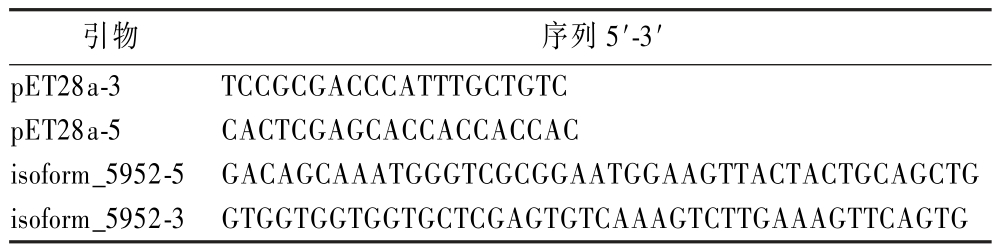
表1 实验中所用的引物
Table 1 Primers used in this experiment
1.3.2 生物信息学分析
利用 Expasy (https://web.expasy.org/cgi-bin/protparam)预测UGT74DU1蛋白质的理化性质。将UGT74DU1与10条已知功能的葡萄糖基转移酶基因序列导入MEGA 11.0软件,采用默认参数进行多序列比对,并基于比对结果选择邻接法(neighbor-joining,NJ)构建系统发育树,以探究其进化关系。将比对后的氨基酸序列提交至ESPript在线工具(https://espript.ibcp.fr/ESPript/cgi-bin/ESPript.cgi),使用默认参数进行保守性分析,以鉴定关键功能域及保守位点,揭示UGT74DU1的潜在催化特征。
1.3.3 UGT74DU1异源表达及纯化
将测序正确的重组质粒及含伴侣蛋白的质粒(pGro7)共转化至E.coli 感受态细胞BL21(DE3),并涂布到含50 mg/L卡那霉素和25 mg/L氯霉素的LB平板上。从平板上挑取单克隆置于装有5 mL(含50 mg/L卡那霉素及25 mg/L氯霉素)LB液体培养基的试管中,在37 ℃、220 r/min条件下培养12 h,即为种子液。将1 mL种子液转接至50 mL(含50 mg/L卡那霉素及25 mg/L氯霉素)LB液体培养基,于37 ℃、220 r/min下培养至OD600值为0.6~0.8;加入终浓度为0.1 mmol/L的异丙基-β-D-硫代半乳糖苷和10 mmol/L的阿拉伯糖,转16 ℃、220 r/min下诱导培养20~22 h。诱导完成后,菌液于4 ℃、4 000 r/min、20 min离心并收集菌体,用10 mL Buffer C重悬菌体,超声破碎10 min,于4 ℃、12 000 r/min、20 min离心并收集上清液,即粗酶液。取20 μL粗酶液加5 μL 5 × loading buffer沸水浴10 min,使蛋白变性,使用SDS-PAGE检测重组蛋白表达情况。使用蛋白纯化仪对重组蛋白进行纯化。将收集后的菌体用蛋白纯化缓冲液C重悬,超声破碎混悬液,离心后取上清液,将上清液过滤膜;使用蒸馏水冲洗蛋白纯化系统及柱子后,再用Buffer A平衡;将上清液上样至蛋白纯化柱中,流速设置为1 mL/min;上样完成后,进行蛋白洗脱(洗脱梯度为0~100%缓冲液B,40 min),并收集洗脱液;通过BCA试剂盒测定蛋白浓度。
1.3.4 体外酶反应
首先称取1.51 mg槲皮素、1.43 mg山奈酚、3.05 mg芦丁、2.32 mg异槲皮苷、2.3 mg原人参二醇、2.07 mg薯蓣皂苷元和2.28 mg熊果酸分别溶于100 μL二甲基亚砜(dimethyl sulfoxide,DMSO) 溶剂中配制成50 mmol/L的不同底物母液,用无菌水分别配制浓度为100 mmol/L的MgCl2及UDP-葡萄糖母液。100 μL反应体系中含1 μL底物母液,即DMSO的终体积分数1%,在1.5 mL离心管中进行体外酶反应,反应体系如表2所示,将体系中各组分混匀,30 ℃金属浴反应2 h后,加入100 μL甲醇终止反应,将反应液放置通风橱挥干后加等体积甲醇萃取,12 000 r/min离心10 min,将上清液过滤膜并取20 μL进行HPLC检测。
表2 UGT74DU1纯酶反应体系
Table 2 The reaction system of UGT74DU1

1.3.5 HPLC及LC-MS分析
使用配有SPD-M40 PDA检测器的Shimadzu LC-20 AD HPLC系统和SilGreen C18 column色谱柱(4.6 mm ×250 mm,5 μm)、乙腈(B)和0.1% (体积分数)甲酸(A)作为流动相,对酶反应后的上清液进行HPLC分析,其中进样量为20 μL,流速为1 mL/min,异槲皮苷、芦丁和毛蕊花糖苷的分析梯度为:5% B,5 min;5%~ 13.2% B,13 min;18%~ 21.6% B,25 min;100% B,7 min;5% B,7 min;槲皮素和山奈酚的分析梯度为5% B,5 min;5%~52.5% B,20 min;100%B,8 min;5% B,7 min;原人参二醇和熊果酸的分析梯度为:5%~100% B,20 min;100% B,5 min;5%B,8 min;薯蓣皂苷元的分析梯度为:70%~100% B,15 min;100% B,5 min;70% B,5 min;LC-MS分析检测条件与HPLC分析检测条件相同。
1.3.6 糖基化产物的制备及纯化
为了鉴定糖基化产物结构,本研究进行了糖基化产物的制备分离。通过扩大酶反应体系(1 mL缓冲液C中含1 mg纯化后的UGT74DU1蛋白、5 mmol/L UDP-葡萄糖和1 mmol/L槲皮素或毛蕊花糖苷)进行产物制备,反应条件为30 ℃下5 h,并用等体积甲醇终止反应。反应液离心后,将上清液置于35 ℃的旋转蒸发仪中浓缩,并用水溶解。利用半制备液相色谱(配有SPD-20 A检测器的Shimadzu LC-6 AD系统和Shim-pack PREP-ODS(H)色谱柱)进行糖基化产物的分离。以乙腈(B)和0.1% (体积分数)甲酸(A)为流动相,流速设置为4 mL/min;槲皮素洗脱梯度条件为:5% B,5 min;5%~52.5% B,20 min;100% B,8 min;5% B,7 min;在254 nm波长下收集糖基化产物;毛蕊花糖苷洗脱条件为5% B,5 min;5%~13.2% B,13 min;18%~21.6% B,25 min;100% B,7 min;5%B,7 min;在312 nm波长下收集糖基化产物。分别取1.5 mg纯化后的糖基化产物溶于氘代甲醇中,使用NMR确定其化合物结构,从而确定UGT74DU1对于槲皮素及毛蕊花糖苷的催化功能。
2 结果与分析
2.1 基因克隆与蛋白表达情况
从短管兔耳草的cDNA中克隆得到基因isoform_5952,通过Expasy预测UGT74DU1蛋白质的理化性质,结果显示isoform_5952编码区全长1 413 bp,可编码470个氨基酸,蛋白质分子质量约为52.6 kDa,理论等电点(isoelectric point,PI)为5.53。将测序验证后的候选基因isoform_5952全长序列提交至NCBI,登录号为PV340610,UGT命名委员会将其命名为UGT74DU1。
在E. coli BL21(DE3)中进行蛋白表达,通过SDS-PAGE检测发现几乎看不到可溶性蛋白表达(图1-a)。利用伴侣蛋白质粒pGro7优化其蛋白表达后,从蛋白胶图上可以看到55 kDa附近有特异性蛋白条带(图1-b),且与预期的重组蛋白大小相近,表明伴侣蛋白显著提高了UGT74DU1的可溶性表达。
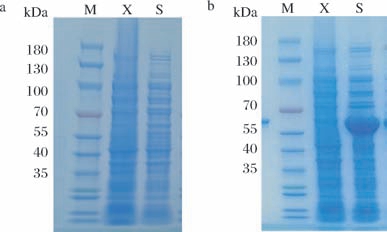
图1 SDS-PAGE检测UGT74DU1在E.coli BL21(DE3)菌株中的表达
Fig.1 SDS-PAGE analysis of UGT74DU1 expressed in E.coli BL21(DE3)
a-未优化蛋白表达;b-优化后蛋白表达
M-蛋白Marker;X-pET28a空载体上清液;S-pET28a-UGT74DU1上清液。
2.2 序列比对及系统进化分析
氨基酸序列比对结果显示UGT74DU1与已报道的UGTs序列相似性较低,不足50%(表3)。参与植物次生代谢产物糖基化修饰的UGTs在C端含有44个氨基酸的保守序列,称为PSPG基序(plant secondary product glycosyltransferase motif),该序列被认为是与UDP-糖供体结合的区域,与糖供体的识别相关[11]。UGT74DU1与相似度相对较高的10条葡萄糖基转移酶PSPG基序比对结果如图2所示,表明UGT74DU1具有典型的葡萄糖基转移酶保守序列,可以识别UDP-葡萄糖作为糖供体。系统发育分析(图3)表明,UGT74DU1与长春花来源的CrUGT74AN3[12]在同一分支上,CrUGT74AN3可以催化黄酮类化合物的C-7-OH、C-4′-OH的葡萄糖基化,推测UGT74DU1可能与CrUGT74AN3的催化功能相似。
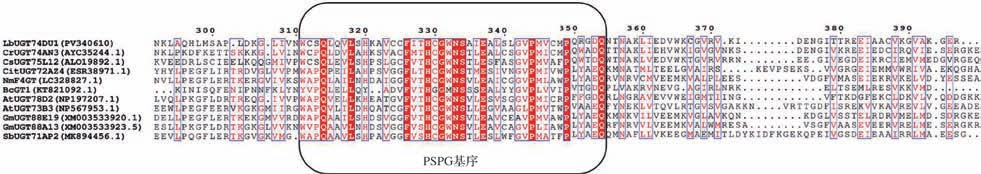
图2 UGT74DU1与10条已鉴定功能的葡萄糖基转移酶的氨基酸序列比对
Fig.2 Amino acid sequence alignment of UGT74DU1 with 10 functionally identified glucosyltransferases
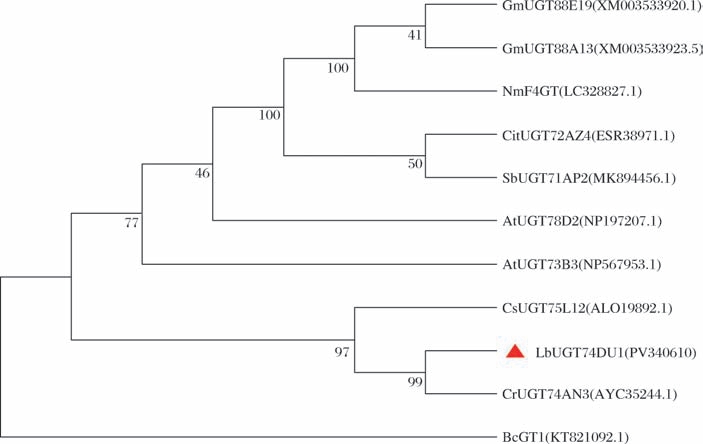
图3 UGT74DU1与10条已鉴定功能的葡萄糖基转移酶系统发育树分析
Fig.3 Phylogenetic tree constructed with UGT74DU1 and 10 functionally characterized glucosyltransferases
表3 UGT74DU1与已鉴定的UGTs氨基酸序列及催化功能对比
Table 3 Comparison of amino acid sequences and catalytic functions between UGT74DU1 and identified UGTs
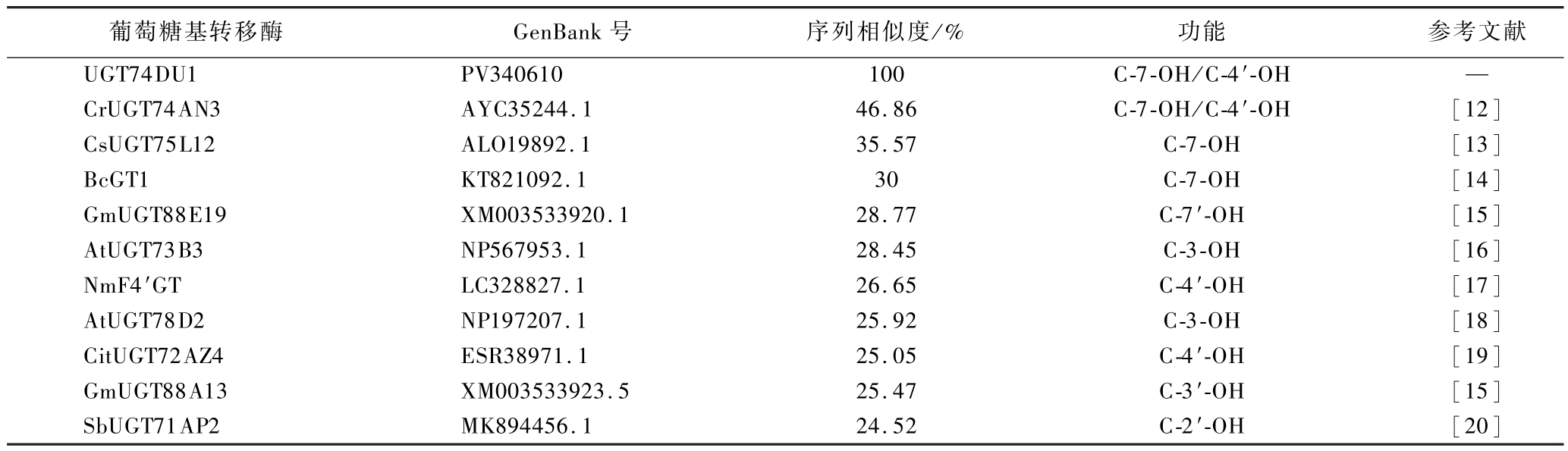
注:—表示无参考文献。
2.3 体外酶促反应结果
本文分别以槲皮素(a)、山奈酚(b)、异槲皮苷(c)及芦丁(d)为底物,以UDP-葡萄糖为糖基供体,进行体外酶反应。HPLC的检测结果显示,UGT74DU1可以催化槲皮素(a)生成2个新峰a1和a2(图4-A);催化山奈酚(b)生成2个新峰b1和b2(图4-A);催化异槲皮苷(c)生成2个新峰c1和c2(图4-B);及催化芦丁(d)生成2个新峰d1和d2(图4-B)。通过LC-MS对新峰产物进行分析,发现a1、b1、c1、d1(图5-A~图5-D)分别在其糖基受体的基础上加了一分子葡萄糖,a2、b2、c2、d2(图5-A~图5-D)分别在其糖基受体的基础上加了两分子葡萄糖,这表明UGT74DU1对多种黄酮类底物具有葡萄糖基化的能力。为进一步确定糖基化的位置及催化顺序,以槲皮素(a)为底物,扩大酶反应体系制备出足量的糖基化产物a1、a2,进行NMR结构鉴定。
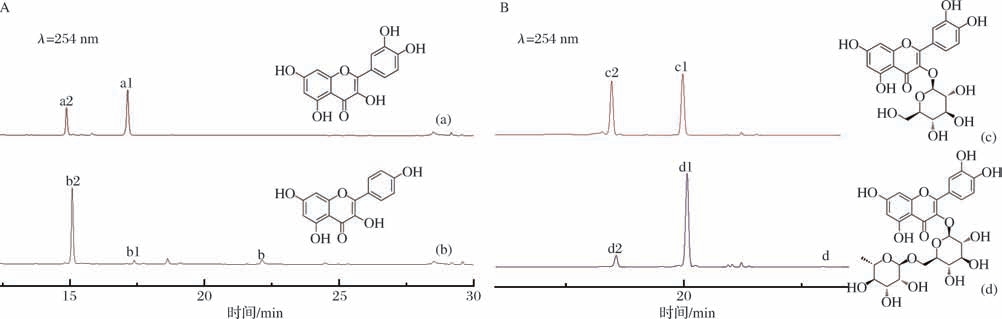
图4 UGT74DU1催化不同底物的HPLC分析
Fig.4 HPLC analysis of the products of UGT74DU1with different substrates
A-槲皮素(a)及山奈酚(b)酶促反应;B-异槲皮苷(c)及芦丁(d)酶促反应
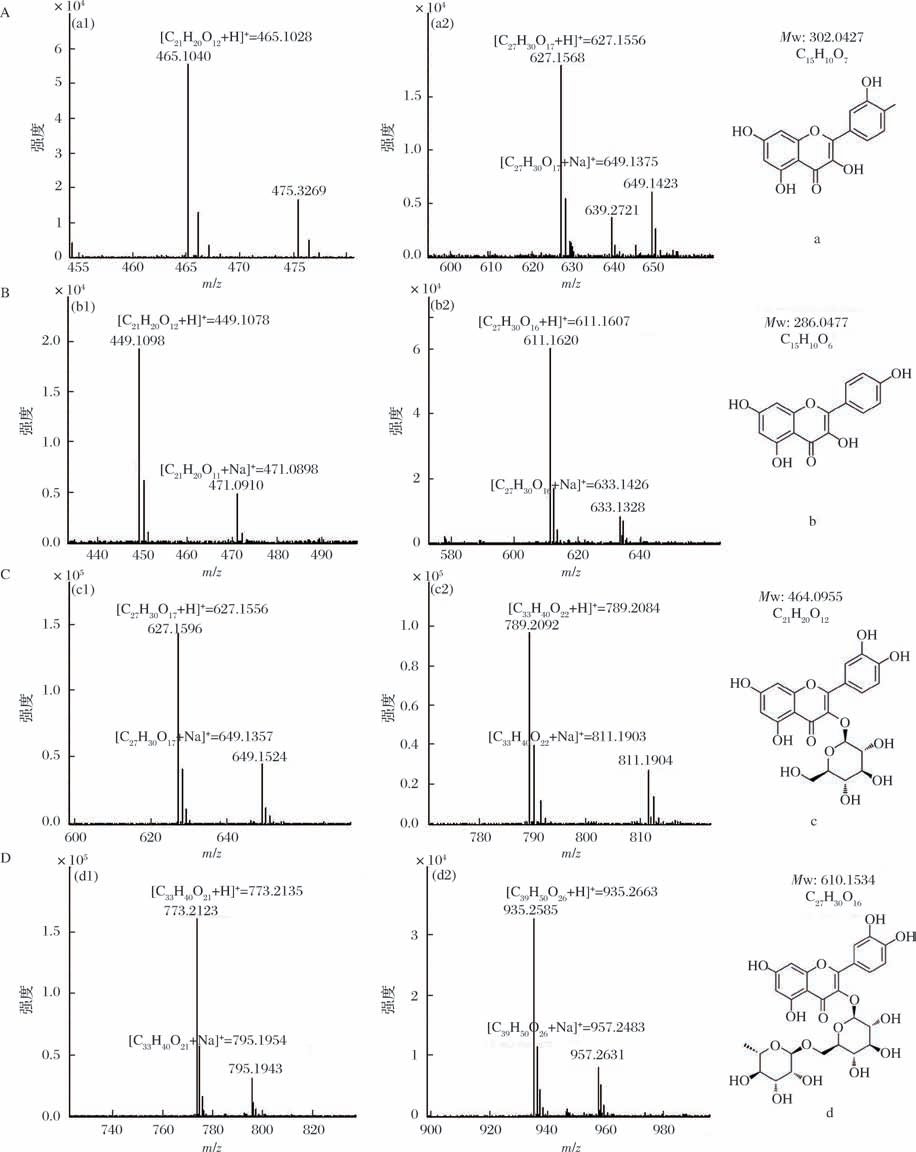
图5 UGT74DU1催化糖苷产物的LC-MS分析
Fig.5 LC-MS analysis of the catalytic products of UGT74DU1
A-槲皮素糖苷a1,a2,槲皮素结构;B-山奈酚糖苷b1,b2,山奈酚结构;C-异槲皮苷糖苷c1,c2,异槲皮苷结构;D-芦丁糖苷d1,d2,芦丁结构
2.4 底物谱分析
为研究UGT74DU1的底物混杂性,分别以苯乙醇苷类化合物毛蕊花糖苷(e),萜类化合物原人参二醇、熊果酸和薯蓣皂苷元(图6-A)为糖基受体,以UDP-葡萄糖为糖基供体,进行体外酶反应。HPLC的检测结果显示,UGT74DU1仅可以催化毛蕊花糖苷(e)生成2个新峰(e1)和(e2)(图6-B)。通过LCMS对新峰产物进行分析,发现e1、e2(图6-C)分别在毛蕊花糖苷的基础上加了一分子葡萄糖,这表明UGT74DU1对苯乙醇苷类化合物毛蕊花糖苷具有葡萄糖基化的能力。
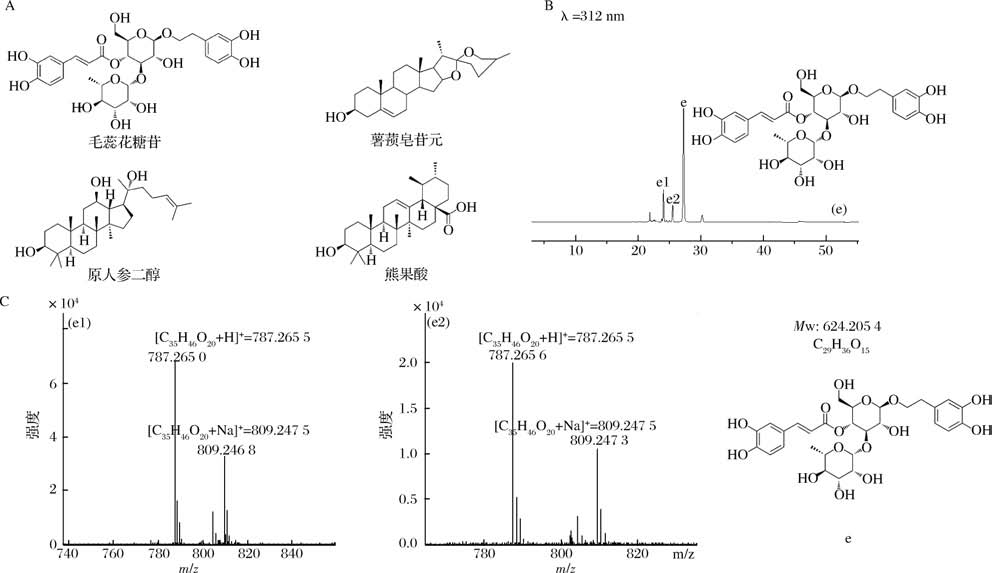
图6 UGT74DU1催化毛蕊花糖苷产物的HPLC及LC-MS分析
Fig.6 HPLC and LC-MS analysis of the glucoside product of verbascoside catalyzed by UGT74DU1
A-底物谱;B-毛蕊花糖苷(e)酶促反应;C-糖苷产物e1,e2,毛蕊花糖苷结构
2.5 糖基化产物NMR鉴定结果
a1的NMR的结果数据:1 H HMR(400 MHz,CD4 OD)δ 7.77(1H,d,J=2.1 Hz,H-2′),7.67(1H,dd,J=8.5,2.1 Hz,H-6′),6.89(1H,d,J=8.5 Hz,H-5′),6.76(1H,d,J=2.1 Hz,H-8),6.47(1H,d,J=2.1 Hz,H-6),5.06(1H,d,J=7.3 Hz,H-1″),3.94(1H,dd,J=12.2,2.1 Hz,H-6″),3.73(1H,dd,J=12.2,5.8 Hz,H-6″);a2的NMR结果数据:1 H HMR(400 MHz,CD4OD)δ 7.79(1H,d,J=2.0 Hz,H-2′),7.75(1H,dd,J=8.7,1.9 Hz,H-6′),7.30(1H,d,J=8.7 Hz,H-5′),6.76(1H,d,J=1.9 Hz,H-8),6.47(1H,d,J=2.0 Hz,H-6),5.06(1H,d,J=7.4 Hz,H-1″),4.91(1H,t,J=13.0 Hz,H-1′″),3.94(1H,dd,J=7.2,4.6 Hz,H-6″),3.74(1H,dd,J=8.4,3.6 Hz,H-6″),3.92(1H,m,H-6′″),3.71(1H,dd,J=21.2,15.4 Hz,H-6′″);e1的NMR的 结果数据:1 H HMR(400 MHz,CD3 OD)δ 7.64 (1H,d,J=15.8 Hz,H-7″),7.54(1H,d,J=1.5 Hz,H-2″),7.20(1H,d,J=8.3 Hz,H-5″),6.87(1H,d,J=8.3 Hz,H-6″),6.69(1H,d,J=1.2 Hz,H-2),6.67(1H,d,J=8.1 Hz,H-5),6.57(1H,d,J=7.8 Hz,H-6),6.39(1H,d,J=15.9 Hz,H-8″),5.21(1H,s,H-1′″),4.93(1H,d,J=9.6 Hz,H-4′),4.81(1H,d,J=7.0 Hz,H-1′″),4.38(1H,d,J=7.8 Hz,H-1′),3.83(1H,t,J=9.2 Hz,H-3'),2.80(2H,t,J=6.7 Hz,H-7),1.10(3H,d,J=6.1 Hz,H-6′″);13C HMR(600 MHz,CD3OD)δ 168.09(C-9″),151.20(C-4″),147.35(C-3″),147.05(C-7″),146.10(C-3),144.64(C-4),131.42(C-1),127.88(C-1″),126.25(C-6″),121.20(C-6),118.06(C-2″),117.39(C-5″),117.05(C-2),116.24(C-5),115.69(C-8″),104.18(C-1′),102.84(C-1′″),81.30(C-3′),72.01(C-8),70.34(C-5′),62.45(C-6′),62.31(C-6″″),36.53(C-7),18.47(C-6′″);e2的NMR的结果数据:1 H HMR(400 MHz,CD3 OD)δ 7.61(1H,d,J=15.9 Hz,H-7″),7.52(1H,d,J=1.6 Hz,H-2″),7.13(1H,d,J=8.1 Hz,H-5″),6.86(1H,d,J=8.3 Hz,H-6″),6.67(1H,d,J=1.5 Hz,H-2),6.62(1H,d,J=7.9 Hz,H-5),6.53(1H,d,J=8.0 Hz,H-6),6.40(1H,d,J=16.0 Hz,H-8′),5.18(1H,s,H-1′″),4.81(1H,d,J=7.1 Hz,H-1″″),4.37(1H,d,J=5.9 Hz,H-1′),2.79(2H,t,J=7.5 Hz,H-7),1.25(3H,d,J=6.2 Hz,H-6‴),13C HMR(600 MHz,CD3 OD)δ 168.97(C-9″),151.21(C-4″),147.07(C-3″),146.65(C-7″),146.14(C-3),144.65(C-4),131.41(C-1),127.94(C-1″),126.26(C-6″),121.27(C-6),118.22(C-2″),117.49(C-5″),117.09(C-2),116.37(C-5),115.88(C-8″),104.29(C-1′),102.73(C-1‴),83.95(C-3′),72.49(C-8),70.04(C-5′),64.65(C-6′),62.47(C-6″″),36.74(C-7),17.87(C-6′″)。将核磁数据与文献中报道的槲皮素-7-O-葡萄糖苷(a1)、槲皮素-4′,7-O-双葡萄糖苷(a2)结构式及核磁数据比较,发现是一致的[21-22];毛蕊花糖苷-3″-O-β-葡萄糖苷(e1)、异毛蕊花糖苷-3″-O-β-葡萄糖苷(e2)的核磁数据与文献报道[23]的数据一致。
由此,确定UGT74DU1可以催化槲皮素的C-7-OH生成产物槲皮素-7-O-葡萄糖苷,进一步糖基化C-4′-OH生成产物槲皮素-4′,7-O-双葡萄糖苷(图7-A);也可以催化毛蕊花糖苷羟基肉桂酰基的C-3″-OH生成毛蕊花糖苷-3″-O-β-葡萄糖苷,毛蕊花糖苷-3″-Oβ-葡萄糖苷的酰基自发迁移后形成异毛蕊花糖苷-3"-O-β-葡萄糖苷(图7-B)。
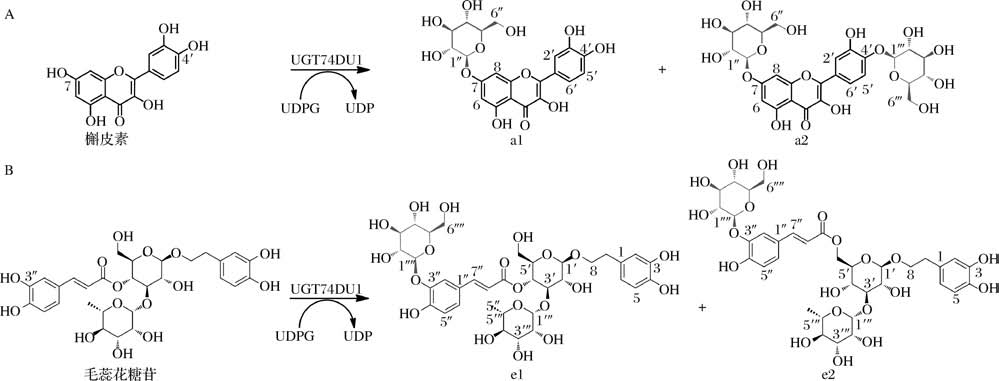
图7 UGT74DU1催化槲皮素和毛蕊花糖苷的糖基化反应
Fig.7 UGT74DU1 catalyzes the glycosylation reaction of quercetin and verbascoside
A-槲皮素反应式;B-毛蕊花糖苷反应式
3 结论与讨论
本研究通过短管兔耳草转录组测序分析、基因克隆,发掘了糖基转移酶UGT74DU1,并借助伴侣蛋白质粒pGro7在E.coli BL21(DE3)中实现可溶性表达。氨基酸序列比对结果显示,UGT74DU1与已报道的UGTs序列相似度较低,约24%~47% (表3),具有植物源葡萄糖基转移酶保守PSPG基序(图2)。体外酶活力验证显示UGT74DU1可以催化槲皮素、芦丁等多种黄酮类化合物的C-7-OH生成黄酮-7-O-葡萄糖苷,并可进一步糖基化C-4′-OH生成黄酮-4′,7-O-双葡萄糖苷,具有相对严格的区域选择性;同时发现其也可以催化苯乙醇苷类化合物毛蕊花糖苷羟基肉桂酰基的C-3"OH糖基化,生成毛蕊花糖苷-3″-Oβ-葡萄糖苷,具有一定的底物宽泛性。在数据库已鉴定功能的UGTs中,本研究克隆的UGT74DU1与长春花来源CrUGT74AN3[12]的氨基酸序列相似性最高,约46.86%,CrUGT74AN3对黄酮类的C-7-OH和C-4′-OH具有一定的区域选择性,优先催化C-7-OH,随后催化C-4′-OH生成4′,7-O-双葡萄糖苷;与酸枣来源的ZjOGT3[24]的序列同源性约39.07%,ZjOGT3先识别类黄酮C-4′-OH,然后识别C-7-OH生成4′,7-O-双葡萄糖苷。已鉴定功能的植物UGTs中可以连续催化C-7-OH和C-4′-OH生成4′,7-O-双葡萄糖苷的UGTs相对较少,UGT74DU1的鉴定为后续深入探究UGTs催化黄酮糖苷类合成反应的区域选择性机制提供了新的案例参考。
近年来,随着植物次生代谢研究的深入,以及基因组、转录组测序技术的发展,大量参与植物天然产物生物合成的糖基转移酶被成功鉴定,极大地丰富了植物糖基转移酶元件库以及行业对植物代谢多样性的认识。本研究首次从短管兔耳草中克隆鉴定一条新的葡萄糖基转移酶UGT74DU1并初步探究了其催化底物谱,为黄酮糖苷及苯乙醇糖苷类的生物合成提供了一种可供选用的酶元件。
[1]JONES P,VOGT T.Glycosyltransferases in secondary plant metabolism:Tranquilizers and stimulant controllers[J].Planta,2001,213(2):164-174.
[2]WANG Z,WANG D,YANG D,et al.The effect of icariin on bone metabolism and its potential clinical application[J].Osteoporosis International,2018,29(3):535-544.
[3]GUO Q H,SHI M K,SARENGAOWA,et al.Recent advances in the distribution,chemical composition,health benefits,and application of the fruit of Siraitia grosvenorii[J].Foods,2024,13(14):2278.
[4]MISHRA P,AHSAN F,MAHMOOD T,et al.Progress of arbutin from dietary supplement to advanced medicine[J].eFood,2024,5(6):e70013.
[5]WANG Z L,WANG S,XU Z,et al.Highly promiscuous flavonoid 3-O-glycosyltransferase from Scutellaria baicalensis[J].Organic Letters,2019,21(7):2241-2245.
[6]YANG Y H,WU Y N,ZHUANG Y B,et al.Discovery of glycosyltransferases involved in the biosynthesis of ligupurpuroside B[J].Organic Letters,2021,23(20):7851-7854.
[7]JIAN X,SUN Q Y,XU W T,et al.Engineering the substrate specificity of UDP-glycosyltransferases for synthesizing triterpenoid glycosides with a linear trisaccharide as aided by ancestral sequence reconstruction[J].Angewandte Chemie (International Ed.in English),2024,63(48):e202409867.
[8]中国科学院西北高原生物研究所.藏药志[M].西宁:青海人民出版社,1991:447.Northwest Institute of Plateau Biology,Chinese Academy of Sciences.Tibetan Medicine Record[M].Xining:Qinghai People’ s Publishing House,1991:447.
[9]YUAN X,WEN H X,CUI Y L,et al.Phenolics from Lagotis brevituba Maxim[J].Natural Product Research,2017,31(3):362-366.
[10]YANGB L,HOU Q,HU F,et al.Total flavones derived from Lagotis brevituba Maxim reduce the levels of inflammatory cytokines in cerebral cortex and hippocampus of Alzheimer’s disease mice[J].Chinese Journal of Cellular &Molecular Immunology,2016,32(7):881-885.
[11]ROSS J,LI Y,LIM E,et al.Higher plant glycosyltransferases[J].Genome Biology,2001,2(2):REVIEWS3004.
[12]HUANG W,ZHANG X L,LI J H,et al.Substrate promiscuity,crystal structure,and application of a plant UDP-glycosyltransferase UGT74AN3[J].ACS Catalysis,2024,14(1):475-488.
[13]DAI X L,SHI X X,YANG C L,et al.Two UDP-glycosyltransferases catalyze the biosynthesis of bitter flavonoid 7-O-neohesperidoside through sequential glycosylation in tea plants[J].Journal of Agricultural and Food Chemistry,2022,70(7):2354-2365.
[14]CHIU H H,HSIEH Y C,CHEN Y H,et al.Three important amino acids control the regioselectivity of flavonoid glucosidation in glycosyltransferase-1 from Bacillus cereus[J].Applied Microbiology and Biotechnology,2016,100(19):8411-8424.
[15]YIN Q G,SHEN G A,DI S K,et al.Genome-wide identification and functional characterization of UDP-glucosyltransferase genes involved in flavonoid biosynthesis in Glycine max[J].Plant and Cell Physiology,2017,58(9):1558-1572.
[16]LIM C E,AHN J H,LIM J.Molecular genetic analysis of tandemly located glycosyltransferase genes UGT73B1 UGT73B2,and UGT73B3,in Arabidopsis thaliana[J].Journal of Plant Biology,2006,49(4):309-314.
[17]OKITSU N,MATSUI K,HORIKAWA M,et al.Identification and characterization of novel Nemophila menziesii flavone glucosyltransferases that catalyze biosynthesis of flavone 7,4′-O-diglucoside,a key component of the blue metalloanthocyanins[J].Plant and Cell Physiology,2018,59(10):2075-2085.
[18]KIM B G,SUNG S H,AHN J H.Biological synthesis of quercetin 3-O-N-acetylglucosamine conjugate using engineered Escherichia coli expressing UGT78D2[J].Applied Microbiology and Biotechnology,2012,93(6):2447-2453.
[19]LIAO B,LIU X J,LI Y J,et al.Functional characterization of a highly efficient UDP-glucosyltransferase CitUGT72AZ4 involved in the biosynthesis of flavonoid glycosides in Citrus[J].Journal of Agricultural and Food Chemistry,2025,73(9):5450-5464.
[20]WANG Z L,DU X Q,YE G,et al.Functional characterization,structural basis,and protein engineering of a rare flavonoid 2′-Oglycosyltransferase from Scutellaria baicalensis[J].Acta Pharmaceutica Sinica B,2024,14(8):3746-3759.
[21]BONACCORSI P,CARISTI C,GARGIULLI C,et al.Flavonol glucoside profile of southern Italian red onion (Allium cepa L.)[J].Journal of Agricultural and Food Chemistry,2005,53(7):2733-2740.
[22]LI C,ROY J K,PARK K C,et al.pH-promoted O-α-glucosylation of flavonoids using an engineered α-glucosidase mutant[J].Bioorganic Chemistry,2021,107:104581.
[23]YAN Y R,MO T,HUANG W Q,et al.Glycosylation of aromatic glycosides by a promiscuous glycosyltransferase UGT71BD1 from Cistanche tubulosa[J].Journal of Natural Products,2022,85(7):1826-1836.
[24]WANG Z L,WEI W Q,WANG H D,et al.Functional characterization,structural basis,and regio-selectivity control of a promiscuous flavonoid 7,4′-di-O-glycosyltransferase from Ziziphus jujuba var.spinosa[J].Chemical Science,2023,14(16):4418-4425.