作为浓香型白酒的糖化发酵剂和生香剂,中温大曲是以小麦为主要原料,经过粉碎过筛、加水拌合、踩制成型、入房培菌和出房贮藏等工艺制成[1]。研究表明,中温大曲内部蕴藏着复杂的微生物体系,包括细菌、霉菌和酵母菌等核心功能菌群[2]。细菌能够代谢产生蛋白酶、淀粉酶、糖化酶以及脂肪酶等多种酶,进而为白酒风味的形成提供多种生香物质;霉菌分泌的糖化酶、液化酶和蛋白酶能分解酿酒原料中的淀粉和蛋白质大分子物质,能够丰富白酒中的芳香类物质含量;酵母菌则将酒曲中淀粉等物质分解产生糖类,为参与发酵的微生物提供营养物质,同时主导乙醇的生成并协同细菌产香[3]。酒曲功能菌群能够产生丰富的酶系和风味物质并进一步影响酒曲品质和酒体质量,因此深入解析中温大曲的微生物多样性是研究酒曲功能菌群、优化酒曲品质以及提升酒体质量的重要基础。
随着分子生物学技术的飞速发展,研究者们逐渐采用更为精准高效的第三代测序技术——单分子实时(single molecule real-time,SMRT)测序技术研究酒曲微生物多样性,该技术可精准解析微生物16S rRNA基因和内转录间隔区(internal transcribed spacer,ITS) 区域全长序列,测序准确率为99.99% 以上[4]。基于PacBio SMRT测序技术,HAN等[5]对来自四川、山东、安徽、江苏和湖南省份的中温大曲细菌多样性进行了研究,发现粘质沙雷氏菌(Serratia marcescens)、鸡葡萄球菌(Staphylococcus gallinarum)和地衣芽孢杆菌(Bacillus licheniformis)是优势细菌属,平均相对含量分别为20.14%、17.41%、9.97%;CAO等[6]探讨了凤香型大曲曲皮微生物的组成,发现优势种为B. licheniformis、直杆糖多孢菌(Saccharopolyspora rectivirgula)、橙色嗜热子囊菌(Thermoascus aurantiacus)、阿姆斯特丹曲霉(Aspergillus amstelodami)和扣囊复膜酵母(Saccharomycopsis fibuligera),平均相对含量分别为43.25%、35.05%、76.51%、10.81%、8.88%;XIANG等[7]对比分析了太原和随州地区清香型低温大曲的微生物群落结构,结果显示明串珠菌属(Leuconostoc)和魏斯氏菌属(Weissella)分别在太原和随州地区样品中显著富集,且血红热放线菌(Thermoactinomyces sanguinis)和T. aurantiacus 等嗜热菌群在随州地区大曲中显著富集。因此,使用PacBio SMRT测序技术能够高效解析酒曲中复杂的微生物多样性,并为大曲微生物研究提供详细且精准的数据支撑。
本研究以宣城地区中温大曲为研究对象,采用常规理化分析和仿生学手段分析其理化性质和感官品质的差异,使用PacBio SMRT测序和纯培养技术分析其微生物多样性,并深入探究了中温大曲品质与微生物间的相关性,以期深入了解宣城地区中温大曲的品质和微生物多样性,并为该地区酒曲品质的提升和功能菌株的挖掘提供数据支持。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
中温大曲样品:从安徽省宣城市(N30.57°,E118.44°)某酒厂采集中温大曲10块,样品编号为XJ1~XJ10。酒曲的纳入标准是:a)外观呈现灰白或棕色;b)断面呈现灰白或有红、黄菌丝,且菌丝整齐;c)曲皮厚度小于1.0 cm;d)具有中温大曲特有香气。共获得10块大曲,将曲块低温运回实验室,粉碎后-20 ℃保存备用。
1.1.2 试剂
理化指标测定所使用试剂均购自西陇科学股份有限公司;电子舌试剂,实验室自配;TIANamp Soil DNA Kit土壤基因组DNA提取试剂盒,天根生化科技(北京)有限公司;DNA Clean-up Kit DNA产物纯化试剂盒,江苏康为世纪生物科技股份有限公司;T-载体、Sloution Ⅰ、引物27F/1495R,宝生物工程(大连)有限公司;营养琼脂(nutrient agar,NA)培养基、MRS培养基,海博生物技术有限公司。
1.2 仪器与设备
VSA水蒸汽吸附分析仪,美国AquaLab公司;K1100全自动定氮仪,济南海能仪器股份有限公司;NMI20-025V-Ⅰ核磁共振成像分析仪,上海纽迈电子科技有限公司;PEN3电子鼻,德国Airsense公司;SA402B电子舌,日本Insent公司;DG250厌氧工作站,英国Don Whitley公司;Veriti FAST梯度PCR仪,美国ABI公司;Sequel 11测序仪,PacBio公司;R930机架式服务器,美国DELL公司。
1.3 实验方法
1.3.1 理化指标的测定
水分含量、酸度、淀粉含量、发酵力、液化力、糖化力、酯化力、灰分、氨基酸态氮和酒化力参照QB/T 4257—2011《酿酒大曲通用分析方法》进行测定,水分活度使用水蒸汽吸附分析仪进行测定,蛋白质含量使用全自动定氮仪进行测定,水分构成使用核磁共振成像分析仪进行测定。所有理化指标均进行3次重复性实验,取平均值作为最终结果。
1.3.2 感官品质的测定
风味品质分析:称取15.0 g大曲样品于电子鼻样品瓶中密封,室温平衡30 min后,参照CAI等[8]的方法进行电子鼻分析。所有样品平行测试3次,选取49、50、51 s的平均响应值作为最终结果。
滋味品质分析:称取30 g大曲样品于250 mL锥形瓶中,添加120 mL纯水搅拌15 min,以10 000 r/min离心10 min后过滤取上清液备用,参照CAI等[8]的测试方法进行电子舌分析。所有样品平行测试3次,取平均值作为最终结果。
1.3.3 DNA提取、PCR扩增和PacBio SMRT测序
使用DNA提取试剂盒提取大曲样品基因组DNA,使用1.0% 琼脂糖凝胶电泳检测其浓度与纯度。依据WU等[9]所建立的PCR扩增体系和操作流程将检测合格的DNA进行PCR扩增。使用琼脂糖凝胶电泳检测扩增产物质量合格后对其进行纯化,纯化后的产物进行PacBio SMRT测序。
1.3.4 生物信息学分析
使用FLASH合并原始双端读长,并使用Trimmomatic软件去除低质量的短片段序列。基于QIIME(v1.9.0)对序列进行生物信息学分析,即使用UCHIME算法检测并去除嵌合体序列,使用USEARCH(v10.0)将相似度不低于97% 的序列聚类到相同操作分类单元(operational taxonomic units,OTU)[10],在核糖体数据库项目(ribosomal database project,RDP)和UNITE数据库比对代表性OTU序列的分类学地位[11],并计算相同测序深度下细菌和真菌的Chao1指数和Shannon指数。
1.3.5 可培养细菌的分离与鉴定
取10 g中温大曲粉末样品于生理盐水锥形瓶内,置于室温下振荡30 min后,进行10倍梯度的连续倍比稀释操作。取10-4、10-5、10-6 的稀释液均匀涂布于NA培养基和MRS培养基上,分别置于30 ℃倒置培养2 d,37 ℃厌氧倒置培养3 d。挑选不同形态的菌落进行三区划线纯化,3次纯化后使用甘油管藏法将菌株保存于-80 ℃备用。对分离株的DNA进行提取,使用引物27F(5′-AGAGTTTGATCCTGGCTCAG-3′)和1495R(5′-CTACGGCTACCTTG-3′)进行PCR扩增、连接和转化,挑取阳性克隆子进行测序。返回序列于美国国立生物技术信息中心(National Center for Biotechnology Information,NCBI)网站进行比对并构建系统发育树。
1.4 数据处理
使用GraphPad Prism 9.0软件进行小提琴图的绘制,使用Origin 2024软件进行百分比堆积柱状图和条形图的绘制,使用SAS 9.4和Cytoscape 3.5.0软件进行相关性分析网络图的绘制,使用DNAMAN 6.0软件和MEGA 7.0软件进行系统发育树的绘制。
2 结果与分析
2.1 宣城地区中温大曲的理化性质分析
本研究首先对宣城地区中温大曲的理化性质进行了测定,测定结果如表1所示。
表1 宣城地区中温大曲样品的理化性质测定结果
Table 1 Determination results of physicochemical properties of medium-temperature Daqu samples in Xuancheng area
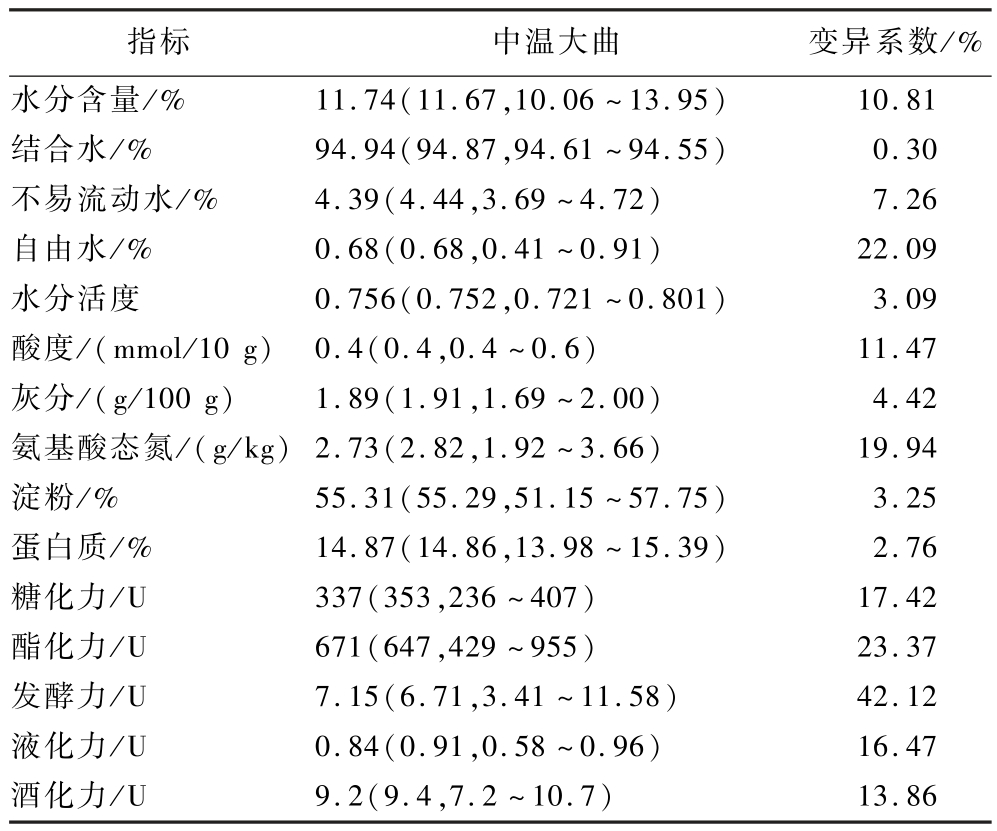
注:数据“11.74(11.67,10.06~13.95)”代表“平均值(中位数,最小值~最大值)”。
由表1可知,宣城地区中温大曲的水分含量为10.06%~13.95%,酸度为0.4~0.6 mmol/10 g,淀粉为51.15%~57.75%,发酵力为3.41~11.58 U,液化力为0.58~0.96 U,糖化力为236~407 U,酯化力为429~ 955 U。根据QB/T 4259—2011《浓香大曲》标准要求合格中温大曲的水分小于14.00%,酸度为0.3~1.5 mmol/10 g,淀粉含量为50.00%~65.00%,发酵力不低于0.20 U,液化力不低于0.20 U,糖化力为100~1 000 U,酯化力不低于150 U,因此纳入本研究的大曲符合中温大曲要求。由表1亦可知,在本研究中水分的存在形式被细分为结合水、不易流动水和自由水3种形态,其中结合水的比例为94.61%~94.55%,不易流动水占比3.69%~4.72%,自由水仅占0.41%~0.91%。纳入本研究中温大曲的水分活度为0.721~0.801,灰分为1.69~2.00 g/100 g,氨基酸态氮为1.92~3.66 g/kg,蛋白质为13.98%~15.39%以及酒化力为7.2~10.7 U。
值得一提的是,本研究计算了各项理化指标的变异系数,发现自由水、氨基酸态氮、糖化力、酯化力、发酵力和液化力这6个指标的变异系数整体偏大,分别为22.09%、19.94%、17.42%、23.37%、42.12%、16.47%。研究表明,自由水作为溶剂和反应介质,在大曲中更容易被温度和湿度等环境条件影响,其含量的变化可能直接影响大曲的微生物活性和发酵过程[12]。氨基酸态氮变异系数偏大可能与贮藏期间大曲中微生物蛋白酶活性变化相关,蛋白酶活性变化影响了蛋白质水解生成氨基酸的速率,导致大曲中氨基酸态氮含量发生波动,变异系数偏高[13]。徐锦等[14]研究发现糖化力与糖化酶、液化力与液化型淀粉酶、酯化力与酯化酶等存在关联,但不同微生物类群生长代谢产生活性酶系及代谢产物不同,进而影响了大曲的发酵性能。因此,对大曲中的微生物类群进行检测和分析是深入了解理化指标的差异及其背后原因的关键。
2.2 宣城地区中温大曲的风味和滋味品质分析
本研究进一步采用电子鼻和电子舌对宣城地区中温大曲的风味和滋味品质进行分析,结果见图1。
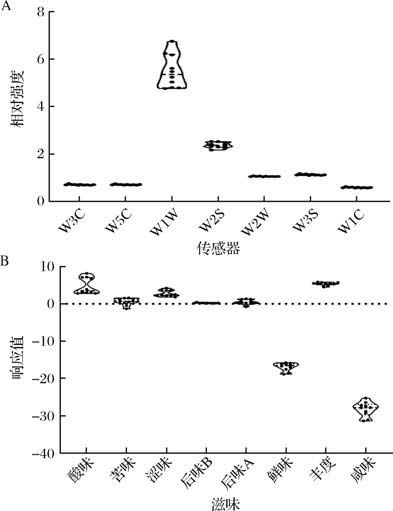
图1 宣城地区中温大曲风味和滋味品质分析
Fig.1 Analysis of flavor and taste quality of medium temperature Daqu in Xuancheng area
注:传感器W3C对氨气、芳香类物质灵敏;传感器W5C对烷烃、芳香类物质灵敏;传感器W1W对有机硫化物、萜类物质灵敏;传感器W2S对乙醇灵敏;传感器W2W对有机硫化物灵敏;传感器W3S对烷烃灵敏;传感器W1C对芳香类物质灵敏;后味B为苦味的回味;后味A为涩味的回味;丰度为鲜味的回味。
由图1-A可知,在风味指标中,传感器W1W和W2S对中温大曲样品响应值较大,而传感器W1C的响应值相对较小,其平均相对强度值分别为5.489、2.376、0.599。由图1-B可知,在滋味指标中,酸味和丰度(鲜味的回味)的响应值较高,鲜味和咸味的响应值较低,平均响应值分别为 4.824、5.352、-16.926、-28.264。上述结果表明,在宣城地区中温大曲中,风味指标中有机硫化物、萜类物质灵敏和乙醇含量较高,芳香类物质含量较低,滋味指标中酸味和丰度(鲜味的回味)物质含量较高,鲜味和咸味物质含量较低。通过计算变异系数发现,滋味指标中传感器W1W的变异系数偏高,变异系数为12.75%,风味指标中酸味、苦味、后味B(苦味的回味)和后味A(涩味的回味)的变异系数偏高,变异系数分别为45.56%、151.22%、37.51%、132.27%。由此可见,宣城地区中温大曲中有机硫化物、萜类物质、酸味、苦味、苦味的回味和涩味的回味物质含量存在明显差异。
2.3 宣城地区中温大曲的微生物多样性分析
微生物的代谢活动可调控酒曲酸度和发酵力等理化指标,还赋予酒曲独特香气、醇厚口感与丰富风味层次,影响酒体品质与风格。因而本研究采用PacBio SMRT测序技术解析了宣城地区中温大曲的微生物多样性。测序结果显示本研究共获得94 561条16S rRNA序列和121 396条ITS序列,被划分为76 958个细菌OTU和22 163个真菌OTU,鉴定为392个细菌属和196个真菌属,567个细菌种和301个真菌种。在测序深度为6 010时,细菌和真菌的Chao1指数平均值分别为399和260,Shannon指数平均值分别为4.93和3.44,且经过Mann-Whitney检验发现,细菌和真菌的Chao1指数和Shannon指数差异均非常显著(P <0.01)。本研究进一步在属和种水平上,对宣城地区中温大曲微生物多样性进行了分析,结果见图2和图3。
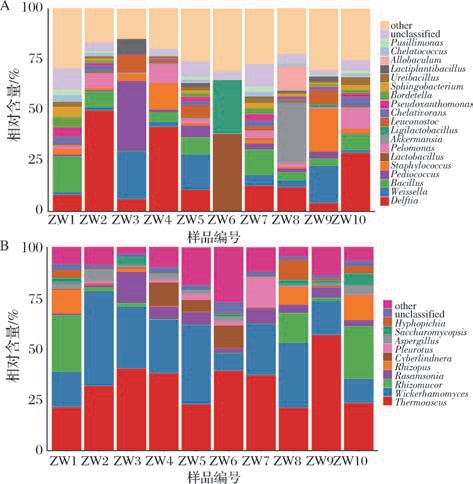
图2 宣城地区中温大曲细菌属和真菌属多样性分析
Fig.2 Diversity analysis of bacterial genus and fungal genus in medium temperature Daqu in Xuancheng area
A-细菌属;B-真菌属
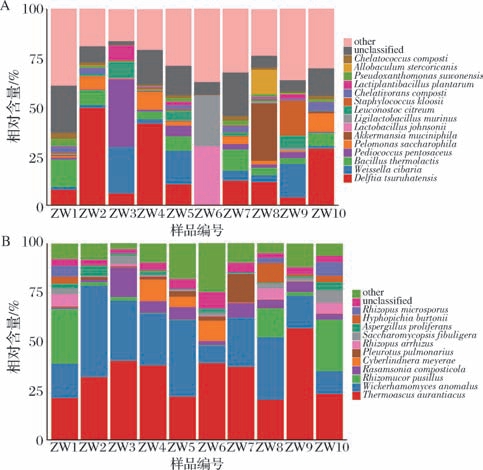
图3 宣城地区中温大曲细菌种和真菌种多样性分析
Fig.3 Diversity analysis of bacterial species and fungal species in medium temperature Daqu in Xuancheng area
A-细菌种;B-真菌种
基于属水平分析可知,宣城地区中温大曲平均相对含量大于1.00%的细菌属有19个,分别为代尔夫特菌属(Delftia)、魏斯氏菌属、芽孢杆菌属(Bacillus)、片球菌属(Pediococcus)、葡萄球菌属(Staphylococcus)、乳酸杆菌属(Lactobacillus)、嗜糖假单胞菌属(Pelomonas)、阿克曼菌属(Akkermansia)、联合乳杆菌属(Ligilactobacillus)、明串珠菌属、根瘤菌属(Chelativorans)、假黄色单胞菌属(Pseudoxanthomonas)、鲍特菌属(Bordetella)、鞘氨醇单胞菌(Sphingobacterium)、尿素芽孢杆菌属(Ureibacillus)、植物乳植杆菌属(Lactiplantibacillus)、异杆菌属(Allobaculum)、螯合球菌属(Chelatococcus)、极小单胞菌属( Pusillimonas),平均相对含量为17.37%、7.47%、6.89%、5.01%、4.93%、3.86%、3.57%、3.13%、2.98%、2.68%、1.79%、1.65%、1.48%、1.42%、1.39%、1.37%、1.29%、1.22%、1.09%。中温大曲平均相对含量大于1.00%的真菌属有10个,分别为嗜热子囊菌(Thermoascus)、威克汉姆酵母属(Wickerhamomyces)、根毛霉属(Rhizomucor)、罗森氏菌属(Rasamsonia)、根霉菌属(Rhizopus)、塞伯林德纳氏酵母属(Cyberlindnera)、侧耳属(Pleurotus)、曲霉属(Aspergillus)、复膜孢酵母属(Saccharomycopsis)、毕赤酵母属(Hyphopichia),平均相对含量分别为 33.30%、25.44%、7.55%、5.12%、3.78%、2.88%、2.34%、2.32%、2.01%、1.8%。LIU等[15]分析了陶融型中温大曲的微生物组成,发现优势细菌属为Bacillus、Lactobacillus、Staphylococcus、Leuconostoc、Weissella 等,平均相对含量分别为38.59%、9.86%、5.02%、2.51%、1.59%;优势真菌属分别为Saccharomycopsis、Thermoascus、Aspergillus、Wickerhamomyce 等,平均相对含量分别为38.61%、24.89%、16.52%、1.67%,该研究结果与本研究相似。
Delftia 最初从土壤、水体等环境样本中分离,该菌属在中温大曲中的存在可能源于原料携带或水源引入,当前对其研究多聚焦于其环境修复潜力,关于其在大曲中的具体功能仍需进一步进行实验验证[16]。 Thermoascus 是酿酒的重要酶源产生菌,可分泌纤维素酶、淀粉酶、蛋白酶等胞外酶,这些酶能分解原料中的淀粉、纤维素和蛋白质等大分子物质,为后续发酵提供可利用的糖类和氨基酸等前体物质,有利于大曲产酒生香[17]。 Wickerhamomyces 在中温大曲中可通过代谢产生乙酸乙酯和己酸乙酯等关键酯类物质,直接提升白酒的香气层次[18]。
种水平分析显示宣城地区中温大曲平均相对含量大于1.00%的细菌种有15个,分别为鹤羽田代尔夫特菌(Delftia tsuruhatensis)、食窦魏斯氏菌(Weissella cibaria)、热酸芽孢杆菌(Bacillus thermolactis)、戊糖片球菌(Pediococcus pentosaceus)、嗜糖假单胞菌(Pelomonas saccharophila)、嗜黏蛋白阿克曼菌(Akkermansia muciniphila)、约氏乳杆菌(Lactobacillus johnsonii)、鼠联合乳杆菌(Ligilactobacillus murinus)、嗜柠檬酸明串珠菌(Leuconostoc citreum)、克氏葡萄球菌(Staphylococcus kloosii)、Chelativorans composti、植物乳植杆菌(Lactiplantibacillus plantarum)、水原假黄单胞菌(Pseudoxanthomonas suwonensis)、粪异杆菌(Allobaculum stercoricanis)、堆肥螯球藻(Chelatococcus composti),平均相对含量分别为17.31%、7.30%、5.72%、5.01%、3.56%、3.13%、3.00%、2.92%、2.52%、2.08%、1.71%、1.37%、1.33%、1.29%、1.21%。中温大曲平均相对含量大于1.00%的真菌种有11个,其中T. aurantiacus、异常威克汉姆酵母(Wickerhamomyces anomalus)、微小根毛霉(Rhizomucor pusillus)、Rasamsonia composticola、玫瑰塞伯林德纳氏酵母(Cyberlindnera meyerae)、肺形侧耳(Pleurotus pulmonarius)、少根根霉(Rhizopus arrhizus)、扣囊复膜孢酵母(Saccharomycopsis fibuligera)、多育曲霉(Aspergillus proliferans)、伯顿丝孢毕赤酵母(Hyphopichia burtonii)、小孢根霉(Rhizopus microsporus),平均相对含量分别为33.05%、25.44%、7.54%、5.12%、2.79%、2.23%、2.06%、2.01%、1.91%、1.89%、1.70%。
基于PacBio SMRT测序技术邓杰等[19]对采集自四川宜宾的中温大曲微生物群落结构进行分析,发现优势细菌种包括清酒乳杆菌(Lactobacillus sakie)、约翰逊不动杆菌(Acinetobacter johnsonii) 和屎肠球菌(Enterococcus faecium) 等,平均相对含量分别为39.32%、18.45%、13.00%;优势真菌种包括热带假丝酵母菌(Candida tropicalis)、奥默柯达酵母(Kodamaea ohmeri) 和丝孢酵母(Trichosporon coremiiforme)等,平均相对含量分别为40.00%、12.80%、10.98%。该结论与本研究存在差异,可能是源于气候环境、原料与工艺和地理生态等多方面因素的综合影响。 D.tsuruhatensis 作为革兰氏阴性好氧菌,在酒曲中的作用尚未被直接报道,但隶属于Delftia 的部分菌株在降解苯胺类污染物时展现出了邻苯二酚2,3-双加氧酶活性,其可能参与大曲发酵中酚类物质的代谢生成醛类风味前体,提升酒体香气物质含量[20]。作为酒曲中的核心耐热真菌,T. aurantiacus 分泌的淀粉酶、纤维素酶、果胶酶和木聚糖酶等酶可以高效分解大曲原料中的淀粉与纤维素,提高原料利用率,同时其展现了水解甘蔗渣、玉米渣和动物饲料的能力,在饲料糖化增效和农业废弃物资源化利用等领域具备显著应用潜力[21-22]。作为非酿酒酵母的典型代表,W.anomalus 菌株能够分泌β-D-葡萄糖苷酶、β-D-木糖苷酶等多种糖苷酶,通过水解前体物质释放芳香成分,显著提升酒体酯香层次[23],在黄酒酿造中该菌株参与发酵可使总酯含量提升15.01%,并新增2-甲基丙酸乙酯等5种特征风味物质,同时降低1-辛烯-3-醇等不良风味物质含量(32.69%)[24]。
2.4 中温大曲优势种与理化性质和感官品质的相关性分析
为深入探究微生物与理化性质和感官品质之间的关系,本研究选取优势种与理化性质和感官品质进行相关性分析,并绘制相关性网络图,结果见图4。
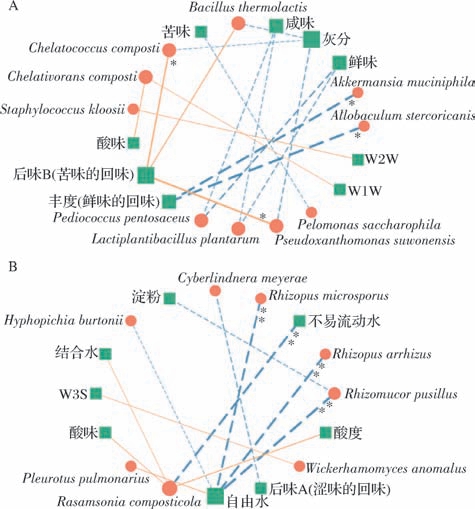
图4 宣城地区中温大曲优势种与理化性质和感官品质的相关性网络图
Fig.4 Network diagram of the correlation between dominant species,physicochemical properties,and sensory quality of medium temperature Daqu in Xuancheng area
注:∗代表P<0.05,表示差异显著;∗∗代表P<0.01,表示差异非常显著。
A-细菌种;B-真菌种
由图4可知,本研究中细菌种与理化性质和感官品质的相关性网络共包括19个节点和16条边,其中丰度(鲜味的回味)与A. stercoricanis 和A. muciniphil呈现显著负相关(P <0.05),相关性系数分别为-0.70和-0.70;后味B(苦味的回味)与C. composti和P.suwonensis 呈现显著正相关(P <0.05),相关性系数分别为-0.61和-0.66。真菌种与理化性质和感官品质的相关性网络共包括16个节点和12条边,其中自由水与R.pusillus、R.arrhizus 和R.microsporus呈现非常显著负相关(P <0.01),相关系数分别为-0.82、-0.80和-0.77;不易流动水与R. composticola 呈现非常显著负相关(P <0.01),相关系数为-0.79。由此可见,在本研究中,与真菌类群相比,细菌类群可能与宣城地区中温大曲的理化性质与感官品质之间的关联程度更加紧密,对该大曲品质所产生的影响更为显著。
2.5 中温大曲可培养细菌的分离鉴定
本研究对中温大曲的可培养细菌进行了分离,共获得62株菌,经过同源性比对发现分离株隶属于9个种,其系统发育树和分布情况如图5所示。
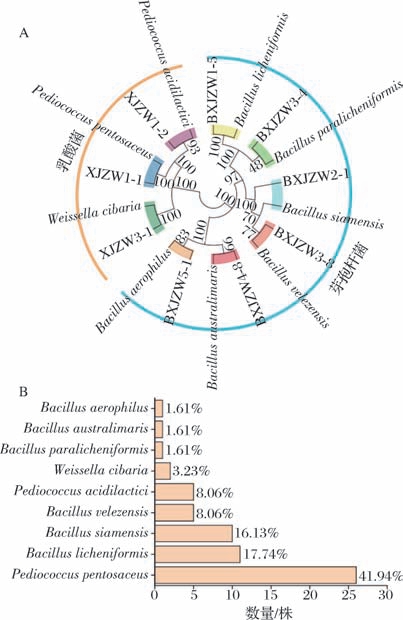
图5 宣城地区中温大曲可培养细菌的系统发育树和分布情况
Fig.5 Phylogenetic tree and distribution of cultivable bacterial in medium-temperature Daqu in Xuancheng area
A-系统发育树;B-分布情况
由图5可知,P. pentosaceus 是宣城地区中温大曲可培养细菌的第一优势细菌种,共有26株被鉴定为P. pentosaceus,占总菌株数量的41.94%。此外,共有11、10、5、5、2、1、1、1株分别被鉴定为B. licheniformis、B. siamensis、贝莱斯芽孢杆菌(Bacillus velezensis)、乳酸片球菌(Pediococcus acidilactici)、W. cibaria、副地衣芽孢杆菌(Bacillus paralicheniformis)、澳洲芽孢杆菌(Bacillus australimaris) 和嗜气芽孢杆菌(Bacillus aerophilus),占比分别为17.74%、16.13%、8.06%、8.06%、3.23%、1.61%、1.61%、1.61%。由此可见,本研究中宣城地区中温大曲的可培养优势细菌为P.pentosaceus、B.licheniformis和B.siamensis。
研究表明,作为乳酸菌的一种,P. pentosaceus 通过发酵葡萄糖产生乳酸降低体系pH值,从而抑制杂菌生长,同时其代谢可产生乙偶姻、乙醛和2,3-丁二酮等挥发性风味物质,能够丰富大曲的香气层次,进一步提升酒体的风味品质[25]。 B. licheniformis 具备分泌淀粉酶、脂肪酶和蛋白酶的能力,可分解大曲中淀粉、脂肪和蛋白质生成还原糖、脂肪酸和氨基酸等风味前体物质[26]。黄晓宁等[27]将其用于强化酿酒,发现能够增强酒醅中乙酸乙酯、苯乙醇和酸类物质的总含量,有助提高酒体中花香及蜂蜜香味。 B. siamensis 具有很强的分泌α-淀粉酶、蛋白酶和纤维素酶的能力,能够加速大曲原料中淀粉和蛋白质的分解,为后续发酵提供更多前体物质[28]。此外,B. siamensis 能够作为饲料发酵剂和添加剂应用于畜禽饲料,有效提高养殖动物的生产性能[29]。
3 结论
宣城地区中温大曲品质符合QB/T 4259—2011《浓香大曲》标准要求,理化指标中自由水、氨基酸态氮、糖化力、酯化力、发酵力和液化力等指标的变异系数偏大,同时大曲中有机硫化物、萜类物质、酸味、鲜味和咸味物质含量存在明显差异。中温大曲中优势细菌种以D.tsuruhatensis 为主,优势真菌种以T. aurantiacus 和W.anomalus 为主,相对于真菌类群,细菌类群与理化性质与感官品质之间的关联程度更加紧密,可培养细菌以P. pentosaceus、B. licheniformis 和B.siamensis 为主。
[1]赵娜,李兆飞,王继华,等.浓香型白酒大曲品质控制的研究现状与展望[J].中国酿造,2025,44(3):15-20.ZHAO N,LI Z F,WANG J H,et al.Research progress and prospect of quality control of strong-flavour Baijiu Daqu[J].China Brewing,2025,44(3):15-20.
[2]黄平,王子豪,郑佳,等.浓香型白酒大曲微生物群落结构研究进展[J].微生物学通报,2023,50(7):3170-3186.HUANG P,WANG Z H,ZHENG J,et al.Research progress in microbial community structure in Nongxiangxing Daqu[J].Microbiology China,2023,50(7):3170-3186.
[3]何小容,张庆,唐家环,等.浓香型白酒大曲发酵过程中主要微生物群系及其作用研究进展[J].中国酿造,2024,43(8):1-6.HE X R,ZHANG Q,TANG J H,et al.Research progress of main microflora and their roles during strong-flavor Baijiu Daqu fermentation[J].China Brewing,2024,43(8):1-6.
[4]ABDE ALIY M,BAYETA S,TAKALE W.Pacific bioscience sequence technology:Review[J].International Journal of Veterinary Science and Research,2022,8(1):27-33.
[5]HAN P J,SONG L,WEN Z,et al.Species-level understanding of the bacterial community in Daqu based on full-length 16S rRNA gene sequences[J].Food Microbiology,2024,123:104566.
[6]CAO D,LV J L,CHU J Y,et al.Relationship between dynamic changes of microorganisms in Qupi and the quality formation of Fengxiangxing Huairang Daqu[J].Frontiers in Microbiology,2024,15:1435765.
[7]XIANG F S,CAI W C,HOU Q C,et al.Comparative analysis of the microbial community structure in light-flavor Daqu in Taiyuan and Suizhou regions,China[J].LWT,2023,177:114599.
[8]CAI W C,XUE Y A,WANG Y R,et al.The fungal communities and flavor profiles in different types of high-temperature Daqu as revealed by high-throughput sequencing and electronic senses[J].Frontiers in Microbiology,2021,12:784651.
[9]WU X Y,JING R X,CHEN W H,et al.High-throughput sequencing of the microbial diversity of roasted-sesame-like flavored Daqu with different characteristics[J].3 Biotech,2020,10(11):502.
[10]TANG J,LIN B,SHAN Y M,et al.Effects of sorghum varieties on microbial communities and volatile compounds in the fermentation of light-flavor Baijiu[J].Frontiers in Microbiology,2024,15:1421928.
[11]DIN A U,AHMAD W,KHAN T M,et al.Metagenomic analysis of liquor starter culture revealed beneficial microbes’ presence[J].Foods,2022,12(1):25.
[12]YAO Y Q,LUO Y,WU M Y,et al.Contribution of moisture to functional microbial succession and functional expression in mediumhigh temperature Daqu[J].Food Bioscience,2025,69:106831.
[13]DENG L,MAO X,LIU D,et al.Comparative analysis of physicochemical properties and microbial composition in high-temperature Daqu with different colors[J].Frontiers in Microbiology,2020,11:588117.
[14]徐锦,冯文聪,朱澳迪,等.不同香型大曲微生态结构及其发酵特性相关性分析[J].食品科学,2024,45(13):104-114.XU J,FENG W C,ZHU A D,et al.Correlation analysis between microecological structure and fermentation characteristics of different aroma types of Daqu[J].Food Science,2024,45(13):104-114.
[15]LIU Y B,WU J Y,LI H D,et al.Combined microbiome and metabolomics analysis of Taorong-type baijiu high-temperature Daqu and medium-temperature Daqu[J].PeerJ,2024,12:e16621.
[16]BRAÑA V,CAGIDE C,MOREL M A.The Sustainable Use of Delftia in Agriculture,Bioremediation,and Bioproducts Synthesis[M].Microbial Models: From Environmental to Industrial Sustainability.Singapore: Springer Singapore,2016: 227-247.
[17]ARBAB S,ULLAH H,KHAN M I U,et al.Diversity and distribution of thermophilic microorganisms and their applications in biotechnology[J].Journal of Basic Microbiology,2022,62(2):95-108.
[18]NIE X,JIA X H,ZHU K X,et al.Dynamic changes and potential correlations between microbial diversity and volatile flavor compounds in Chinese medium-temperature Daqu during manufacturing[J].Molecules,2024,29(20):4851.
[19]邓杰,张曼,周杰,等.2种浓香型白酒大曲中微生物群落结构及功能研究[J].食品科学技术学报,2024,42(4):75-85.DENG J,ZHANG M,ZHOU J,et al.Research on microbial community structure and function in 2 strong flavor Baijiu Daqu[J].Journal of Food Science and Technology,2024,42(4):75-85.
[20]XIAO C B,NING J,YAN H,et al.Biodegradation of aniline by a newly isolated Delftia sp.XYJ6[J].Chinese Journal of Chemical Engineering,2009,17(3):500-505.
[21]ELNAHAS M O,ELKHATEEB W A,DABA G M.All in one Thermoascus aurantiacus and its industrial applications[J].International Journal of Pharma Research and Health Sciences,2020,8(6):3237-3241.
[22]ALMEIDA BATTISTI J,ROCHA G B,RASBOLD L M,et al.Purification,biochemical characterization,and biotechnological applications of a multifunctional enzyme from the Thermoascus aurantiacus PI3 S3 strain[J].Scientific Reports,2024,14:5037.
[23]PADILLA B,GIL J V,MANZANARES P,et al.Challenges of the non-conventional yeast Wickerhamomyces anomalus in winemaking[J].Fermentation,2018,4(3):68.
[24]白永平,廖剑桥,刘克,等.异常威克汉姆酵母的筛选及其对黄酒风味影响的研究[J].食品与发酵科技,2024,60(6):53-61.BAI Y P,LIAO J Q,LIU K,et al.Screening of Wickerhamomyces anomalus and its effect on the flavor of yellow rice wine[J].Food and Fermentation Science &Technology,2024,60(6):53-61.
[25]HU Y Y,ZHANG L,WEN R X,et al.Role of lactic acid bacteria in flavor development in traditional Chinese fermented foods:A review[J].Critical Reviews in Food Science and Nutrition,2022,62(10):2741-2755.
[26]CAI L,CHEN J,GAO J J,et al.Overview of microbials in traditional Chinese fermented soybean products:Origin,functionality and flavor profile[J].Food Reviews International,2024,40(10):3690-3709.
[27]黄晓宁,刘晶晶,韩北忠,等.基于酶学特性筛选大曲来源芽孢杆菌用于强化酿酒[J].食品科学,2021,42(10):218-224.HUANG X N,LIU J J,HAN B Z,et al.Screening of Bacillus from Daqu by enzymatic characteristics to enhance the fermentation of Chinese Baijiu[J].Food Science,2021,42(10):218-224.
[28]林志楷,林文珍.暹罗芽孢杆菌研究进展[J].亚热带植物科学,2019,48(4):391-396.LIN Z K,LIN W Z.Research progress on Bacillus siamensis[J].Subtropical Plant Science,2019,48(4):391-396.
[29]LIU H W,LIU X Y,LIU H Y,et al. Bacillus siamensis improves the immune status and intestinal health of weaned piglets by improving their intestinal microbiota [J].Microorganisms,2024,12(5):1012.