大曲作为中国传统固态发酵工艺的核心糖化发酵剂,在白酒酿造过程中占据不可替代的核心地位。其中,中高温大曲作为浓香型白酒风味塑造的载体,酿造的白酒呈现出“窖香浓郁、醇厚绵甜”的典型风格特征,在白酒市场占据较大消费份额,深受消费者喜爱。然而,传统中高温曲“开放制作、自然富集、堆积发酵、翻转调节”的生产工艺采用单层地面堆积发酵,培养过程中需多次翻曲,所需发酵室数量多,存在劳动强度大、曲房空间利用率低等问题[1]。
为不断优化传统工艺,行业近年来积极探索立体化制曲模式,为大曲产质量提升提供新路径。例如,习酒的“中温架式曲工艺”[2]、尚英等[3]报道的“中高温大曲多层曲坯立体培菌发酵工艺”等,标志着传统制曲工艺正在向标准化、智能化转型迈出关键一步。目前,现有研究大多局限于工艺参数优化,鲜少对立式发酵曲与传统中高温曲理化特性、微生物群落结构及挥发性风味物质组成等方面进行解析。本研究从传统中高温曲与立式发酵曲理化指标、微生物、挥发性风味物质3个维度,解析传统中高温曲与立式发酵曲的质量差异,为制曲工艺优化与升级提供依据。
1 材料与方法
1.1 材料与试剂
样品来源于四川某中高温大曲常规半成品曲房和立式发酵曲曲房,分别在6间立式发酵曲和传统中高温大曲曲房中,从临门、中部、临窗处上、中、下层各抽取1块大曲,粉碎混匀,以每间曲房作为1个独立样品(共12个样品,每组6个),立式发酵曲分别命名为JS1、JS2、JS3、JS4、JS5、JS6,传统中高温大曲分别命名为CT1、CT2、CT3、CT4、CT5、CT6。将每个样品分为3份,其中2份用于挥发性风味物质及理化指标测定,另1份经液氮速冻后送样进行微生物组成分析。
1.2 仪器与设备
7890B-5977B气相色谱-质谱联用仪(GC-MS)、50/30 μm DVB/CAR/PDMS三相萃取头、DB-WAX色谱柱(60 m ×0.25 mm ×0.25 μm),美国安捷伦科技公司;PAL多功能自动进样器,瑞士斯特分析仪器有限公司。
1.3 实验方法
1.3.1 大曲理化指标检测
参照QB/T 4257—2011《酿酒大曲通用分析方法》。测定指标包括水分、酸度、糖化力、酯化力、发酵力、液化力。
1.3.2 大曲微生物群落结构检测
将样品送至天津诺禾致源科技有限公司,基于NovaSeq 6000平台进行高通量测序,扩增区域16SV34 +ITS1-1F。
1.3.3 大曲风味物质检测
大曲前处理方法:准确称取10 g大曲于50 mL离心管中,加入30 mL饱和NaCl,超声浸泡提取1 h,4 000 r/min离心5 min后过滤上清液;将上清液倒入500 mL分液漏斗中,加入50 mL二氯甲烷,振荡萃取5 min,取下层有机液,重复萃取2次合并有机相,再加入5 g无水硫酸钠干燥过夜,氮吹浓缩至1 mL后上机分析。
气相色谱条件:色谱柱为DB-WAX色谱柱,载气为高纯氦气(纯度为99.999%),流速1 mL/min,进样量1 μL;分流比10∶1,进样口温度250 ℃;程序升温:初始温度35 ℃保持5 min,以3 ℃/min升温至90 ℃,保持1 min,再以3 ℃/min升温至150 ℃,保持1 min,再以5 ℃/min升温至190 ℃,保持1 min,最后再以10 ℃/min升温至220 ℃,保持8 min。质谱条件:离子源EI,电离能量70 eV,离子源温度230 ℃,四级杆温度150 ℃,检测方式为选择离子监测(selected ion monitoring,SIM),质谱扫描范围20~300 m/z。
定性定量方法:根据质谱信息,与NIST20谱库进行对比,同时结合保留指数对化合物进行定性分析;采用内标法定量曲样中各挥发性物质的含量,所有曲样重复测定3次。
1.4 数据处理
采用SPSS 20.0软件进行平均值及标准差计算,SIMCA 14.0软件对数据进行正交偏最小二乘判别分析(orthogonal projections to latent structures discriminant analysis,OPLS-DA)及变量投影重要性(variable importance in projection,VIP)排序,使用Origin 2024、联川生物云平台(https://www.omicstudio.cn)、Metware Cloud (https://cloud.metware.cn)作图。
2 结果与分析
2.1 立式发酵曲与传统中高温曲理化差异
大曲的理化特性是评价大曲质量的重要指标。通过单因素方差分析比较立式发酵曲与传统中高温曲的理化指标差异(图1),结果显示,立式发酵曲与传统中高温曲的糖化力、酸度、酯化力、液化力指标无显著差异(P >0.05),但两者的水分与发酵力差异显著(P <0.05)。大曲水分含量主要受制曲温度、发酵条件等因素调控[4]。立式发酵曲表面未使用覆盖物,曲块表皮在发酵过程中快速干燥,可能导致其内部水分难以挥发,故其水分含量显著高于传统中高温曲(P <0.05)。同时,已有研究表明发酵力指标与大曲中酵母菌丰度呈正相关[5],立式发酵曲的立体堆积结构增强了曲块间的空气流通,有利于酵母菌及其他好氧微生物的生长繁殖,这可能是其发酵力指标高于传统中高温曲的主要原因。
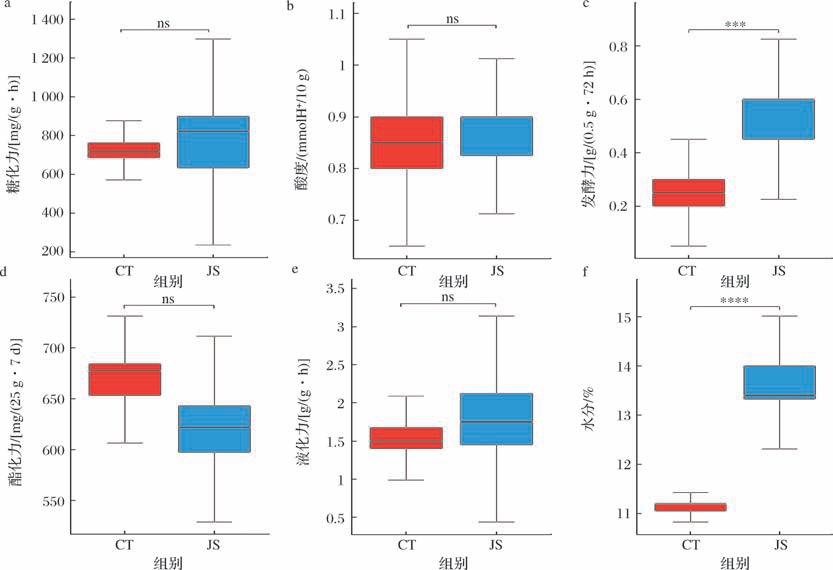
图1 立式发酵曲和传统中高温曲理化指标对比
Fig.1 Comparison of physical and chemical indexes between JS and CT
注:ns表示不显著;∗∗∗表示P <0.001;∗∗∗∗表示P <0.000 1(下同)。
a-糖化力;b-酸度;c-发酵力;d-酯化力;e-液化力;f-水分
2.2 立式发酵曲与传统中高温曲微生物多样性和群落组成及差异
2.2.1 微生物α-多样性和群落组成
立式发酵曲与传统中高温曲细菌observed_species、Chao1指数和ACE指数(abundance-based coverage estimator)存在显著差异(P <0.05),且传统中高温曲中细菌的observed_species、Chao1指数和ACE指数显著高于立式发酵曲(图2-a),说明传统中高温大曲细菌物种丰富度显著高于立式发酵曲。真菌群落方面,如图2-b所示,2组样品的observed_species、Shannon指数、Simpson指数、Chao1指数和ACE指数均无显著差异(P >0.05)。说明传统中高温制曲独特的“堆积发酵、翻转调节”工艺更有利于维持细菌群落的多样性。同时,2种制曲工艺对真菌群落的影响较小,表明真菌群落结构可能受其他因素调控。
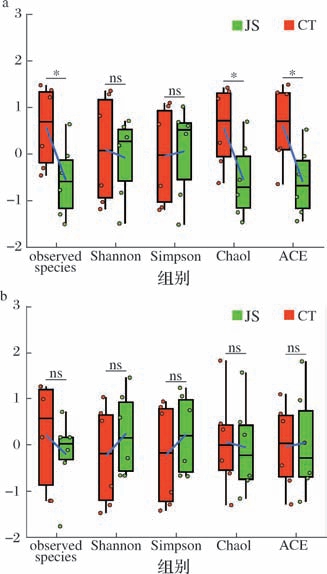
图2 立式发酵曲和传统中高温曲微生物多样性
Fig.2 Differential microbial diversity between JS and CT
注:∗表示P <0.05(下同)。
a-细菌α-多样性;b-真菌α-多样性
基于相对丰度分类统计(高于1% 菌属单独列出,低于1%统一归为“others”),如图3-a所示,立式发酵曲与传统中高温曲细菌群落结构相似,其优势细菌属(相对丰度大于5%)分别有泛菌属(Pantoea)、芽孢杆菌属(Bacillus)、unidentified_Mitochondria。其中,泛菌属在样品JS和CT中相对丰度最高,分别为47.9%、51.3%,该菌属作为浓香型白酒大曲的典型优势菌属[6],与酯类前体成分形成有较强相关性[7]。其次,芽孢杆菌属在样品JS和CT中相对丰度分别为17.2%、6.1%,该菌属普遍存在于各类大曲中,具有突出的产蛋白酶、淀粉酶等水解酶的能力[8-9],倾向于在发酵温度较高的大曲中富集[10],立式发酵曲中较高的芽孢杆菌属相对丰度可能是由于立式发酵曲独特的堆叠式发酵结构,促进了嗜热性芽孢杆菌的富集。此外,unidentified_Mitochondria 在样品JS和CT中相对丰度分别为6.3%和9.3%,其功能可能与大曲发酵力及酸度调控相关[11],但具体作用机制尚需进一步解析。真菌中的优势真菌属(相对丰度大于5%)有嗜热子囊菌属(Thermoascus)和嗜热丝孢菌属(Thermomyces)。其中,嗜热子囊菌属在样品JS和CT中相对丰度分别为76.7%和82.2%(图3-b),能够产生纤维素酶、蛋白酶、淀粉酶、脂肪酶等多种热稳定性酶,具有很强的耐热性,有利于大曲产酒生香。嗜热丝孢菌属在样品JS和CT中相对丰度分别为16.6%和13.1%,其代谢产物为酿酒发酵所需的纤维素酶、蛋白酶、淀粉酶、脂肪酶等,是酿酒生产的重要微生物[12]。
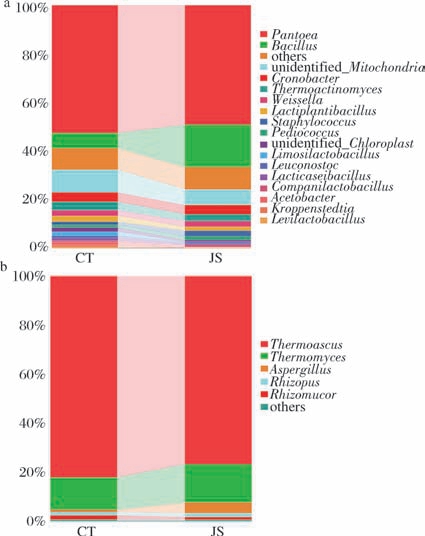
图3 立式发酵曲和传统中高温曲微生物群落组成
Fig.3 Differential microbial community composition between JS and CT
a-细菌属水平群落结构;b-真菌属水平群落结构
2.2.2 立式发酵曲与传统中高温曲微生物群落差异
为探究立式发酵曲与传统中高温曲微生物群落差异,采用线性判别分析效应值(linear discriminant analysis effect size,LEfSe)对差异微生物进行分析(细菌属筛选标准:LDA >3,P <0.3;真菌属筛选标准:LDA >3,P <0.5)。如图2-c所示,共鉴定出12个差异细菌属和5个差异真菌属。
差异细菌属中(图4-a、图4-b),葡萄球菌属(Staphylococcus)、链霉菌属(Streptomyces)和酒乳杆菌属(Liquorilactobacillus)存在显著差异(P <0.05)。葡萄球菌属在立式发酵曲中相对丰度(2.27%)显著高于传统中高温曲(1.25%),这可能是造成2种大曲发酵力差异的原因之一[13];链霉菌属在立式发酵曲中的相对丰度(0.21%) 显著高于传统中高温曲(0.01%),与大曲发酵力和液化力呈正相关[14];酒乳杆菌属仅在传统中高温曲中被检出,并在后续酿酒发酵阶段持续存在,说明其可能在白酒发酵过程中发挥特定作用[15]。如图4-c和图4-d所示,差异真菌属中,复膜孢酵母属(Saccharomycopsis)在立式发酵曲中的相对丰度(0.12%)显著高于传统中高温曲(0.01%),该菌属同样与大曲发酵力呈正相关[16]。上述结果表明,立式发酵曲中葡萄球菌属、复膜孢酵母属、链霉菌属均显著高于传统中高温大曲,可能是其发酵力高于传统中高温曲的原因。
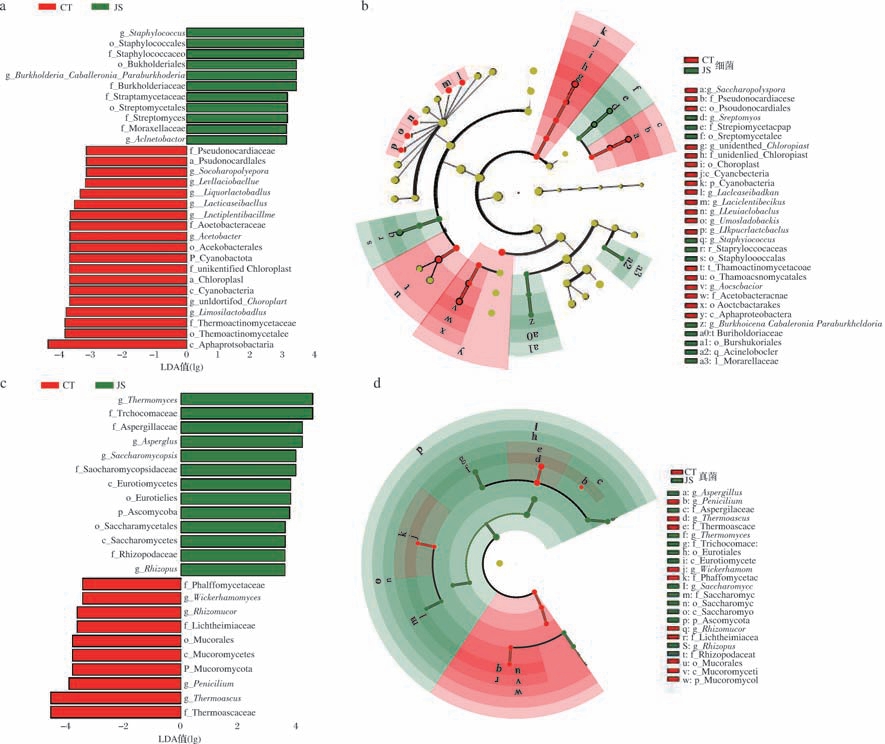
图4 立式发酵曲和传统中高温曲微生物群落差异
Fig.4 Differential microbial communities between JS and CT
a-细菌LDA判别柱形图;b-细菌进化分支图;c-真菌LDA判别柱形图;d-真菌进化分支图
2.3 立式发酵曲与传统中高温曲挥发性风味物质组成及差异分析
2.3.1 立式发酵曲与传统中高温曲挥发性风味物质组成
为研究2种大曲挥发性风味物质组成,采用液液萃取结合GC-MS技术对立式发酵曲和传统中高温大曲的挥发性风味物质进行分析。如图5-a所示,共鉴定出58种挥发性化合物,包括醇类13种、酯类12种、酸类8种、醛类7种、吡嗪类6种、芳香族化合物4种、酮类4种及其他化合物4种。分析结果显示,醇类化合物在两类大曲中均占比最高,是大曲中重要的呈香物质和香味合成前体,亦是大曲香气特征形成的关键组分[17]。
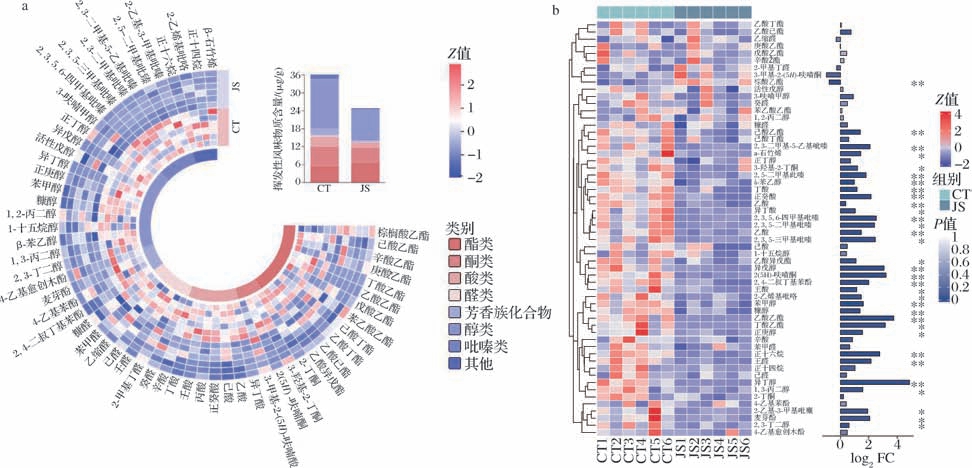
图5 立式发酵曲和传统中高温曲挥发性风味物质比较热图
Fig.5 Heat map of volatile flavor compounds comparison between JS and CT
a-挥发性风味物质分类堆积图;b-挥发性风味物质差异热图
同时,传统中高温曲中的醇类、酸类、醛类、吡嗪类、芳香族化合物及酮类含量高于立式发酵曲,酯类化合物含量低于立式发酵曲。总体而言,传统中高温曲的挥发性风味物质总含量高于立式发酵曲,为立式发酵曲的1.5倍。
为比较2种大曲挥发性风味物质差异,通过Metware Cloud平台绘制挥发性物质的热图(图5-b),分析结果显示,乙缩醛、棕榈酸乙酯、3-甲基-2-(5H)-呋喃酮和2-甲基丁醛在立式发酵曲中富集较多,而传统中高温曲中54种挥发性风味物质含量更高,33种挥发性风味物质存在显著差异(P <0.05)。其中,立式发酵曲中棕榈酸乙酯含量显著(P <0.05)高于传统中高温曲,其余32种(如己酸乙酯、2,3,5,6-四甲基吡嗪)挥发性风味物质含量显著低于传统中高温曲(P <0.05)。
2.3.2 立式发酵曲与传统中高温曲挥发性风味物质组成
为进一步确定2种大曲挥发性物质差异,构建OPLS-DA模型,如图6所示,模型体现了2组样品在得分图中呈现显著分离趋势(R2 Y=0.997,Q2 Y=0.934),且模型未过拟合(置换检验结果 Q2=-0.263)。基于VIP >1筛选出30种关键差异物质,包括乙酸、麦芽酚等,其中,棕榈酸乙酯含量在立式发酵曲中显著高于传统中高温曲,可视为立式发酵曲的特征风味物质(P <0.05,VIP >1)。传统中高温曲中筛选出29种特征物质(P <0.05,VIP >1),包括多种吡嗪类(2,3,5,6-四甲基吡嗪、2,3-二甲基-5-乙基吡嗪等)、醇类(苯甲醇、β-苯乙醇等)、酯类(己酸乙酯、乙酸乙酯等)及酸类(乙酸、丁酸等)物质等,这些物质共同构成了传统中高温大曲复杂而丰富的风味特征。
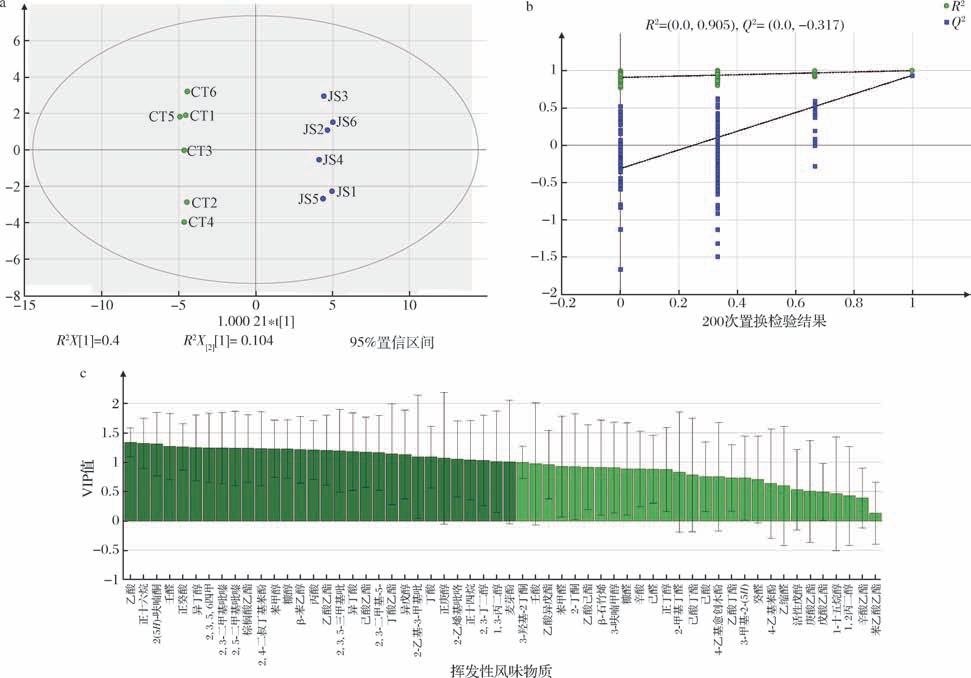
图6 立式发酵曲和传统中高温曲挥发性风味物质差异
Fig.6 Difference of volatile flavor compounds between JS and CT
a-OPLS-DA得分图;b-置换检验结果图;c-VIP值图
目前,大曲质量判定仍以感官和理化结合的方式进行,大曲香气特征是质量评价的关键指标[18]。传统中高温曲在特征挥发性物质种类和挥发性物质总含量上均高于立式发酵曲,验证了传统工艺在风味物质积累方面的优势。
2.4 立式发酵曲与传统中高温曲微生物群落与理化指标及风味物质的关联分析
2.4.1 差异微生物与理化指标相关性分析
基于Spearman法构建差异微生物与大曲关键理化指标(酯化力、糖化力、液化力、酸度、发酵力、水分)的相关性热图。如图7-a所示,葡萄球菌属、链霉菌属与大曲发酵力、水分呈显著正相关(P <0.05)。进一步验证了葡萄球菌属、链霉菌属是发酵力指标偏高的关键菌群,其生长可能与大曲中水分含量呈正相关[19-20]。酒乳杆菌属与大曲发酵力、水分呈极显著(P <0.01)负相关。
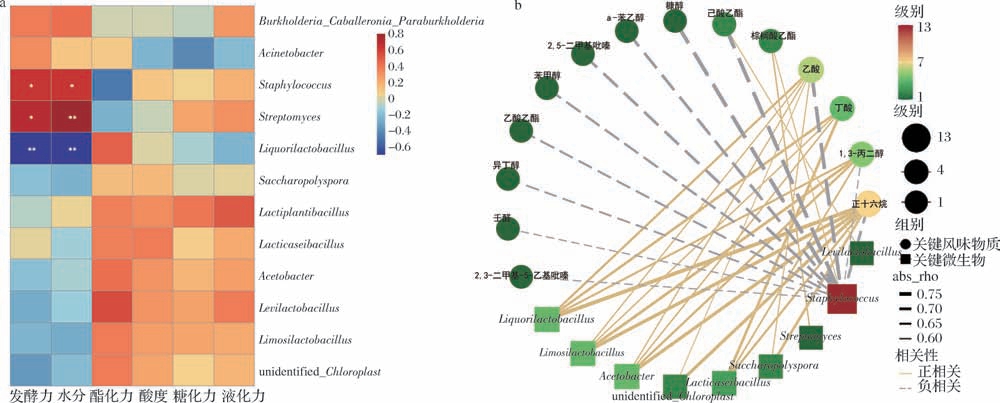
图7 立式发酵曲和传统中高温曲差异微生物、理化、挥发性风味物质相关性
Fig.7 Correlation of differential microorganisms,physicochemical properties,and volatile flavor substances
a-差异微生物与理化相关性热图;b-差异微生物与特征风味物质相关性网络图
2.4.2 差异微生物与关键挥发性风味物质相关性分析
基于Spearman法绘制微生物相关性网络图(|R| >0.5,P <0.05),分析差异微生物与特征挥发性风味物质相关性。如图7-b所示,醋杆菌属(Acetobacter)、粘液乳杆菌属(Limosilactobacillus)、酒乳杆菌属与正十六烷、1,3-丙二醇、丁酸、乙酸呈正相关;乳酸酪杆菌属(Lacticaseibacillus)与丁酸、正十六烷、1,3-丙二醇呈正相关;轻链乳杆菌属(Levilactobacillus)与己酸乙酯呈正相关;糖多孢菌属(Saccharopolyspora)、unidentified_Chloroplast 与正十六烷、乙酸呈正相关;葡萄球菌属与己酸乙酯、乙酸、β-苯乙醇、2,5-二甲基吡嗪等呈负相关,与棕榈酸乙酯呈正相关[21];链霉菌属仅与棕榈酸乙酯呈正相关[22]。其具体微生物功能角色还需进一步解析。
3 结论与讨论
本研究系统分析了立式发酵曲与传统中高温曲在理化特性、微生物群落及挥发性风味物质方面的差异。结果表明,立式发酵曲发酵力和水分含量显著高于传统中高温曲(P <0.05),其原因可能是由于立式发酵曲的立体堆积结构促进了酵母菌等好氧微生物的生长,导致其发酵力较高。微生物群落方面,2种大曲微生物群落结构相似,但立式发酵曲的细菌α-多样性显著低于传统曲,真菌群落无显著差异;葡萄球菌属、链霉菌属和复膜孢酵母属在立式发酵曲中显著高于传统中高温曲,可能是导致其发酵力高于传统中高温曲的原因之一。挥发性风味物质方面,传统中高温曲的风味物质总含量(35.9 μg/g)为立式发酵曲的1.5倍,含有吡嗪类、醇类、酯类、酸类等29种特征风味物质,而立式发酵曲的特征风味物质为棕榈酸乙酯,说明传统中高温大曲生产工艺在风味物质积累方面具有一定优势。微生物-理化-风味关联性分析发现,醋杆菌属、粘液乳杆菌属、酒乳杆菌属、乳酸酪杆菌属与丁酸、正十六烷、1,3-丙二醇含量呈正相关;而葡萄球菌属、链霉菌属与棕榈酸乙酯含量呈正相关,与发酵力、水分指标呈显著(P <0.05)正相关。本研究通过对比分析,揭示了立式发酵曲与传统中高温曲在理化指标、微生物群落及风味物质组成上的差异,为制曲工艺优化升级及立式发酵曲品质提升和风味物质调控提供了理论依据。
[1]邵虎,黄亚东.隧道式智能化架式制曲装置开发与应用[J].酿酒科技,2012(12):61-64.SHAO H,HUANG Y D.Development and application of intelligent tunnel-type shelf Daqu-making devices[J].Liquor-Making Science&Technology,2012(12):61-64.
[2]吕相彩,杨刚仁.习酒中温架式曲的工艺特点[J].酿酒科技,2010(7):46-48.LU X C,YANG G R.Technical characteristicts of Xijiu medium temperature shelf fermented starter[J].Liquor-Making Science &Technology,2010(7):46-48.
[3]尚英,许德富,张宿义,等.中高温大曲多层曲坯立体培菌发酵过程的温度演变趋势探讨[J].酿酒,2017,44(3):30-35.SHANG Y,XU D F,ZHANG S Y,et al.Discussion on the change of temperature during three-dimensional microbial cultivation and fermentation in multi-layer koji bricks at medium-high temperature[J].Liquor Making,2017,44(3):30-35.
[4]吴树坤,谢军,程铁辕,等.不同地区浓香型大曲质量指标与细菌群落相关性研究[J].食品研究与开发,2019,40(4):158-164.WU S K,XIE J,CHENG T Y,et al.Correlation between quality index and bacterial community of Luzhou flavor Daqu[J].Food Research and Development,2019,40(4):158-164.
[5]DENG J,ZHENG J,HUANG D,et al.Characterization of physicochemical properties,volatile compounds and microbial community structure in four types of Daqu[J].LWT,2023,184:115064.
[6]陈勇,林涵瑞,陈晓茹,等.川派浓香型白酒大曲的典型产区差异性分析[J].中国酿造,2024,43(11):34-40.CHEN Y,LIN H R,CHEN X R,et al.Difference analysis of Sichuan strong-flavor Baijiu Daqu in typical producing areas[J].China Brewing,2024,43(11):34-40.
[7]QUAN S K,WANG Y,RAN M F,et al.Contrasting the microbial community and non-volatile metabolites involved in ester synthesis between Qing-flavor Daqu and Nong-flavor Daqu[J].Journal of Bioscience and Bioengineering,2023,136(3):213-222.
[8]商海林.中高温大曲高产糖化酶及蛋白酶活力菌株的筛选与应用研究[D].济南: 齐鲁工业大学,2024.SHANG H L.Screening and application of high-yield glucoamylase and protease strains in medium-high temperature Daqu[D].Jinan:Qilu University of Technology,2024.
[9]纪圩,廖辉,吴梦尧,等.中高温大曲发酵过程中芽孢杆菌生物膜对保水性的调控机制研究[J].食品与发酵工业,2025,51(22):32-40.JI W,LIAO H,WU M Y,et al.Regulatory mechanism of Bacillus biofilm on water retention during medium-high temperature Daqu fermentation[J].Food and Fermentation Industries,2025,51 (22):32-40.
[10]ZHU C T,WEI J L,YANG Y,et al.Regional fingerprint,enrichment and flavor contribution of Bacillus community in Daqu for Chinese Baijiu[J].Food Research International,2025,211:116460.
[11]何猛超,任义平,熊林,等.茅台地区不同高温大曲微生物群落结构解析[J].中国酿造,2022,41(6):51-57.HE M C,REN Y P,XIONG L,et al.Microbial community structure of different high-temperature Daqu in Maotai area[J].China Brewing,2022,41(6):51-57.
[12]刘孟华,陈仪,樊科权,等.不同制曲季节浓香型大曲真菌群落结构多样性的研究[J].食品与发酵科技,2024,60(3):82-85;116.LIU M H,CHEN Y,FAN K Q,et al.Study on the diversity of fungal community structure of Nongxiangxing Daqu in different kojimaking seasons[J].Food and Fermentation Science &Technology,2024,60(3):82-85;116.
[13]刘文虎,柴丽娟,张立强,等.基于宏基因组学解析不同质量等级中温大曲微生物组的异质性[J].微生物学报,2023,63(11):4383-4398.LIU W H,CHAI L J,ZHANG L Q,et al.Metagenomics unveils the microbiome heterogeneity of medium-temperature Daqu with different quality grades[J].Acta Microbiologica Sinica,2023,63(11):4383-4398.
[14]曹敬华,李恬心,刘雄锋,等.不同工艺高温大曲的理化指标变化趋势研究[J].食品科技,2023,48(3):102-109.CAO J H,LI T X,LIU X F,et al.The changing trend of physical and chemical indexes of high-temperature Daqu with different processes[J].Food Science and Technology,2023,48(3):102-109.
[15]王宏楠,陈忻,钟先锋,等.岭南特色小曲白酒发酵过程中细菌菌群演替变化规律[J].食品与发酵工业,2025,51(24):105-110.WANG H N,CHEN X,ZHONG X F,et al.Bacterial community succession during fermentation of Lingnan-style Xiaoqu Baijiu[J].Food and Fermentation Industries,2025,51(24):105-110.
[16]毛文定,冯文聪,孙威,等.不同香型白酒酿造大曲微生物群落与理化指标关联分析[J].中国酿造,2024,43(7):147-153.MAO W D,FENG W C,SUN W,et al.Correlation analysis between microbial community and physiochemical indexes in Daqu for different flavor Baijiu brewing[J].China Brewing,2024,43(7):147-153.
[17]王秀秀,吕志远,刘玉涛,等.大曲微生物群落结构及其风味组分相关性研究[J].酿酒科技,2025(2):31-38.WANG X X,LÜ Z Y,LIU Y T,et al.Correlation analysis of microbial community structure and flavor components of medium/high-temperature Daqu[J].Liquor-Making Science &Technology,2025(2):31-38.
[18]李建勋,李清亮,陈鹏,等.白酒大曲质量鉴别的研究进展[J].中国酿造,2024,43(10):13-17.LI J X,LI Q L,CHEN P,et al.Research progress on quality identification of Baijiu Daqu[J].China Brewing,2024,43(10):13-17.
[19]陈绍依,郎莹,邱树毅,等.茅台镇不同区域酱香大曲微生物群落结构及生产性能对比[J].食品科学,2023,44(14):134-143.CHEN S Y,LANG Y,QIU S Y,et al.Comparative studies on microbial community structure and production performance of Jiangflavor Daqu in different areas of Maotai Town[J].Food Science,2023,44(14):134-143.
[20]黄静.保宁醋“中药醋曲”发酵过程中微生物菌群与理化性质动态解析[D].雅安: 四川农业大学,2020.HUANG J.Dynamic analysis of microbial flora and physicochemical properties during fermentation of Baoning vinegar with “Chinese herbal vinegar starter”[D].Yaan: Sichuan Agricultural University,2020.
[21]徐欢.传统呷酒中微生物多样性对风味的影响及发酵工艺优化[D].成都: 西华大学,2023.XU H.The influence of microbial diversity on flavor and optimization of fermentation process in traditional wine tasting[D].Chengdu: Xihua University,2023.
[22]吴双.不同温度对青砖茶发酵品质形成的影响[D].武汉: 华中农业大学,2022.WU S.Effects of different temperatures on the quality formation of Qingzhuan tea fermentation[D].Wuhan: Huazhong Agricultural University,2022.