作为酱香型白酒酿造的核心糖化发酵剂,高温大曲以小麦为主要原料,经高温发酵制成。其制作过程中高达60 ℃以上的高温环境塑造了独特的微生物群落结构,进而为白酒的酿造提供了独特的酱香成分和前体物质,因而其微生物组成的解析及其功能特性受到广泛关注[1]。例如PANG等[2]对华北地区高温大曲的理化指标、挥发性风味物质和微生物特性进行了分析,发现芽孢杆菌属(Bacillus)、克罗彭斯特菌属(Kroppenstedtia)和海洋芽胞杆菌属(Oceanobacillus)等是主要细菌属,曲霉属(Aspergillus)和丝衣霉菌(Byssochlamys)与糖化和发酵能力呈显著正相关,Oceanobacillus 能够促进酯酶和淀粉酶的产生,并与部分酯、醇、酸和四甲基吡嗪等物质呈正相关;DENG等[3]研究了高温大曲中优势群落与理化性质的相关性,发现水分含量和液化力与Kroppenstedtia 呈正相关,糖化力与葡萄球菌属(Staphylococcus)呈正相关,酯化力与高温放线菌属(Thermoactinomyces)呈正相关。上述研究表明,酒曲微生物群落不仅能够产生丰富的酶系和风味物质,更影响了糖化力、液化力和发酵力等关键理化指标。因此,系统推进酒曲微生物群落结构研究,是解析酿造微生物菌群分布规律及其与发酵特性之间关系研究体系的理论基石。
传统培养方法难以全面解析高温环境下微生物群落的真实组成,这促使研究者转向更精准的分子生物学技术以揭示其内在关联。单分子实时(single molecule real-time,PacBio SMRT)测序技术以其超长读长、单分子实时测序和高度均一性的技术优势,为酒曲微生物多样性的深度解析提供了工具[4]。基于PacBio SMRT测序技术,ZHANG等[5]揭示了高温大曲在成熟3个月和成熟6个月的微生物群落组成,结果表明,血红热放线菌(Thermoactinomyces sanguinis)相对丰度从73.08% 降低到18.36%,扁豆类芽孢杆菌(Paenibacillus lentimorbus)的比例从12.94% 下降到3.17%;HAN等[6]比较了合格和劣质大曲的微生物群落组成,发现地衣芽孢杆菌(Bacillus licheniformis)、扣囊复膜酵母(Saccharomycopsis fibuligera)和分支横梗霉(Lichtheimia ramosa)在合格大曲中显著高于劣质大曲;丁芳等[7]比较了不同等级高温大曲微生物群落的差异,结果表明一级大曲中优势菌属为慢生芽孢杆菌属(Lentibacillus)、Kroppenstedtia、Staphylococcus和Aspergillus 等,优级大曲中优势菌属为Bacillus、Kroppenstedtia 和踝节菌属(Rasamsonia)等,特级大曲中优势菌属为Bacillus、Kroppenstedtia 和Aspergillus 等。上述研究成果表明,采用第三代PacBio SMRT测序平台能有效解析大曲样本中的复杂微生物群落结构特征,为深入探究其物种多样性及功能特性提供重要技术支持。
本研究以采集自山东省潍坊市安丘市景芝镇的高温大曲为研究对象,首先使用PacBio SMRT测序技术从属和种水平分析其微生物群落组成,并使用纯培养技术分析其中可培养微生物的组成,然后采用常规理化分析和仿生学手段分析其理化性质和感官品质,并进一步分析其与优势微生物的相关性。本研究全面解析了景芝镇高温大曲的微生物群落组成及其理化性质和感官品质,以期为高温大曲微生物的挖掘和品质的提升提供数据支持,并为强化大曲的开发提供菌株支撑。
1 材料与方法
1.1 材料与试剂
高温大曲样品:采集自山东省潍坊市安丘市景芝镇(N119.33°,E36.27°)某酒厂,样品编号为JZ1~JZ10。选取曲房入口处、中心高温区和角落低温区3个区域,每个区域分为上中下3层,每层随机选取1~2块,共选取10块高温大曲,立即运回实验室进行粉碎,低温保存备用。
TIANamp Soil DNA Kit土壤基因组DNA提取试剂盒,天根生化科技(北京)有限公司;DNA Clean-up Kit DNA产物纯化试剂盒,江苏康为世纪生物科技股份有限公司;营养琼脂(nutrient agar,NA)培养基、PDA培养基、MRS培养基,海博生物技术有限公司。
1.2 仪器与设备
SW-CJ-1D单人单面垂直送风净化工作台,上海沪净医疗器械有限公司;LRH-150B生化培养箱,青岛聚创环保集团有限公司;DG250厌氧工作站,英国Don Whitley公司;Veriti FAST梯度PCR仪,美国ABI公司;Sequel 11测序仪,PacBio公司;R930机架式服务器,美国DELL公司;PEN3电子鼻,德国Airsense公司;SA402B电子舌,日本Insent公司。
1.3 实验方法
1.3.1 DNA提取、PCR扩增和PacBio SMRT测序
依据TIANamp Soil DNA Kit土壤基因组DNA提取试剂盒说明书的操作步骤提取样品基因组DNA。得到的DNA片段使用琼脂糖凝胶电泳检测其浓度与纯度,将检测合格的DNA进行PCR扩增[8]。使用纯化试剂盒对PCR扩增产物进行纯化,纯化后的产物进行PacBio SMRT测序。
1.3.2 生物信息学分析
使用FLASH合并原始双端读长,并去除低质量的短片段序列。基于QIIME(v1.9.0)平台进行生物信息学分析,使用UCHIME鉴定和去除嵌合体序列,根据97%相似度划分操作分类单元(operational taxonomic units,OTU),并在核糖体数据库项目(ribosomal database project,RDP)和UNITE数据库进行比对[9],确定分类学地位,并计算其α 多样性指数。
1.3.3 可培养的分离与鉴定
在生理盐水锥形瓶中加入10 g高温大曲样品,室温振荡30 min,吸取1 mL混匀的液体样品进行10倍梯度倍比稀释。取10-3~10-5 梯度的稀释液涂布于NA培养基、PDA培养基和MRS培养基,培养条件分别为30 ℃倒置培养2 d、28 ℃正置培养5 d和37 ℃厌氧倒置培养3 d。待菌落出现后,挑取不同形态的菌落在培养基上进一步划线纯化。收集纯化后的菌株进行DNA提取、PCR扩增[10]、连接和转化,挑取阳性克隆子进行测序,返回序列进行比对后构建系统发育树。
1.3.4 理化性质和感官品质分析
参照QB/T 4257—2011《酿酒大曲通用分析方法》测定样品理化指标。参照张顶坤等[11]的方法,使用电子舌和电子鼻对高温大曲的感官指标进行测定。其中电子舌的传感器为酸味、苦味、涩味、咸味、鲜味5个基本味和后味B(苦味的回味)、后味A(涩味的回味)和丰度(鲜味的回味)3个回味;电子鼻的传感器为W1C、W3C、W5C、W1W、W2S、W2W[12]。
1.4 数据处理
采用GraphPad Prism 9.0软件绘制小提琴图,采用Origin 2024软件绘制百分比堆积柱状图,采用DNAMAN 6.0软件和MEGA 7.0软件绘制系统发育树,采用SAS 9.4和Cytoscape 3.5.0软件相关性分析网络图。
2 结果与分析
2.1 景芝镇高温大曲微生物多样性分析
本研究利用PacBio SMRT测序技术对景芝镇高温大曲进行了测序,结果显示10份高温大曲共获得120 247条16S rDNA序列和131 075条ITS序列,同时计算了高温大曲的细菌和真菌群落的α 多样性指数,结果见图1。
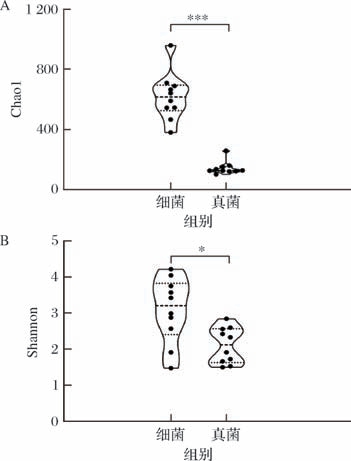
图1 景芝镇高温大曲微生物α 多样性分析
Fig.1 Analysis of alpha diversity of high-temperature Daqu microorganisms in Jingzhi Town
注:Chao1指数和Shannon指数均在测序量为7 010条序列时计算所得;∗∗∗表示组间存在极显著差异(P <0.001),∗表示存在显著差异(P <0.05)(下同)。
A-Chao1指数;B-Shannon指数
由图1可知,景芝镇高温大曲的细菌菌群和真菌菌群的Chao1指数平均值分别为618和143,Shannon指数平均值分别为3.08和2.11。经Mann-Whitney检验显示Chao1指数差异极显著(P <0.001),Shannon指数差异显著(P <0.05)。α 多样性指数反映群落内物种丰富度(Chao1指数)和多样性(Shannon指数),指数越高表明物种丰富度和多样性越好[13]。因此,在本研究中景芝镇高温大曲的细菌菌群物种丰富度和多样性均显著高于真菌菌群(P <0.05)。
2.2 景芝镇高温大曲微生物群落结构分析
2.2.1 景芝镇高温大曲细菌群落结构分析
为确定景芝镇高温大曲中微生物群落结构差异,分别于属水平和种水平进行菌群结构分析,其中景芝镇高温大曲细菌群落结构分析如图2所示。
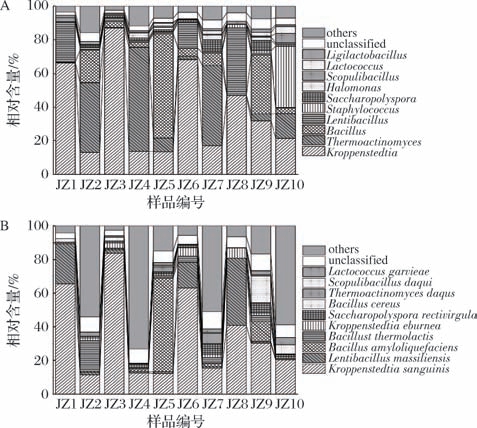
图2 景芝镇高温大曲细菌属和细菌种菌群结构分析
Fig.2 Analysis of the bacterial community structure of the genus and species of high-temperature Daqu in Jingzhi Town
注:unclassified为未鉴定物种;others为平均相对含量小于1.00%属或种的总和(下同)。
A-细菌属;B-细菌种
细菌属水平分析表明,景芝镇高温大曲中主要细菌属为 Kroppenstedtia、 Thermoactinomyces、 Bacillus、Lentibacillus、 Staphylococcus、糖多孢菌属(Saccharopolyspora)、盐单胞菌属(Halomonas)、火山渣芽孢杆菌属(Scopulibacillus)、乳酸乳球菌(Lactococcus)和联合乳杆菌属(Ligilactobacillus),平均相对含量分别为37.94%、18.02%、13.96%、8.67%、4.21%、1.94%、1.13%、1.10%、1.07%和1.07%。
细菌种水平分析表明,景芝镇高温大曲中主要细菌种为血液克罗彭施泰特氏菌(Kroppenstedtia sanguinis)、马赛慢生芽孢杆菌(Lentibacillus massiliensis)、解淀粉芽孢杆菌(Bacillus amyloliquefaciens)、热酸芽孢杆菌(Bacillus thermolactis)、象牙色克罗彭施泰特氏菌(Kroppenstedtia eburnea)、直杆糖多孢菌(Saccharopolyspora rectivirgula)、蜡样芽孢杆菌(Bacillus cereus)、大曲高温放线菌(Thermoactinomyces daqus)、大曲岩石芽孢杆菌(Scopulibacillus daqui)和格氏乳球菌(Lactococcus garvieae),平均相对含量分别为35.60%、8.66%、7.27%、3.17%、2.33%、1.91%、1.89%、1.18%、1.10% 和1.07%。HAN等[14]采用PacBio SMRT测序技术对采集自贵州省、山东省和江苏省的高温大曲细菌多样性进行了研究,发现在贵州样品中大曲慢生芽孢杆菌(Lentibacillus daqui)、淤泥大洋芽孢杆菌(Oceanobacillus caeni)和嗜热乳杆菌(Caldibacillus thermolactis)是最丰富的物种,平均相对含量分别为19.09%、12.09%和8.00%;在江苏样品中粘质沙雷氏菌(Serratia marcescens)是最丰富的细菌,占总序列的75.47%;在样品中发现了14种细菌,但只有巨大普里斯特氏菌(Priestia megaterium)、B.cereus 和Mixta calida 是优势物种。该研究结果与本研究存在差异,究其原因可能在于地理环境、工艺参数和微生物相互作用的差异,这些差异导致微生物代谢功能调控及群落动态平衡的改变,进而影响高温大曲的微生物群落构成。作为景芝镇高温大曲中绝对优势细菌种,K. sanguinis 是典型的耐高温菌,因而其在高于60 ℃的顶温发酵阶段能够存活并成为优势菌群[15]。此外,隶属于该菌属的菌种能够通过代谢产生乳酸和乙酸等酸性物质抑制杂菌生长,并且在发酵中后期与产酸菌竞争,导致大曲发酵环境pH值下降,为酵母菌的乙醇代谢创造适宜环境[16]。
2.2.2 景芝镇高温大曲真菌群落结构分析
景芝镇高温大曲真菌群落结构分析见图3。
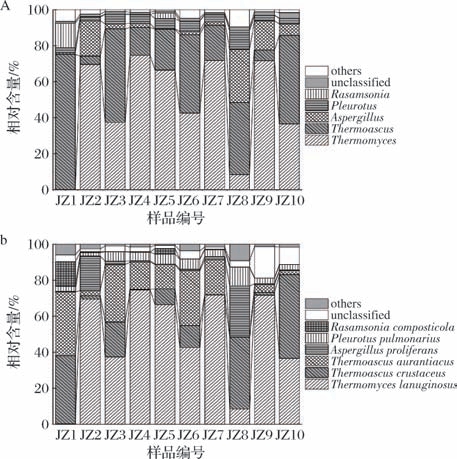
图3 景芝镇高温大曲真菌属和真菌种菌群结构分析
Fig.3 Analysis of the fungal genus and fungal species community structure of high-temperature Daqu in Jingzhi Town
A-真菌属;B-真菌种
真菌属水平分析表明,景芝镇高温大曲中主要真菌属为嗜热真菌属(Thermomyces)、嗜热子囊菌属(Thermoascus)、 Aspergillus、侧耳属( Pleurotus) 和Rasamsonia,平均相对含量分别为47.98%、32.79%、8.16%、4.75%和1.72%。真菌种水平分析表明,景芝镇高温大曲中主要真菌种为疏棉状嗜热丝孢菌(Thermomyces lanuginosus)、坚脆嗜热子囊菌(Thermoascus crustaceus)、橙色嗜热子囊菌(Thermoascus aurantiacus)、多育曲霉(Aspergillus proliferans)、肺形侧耳(Pleurotus pulmonarius)和Rasamsonia composticola,平均相对含量分别为47.97%、16.81%、15.59%、5.33%、4.70% 和1.72%。吴成等[17] 采用PacBio SMRT测序技术对采集自贵州省的酱香型高温大曲真菌多样性进行了研究,发现仿生机制高温大曲和传统人工高温大曲均以T. aurantiacus、T. crustaceus 和T.lanuginosus 为优势菌种。沈毅等[18]发现四川郎酒公司的酱香型高温大曲的优势属为Thermomyces、Aspergillus和Thermoascus,其平均相对含量分别为54.9%、24.2%和18.5%,优势种为T. lanuginosus 和Aspergillus cibarius,平均相对含量分别为54.9% 和24.2%。崔梦君等[19]发现湖北省宜昌地区高温大曲的优势属以Thermomyces 和Thermoascus 为主,平均相对含量分别为 74.02% 和 16.06%,优势种以T.lanuginosus和T. crustaceus 为主,平均相对含量分别为73.81%和14.10%。上述研究结果与本研究相似,可能与高温大曲制作过程中微生物的适应性以及高温环境的筛选作用有关,即高温大曲的制作过程中,60~70 ℃的发酵环境会淘汰不耐热微生物,富集具备代谢优势且能适应高温环境并生长繁殖的特殊微生物群落,进而使得不同地区在制作高温大曲时,都可能形成以耐热菌为优势菌属的群落结构[20]。
T. lanuginosus 作为景芝镇高温大曲中第一真菌优势种,具有的嗜热特性使其在高温制曲过程中仍能保持酶活性,并分泌蛋白酶、纤维素酶、淀粉酶和糖化酶,加速大曲中淀粉和蛋白质的分解,促进大曲中醇类、酯类、酸类等风味物质的生成,提升大曲的香气和发酵效率[21]。 T. crustaceus 和T. aurantiacus 能够分泌淀粉酶、蛋白酶和纤维素酶等,将谷物原料中的淀粉和蛋白质等大分子物质分解为糖类和氨基酸等小分子物质,为酒体提供风味物质的前体,并在后续的发酵和陈酿过程中转化为具有特殊香气的化合物,进一步丰富酒体的风味和口感[22]。此外,T. aurantiacus 还具有较强的分解木质素、纤维素的能力,在高温大曲发酵过程中,将大曲中的木质素、纤维素等大分子物质分解为小分子物质,为后续发酵提供可利用的营养成分[23]。
2.2.3 景芝镇高温大曲中可培养微生物的分离鉴定
进一步使用纯培养技术从景芝镇高温大曲中分离可培养微生物,根据菌落大小、颜色、形态等特征的不同共获得23株菌,对分离的菌株进行序列比对并构建系统发育树,结果如图4所示。
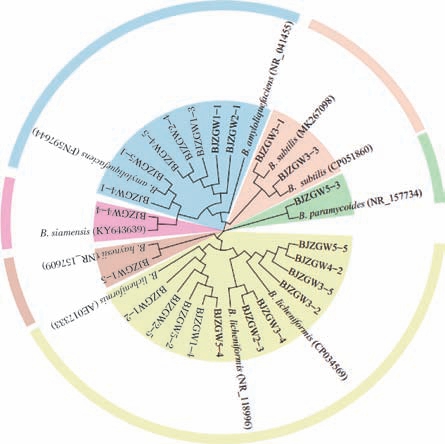
图4 景芝镇高温大曲可培养微生物的系统发育树
Fig.4 Phylogenetic tree of cultivable microorganisms of high-temperature Daqu in Jingzhi Town
由图4可知,分离的菌株中有11株被鉴定为B.licheniformis,7株被鉴定为B. amyloliquefaciens,2株被鉴定为枯草芽孢杆菌(Bacillus subtilis),1株被鉴定为暹罗芽孢杆菌(Bacillus siamensis),1株被鉴定为蕈状芽孢杆菌(Bacillus paramycoides),1株被鉴定为海氏芽孢杆菌(Bacillus haynesii)。在本研究中,分离的菌株均被鉴定为芽孢杆菌,并未分离出其他细菌和真菌,可能是因为使用的培养基是基础培养基,适合营养需求较高的微生物生长,却不适用于苛养型微生物生长[24]。此外,高温大曲制作过程中需经历60~70 ℃的高温堆积发酵阶段,这种极端高温环境会抑制不耐热乳酸菌、醋酸菌、酵母菌和霉菌的生长繁殖,但芽孢杆菌因其独特的芽孢结构能够耐受高温,从而成为高温大曲的优势菌群[20]。
分离菌株中B.licheniformis 和B. amyloliquefaciens数量最多,是典型的嗜热芽孢杆菌,也是大曲中产酱香功能细菌,其中B.amyloliquefaciens 在测序结果中为优势微生物之一。 B. licheniformis 和B. amyloliquefaciens在高温大曲中通过其耐高温特性在高温环境下存活并分泌淀粉酶、脂肪酶和蛋白酶等生物酶促进糖化发酵,同时产生吡嗪类等风味前体物质增强酒体酱香风味,最终优化酒体的风味与品质[25]。研究表明,在酱香型高温大曲制作过程中,添加由B. amyloliquefaciens 和B.cereus 制备的菌种发酵液,在一定程度上改善了强化高温大曲的感官质量[26]。此外,黄治国等[27]利用B.licheniformis 和贝莱斯芽孢杆菌(Bacillus velezensis)制成的芽孢杆菌麸曲进行小曲白酒固态酿造实验,成功降低了酒体中异戊醇与异丁醇的含量,并产生了微量的正戊醇,为解决小曲白酒中高级醇含量偏高的问题提供了有效的方法。因此,在未来可以进一步通过强化大曲的制作,筛选出具有特定功能的B. licheniformis 和B. amyloliquefaciens 菌株,以提高酒曲的品质和出酒率。
2.3 景芝镇高温大曲理化性质和感官品质分析
对景芝镇高温大曲的理化性质和感官品质进行分析,结果见表1和表2。
表1 景芝镇高温大曲样品的理化性质测定结果
Table 1 Determination results of physicochemical properties of high-temperature Daqu samples in Jingzhi Town
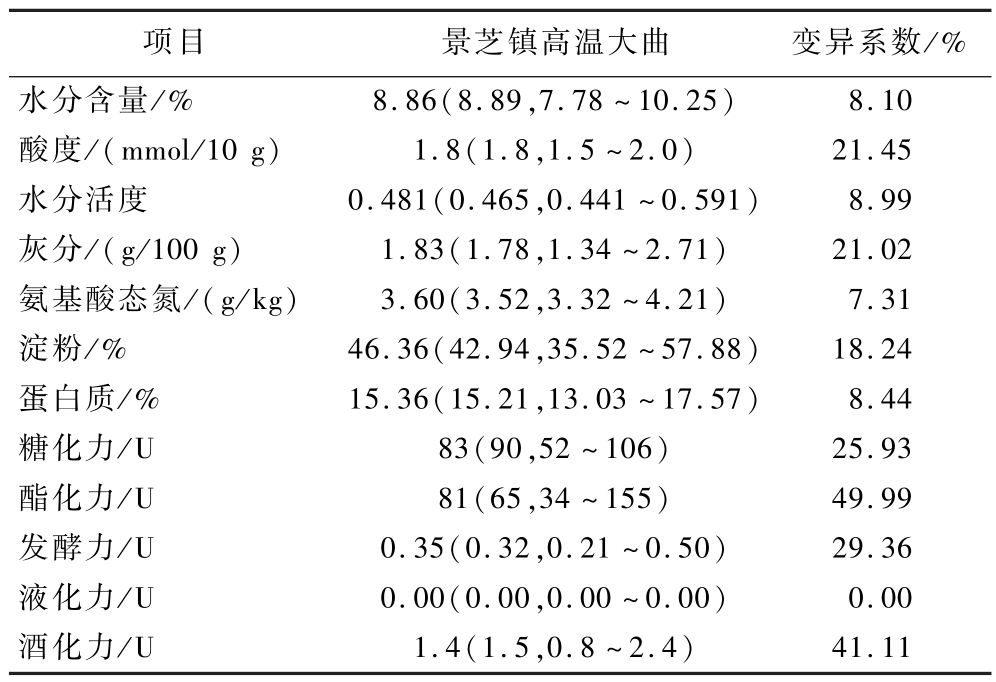
注:数据“8.86(8.89,7.78~10.25)”代表“平均值(中位数,最小值~最大值)”(下同)。
表2 景芝镇高温大曲样品的感官品质指标测定结果
Table 2 Sensory quality index determination results of high temperature Daqu samples in Jingzhi Town
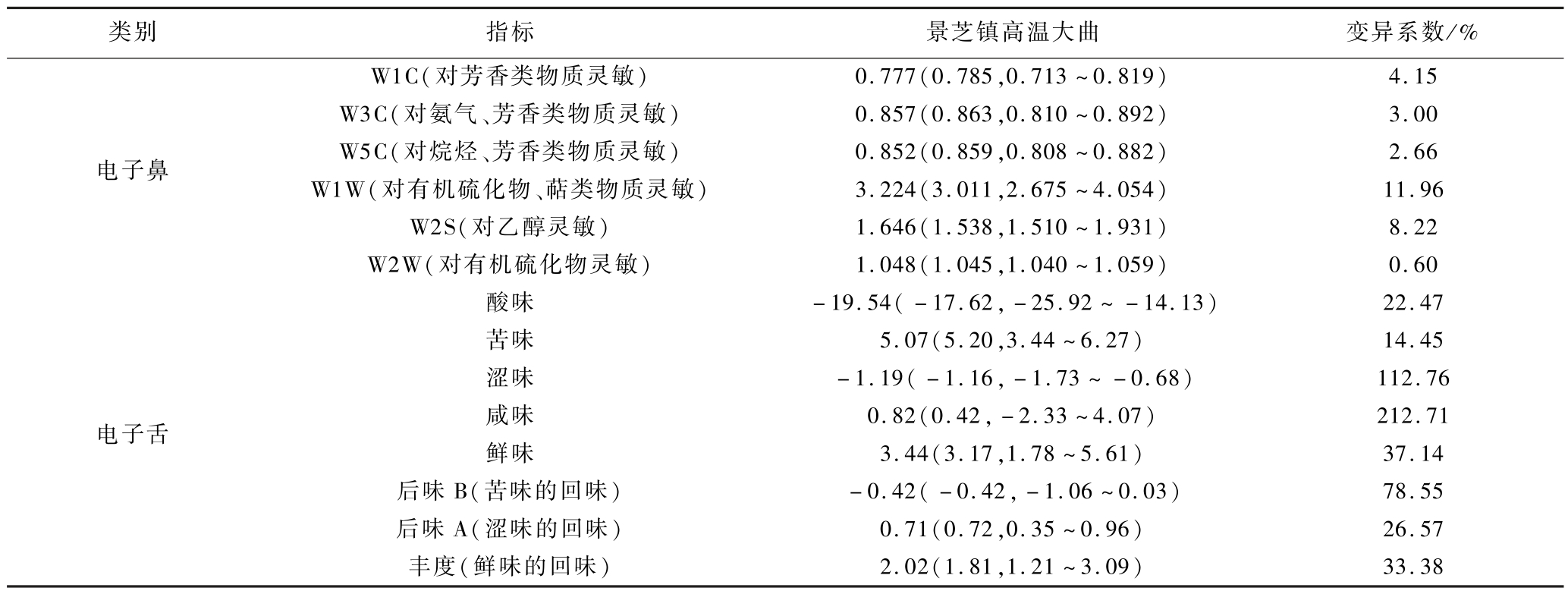
根据优质高温大曲的理化性质,即大曲的水分含量≤11%,酸度为1.5~ 2.0 mmol/10 g,发酵力为0.2~0.5 U,糖化力为50~150 U,纳入本研究的高温大曲样品的水分含量、酸度、发酵力和糖化力均符合优质高温大曲的理化要求。由表1亦可知,高温大曲样品的酯化力和酒化力变异系数明显高于其他理化指标,分别为49.99% 和41.11%。高温发酵的工艺为高温大曲赋予了独特风味,使其含有种类繁多的挥发性芳香物质以及各类呈味成分,因而深入剖析其感官品质特征对于后续全面了解景芝镇高温大曲风味形成机制具有重要意义,其感官品质指标测定结果见表2。
由表2可知,对应于有机硫化物与萜类物质和对应于乙醇的传感器W1W和W2S响应值大于其他各传感器的响应值,且其变异系数明显高于其他气味指标,分别为11.96% 和8.22%。在滋味指标中,酸味指标的响应值明显高于其他滋味指标响应值,此外,对应于涩味和咸味响应值的变异系数较大,分别为112.76% 和212.71%。由此可见,景芝镇高温大曲在气味指标的差异体现在有机硫化物、萜类物质和乙醇上,在滋味指标的差异体现在涩味和咸味上。王利萍等[28]利用电子舌和电子鼻技术分析贵州仁怀地区5种酱香型白酒大曲的风味差异,发现气味物质差异主要体现在有机硫化物和萜类物质上,滋味物质差异主要体现在酸味、咸味和鲜味上,与本研究结果相似。
为了更直观了解高温大曲中核心微生物对理化性质和感官品质的影响,取种水平上平均相对含量大于1.00%的微生物种与景芝镇高温大曲理化性质和感官品质进行相关性分析,以相关性|r| >0.8,P <0.05作为阈值构建相关性网络图,结果如图5所示。
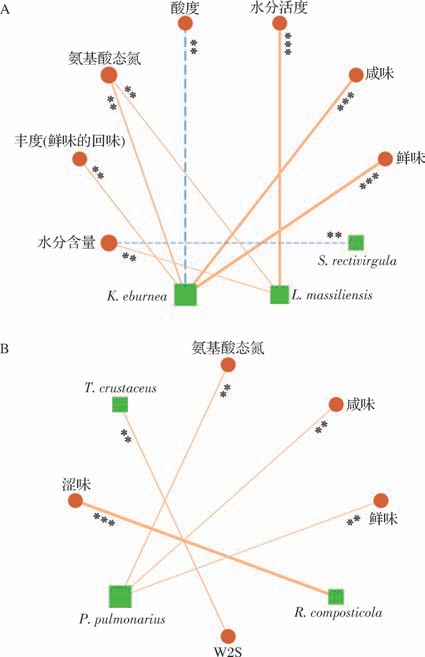
图5 景芝镇高温大曲优势种与理化性质和感官品质的相关性网络图
Fig.5 Network diagram of the correlation between dominant species,physicochemical properties,and sensory quality of high-temperature Daqu in Jingzhi Town
注:图中线越粗代表相关性越大,∗∗代表存在非常显著差异(P <0.01);∗∗∗代表存在极显著差异。
A-细菌种;B-真菌种
相关性分析显示,细菌种与理化性质和感官品质间具有9个相关关系,其中K. eburnea 与鲜味、咸味呈极显著正相关(P <0.001),L.massiliensis 与水分活度呈极显著正相关(P <0.001);真菌种与理化性质和感官品质间具有5个相关关系,其中R. composticola 与涩味呈极显著正相关(P <0.001)。此外,本研究中细菌种与理化性质和感官品质的相关性网络共包括10个节点和9条边,真菌种与理化性质和感官品质的相关性网络共包括8个节点和5条边,因此,在本研究中细菌类群可能对景芝镇高温大曲的理化性质和感官品质的关联性更强,对其品质产生的影响更大。
据报道,优势功能物种K. eburnea 在酒醅堆积发酵的复杂生化反应中,能显著促进风味物质合成体系的高效运作,特别是醇类、酸类和吡嗪类等酱香型白酒特征风味物质的累积[29]。 L.massiliensis 的氨基酸代谢是代谢功能的重要组成部分,研究显示部分Lentibacillus 物种可以分泌蛋白酶并参与氨基酸代谢[30]。然而,目前对于优势功能物种K. eburnean 和L.massiliensis 中风味物质的特定代谢途径尚不清楚,仍有待探索。嗜热新种R. composticola 于2013年首次从云南堆肥样品中分离得到,最适生长温度为45~50 ℃[31],目前在大曲研究中仍鲜有报道。但Rasamsonia 是中温大曲和普洱茶风味形成的潜在功能微生物,其产生的β-葡聚糖酶和木聚糖酶被批准用于食品加工,提升食品质量和工艺效率[32-33]。
3 结论
景芝镇高温大曲中以K. sanguinis 为主要细菌种,以T. lanuginosus、T. crustaceus、T. aurantiacus 为主要真菌种,以B. licheniformis 和B. amyloliquefaciens 为主要可培养微生物;微生物与理化性质和感官品质之间存在显著相关关系,且细菌类群可能对高温大曲的理化性质和感官品质产生更大的影响。
[1]蒋倩儿,陈文浩,孙金沅,等.酱香型白酒大曲微生物研究进展[J].中国酿造,2021,40(12):1-5.JIANG Q E,CHEN W H,SUN J Y,et al.Research progress on microorganism of sauce-flavor Baijiu Daqu[J].China Brewing,2021,40(12):1-5.
[2]PANG Z M,LI W W,HAO J,et al.Correlational analysis of the physicochemical indexes,volatile flavor components,and microbial communities of high-temperature Daqu in the northern region of China[J].Foods,2023,12(2):326.
[3]DENG L,MAO X,LIU D,et al.Comparative analysis of physicochemical properties and microbial composition in high-temperature Daqu with different colors[J].Frontiers in Microbiology,2020,11:588117.
[4]ZHANG H X,WANG L,WANG H Y,et al.Effects of initial temperature on microbial community succession rate and volatile flavors during Baijiu fermentation process[J].Food Research International,2021,141:109887.
[5]ZHANG Y D,XU J G,JIANG Y L,et al.Microbial characteristics and metabolite profiles of high-temperature Daqu in different maturation stages[J].World Journal of Microbiology and Biotechnology,2022,38(12):234.
[6]HAN P J,LUO L J,HAN Y,et al.Microbial community affects Daqu quality and the production of ethanol and flavor compounds in Baijiu fermentation[J].Foods,2023,12(15):2936.
[7]丁芳,张原頔,蒋英丽,等.不同等级高温大曲微生物群落和代谢物的特征分析[J].中国酿造,2022,41(11):24-30.DING F,ZHANG Y D,JIANG Y L,et al.Microbial communities and metabolites characteristics of high temperature Daqu with different grades[J].China Brewing,2022,41(11):24-30.
[8]CAI W C,WANG Y R,HOU Q C,et al.PacBio sequencing combined with metagenomic shotgun sequencing provides insight into the microbial diversity of Zha-chili[J].Food Bioscience,2021,40:100884.
[9]WU X Y,JING R X,CHEN W H,et al.High-throughput sequencing of the microbial diversity of roasted-sesame-like flavored Daqu with different characteristics[J].3 Biotech,2020,10(11):502.
[10]贾鑫,高鹏,周瑞,等.基于纯培养法结合高通量测序技术解析胀袋辐照凤爪中的微生物多样性[J].食品与发酵工业,2024,50(12):135-141.JIA X,GAO P,ZHOU R,et al.Analysis of microbial diversity in swollen irradiated chicken feet based on pure culture method and high-throughput sequencing technology[J].Food and Fermentation Industries,2024,50(12):135-141.
[11]张顶坤,邓秋红,岳秦,等.不同发酵时间猕猴桃米酒品质变化的研究[J].中国酿造,2022,41(3):187-192.ZHANG D K,DENG Q H,YUE Q,et al.Change of quality of kiwi rice wine at different fermentation time[J].China Brewing,2022,41(3):187-192.
[12]LIU X T,WANG X L,CHENG Y W,et al.Variations in volatile organic compounds in Zhenyuan Daocai samples at different storage durations evaluated using E-nose,E-tongue,gas chromatography,and spectrometry[J].LWT,2023,173:114186.
[13]谢丹,吴成,程平言,等.应用单分子实时测序技术解析酱香型白酒高温大曲制作过程细菌多样性[J].食品与发酵工业,2022,48(19):58-64.XIE D,WU C,CHENG P Y,et al.Analysis of bacteria diversity during the production of high-temperature Daqu of Maotai-flavor Baijiu using SMRT technology[J].Food and Fermentation Industries,2022,48(19):58-64.
[14]HAN P J,SONG L,WEN Z,et al.Species-level understanding of the bacterial community in Daqu based on full-length 16S rRNA gene sequences[J].Food Microbiology,2024,123:104566.
[15]薄涛,吕娜,杨凯环,等.白酒大曲发酵过程中微生物群落及功能研究进展[J].食品科学,2023,44(19):385-393.BO T,LYU N,YANG K H,et al.Recent advances in understanding the composition and functions of microbial community in the fermentation of Baijiu Daqu[J].Food Science,2023,44(19):385-393.
[16]XIE M W,LV F X,MA G X,et al.High throughput sequencing of the bacterial composition and dynamic succession in Daqu for Chinese sesame flavour liquor[J].Journal of the Institute of Brewing,2020,126(1):98-104.
[17]吴成,程平言,谢丹,等.酱香型白酒高温大曲发酵过程中真菌多样性研究[J].食品与生物技术学报,2023,42(6):95-103.WU C,CHENG P Y,XIE D,et al.Investigation on fungal diversity during high-temperature Daqu fermentation of sauce-flavor Baijiu[J].Journal of Food Science and Biotechnology,2023,42(6):95-103.
[18]沈毅,程伟,邓小波,等.酱香高温大曲、酒醅和窖泥的真菌多样性分析[J].酿酒科技,2019(3):17-23.SHEN Y,CHENG W,DENG X B,et al.Fungal diversity in hightemperature Jiangxiang Daqu,fermented grains and pit mud[J].Liquor-Making Science &Technology,2019(3):17-23.
[19]崔梦君,王玉荣,侯强川,等.基于三代测序技术高温和中高温大曲真菌多样性解析及酵母菌的分离鉴定[J].食品工业科技,2025,46(2):175-183.CUI M J,WANG Y R,HOU Q C,et al.Analysis of fungal diversity and isolation and identification of yeast in high-temperature and medium-high-temperature daqu using three generation sequencing technology[J].Science and Technology of Food Industry,2025,46(2):175-183.
[20]ZHU M,ZHENG J,XIE J,et al.Effects of environmental factors on the microbial community changes during medium-high temperature Daqu manufacturing[J].Food Research International,2022,153:110955.
[21]YANG X Y,ZHANG J X,DING Q Y,et al.Metabolites from two dominant thermophilic fungal species Thermomyces lanuginosus and Scytalidium thermophilum[J].Chemistry &Biodiversity,2020,17(5):e2000137.
[22]杨阳,牛曼思,戴秋涟,等.同一地区中温和高温大曲理化性质及真菌群落组成的比较研究[J].食品工业科技,2023,44(13):150-159.YANG Y,NIU M S,DAI Q L,et al.A comparative study on physicochemical indices and fungal community composition of medium-temperature and high-temperature Daqus from the same region[J].Science and Technology of Food Industry,2023,44(13):150-159.
[23]MCCLENDON S D,BATTH T,PETZOLD C J,et al.Thermoascus aurantiacus is a promising source of enzymes for biomass deconstruction under thermophilic conditions[J].Biotechnology for Biofuels,2012,5(1):54.
[24]卢萌萌,任聪,聂尧,等.白酒酿造窖泥未培养微生物菌群的可培养化策略[J].食品与发酵工业,2020,46(19):9-16.LU M M,REN C,NIE Y,et al.Cultivation strategy for unculturable microbiota in pit mud involved in strong-flavor Baijiu fermentation[J].Food and Fermentation Industries,2020,46(19):9-16.
[25]KHAJEH K,SHOKRI M M,ASGHARI S M,et al.Acidic and proteolytic digestion of α-amylases from Bacillus licheniformis and Bacillus amyloliquefaciens:Stability and flexibility analysis[J].Enzyme and Microbial Technology,2006,38(3-4):422-428.
[26]何琪,张亚东,晏永,等.菌种发酵液添加对酱香型高温大曲品质的影响研究[J].酿酒科技,2025(3):65-70.HE Q,ZHANG Y D,YAN Y,et al.Effects of adding bacterial fermentation broth on the quality of high-temperature Jiangxiang Daqu[J].Liquor-Making Science &Technology,2025(3):65-70.
[27]黄治国,罗润森,李彦中,等.芽孢杆菌强化发酵降低小曲白酒中高级醇的含量[J].现代食品科技,2023,39(2):145-151.HUANG Z G,LUO R S,LI Y Z,et al.Concentration of higher alcohols in Xiaoqu liquor induced by enhanced fermentation with strains of Bacillus[J].Modern Food Science &Technology,2023,39(2):145-151.
[28]王利萍,郎莹,邱树毅,等.电子鼻结合电子舌技术对五种酱香型白酒大曲的风味物质分析[J].酿酒科技,2022(9):116-122.WANG L P,LANG Y,QIU S Y,et al.Analysis of flavor substances in five kinds of Jiangxiang Daqu by electronic nose and electronic tongue[J].Liquor-Making Science &Technology,2022(9):116-122.
[29]吴双全,柴丽娟,黄廷财,等.酱香型白酒堆积酒醅中象牙色克罗彭斯特德菌的分离筛选及其代谢特性解析[J].微生物学报,2024,64(7):2502-2521.WU S Q,CHAI L J,HUANG T C,et al.Isolation,screening,and metabolic characterization of Kroppenstedtia eburnea from the fermented grains of Jiang-flavor Baijiu[J].Acta Microbiologica Sinica,2024,64(7):2502-2521.
[30]WANG L M,CHENG Y X,HU X X,et al.Analysis of bacterial diversity and functional differences of Jiang-flavored Daqu produced in different seasons[J].Frontiers in Nutrition,2023,9:1078132.
[31]SU Y Y,CAI L.Rasamsonia composticola,a new thermophilic species isolated from compost in Yunnan,China[J].Mycological Progress,2013,12(2):213-221.
[32]FRANCO D G,DE ALMEIDA A P,GALEANO R M S,et al.Exploring the potential of a new thermotolerant xylanase from Rasamsonia composticola (XylRc):Production using agro-residues,biochemical studies,and application to sugarcane bagasse saccharification[J].3 Biotech,2023,14(1):3.
[33]张晶,张浩睿,曹云,等.嗜热纤维素降解菌研究进展[J].生物技术通报,2023,39(6):73-87.ZHANG J,ZHANG H R,CAO Y,et al.Research progress in thermophilic microorganisms for cellulose degradation[J].Biotechnology Bulletin,2023,39(6):73-87.