麦醇溶蛋白是小麦面筋蛋白的主要组分,占面筋蛋白总量的40%~50%,其分子结构中富含谷氨酰胺和疏水氨基酸,具有良好的成膜性和生物相容性[1]。茶多酚(tea polyphenols,TP)是茶叶中富含的天然植物酚类化合物,主要成分为儿茶素类[表没食子儿茶素没食子酸酯(epigallocatechin gallate,EGCG)、表儿茶素没食子酸酯(epicatechin gallate,ECG)、表没食子儿茶素(epigallocatechin,EGC)、表儿茶素(epicatechin,EC)等],具有清除自由基、抗炎及调节肠道菌群等生理功能[2]。近年来,麦醇溶蛋白与TP通过非共价(疏水作用、氢键、静电作用)或共价结合形成的复合物,因兼具蛋白的载体特性和多酚的生物活性,在功能食品开发(如抗氧化剂、多酚递送载体)等领域备受关注[3-4]。
在食品加工中温度是核心工艺参数,其不仅影响蛋白的构象稳定性,还可能改变多酚与蛋白的结合方式及效率[5],从而影响其复合物的功能活性[6]。已有研究表明,适度加热可使蛋白构象舒展并暴露疏水位点和活性基团,促进与多酚的非共价结合[7];但过高温度可能导致蛋白过度变性聚集,掩盖结合位点,甚至引发多酚氧化降解,反而削弱两者的相互作用[8]。目前,关于温度驱动蛋白-多酚相互作用的研究多集中于牛奶蛋白、大豆蛋白等水溶性蛋白体系,如文鹏程等[9]通过分析茶多酚在不同温度下对牛奶蛋白的影响,发现65 ℃处理时可促进结合,降低浊度并增加游离巯基含量;而当温度高达95 ℃时,则会使蛋白发生聚集,抑制了结合。QIE等[10]在EGCG与β-乳球蛋白的相互作用中,进一步发现当温度为60 ℃时氢键和范德华力占主导,而在85 ℃时静电相互作用占主导。GE等[11]研究EGCG与大豆蛋白在25 ℃、100 ℃和121 ℃下的相互作用时,发现加热后EGCG更易与大豆蛋白的α/α′亚基和A亚基结合,且在高温(100 ℃)下结合更显著。但针对麦醇溶蛋白独特的醇溶蛋白特性[12],与其他水溶性蛋白存在差异,温度对其反应环境的影响会更复杂[13],且相关研究鲜见报道。因此,本文针对麦醇溶蛋白-茶多酚互作体系在不同温度条件下的荧光和紫外光谱变化、相互作用中主要化学作用力变化、体系浊度和复合物表面疏水性、粒径分布、Zeta电位以及抗氧化活性等特征变化展开多维度的分析,以期揭示温度对麦醇溶蛋白-茶多酚相互作用的动态影响及其抗氧化活性的响应差异,筛选并提出麦醇溶蛋白-茶多酚互作的最佳温度区间,为麦醇溶蛋白-茶多酚复合物加工过程合理控制温度参数,优化其功能特性(如稳定性、抗氧化性能等)提供实验支撑。
1 材料与方法
1.1 材料与试剂
麦醇溶蛋白、儿茶素单体标准品,美国sigma公司;茶多酚、DPPH自由基清除能力检测试剂盒、ABTS阳离子自由基清除能力检测试剂盒、羟自由基清除能力检测试剂盒,北京索莱宝有限公司;色谱级甲醇、乙腈,Thermo Fisher公司;色谱级85% 磷酸,ROE公司;其他试剂均为分析纯,国药集团化学试剂有限公司。
1.2 仪器与设备
X-8S紫外可见分光光度计,上海元析仪器有限公司;Chromaster高效液相色谱仪、F-4500荧光分光光度计,日本日立公司;WGZ-2000浊度仪,上海昕瑞仪表有限公司;Malvern panalytical-zetasizer pro纳米粒度电位仪,英国马尔文仪器有限公司;HHS电热恒温水浴锅,上海博讯实业有限公司。
1.3 实验方法
1.3.1 麦醇溶蛋白-茶多酚互作体系的制备
参考李春翼等[14]的方法稍作修改,采用反溶剂法制备麦醇溶蛋白及麦醇溶蛋白-茶多酚溶液。称取麦醇溶蛋白0.1 g、茶多酚0.01 g,在磁力搅拌下将其分别溶解于50 mL 0.01 mol/L乙酸溶液、50 mL 70%(体积分数)乙醇水溶液中,在4 ℃下避光贮存12 h后混匀。按V(混合相)∶V(水相)=1∶3,将混匀溶液逐滴滴入转速为8 000 r/min的去离子水中,均质后制得麦醇溶蛋白含量为0.25 g/L、茶多酚含量为0.025 g/L的互作体系的样品。相同条件在不添加茶多酚的情况下制备麦醇溶蛋白对照体系的样品(麦醇溶蛋白含量为0.25 g/L)。将上述样品分别在25、50、75、100 ℃恒温水浴锅中加热处理30 min,随即置于冰水浴中冷却至室温以待测定。
1.3.2 荧光光谱测定
1.3.2.1 内源荧光光谱测定
参考WANG等[15]的方法稍作修改。吸取1 mL待测样于比色皿中,采用荧光分光光度计测定内源荧光光谱。检测条件:激发波长282 nm,发射波长范围300~500 nm,电压700 V,狭缝宽度5.0 nm。
1.3.2.2 同步荧光光谱测定
参考余霞[16]的方法稍作修改。吸取1 mL待测样于比色皿中,采用荧光分光光度计测定同步荧光光谱。检测条件:波长差Δλ 为15、60 nm,波长扫描范围200~500 nm,电压700 V、狭缝宽度5.0 nm、扫描速度1 200 nm/min。
1.3.3 紫外光谱测定
吸取2 mL待测样于比色皿中,采用紫外可见分光光度计测定样品在200~600 nm范围内的紫外吸收光谱。
1.3.4 化学作用力测定
参考皮俊翔[17]的方法稍作修改。将1.5 g待测样分别与10 mL 0.05 mol/L NaCl溶液(a)、10 mL 0.6 mol/L NaCl溶液(b)、10 mL 0.6 mol/L NaCl与1.5 mol/L尿素混合溶液(c)、10 mL 0.6 mol/L NaCl与8 mol/L尿素混合溶液(d)、10 mL 0.6 mol/L NaCl、8 mol/L尿素和1.5 mol/L β-巯基乙醇混合溶液(e),在8 000 r/min下均质30 min后,置于4 ℃冷却静置1 h,然后再以7 654 × g 冷冻离心20 min,测定上清液中蛋白质的含量。各个化学作用力的相对含量分别按公式(1)~公式(4)计算:
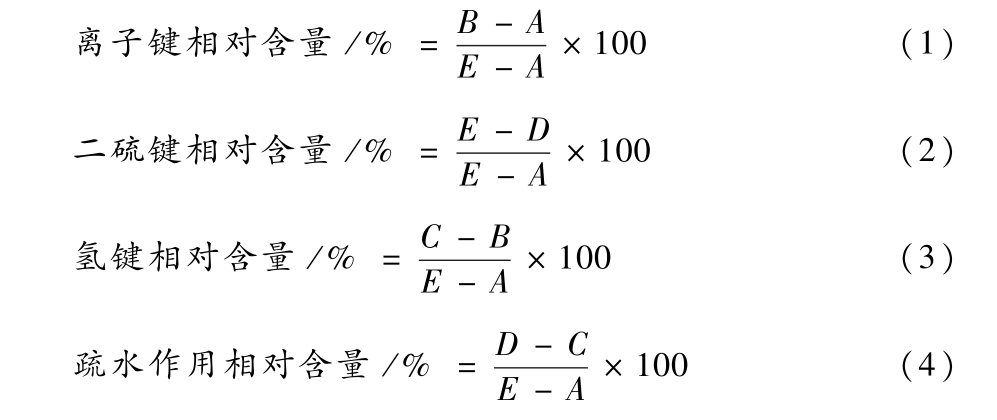
式中:A,溶解于a溶液中的蛋白质含量,g/L;B,溶解于b溶液中的蛋白质含量,g/L;C,溶解于c溶液中的蛋白质含量,g/L;D,溶解于d溶液中的蛋白质含量,g/L;E,溶解于e溶液中的蛋白质含量,g/L。
1.3.5 儿茶素组分含量测定
将待测样以7 654 × g 冷冻离心20 min,取上清液用0.45 μm滤膜过滤,采用高效液相色谱法测定。参考徐玉婕等[18]的方法稍作修改,检测条件:C18色谱柱,柱温40 ℃,流速1 mL/min。流动相:A为0.04%(体积分数)磷酸溶液,B为V(甲醇)∶V(乙腈)=3∶2。洗脱程序:0~20 min,10%~15% B;20~30 min,15%~35% B;30~ 40 min,35%~ 60% B;40~ 43 min,60%~10% B;43~52 min,10% B。以标准品绘制标准曲线,计算儿茶素组分含量。
1.3.6 浊度测定
选用散射光法,利用浊度仪检测样品的浊度。用去离子水调零,福尔马肼浊度标准溶液校准仪器。取15 mL待测样于浊度杯中消除气泡,量程取0~100 NTU进行测量,仪器自动检测散射光强度并换算为样品浊度值(NTU)。此外,还对其外观形貌进行观测。
1.3.7 表面疏水性测定
参考薛艾莲等[19]的方法稍作测定。取1 mL待测样加入200 μL 1 mg/mL溴酚蓝溶液,涡旋混匀后,以7 654 ×g 离心10 min,用去离子水将上清液稀释10倍后,在595 nm波长处测定吸光度。以溴酚蓝结合量表征表面疏水性,按公式(5)计算:
式中:A对照,不加样品的吸光度;A样品,待测样的吸光度。
1.3.8 粒径、电位测定
参考张冉冉等[20]的方法稍作修改。按1 ∶30体积比用去离子水稀释待测样,溶液的折射率设置为1.33,利用纳米粒度电位仪检测样品的粒径、多分散指数和Zeta电位。
1.3.9 抗氧化活性测定
采用DPPH自由基清除能力检测试剂盒、ABTS阳离子自由基清除能力检测试剂盒、羟自由基清除能力检测试剂盒测定,步骤参考试剂盒说明书。
1.4 数据处理与分析
所有实验重复3次,结果均以“平均值± 标准差”表示;采用Origin 2024软件和Excel 2016软件处理数据并绘图;利用SPSS 27.0软件进行ANOVA差异显著性分析,其中P <0.05表示差异显著。
2 结果与分析
2.1 温度对麦醇溶蛋白-茶多酚互作体系的荧光光谱影响
2.1.1 内源荧光光谱分析
内源荧光光谱是基于蛋白质中芳香族氨基酸残基的荧光特性变化来分析配体与蛋白质之间相互作用的光谱分析方法[15]。如图1所示,纯麦醇溶蛋白体系和麦醇溶蛋白-茶多酚互作体系均在340 nm波长附近的荧光强度最强;随着茶多酚的介入,在所有实验温度下,麦醇溶蛋白-茶多酚互作体系的荧光强度均有所降低,荧光猝灭率分别为25 ℃:40.96%,50 ℃:44.59%,75 ℃:40.64%,100 ℃:40.12%;同时,最大发射波长伴随着不同程度的红移现象,依次为25 ℃:344.4 nm→346.1 nm,50 ℃:345.5 nm→347.6 nm,75 ℃:345.4 nm →347.3 nm,100 ℃:345.3 nm →347.1 nm;这表明麦醇溶蛋白与茶多酚之间发生了显著的相互作用(P <0.05),并且温度明显影响两者的作用强度。当互作体系经50 ℃恒温处理时,其荧光淬灭率最高(44.59%),最大发射波长红移现象最明显(2.1 nm),这可能归因于适当升温诱导了麦醇溶蛋白结构的展开,使得更多的氨基酸残基暴露出来[21],为茶多酚分子中羟基的结合提供了更多的结合位点,从而增强了麦醇溶蛋白与茶多酚之间的相互作用。
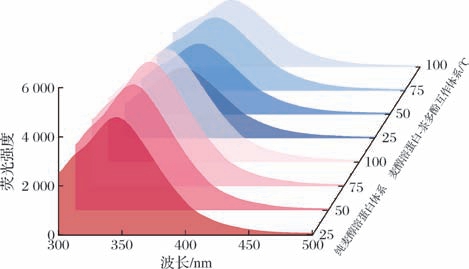
图1 温度对麦醇溶蛋白-茶多酚互作体系的内源荧光光谱影响
Fig.1 Effect of temperature on fluorescence spectra of gliadin-tea polyphenols interaction system
2.1.2 同步荧光光谱分析
同步荧光光谱是研究蛋白质中相应荧光团微环境变化的高灵敏度技术[16]。当激发波长和发射波长的固定波长差(Δλ)为15 nm时,主要反映酪氨酸残基的微环境变化;当Δλ 为60 nm时,主要反映色氨酸残基的微环境变化。由图2可知,麦醇溶蛋白-茶多酚互作体系的荧光强度均低于纯麦醇溶蛋白体系,说明酪氨酸和色氨酸均参与了麦醇溶蛋白与茶多酚间的相互作用。但在不同温度处理下,麦醇溶蛋白-茶多酚互作体系在Δλ 为15 nm时的荧光猝灭率均低于Δλ 为60 nm时;且当Δλ 为15 nm时,最大发射波长红移较小(0.1~0.5 nm),当Δλ 为60 nm时,红移较大(0.6~1.3 nm)。由此可见,同一温度下色氨酸残基对蛋白固有荧光的猝灭贡献更大,且其微环境的极性变化也更为明显。但随着处理温度的升高,互作体系的荧光猝灭率和最大发射波长的红移程度均呈现先升高后降低的趋势,并在50 ℃达到峰值,这也与内源荧光光谱分析的趋势一致。上述结果表明麦醇溶蛋白与茶多酚的结合位点更靠近于色氨酸残基,两者的相互作用主要影响色氨酸残基周围的微环境,使其极性增强、构象趋向松散,且这种变化受温度的影响明显。适度升温(≤50 ℃)可能通过增强分子热运动和蛋白部分构象的展开,促进多酚与蛋白间的结合,因此,荧光猝灭率和红移程度上升;而更高温度(75~100 ℃)则可能引发蛋白的部分变性或聚集,掩蔽部分结合位点,同时,茶多酚的分子结构可能受损(如酚羟基氧化),降低其与蛋白的结合能力,从而导致结合程度减弱。
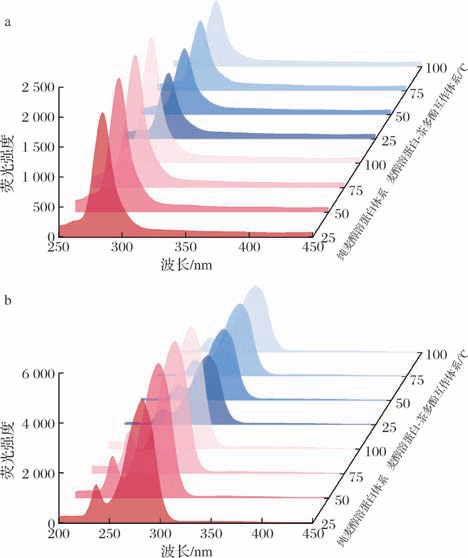
图2 温度对麦醇溶蛋白-茶多酚互作体系的同步荧光光谱影响
Fig.2 Effect of temperature on synchronous fluorescence spectra of gliadin-tea polyphenols interaction system
a-Δλ=15 nm;b-Δλ=60 nm
2.2 温度对麦醇溶蛋白-茶多酚互作体系的紫外光谱影响
紫外光谱可用来探究麦醇溶蛋白和茶多酚相互作用后蛋白的结构及化学变化[22]。如图3所示,纯麦醇溶蛋白体系和麦醇溶蛋白-茶多酚互作体系在波长210 nm附近和280 nm附近均存在一个吸收峰,其中在波长210 nm附近的吸收峰主要由多肽骨架结构C ═O产生,波长280 nm附近的吸收峰由酪氨酸和色氨酸等芳香族氨基酸残基产生[23]。随着茶多酚的介入,所有样品在不同温度处理下紫外吸收强度均显著增强。在波长210 nm附近,复合物的紫外吸收强度显著变大(P <0.05),最大吸收峰波长发生了红移(5 nm左右),说明茶多酚与麦醇溶蛋白发生了相互作用,使得蛋白的构象发生改变。在波长280 nm附近,复合物的紫外吸收强度也显著变大(P <0.05),但最大吸收峰波长发生了蓝移(4 nm左右),说明茶多酚与麦醇溶蛋白的相互作用改变了蛋白周围的微环境,使得酪氨酸和色氨酸残基中芳香杂环疏水基团更多地暴露在蛋白质表面。但随着温度的升高,紫外吸收强度呈现出“先增后减”的趋势,尤其在50 ℃时达到最大值,当温度大于75 ℃时,紫外吸收强度开始下降。由此可见,温度能改变蛋白分子内氨基酸残基的构象和微环境,进而影响其与茶多酚的相互作用。
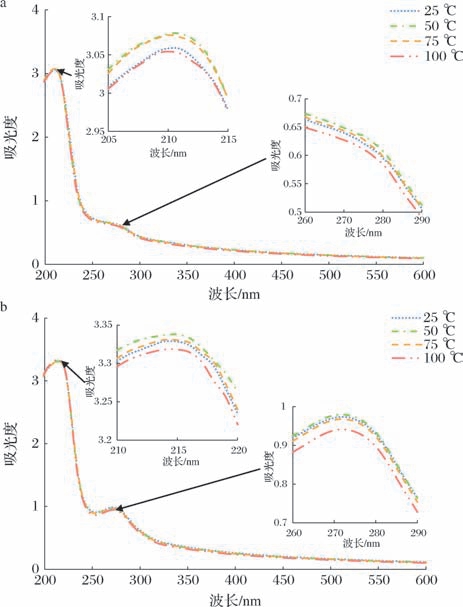
图3 温度对麦醇溶蛋白-茶多酚互作体系的紫外光谱影响
Fig.3 Effect of temperature on UV spectra of gliadin-tea polyphenols interaction system
a-纯麦醇溶蛋白体系;b-麦醇溶蛋白-茶多酚互作体系
2.3 温度对麦醇溶蛋白-茶多酚互作体系内化学作用力的影响
疏水作用、氢键、二硫键、离子键是蛋白与多酚相互作用的主要化学作用力[17]。由图4可知,在所有实验温度下,纯麦醇溶蛋白体系的主要化学作用力中疏水作用占比45%~47%、氢键占比37%左右,而二硫键和离子键所占的比例均较小。麦醇溶蛋白-茶多酚互作体系中主要化学作用力仍是疏水作用和氢键,其分别占比48%~50%、39%~40%;与纯蛋白体系相比,疏水作用和氢键的作用均有所增加,这表明麦醇溶蛋白和茶多酚的相互作用主要是通过疏水作用和氢键相结合,而二硫键和离子键的作用相对较弱。随着温度的升高,麦醇溶蛋白-茶多酚互作体系中化学作用力均为疏水作用>氢键>离子键>二硫键,说明温度不会改变蛋白与多酚相互作用的化学作用力贡献。与同一温度下的纯蛋白体系相比,麦醇溶蛋白-茶多酚相互作用的主要化学作用力中疏水作用增幅为25 ℃:6.83%,50 ℃:7.30%,75 ℃:7.09%,100 ℃:5.81%;氢键增幅为25 ℃:3.34%,50 ℃:6.43%,75 ℃:4.22%,100 ℃:4.15%;均随温度升高呈现出“先增后减”的趋势,这表明适当升温促使疏水作用和氢键的作用力增强,有利于促进麦醇溶蛋白和茶多酚的结合。其原因可能归于,温度升高初期(≤50 ℃)麦醇溶蛋白因受热而适度展开,使得内部的疏水基团和氢键位点暴露,为茶多酚羟基分子提供了更多的结合位点,从而促使疏水作用和氢键的作用力增强;当温度超过50 ℃时,将会破坏已形成的疏水作用和氢键,削弱其化学作用力。
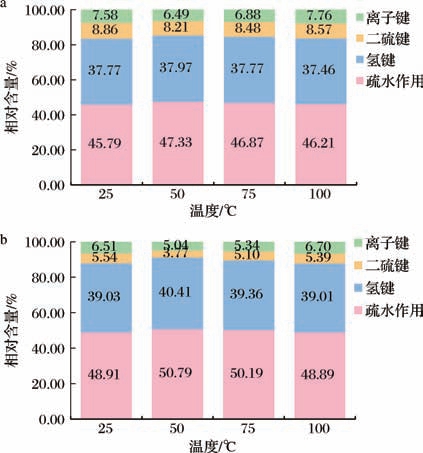
图4 温度对麦醇溶蛋白-茶多酚互作体系内化学作用力的影响
Fig.4 Effect of temperature on chemical forces in gliadin-tea polyphenols interaction system
a-纯麦醇溶蛋白体系;b-麦醇溶蛋白-茶多酚互作体系
2.4 温度对麦醇溶蛋白和茶多酚之间结合率的影响
不同温度下麦醇溶蛋白与茶多酚的相互作用,从HPLC检测结果(表1)可知,随着处理温度的升高,麦醇溶蛋白与茶多酚的结合率呈先略微上升而后显著下降的趋势;在50 ℃时,结合率最高达(50.20±0.81)%;表明适当升温有利于茶多酚与麦醇溶蛋白的疏水相互作用和氢键形成,进而提高两者的结合率。然而,当温度过高时(≥75 ℃),麦醇溶蛋白易变性,其空间结构发生改变,使得结合位点减少,导致结合率显著下降。在相同温度下,茶多酚各组分中EGCG与麦醇溶蛋白的结合率始终最高,而当高于75 ℃后,EGCG与麦醇溶蛋白的结合率出现显著下降(P <0.05)。
表1 温度对麦醇溶蛋白和茶多酚之间结合率的影响
Table 1 Effect of temperature on the binding rate between gliadin and tea polyphenols
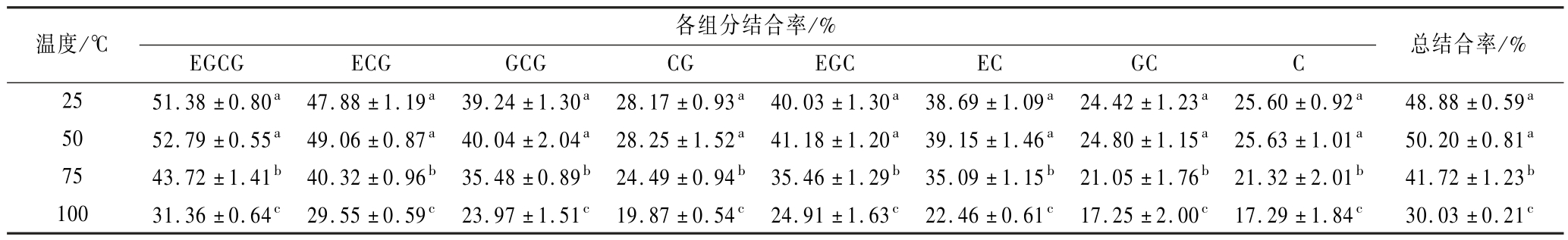
注:同列不同小写字母表示差异显著(P <0.05)(下同)。
2.5 温度对麦醇溶蛋白-茶多酚互作体系的浊度影响
浊度的测定可以验证蛋白-多酚相互作用程度及两者结合后蛋白结构的变化信息[24]。由图5所示,在不同温度处理下,纯麦醇溶蛋白体系均呈浅乳白色,浊度为48~50 NTU;麦醇溶蛋白-茶多酚互作体系均呈淡黄色,浊度为55~56 NTU。与纯蛋白体系相比,由于麦醇溶蛋白与茶多酚发生相互作用,互作体系的浊度均有升高。随着温度的升高,纯蛋白体系的浊度在25~75 ℃时变化不显著(P >0.05),当温度大于75 ℃时呈显著下降趋势(P <0.05);而麦醇溶蛋白-茶多酚互作体系的浊度呈现“先升后降”的趋势,在温度为50 ℃时,浊度最大达(56.41±0.22) NTU,说明茶多酚与麦醇溶蛋白发生了较强的相互作用,这进一步验证了2.4节中的结果。
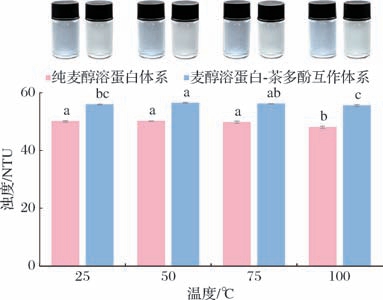
图5 温度对麦醇溶蛋白-茶多酚互作体系的浊度影响
Fig.5 Effect of temperature on turbidity of gliadin-tea polyphenols interaction system
注:不同小写字母表示差异显著(P <0.05)(下同)。
2.6 温度对麦醇溶蛋白-茶多酚复合物表面疏水性的影响
蛋白质表面疏水性反映其理化特性和空间构象特征,溴酚蓝作为一种疏水性探针,可与蛋白质表面的疏水位点结合,其结合量与蛋白质表面疏水性呈正相关[19]。如图6所示,不同温度处理下麦醇溶蛋白-茶多酚复合物的溴酚蓝结合量均高于纯麦醇溶蛋白样品,标示麦醇溶蛋白-茶多酚复合物的表面疏水性更强,由于多酚类化合物与麦醇溶蛋白相互作用后,改变了蛋白的构象,促进了疏水性氨基酸的暴露[25]。随着温度的升高,麦醇溶蛋白-茶多酚复合物的溴酚蓝结合量呈现显著的先升后降趋势(P <0.05);在50 ℃时达到最高值[(58.98±0.70) μg],说明麦醇溶蛋白-茶多酚复合物的表面疏水性最强。适当升温会诱导蛋白空间结构展开,促使内部疏水基团向蛋白表面移动;但温度过高时,会进一步促使蛋白分子聚集形成更大的聚集体,把暴露的疏水基团又重新包裹在聚集体内部[26]。
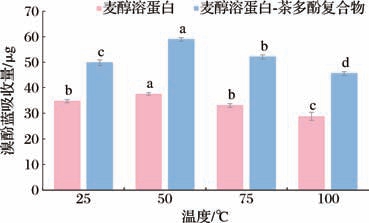
图6 温度对麦醇溶蛋白-茶多酚复合物表面疏水性的影响
Fig.6 Effect of temperature on surface hydrophobicity of gliadin-tea polyphenols complexes
2.7 温度对麦醇溶蛋白-茶多酚互作体系的粒径和电位影响
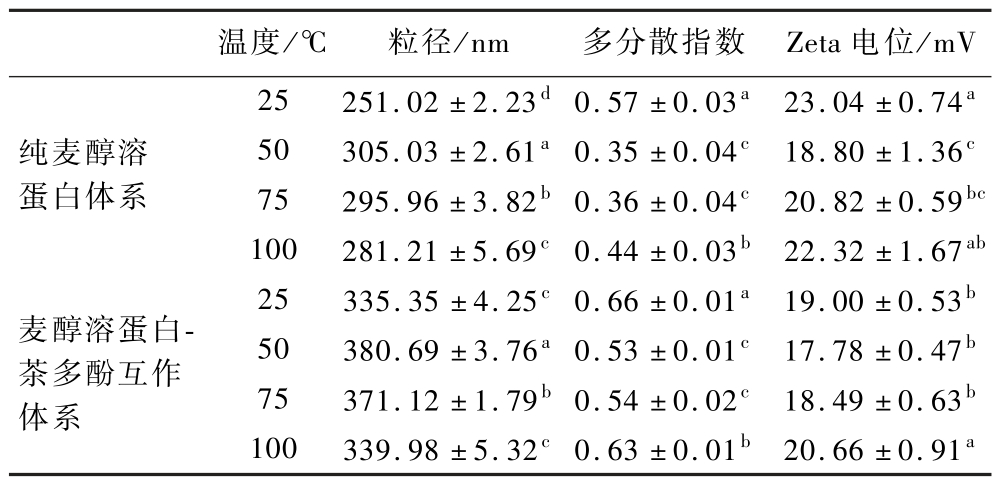
通过对麦醇溶蛋白-茶多酚互作体系中粒径、多分散指数、Zeta电位的检测,由表2可知,麦醇溶蛋白-茶多酚互作体系中粒径与多分散指数均大于纯麦醇溶蛋白体系,其Zeta电位低于纯麦醇溶蛋白体系,表明麦醇溶蛋白与茶多酚形成的复合物使粒径增大且分布变宽,粒子之间静电排斥力减弱,蛋白-多酚间的结合以疏水作用和氢键占据主导。随着温度的升高(25~100 ℃),复合物的粒径呈现“先升后降”的趋势,多分散指数和Zeta电位均却呈现“先降后升”的趋势,当温度达50 ℃时,粒径最大[(380.69±3.76) nm]、多分散指数最小(0.53±0.01)、Zeta电位最低[(17.78±0.47) mV],表明适当升温可以促进麦醇溶蛋白与茶多酚之间由疏水作用和氢键主导的相互作用,形成粒径较大且分布更均匀的复合物。由此可见,温度能调控麦醇溶蛋白与茶多酚相互作用的强度。合理升温可促使蛋白空间构象适度展开,能增强茶多酚与麦醇溶蛋白的结合;同时,由升温导致的Zeta电位下降,削弱了粒子间静电斥力,增强了麦醇溶蛋白-茶多酚间的疏水作用和氢键结合力,有利于促进形成粒径较大且分布更均匀的复合物。然而,当温度超过最优阈值(50 ℃)后,升温将破坏维持复合物结构的疏水作用、氢键等非共价作用力,同时可能会导致蛋白过度变性引发无序聚集以及茶多酚的分解,不利于麦醇溶蛋白-茶多酚复合物的形成。
表2 温度对麦醇溶蛋白-茶多酚互作体系的粒径和电位影响
Table 2 Effect of temperature on particle size and Zeta potential of gliadin-tea polyphenols interaction system
2.8 温度对麦醇溶蛋白-茶多酚互作体系的抗氧化活性影响
DPPH自由基、ABTS阳离子自由基和羟自由基的清除能力是衡量物质抗氧化活性的重要评价指标[27]。鉴于三者在自由基特性及反应机制上存在差异,仅靠单一指标难以全面表征物质的抗氧化活性。因此,将这3种指标相结合进行分析,才能更系统、全面地评价物质的抗氧化活性。由图7可知,随着温度升高,纯麦醇溶蛋白体系对3种自由基的清除率均无明显变化(<3%),因纯麦醇溶蛋白本身抗氧化活性较弱,温度对纯麦醇溶蛋白体系抗氧化能力的影响不敏感;但麦醇溶蛋白-茶多酚互作体系随着温度升高,对3种自由基的清除率均呈现先略微升高后显著下降的趋势,并显现出50 ℃的“最佳活性温度”,在此温度下互作体系对DPPH自由基清除率达(87.25±1.05)%、ABTS阳离子自由基清除率达(74.56±0.62)%、羟自由基清除率达(64.64±0.93)%,均为最高值。由此可见,麦醇溶蛋白与茶多酚互作后,源于茶多酚自身的强抗氧化能力[28],可显著增强复合物的抗氧化活性,其抗氧化能力呈现温度敏感性,这与温度对麦醇溶蛋白-茶多酚互作体系内的化学作用力、粒径、多分散指数、电位、蛋白-多酚复合物的结合率及其表面疏水性等特性的影响相一致。适度升温(≤50 ℃)由于增强麦醇溶蛋白与茶多酚的结合效率,形成更稳定的蛋白-多酚复合物,能暴露更多的抗氧化活性位点(如茶多酚的酚羟基),从而提升自由基清除能力。但高温(75~100 ℃)会导致麦醇溶蛋白与茶多酚的结合位点被破坏,复合物解离,游离态茶多酚的酚羟基易被氧化,或其分子结构被破坏,丧失部分抗氧化活性,从而降低麦醇溶蛋白-茶多酚互作体系的抗氧化活性。
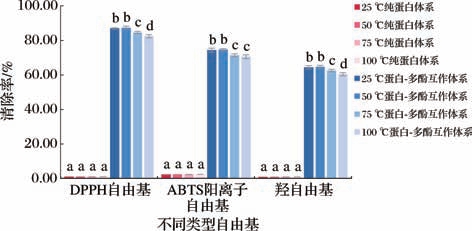
图7 温度对麦醇溶蛋白-茶多酚互作体系的抗氧化活性影响
Fig.7 Effect of temperature on antioxidant activity of gliadin-tea polyphenols interaction system
3 结论
本研究揭示了麦醇溶蛋白与茶多酚是以疏水作用和氢键为主要非共价作用力相结合,调控互作温度仅影响两者的作用强度,不会新增和改变主要化学作用力类型。温度对麦醇溶蛋白-茶多酚的互作呈现适度促进、过高抑制的规律。
在25~50 ℃内,升温对麦醇溶蛋白-茶多酚相互作用及其复合物功能呈正向调控作用。随着温度升高,疏水作用与氢键的结合效率显著提升,促使复合物的浊度、表面疏水性及粒径同步增加,且粒径分布更均匀、Zeta电位降低,相应复合物的抗氧化活性持续增强;其中50 ℃为最优作用温度,此时复合物的各项理化指标与抗氧化活性均处于最佳峰值。
当温度超过50 ℃时,高温会破坏维持麦醇溶蛋白-茶多酚复合物结构的疏水作用与氢键,导致复合物解离,显著抑制其形成。此条件下,复合物的浊度、表面疏水性及粒径均下降,粒径分布均匀性变差,其抗氧化能力也随之降低,高温对复合物的结构稳定性与功能活性具有负面效应。
综上,研究明确了麦醇溶蛋白-茶多酚复合物的最优制备温度区间(25~50 ℃,最优50 ℃),为基于该复合物的天然抗氧化剂开发、食品功能配料制备等相关工艺的温度参数优化提供了直接的实验依据与数据支撑。
[1]黄慧,李学艳,王君文,等.醇溶蛋白荷载食品功能组分的研究进展[J].食品科学,2019,40(19):318-325.HUANG H,LI X Y,WANG J W,et al.Recent progress in prolamines as a food nutrient carrier[J].Food Science,2019,40(19):318-325.
[2]LUO Q X,LUO L B,ZHAO J M,et al.Biological potential and mechanisms of Tea’s bioactive compounds: An Updated review[J].Journal of Advanced Research,2024,65:345-363.
[3]GÜNAL-KÖROGˇLU D,LORENZO J M,CAPANOGLU E.Plant-Based Protein-Phenolic Interactions: Effect on different matrices and in vitro gastrointestinal digestion[J].Food Research International,2023,173:113269.
[4]HE W J,CHEN N,YU Z L,et al.Gliadin interacted with tea polyphenols: Potential application and action mechanism[J].International Journal of Food Sciences and Nutrition,2022,73(6):786-799.
[5]EBRAHIMI P,LANTE A N,GROSSMANN L.Protein-polyphenol complexation vs.conjugation: A review on mechanisms,functional differences,and antioxidant-emulsifier roles[J].Food Hydrocolloids,2025,169:111590.
[6]陈晓玲,管维良,施佩影,等.谷物醇溶蛋白与植物多酚的互作机理及应用研究进展[J].食品科学,2022,43(17):353-361.CHEN X L,GUAN W L,SHI P Y,et al.Review on recent progress in the mechanism and application of interaction between prolamins and polyphenols[J].Food Science,2022,43(17):353-361.
[7]SONG Y Q,ZHAO Y,YAO G L,et al.Heat treatment effect on whey protein-epigallocatechin gallate interaction: A fluorescence spectroscopic analysis[J].Food Chemistry: X,2023,20:100917.
[8]TOSIF M M,NAJDA A,BAINS A,et al.A comprehensive review on the interaction of milk protein concentrates with plant-based polyphenolics[J].International Journal of Molecular Sciences,2021,22(24): 13548.
[9]文鹏程,焦瑶瑶,张卫兵,等.茶多酚对牛奶蛋白结构的影响[J].食品与发酵工业,2020,46(8):40-47.WEN P C,JIAO Y Y,ZHANG W B,et al.Effect of tea polyphenols on the structure of milk protein[J].Food and Fermentation Industries,2020,46(8):40-47.
[10]QIE X J,CHEN Y,QUAN W,et al.Analysis of β-lactoglobulinepigallocatechin gallate interactions: The antioxidant capacity and effects of polyphenols under different heating conditions in polyphenolic-protein interactions[J].Food &Function,2020,11(5):3867-3878.
[11]GE G,ZHAO J S,ZHENG J B,et al.Green tea polyphenols bind to soy proteins and decrease the activity of soybean trypsin inhibitors (STIs) in heated soymilk[J].Food &Function,2022,13(12):6726-6736.
[12]URADE R,SATO N,SUGIYAMA M.Gliadins from wheat grain:An overview,from primary structure to nanostructures of aggregates[J].Biophysical Reviews,2018,10(2):435-443.
[13]PETKER K,PEYRONEL F,PINK D,et al.Probing the particle formation and aggregation behaviour of gliadin in aqueous ethanol with ultra-small-and small-angle X-ray scattering [ J].Food Hydrocolloids,2025,168:111536.
[14]李春翼,王启明,张驰,等.热诱导对麦醇溶蛋白-芦丁相互作用及其乳化特性的影响[J].2022(12):63-71.LI C Y,WANG Q M,ZHANG C,et al.Effect of heat induction on gliadin-rutin interaction and its emulsification characteristics[J].Journal of Chinese Institute of Food Science and Technology,2022(12):63-71.
[15]WANG Q M,TANG Y W,YANG Y X,et al.Interaction between wheat gliadin and quercetin under different pH conditions analyzed by multi-spectroscopy methods[J].Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2020,229:117937.
[16]余霞.茶多酚、茶黄素与蛋白质相互作用及其对茶乳酪形成的影响[D].重庆: 西南大学,2021.YU X.Interaction of Tea Polyphenols and Theaflavin with Proteins and Their Effects on the Formation of Tea Cream[D].Chongqing:Southwest University,2021.
[17]皮俊翔.茶多酚对面筋蛋白网络结构影响机制的研究[D].无锡: 江南大学,2020.PI J X.Study on the mechanism of tea polyphenols influencing gluten network structure[D].Wuxi: Jiangnan University,2020.
[18]徐玉婕,周汉琛,张晓磊,等.贮藏对祁门红茶风味品质及化学成分的影响[J].食品与发酵工业,2025,51(4):177-187.XU Y J,ZHOU H C,ZHANG X L,et al.Differences in flavor quality and chemical composition of 1-year-stored Keemun black tea[J].Food and Fermentation Industries,2025,51(4):177-187.
[19]薛艾莲,李春翼,王启明,等.超声处理对麦醇溶蛋白/芦丁相互作用及结构特性的影响[J].食品科学,2022,43(7):45-51.XUE A L,LI C Y,WANG Q M,et al.Effect of ultrasonic treatment on the interaction and structural properties of gliadin-rutin complex[J].Food Science,2022,43(7):45-51.
[20]张冉冉,王佳蓉,由远慧,等.预热处理对松仁蛋白与表没食子儿茶素没食子酸酯相互作用及其复合物结构和功能特性的影响[J].食品与发酵工业,2024,50(24):261-271.ZHANG R R,WANG J R,YOU Y H,et al.Effect of preheating treatment on interaction of pine nut kernel protein with epigallocatechin gallate and its complex structure and functional characteristics[J].Food and Fermentation Industries,2024,50(24):261-271.
[21]王立峰,朱洁,熊文飞,等.热效应对小麦醇溶蛋白起泡性与结构的影响[J].中国农业科学,2021,54(4):820-830.WANG L F,ZHU J,XIONG W F,et al.Insight into the impact of heat treatment on the foamability and structure of gliadin colloidal particles[J].Scientia Agricultura Sinica,2021,54(4):820-830.
[22]WANG Y,ZHANG J,ZHANG L F.Study on the mechanism of non-covalent interaction between rose anthocyanin extracts and whey protein isolate under different pH conditions [ J].Food Chemistry,2022,384:132492.
[23]CHENG J,LIU J H,PRASANNA G,et al.Spectrofluorimetric and molecular docking studies on the interaction of cyanidin-3-O-glucoside with whey protein,β-lactoglobulin[J].International Journal of Biological Macromolecules,2017,105(Pt 1):965-972.
[24]王丽颖.多酚与麦醇溶蛋白复合物的形成机制及结构表征[D].重庆: 西南大学,2018.WANG L Y.Fabrication Mechanism and Structure Characterization of Polyphenols and Gliadin Complexes[D].Chongqing: Southwest University,2018.
[25]WANG Y,XIE Y,WANG A D,et al.Insights into interactions between food polyphenols and proteins: An updated overview[J].Journal of Food Processing and Preservation,2022,46(5):e16597.
[26]张司雨,聂宇嫦,夏明杰,等.热条件下膳食纤维对面筋蛋白的影响及其在面制品中应用的研究进展[J].食品工业科技,2025,46(5):387-396.ZHANG S Y,NIE Y C,XIA M J,et al.Research progress on the effect of dietary fiber on gluten proteins under thermal treatment and its application in flour products[J].Science and Technology of Food Industry,2025,46(5):387-396.
[27]LIU X J,SONG Q B,LI X,et al.Effects of different dietary polyphenols on conformational changes and functional properties of protein-polyphenol covalent complexes[J].Food Chemistry,2021,361:130071.
[28]WANG Z K,HAN Z S,ZHANG L.Advances and outlook of tea polyphenol chemistry: A review[J].Journal of Agricultural and Food Chemistry,2025,73(37):22994-23002.