高血压是一种以动脉收缩压或舒张压升高为特征的临床综合征,可能导致心肌梗死、心力衰竭、中风和肾衰竭等多种疾病[1]。肾素-血管紧张素系统(renin-angiotensin system,RAS)是哺乳动物最重要的心血管调节通路[2],血管紧张素转化酶(angiotensinconverting enzyme,ACE)是维持肾素-血管紧张素和激肽释放酶系统(kallikrein-kinin system,KKS)之间平衡的关键酶,可以通过裂解His-Leu灭活血管舒张剂缓激肽(血管紧张素Ⅰ),生成强效血管收缩剂血管紧张素Ⅱ,引起血压升高。ACE抑制剂可以降低血管紧张素Ⅱ水平,实现降血压的作用[3-4]。目前发现的ACE抑制剂较少,且使用后还存在一些不良反应,因此,开发新的高效且低副作用的ACE抑制剂对于高血压的治疗和预防具有重要的临床意义[5]。
黄水是白酒酿造过程中起糟滴窖产生的黄色或棕黄色黏稠、浑浊液体,是白酒酿造过程的特有副产物[6]。白酒酿造是以大米、糯米、高粱、玉米、小麦等粮食为原料,以酒曲为发酵剂,长时间的自然发酵过程。酒曲中的蛋白酶、糖化酶和酯化酶等各种酶系以及霉菌、细菌等微生态体系,分解利用原料中的蛋白质、淀粉等大分子物质,生成分子质量更小的多糖,寡糖、单糖、多肽、小分子肽、氨基酸、乙醇以及白酒风味组分所构成的复杂体系,伴随酒醅中的过饱和水分以及酵母有氧呼吸产生的水分,在起糟滴窖过程中一起下渗至窖池底部,形成黄水[7]。黄水中富含来自于粮食原料的植物蛋白和来自于微生物群落的菌体蛋白,在白酒酿造过程中水解成小分子的肽、氨基酸等。肽因其调节免疫力[8]、降血压[9-10]、抗氧化[11-12]、降血糖[13-14]、改善记忆[15-16]等多方面的功能活性越来越受关注,截止目前,全球已批准了100多个用于疾病诊断或治疗的多肽药物[17-18]。肽的制备方法主要有酶解法、分离提取法、化学合成法、微生物发酵法和基因重组法,而黄水相当于酶解法和微生物发酵法协同作用的蛋白水解产物,是可以直接用于分离纯化肽的低成本原料。分离鉴定黄水中的肽类化合物并研究其功能活性,可以为开发黄水的资源化利用新途径提供技术参考。黄水的资源化利用可以提升黄水的附加值,促进白酒生产企业节能减排,产生一定的经济效益和社会效益。
1 材料与方法
1.1 材料与试剂
黄水,由宜宾五粮液股份有限公司提供。
10 kDa、1 kDa、150 Da卷式膜,厦门福美科技有限公司;DA201大孔树脂,北京索莱宝科技有限公司;95%(体积分数)食用酒精,河南鑫河阳酒精有限公司;甲醇(LC-MS级)、马尿酰-组氨酰-亮氨酸(Nhippuryl-His-Leu hydrate,HHL)、马尿酸(hippuric acid,Hip),德国Sigama-Aldrich;双缩脲试剂盒,北京盒子生工有限公司;ACE,默克公司。
1.2 仪器与设备
1290系列高效液相色谱仪(HPLC)-6520B系列质谱检测器,美国Agilent公司;RNF0460多功能卷式膜设备,厦门福美科技有限公司;Milli-Q超纯水机,美国Mimpore公司;GENESYSTM 180紫外分光光度计,赛默飞世尔科技公司;RE-52AA旋转蒸发仪,上海亚荣生化仪器厂。
1.3 实验方法
1.3.1 黄水肽的提取
参考团队前期研究成果[19],采用有机溶剂沉淀法。新鲜黄水室温静置24 h,将上清液以纱布过滤除去其中的糠壳等颗粒物,得到黄水清液10 L置于60 L的塑料桶中,加入95% 的食用酒精40 L,搅匀,静置24 h,待黄水中的蛋白和多糖等大分子组分沉淀下来后,将上清液于60 ℃减压蒸馏,回收酒精,得到黄水肽提取液12 L。
1.3.2 ACE抑制肽的制备
采用膜过滤技术。分别采用10、1、0.15 kDa分子质量截留的卷式膜,以去离子水循环过膜清洗膜管2 h后备用。将1.3.1节中的黄水肽提取液与去离子水以体积比1∶2混合后,循环过10 kDa卷式膜,得到10 kDa分子截留段M1(分子质量>10 kDa),透过液进一步通过1 kDa卷式膜处理,得到1 kDa分子截留段M2(分子质量1~10 kDa),此透过液再通过0.15 kDa卷式膜处理,得到0.15 kDa分子截留段M3(分子质量0.15~1 kDa)和余液(分子质量<150 Da),即将黄水肽分段收集成M1、M2、M3三个肽段。
1.3.3 大孔树脂柱层析
将M3组分以超纯水溶解并稀释至质量浓度20 mg/ mL,上样已洗净的大孔树脂柱,流速为5 mL/min。以乙醇-水为洗脱剂,乙醇体积分数0%、20%、40%、60%、80%、100% 的比例各10 L依次进行梯度洗脱,每500 mL一瓶收集各段洗脱液,60 ℃减压蒸馏后,自然干燥,得到120个组分。
1.3.4 肽序列鉴定
采用高效液相色谱四级杆飞行时间质谱法,结合多肽从头测序技术进行肽序列测定。
色谱条件:Agilent Eclipse Plus C18 (2.1 mm ×100 mm,1.8-micron);流动相:甲醇B(液质级),超纯水A(含0.05% 甲酸),0~ 10 min,5%~ 100% B;15.1~ 20 min,100% B;20.1 min,5% B;22 min,stop;柱温30 ℃;流速0.2 mL/min;进样体积2 μL。
质谱条件:DESI源,正模式;Gas Temp:325 ℃;Drying Gas:10 L/min;Nebulizer:40 psig;Vcap:4 000 V;Fragmentor:60 V。
1.3.5 总肽含量测定
采用双缩脲法测定,参考北京盒子生工有限公司双缩脲试剂盒法。
1.3.6 ACE抑制活性测定
采用高效液相色谱法。
色谱条件:VenusilASB C18 (4.6 mm ×250 mm,5-micron);流动相:A为超纯水(含1 g/L甲酸),B为甲醇(含1 g/L甲酸),0~25 min:5%~95% B(仪器自动实现梯度变化);25.1~27 min:95% B;27.1~30 min:5% B;30 min停止洗脱。柱温为30 ℃,流速为1 mL/min,进样量为10 μL。
1.3.7 分子对接
参考钟玉旺等[20]方法,从PDB数据库(https://www.rcsb.org/)获得ACE天然晶体的3D结构(PDBID:1O8A),去水,加全氢,计算电荷,并设置为受体。利用ChemDraw 21.0.0绘制各黄水肽的3D结构,加全氢,计算电荷,设置为配体,与ACE受体蛋白对接以研究其结合模式。设置对接盒子,间距0.542 Å,活性中心坐标(A:33.953;Y:38.432;Z:38.648)。挑选最低结合能的结合方式,并采用Pymol 2.6和Lig-Plot+v.2.2.9将对接结果可视化。
1.4 数据分析
采用Origin 2021对数据进行处理分析,所有数据和分析是3次平行实验的结果,数据表示为3次的“平均值±标准差”。使用Adobe Illustrator 2025处理图像。
2 结果与分析
2.1 膜过滤对黄水肽的富集效果
膜过滤是利用膜孔隙的选择透过性进行两项分离的技术,可以实现黄水中不同分子质量区间化合物的分离。本研究首先采用有机溶剂萃取法除去黄水中的大分子蛋白和多糖等杂质成分,得到黄水提取液,再将黄水提取液通过膜过滤得到不同分子质量区间的肽组分,最后通过纳滤膜除去黄水肽提取液中大量的水分和小分子的有机酸和醇酯,即M4组分的主体成分是水,实现了黄水肽的粗制备。制备所得的M1(分子质量>10 kDa)、M2(分子质量1~10 kDa)、M3(分子质量0.15~1 kDa)组分分别于50 ℃减压浓缩后,冻干并测定总肽含量。结果如图1所示,组分M1(分子质量>10 kDa)、M2(分子质量1~10 kDa)和M3(分子质量0.15~1 kDa)的总肽含量分别为(17.64±2.1)、(34.36±3.2)、(61.75±2.8) mg/mL,其中M3的总肽含量最高,说明醇提黄水游离肽主要集中在0.15~1 kDa分子质量区间。
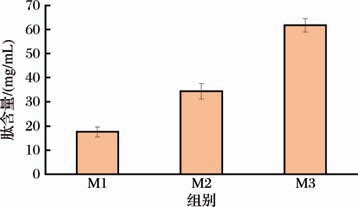
图1 各组分的肽含量对比
Fig.1 Comparison of peptide contents of each component
2.2 各分子截留段组分的ACE抑制能力
HHL在ACE的催化下快速地分解产生马尿酸(Hip)和二肽(His-Leu,HL),马尿酸在228 nm处有最大吸收。当加入血管紧张素转化酶抑制剂(angiotensin-converting enzyme inhibitors,ACEI) 样品时,ACE的活性受到抑制,马尿酸生成量减少,所以可通过高效液相色谱测定马尿酸的生成量来评估ACEI对ACE活性的抑制率[21]。M1、M2、M3组分,分别稀释至100 mg/mL的质量浓度,进行ACE抑制能力测定。结果如图2所示,各组分的ACE抑制率分别为(7.81±2.50)%、(16.25±3.72)%、(39.86±1.65)%,其中M3组分最高,可见分子质量大小与ACE抑制率有明显的关系,分子质量最小的组分有最高的ACE抑制率,这与YANG等[22]ACE抑制肽的研究结果一致。以此,选择M3组分作为后续ACE抑制肽分离鉴定的研究样本。
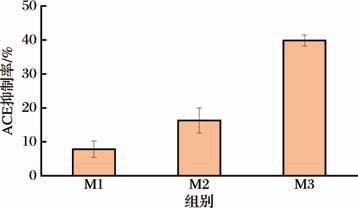
图2 各组分的ACE抑制率对比
Fig.2 Comparison of ACE inhibition rates of each component
2.3 黄水肽的分离鉴定
通过大孔树脂柱层析,进一步实现了M3组分中各黄水肽的分离富集。利用高效液相色谱四级杆飞行时间质谱分析检测1.3.3节中的120个组分,依据质荷比、同位素相对丰度、同位素比例等的相似度初步确定疑似肽类化合物,结合多肽从头测序技术,以各疑似肽的二级质谱特征离子为依据,对应解析黄水中的肽类化合物,结果如电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.043234,下同)所示。
在黄水中共分离鉴定出肽类化合物61种,分别是Val-Ala、Leu-Gly、Pro-Val、Leu-Ala、Val-Tyr、Pro-Ala、Leu-Phe、Pro-Leu、Val-Leu、Pro-Phe、Val-Phe、Leu-Leu、Pro-Tyr、Cyclo (Arg-Pro)、Cyclo(Pro-Val)、Cyclo(Glu-Leu)、Cyclo(Glu-Phe)、Cyclo(Pro-Leu)、Cyclo(Ileu-Pro)、Cyclo(Pro-Phe)、Cyclo(Val-Phe)、Cyclo(Pro-Pro)、Cyclo(Val-Val)、Cyclo(Leu-Ala)、Cyclo(Val-Ala)、Cyclo(Val-Leu)、Cyclo(Phe-Phe)、Cyclo(Leu-Phe)、Cyclo(Pro-Ala)、Cyclo(Pro-Glu)、Cyclo(Pro-Tyr)、Cyclo(Pro-Thr)、Cyclo(Phe-Ala)、Cyclo(Leu-Leu)、Cyclo(Leu-Tyr)、Cyclo(Val-Tyr)、Cyclo(Glu-Tyr)、Cyclo(Leu-Arg)、Cyclo(Phe-Arg)、Leu-Pro-ethanol、Leu-Val-ethanol、Pro-Phe-ethanol、Pro-Valethanol、Leu-Glu-propionyl、Leu-Leu-ethanol、Cyclo(Glu-Leu)-ethanol、Cyclo(Glu-Phe)-ethanol、Pro-Val-Ala、Val-Val-Ala、Pro-Ala-Leu、Val-Pro-Leu、Val-Ala-Leu、Pro-Val-Val、Val-Val-Leu、Ala-Leu-Leu、Pro-Leu-Leu、Cyclo(Pro-Glu-Leu)、Cyclo(Pro-Glu-Phe)、Cyclo(Val-Glu-Leu)、Pro-Pro-Val-Val、Leu-Leu-Leu-Ala。团队前期利用制备色谱在酿造五粮浓香型白酒的副产物黄水中分离鉴定出32个二肽和环二肽[23],此次以膜过滤技术和大孔树脂柱层析进行黄水肽的富集分离,新发现了大量的环二肽、三肽、环三肽和四肽及其衍生物。
2.4 分子对接虚拟筛选ACE抑制肽
药物(配体)与靶酶(受体)分子对接需同时考虑形状和能量的最佳匹配,配体与受体的结合能越低,形成的复合物结构越稳定。一般而言,配体与受体的结合能小于-5 kcal/mol,说明配体与受体能形成较稳定的化合物;配体与受体的结合能小于-7 kcal/mol,说明配体与受体能形成稳定的化合物[24]。分子对接结果的评价主要看结合自由能,但能量最低的构象不一定是最合理的构象,由此引入氢键数量作为评价指标,要求小分子与受体蛋白结合时需形成2个及以上氢键[25]。ACE的活性中心由S1(Ala354、Glu384和Tyr523)、S2 (Gln281、His353、Lys511、His513和Tyr520)和S′(Glu162)活性口袋构成,小肽与ACE活性中心残基形成氢键可以产生高ACE抑制活性,而疏水作用又与两者结合的稳定性密切相关[20]。以此,为从分离鉴定出的61个黄水肽中筛选出潜在的高活性ACE抑制肽,采用分子对接技术研究61个小肽与ACE靶酶之间的结合模式及结合能,结果如电子版增强出版附表2所示。
61个小肽与ACE靶酶的结合能均小于-5 kcal/mol,53个小肽均与ACE残基形成2个以上氢键作用力,形成较稳定的复合物。其中Val-Tyr、Cyclo(Arg-Pro)、Cyclo(Glu-Leu)、Cyclo(Pro-Leu)、Cyclo(Pro-Tyr)、Cyclo(Leu-Arg)、Pro-Val-Ala、Pro-Val-Val 8个小肽与ACE靶酶的结合能均小于-7 kcal/mol,形成稳定的复合物。Val-Tyr与 ACE残基 Glu376、Thr282、Asn277、Gln281、Lys511形成7个氢键,且与S2活性中心残基Gln281、Lys511形成氢键作用力,与ACE的7个残基(Asp415、His383、Val380、Phe527、Trp279、His353、Thr166)形成疏水作用(图3)。Cyclo(Arg-Pro)与ACE残基His353、Asn70、Asn66、Ser516形成4个氢键,且与S2活性中心残基His353形成氢键作用力,与ACE的9个 残基(Phe512、Lys368、Val351、Trp357、Ser355、Val518、Leu140、Glu143、Leu139)形成疏水作用(图4)。Cyclo(Glu-Leu)与ACE残基His353、Lys368、Ser355、Asn66形成6个氢键,且与S2活性中心残基His353形成氢键作用力,与ACE的8个残基(Phe512、Asn70、Trp357、Tyr62、Glu143、Val351、Leu139、Arg124)形成疏水作用(图5)。Cyclo(Pro-Leu)与ACE残基Gln281、Thr282形成2个氢键,且与S2活性中心残基Gln281形成氢键作用力,与ACE的4个残基(Glu376、His353、Val380、Trp279)形成疏水作用(图6)。Cyclo(Pro-Tyr) 与ACE残基His353、Ser355、Lys368、Asn66、Ser516形成5个氢键,且与S2活性中心残基His353形成氢键作用力,与ACE的6个残基(Glu143、Leu139、Tyr62、Phe512、Val351、Asn70)形成疏水作用(图7)。Cyclo(Leu-Arg) 与 ACE残基 Cys370、Glu162、Thr282、Asp377形成5个氢键,且与S′活性中心残基Glu162形成氢键作用力,与ACE的3个残基(Gln369、Phe527、Val380)形成疏水作用(图8)。Pro-Val-Ala与ACE残基Thr282、Glu376、Cys352、Gln281、Glu162形成5个氢键,且与S2活性中心残基Gln281,与S′活性中心残基Glu162形成氢键作用力,与ACE的7个残基(His353、Asp377、Ala354、Gln369、Asp453、Val380、Trp279)形成疏水作用(图9)。Pro-Val-Val与ACE残基Glu376、Gln281形成2个氢键,且与S2活性中心残基Gln281形成氢键作用力,与ACE的10个残基(His353、Glu162、Asp377、Gln369、Asp453、Thr282、Asn277、Ala354、Val380、Trp279) 形成疏水作用(图10)。8个小肽均与ACE活性中心残基形成氢键作用和疏水作用,表现出潜在的ACE抑制活性,是潜在的ACE抑制肽,具有一定的研究价值。
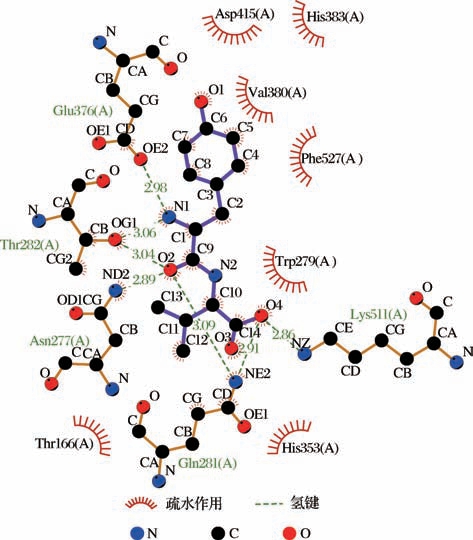
图3 肽Val-Tyr与ACE对接构象图
Fig.3 Conformation diagram of peptide Val-Tyr docking with ACE
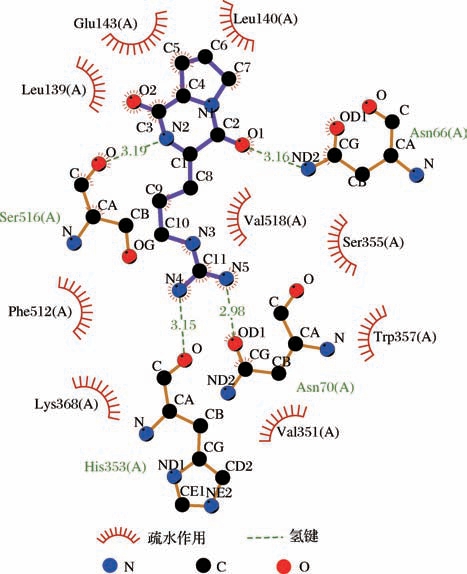
图4 肽Cyclo(Arg-Pro)与ACE对接构象图
Fig.4 Conformation diagram of peptide Cyclo(Arg-Pro)docking with ACE
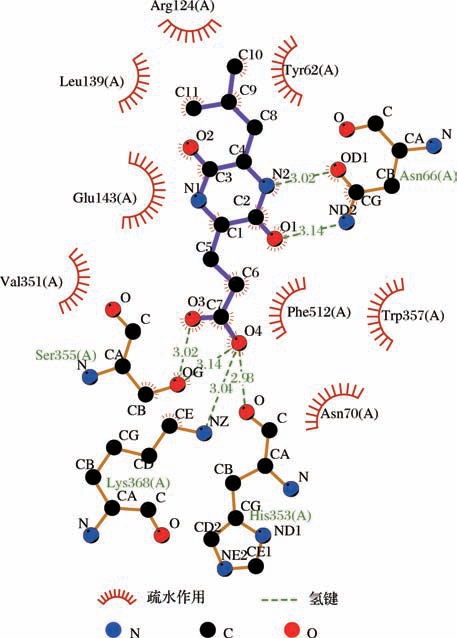
图5 肽Cyclo(Glu-Leu)与ACE对接构象图
Fig.5 Conformation diagram of peptide Cyclo(Glu-Leu)docking with ACE
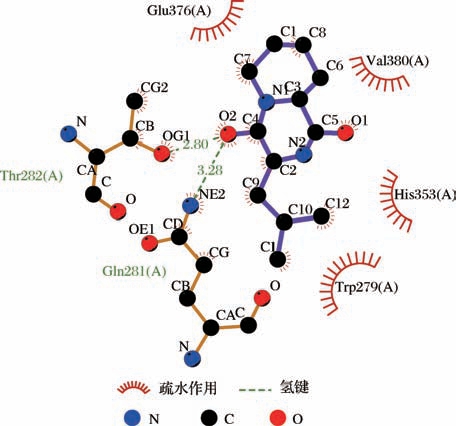
图6 肽Cyclo(Pro-Leu)与ACE对接构象图
Fig.6 Conformation diagram of peptide Cyclo(Pro-Leu)docking with ACE
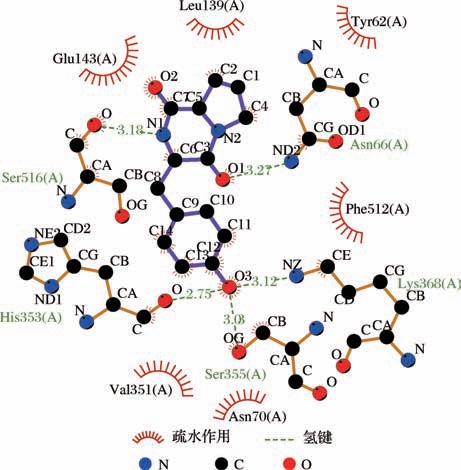
图7 肽Cyclo(Pro-Tyr)与ACE对接构象图
Fig.7 Conformation diagram of peptide Cyclo(Pro-Tyr)docking with ACE
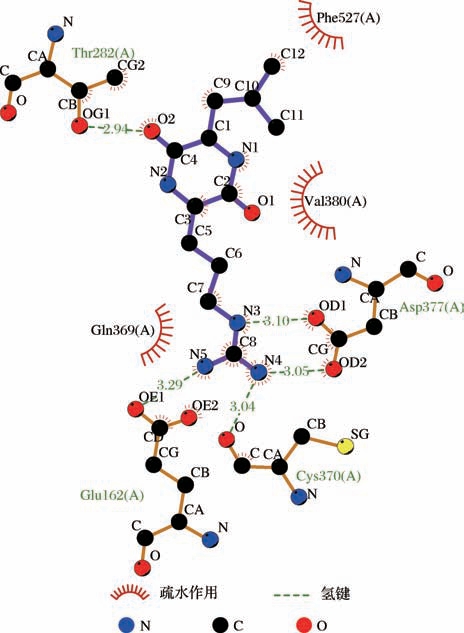
图8 肽Cyclo(Leu-Arg)与ACE对接构象图
Fig.8 Conformation diagram of peptide Cyclo(Leu-Arg)docking with ACE
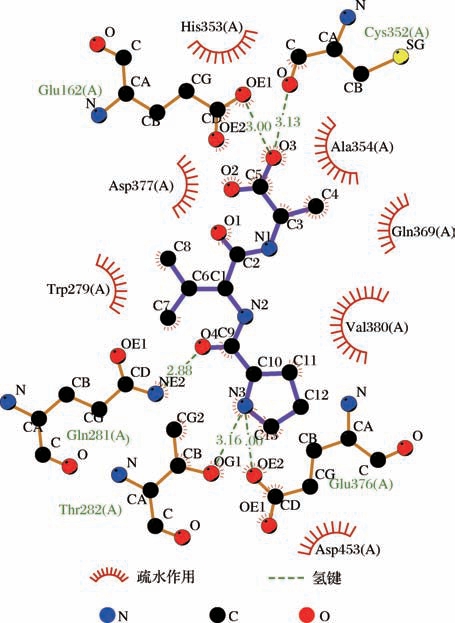
图9 肽Pro-Val-Ala与ACE对接构象图
Fig.9 Conformation diagram of peptide Pro-Val-Ala docking with ACE
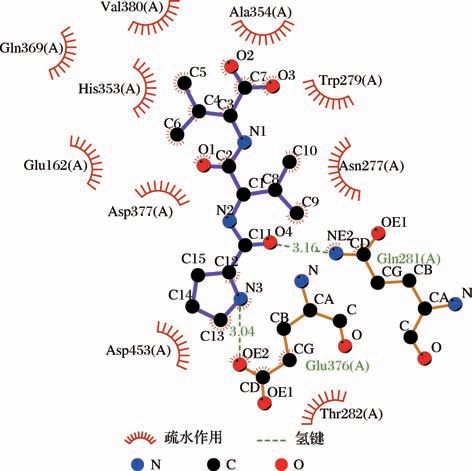
图10 肽Pro-Val-Val与ACE对接构象图
Fig.10 Conformation diagram of peptide Pro-Val-Val docking with ACE
3 结论与讨论
综合利用有机溶剂沉淀、膜过滤技术,大孔树脂柱层析等分离技术,高效液相色谱-四级杆飞行时间质谱分析技术,首次从黄水中分离鉴定出61个小肽。利用分子对接虚拟筛选ACE抑制肽结果表明,Val-Tyr、Cyclo (Arg-Pro)、Cyclo (Glu-Leu)、Cyclo (Pro-Leu)、Cyclo(Pro-Tyr)、Cyclo(Leu-Arg)、Pro-Val-Ala、Pro-Val-Val 8个小肽与ACE靶酶的结合能均小于-7 kcal/mol,且能与ACE活性中心残基形成氢键和疏水作用力,形成稳定的复合物,表现出潜在的高ACE抑制活性,是潜在的ACE抑制肽,具有深入研究价值。
本研究旨在分离鉴定黄水中可能存在的活性肽,并初步探讨其中潜在的ACE抑制肽,为黄水肽可能在ACE抑制剂方面的开发利用提供理论参考,但仍需进一步通过分离纯化或化学合成的方式获得8个小肽的纯品,以深入研究其ACE抑制效果、药代动力学特性及安全性等,以验证分子对接结果的可靠性。
[1]DZAU V J,HODGKINSON C P.Precision hypertension[J].Hypertension,2024,81(4):702-708.
[2]CAREY R M.The intrarenal renin-angiotensin system in hypertension[J].Advances in Chronic Kidney Disease,2015,22(3):204-210.
[3]BAKHLE Y S.How ACE inhibitors transformed the renin-angiotensin system[J].British Journal of Pharmacology,2020,177(12):2657-2665.
[4]JOBE A,ANTONY P,ALTABBAL S,et al.Interaction of hemorphins with ACE homologs[J].Scientific Reports,2023,13:3743.
[5]CUTRELL S,ALHOMOUD I S,MEHTA A,et al.ACE-inhibitors in hypertension:A historical perspective and current insights[J].Current Hypertension Reports,2023,25(9):243-250.
[6]王子豪,黄平,郑佳,等.白酒酿造副产物黄水研究现状及综合利用研究进展[J].中国酿造,2023,42(4):20-28.WANG Z H,HUANG P,ZHENG J,et al.Research progress and comprehensive utilization of Huangshui,a by-product from Baijiu brewing[J].China Brewing,2023,42(4):20-28.
[7]谢旭,黄永军,洪胜,等.黄水形成及其对酒醅风味物质影响的研究[J].酿酒,2019,46(4):20-23.XIE X,HUANG Y J,HONG S,et al.Study on the regularity of yellow water and its influence to the fermented grains[J].Liquor Making,2019,46(4):20-23.
[8]李富强,张廷新,朱丽萍,等.食物蛋白源免疫调节肽研究进展[J].食品与发酵工业,2022,48(1):308-314.LI F Q,ZHANG T X,ZHU L P,et al.Advance of immunomodulatory peptides from dietary-protein source[J].Food and Fermentation Industries,2022,48(1):308-314.
[9]MA K E,WANG Y J,WANG M J,et al.Antihypertensive activity of the ACE-renin inhibitory peptide derived from Moringa oleifera protein[J].Food &Function,2021,12(19):8994-9006.
[10]PRANGTHIPP,PANBANGRED W,REAMTONG O.Potential antihypertensive activity of novel peptides from green basil leaves[J].BMC Complementary and Medicine and Therapies,2023,23(1):282.
[11]GUO H K,GUO S Y,LIU H M.Antioxidant activity and inhibition of ultraviolet radiation-induced skin damage of Selenium-rich peptide fraction from selenium-rich yeast protein hydrolysate [ J].Bioorganic Chemistry,2020,105:104431.
[12]YU X,CHEN Y N,QI Z G,et al.Preparation and identification of a novel peptide with high antioxidant activity from corn gluten meal[J].Food Chemistry,2023,424:136389.
[13]HUANG T H,LIU P Y,LIN Y L,et al.Hypoglycemic peptide-enriched hydrolysates of Corbicula fluminea and Chlorella sorokiniana possess synergistic hypoglycemic activity through inhibiting α-glucosidase and dipeptidyl peptidase-4 activity[J].Journal of the Science of Food and Agriculture,2022,102(2):716-723.
[14]LI W H,FU X H,ZHANG T Y,et al.Isolation and identification of an α-glucosidase inhibitory peptide from extruded soybean protein and its hypoglycemic activity in T2DM mice[J].Food &Function,2023,14(9):4288-4301.
[15]于晓晨,李臻,刘欣然,等.乳清蛋白肽对衰老模型小鼠的抗氧化和学习记忆改善作用[J].中国食物与营养,2021,27(12):61-66;89.YU X C,LI Z,LIU X R,et al.Effects of whey protein peptide on antioxidant and learning and memory improvement in aging model mice[J].Food and Nutrition in China,2021,27(12):61-66;89.
[16]WANG S G,SU G W,ZHANG X,et al.Characterization and exploration of potential neuroprotective peptides in walnut (Juglans regia) protein hydrolysate against cholinergic system damage and oxidative stress in scopolamine-induced cognitive and memory impairment mice and zebrafish[J].Journal of Agricultural and Food Chemistry,2021,69(9):2773-2783.
[17]DE LA TORRE B G,ALBERICIO F.The pharmaceutical industry in 2023:An analysis of FDA drug approvals from the perspective of molecules[J].Molecules,2024,29(3):585.
[18]聂彩辉,徐寒梅.多肽药物的发展现状[J].药学进展,2014,38(3):196-202.NIE C H,XU H M.Current development of peptide drugs[J].Progress in Pharmaceutical Sciences,2014,38(3):196-202.
[19]廖勤俭,郭艳,周韩玲,等.环(酪氨酸-亮氨酸)的制备方法:中国,CN202211594040.4[P].2024-12-13.LIAO Q J,GUO Y,ZHOU H L,et al.The preparation method of peptide cyclo(Tyr-Leu):China,CN202211594040.4[P].2024-12-13.
[20]钟玉旺,徐万莉,范尧珠,等.辣木籽ACE抑制肽的分离纯化、结构鉴定及其体外活性评价[J].食品科学,2023,44(24):118-126.ZHONG Y W,XU W L,FAN Y Z,et al.Isolation,structural identification and in vitro activity evaluation of angiotensin-converting enzyme inhibitory peptides from Moringa oleifera seeds[J].Food Science,2023,44(24):118-126.
[21]姜瞻梅,田波,吴刚,等.高效液相色谱法快速测定降血压肽的血管紧张素转换酶抑制活性[J].食品与发酵工业,2007,33(8):122-126.JIANG Z M,TIAN B,WU G,et al.Fast determination of inhibitory activity of antihypertensive peptides by high performance liquid chromatography[J].Food and Fermentation Industries,2007,33(8):122-126.
[22]YANG G L,QIN S,LI W J.Purification and characterization of a novel angiotensin I-converting enzyme-inhibitory peptide derived from Alaska pollack skins[J].Journal of Food Science,2021,86(6):2457-2467.
[23]廖勤俭,安明哲,李杨华,等.酒糟黄水中二肽和环二肽的研究[J].酿酒科技,2018(10):17-23.LIAO Q J,AN M Z,LI Y H,et al.Study of dipeptide and cyclodipeptide in yellow water of distillers grains[J].Liquor-Making Science &Technology,2018(10):17-23.
[24]CRAMPON K,GIORKALLOS A,DELDOSSI M,et al.Machinelearning methods for ligand-protein molecular docking[J].Drug Discovery Today,2022,27(1):151-164.
[25]STANZIONE F,GIANGRECO I,COLE J C.Use of molecular docking computational tools in drug discovery[J].Progress in Medicinal Chemistry,2021,60:273-343.