植物乳植杆菌Lactiplantibacillus plantarum 广泛分布于水果和蔬菜中,其通常可以产生酸性代谢物降低环境pH,抑制致病菌和腐败菌等微生物的生长,进而表现出广谱抑菌性[1-2]。植物乳植杆菌也被证明是益生菌的重要来源之一,已有研究发现其可能具有调节肠道菌群平衡、增强免疫调节作用、抗氧化与抗炎等功效。因此,将植物乳植杆菌负载于食用基材中制备可食用乳酸菌保鲜膜表现出广阔的市场应用前景。LÓPEZ DE LACEY等[3]将嗜酸乳杆菌和双歧杆菌加入明胶涂层中应用于鱼肉保鲜,可显著抑制腐败菌的增殖,延长鱼肉的货架期。TEMIZ等[4]将鼠李糖乳酪杆菌和菊粉制备成保鲜膜并应用于草莓保鲜,所制备的保鲜膜在整个草莓贮藏期间能够有效减少草莓失重并抑制霉菌的生长,从而保持草莓正常的理化性质。
研究团队前期从发酵泡菜中筛选获得一株植物乳植杆菌SCSL-1,其不仅具有良好的抑菌活性,同时表现出调节肠道菌群、降血糖和血脂的益生作用。本论文制备了负载植物乳植杆菌SCSL-1的可食用保鲜膜,探究不同甘油与明胶配比对保鲜膜理化参数、成膜性能,以及菌株在膜贮藏过程中活菌数变化的影响,进而确定保鲜膜制备的优化基料参数,并对其进行微观形貌表征。在此基础上,将负载乳酸菌保鲜膜应用于芒果保鲜并进行评价并取得良好的效果。研究结果可望为新型果蔬保鲜材料的开发与应用提供有价值的参考。
1 材料与方法
1.1 菌株与试剂
植物乳植杆菌SCSL-1 (贮藏编号:CCTCC M 20231830)由前期工作中从发酵泡菜中筛选获得。霉菌由中国热带农业科学院热带生物技术研究提供。菌株在使用前活化转接2次并制成菌悬液,置于4 ℃保藏待用。明胶和甘油为食品级试剂,其他试剂均为国产分析纯。
1.2 仪器与设备
CM-5色度色差仪,柯尼卡美能达有限公司;UV-6000PC紫外可见分光光度计,上海元析仪器有限公司;C-2030高效液相色谱仪,美国安捷伦科技公司;Nicolet iS10红外光谱仪、Azetc X-Max电子扫描电镜,美国赛默飞世尔科技公司。
1.3 实验方法
1.3.1 负载菌株SCSL-1可食用保鲜膜的制备
取3.5 g明胶(gelatin,GE)加入100 mL蒸馏水中,于40 ℃搅拌溶解。分别加入0 g、0.7 g、1.4 g和2.1 g甘油(甘油添加量为明胶质量的0%、20%、40%、60%,质量分数) 并混合15 min,80 ℃水浴30 min,冷却至室温后加入菌株SCSL-1菌悬液,得到菌浓度为109 CFU/mL的不同甘油含量的成膜液[5]。取15 mL成膜液于内径9 cm无菌培养皿中,37 ℃静置12 h。然后将干燥后薄膜剥离并置于含有饱和硝酸镁溶液的干燥器中室温下平衡72 h,再分别于5 ℃、10 ℃和25 ℃下贮藏。
1.3.2 可食用保鲜膜中活菌数的测定
采用涂布计数法测定保鲜膜中活菌数。取0.2 g含有乳酸菌的薄膜,并加入1.8 mL无菌生理盐水,于37 ℃振荡溶解。用无菌生理盐水梯度稀释,并于MRS固体琼脂上涂布,37 ℃培养48 h后计数并表示为lg CFU/g。
1.3.3 可食用保鲜膜厚度、含水量、溶胀率和水溶性的测定
厚度根据GB/T 6672—2001《塑料薄膜和薄片厚度测定 机械测量法》进行测量,将薄膜裁成2 cm ×2 cm的样条,采用游标卡尺测量厚度,单位为μm。可食用保鲜膜的含水量、溶胀率和水溶性的测定方法依据SUN等[6]方法进行,单位均表示为%。
1.3.4 可食用保鲜膜水蒸气透过率(water vapor permeability,WVP)和力学性能的测定
采用拟杯子法测定可食用保鲜膜的WVP[7],单位为g/(Pa·s·m)。取10 g氯化钙干燥剂于试管中,将可食用保鲜膜固定在试管口并置于干燥器中,间隔1 d测定试管质量变化。依据国家标准GB/T 1040.2—2022《塑料 拉伸性能的测定 第2部分:模塑和挤塑塑料的试验条件》,采用AI-7000S拉力试验机测定薄膜的拉伸强度(tensile strength,TS)和断裂伸长率(elongation at break,EB),单位分别为MPa和%。
1.3.5 色度和透光率的测定
采用色差仪测定可食用保鲜膜的色度,测试结果表示为L∗、a∗、b∗和ΔE 值,每个样品平行测试6次,结果取“平均值± 标准差”。采用紫外分光光度计测定可食用保鲜膜在280 nm和550 nm下的透光率T280nm和T550nm,以考察薄膜的抗紫外线和可见光性能。
1.3.6 扫描电镜(scanning electron microscopy,SEM)和傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)分析
采用SEM在5~15 kV工作电压和1 500~10 000放大倍率对可食用保鲜膜表面形貌进行观察。利用ATR Golden Gate的FTIR光谱仪对薄膜的FTIR进行分析,分辨率为4 cm-1。
1.3.7 负载乳酸菌可食用保鲜膜在芒果贮藏保鲜中的应用
选择大小、颜色均匀且无明显缺陷的芒果,用0.05% (质量分数)次氯酸钠水溶液消毒,然后用蒸馏水冲洗,自然干燥。测试样品分为6组,a)空白组:无膜保鲜;b)GE:1.4 g甘油涂层保鲜;c)GE+L.P:含乳酸菌的1.4 g甘油涂层保鲜;d)穿刺空白组:取霉菌孢子穿刺芒果;e)穿刺GE:取霉菌孢子穿刺芒果后涂层保鲜;f)穿刺GE +L.P:取霉菌孢子穿刺后含菌涂层保鲜。所有样品在室温[(25±2) ℃]下贮藏10 d,间隔2 d测定芒果的患病率(%)和病变直径(mm)。患病率是以患病水果的百分比计算,当水果受伤区域外的可见病变范围大于1 mm宽时,认为是患病水果。通过数字游标卡尺测量病变直径以反映水果患病严重程度。
2 结果与分析
2.1 不同甘油含量下可食用保鲜膜贮藏过程中乳酸菌的消长规律
不同甘油含量的可食用保鲜膜贮藏在25 ℃、10 ℃和5 ℃下乳酸菌的消长情况如图1所示。随着贮藏时间的延长,可食用保鲜膜中活菌数呈现逐渐降低趋势,且乳酸菌在5 ℃的消减速率明显低于10 ℃和25 ℃的情况。未添加甘油、甘油添加量为0.7 g、1.4 g、2.1 g的含菌保鲜膜在5 ℃贮藏14 d时活菌数分别下降0.51、2.42、2.24、1.91个数量级。KHODAEI等[8]发现明胶薄膜中植物乳植杆菌在4 ℃下贮存42 d内活菌数基本不变。此外,随着保鲜膜中甘油添加量的增加,负载乳酸菌数量在贮藏过程中的下降速率越快,甘油添加量为0.7 g、1.4 g、2.1 g的含菌保鲜膜在25 ℃贮藏14 d时活菌数分别为6.40、6.05、4.50 lg CFU/g,未添加甘油的含菌保鲜膜在5 ℃贮藏14 d时活菌数仅下降0.51个数量级,显著低于甘油添加组(下降1.91~2.42个数量级)(P <0.05)。此外,在25 ℃贮藏14 d后,40%与60%甘油组的活菌数(6.05、4.50 lg CFU/g)存在显著差异(P <0.05),表明高甘油含量显著加速了菌体死亡。乳酸菌在贮藏过程中通过糖酵解产酸,导致pH下降,当pH <3.6时,酶活性受抑制,乳酸菌数量呈总体下降趋势;此外,随着贮藏时间延长营养物质逐渐耗尽,同时乳酸积累形成负反馈,抑制菌体生长。在5 ℃低温下,乳酸菌代谢近乎停滞,进入休眠状态,活菌数基本保持稳定。
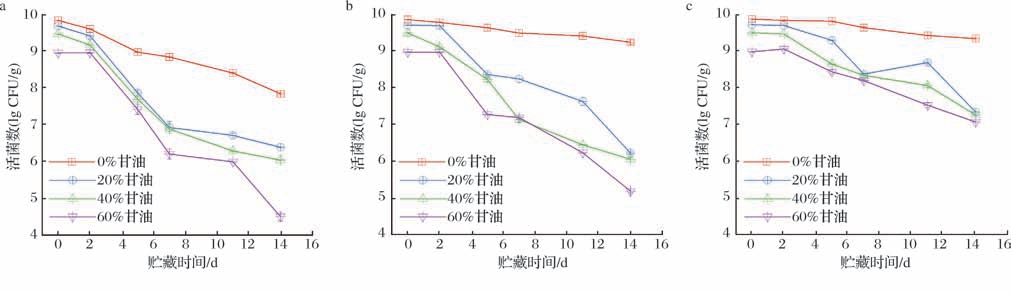
图1 在25、10、5 ℃贮存期间明胶薄膜中植物乳植杆菌SCSL-1的活菌数量变化
Fig.1 Changes in the viable counts of L.plantarum SCSL-1 in gelatin films during storage at 25 ℃,10 ℃,and 5 ℃
a-25 ℃;b-10 ℃;c-5 ℃
2.2 不同甘油含量下可食用保鲜膜厚度、含水量、溶胀率和水溶性的变化规律
薄膜厚度对水和气体的传输以及食品外观等方面起着重要的作用,含水量则表明了膜内组分与水的亲和力,也是保障食品质量的重要指标。如图2所示,随着甘油含量的增加,薄膜的厚度以及含水量呈现逐渐增加的趋势(P <0.05),原因是甘油可以增加明胶膜基质的流动性和自由体积,从而提高薄膜厚度和水分含量[9]。同时结果也显示,菌株SCSL-1的添加基本未改变薄膜的厚度和含水量(P >0.05),SHAHRAMPOUR等[10]也报道过添加益生菌对薄膜厚度没有显著影响。
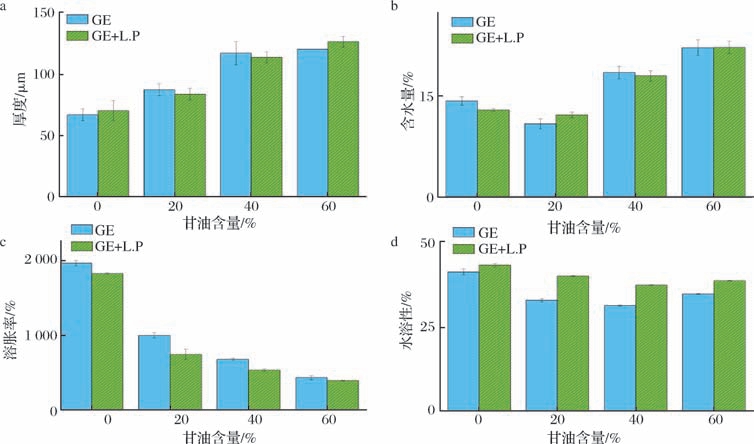
图2 不同甘油含量下薄膜厚度、含水量、溶胀率和水溶性的变化规律
Fig.2 Effect of glycerol content on film thickness,moisture content,swelling degree,and water solubility
a-厚度;b-含水量;c-溶胀率;d-水溶性
薄膜的溶胀率和水溶性则是决定薄膜耐水性的重要指标,膜的耐水性越好,应用范围一般更广。如图2所示,随着甘油含量增加,明胶薄膜的溶胀率与水溶性呈现下降的趋势。在鹰嘴豆粉中增加2% 甘油和波斯胶中增加0.3% 甘油均会引起薄膜溶胀率的降低。值得注意的是,添加菌株SCSL-1后明显降低了薄膜的溶胀率,增加了水溶性(P <0.05)。这与KHODAEI等[11]研究报道分别在明胶膜中添加植物乳植杆菌、干酪乳酪杆菌、博拉氏酵母菌会增加薄膜水溶性的结果一致。所以甘油的添加会增大明胶薄膜的厚度和含水量,减小溶胀率与水溶性,植物乳植杆菌SCSL-1的添加主要降低了薄膜的溶胀率,增加了水溶性。
2.3 不同甘油含量下可食用保鲜膜WVP变化规律
水分是导致食物变质的主要因素,薄膜作为食品表层屏障在阻隔食物与空气中的水分交换和其他不良反应的发生等方面起着重要作用。如图3所示,薄膜中的WVP随甘油含量的增加呈现增大的趋势,这与高直链淀粉薄膜的WVP随着增塑剂含量的增加而增加的变化情况一致[12]。甘油作为亲水性小分子,其羟基会竞争性破坏明胶蛋白链间氢键,使结构松散,增加水蒸气吸附与渗透。因此,甘油含量越低,薄膜结构越致密,WVP越低。此外,添加菌株SCSL-1后,各甘油含量下薄膜的WVP与对照相比均无显著变化(P >0.05),表明决定膜WVP的主要因素是明胶-甘油基质的结构特性。
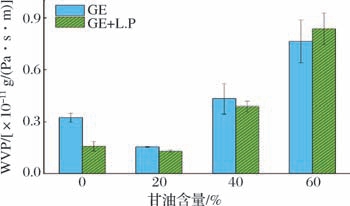
图3 薄膜的WVP
Fig.3 WVP of films
2.4 不同甘油含量下可食用保鲜膜的力学性质
良好的机械性能是用作食品包装可食用薄膜的基本力学要求之一,保护食品在贮运过程中的完整性,也是判断包装膜耐久性的依据。如图4所示,随着甘油含量增加,薄膜的TS逐渐减少,而EB逐渐上升(P <0.05)。这可能是由于明胶与甘油相互作用形成氢键,减少了蛋白质分子间作用力,提高了材料延展性,降低了材料强度[13]。同时,添加菌株SCSL-1并不会改变薄膜的力学特性(P >0.05),GIALAMAS等[14]也得到了同样的结论。值得注意的是,20%甘油的明胶薄膜EB仅为8.14%,与0%甘油的明胶基薄膜之间无显著性差异(P >0.05)。综上,添加40%甘油的明胶薄膜力学性质最佳,且添加菌株SCSL-1不会改变薄膜的力学性质。值得注意的是,薄膜的TS还与WVP呈显著负相关(P <0.05)。明胶分子链形成的氢键网络结构有助于提升薄膜TS,但可能对水蒸气透过有阻碍作用,导致薄膜WVP下降。甘油加入后会破坏原有氢键网络结构,同时易于形成水分子扩散通道,使薄膜WVP升高。
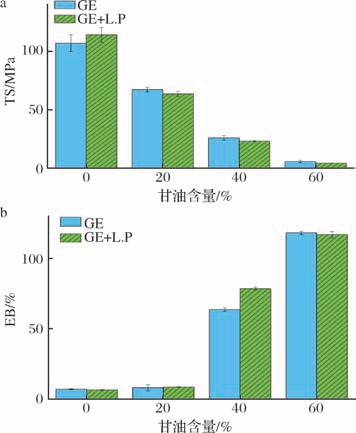
图4 不同甘油含量下薄膜的TS与EB区别
Fig.4 TS and EB of films with different glycerol content
a-TS;b-EB
2.5 不同甘油含量下可食用保鲜膜的光学性质
附着于食物表面的薄膜颜色会直接影响消费者对产品的认识和喜好度,薄膜的光学特性是影响偏好的重要特征。随着甘油含量的增加,薄膜L∗值和b∗值分别呈现减小和增大的趋势,如表1所示,随着甘油含量从0%增加至60%,薄膜的L∗值(亮度)显著降低(P <0.05),且各甘油水平间多数存在显著差异(P <0.05)。然而,在相同甘油含量下,比较GE与GE +L.P组,其L∗、a∗、b∗值基本未发生明显变化,证实菌株SCSL-1添加未改变薄膜的色泽。同样,SETTIER-RAMÍREZ等[15]将乳酸乳球菌乳酸亚种掺入含有蛋白质的聚乙烯醇薄膜后,薄膜的颜色并未变化。所以菌株SCSL-1的加入不会引起明胶薄膜外观的变化[16]。
表1 薄膜的颜色和透过率
Table 1 Color and transmittance of films
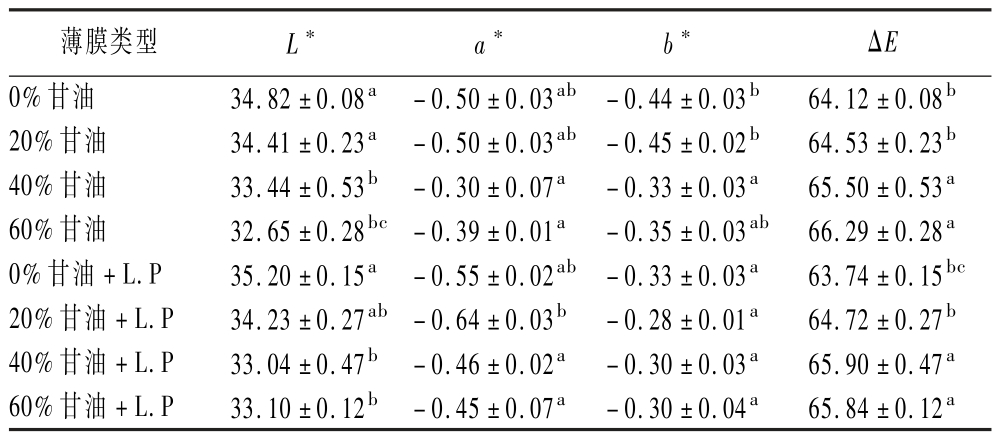
注:不同小写字母表示组间差异显著(P <0.05),相同小写字母表示组间差异不显著(P >0.05)。
薄膜的光阻隔性能可以减少包装食品中的脂质过氧化等有害化学反应,选择具备较强抗紫外线和可见光的薄膜作为食品包装材料对防止产品颜色褐变、延长产品货架期等是十分重要的。结果如图5所示,不同甘油含量的明胶薄膜在550 nm的透过率无显著差别(P >0.05),约为89.81%,但添加菌株SCSL-1后,薄膜的透过率均有不同程度的下降,平均降低了3.49%。值得注意的是,薄膜在280 nm的透过率普遍较低,约为30.99%,且在添加菌株SCSL-1后透过率显著下降(P <0.05),平均为4.69%。分析是由于明胶蛋白中含有色氨酸、酪氨酸和苯丙氨酸等在280 nm附近有强吸收的氨基酸残基,使得明胶薄膜在280 nm处具有较低的透过率[17]。此外,菌株SCSL-1的添加导致薄膜在550 nm与280 nm处透过率更低,可能与菌株混合后的薄膜内部结构变化有关[18]。综上所述,甘油的添加量会影响膜的L∗、a∗、b∗值,菌株SCSL-1的添加不会影响薄膜颜色的变化,但会明显赋予其优良的紫外光屏蔽效果。
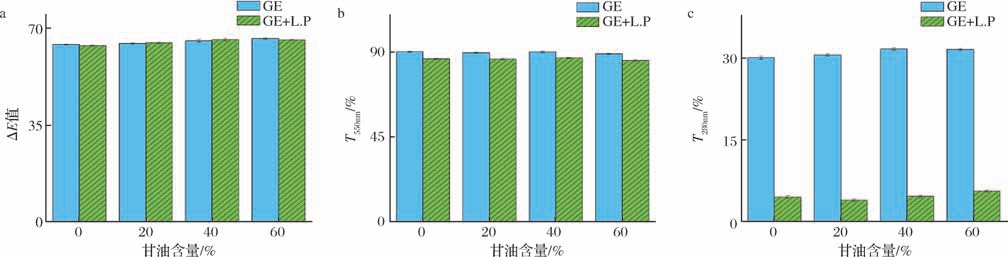
图5 不同甘油含量下薄膜的ΔE 与T550nm 和T280nm 变化趋势
Fig.5 Effect of glycerol content on the ΔE, T550nm,and T280nm of the films
a-ΔE;b-T550;c-T280
综上可以得出结论:a)植物乳植杆菌菌株SCSL-1的加入基本未改变其薄膜原来的厚度、含水量、机械性能、水蒸气透过率且对薄膜微观形貌和二级结构基本无影响,但却明显降低了薄膜在280 nm处的透过率(P <0.05),T280nm约为4.69%,因此植物乳植杆菌菌株SCSL-1的加入会使薄膜具有优良的紫外屏蔽效果;b)随着薄膜中甘油含量的不断增加,贮藏过程中薄膜负载植物乳植杆菌数量下降速率越快,而明胶薄膜的溶胀率、水溶性也随着甘油添加量的增加呈现下降趋势,但其厚度,含水量和水蒸气透过率却随着甘油含量的增加呈相反趋势。综合考虑明胶薄膜的各项参数以及薄膜的机械强度,最终采取甘油添加量为1.4 g(即甘油添加量为明胶质量的40%)的明胶薄膜作为菌株SCSL-1的负载材料。
2.6 可食用保鲜膜的微观形貌及红外表征
通过扫描电镜观察薄膜的微观结构特征。如图6-a所示,观察到明胶薄膜表面普遍呈现出平整光滑、均匀致密且无孔隙的特点,菌株SCSL-1的添加并未改变薄膜形貌,只存在少数的隆起,可能是菌株添加不均匀分布或扩散的缘故。薄膜截面分布大小不均的凹陷,菌株添加后使得截面略微平整,且清晰可见菌株的存在。这与GUIMARÃES等[19]和SETTIER-RAMÍREZ等[15]研究的薄膜微观情况一致,菌株的加入并不会对薄膜的微观形貌有较大改变。
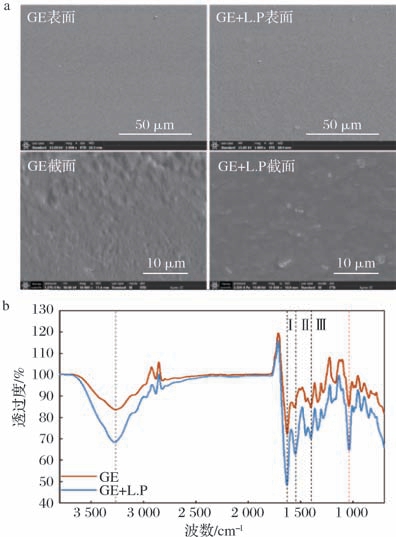
图6 薄膜的扫描电镜和FTIR光谱图
Fig.6 SEM image and FTIR spectrum of the films
a-扫描电镜图;b-FTIR光谱图
利用FTIR评估菌株的添加对明胶薄膜分子间作用力的影响。如图6-b所示,GE与GE +L.P薄膜的酰胺Ⅰ带波数基本一致,所以其振动模式中CN拉伸,CCN变形和平面NH弯曲模式耦合的C ═O伸缩振动基本未发生变化;酰胺A带为O—H和N—H的伸缩振动吸收峰,当氢键形成时,谱带会向较低的波数方向移动,通常氢键越强,降低越明显。酰胺Ⅱ带和酰胺Ⅲ带分别表示N—H的弯曲振动和C—H的伸缩振动,GE与GE +L.P薄膜的酰胺Ⅱ带和酰胺Ⅲ带的出峰位置相差均不大。所以菌株SCSL-1的添加对明胶薄膜二级结构基本没有较大的影响。
2.7 可食用保鲜膜对芒果贮藏的影响
无涂层组芒果表皮颜色逐渐由绿转黄,在贮藏过程表皮逐渐皱缩,贮藏后期表皮出现了病害病斑。相比而言,涂层赋予了芒果明显的光泽感,且贮藏10 d内表皮的颜色一直呈现原本的亮黄色或亮红色。此外,涂层处理减少了果实表皮黑斑黑点的覆盖面积,且延迟了黑斑黑点出现的时间,尤其是含菌涂层组较为明显。可能是含菌涂层具备良好屏障效果,减缓了果实呼吸速率和减少了腐败菌侵染的机会,从而保持了原本的品质[20]。如图7所示,随着贮藏时间延长,芒果在贮藏期间患病率和患病程度逐渐增大。无涂层组芒果在贮藏第4天出现患病果实,在第10天患病率为86.7%,患病直径约为24.5 mm;相比之下,涂层组贮藏10天患病率分别为56.5%、42.4%,患病直径分别为16.5、7.6 mm,说明涂层覆盖可以抑制腐败菌生长,且添加菌株SCSL-1后的涂层抑制效果更为显著(P <0.05)。HASHEMI等[21]采取含有植物乳植杆菌的魔芋胶保鲜鲜切猕猴桃时,降低了霉菌和酵母的侵染(106 CFU/g以下)。值得注意的是,接种了霉菌孢子且未涂层的实验组在第2天便出现了83%的患病率,第4天后患病率达到了100%,贮藏第10天患病直径达到了35.0 mm。经过涂层后显著降低了果实的患病率(P <0.05),贮藏10 d患病率和患病直径分别为52.33%、10.20 mm,说明含菌涂层在抑制霉菌生长方面具有更好的效果。涂层的覆盖可以隔绝氧气,阻止部分好氧霉菌的生长,且加入活植物乳植杆菌可以通过争夺空间和营养物质或产生抗菌物质抑制病原体,贮藏第10天,含菌涂层组(GE+L.P)的患病率(42.4%)与患病直径(7.6 mm)均显著低于无菌涂层组(GE,56.5%,16.5 mm)(P <0.05),而GE组又显著低于未涂层对照组(86.7%,24.5 mm)(P <0.05)。这表明,SCSL-1菌株的引入进一步强化了涂层的保鲜效果,能有效抑制芒果的腐败真菌,延长贮藏周期。
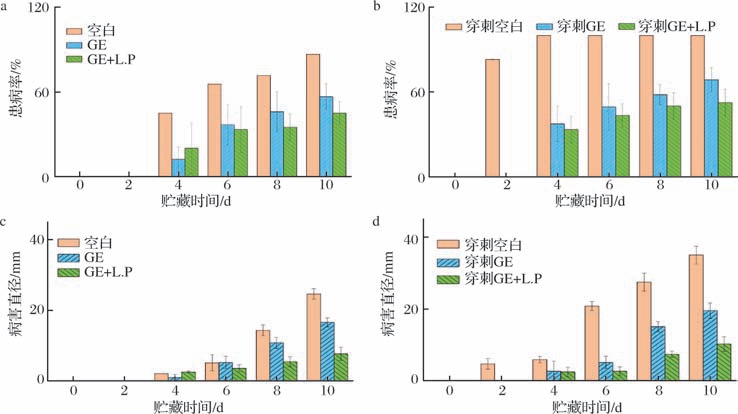
图7 芒果非穿刺组与穿刺组贮藏期间的患病率及病害直径
Fig.7 Disease incidence and lesion diameter in non-punctured and punctured mango groups during storage
a-非穿刺组患病率;b-穿刺组患病率;c-非穿刺组病害直径;d-穿刺组病害直径
3 结论
本文研究了菌株SCSL-1含菌薄膜的制备方法,当甘油添加量为1.4 g时,该可食用保鲜膜具有理想的机械性能、含水量、溶胀率、水溶性、WVP以及透光率等理化数值,菌株SCSL-1的加入基本未改变薄膜的以上性质,却明显降低了薄膜在280 nm处的透光率(P <0.05),这意味随着菌株SCSL-1的加入会使薄膜具有优良的紫外屏蔽效果。在芒果实际保鲜中,含SCSL-1菌涂层的处理赋予了芒果光泽感,降低了转黄率,有效延缓芒果表皮黑斑黑点出现的时间。研究结果阐明了含菌可食用明胶涂层在芒果贮藏保鲜方面的应用潜力,可为易腐败变质的水果生物保鲜提供参考。
[1]ZHANG Y L,CUI Q L,WANG Y,et al.Effect of carboxymethyl chitosan-gelatin-based edible coatings on the quality and antioxidant properties of sweet cherry during postharvest storage[J].Scientia Horticulturae,2021,289:110462.
[2]KINGWASCHARAPONG P,ARISA K,KARNJANAPRATUM S,et al.Effect of gelatin-based coating containing frog skin oil on the quality of persimmon and its characteristics[J].Scientia Horticulturae,2020,260:108864.
[3]LÓPEZ DE LACEY A M,LÓPEZ-CABALLERO M E,GÓMEZ-ESTACA J,et al.Functionality of Lactobacillus acidophilus and Bifidobacterium bifidum incorporated to edible coatings and films[J].Innovative Food Science &Emerging Technologies,2012,16:277-282.
[4]TEMIZ N N,ÖZDEMIR K S.Microbiological and physicochemical quality of strawberries (Fragaria × Ananassa) coated with Lactobacillus rhamnosus and inulin enriched gelatin films[J].Postharvest Biology and Technology,2021,173:111433.
[5]LIU W X,WANG J J,XIAO X K,et al.Antimicrobial effects and metabolomics analysis of cell-free supernatant produced by Pediococcus acidilactici LWX 401 isolated from Yunnan traditional pickles[J].LWT,2024,191:115626.
[6]SUN L J,SUN J J,CHEN L,et al.Preparation and characterization of chitosan film incorporated with thinned young apple polyphenols as an active packaging material[J].Carbohydrate Polymers,2017,163:81-91.
[7]ZHAO G Y,ZHOU C Y,FAN F Y.Preparation and properties of soy protein isolate/cotton-nanocrystalline cellulose films[J].International Journal of Polymer Science,2021,2021:5518136.
[8]KHODAEI D,HAMIDI-ESFAHANI Z,LACROIX M.Gelatin and low methoxyl pectin films containing probiotics: Film characterization and cell viability[J].Food Bioscience,2020,36:100660.
[9]LIU F,CHIOU B S,AVENA-BUSTILLOS R J,et al.Study of combined effects of glycerol and transglutaminase on properties of gelatin films[J].Food Hydrocolloids,2017,65:1-9.
[10]SHAHRAMPOUR D,KHOMEIRI M,ALI RAZAVI S M,et al.Development and characterization of alginate/pectin edible films containing Lactobacillus plantarum KMC 45 [J].LWT,2020,118:108758.
[11]KHODAEI D,HAMIDI-ESFAHANI Z.Influence of bioactive edible coatings loaded with Lactobacillus plantarum on physicochemical properties of fresh strawberries[J].Postharvest Biology and Technology,2019,156:110944.
[12]BERTUZZI M A,CASTRO VIDAURRE E F,ARMADA M,et al.Water vapor permeability of edible starch based films[J].Journal of Food Engineering,2007,80(3):972-978.
[13]BANDEIRA S F,DE SOUZA GOMES DA SILVA R,DE MOURA J M,et al.Modified gelatin films from croaker skins: Effects of pH,and addition of glycerol and chitosan[J].Journal of Food Process Engineering,2015,38(6):613-620.
[14]GIALAMAS H,ZINOVIADOU K G,BILIADERIS C G,et al.Development of a novel bioactive packaging based on the incorporation of Lactobacillus sakei into sodium-caseinate films for controlling Listeria monocytogenes in foods[J].Food Research International,2010,43(10):2402-2408.
[15]SETTIER-RAMÍREZ L,LÓPEZ-CARBALLO G,GAVARA R,et al.Antilisterial properties of PVOH-based films embedded with Lactococcus lactis subsp.lactis[J].Food Hydrocolloids,2019,87:214-220.
[16]MA D H,JIANG Y,AHMED S,et al.Physical and antimicrobial properties of edible films containing Lactococcus lactis[J].International Journal of Biological Macromolecules,2019,141:378-386.
[17]AYAD SHAMSALLAH A,OMER RASHID S.Development in gelatin-matrix composite films: The incorporation of vitamin C adducts enhances the optical behaviors of gelatin films[J].Arabian Journal of Chemistry,2024,17(2):105541.
[18]LI S Y,MA Y L,JI T T,et al.Cassava starch/carboxymethylcellulose edible films embedded with lactic acid bacteria to extend the shelf life of banana[J].Carbohydrate Polymers,2020,248:116805.
[19]GUIMARÃES A,ABRUNHOSA L,PASTRANA L M,et al.Edible films and coatings as carriers of living microorganisms: A new strategy towards biopreservation and healthier foods[J].Comprehensive Reviews in Food Science and Food Safety,2018,17(3):594-614.
[20]YANG Z M,GUAN C,ZHOU C,et al.Amphiphilic chitosan/carboxymethyl gellan gum composite films enriched with mustard essential oil for mango preservation[J].Carbohydrate Polymers,2023,300:120290.
[21]HASHEMI S M B,JAFARPOUR D.Bioactive edible film based on Konjac glucomannan and probiotic Lactobacillus plantarum strains:Physicochemical properties and shelf life of fresh-cut kiwis[J].Journal of Food Science,2021,86(2):513-522.