大曲作为中国传统白酒酿造的核心发酵剂和关键原料,素有“酒之骨”之称[1]。根据培养温度的差异,大曲可分为高温、中高温和低温3种类型[2]。值得注意的是,大曲在批次间的性质差异和时空异质性仍是制约生产标准化、机械化及智能技术应用的主要障碍之一。近年来,组学和生物信息技术的应用为揭示大曲制曲过程的科学规律提供了重要支撑[3],并取得了显著进展。大曲微生物群落的聚集与优先效应密切相关[4-6]。优先效应是指先定殖物种通过改变营养成分或微环境条件,影响后定殖物种的生长代谢,从而驱动群落聚集,具体表现为促进、抑制和抢占这3种生态位模式。NIKOLOUDAKI等[7]研究发现,发酵食品的群落演替具有复杂特性,而合成微生物菌群(synthetic microbial communities,SMCs)可作为研究其动态的“模型系统”和“可调控载体”。JIANG等[8]进一步总结了群落结构和聚集机制,提出了基于SMCs模拟微生态系统的策略。
随后的研究表明,这些策略对大曲群落的定向调控及代谢调控具有显著效果。例如,XU等[9]利用地衣芽孢杆菌(Bacillus licheniformis)和贝莱斯芽孢杆菌(Bacillus velezensis)构建的SMCs显著提高了中高温大曲中22个优势菌属的丰度,同时提升了酯化力及醇、酸、酮等挥发性代谢物(volatile compounds,VOCs)的含量。吴秋霞等[10]采用枯草芽孢杆菌D-31(Bacillus subtilis D-31)和B.velezensis M-14构建的SMCs也观察到类似结果,并进一步证实SMCs能够提高淀粉和纤维素水解相关基因的丰度,同时上调乙酸乙酯合酶和2,3-丁二醇脱氢酶编码基因的表达。LI等[11]的研究同样表明,SMCs的引入能够维持大曲的理化性质及群落结构稳定性。ZHANG等[12]关于酱曲添加母曲的研究表明,母曲微生物对高温大曲群落的贡献率为真菌26.76%、细菌8.11%,其关键作用在于提供独特功能菌群,促进微生态分化及特定代谢产物的合成,同时抑制食源性致病菌的生长。LIU等[13]对不同生长阶段曲坯的强化作用研究表明,培养时间和母曲用量显著影响初始阶段的升温速率、酸度等理化性质,以及功能菌群的结构和丰度。然而,以优质中高温大曲作为母曲的研究显示,发酵后期母曲对群落的贡献率显著提高,细菌和真菌的贡献率分别达到58.87%和93.25%[14]。
本研究以河套浓香型大曲为研究对象,分别采用质量分数0.2%(M2)和0.4%(M4)母曲进行强化,通过扩增子测序、HPLC和顶空固相微萃取-气相色谱-质谱(headspace solid-phase microextraction gas chromatography-mass spectrometry,HS-SPME-GC-MS)技术,系统解析母曲添加量对群落聚集机制及功能代谢组分差异化分布的影响,旨在为大曲生产工艺的定向优化提供理论依据,并为提升浓香型白酒的风味稳定性提供新思路。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
2种不同类型大曲分别是接种了质量分数0.2%和0.4%的母曲,没有接种母曲作为对照。这些样品分别标注为M2、M4、M0。实验所用母曲为四川泸州老窖股份有限公司秋季生产的浓香型大曲(生产批次:2022-09),经6个月常温贮藏。该大曲符合QB/T 4259—2011《浓香大曲》标准。感官指标:外观呈灰白色,断面菌丝分布均匀,具有典型的窖香复合香气;理化指标:糖化力≥800 U/g,发酵力≥0.20 CO2 g/(g·72 h),酯化力≥150 mg/(g·100 h);微生物指标:细菌总数≥1 ×107 CFU/g,霉菌数≥1 ×106 CFU/g。小麦原料产自内蒙古河套地区。大曲生产按照文献[1]所述方法进行工艺调控,生产周期为28 d。本次实验采用标准化大曲生产流程,单房投粮量7.5 t(高粱∶小麦=6∶4,质量比),共56间曲房,总投料量420 t。为控制空间异质性对微生物群落的影响,采用随机区组设计安排曲房位置,确保不同处理组的空间分布均衡。大曲成型后采用“井”字形码堆(12层,层间距15 cm),贮藏期间保持环境温度(25±3) ℃、相对湿度(70±5)%,自然通风条件下熟化6个月。最终成曲率达90% (378 t),选取代表性样品(n=120,按5%抽样率均匀取样)进行后续分析。
1.1.2 试剂
OMEGA Soil DNA Kit (D5635-02)试剂盒,美国欧米伽生物科技公司;Quant-iT PicoGreen双链DNA检测试剂盒,美国英杰生命技术有限公司;其他化学试剂(分析纯),成都金山化学试剂有限公司。
1.2 仪器与设备
DHG-9070A鼓风干燥箱,上海一恒科学仪器有限公司;TGL-16M高速冷冻离心机,湘麓离心机仪器公司;Agilent 1260 HPLC、1290 infinity Ⅱ-G6546A高分辨液相色谱飞行时间质谱联用仪(ultra performance liquid chromatography-quadrupole/time-of-flight mass spectrometry,LC-Q/TOF-MS),安捷伦科技(中国)有限公司;TSQ9000 GC-MS、NanoDrop ND-1000分光光度计,赛默飞世尔科技;Illumina Miseq测序仪,美国因美纳公司。
1.3 实验方法
1.3.1 样品采集
取样:参照唐慧芳等[15]的方法并稍作修改。分别从堆积的大曲上、中、下3层随机各取3块,粉碎后混合均匀,堆积呈圆锥形。采用五点取样法各点取500 g,混合均匀后取500 g样品,其中400 g样品置于-20 ℃用于理化性质和代谢组分的检查,另100 g样品置于-80 ℃保藏用于微生物群落测定。
1.3.2 理化指标的测定
样品的水分含量、酸度、氨基酸态氮、酯化力、糖化力、液化力和发酵力的测定参照QB/T 4257—2011《酿酒大曲通用分析方法》所述的方法检测。
1.3.3 有机酸的测定
有机酸的测定参照TANG等[16]的方法并稍作修改。主要步骤概述如下,准确称取5.00 g样品,置于25 mL离心管中,加入20 mL 9 mmol/L H2SO4溶液。涡旋5 min(200 r/min)后,超声(100 W,40 kHz)萃取60 min(每隔15 min涡旋1 min)后,4 ℃环境下7 500 r/min离心分离5 min收集上清液。上清液注入到活化后的固相萃取小柱的洗脱液经0.22 μm滤膜过滤后,将滤液注入HPLC系统,配备Alltech OA-1000 OA色谱柱,并保持在75 ℃。以脱气的9 mmol/L H2 SO4 溶液为流动相,用紫外检测器(215 nm)检测提取物。以草酸、柠檬酸、苹果酸、乳酸和乙酸标准品色谱峰的保留时间鉴定样品中的有机酸,采用外标法进行定量。
1.3.4 VOCs的测定
参考陈晓茹等[17]的方法和步骤并稍作修改,采用HS-SPME-GC-MS技术。样品预处理:准确称取1.00 g样品置于20 mL的顶空瓶中,加入10 μL内标(0.078 mg/mL辛酸甲酯)后,插入固相微萃取头(50/30 μm DVB/CAR/PDMS,Supleco)60 ℃下萃取45 min后,取出插入GC进样口250 ℃解吸5 min。气相色谱条件:进样口温度250 ℃,载气:高纯氦气(He)(>99.999%),流速1 mL/min不分流模式;升温程序:初始温度40 ℃,维持5 min,以4 ℃/min升温至100 ℃,以6 ℃/min升温至230 ℃,维持10 min。质谱条件:离子源温度250 ℃,传输线温度300 ℃,电离方式为电子电离源,电子能量70 eV,扫描范围35~400 amu。
1.3.5 非挥发性代谢物的测定
参考MU等[18]所述的方法和步骤,采用LC-Q/TOF-MS方法检测。主要步骤概述如下:准确取5.00 g大曲与20 mL无菌生理盐水(10 g/L CaCl2)混合均匀,4 ℃浸泡过夜。次日,在冰浴中超声30 min后,冷冻10 000 ×g 离心20 min(<4 ℃)取其上清液,加入102 μg/L内标2-氯-L-苯丙氨酸后,真空冷冻干燥72 h。10 mL体积分数80%甲醇溶液复溶其冻干物,并涡旋混匀后,经0.22 μm尼龙滤膜备用。从每个待测样本各取100 μL混合成质控样本,以校正混合样品分析结果的偏差及仪器误差。
液相色谱条件:使用配备Zorbax Eclipse Plus C18柱的LC系统(Agilent 1290 Infinity Ⅱ)在40 ℃下分离大曲中的非挥发性代谢物。2种流动相包括体积分数0.1%的甲酸水(A)和乙腈(B),进样量和流速分别为2 μL和0.3 mL/min,线性梯度程序为:0~5 min,98% A;5~13 min,98%~90% A;13~23 min,90%~ 5% A;23~ 26 min,5% A;26~ 26.1 min,5%~98% A;26.1~30 min,98% A。采用Q/TOF-MS结合Dual AJS ESI离子源分别进行正、负离子模式下的代谢物检测。正、负离子的毛细管电压分别为4 000、3 500 V,喷嘴电压分别为0、500 V。以分辨率60 000进行全扫描,质量范围为m/z 100~1 000,扫描速率为3 spectra/s。Auto MS/MS实验利用碰撞诱导解离技术进行二级裂解,碰撞能量为20、40 eV,同时采用动态排除去除无必要的二级质谱信息。仪器参数:干燥气体温度为300 ℃;干燥气体流速为10 L/min;雾化器压力为60 psi;氮气温度为350 ℃;氮气流速为11 L/min。
使用MassHunter Profinder v10.0.2软件处理原始数据,对每个信号峰进行峰对齐、面积提取及半定量。主要参数设置如下:峰对齐的保留时间和质量偏差为0.30 min和20 ppm;峰匹配的保留时间和质量偏差为0.15 min和10 ppm;绝对峰高≥20 000;得分≥70。随后,使用Mass Hunter Qualitative Analysis v10.0软件对每个信号峰进行MS/MS库和在线数据库检索,获得准确的定性结果。根据内标含量与其峰面积的比值对各物质进行半定量。
1.3.6 大曲微生物群落结构分析
参照TANG等[19]所述方法稍作修改。具体步骤概述如下:使用OMEGA Soil DNA Kit (D5635-02)试剂盒从2.00 g大曲中提取总基因组DNA,并通过0.8%琼脂糖凝胶电泳和分光光度计评估DNA的浓度含量、纯度(A260/A280比值)和完整性。使用引物338F/806R(5′-ACTCCTACGGGAGGCAGCA-3′/5′-GGACTACHVGGGTWTCTAAT-3′) 扩增细菌的 16S rRNA V3~V4区,用ITS5/ITS1(5′-GGAAGTAAAAGT CGTAACAAGG-3′/5′-GCTGCTTCTTCATCGATGC-3′)扩增真菌ITS1区。PCR反应体系:5 μL Q5高保真反应缓冲液(5 ×)、5 μL Q5高保真GC缓冲液(5 ×)、0.25 μL Q5高保真DNA聚合酶(5 U/μL)、2 μL dNTPs(2.5 mmol/L)、正反引物各1 μL(10 μmol/L)、2 μL DNA模板、8.75 μL ddH2 O。扩增程序:细菌:98 ℃预变性2 min,98 ℃变性15 s,55 ℃退火30 s,72 ℃延伸30 s,共25个循环,最后72 ℃延伸5 min;真菌:95 ℃预变性3 min,95 ℃变性30 s,61 ℃退火30 s,72 ℃延伸45 s,共32个循环,最后72 ℃延伸10 min。PCR扩增产物经Vazyme VAHTSTM DNA磁珠纯化后,使用Quant-iT PicoGreen双链DNA检测试剂盒定量检测。等量混合纯化产物后,采用TruSeq Nano DNA LT Library Prep Kit构建文库后,送上海派森诺公司在Illumina NovaSeq平台(https://www.illumina.com.cn/)进行双端2 ×250 bp测序。
使用QIIME2(2019.4)[20]流程处理原始数据:使用demux插件解码原始序列后,用cutadapt v2.3插件(https://cutadapt.readthedocs.io/en/stable/)切除引物序列。使用DADA2插件[21]对序列进行质量过滤、去噪、合并和嵌合体去除等后。所得的序列按100%的序列相似度进行归并,生成特征性序列ASVs以及丰度数据表格,剔除单样本单序列的稀有ASV后,使用特征分类器的classify-sklearn[22] (https://github.com/QIIME2/q2-feature-classifier)朴素贝叶斯分类器,在Silva v132(https://www.arb-silva.de)[23]和UNITE v8.0(https://unite.ut.ee)数据库检索,物种分类分配至ASV。在PICRUSt2[24] (Phylogenetic Investigation of Communities by Reconstruction of Unobserved States)和KEGG(https://www.kegg.jp/)、MetaCyc(https://metacyc.org/)数据库对比,完成基因功能进行注释,代谢通路信息及代谢途径中相关酶表达的相对丰度。
1.4 数据分析
所有实验重复3次,数据以“平均值± 标准差”表示,采用单因素方差分析和Duncan多重比较检验,使用SPSS 26.0软件进行显著性评估。误差柱状图、主成分分数(principal component analysis,PCA)、箱线图、主坐标分析(principal coordinate analysis,PCoA)、交互堆叠柱状图、热图在派森诺云平台(https://www.genescloud.cn/home)完成。共现网络图、中性群落图、冗余分析(redundancy analysis,RDA)在图图云平台(http://cloudtutu.com.cn/)完成。线性判别分析[linear discriminant analysis(LDA) effect size,LEfSe]在生科云平台(https://www.bioincloud.tech/)完成。通过Chao1丰富度估计指数评估物种总数(丰富度),Shannon指数衡量群落的多样性(丰富度和均匀度),Simpson指数评估优势度,Pielou_e均匀度指数量化物种分布的均匀性。
2 结果与分析
2.1 大曲理化性质和有机酸分析
如表1所示,3种不同类型大曲(M0、M2和M4)的理化性质符合QB/T 4259—2011《浓香大曲》标准要求,但差异显著。与M0比较,M2和M4的液化力和糖化力分别降低了19.05%~25.40%和3.38%~11.18%,酯化力分别提高了13.94%和110.77%,而M2的发酵力提高了20.00%。M4的酸度[(0.80±0.02) mmol/10 g]和氨酸态氮含量[(2.17±0.02) g/kg]最高。作为微生物生长的重要代谢物-有机酸[25],其组成分布呈明显的组间差异(表2)。分布的特征是M4中草酸等4种有机酸的含量最高。M2中的乙酸含量最高[(115.71±1.84) mg/100 mL],较M0高65.11%,未检出草酸。仅在M0中检出了琥珀酸[(135.60±4.62) mg/100 mL]。这些结果表明,母曲添加影响有机酸的组成,有机酸总量与其添加量呈正相关(R2=0.89)。
表1 大曲的理化性质与酶活性
Table 1 The physicochemical properties and enzymatic activities of Daqu

注:同一列中的不同字母表示显著差异(P <0.05)(下同)。
表2 大曲中主要有机酸组成与含量 mg/100 mL
Table 2 The main organic acid composition and content of Daqu

2.2 大曲挥发性物质组成和轮廓
在所有样品中,共检出了53种VOCs成分,包括酯类(20种)、醇类(14种)、酸类(6种)、醛类(1种)、酮类(1种)、吡嗪类(3种)、萜烯类(2种)和其他类(6种),其含量为(451.24±41.72)~ (659.07±38.11)μg/kg。母曲用量显著改变了大曲VOCs的含量和组成轮廓。M2的VOCs为(659.07±38.11) μg/kg,显著高于M0和M4,后两者间仅略有差异。主要是M2的酸类、醇类和吡嗪类显著提高。此外,M2的酯类、萜烯类和其他类组分含量也被提高,M4的酯类降低。
LEfSe(LDA分值≥2)结果显示,M0、M2、M4分别具有9、18、13个显著差异特征标志物。其中,M2的标志物成分包括(E)-5-羟基-3,4,4-三甲基-2-己烯酸、2,5-二甲基吡嗪、β-石竹烯和异戊酸等。2,5-二甲基吡嗪呈炒花香和巧克力香,β-石竹烯呈木质辛辣香[26],而异戊酸赋予甜润果香。这些成分赋M2独特的复合香气。M0和M4以酯类和醇类为主,特色风味物质较少。M2的VOCs含量是M0的1.89倍,酸类、吡嗪类等颇具特色组分显著增高,使组成轮廓更复杂。M4和M0不仅其VOCs总量类似,且酯类和醇类分别是总VOCs的54.37% 和59.63%,仅略有差异。PCoA表明,3组样品(M0、M2、M4)的群落结构呈现显著分离(图1-b)。真菌群落的PCoA的前2轴(PC1和PC2)共解释了86.5%的群落变异,表明母曲添加量是驱动真菌群落结构变化的主要因素。母曲的添加显著提高了组内一致性,尤其是M4,表明高比例母曲提供了更稳定的真菌群落环境。细菌群落的PCoA的2个主轴共解释了95.8%的群落变异,3组样品呈现“三角形”分布,表明细菌群落对母曲添加的响应更为复杂。其中PC1轴(68.9%)清晰区分了M0与M2/M4,表明有无母曲添加是影响细菌群落的主要因素;PC2轴(26.9%)则分离了M2与M4,说明母曲的有无是影响细菌群落的差异化。PC2轴则进一步分离了M2,表明母曲的用量导致细菌群落有差异化。值得注意的是,M2的样品点分布最为集中,说明0.2%母曲的添加量为细菌群落提供了最稳定的生态环境。真菌和细菌群落的β 多样性模式存在差异,表明二者对母曲添加的响应机制不同。这一现象可能与母曲中引入的微生物与原有微生物之间的复杂互作(资源竞争、代谢抑制等)有关,也是真菌和细菌群落呈现不同变化模式的重要原因。
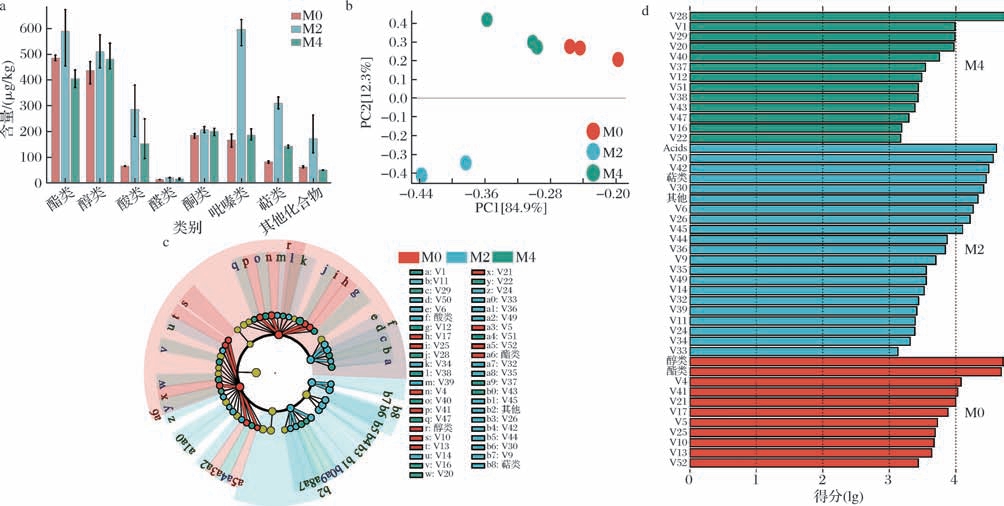
图1 大曲的挥发性化合物组成及主要特征
Fig.1 The composition and main characteristics of volatile compounds of Daqu
a-不同种类挥发性化合物含量差异;b-挥发性物质PCA;c-挥发性物质LEfSe-cladogram分析;d-挥发性物质LEfSe
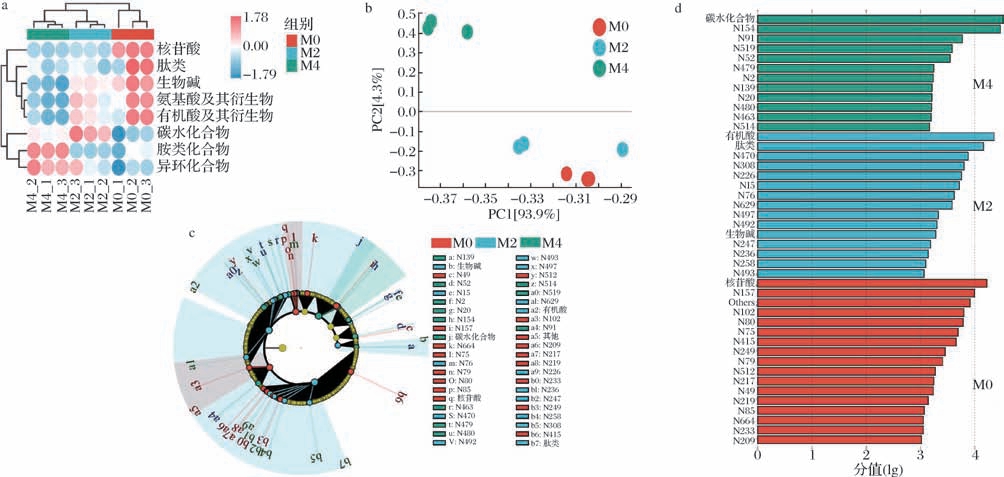
图2 大曲的非挥发代谢物组成及主要特征
Fig.2 The composition and main characteristics of non-volatile metabolites of Daqu
a-不同种类非挥发性化合物含量差异;b-非挥发化合物PCA;c-非挥发化合物LEfSe-cladogram分析;d-非挥发化合物LEfSe
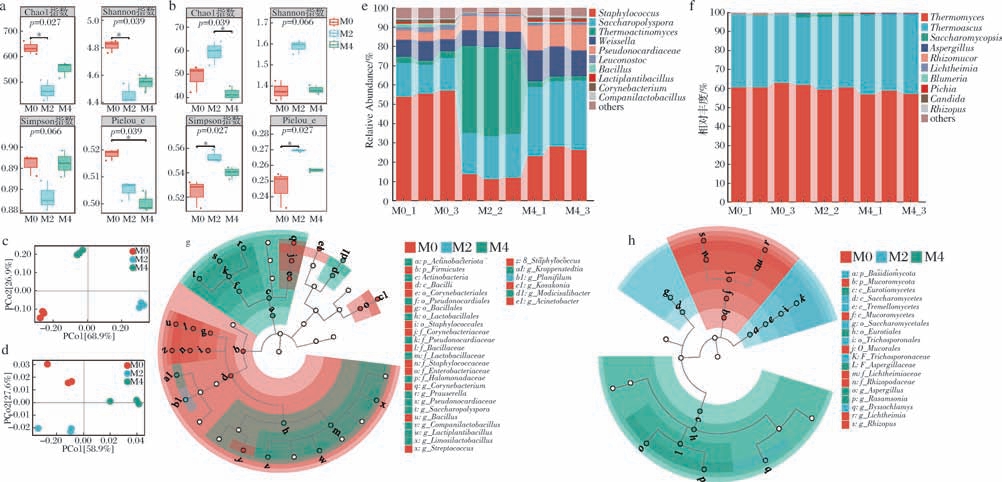
图3 大曲微生物组成及差异多样性
Fig.3 The microbial composition and diversity of Daqu
注:∗表示差异显著(P <0.05)。
a-细菌α 多样性箱线图;b-真菌α 多样性箱线图;c-细菌组成PCoA;d-真菌组成PCoA;e-细菌属交互堆叠柱状图;f-真菌属交互堆叠柱状图;g-细菌LEfSe-cladogram分析;h-真菌LEfSe-cladogram分析
2.3 大曲非挥发性物质组成和轮廓
基于UPLC-Q-ToF/MS分析,共鉴定到683种非挥发代谢物,主要包括以下类别:有机酸及其代谢物(185种)、氨基酸及其代谢物(45种)、小肽(259种)、核苷酸(16种)、胺类(29种)、碳水化合物(50种)、生物碱(16种)、杂环化合物(35种)和其他化合物(47种)。非挥发代谢物总含量分别是(4 630.34±337.03) mg/kg(M0)、(4 608.92± 140.34) mg/kg(M2)、(4 330.52±102.88) mg/kg(M4)。其中有机酸及其衍生物的含量最高,母曲添加降低了其含量,与M0相比,M2和M4分别减少了4.30%和12.38%,这一趋势与VOCs的变化是不同的,可能是母曲改变了酸的代谢途径。此外,母曲添加使小肽含量略减少(8.29%~8.58%),这可能是母曲携带的功能菌群促进使微生态分化,例如吡嗪类合成及功能菌群的增殖,从而显著增高了M2和M4间组成轮廓的相似性,其具体机制仍需进一步研究。母曲使核苷酸含量减少了42.47%(M2)和46.41% (M4),同时增加了胺类的含量(M4增幅达15.79%)。这一现象可能是M4中含有氨基酸羧化能力强的乳酸菌菌群(优势菌群)有关。此外,M2的生物碱的含量降低了11.65%,M4则降低了31.52%,同时杂环化合物含量略有增加。
2.4 大曲微生物群落结构分析
如表3所示,微生物测序分析结果显示:9个样品的细菌和真菌有效序列数分别为69 744~81 304条和103 756~124 928条,其中高质量序列占比分别是68.58%和92.33%,说明测序深度足以涵盖样本中微生物多样性[27]。真菌群落α 多样性分析表明,M2的物种丰富度(Chao1指数)和Shannon指数显著高于M0和M4。添加0.2%母曲显著提高了真菌群落的α 多样性(Simposon指数升高),并使群落结构分布更加均匀。相比之下,细菌群落的α 多样性呈下降趋势,其中M2的多样性指数显著降低(P <0.05),而M4较M2略增。这一现象可能与母曲中固有细菌的影响以及M4中部分细菌对真菌抑制性的耐受性增强有关。细菌群落的Shannon指数(4.4~4.8)显著高真菌群落的(1.3~1.6),表明细菌群落结构具有更高的复杂性。
表3 样品的ASVs分布水平
Table 3 ASVs distribution on samples

在真菌群落中,高温放线菌属(Thermoactinomyces)和Thermoascus 是绝对优势菌属,其相对丰度(relative abundance,RA)之和超过90%。M2中Thermomyces的RA略高于M4,而Thermoascus 的RA则在M4中显著升高(P <0.05),这可能与两者的生态位竞争有关。此外,M2中糖多孢菌属(Saccharopolyspora)的RA显著增加,该菌属具有较强的水解淀粉和水解蛋白质能力[28],可能是导致M2的发酵力和氨基态氮含量较高的原因。母曲强化显著改变了细菌群落结构,Staphylococcus 的RA从M0的55.50%降至12.25%(M2)和25.91% (M4);而Saccharopolyspora 则是从M0的16.55%增至M2的22.23%和M4的35.24%。这些结果表明,母曲显著抑制了Staphylococcus 的生长,同时促进Saccharopolyspora 等功能菌群属的富集,从而显著改变了大曲的群落结构显著改变。如真菌群落从Thermomyces 绝对优势转向Thermomyces 和Thermoascus 共同优势,而细菌群落从Staphylococcus优势转向Saccharopolyspora、Thermoactinomyces 和魏斯氏菌属(Weissella)共同优势。这一变化降低了群落的优势度,提高了均匀度、结构趋于平衡和稳定。
2.5 微生物共现网络分析
真菌群落的共现网络分析表明,母曲添加量影响网络规模的结构(图4)。如M2的网络复杂度显著大于M0和M4,其节点(41)和边数(408)显著大于M0(节点25、边149)和M4(节点29、边200)。这一结果表明,0.2%的母曲添加量不仅增加了真菌类群数量,还显著增强了真菌类群间的生态关联。网络拓扑参数分析结果进一步揭示了母曲添加对真菌互作模式的影响。连接密度呈现M2(平均密度19.90) >M4(平均密度13.79) >M0(平均密度11.92)的趋势,表明0.2%的母曲添加促进了更为复杂的种间互作网络。此外,M4(1.68)和M2(1.67)的平均路径长度低于M0(1.86),说明母曲提高了真菌群落代谢物交换和信号传导的效率。3种大曲的网络直径都是3,表明网络整体保持稳定的“紧凑性”,但M2、M4和M0的聚类系数分别是0.77、0.75、0.80,说明母曲添加整合了真菌群落结构。综上所述,母曲添加降低了真菌群落的异质性和中心性,促使其从“主导型”结构(少数关键物种控制)向“协作型”结构转变。尽管网络规模减小,细菌网络仍表现出以下重要特征:平均度呈下降趋势(M0:43.70;M2:36.49;M4:34.45),但仍显著高于真菌网络(P <0.05),表明细菌群落保持着更频繁的种间互作;平均路径长度(1.67~1.69)和网络直径(均为3)保持稳定,说明物质传递效率未受显著影响;聚类系数维持在0.78~0.79的高水平,保证了功能模块结构的稳定性;网络密度稳定在约0.5,与真菌网络类似,表明约50%的潜在细菌对存在显著关联。
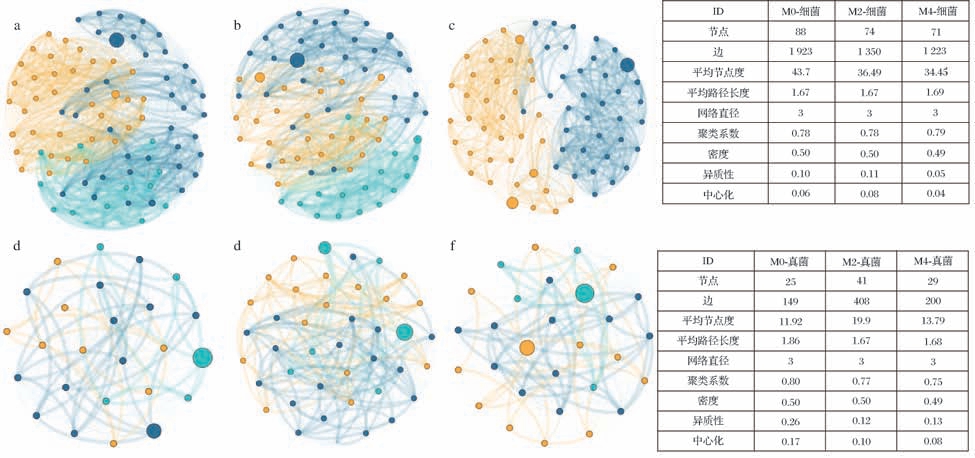
图4 大曲微生物群落共现网络图
Fig.4 Co-occurrence network diagram of the Daqu microbial community
a-M0细菌;b-M2细菌;c-M4细菌;d-M0真菌;e-M2真菌;f-M4真菌
M4组的网络异质性和中心性显著降低(分别为0.05和0.04),表明高浓度母曲添加使细菌群落结构更加均质化,生态功能更趋去中心化。而M2组的中心性指标小幅上升,这可能与Thermoactinomyces 在该条件下的显著富集有关(图3-e),提示该属细菌可能在网络中扮演核心角色,维持了过渡状态下的网络稳定性。
2.6 中性群落模型分析
中性群落模型(neutral community model,NCM)分析表明,不同群落的聚集机制差异显著(图5)。真菌群落的拟合优度(R2)以M2最高(0.474),其次是M0(0.385),而M4最低(0.290),表明M2增强了真菌群落的随机性过程,但M4则转向了以确定性过程(如环境选择或竞争排斥)为主。迁移率分析显示,M2和M4的迁移率分别是0.037和0.017,较M0(0.040)分别降低了7.5%和57.5%,表明高加母曲量促进了真菌群落的扩散,使其更依赖局部环境(如pH、底物)和种间互作(如竞争/共生)。此外,母曲添加降低了潜在多样性(Nm),其中M2的Nm高于M4的,与α 多样性的变化趋势是一致的,进一步印证了确定性过程的重要性。细菌群落的R2值为0.321~0.347(均小于0.5),表明其聚集主要是由确定性过程(如环境过滤)驱动。细菌迁移率(m)为0.166~0.225,显著高于真菌,表明其受到扩散限制更小。M2的Nm值最高,M4降低,与α 多样性趋势一致,但差异进一步凸显了确定过程的调控作用。由此可见,母曲添加改变了群落的聚集方式,真菌菌落聚集从随机性转向确定性过程,而细菌群落始终以随机性过程为主,适应性较强但扩散受限。
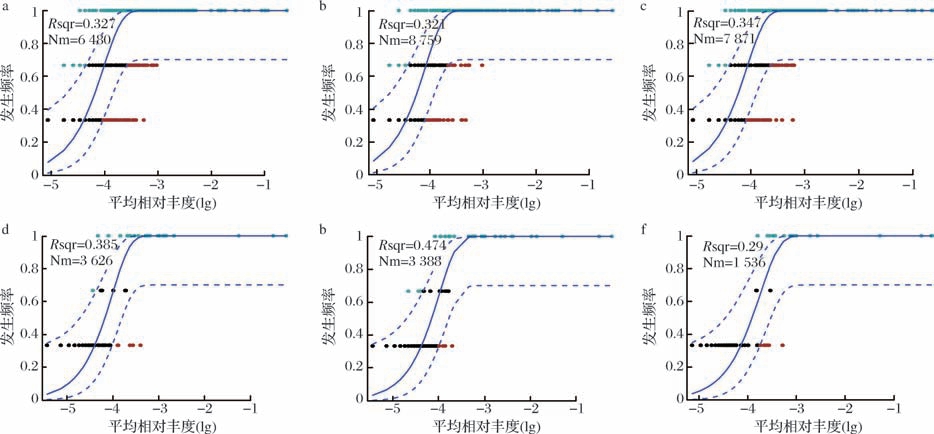
图5 大曲微生物中性群落模型分析
Fig.5 Analysis of the neutral community model of Daqu microorganisms
a-M0细菌;b-M2细菌;c-M4细菌;d-M0真菌;e-M2真菌;f-M4真菌
2.7 微生物与代谢物关联分析
RDA结果表明(图6),理化参数对微生物群落组成有显著影响(P <0.01)。前2轴(RDA1和RDA2) 分别解释了细菌群落变异的77.09% 和20.36%(累计解释率97.45%),环境因子对细菌群落结构具有强筛选作用[29]。关键理化因子的影响的特征如下:在M0中,液化力和糖化力是主要驱动因子;在M2中,发酵力和氨基态氮主导群落变化;而在M4中酯化力和酸度影响最大。 Staphylococcus 与液化力、糖化力正相关,解释了M0糖化力和液化力较高的原因[12]。 Weissella 和Saccharopolyspora 与酯化力和酸度正相关,促进M4的酯类合成和酸性环境的适应能力。 Thermoactinomyces 与发酵力和氨基态氮正相关,驱动M2的快速发酵和氨基态氮(可能与蛋白酶分泌相关)。真菌群落的RDA前两轴解释了58.18%(RDA1)和30.75% (RDA2)的变异,表明理化因子对真菌的影响略低于细菌的,但仍具有显著性。关键菌属与功能相关性的分析结果表明,Thermoascus、假丝酵母属(Candida)、毕赤酵母属(Pichia)与酯化力显著正相关,其中Candida 产生的有机酸可能抑制了不耐酸微生物生长[29-30],解释了M4的高酸度;根霉属(Rhizopus)和根毛霉属(Rhizomucor)与液化力正相关,其分泌的高活性淀粉酶[19]驱动M0的糖化力和液化力。Spearman相关分析进一步揭示微生物与代谢物的功能关系。M0中富集的Staphylococcus 与20种特征性VOCs和13种非挥发代谢物显著负相关,表明其可能竞争性抑制产香微生物的生长。 Rhizomucor 与6种VOCs和14种非挥发代谢物显著正相关,可能是分泌酸性蛋白酶[31]促进了蛋白质降解与代谢。曲霉属(Aspergillus)与苯乙醇呈显著正相关,与CHEN等[32]的结果一致。
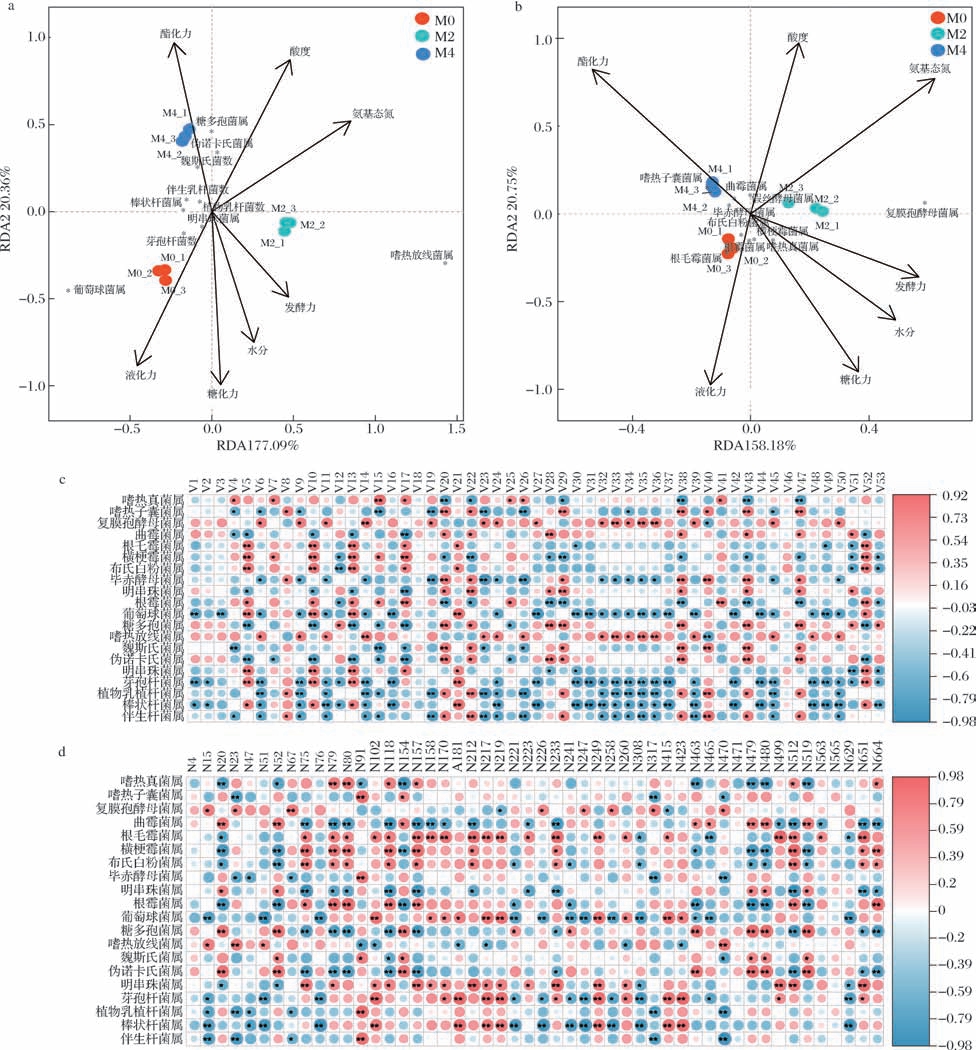
图6 理化性质、特征性代谢物与微生物相关性分析
Fig.6 Correlation analysis of physicochemical properties,characteristic metabolites,and microorganisms
注:∗∗代表差异极显著(P <0.01);∗代表差异显著(P <0.05)。
a-理化性质和细菌RDA(数据预处理方法:hellinger转化);b-理化性质和真菌RDA;c-特征性VOC和微生物相关性热图(spearman相关性分析);d-特征性非挥发化合物和微生物相关性热图
母曲添加量显著影响的群落结构、代谢功能及品质特性。M0的群落结构中Staphylococcus 和Thermomyces 为绝对优势菌,群落多样性较低且群落结构失衡。糖化力和液化力高与Staphylococcus 和Rhizopus等产酶菌的高丰度有关。此外,其酯类、醇类和核苷酸类是代谢组分的优势,特色风味物质较少。真菌群落呈现异质性和中心性高的“主导型”结构;细菌网络规模最大,但确定性构建过程占主导。M2的群落结构呈现其多样性和结构平衡性最优,Thermoactinomyces 的RA显著增加(为M0的15倍),形成Thermoactinomyces、Saccharopolyspora、Weissellas 共存的优势群落,共同优势菌群结构显著提升了大曲的微生态稳定性和风味代谢多样性,但共同优势菌群并不总是优于单一优势菌群,由Sporolactobacillus 为主导的微生物群落可实现高效产氢[33]。发酵力和氨基态氮含量最高,非挥发代谢物总量及多样性均较高,尤其是酸类、吡嗪类和杂环类显著增加。真菌共现网络规模和拓扑结构最优,且随机性聚集过程贡献增加;细菌网络规模减小但仍保持高效连接,确定性聚集过程仍占主导。M4形成 Saccharopolyspora、 Thermoascus、Weissella 共存的优势群落,酯化力和总酸含量最高,胺类和杂环化合物增多,但VOCs总量和多样性低于M2,表明共同优势菌群促进生态稳态,但也可能加剧种间竞争和资源分散,多菌共同优势不等于代谢性能最大化。M4群落共现网络均呈现均质化和去中心化,其中真菌群落的确定性聚集过程增强,而细菌群落仍以保持高度确定性聚集过程为主。
本研究结果与现有关于中高温大曲微生物强化的多项研究结果具有一致性,又具有补充价值。柯涛等[34]的研究表明,功能微生物与母曲按特定比例联合添加可显著促进VOCs的合成,这与本研究中M2组酸类、吡嗪类和杂环类化合物含量升高的结果高度一致。HE等[35]采用B. velezensis 和B. subtilis 双菌株接种构建大曲微生态基础结构的研究表明,特定的优势菌群结构不仅能够提升大曲的理化指标,还能维持其稳定性。这一发现与本研究M2组中观察到的氨基态氮含量升高及微生物群落结构趋于稳定的结果一致。综合分析表明,尽管在微生物添加方式、母曲来源及用量等方面存在差异,但本研究结果支持“通过微生态调控可定向引导目标代谢途径”的作用机制,进一步证实了定向微生态调控技术在大曲风味品质改良中的可行性和普适性。
3 结论
本研究系统探究了不同添加量(0.2%、0.4%,质量分数)的母曲对河套浓香型大曲微生物组成和代谢特性的影响。结果表明,0.2%的添加量在功能指标和微生物生态特性方面均表现出显著优势,具体表现为:形成了以Thermoactinomyces-Saccharopolyspora-Weissella 为主的多元化群落;产生了最丰富风味物质谱系,特别是显著提升了酸类、吡嗪类和杂环类物质的含量,构建了优化的真菌共现网络拓扑结构。本研究通过共现网络分析和中性群落模型揭示了母曲添加量调控群落聚集机制:真菌群落的聚集过程呈现从相对随机(M2)向确定性(M4)转变的趋势;细菌群落则始终以确定性聚集过程为主导。本研究从微生物生态学角度阐明了母曲添加量影响大曲品质的作用机制,不仅为理解大曲微生物群落的组织原理提供了新见解,也为河套浓香型大曲的工艺优化和产品创新奠定了理论基础。
[1]HE G Q,HUANG J,ZHOU R Q,et al.Effect of fortified Daqu on the microbial community and flavor in Chinese strong-flavor liquor brewing process[J].Frontiers in Microbiology,2019,10:56.
[2]PAN Q L,HUANG J,ZHANG S Y,et al.Response of microbiota to exogenous inoculation improved the enzymatic activities of mediumtemperature Daqu[J].Frontiers in Microbiology,2022,13:1047041.
[3]张柱,黄钧,周荣清,等.红曲霉对高温大曲的扰动及制曲工艺探究[J].食品与发酵工业,2025,51(2):275-284.ZHANG Z,HUANG J,ZHOU R Q,et al.Exploration of Monascus disturbance on high-temperature Daqu and their manufacturing process[J].Food and Fermentation Industries,2025,51(2):275-284.
[4]DEBRAY R,HERBERT R A,JAFFE A L,et al.Priority effects in microbiome assembly[J].Nature Reviews Microbiology,2022,20(2):109-121.
[5]ALEX CHEONG J Z,JOHNSON C J,WAN H X,et al.Priority effects dictate community structure and alter virulence of fungal-bacterial biofilms[J].The ISME Journal,2021,15(7):2012-2027.
[6]WEIDLICH E W A,NELSON C R,MARON J L,et al.Priority effects and ecological restoration[J].Restoration Ecology,2021,29(1):e13317.
[7]NIKOLOUDAKI O,AHETO F,DI CAGNO R,et al.Synthetic microbial communities:A gateway to understanding resistance,resilience,and functionality in spontaneously fermented food microbiomes[J].Food Research International,2024,192:114780.
[8]JIANG X Y,PENG Z,ZHANG J,.Starting with screening strains to construct synthetic microbial communities (SynComs) for traditional food fermentation[J].Food Research International,2024,190:114557.
[9]XU B Y,XU S S,CAI J,et al.Analysis of the microbial community and the metabolic profile in medium-temperature Daqu after inoculation with Bacillus licheniformis and Bacillus velezensis[J].LWT,2022,160:113214.
[10]吴秋霞,黄钧,江东材,等.基于共培强化提高浓香大曲吡嗪类及4-乙基愈创木酚组分含量的研究[J].食品科技,2017,42(5):2-6.WU Q X,HUANG J,JIANG D C,et al.Exploring the improvement of contents of pyrazines and 4-EG in Luzhou-flavor Daqu based on fortifying by co-culture[J].Food Science and Technology,2017,42(5):2-6.
[11]LI H M,HOU Y C,ZOU W,et al.Synthesis of an autochthonous microbiota responsible for the prepared process improving,flavor profile and brewing attributes of high-temperature Daqu[J].Food Bioscience,2025,68:106444.
[12]ZHANG Y,ZHANG Z,HUANG J,et al.Characterizing the contribution of strain specificity to the microbiota structure and metabolites of Muqu and fresh high-temperature Daqu[J].Foods,2024,13(19):3098.
[13]LIU W H,CHAI L J,WANG H M,et al.Community-level bioaugmentation results in enzymatic activity-and aroma-enhanced Daqu through altering microbial community structure and metabolic function[J].Food Bioscience,2024,57:103630.
[14]LIU S P,ZHOU Y,MA D N,et al.Environment microorganism and mature daqu powder shaped microbial community formation in mechanically strong-flavor daqu[J].Food Bioscience,2023,52:102467.
[15]唐慧芳,黄钧,周荣清,等.场地异质性对中高温大曲微生物群落及品质影响的研究[J].食品与发酵工业,2023,49(8):237-244.TANG H F,HUANG J,ZHOU R Q,et al.Effect of site heterogeneity on microbial community and quality of medium-high temperature Daqu[J].Food and Fermentation Industries,2023,49(8):237-244.
[16]TANG Q X,ZHANG Y,HUANG J,et al.Unraveling the unique microbiota and metabolites in three different colors Jiangqu through multidimensional analysis[J].Food Chemistry,2025,466:142256.
[17]陈晓茹,黄钧,周荣清,等.强化曲贮存过程中群落与代谢组分的变化规律[J].食品与发酵工业,2022,48(3):63-69.CHEN X R,HUANG J,ZHOU R Q,et al.Changes of community and metabolic components during the storage of fortified Daqu[J].Food and Fermentation Industries,2022,48(3):63-69.
[18]MU Y,HUANG J,ZHOU R Q,et al.Comprehensive analysis for the bioturbation effect of space mutation and biofortification on strong-flavor Daqu by high-throughput sequencing,volatile analysis and metabolomics[J].Food Chemistry,2023,403:134440.
[19]TANG Q X,HE G Q,HUANG J,et al.Characterizing relationship of microbial diversity and metabolite in Sichuan Xiaoqu[J].Frontiers in Microbiology,2019,10:696.
[20]BOLYEN E,RIDEOUT J R,DILLON M R,et al.Reproducible,interactive,scalable and extensible microbiome data science using QIIME 2[J].Nature Biotechnology,2019,37(8):852-857.
[21]CALLAHAN B J,MCMURDIE P J,ROSEN M J,et al.DADA2:High-resolution sample inference from Illumina amplicon data[J].Nature Methods,2016,13(7):581-583.
[22]BOKULICH N A,KAEHLER B D,RIDEOUT J R,et al.Optimizing taxonomic classification of marker-gene amplicon sequences with QIIME 2’ s q2-feature-classifier plugin [J].Microbiome,2018,6(1):90.
[23]QUAST C,PRUESSE E,YILMAZ P,et al.The SILVA ribosomal RNA gene database project:Improved data processing and webbased tools[J].Nucleic Acids Research,2013,41(Database issue):D590-D596.
[24]DOUGLAS G M,MAFFEI V J,ZANEVELD J R,et al.PICRUSt2 for prediction of metagenome functions[J].Nature Biotechnology,2020,38(6):685-688.
[25]QIAN W,LU Z M,CHAI L J,et al.Cooperation within the microbial consortia of fermented grains and pit mud drives organic acid synthesis in strong-flavor Baijiu production[J].Food Research International,2021,147:110449.
[26]FENG K,KAN X Y,YAN Y J,et al.Identification and characterization of terpene synthase OjTPS1 involved in β-caryophyllene biosynthesis in Oenanthe javanica (Blume) DC[J].Industrial Crops and Products,2023,192:115998.
[27]陈晓茹,黄钧,周荣清,等.不同强化方式对浓香型白酒大曲特性的影响[J].食品与发酵工业,2021,47(15):50-55.CHEN X R,HUANG J,ZHOU R Q,et al.Effects of fortifying patterns on the characteristics of strong flavor type Daqu[J].Food and Fermentation Industries,2021,47(15):50-55.
[28]孙思佳,翟磊,于学健,等.扣囊复膜孢酵母CICC 33077对芝麻香白酒高温大曲微生物群落结构和功能特性的影响[J].食品与发酵工业,2023,49(7):99-105.SUN S J,ZHAI L,YU X J,et al.Influences of Saccharomycopsis fibuligera CICC 33077 on microbial community and functional characteristics of high temperature Daqu in sesame flavor Baijiu[J].Food and Fermentation Industries,2023,49(7):99-105.
[29]GUAN T W,WEI X Y,QIU X P,et al.Precipitation and temperature drive microbial community changes affecting flavor quality of Nongxiangxing Daqu[J].Food Chemistry:X,2024,24:102063.
[30]ZHANG M Z,WU X F,MU D D,et al.Profiling the influence of physicochemical parameters on the microbial community and flavor substances of Zaopei[J].Journal of the Science of Food and Agriculture,2021,101(15):6300-6310.
[31]CAO R J,MA Y S,ZHOU Q W,et al.Mucorpepsin from Rhizomucor pusillus relates the quality of medium-temperature Daqu[J].Food Bioscience,2024,59:104027.
[32]CHEN G M,YUAN Y J,TANG S W,et al.Comparative analysis of microbial communities and volatile flavor components in the brewing of Hongqu rice wines fermented with different starters[J].Current Research in Food Science,2023,7:100628.
[33]PALOMO-BRIONES R,DE JESÚS MONTOYA-ROSALES J,RAZO-FLORES E.Advances towards the understanding of microbial communities in dark fermentation of enzymatic hydrolysates:Diversity,structure and hydrogen production performance[J].International Journal of Hydrogen Energy,2021,46(54):27459-27472.
[34]柯涛,周业皓,姜鹏,等.中高温强化大曲生产工艺及特性研究[J].中国酿造,2019,38(2):47-52.KE T,ZHOU Y H,JIANG P,et al.Production process and characteristics of medium and high temperature fortified Daqu[J].China Brewing,2019,38(2):47-52.
[35]HE G Q,DONG Y,HUANG J,et al.Alteration of microbial community for improving flavor character of Daqu by inoculation with Bacillus velezensis and Bacillus subtilis[J].LWT,2019,111:1-8.