随着经济发展和城市化进程加快,全球餐厨垃圾产量急剧增加[1-2]。在我国,餐厨垃圾占城市生活垃圾的40%~ 60%,预计到2026年底其产量会达到1.81亿t[3]。餐厨垃圾有机物丰富、含水量高,在收集、运输、存储过程中极易滋生各类乳酸菌,该类微生物发酵餐厨垃圾产生大量乳酸[4-5]。乳酸是一种糖基化学物质,餐厨垃圾中成分复杂,含有大量的蛋白质、残糖、无机盐和有机酸等杂质,使得乳酸分离纯化困难,且成本很高[6-8]。而且乳酸菌群在餐厨垃圾环境中属于开放式发酵,产生的乳酸光学纯度低,低纯度的乳酸难以满足工业应用[9]。因此采用分离纯化的方式将乳酸从餐厨垃圾中分离提取出来的可行性不高。然而,乳酸作为一种优质的碳源可用于微生物培养生产单细胞蛋白,促进微生物生长代谢,实现餐厨垃圾的最大资源化、无害化利用。
但研究表明乳酸会破坏细胞壁和细胞膜的完整性,以未解离的分子形式通过被动扩散轻松穿透细胞膜进入细胞质。在接近中性的细胞质中,乳酸会解离并释放乳酸根离子和氢离子,使细胞质酸化。这些离子会在细胞中积累,导致细胞内pH发生改变,从而引发能量消耗大的应激反应以恢复体内平衡,从而影响细胞整体生长和代谢功能[10-11]。因此了解功能性菌株对乳酸应激响应机制至关重要。酿酒酵母(Saccharomyces cerevisiae)是一种著名的、公认安全的模式微生物,因其操作简便、发酵效率高、培养成本低、耐受低pH和高渗透压等特性被广泛应用于食品工业、生物制药、生物能源等领域[12-13]。然而,目前对餐厨垃圾发酵过程中,酿酒酵母如何应对乳酸胁迫以保证细胞活力和代谢的研究尚不充分。
因此,本研究将通过测定乳酸胁迫对酿酒酵母的细胞表面形态、细胞膜通透性和胞外腺苷三磷酸(adenosine triphosphate,ATP)含量的影响,结合转录组学分析深入揭示酿酒酵母对乳酸的应激响应机制和代谢调控,为阐明酿酒酵母应对乳酸胁迫的作用机制和后续餐厨垃圾发酵工艺的优化提供理论支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 实验菌株与培养基
酿酒酵母N85,由暨南大学生命科学技术学院生命与健康工程研究院生物质资源能源研究所保藏。
YPD培养基(g/L):酵母提取物10.0、蛋白胨20.0、无水葡萄糖20.0(单独灭菌),去离子水溶解后定容。
酵母浸出粉胨乳酸(yeast extract peptone lactate,YPL)培养基(g/L):酵母提取物10.0、蛋白胨20.0、不同浓度乳酸,去离子水溶解后定容。
上述培养基菌在121 ℃,高压灭菌20 min。
1.1.2 实验试剂
蛋白胨、酵母提取物,英国Oxoid公司;无水葡萄糖和乳酸,上海麦克林有限公司;无水乙醇,广州化学试剂厂;电镜固定液,塞维尔生物科技有限公司;ATP含量试剂盒,南京建成生物工程研究所。
1.2 仪器与设备
H2050R高速冷冻离心机,湖南湘仪实验室仪器开发有限公司;YLD-2000电热恒温鼓风干燥箱,黄石市恒丰医疗器械有限公司;Nano-00微量分光光度计,杭州奥盛仪器科技有限公司;Ultra-55场发射扫描电子显微镜(field emission scanning electron microscope,FE-SEM),德国蔡司公司。
1.3 实验方法
1.3.1 酿酒酵母在不同浓度乳酸下培养
将保存的酿酒酵母按1%接种量接种至5 mL YPD培养基中,30 ℃,200 r/min培养活化菌种。将活化好的菌株以1%的接种量分别转接至50 mL YPD培养基中扩大培养。将扩大培养的菌种分别接种至不同体积分数(1%、2%、3%、4%、5%)乳酸为唯一碳源的YPL培养基中,初始OD600=1.0,30 ℃,200 r/min培养。每隔24 h取样测定酿酒酵母生长曲线。
1.3.2 细胞外ATP含量测定
使用ATP含量试剂盒来测定细胞外ATP含量来阐明乳酸对酿酒酵母细胞损伤的影响[14]。酿酒酵母在YPD培养基中培养至对数生长期,收集菌体,并用无菌水洗涤菌体3次。使用无菌水和30 g/L乳酸重悬菌体,并分别处理3、6、9 h。4 ℃,4 000 r/min离心10 min,收集上清液。以未处理组为对照,根据ATP试剂盒说明书步骤与试剂反应后用酶标仪测定636 nm处的吸光值来测定胞外ATP含量。
1.3.3 细胞膜通透性分析
通过测定细胞内核酸和蛋白质的泄漏情况间接反映细胞膜的通透性[15]。酿酒酵母在YPD培养基中培养至对数生长期,收集菌体,并用无菌水洗涤菌体2次。使用无菌水和30 g/L乳酸重悬菌体,并分别处理3、6 h。4 ℃,4 000 r/min离心10 min,收集上清液。通过用微量分光光度计分别测量260 nm和280 nm处的吸光度来测定上清液中的核酸和蛋白质含量。
1.3.4 细胞表面形态分析
使用FE-SEM观察乳酸处理前后酿酒酵母细胞形态结构的变化[16]。酿酒酵母在YPD培养基中培养至对数生长期,收集菌体,并用无菌水洗涤菌体2次。使用30 g/L乳酸重悬菌体,并分别处理3 h和6 h。4 ℃,8 000 r/min离心10 min,收集菌体,并用无菌水洗涤菌体3次,以未处理组为对照。细胞用体积分数2.5%戊二醛溶液在4 ℃下过夜固定,然后用不同体积分数的乙醇溶液(30%、50%、70%、80%、90%,95%、100%)梯度洗脱,干燥后喷金处理,置于FE-SEM下扫描观察细胞表面形态。
1.3.5 转录组测序样本的制备及测序
将保存的酿酒酵母按1% 接种量接种至5 mL YPD培养基中,30 ℃,200 r/min培养活化菌种。将活化好的菌种分别接种至YPD培养基和含30 g/L乳酸的YPL培养基中,30 ℃,200 r/min培养至对数生长期取样。样品在4 ℃,10 000 r/min离心2 min,用PBS洗涤菌体3次。菌体用液氮速冻30 min后保存于-80 ℃冰箱中用于转录组测序,每个样品做3个重复。RNA提取、文库构建及测序由上海美吉生物医药科技有限公司完成。
1.3.6 原始数据质控及基因组比对分析
使用软件fastp(https://github.com/OpenGene/fastp)对原始测序数据进行质控,得到高质量的测序数据。使用HiSat2(http://ccb.jhu.edu/software/hisat2/index.shtml)将质控后的数据与参考基因组(https://www.ncbi.nlm.nih.gov/datasets/genome/GCF_000146045.2/)比对,获得用于后续转录本组装、表达量计算等的比对数据,同时对该次转录组测序的比对结果进行质量评估。
使用软件 RSEM (http://deweylab.github.io/RSEM/)分别对基因和转录本的表达水平进行定量分析,以便后续分析不同样本间基因/转录本的差异表达情况,并可通过结合序列功能信息,揭示基因的调控机制。
1.3.7 基因差异表达分析
使用软件DESeq2(http://bioconductor.org/packages/stats/bioc/DESeq2/)进行基因差异表达分析,显著差异表达基因的默认筛选标准为:FDR <0.05&|log2FC|≥1,当1个基因同时满足这2个条件时,则视该基因为差异表达基因(differentially expressed genes,DEGs)。
使用软件 Goatools (https://github.com/tanghaibao/GOatools)进行富集分析,使用方法为Fisher精确检验。使用4种多重检验方法(Bonferroni,Holm,Sidak和false discovery rate)对P 值进行校正,通常情况下,当经过校正的P 值<0.05时,认为此GO功能存在显著富集情况。使用Python软件包(https://scipy.org/install/)进行KEGG PATHWAY富集分析,使用Fisher精确检验进行计算。采用BH(FDR)方法进行多重检验,经过校正的P 值以0.05为阈值,满足此条件的KEGG通路定义为在差异表达基因中显著富集的KEGG通路。
1.3.8 实时荧光定量聚合酶链式反应(polymerase chain reaction,PCR)分析
为了评估转录组数据差异表达基因的准确性和可靠性,从测序结果中随机挑选11个显著上调和下调基因进行实时定量荧光PCR评估转录组数据的有效性。以ALG9作为内参基因[17],使用SnapGene 4.3.6(Dotmatics)软件设计11个选定目标基因以及内参基因的引物用于实验(引物序列如表1所示)。采用2-ΔΔCt法对结果进行分析,并与转录组测序结果相关基因表达量进行比较。
表1 实时定量荧光PCR所用引物序列
Table 1 Primer sequences used for quantitative real-time PCR

培养酿酒酵母细胞生长至指数期取样,4 ℃,12 000 ×g 离心5 min获得酿酒酵母细胞。使用通用型RNA小提试剂盒提取酿酒酵母RNA。用Evo MMLV反转录预混型示踪试剂盒将其逆转录为cDNA,用Hieff® qPCR SYBR Green Master Mix和CFX ConnectTM实时PCR检测系统(Bio-Rad)进行实时荧光定量PCR反应。
1.4 数据处理
实验3次重复,数据均用“平均值± 标准差”进行描述。使用IBM Spss Statistics 26.0软件对实验数据进行统计学分析,2组数据间比较采用独立样本t检验;多组数据间采用单因素方差分析Fisher最小显著差数法(least significant difference,LSD)检验;P <0.05为差异显著。使用Origin 2018软件绘图。
2 结果与分析
2.1 乳酸对酿酒酵母生长生理特性的影响
2.1.1 不同浓度乳酸对酿酒酵母生长的影响
酿酒酵母在不同浓度的乳酸条件下的细胞生长情况如图1-a所示。乳酸浓度对酿酒酵母的生长具有显著影响,且浓度越高,对酵母生长的抑制作用越明显。在低乳酸浓度下(1% 和2%),酿酒酵母生长基本不受影响。乳酸浓度升高至3%、4%、5%时,酿酒酵母的生长受到了抑制,滞后期相应延长。在3%和4%乳酸浓度下,酿酒酵母的生长受到轻微抑制。当乳酸浓度升高至5%时,酵母细胞的生长受到显著抑制,滞后期延长至72 h。根据菌体生长情况和餐厨垃圾乳酸测定数据选择30 g/L作为后续应激响应和转录组测序分析实验浓度。
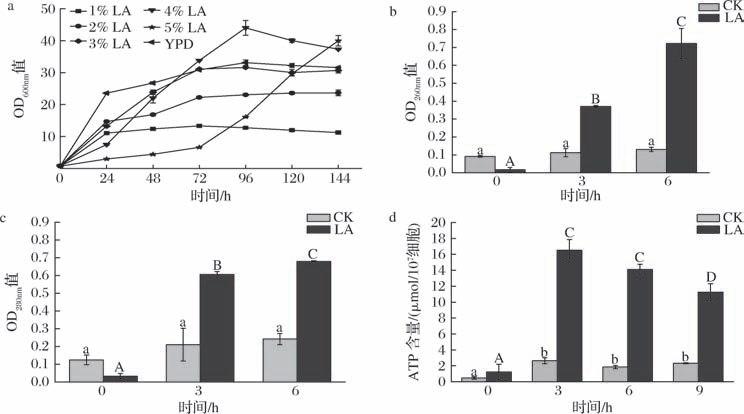
图1 乳酸处理对酿酒酵母生长生理特性的影响
Fig.1 Effect of lactic acid treatment on the growth and physiological characteristics of S.cerevisiae
注:图中字母表示显著性差异(P <0.05,下同)。
a-生长曲线;b-胞外核酸含量;c-胞外蛋白质含量;d-胞外ATP含量
2.1.2 乳酸处理对细胞膜通透性的影响
核酸和蛋白质是细胞内重要的生物大分子,在细胞膜通透性正常的情况下,一般不会泄漏至细胞外。核酸中嘌呤和嘧啶碱基的共轭双键吸收峰在260 nm处,蛋白质中色氨酸和苯丙氨酸残基含有苯环,吸收峰在280 nm处,因此通过测定上清液在260、280 nm处的吸光值来间接反映酿酒酵母细胞膜的通透性。如图1-b和图1-c所示,经乳酸处理后,酿酒酵母细胞中蛋白质和核酸的释放显著升高(P <0.05),处理时间越长,上清液中核酸和蛋白质释放量越高。与对照组相比,乳酸处理3 h后上清液中核酸和蛋白质浓度分别增加了3.29和3.00倍。处理6 h后上清液中核酸和蛋白质含量分别增加了5.53和2.80倍。上述结果说明,在乳酸胁迫下酵母细胞膜的通透性显著增加,细胞内的核酸和蛋白质大量泄露细胞外。
2.1.3 乳酸处理对细胞外ATP含量的影响
ATP广泛存在于所有生物细胞中,是重要的能量分子之一,也是应激条件下生理状态的重要指标。因此可通过测定细胞外ATP含量的变化来反映酿酒酵母细胞对乳酸的应激响应(图1-d)。结果表明,乳酸处理后酿酒酵母细胞外ATP含量显著增加(P <0.05)。在乳酸处理3 h后,细胞外ATP含量升高至(16.5±1.36) μmol/107细胞,与对照组相比增加了7.05倍。当处理时间延长至6 h和9 h时,细胞外ATP的含量开始逐渐下降,这可能是因为细胞逐渐适应酸性环境后调整了能量代谢,减少ATP的分泌,将更多能量用于其他关键代谢和修复机制,帮助细胞维持生存和代谢平衡。上述结果表明,在乳酸条件下酿酒酵母细胞会分泌大量ATP至细胞外,其原因可能是酸胁迫导致细胞内pH下降,细胞通过细胞膜上的H+-ATPase将H+泵出细胞外维持细胞内环境酸碱平衡,这一过程可能导致细胞外ATP浓度升高[18-19]。此外,乳酸处理后会使细胞膜通透性发生改变,导致细胞内ATP泄漏到细胞外。随着胁迫时间的延长,酿酒酵母细胞会通过减少细胞外ATP的分泌来维持自身内部的能量需求和生理功能。
2.2 乳酸处理对酿酒酵母细胞表面形态的影响
在强酸强碱胁迫下,细胞膜会首先被破坏,因此通过FE-SEM观察酿酒酵母细胞表面形态的变化,发现乳酸处理前后酿酒酵母的细胞膜表面形态具有明显差异,未用乳酸处理的细胞表面光滑、饱满、平整、芽痕多,外观呈椭圆形或圆形(图2-a)。而在乳酸处理后细胞表面发生明显变形,细胞膜表面变得粗糙、凹凸不平、出现缝隙甚至破裂,芽痕数量少,细胞相互粘连并凝聚(图2-b和图2-c),并且随着处理时间的延长,细胞表面粗糙程度和细胞粘连更明显。细胞表面变得粗糙、凹凸不平可能是由于细胞膜的脂质和蛋白质结构受到破坏,导致细胞膜的紧密性降低[20]。
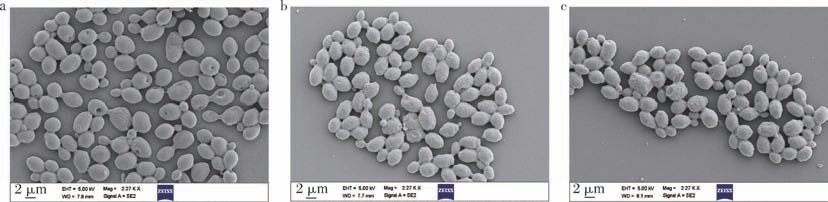
图2 酿酒酵母细胞FE-SEM图
Fig.2 FE-SEM images of S.cerevisiae cells
a-对照组;b-乳酸处理3 h;c-乳酸处理6 h
2.3 乳酸胁迫下酿酒酵母转录组学分析
2.3.1 转录组测序数据质量控制及评估
采用Illumina高通量测序技术对样品进行转录组测序,WT_G1、G2、G3表示以葡萄糖为碳源的3组平行,WT_L1、L2、L3表示以乳酸为碳源的3组平行。所有样品质控数据均达到质量要求,结果如表2所示。所有样品经过滤后获得了5~ 6 G的Clean reads,Q20和Q30都在95%以上,GC含量在41%左右,说明转录组测序原数据准确可靠,可用于后续分析。
表2 样本测序数据统计
Table 2 Sequencing data statistics for samples
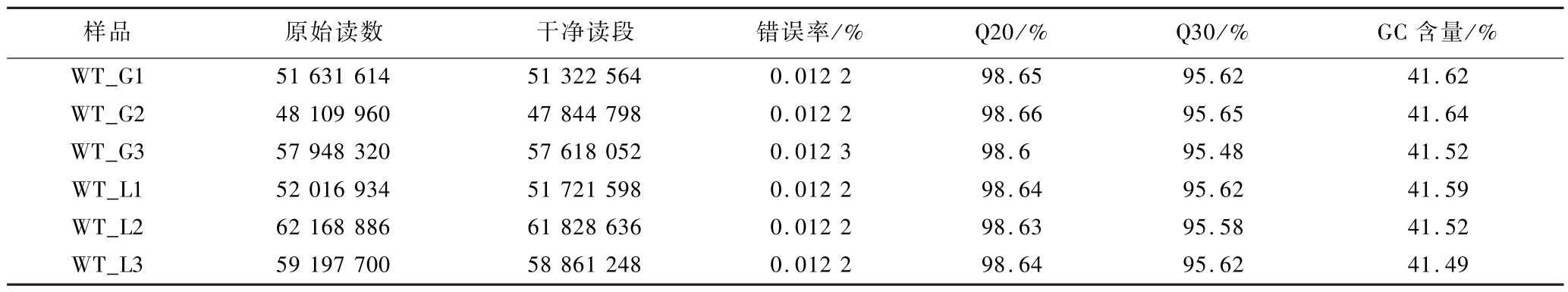
注:Q20与Q30表示质量值≥20或30的碱基所占百分比。
2.3.2 表达量差异分析
对各组间的基因表达情况进行差异分析,筛选出酿酒酵母在葡萄糖和乳酸条件下的DEGs。结果如图3所示,在上述标准下一共筛选出1 757个DEGs,包括908个上调基因和849个下调基因。
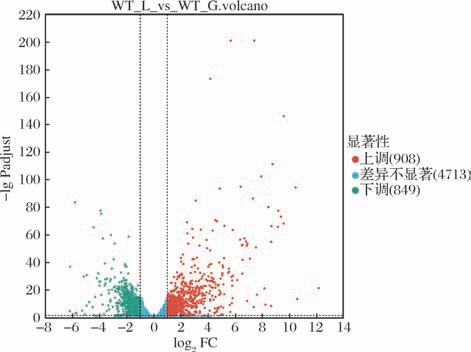
图3 差异表达基因火山图
Fig.3 Volcano plot of differentially expressed genes
2.3.3 差异表达基因富集分析
将上述筛选得到的差异表达基因进行进一步GO富集分析可以研究基因的功能(图4-a)。GO基因富集可以描述为三类:生物学过程、细胞的组分和分子功能。对葡萄糖和乳酸处理条件下酿酒酵母DEGs进行GO富集发现,20条显著富集的通路中有9条与核糖体功能有关,这些DEGs在乳酸胁迫下表达水平发生改变,核糖体蛋白基因表达的差异可能与细胞对环境变化的适应性有关。有3条与酸代谢过程相关,包括羧酸代谢过程、含氧酸代谢过程和有机酸代谢过程,在乳酸胁迫下,参与有机酸代谢过程的基因表达发生了改变,细胞通过有机酸的代谢以维持内部环境的稳定。
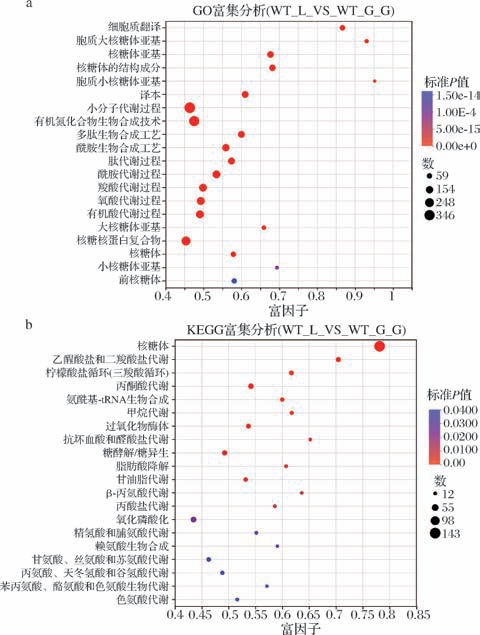
图4 差异表达基因富集分析汽泡图
Fig.4 Bubble plot of enrichment analysis for differentially expressed genes
a-GO富集分析;b-KEGG富集分析
葡萄糖和乳酸处理条件下酿酒酵母DEGs的KEGG富集分析主要集中在核糖体、碳水化合物代谢、能量代谢等过程(图4-b)。值得注意的是,有143个DEGs富集在核糖体途径,大部分与细胞质和线粒体核糖体生物合成相关的基因下调,说明核糖体在乳酸胁迫下发挥着重要作用,这与GO富集分析的结果一致。此外,29个DEGs富集在三羧酸循环,29个DEGs富集在乙醛酸和二羧酸代谢,39个DEGs富集在丙酮酸代谢中,34个DEGs富集在糖酵解/糖异生代谢,40个DEGs富集在氧化磷酸化,17个DEGs富集在丙酸代谢中。有趣的是,本文还发现参与各类氨基酸代谢和生物合成的基因也有显著差异表达,这表明氨基酸代谢在乳酸应激反应中也发挥作用。
2.3.4 实时荧光定量PCR验证转录组数据有效性
为了验证转录组数据的有效性和可靠性,从测序结果中随机挑选11个显著DEGs进行实时荧光定量PCR。包括5个上调基因和6个下调基因,以内参基因ALG9归一化进行定量,采用2-ΔΔCt 法进行分析。结果如图5所示,所挑选的差异表达基因实时荧光定量RCR验证结果与转录组数据表现出一致的趋势,表明转录组数据的可靠性和准确性。
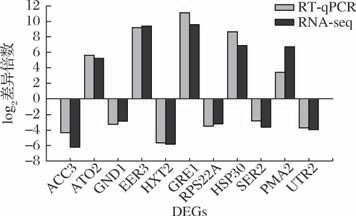
图5 差异表达基因的RT-qPCR验证
Fig.5 RT-qPCR validation of differentially expressed genes
2.3.5 乳酸胁迫下相关基因表达分析
2.3.5.1 乳酸分解代谢
基于转录组数据,酿酒酵母在乳酸胁迫下的乳酸分解代谢调控及其关键相关基因表达变化如表3所示。乳酸的摄取和转运是乳酸分解代谢的第一步,单羧酸转运蛋白通过跨膜运输将乳酸从细胞外转运到细胞内,在乳酸的转运上起着关键作用[21]。在以乳酸为碳源的条件下,编码乳酸转运蛋白的JEN1 和ADY2 基因表达量分别显著上调了6.55和3.42倍。乳酸进入细胞后被CYB2 和DLD1 基因编码的L/D-乳酸-细胞色素C氧化还原酶氧化成丙酮酸,是乳酸分解代谢的关键步骤。转录组数据显示,CYB2 和DLD1 基因的表达水平显著上调,并且参与非发酵碳源的代谢调控和应激响应的转录因子ADR1 和HAP4等被激活。丙酮酸最后转化为乙酰辅酶A进入三羧酸循环来维持细胞能量代谢,通过糖异生途径参与其他生物分子的合成。 PYC1 和PCK1 基因分别编码丙酮酸羧化酶和磷酸烯醇式丙酮酸羧激酶,在糖异生和三羧酸循环途径中发挥重要作用[22-23]。参与三羧酸循环的PDC6、CIT3、IDP2、IDP3、KGD2 等相关基因表达水平整体显著上调,为细胞的正常生理活动提供能量。
表3 乳酸分解代谢相关差异表达基因
Table 3 Differentially expressed genes related to lactic acid degradation metabolism
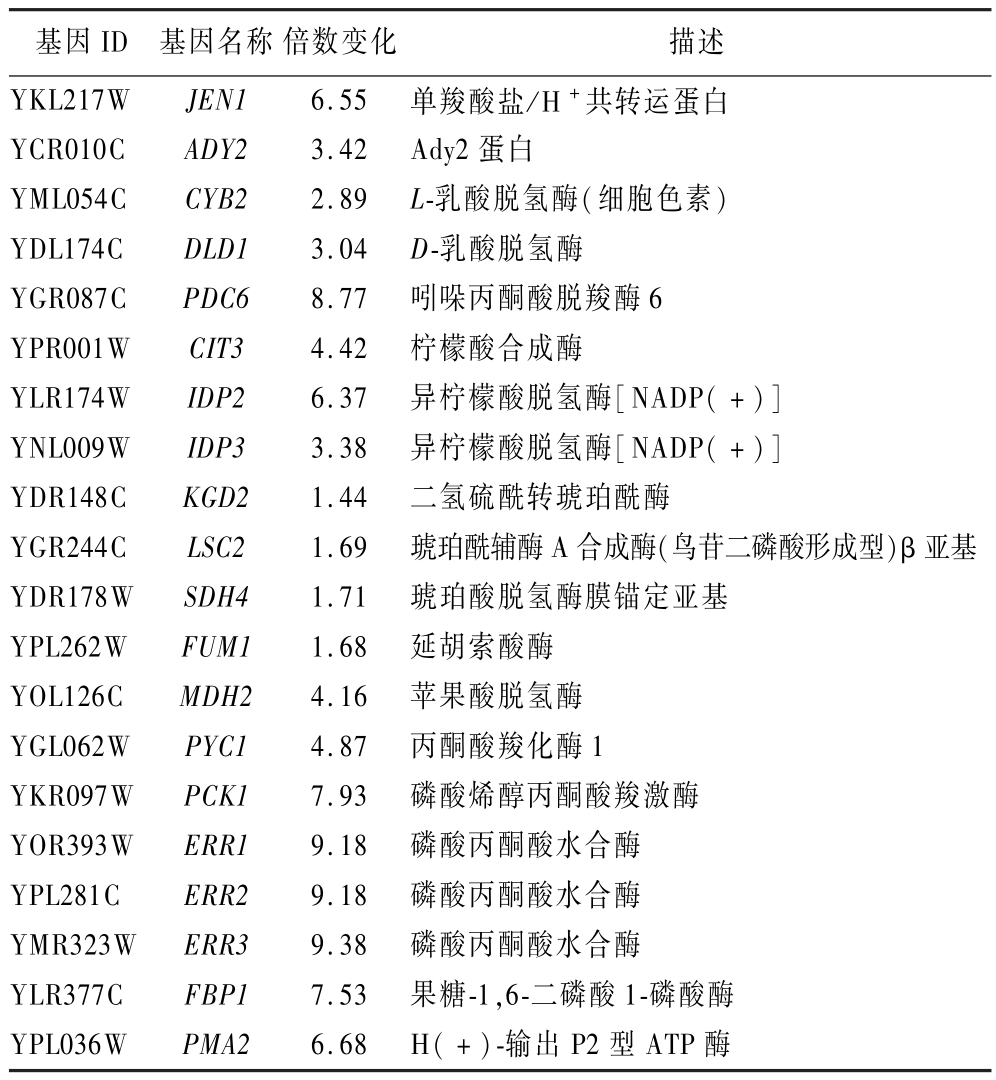
乳酸分解代谢调控过程除了转运和氧化分解代谢基因上调之外,调节H+转运的相关基因也发生了显著变化。其中编码质膜氢离子泵的PMA2 基因表达水平显著上调,该基因表达水平的增加为H+转运提供充足的能量,同时加速H+ 转运至细胞外,维持细胞内酸碱平衡和离子稳态,从而提高酿酒酵母细胞对乳酸的耐受性[24]。
综上所述,酿酒酵母通过对乳酸的转运、氧化分解、丙酮酸代谢以及三羧酸循环等一系列过程关键相关基因的调控,来实现乳酸的有效分解代谢。
2.3.5.2 核糖体代谢
真核生物核糖体由一个40S亚基、一个60S亚基和4种RNA组成,其结构和功能受营养状态、能量代谢、应激反应、生长阶段等多种因素的调控[25-26]。酿酒酵母核糖体代谢部分相关基因(RPL 基因和RPS基因)的表达变化如表4所示。核糖体是蛋白质合成的场所,蛋白质的合成和维持需要消耗大量能量和资源。在乳酸条件下,核糖体代谢相关基因的表达全部显著下调,表明酿酒酵母细胞可能通过抑制核糖体生物合成来减少蛋白质合成,降低能量消耗和代谢负担,将更多资源用于应激反应和其他能量代谢通路。此外,核糖体基因下调可能是酵母细胞调控氧化损伤修复的策略之一。酸性环境会间接导致活性氧积累,引发核糖体损伤,酿酒酵母通过减少蛋白质合成降低细胞内的氧化应激水平并且防止错误蛋白的积累[27]。上述结果表明,酿酒酵母通过下调核糖体相关基因的表达,减少蛋白质的合成、降低代谢负担和激活氧化损伤修复从而响应乳酸胁迫。
表4 核糖体代谢相关差异表达基因
Table 4 Differentially expressed genes related to ribosome metabolism

2.3.5.3 能量代谢
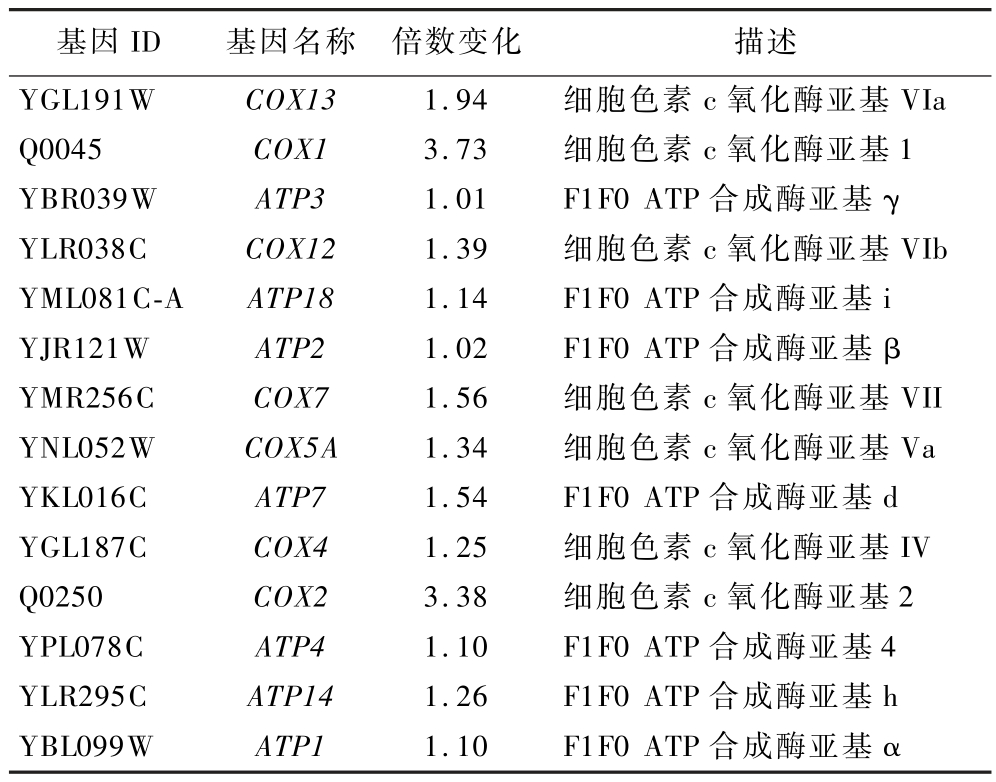
线粒体是细胞的能量工厂,通过氧化磷酸化过程产生细胞的能量货币ATP。在细胞面临能量需求增加或环境胁迫时,参与ATP合成和能量代谢的基因表达水平会上调,以满足细胞的能量需求[28]。乳酸胁迫下,酿酒酵母能量代谢相关基因的转录变化如表5所示。转录组数据显示编码线粒体呼吸链复合体的基因(COX 基因)和ATP合酶的基因(ATP 基因)的表达水平显著上调。 COX13、COX12、COX7、COX5A 不仅与线粒体呼吸链复合物Ⅳ、Ⅴ、线粒体电子传递和氧化磷酸化有关,还可编码细胞色素氧化酶(cytochrome C oxidase,COX),这种酶催化电子从细胞色素C转移到分子氧和质子泵穿过线粒体内膜以产生大量ATP。在酿酒酵母的能量代谢过程中,发挥着重要作用的能量相关基因ATP18、ATP2、ATP7、ATP14、ATP12 的表达水平显著升高。这类物质通过参与ATP合酶的组装、稳定性和催化活性的调节,确保细胞能够高效地产生和利用能量。
表5 能量代谢相关差异表达基因
Table 5 Differentially expressed genes related to energy metabolism
2.3.5.4 细胞壁和细胞膜合成代谢
酸性环境会破坏细胞膜和细胞壁的完整性、细胞壁的修复与细胞膜的组成变化协同作用,对于细胞的生存至关重要。在乳酸胁迫下,参与细胞膜和细胞壁合成代谢的相关表达基因如表6所示。细胞壁作为酵母细胞最外层结构具有保护细胞、维持细胞形态、为细胞表面蛋白提供吸附支架等功能[29-30]。细胞壁的完整性对细胞抵御外部胁迫至关重要,在酸胁迫下细胞壁的完整性会受到破坏,对编码细胞壁蛋白相关基因的表达进行调控有助于增强细胞壁的稳定。CWP1 和CWP2 编码细胞壁甘露糖蛋白,是细胞壁的重要组成部分[31]。 PIR3 和YGP1 分别编码O-糖基化的共价结合细胞壁蛋白和分泌性的高度N-糖基化的糖蛋白,参与细胞壁的生物合成和维持细胞壁稳定性。 FKS3 是合成细胞壁β-1,3-葡聚糖的关键基因,同样的对细胞壁的合成和维持细胞形态起着重要作用[32-33]。在乳酸胁迫下,酿酒酵母通过上调这些基因的表达来增强细胞壁合成、修复和重塑,从而维持细胞壁的完整性和稳定性。
表6 细胞壁和细胞膜合成代谢相关差异表达基因
Table 6 Differentially expressed genes related to cell wall and cell membrane biosynthesis metabolism
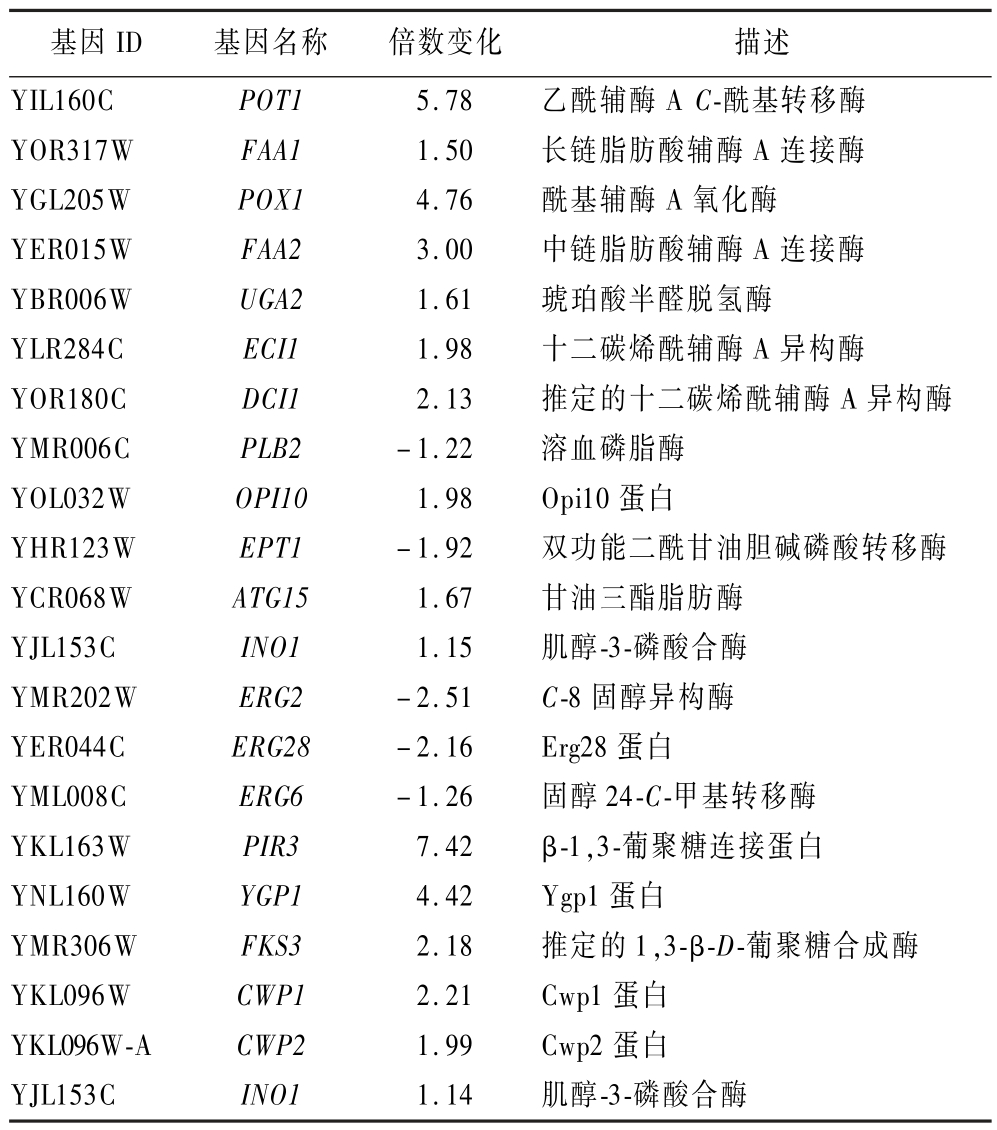
酿酒酵母细胞膜主要由磷脂、麦甾醇和蛋白质构成,酸胁迫会使酿酒酵母细胞膜的组成发生改变。麦角甾醇是酿酒酵母细胞膜的重要脂质成分,转录组数据显示参与调控麦甾醇生物合成的相关基因(ERG基因)在乳酸胁迫下下调,可能是由于乳酸增加了细胞膜通透性与流动性。参与脂肪酸代谢过程的POT1、POX1、FAA1、FAA2、UGA2、ECI1、DCI1 等关键基因的表达显著上调。其中FAA1 基因编码长链脂肪酸酰基-CoA合成酶催化游离脂肪酸转化为脂酰辅酶A,可用于膜磷脂再合成,促进细胞膜修复[34-35]。肌醇是细胞膜磷脂的重要组成部分,INO1 基因表达上调促进肌醇的生物合成,有助于维持细胞膜的完整性和功能。此外,与磷脂生物合成的相关基因OPI10、EPT1、TGL4、ATG15、PLB2 等表达也发生了变化。总体来说,酿酒酵母是通过动态调控细胞膜合成相关基因的表达,改变细胞膜的组成和结构从而抵抗乳酸胁迫。
3 讨论与结论
餐厨垃圾作为一种富含有机质的废弃物,具有显著的资源回收利用价值。通过酿酒酵母发酵可将其转化为生物燃料和单细胞蛋白等高附加值产品[13]。然而,在发酵过程中,酿酒酵母的生长代谢常受到抑制性物质的影响。其中乳酸是餐厨垃圾中的主要抑制物,对细胞生长和代谢具有显著的影响,进而降低发酵效率及产物得率[36]。
本研究系统探究了乳酸胁迫对酿酒酵母生长生理特性及分子调控机制的影响。研究结果表明,乳酸抑制酿酒酵母的生长,乳酸浓度越高抑制作用越明显。乳酸显著增加细胞膜的通透性,在乳酸胁迫下细胞外核酸和蛋白质的释放量相比于对照组显著升高,其原因可能与乳酸破坏了细胞膜的完整性有关,导致细胞膜失去选择性通透屏障功能,类似现象在甲酸胁迫中亦有报道[37]。此外,酿酒酵母可通过动态调节细胞外ATP含量来应对乳酸胁迫。短时间胁迫下,细胞通过增加细胞外ATP的合成调节细胞内pH;随着胁迫时间的延长,细胞会减少细胞外ATP的分泌来维持自身内部的能量需求。这种调节机制有助于酵母在酸胁迫下维持生存和代谢。扫描电镜观察显示,乳酸处理后酿酒酵母细胞膜表面变得粗糙、凹凸不平、出现缝隙,细胞相互粘连并凝聚,这进一步证实乳酸破坏了细胞膜的表面结构。转录组分析表明,乳酸胁迫影响核糖体代谢、三羧酸循环、丙酮酸代谢、脂质代谢和氧化磷酸化等关键通路。具体而言,酿酒酵母通过多个层面的基因表达调控来响应乳酸胁迫,包括上调乳酸分解代谢相关基因以促进乳酸分解;下调核糖体生物合成相关基因以减少蛋白质合成和降低代谢负担;上调能量代谢相关基因的表达以维持细胞的能量平衡和正常生理功能;动态调控细胞膜和细胞壁合成代谢相关基因以抵抗乳酸胁迫。这种协同调控机制揭示了酿酒酵母应对乳酸胁迫的系统性响应。
综上所述,本研究从生理、细胞形态和分子调控3个层面揭示了酿酒酵母响应乳酸胁迫的分子机制,为酿酒酵母的遗传改造提供了潜在的基因靶点,也为优化餐厨垃圾发酵工艺提供理论依据。未来研究将进一步探索关键基因靶点的功能验证,并结合合成生物学和代谢工程手段开发出更具耐受性的酿酒酵母菌株,以提高餐厨垃圾资源转化效率。
[1]SAHA T R,KANG N K,LEE E Y.Advanced metabolic Engineering strategies for the sustainable production of free fatty acids and their derivatives using yeast[J].Journal of Biological Engineering,2024,18(1):73.
[2]STOEVA K,ALRIKSSON S.Influence of recycling programmes on waste separation behaviour[J].Waste Management,2017,68:732-741.
[3]XIONG X L,ZHANG W X,HA X,et al.The preparation processes and influencing factors of biofuel production from kitchen waste[J].Fermentation,2023,9(3):247.
[4]YUKESH KANNAH R,SIVASHANMUGHAM P,Kavitha S,et al.Chapter 3-Valorization of Food Waste for Bioethanol and Biobutanol Production[M].Pittsburgh: Academic Press,2020:39-73.
[5]TANG J L,WANG X C,HU Y S,et al.Effect of pH on lactic acid production from acidogenic fermentation of food waste with different types of inocula[J].Bioresource Technology,2017,224:544-552.
[6]HUANG S Y,XUE Y F,YU B,et al.A review of the recent developments in the bioproduction of polylactic acid and its precursors optically pure lactic acids[J].Molecules,2021,26(21):6446.
[7]DIN N A S,LIM S J,MASKAT M Y,et al.Lactic acid separation and recovery from fermentation broth by ion-exchange resin:A review[J].Bioresources and Bioprocessing,2021,8(1):31.
[8]LI C L,GAO M,ZHU W B,et al.Recent advances in the separation and purification of lactic acid from fermentation broth[J].Process Biochemistry,2021,104:142-151.
[9]SONG L,YANG D H,LIU R,et al.Microbial production of lactic acid from food waste:Latest advances,limits,and perspectives[J].Bioresource Technology,2022,345:126052.
[10]DENG N,DU H,XU Y.Cooperative response of Pichia kudriavzevii and Saccharomyces cerevisiae to lactic acid stress in Baijiu fermentation[J].Journal of Agricultural and Food Chemistry,2020,68(17):4903-4911.
[11]WEI J L,NIE Y,DU H,et al.Serine improves lactic acid stress tolerance and ethanol production in Zygosaccharomyces bailii in baijiu fermentation[J].Journal of Agricultural and Food Chemistry,2023,71(50):20295-20303.
[12]LIAN J Z,MISHRA S,ZHAO H M.Recent advances in metabolic engineering of Saccharomyces cerevisiae:New tools and their applications[J].Metabolic Engineering,2018,50:85-108.
[13]WANG S,ZHAO F G,YANG M L,et al.Metabolic engineering of Saccharomyces cerevisiae for the synthesis of valuable chemicals[J].Critical Reviews in Biotechnology,2024,44(2):163-190.
[14]IGBINOSA E O,BESHIRU A,IGBINOSA I H.Mechanism of action of secondary metabolites from marine-derived Streptoymces on bacterial isolates by membrane permeability[J].Microbial Pathogenesis,2020,149:104532.
[15]LONG X F,XU Y L,ZHAO X M.Response mechanism of Saccharomyces cerevisiae under benzoic acid stress in ethanol fermentation[J].Scientific Reports,2024,14:28757.
[16]XIANG Q S,LIU X F,LI J G,et al.Effects of dielectric barrier discharge plasma on the inactivation of Zygosaccharomyces rouxii and quality of apple juice[J].Food Chemistry,2018,254:201-207.
[17]TESTE M A,DUQUENNE M,FRANÇOIS J M,et al.Validation of reference genes for quantitative expression analysis by real-time RT-PCR in Saccharomyces cerevisiae[J].BMC Molecular Biology,2009,10(1):99.
[18]HOLYOAK C D,STRATFORD M,MCMULLIN Z,et al.Activity of the plasma membrane H(+)-ATPase and optimal glycolytic flux are required for rapid adaptation and growth of Saccharomyces cerevisiae in the presence of the weak-acid preservative sorbic acid[J].Applied and Environmental Microbiology,1996,62(9):3158-3164.
[19]STRATFORD M,NEBE-VON-CARON G,STEELS H,et al.Weak-acid preservatives:pH and proton movements in the yeast Saccharomyces cerevisiae[J].International Journal of Food Microbiology,2013,161(3):164-171.
[20]GU H Q,ZHANG J,BAO J.High tolerance and physiological mechanism of Zymomonas mobilis to phenolic inhibitors in ethanol fermentation of corncob residue[J].Biotechnology and Bioengineering,2015,112(9):1770-1782.
[21]CASAL M,PAIVA S,ANDRADE R P,et al.The lactate-proton symport of Saccharomyces cerevisiae is encoded by JEN1[J].Journal of Bacteriology,1999,181(8):2620-2623.
[22]HUET C,MENENDEZ J,GANCEDO C,et al.Regulation of pyc1 encoding pyruvate carboxylase isozyme I by nitrogen sources in Saccharomyces cerevisiae[J].European Journal of Biochemistry,2000,267(23):6817-6823.
[23]PROFT M,GRZESITZA D.Identification and characterization of regulatory elements in the phosphoenolpyruvate carboxykinase gene PCK1 of Saccharomyces cerevisiae[J].Molecular and General Genetics MGG,1995,246(3):367-373.
[24]SUPPLY P,WACH A,THINÈS-SEMPOUX D,et al.Proliferation of intracellular structures upon overexpression of the PMA2 ATPase in Saccharomyces cerevisiae[J].Journal of Biological Chemistry,1993,268(26):19744-19752.
[25]PARKER M D,KARBSTEIN K.Quality control ensures fidelity in ribosome assembly and cellular health[J].The Journal of Cell Biology,2023,222(4):e202209115.
[26]GRANNEMAN S,BASERGA S J.Ribosome biogenesis:Of knobs and RNA processing[J].Experimental Cell Research,2004,296(1):43-50.
[27]MEYDAN S,BARROS G C,SIMÕES V,et al.The ubiquitin conjugase Rad6 mediates ribosome pausing during oxidative stress[J].Cell Reports,2023,42(11):113359.
[28]SETTEMBRE C,FRALDI A,MEDINA D L,et al.Signals from the lysosome:A control centre for cellular clearance and energy metabolism[J].Nature Reviews Molecular Cell Biology,2013,14(5):283-296.
[29]KLIS F M,MOL P,HELLINGWERF K,et al.Dynamics of cell wall structure in Saccharomyces cerevisiae[J].FEMS Microbiology Reviews,2002,26(3):239-256.
[30]张明芳,王金晶,钮成拓,等.啤酒酵母细胞壁环境压力应答机制研究进展[J].生物工程学报,2019,35(7):1214-1221.ZHANG M F,WANG J J,NIU N,et al.Progress in brewer’s yeast cell wall stress response[J].Chinese Journal of Biotechnology,2019,35(7):1214-1221.
[31]RAMOS-VIANA V,MØLLER-HANSEN I,KEMPEN P,et al.Modulation of the cell wall protein Ecm33p in yeast Saccharomyces cerevisiae improves the production of small metabolites[J].FEMS Yeast Research,2022,22(1):foac037.
[32]BRENNAN T C R,KRÖMER J O,NIELSEN L K.Physiological and transcriptional responses of Saccharomyces cerevisiae to d-limonene show changes to the cell wall but not to the plasma membrane[J].Applied and Environmental Microbiology,2013,79(12):3590-3600.
[33]杨歌,王金晶,李佳,等.FKS家族基因对酿酒酵母压力耐性的影响[J].食品与生物技术学报,2019,38(10):126-134.YANG G,WANG J J,LI J,et al.Effects of FKS family genes on the ability of Saccharomyces cerevisiae stress resistance[J].Journal of Food Science and Biotechnology,2019,38(10):126-134.
[34]METUR S P,KLIONSKY D J.As (and when) you like it:On-demand phospholipid synthesis drives phagophore expansion during autophagy[J].Autophagy,2020,16(5):779-781.
[35]BAUMANN V,ACHLEITNER S,TULLI S,et al.Faa1 membrane binding drives positive feedback in autophagosome biogenesis via fatty acid activation[J].The Journal of Cell Biology,2024,223(7):e202309057.
[36]ZHANG Z S,TSAPEKOS P,ALVARADO-MORALES M,et al.Enhanced fermentative lactic acid production from source-sorted organic household waste:Focusing on low-pH microbial adaptation and bio-augmentation strategy[J].Science of the Total Environment,2022,808:152129.
[37]ZENG L J,SI Z Y,ZHAO X M,et al.Metabolome analysis of the response and tolerance mechanisms of Saccharomyces cerevisiae to formic acid stress[J].The International Journal of Biochemistry &Cell Biology,2022,148:106236.