植物精油具有杀菌抗虫[1-2]、提神醒脑[3]和净化空气[4]等多功效,在农业、食品和医药等领域均可发挥作用,因其具有广谱的抗菌活性,在国内外都有大量的研究报道[5]。其中,香芹酚(carvaceol,CV)[1-3]与肉桂醛(cinnamaldehyde,CA)[4-5]作为植物源活性成分,对食源性致病菌具有显著抑制作用,牛力源等[6]研究发现香芹酚可以通过破坏酿酒酵母细胞膜通透性、阻碍其生物合成以抑制其生命活动,从而使易受酿酒酵母污染的果蔬产品得以延长保质期;黄露露等[7]研究发现4-甲氧基肉桂醛处理能通过调控有机酸代谢增强脐橙果实对采后青霉病的抗性;蒋帅[8]发现肉桂精油熏蒸可以抑制苹果灰霉病的发生。但植物精油的强挥发性、低水溶性与化学不稳定性限制了其实际应用。为了改善植物精油的溶解性、稳定性和生物利用度,常采用包合技术将这些抑菌物质包裹在特定的壁材中,从而提高其水溶性和稳定性,增强其抑菌性能和应用潜力。ERTAN等[9]将γ-环糊精和香芹酚的包合物整合到明胶/支链淀粉纳米纤维中,极大减少了精油的损失;李森等[10]制备出硅藻土负载香芹酚的明胶基复合膜,发现香芹酚经过硅藻土负载后,明胶膜的抑菌性能明显提升;PANT等[11]筛选出不同比例的α/β-环糊精的环糊精纳米海绵,负载肉桂醛可提升抗氧化能力。
基于植物精油的小分子结构,环糊精(cyclodextrin,CD)是包合精油的良好壁材,因其独特的环状结构和疏水空腔而备受关注[12],是一种经典的包合壁材。其制备通常采用酶法手段,先酶解获得环糊精混合物,再通过进一步脱盐脱色、浓缩分离、纯化、结晶等步骤获得单一环糊精成品[13],但因产物抑制作用及纯化分离困难,得率较低[14]。目前工业上生产环糊精通常会引入有机溶剂作为络合剂以减弱产物抑制并及时使产物形成包合物而分离,以此提高得率,后续去除有机溶剂不仅存在毒性残留风险,还增加了成本。因此,本研究团队前期提出了酶法生产环糊精过程一步法包合植物精油的新方法,即在酶法生产环糊精过程中添加植物精油作为络合剂,植物精油在促进环糊精生成的同时又能实现对环糊精产物对植物精油的包合[15],省却了后续分离纯化的步骤,同时生成的环糊精混合物可能比单一环糊精包合效果更好,对包合物的结构和抑菌特性有待进一步深入研究。
前期通过一步法成功制备环糊精-复配植物精油包合体系,本研究以包合物为对象,对其进行系统表征与抑菌性能测定,旨在解决以下问题:a)混合环糊精包合精油的结构表征不充分,未明确建立结构模型;b)复合包合物对细菌的接触抑制与熏蒸抑制协同机制不明;c)包合物挥发动力学与抑菌时效的关联性需进一步验证。通过解析包合物结构特性,并对比其与游离单体的抑菌活性差异,明确复合包合体系的缓释规律与增效机制。研究结果可为天然抗菌剂的功能强化及在食品控菌领域的应用提供技术参考与理论支撑。
1 材料与方法
1.1 材料与试剂
香芹酚(>99%),广州日化化工有限公司;肉桂醛(>99%)、甲基橙、酚酞、溴甲酚绿以及其他常用分析纯化学试剂,国药化学试剂有限公司;大肠杆菌(ATCC 25922)、沙门氏菌(ATCC 14028)、金黄色葡萄球菌(ATCC 6538)、枯草芽孢杆菌(CMCC 63501)、白色念珠菌(ATCC 10231)、黑曲霉(ATCC 16404),以上菌株的二代斜面菌种,上海鲁微科技有限公司;沙氏葡萄糖液体(sabouraud dextrose broth,SDB)培养基、PDA培养基,青岛高科技工业园海博生物技术有限公司;胰蛋白胨大豆肉汤(tryptone soy broth,TSB)培养基,实验室自制;刃天青,北京索莱宝科技有限公司;β-环糊精葡萄糖基转移酶(β-cyclodextrin glycosyltransferase,β-CGT酶,来源于 Bacillus circulans,30 U/mL),自制并保藏于本实验室;玉米淀粉(水分含量11.94%),河北玉峰实业集团有限公司;麦芽糊精(DE=4),罗盖特精细化工(中国)有限公司;α-、β-和γ-环糊精标准品,美国Sigma-Aldrich公司。
1.2 仪器与设备
Julabo TW12恒温水浴锅,德国优莱博;RW 20 D S25悬臂搅拌机、T18型高速剪切机,德国IKA(中国)有限公司;SD-1500实验型喷雾干燥机,上海沃迪自动化装备股份有限公司;SU8100冷场发射扫描电子显微镜,日本日立高新技术株式会社;S3500激光粒度分析仪,美国Microtrac公司;A560双光束紫外可见分光光度计,翱艺仪器(上海)有限公司;Avance III-400 MHz核磁共振仪,德国Bruker AXS公司;GRZ-136S隔水式恒温培养箱,上海森信实验仪器有限公司;SW-CJ-G单人净化工作台,苏净集团苏州安泰空气技术有限公司;G154T立式自动压力蒸汽灭菌器,致微(厦门)仪器有限公司;ZQZY-70BF振荡培养箱,上海知楚仪器有限公司;RJ-LD-50G低速大容量离心机,无锡市瑞江分析仪器有限公司。
1.3 实验方法
1.3.1 复合植物精油包合物的制备
采用LIU等[15]的方法进行实验并优化:将质量分数10%的小麦淀粉乳加入四口烧瓶中,设置转速300 r/min,起始温度50 ℃。加入2 U/(g淀粉)(单位下同)的β-CGT酶,升温至90 ℃保温30 min进行液化。然后降温至50 ℃,加入1 U/g的β-CGT酶进行环化反应,开始后以芯壁比按照质量比1∶6的比例加入复配精油,再加入芯材与壁材总质量的5%的乳化剂吐温80,搅拌均匀,反应12 h结束。后以1.4 ×104 r/min高速剪切2 min。设置进风温度、出风温度分别为180、80 ℃,进料流速为0.4 L/h进行喷雾干燥,获得复合植物精油包合物粉末。
1.3.2 菌悬液的制备
细菌:取4 ℃保存的二代斜面菌株,用无菌接种环挑取菌落接种于TSB培养基中,37 ℃振荡培养12 h至对数期。经平板计数法测定浓度后,将菌悬液与等体积60%甘油混合,分装保菌管于-80 ℃保存备用。
白色念珠菌:取4 ℃保存的二代斜面菌株,用无菌接种环挑取菌落接种于SDB培养基中,25 ℃振荡培养24 h,后续同上。
黑曲霉:取4 ℃保存的二代斜面菌株,用5 mL无菌水洗下斜面表层孢子,与等体积60%甘油混合后,分装保菌管中于-80 ℃保存备用。用无菌接种棒蘸取管中菌液,在PDA培养基斜面中划线培养,培养温度为25 ℃,培养时间5 d。用5 mL无菌水洗下斜面表层孢子,采用血球计数法测定总菌浓度。
1.3.3 抑菌活性的测定
参考《药理实验方法学》采用杯碟法进行实验,操作均在无菌条件下进行[16]。取直径90 mm的玻璃平皿,倾注融化的琼脂培养基,使其在平板内均匀摊布,于水平台面凝固,作为底层。在各平板中以等距离均匀安置牛津杯备用。另取半固体琼脂培养基(琼脂含量为0.8%)适量加热融化后,放冷至45~50 ℃,接入指示菌菌悬液(菌浓度在105~106 CFU/mL),在每个平板中分别加入5 mL,使其在底层上均匀摊布,作为菌层。待菌层凝固取出牛津杯,于孔洞分别滴装200 μL一定浓度的抑菌溶液,将培养皿放入恒温培养箱,细菌37 ℃培养12 h,白色念珠菌25 ℃培养24 h,黑曲霉25 ℃培养5 d。用十字交叉法测量各抑菌圈直径,每株菌重复3次取平均值,并用无菌水作空白对照。
1.3.4 植物精油的复配
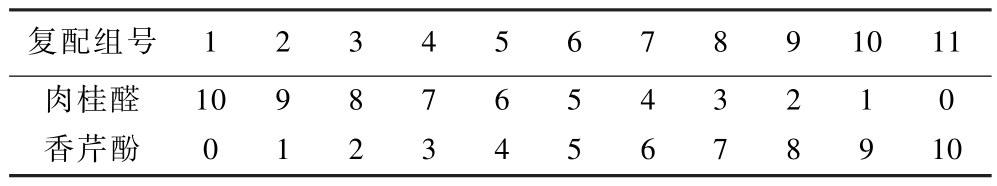
选取抑菌活性较强的肉桂醛和香芹酚,根据不同质量比设计2组分复配精油抗菌剂,各组组分比例如表1所示。选择金黄色葡萄球菌、大肠杆菌、沙门氏菌、枯草芽孢杆菌、白色念珠菌和黑曲霉为供试菌,按照1.3.3节方法进行抑菌实验操作,比较抑菌效果。
表1 二组分精油复合抑菌剂的复配方案(质量比)
Table 1 Compound scheme of two component essential oil (mass ratio)
1.3.5 包合物微观形态观察
用木棒蘸取少量粉末样品点在预先贴好导电胶的样品台上,洗耳球吹尘,置于离子溅射仪中喷金30 s,采用扫描电子显微镜在加速电压5.0 kV的条件下进行观察和拍摄,放大倍数5 000~9 000倍。
1.3.6 包合物粒径分布的测定
采用激光粒度分析仪,干法测定包合物的粒径分布[17]。将适量粉末样品均匀铺洒在样品台上,设定折光率为1.52,测定时间为10 s,启动测定程序,获得包合物的粒径分布结果。
1.3.7 包合稳定常数的测定
参考卢滋等[18]和李泽西[19]的方法,采用竞争紫外-可见光谱法测定。
1.3.8 核磁共振测定
一维和二维核磁均采用全数字化核磁共振波谱仪进行测定。分别称取20 mg环糊精单体、香芹酚单体、肉桂醛单体以及3种环糊精与2种精油组成的包合物溶解于0.5 mL氘代二甲基亚砜(dimethyl sulfoxide-d6,DMSO-d6)有机溶剂,加入四甲基硅烷设定在0.00 ppm化学位移处出峰,作为内标。实验温度设置303 K,共振频率400 MHz,二维核磁中设定混合时间为500 ms。
1.3.9 最小抑菌浓度的测定
包合物处理:用无菌水将包合物配制成10 mg/mL的溶液,待测。精油无需前处理。
最小抑菌浓度采用微量肉汤二倍稀释法测定[20]。于96孔细胞培养板内孔中均加入100 μL液体培养基,在2列孔中加入100 μL待测溶液,混合均匀(测定纯精油时,直接取2 μL加入200 μL液体培养基,反复吹吸混匀)。于2列孔中取100 μL混合液移入3列孔,混匀,再取100 μL混合液移入4列孔,依此类推以达到样品二倍梯度稀释的目的,梯度稀释至10列孔,混匀弃去100 μL,11列孔不含抑菌剂作为空白对照。然后,向各内孔中添加50 μL菌悬浮液(105~106 CFU/mL),盖上孔板盖,于恒温培养箱进行培养(细菌37 ℃孵育12 h,白色念珠菌25 ℃孵育24 h,黑曲霉25 ℃孵育5 d)。孵育完成后,各内孔加入50 μL过滤除菌0.1 g/L刃天青显色液,于培养箱中继续孵育1 h,记录各孔颜色变化。若刃天青显色液颜色从蓝色变为粉色意味着菌的生长,故以保持蓝色的最低样品浓度为最小抑菌浓度。每个样品做3次平行。
1.3.10 包合物熏蒸抑菌性能测定
采取培养皿倒置培养法,在无菌环境中对植物精油包合物熏蒸时的最低抑菌浓度进行研究[21]。首先,吸取5 μL 105 CFU/mL黑曲霉孢子悬浮液于PDA培养基中心干燥10 min,随后将不同浓度的精油或包合物置于培养皿盖子中心,将已接种的培养皿轻扣在皿盖上,25 ℃倒置培养7 d,观察菌落生长情况,计算时考虑培养皿的空间与添加量,培养皿内空间约保持在9 cm ×9 cm ×0.8 cm。
1.3.11 包合物挥发曲线测定
挥发曲线的测定采用恒温恒湿箱,固定湿度为35%~40%相对湿度,固定温度为室温25 ℃。每隔一段时间取样用分光光度法测定精油含量,计算精油的保留率,从而得出包合物的挥发曲线。
1.3.12 包合物挥发后抑菌性能测定
根据1.3.10节及1.3.11节的测定结果,确定挥发后抑菌性能的挥发时间,即在培养皿的盖子中央加入精油或包合物,置于25 ℃恒温恒湿培养箱中敞口静置0、1、2、4、8、16、32 d后,于PDA培养基中央接种5 μL 105 CFU/mL黑曲霉孢子悬浮液,静置干燥10 min,再将培养皿轻轻扣在含有精油或精油包合物的皿盖上,25 ℃倒置培养7 d,菌圈直径采用十字交叉法测量,实验平行3次,以未添加精油或精油包合物为空白对照组。
1.4 数据处理与分析
实验结果为3次或以上独立实验的平均值,用“平均值±标准差”表示;采用Excel 2019和Origin 2019软件进行作图与数据处理;采用IBM SPSS Statistics 25软件分析显著性差异(P <0.05),程序选择:单因素方差分析(AVOVA)—Duncan。
2 结果与分析
2.1 植物精油复配比的确定
选择2种已知抑菌性较强的单一成分精油,分别是香芹酚和肉桂醛。6种食品常见腐败菌大肠杆菌、金黄色葡萄球菌、沙门氏菌、枯草芽孢杆菌、白色念珠菌、黑曲霉作为供试菌,通过研究精油对供试菌的抑菌活性,设计复合精油比例,以达到最佳的抑菌效果。从表2可看出,随着肉桂醛质量占比减少,复合精油对4种细菌的抑菌圈总体呈先增再减的趋势,对白色念珠菌的抑菌圈呈先增后减又增的趋势,对黑曲霉的抑菌圈呈先减小后增大又减小的趋势,但在肉桂醛与香芹酚质量比为6∶4时抑菌圈均明显最大(P <0.05)。综合以上结果,确定肉桂醛与香芹酚的最佳复配比例为6∶4(质量比),此时复配精油对4种供试细菌和2种供试真菌的抑菌活性最强,具有广谱的抑菌活性。后续制备包合物选取抑菌活性最强的肉桂醛与香芹酚质量比为6∶4为复合精油。
表2 复配精油对供试细菌的抑菌圈直径
Table 2 Diameter of inhibition zone of compound essential oil against tested bacteria
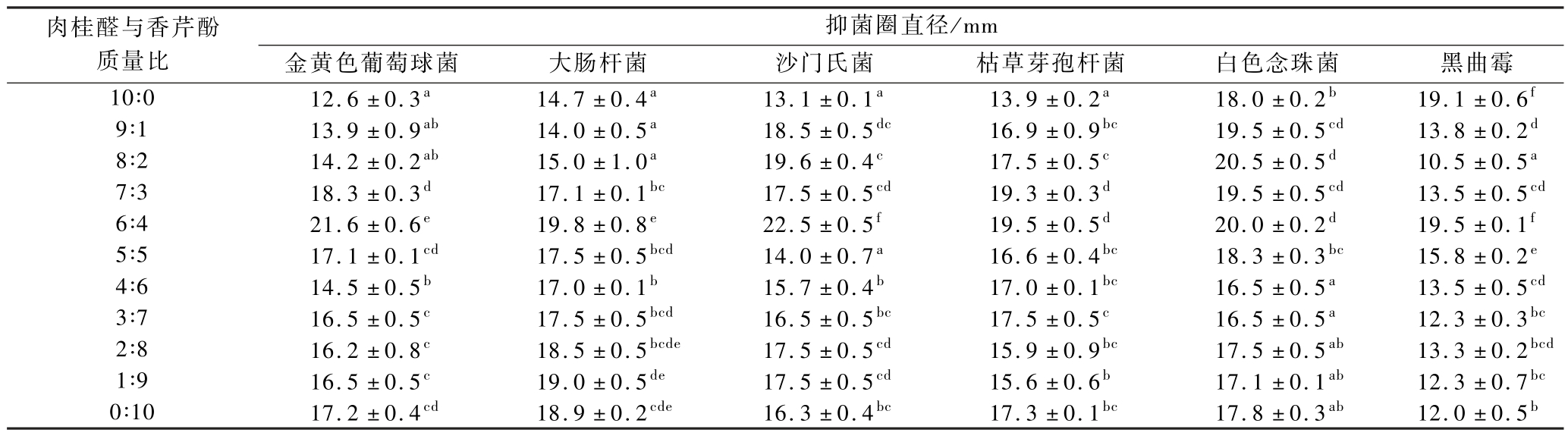
注:表中不同字母代表同一列数据之间具有显著性差异(P <0.05)。
2.2 植物精油包合物的结构表征
了解包合物的结构有助于建立酶法体系包合物的模型,从而探索更深层应用价值,也为后续酶法体系包合更多其他功能性客体分子打好理论基础。因此测定了包合物的形貌结构和包合稳定常数,并通过核磁共振解析等手段,对包合物的结构进行表征。
2.2.1 包合物的微观形态
采用扫描电镜对植物精油包合物进行微观形态观察,结果如图1-a所示。球形颗粒表面有明显的内陷,没有破裂,说明壁材完整性较好,既保护芯材,又降低壁材对氧气和水蒸气的渗透性[22]。表面的凹陷是由快速干燥和冷却过程中的收缩引起,是喷雾干燥制备的粉末的典型特征[23-24]。不均匀的表面结构增加了表面积,可以捕捉到更多的芯材。在图1-b中,包合物的粒径主要在1~10 μm,大小颗粒分布均匀。本实验制备的酶法包合物相比于与传统纯环糊精包合物有更高的芯材载量。这是因为对于纯环糊精包合物,其晶体结构多平整光滑,颗粒表面积较小,封装能力有限;且没有多种环糊精协同包合,仅仅依靠环糊精的疏水空腔,精油芯材多在颗粒内部,包不住未完全进入空腔的游离精油,导致载量偏低。而酶法生产环糊精体系由于较高的表面积和剩余底料的存在,实现了载量的提升。
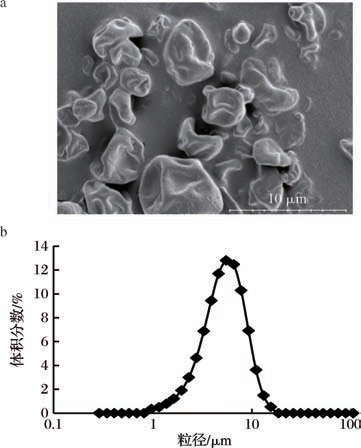
图1 植物精油包合物的扫描电镜图像及粒径分布
Fig.1 Scanning electron microscope images and particle size distribution of essential oil microcapsules
a-扫描电镜图像;b-粒径分布
2.2.2 包合稳定常数分析
包合稳定常数反映了主客体形成复合物的能力[25],已有研究通过竞争紫外-可见光谱法测定3种环糊精的香芹酚包合物稳定常数[15],采用同种方法测定3种环糊精的肉桂醛包合物稳定常数,结果如表3所示。
表3 香芹酚和肉桂醛与3种类型环糊精的包合稳定常数(25 ℃)
Table 3 Inclusion stability constants of the carvacrol,cinnamaldehyde,and three cyclodextrins (25 ℃)

注:表中大写字母表示不同精油具有显著性差异(P <0.05);小写字母表示不同环糊精具有显著性差异(P <0.05)。
由表3可以看出香芹酚、肉桂醛与β-环糊精的包合稳定常数均最大,与α-环糊精包合稳定常数均最小,表明2种精油与β-环糊精的包合作用均为最强,与α-环糊精的包合作用均为最弱。苯酚更容易被β-环糊精识别,主要受环糊精空腔与芯材化学结构的匹配控制。芯壁材的紧密空间互补对于形成稳定的包容综合体非常重要。接下来,利用核磁共振和分子模拟对这3种包合物的结构进行了探讨。
2.2.3 核磁共振(nuclear magnetic resonance,NMR)构象解析
2.2.3.1 1H核磁共振解析
已有研究对香芹酚、α-环糊精、β-环糊精、γ-环糊精以及与3种环糊精以1∶1、2∶1摩尔比的包合物进行核磁共振分析。结果表明,香芹酚和环糊精的作用具有一定的方向性,虽能与3种环糊精都发生包合,但与β-环糊精的包合能力最强。
对肉桂醛、α-环糊精、β-环糊精、γ-环糊精以及2种精油与3种环糊精以1∶1、2∶1摩尔比的包合物进行核磁共振分析。图2显示了环糊精、肉桂醛分子的分子结构和原子标记,图3为肉桂醛分别与环糊精包合的1H NMR谱图,包合前后主客体质子化学位移的变化情况,以及由特征峰面积计算出的实际络合化学计量比整理在表4、表5和表6中。
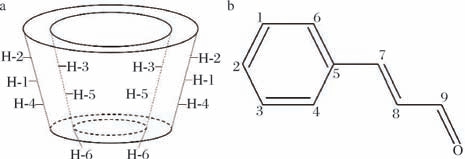
图2 主客体分子的原子标记
Fig.2 Proton labeling of host and guest molecules
a-环糊精;b-肉桂醛
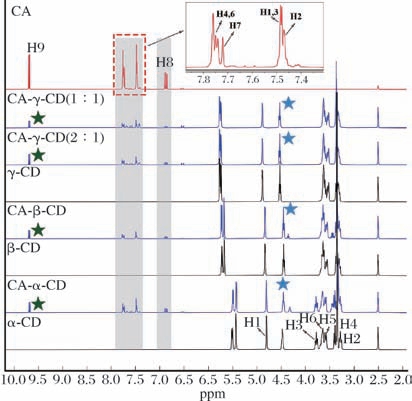
图3 室温下DMSO-d6中纯肉桂醛、纯环糊精和包合物的1 H NMR谱图
Fig.3 1 H NMR spectra of cinnamaldehyde,cyclodextrin,and their inclusion complex in DMSO-d6 at room temperature
表4 室温下游离和与肉桂醛络合的环糊精在DMSO-d6中的1 H-NMR化学位移
Table 4 1 H-NMR chemical shifts of free and complexed cyclodextrins in DMSO-d6 at room temperature
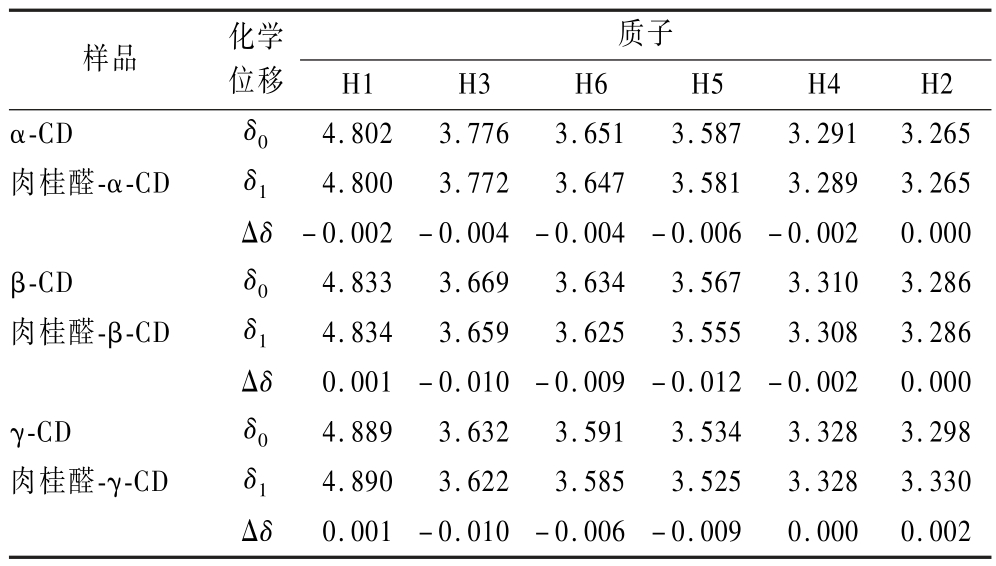
表5 室温下游离和络合的肉桂醛在DMSO-d6中的1 H-NMR化学位移
Table 5 1 H-NMR chemical shifts of free and complexed cinnamaldehyde in DMSO-d6 at room temperature
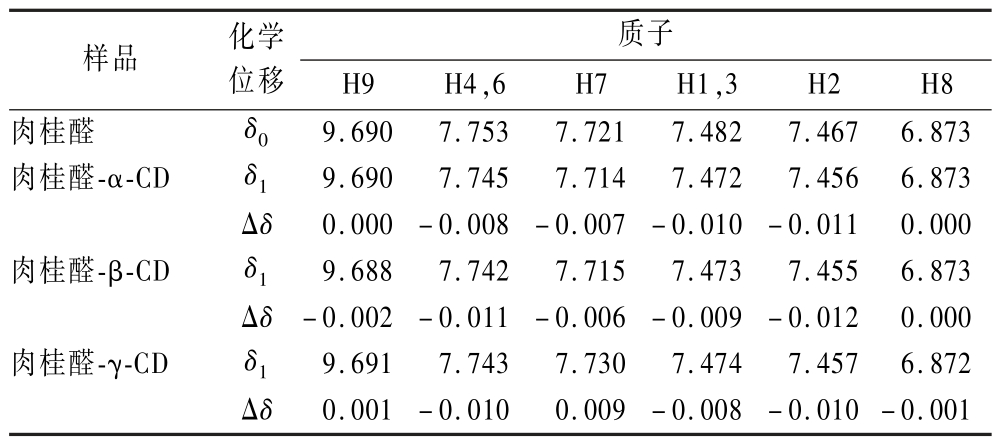
表6 肉桂醛客体特征峰面积(9.7 ppm)与环糊精主体特征峰面积(4.5 ppm)比值
Table 6 The ratio of cinnamaldehyde characteristic peak area (9.7 ppm) to that of cyclodextrin (4.5 ppm)
注:环糊精峰面积为校正重复葡萄糖数目之后的峰面积。
由表4可看出,α-环糊精、β-环糊精和γ-环糊精在和肉桂醛包合后,主要的H3、H5、H6质子发生了明显的前场位移变化趋势。质子H3和H5位于环糊精的疏水空腔中,其位移变化表明精油在一定程度上进入了空腔;质子H6位于环糊精外部的窄口端,可以确定H6的化学位移是由于精油深嵌空腔造成。相同质子比较说明,尽管肉桂醛能与3种环糊精都发生包合,但与β-环糊精的包合能力最强,这与β-环糊精空腔尺寸同香芹酚最适配有关,小空腔的α-环糊精最不利于包合肉桂醛。
由表5可看出,肉桂醛苯环上的H1,3、H2、H4,6质子发生了较大位移变化,表明肉桂醛由苯环进入环糊精空腔,苯环上连接的丙烯醛则朝向外部。相同质子的位移变化量相差较小,质子H2在肉桂醛-α-环糊精、肉桂醛-β-环糊精和肉桂醛-γ-环糊精中的Δδ 分别为-0.011、-0.012、-0.010,说明苯环上丙烯醛对位的H原子均受到程度相似的环电流屏蔽作用;再比较接近丙烯醛的质子H4,6的位移变化值,得出β-环糊精与肉桂醛包合更紧密,α-CD的包合能力依然最弱,同表5结果一致。
根据单体特征峰的峰面积比值,可以计算出包合物实际的包合摩尔比,结果列于表6。由表6可看出,β-环糊精能够以1 ∶1的摩尔比与肉桂醛进行包合,而α-环糊精因空腔较小,故无法容纳整个肉桂醛分子,γ-环糊精的空腔尺寸较大,甚至可以与肉桂醛以接近2∶1摩尔比发生包合。
2.2.3.2 二维旋转坐标核欧佛豪瑟效应频谱(2D rotating-frame overhauser effect spectroscopy,2D ROESY)
为了进一步确定精油分子与环糊精包合物的相互作用,采用二维核磁ROESY (2D ROESY)技术进行研究,其图谱上的交叉峰表示原子核在空间上的距离关系,从而推断分子的空间结构。若相应的2个氢原子距离小于4 Å,即可获得相应的核欧沃豪瑟效应交叉峰[26]。肉桂醛与3种环糊精包合物的ROESY谱图,如图4所示。其中肉桂醛-β-环糊精体系,肉桂醛的H1,3、H2、H4,6和H7质子与β-环糊精的H3、H5质子存在交叉峰关联,说明肉桂醛的苯基完全进入β-环糊精空腔,但H8质子没有出现交叉峰,表明“尾巴”丙烯醛基未被包合。而肉桂醛-α-环糊精体系中只观察到微弱的交叉峰,表明α-环糊精不能完整包合肉桂醛。对于肉桂醛-γ-环糊精,观察到肉桂醛的H1,3、H2、H4,6质子与γ-环糊精的H2、H3、H4和H5质子之间的交叉峰关联,说明肉桂醛分子也与γ-环糊精发生了包合作用。该结果验证了1 H NMR的结果,已有研究的香芹酚与肉桂醛结果类似,具有相似的络合能力,与β-环糊精的包合作用强于α-环糊精和γ-环糊精。
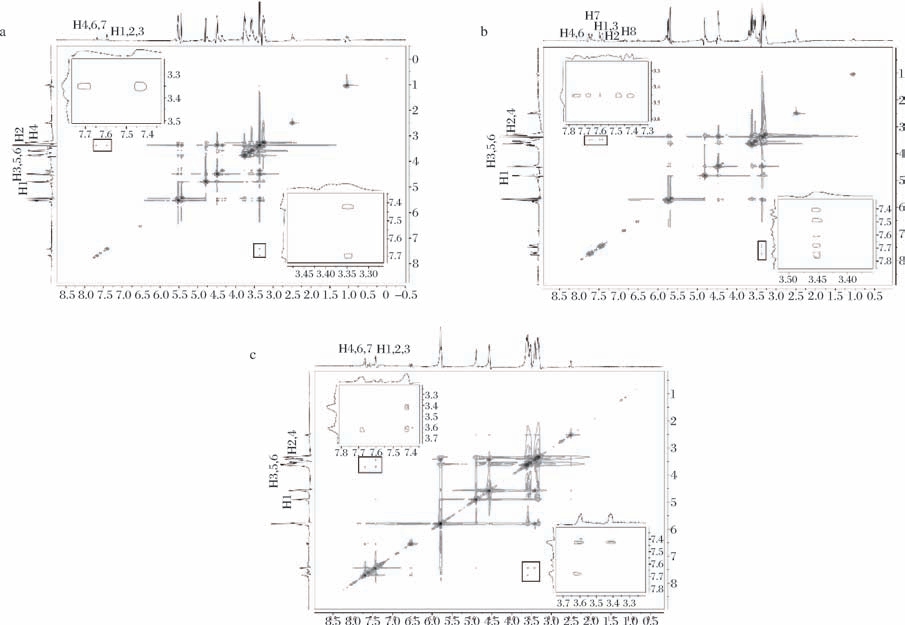
图4 肉桂醛与α-、β-、γ-环糊精包合物的2D ROESY NMR谱图
Fig.4 2D ROESY spectra of cinnamaldehyde with α-,β-,and γ-CD inclusion
a-肉桂醛与α-环糊精包合物;b-肉桂醛与β-环糊精包合物;c-肉桂醛与γ-环糊精包合物
精油分子与不同环糊精的包合模式主要与疏水作用力和分子大小有关。由于香芹酚和肉桂醛分子都含有疏水性芳香环,能够与环糊精的疏水空腔有明显的相互作用;但是,由于环糊精空腔大小不同造成与精油分子出现不同的空间匹配效应,最终产生多种包合构象协同作用的模式。
2.3 植物精油包合体系的结构模型建立
结合上节对包合物形貌和结构的分析,推测出8种包合构象,如图5所示,这些不同构象的包合物共同存在于水包油型乳液中,借助喷雾干燥技术形成稳定的包合物粉末。
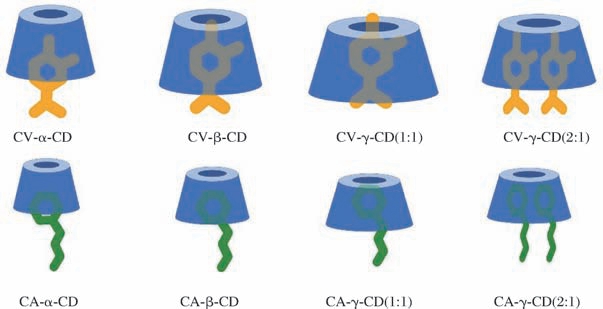
图5 香芹酚、肉桂醛与α-,β-,γ-环糊精包合模型图
Fig.5 The structural representation of the inclusion of carvacrol,cinnamaldehyde with α-,β-,and γ-CD
通过包合模型的建立,可以推测结构与应用性能的关系。3种环糊精的协同包合作用可以充分包合精油分子,同时剩余底料又对精油进行了二次包埋,模型如图6所示,该包合结构可以极大程度避免精油与外界环境的直接接触,这在对精油缓释性能和保藏性能要求较高的领域有着很大的优势。例如在防腐保鲜领域,往往需要精油稳定长效地发挥抑菌作用[27],因此在下一节的研究中,将探讨包合物的抑菌特性,说明包合物缓释作用对抑菌特性的影响。
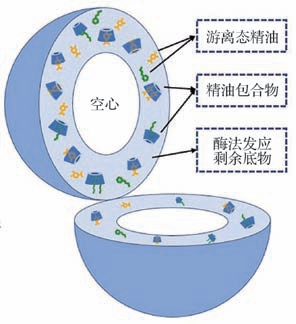
图6 酶法生产环糊精体系包合复配精油的包合模型图
Fig.6 The structural representation of essential oil microcapsule prepared during enzymatic synthesis of cyclodextrin
2.4 包合物的直接接触抑菌活性
为比较包合前后精油直接接触抑菌性能的差异,测定了不同精油与不同精油包合物的最小抑菌浓度,结果如表7所示,单组分精油的最小抑菌浓度在包合前后发生一定变化,这说明包合对单组分精油的抑菌性具有一定的影响,香芹酚包合后增强了对真菌黑曲霉的抑菌特性,对革兰氏阴性菌大肠杆菌和沙门氏菌的抑制性能降低;肉桂醛包合后减弱了对大肠杆菌的抑菌特性。对于复配精油,其包合物对金黄色葡萄球菌、大肠杆菌、沙门氏菌和枯草芽孢杆菌4种细菌的最小抑菌浓度变大,对白色念珠菌和黑曲霉这2种真菌的最小抑菌浓度变小,与单组分精油包合后的变化趋势相同且更为明显,说明酶法体系包合可增强精油对真菌的抑菌特性,对细菌的抑菌特性增强并不明显。其原因可能是精油经包合后释放速率明显降低,细菌的繁殖速度较快,因此包合后精油释放速率的显著降低会导致同浓度条件下的抑菌效力减弱;而真菌繁殖较慢,包合物的抑菌效果增强。
表7 精油与包合物对供试菌的最小抑菌浓度
Table 7 Minimal inhibit concentration of essential oil and microcapsules to different bacteria
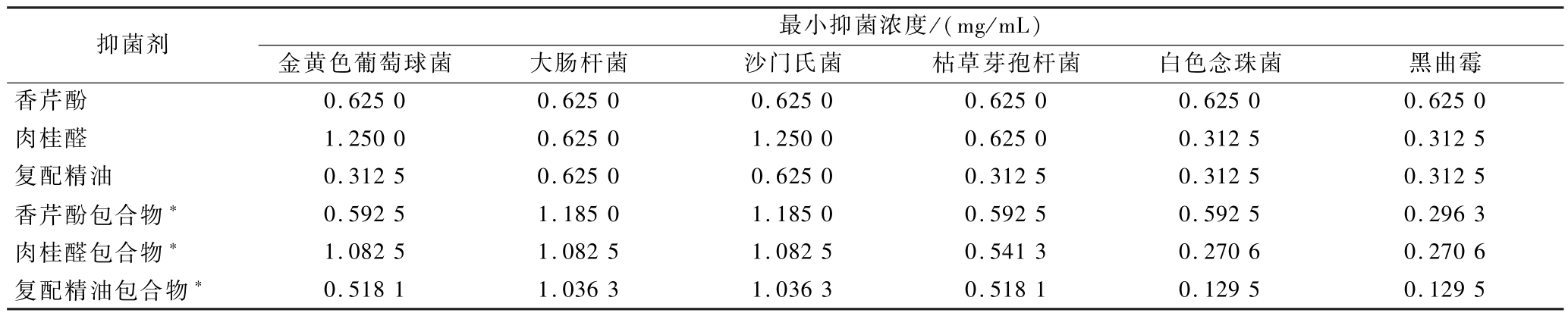
注:∗表示最小抑菌浓度换算为包合物中精油浓度。
2.5 包合物的熏蒸最小抑菌浓度
为研究包合对植物精油熏蒸时的抑菌性能,测定了酶法生产环糊精体系制备的精油包合物对黑曲霉的熏蒸最小抑菌浓度。如表8所示,单组份精油和复配精油的熏蒸最小抑菌浓度经包合后均增大,这是由于精油被包合后的释放速率降低,在黑曲霉菌生长的初期不能够释放足够的精油来抑制生长,在一定程度上减弱了其熏蒸抑菌性能。之后将通过测定包合物挥发曲线来判断精油包合物中精油的扩散机制,研究缓释作用对精油包合物熏蒸抑菌性能的影响。
表8 精油与包合物的熏蒸最小抑菌浓度
Table 8 Fumigation minimum inhibitory concentration of essential oil and microcapsules
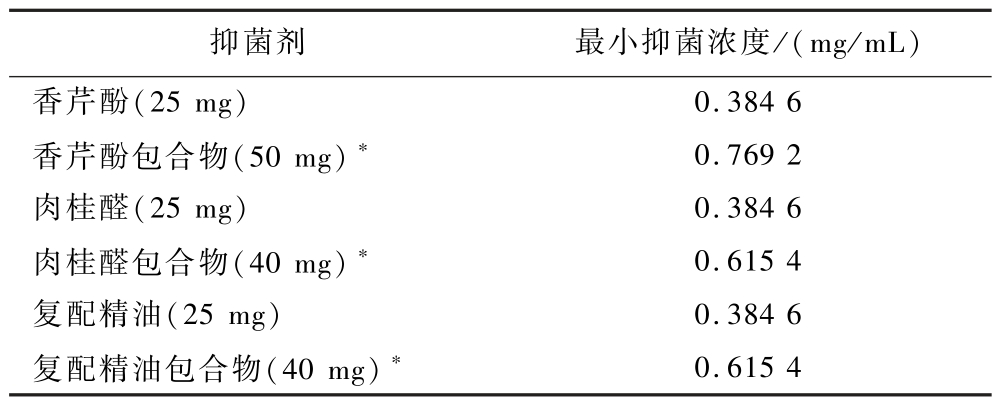
注:∗表示熏蒸最小抑菌浓度换算为包合物中精油浓度。
2.6 包合物的挥发曲线
本小节探究室温(25 ℃)条件下纯植物精油和酶法生产环糊精体系制备的精油包合物的挥发特性。如图7所示,经过30 d的暴露,单组份精油与复配精油经过包合之后的保留率都大大提升,精油的释放速率在包合后明显降低。香芹酚的保留率从27%变为81%;肉桂醛的保留率从28%变为77%;复配精油的保留率从25%变为75%。从挥发曲线还可看出,精油释放分为快速释放和缓慢释放2个阶段。快速释放是在0~8 d,8 d之后直到30 d精油的释放速度减缓,且状态越来越趋于平稳。而包合物总体释放速率较小,故两阶段变化并不明显。出现阶段性变化的原因可能是精油具有较强的挥发性,未被包合时容易与外界环境相接触从而迅速挥发;包合物中,初期释放的精油多是未被包合或未被完全包合的精油,位于包合物外表面及外层,而随着释放的持续进行,被包合的精油与壁材之间的相互作用力减缓了精油逸出的速度。
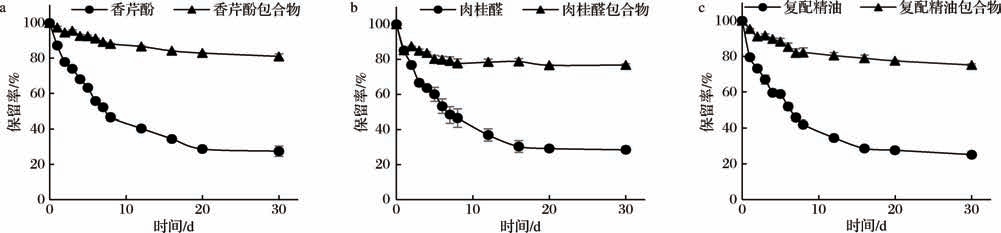
图7 香芹酚及其包合物,肉桂醛及其包合物,复配精油及其包合物在25 ℃下的释放曲线
Fig.7 Release curve of carvacrol and carvacrol microcapsules,cinnamaldehyde and cinnamaldehyde microcapsules,compound essential oils,and the microcapsules at 25 ℃
a-香芹酚及其包合物;b-肉桂醛及其包合物;c-复配精油及其包合物
2.7 缓释作用对包合物抑菌活性的影响
如表9所示,菌圈直径越小说明精油及其包合物对黑曲霉的抑制效果越好,可看出挥发8 d和16 d的实验组菌圈直径明显小于对照组,单一精油与复合精油经过包合后,缓释8 d仍能够抑制黑曲霉的生长,相比于游离精油能明显延长熏蒸抑菌至少4 d,说明包合的缓释作用显著延长抑菌时间,提高精油的抑菌性能。对于不同精油,香芹酚暴露8 d的菌圈直径显著大于肉桂醛和复配精油,说明香芹酚的抑菌性能弱于肉桂醛及复配精油,这与熏蒸最小抑菌浓度的结果一致;但暴露16 d的菌圈直径,3种精油无显著差异,可能是因为精油挥发太久,剩余量相似,能发挥的抑菌作用相似。不同精油包合物(25 mg)暴露16 d的菌圈直径无明显差异,说明包合物中精油的挥发速度相似。由图8可看出,含有熏蒸最小抑菌浓度含量的包合物暴露32 d,依然能够完全抑制黑曲霉的生长,与含有相同精油量(25 mg)的包合物相比,熏蒸抑菌性能明显增强,表明包合物的缓释特性显著提高了植物精油的熏蒸抑菌特性,延长有效抑菌的时间。
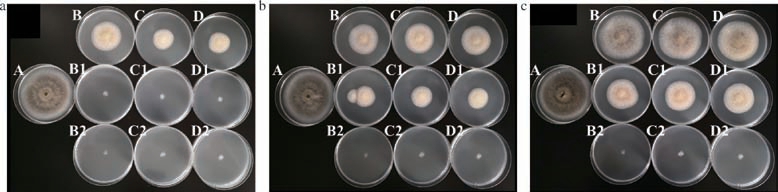
图8 释放8、16、32 d的植物精油与包合物对黑曲霉菌圈生长情况影响
Fig.8 Effects of essential oils and inclusion compounds released at 8,16,and 32 d on the growth of Aspergillus niger circles
A-对照组;B-香芹酚(25 mg);B1-香芹酚包合物(25 mg);B2-香芹酚包合物(50 mg);C-肉桂醛(25 mg);C1-肉桂醛包合物(25 mg);C2-肉桂醛包合物(40 mg);D-复配精油(25 mg);D1-复配精油包合物(25 mg);D2-复配精油包合物(40 mg)。a-释放8 d;b-释放16 d;c-释放32 d
表9 缓释时间对植物精油包合物熏蒸抑菌活性的影响
Table 9 Effect of release time on the bacteriostatic properties of plant essential oil inclusion compounds in fumigation
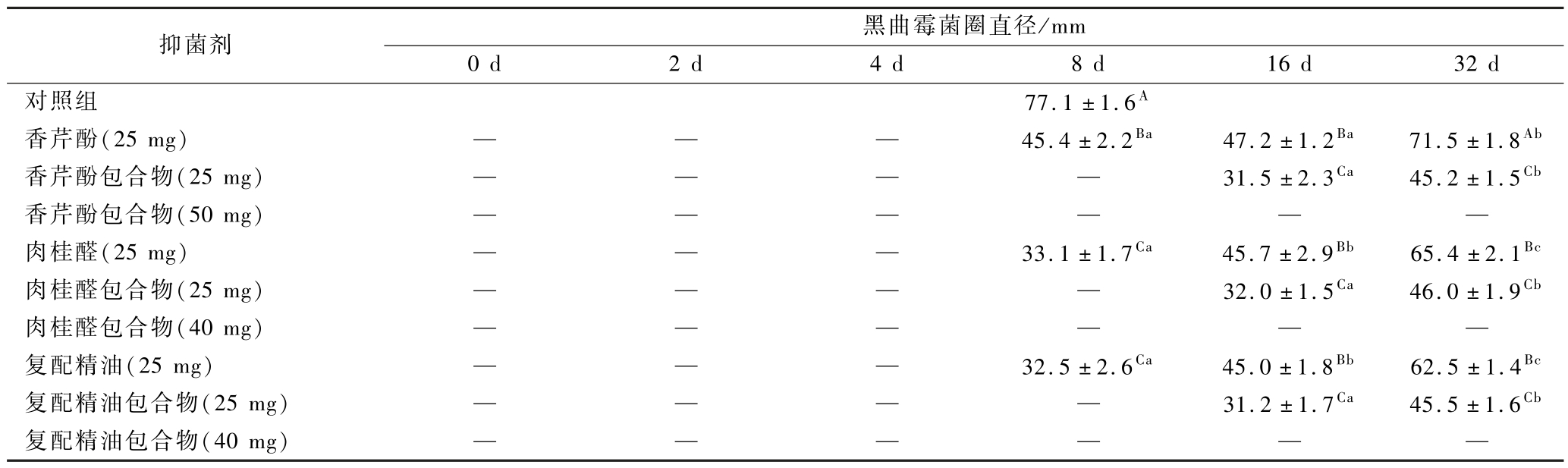
注:—表示菌圈不生长;A、B、C:各精油和精油包合物的显著性差异分析(P <0.05);a、b:同一样品不同时间的显著性差异分析(P <0.05);25 mg:精油用量和含有相同精油含量的包合物;40 mg、50 mg:含有熏蒸最小抑菌浓度精油含量的包合物。
3 结论
本研究以肉桂醛-香芹酚复合包合物为对象,通过测定包合物的微观结构和包合稳定常数,并进行核磁共振解析等手段,建立了酶法生产环糊精包合复配精油的稳定包合结构模型,后续实验证实该复合包合物对黑曲霉具有显著抑菌活性,直接接触模式下,包合物能够更好地抑制黑曲霉的生长;在熏蒸模式下,精油包合物的熏蒸最小抑菌浓度虽增大,但其缓释性能使抑菌作用时间延长至32 d以上,其阶段释放特性可同步满足快速抑菌与长效防护需求。研究结果阐明了包合结构对精油活性成分稳定化与功能增效的协同机制,为开发高效、低耗的植物源食品保鲜剂提供了理论支撑。未来研究需重点考察包合物在复杂食品体系中的释放-抑菌联合效应及其安全性评估,以推动实际应用。
[1]SCHWÄMMLE B,WINKELHAUSEN E,KUZMANOVA S,et al.Isolation of carvacrol assimilating microorganisms[J].Food Technology and Biotechnology,2001,39(4):341-345.
[2]MARINELLI L,DI STEFANO A,CACCIATORE I.Carvacrol and its derivatives as antibacterial agents[J].Phytochemistry Reviews,2018,17(4):903-921.
[3]M CZKA W,TWARDAWSKA M,GRABARCZYK M,et al.Carvacrol:A natural phenolic compound with antimicrobial properties[J].Antibiotics,2023,12(5):824.
CZKA W,TWARDAWSKA M,GRABARCZYK M,et al.Carvacrol:A natural phenolic compound with antimicrobial properties[J].Antibiotics,2023,12(5):824.
[4]ZHANG G Y,LI T L,LIU J,et al.Cinnamaldehyde-contained polymers and their biomedical applications[J].Polymers,2023,15(6):1517.
[5]黄玉华,张猛猛,辛璇,等.肉桂精油提取及其生物活性与作用机制研究进展[J].食品工业科技,2025,46(17):468-479.HUANG Y H,ZHANG M M,XIN X,et al.Research progress on extraction,bioactivity,and mechanism of action of cinnamon essential oil[J].Science and Technology of Food Industry,2025,46(17):468-479.
[6]牛力源,孙晓诚,刘静飞,等.香芹酚胁迫下酿酒酵母的生理特性和转录组分析[J].食品科学,2024,45(9):75-83.NIU L Y,SUN X C,LIU J F,et al.Physiological characteristics and transcriptomic analysis of Saccharomyces cerevisiae under carvacrol stress[J].Food Science,2024,45(9):75-83.
[7]黄露露,侯天玉,张欣雨,等.4-甲氧基肉桂醛对柑橘果实采后青霉病抗性的影响[J].食品科学,2025,46(8):302-310.HUANG L L,HOU T Y,ZHANG X Y,et al.Effect of 4-methoxy cinnamaldehyde on postharvest resistance to blue mold in Citrus fruit[J].Food Science,2025,46(8):302-310.
[8]蒋帅.肉桂精油对苹果灰霉病防治效果的影响[D].杨凌:西北农林科技大学2017.JIANG S.The influence of control effect on apple gray mold of cinnamon essential oil[D].Yangling:Northwest A&F University,2017.
[9]ERTAN K,CELEBIOGLU A,CHOWDHURY R,et al.Carvacrol/cyclodextrin inclusion complex loaded gelatin/pullulan nanofibers for active food packaging applications[J].Food Hydrocolloids,2023,142:108864.
[10]李森,马灵,李婷,等.含硅藻土负载香芹酚复合体的明胶基缓释抗菌膜的制备与性能[J].食品科学,2023,44(21):204-212.LI S,MA L,LI T,et al.Preparation and characterization of gelatin-based antibacterial film incorporating diatomite/carvacrol complex[J].Food Science,2023,44(21):204-212.
[11]PANT K,BHATTACHARYA B.Efficacy of cyclodextrin nanosponges in protecting the bioactivity of cinnamon bark extract and trans-cinnamaldehyde[J].Food Bioscience,2024,62:105187.
[12]MARTIN DEL VALLE E M.Cyclodextrins and their uses:A review[J].Process Biochemistry,2004,39(9):1033-1046.
[13]柏玉香,吴浩.γ-环糊精工业化生产的研究进展[J].食品与发酵工业,2021,47(22):279-287.BAI Y X,WU H.Research progress in industrial production of γcyclodextrin[J].Food and Fermentation Industries,2021,47(22):279-287.
[14]LI C M,XU Q,GU Z B,et al.Cyclodextrin glycosyltransferase variants experience different modes of product inhibition[J].Journal of Molecular Catalysis B:Enzymatic,2016,133:203-210.
[15]LIU T H,FENG C Q,LI Z F,et al.Efficient formation of carvacrol inclusion complexes during β-cyclodextrin glycosyltransferasecatalyzed cyclodextrin synthesis[J].Food Control,2021,130:108296.
[16]魏伟,吴希美,李元建.药理实验方法学[M].药理实验方法学,2010.WEI W,WU X M,LI Y J.Pharmacological Experimental Methodology[M].Pharmacological Experimental Methodology,2010.
[17]CHEN S D,LI Z F,GU Z B,et al.A new micro-agar dilution method to determine the minimum inhibitory concentration of essential oils against microorganisms [ J].Journal of Microbiological Methods,2023,211:106791.
[18]卢滋,李兆丰,顾正彪,等.竞争紫外-可见光谱法研究β-环糊精与链状饱和一元醇的包合作用[J].分析科学学报,2013,29(2):201-205.LU Z,LI Z F,GU Z B,et al.Competitive UV-vis spectrophotometric studies on inclusion interaction between β-cyclodextrin and chainlike saturated monohydric alcohol[J].Journal of Analytical Science,2013,29(2):201-205.
[19]李泽西.环糊精-三丁酸甘油酯包合体系的酶法构建、表征及其包合机理研究[D].无锡:江南大学2020.LI Z X.Enzymatic preparation,characterization and inclusion mechanism of cyclodextrin-tributyrin inclusion complex[D].Wuxi:Jiangnan University,2020.
[20]FRANZBLAU S G,WITZIG R S,MCLAUGHLIN J C,et al.Rapid,low-technology MIC determination with clinical Mycobacterium tuberculosis isolates by using the microplate Alamar Blue assay[J].Journal of Clinical Microbiology,1998,36(2):362-366.
[21]KAMIMURA J A,SANTOS E H,HILL L E,et al.Antimicrobial and antioxidant activities of carvacrol microencapsulated in hydroxypropyl-beta-cyclodextrin[J].LWT-Food Science and Technology,2014,57(2):701-709.
[22]JANISZEWSKA-TURAK E,B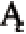 K P,KRZYKOWSKI A,et al.The influence of the carrier addition and spray drying temperatures on physicochemical properties of microencapsulated carrot juice powder[J].International Journal of Food Science &Technology,2021,56(6):2768-2779.
K P,KRZYKOWSKI A,et al.The influence of the carrier addition and spray drying temperatures on physicochemical properties of microencapsulated carrot juice powder[J].International Journal of Food Science &Technology,2021,56(6):2768-2779.
[23]JAFARI S M,ASSADPOOR E,HE Y H,et al.Encapsulation efficiency of food flavours and oils during spray drying[J].Drying Technology,2008,26(7):816-835.
[24]ALVARENGA BOTREL D,VILELA BORGES S,VICTÓRIA DE BARROS FERNANDES R,et al.Evaluation of spray drying conditions on properties of microencapsulated oregano essential oil[J].International Journal of Food Science &Technology,2012,47(11):2289-2296.
[25]邓颖慧,张东京,王海琨,等.阳离子型环糊精对甘草素的超分子包合行为及增溶作用[J].分析化学,2025,53(2):289-310.DENG Y H,ZHANG D J,WANG H K,et al.Supramolecular binding behavior and solubilization of cationic cyclodextrins towards liquiritigenin[J].Chinese Journal of Analytical Chemistry,2025,53(2):289-310.
[26]DODZIUK H,KOZ'MIN'SKI W,EJCHART A.NMR studies of chiral recognition by cyclodextrins[J].Chirality,2004,16(2):90-105.
[27]CHEN G,LIU B.Cellulose sulfate based film with slow-release antimicrobial properties prepared by incorporation of mustard essential oil and β-cyclodextrin[J].Food Hydrocolloids,2016,55:100-107.