榨菜是世界三大著名腌菜之一[1],涪陵是榨菜生产的发源地,目前是我国规模最大、最集中的榨菜产区,被誉为“中国搾菜之乡”。涪陵榨菜是以茎瘤芥(Brassica juncea var.tumida Tsen et Lee)为原料,经过“三腌三榨”加工工艺而腌制的一种酱腌制品[2]。榨菜在腌制过程中经过微生物发酵、蛋白质分解等一系列化学作用产生各种风味物质,赋予榨菜特有的风味和营养成分[3-5]。因此,探究涪陵榨菜腌制过程中微生物群落结构及功能,对进一步提升榨菜品质和调控发酵过程具有重要意义。
国内外关于涪陵榨菜的研究主要集中在:榨菜加工工艺研究[6-7];乳酸菌的分离鉴定及在榨菜腌制中的应用研究[8-9];加工废水的处理[9-10]等方面。而有关榨菜中微生物群落多样性的研究也有少量文献报道[4,11-14],且研究方法多采用传统的高通量测序技术,例如,ZHANG等[13]基于细菌16S rRNA和真菌ITS序列的高通量测序技术分析了榨菜腌制过程中微生物多样性,发酵30 d后,细菌属以嗜盐菌(Halomonas, Idiomarina)和乳酸菌(Lactobacillus-related, Weissella)为主,随着发酵的进行,真菌属德巴利酵母属(Debaryomyces)、梗孢酵母属(Sterigmatomyces)、锁掷酵母属(Sporidiobolus)的相对丰度增加。LI等[14]利用PacBio Sequel技术分别对细菌16S rRNA和真菌ITS基因全长进行测序,发现涪陵榨菜在4个发酵阶段中优势菌属分别为明串珠菌属(Leuconostoc)和乳杆菌属(Lactobacillus),优势真菌属分别为曲霉属(Aspergillus)、哈萨克斯坦酵母属(Kazachstania)、德巴利酵母属。值得注意的是,由于受引物的选择性和测序片段长度的限制,只能在属水平上揭示微生物的群落结构组成,无法充分揭示在种水平和功能方面的特征。而宏基因组测序技术可对样品中全部微生物基因组DNA进行提取和测序,不仅能够在种水平分析微生物菌群多样性,且能够对微生物功能进行注释分析,更全面、更系统的了解微生物群落、功能特性及相互关系[15-17]。但目前尚无基于宏基因组对涪陵榨菜发酵过程中微生物多样性的系统研究。
本研究以涪陵榨菜为原料,采用宏基因组测序技术解析不同发酵阶段涪陵榨菜微生物群落结构动态变化规律以及微生物多样性,并利用非冗余蛋白质序列(non-redundant protein sequence database,NR)、直系同源簇(cluster of orthologous groups,COG)、KEGG、碳水化合物活性酶(carbohydrate active enzyme database,CAZy)等功能数据库对微生物物种和功能基因进行注释,为涪陵榨菜工艺改进和品质提升提供理论依据,也为探讨优势菌群与涪陵榨菜风味物质的相关性研究奠定基础。
1 材料与方法
1.1 实验材料
新鲜茎瘤芥,当地农户;E.Z.N.A.® Soil DNA Kit试剂盒,美国Omega公司;NEXTFLEX® Rapid DNASeq Kit,美国Bioo Scientific公司;NovaSeq 6000 S4 Reagent Kit v1.5 (300 cycles),美国Illumina公司;DNeasy® PowerSoil® Pro Kit,德国Qiagen公司;琼脂糖,Biosharp公司;实验用水为超纯水。
1.2 仪器与设备
Eppendorf 5424 R高速台式冷冻离心机,德国Eppendorf公司;FastPrep-24 5G研磨仪,美国MP公司;Qubit 4.0荧光定量仪、NanoDrop 2000超微量分光光度计,美国Thermo Fisher Scientific公司;Novaseq6000测序仪,美国Illumina公司;Powerpac 300电泳仪、Gel Doc XR+凝胶成像仪,美国Bio-rad公司;MS105DU电子天平,瑞士Mettler Toledo公司;SW-CJ-2FD超净工作台,江苏苏净公司;优普超纯水制造系统,成都超纯科技有限公司。
1.3 实验方法
1.3.1 样品的制备与采集
将新鲜茎瘤芥进行修剪后,清洗、晾干。按三腌三榨方法进行腌制[4]:采用“一层青菜头一层盐”的方式,一腌加3%(质量分数,下同)的食用盐进行腌制,腌制5 d(简称YY);二腌加5% 的食用盐,腌制11 d(简称EY);三腌加8%的食用盐,腌制60 d(简称SY),最上层用重石压实。每个阶段腌制结束后,将榨菜块全部捞出,置于洁净的盆中进行囤压24 h,囤压结束后将盐菜块计重再入坛进行下一次腌制。腌制过程中,在3个发酵坛中分别于一腌、二腌和三腌结束后采集发酵液,样品分别命名为YY、EY、SY。为保证取样均匀,用灭菌采样器分别在容器的上、中、下3层收集50 mL发酵溶液。将收集的发酵液于4 ℃下5 000 × g 离心10 min,沉积物保存在液氮中备用。
1.3.2 样品基因组提取
发酵液样品中微生物宏基因组DNA提取是按照E.Z.N.A.® Soil DNA Kit试剂盒说明书操作。然后通过使用1% 的琼脂糖凝胶电泳检测抽提的基因组DNA的质量,利用超微量分光光度计分析DNA的纯度和浓度,收集OD260/280值在1.8~2.0、DNA质量浓度不低于50 ng/μL的DNA样品(电泳条带清晰,无拖尾)送上海美吉生物医药科技有限公司进行文库构建和宏基因组测序。
1.3.3 宏基因组测序及数据分析
将质量检测合格的DNA按照NEXTFLEX Rapid DNA-Seq Kit试剂盒说明书进行文库构建,构建的文库使用Qubit3.0仪器进行片段检测和定量检测,然后使用Illumina novasq6000测序平台进行宏基因组测序。使用Fastp软件删除原始数据中长度≤50 bp、平均碱基质量值<20 bp且含N碱基的reads,得到高质量的有效序列(clean reads)。使用MegaHit软件对clean reads进行拼接组装,筛选长度≥300 bp的重叠群(contigs)构建序列集。然后采用Prodigal软件对contigs进行开放阅读框(open reading frame,ORFs)预测,并过滤除去预测结果中长度<100 bp的信息。预测的基因序列采用CD-HIT软件对其进行聚类(90% identity,90% coverage)分析,构建非冗余基因集。使用SOAPaligner软件将各样品中的高质量clean reads与非冗余基因集进行比对(95% identity),并统计各样品中基因的丰度。对预测出的基因进行物种和功能注释,主要注释数据库包括NR、COG、KEGG和CAZy,并对注释结果进行功能归类和差异分析。
1.4 数据处理
实验数据使用Excel 2010软件进行统计,使用Origin 7.5和R软件完成统计分析和作图,数据结果采用“平均值± 标准差”方式表示。NR、COG、KEGG和CAZy分析均采用Kruskal-Wallis秩和检验方法。
2 结果与分析
2.1 基因测序与组装质量分析
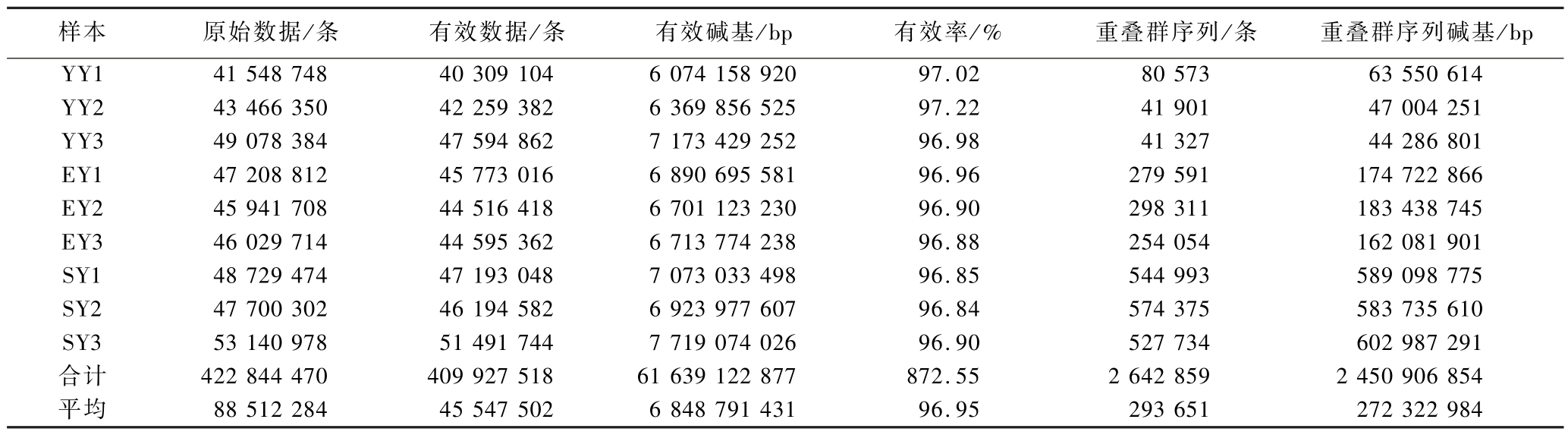
表1显示,从9个样本组中共得到422 844 470条原始序列(raw reads),经过质控后得到高质量的clean reads 409 927 518条,有效序列的总长度为61 639 122 877 bp,有效率(clean reads占raw reads的百分比)平均值为96.95%,对优化后序列拼接组装后,共获得2 642 859条重叠群序列(contigs)。以上数据说明基因组测序结果较好,基因组装具有较高的完整性,可用于进行后续分析。
表1 样本测序信息
Table 1 Sequencing information of the samples
2.2 基因集构建与分析
对总 contigs进行开放阅读框预测,共获得2 652 873个ORFs,均长429.82 bp。基于ORF的预测基因进一步聚类,构建非冗余基因集,非冗余基因集共有687 594个基因,非冗余基因集基因的平均序列长度为416.15 bp。非冗余基因集长度分布如图1所示,测序样本基因片段长度主要集中在0~600 nt,短片段长度基因占据大多数。
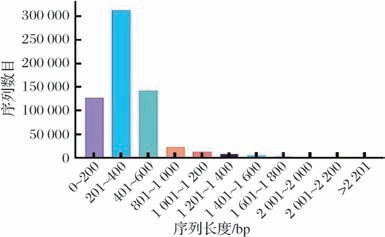
图1 榨菜发酵液样本基因长度分布图
Fig.1 Gene length of brine soup samples of Zhacai
2.3 榨菜不同发酵阶段微生物群多样性分析
2.3.1 Alpha多样性分析
Alpha多样性可以反映样品间的物种多样性与物种丰富度之间的差别,Chao指数表示群落丰富度,Shannon和Simpson指数表示微生物群落多样性。不同发酵阶段榨菜样品α-多样性指数如表2和图2所示,随着发酵时间的延长,Chao指数和Simpson指数均呈先升后降的变化趋势,且都在二腌阶段达到最大,说明榨菜发酵过程中微生物群落的丰富度和多样性不断变化,呈现先增加后下降趋势。这种现象可能与榨菜发酵环境有关,随着发酵时间的延长,发酵液酸度逐渐升高,这种酸性环境可以抑制不耐受低pH值的微生物的生长繁殖,这可能是影响微生物群落多样性的主要因素[11]。
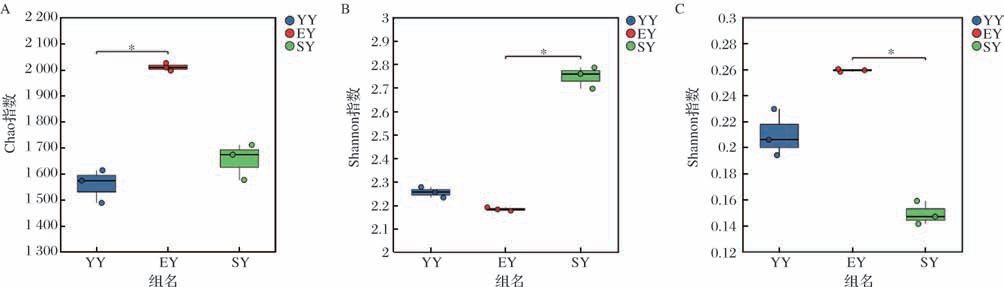
图2 榨菜不同发酵阶段微生物α-多样性指数的箱型图
Fig.2 Box plots of α-diversity indexes at different fermentation stages of Zhacai
注:∗表示差异显著(P <0.05)。
A-Chao指数;B-属Shannon指数;C-Simpson指数
表2 榨菜不同发酵阶段微生物多样性指数分析
Table 2 Microbial diversity index at different fermentation stages of Zhacai
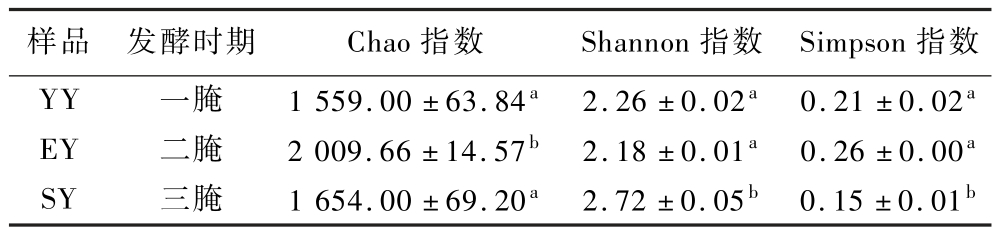
注:同列中不同小写字母表示差异显著(P <0.05)。
2.3.2 微生物群落主坐标分析
对不同腌制阶段的微生物群落多样性进行即主坐标分析(principal co-ordinates analysis,PCoA)。结果表明,在门水平上(图3-A),PCoA的第一主坐标和第二主坐标的贡献率分别为99.25%和0.49%,2个主成分共解释了99.74%的变量。在属水平上(图3-B),第一主坐标(PC1)和第二主坐标(PC2)的贡献率分别为95.41%和3.81%,2个主成分共解释了99.22%的变量。在种水平上(图3-C),第一主坐标(PC1)和第二主坐标(PC2)的贡献率分别为94.53%和4.01%,2个主成分共解释了98.52%的变量。在门、属、种的水平上,YY、EY、SY组均分散在不同的象限,不同发酵阶段样品组均能较好的区分,表明不同发酵阶段的微生物群落结构差异较大,呈现出明显的时间异质性。
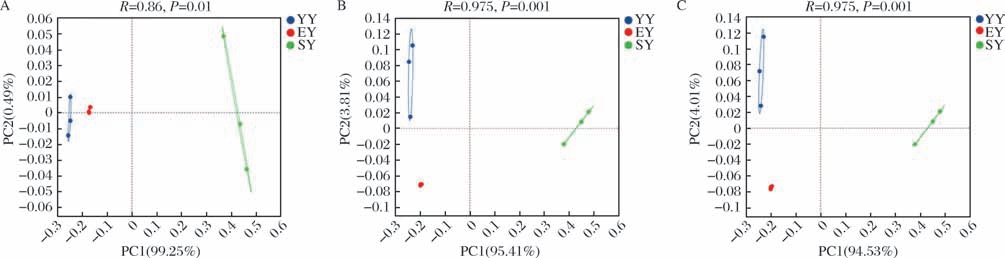
图3 榨菜不同发酵阶段微生物群落PCoA分布图
Fig.3 PCoA analysis of microbial communities at different fermentation stages of Zhacai
A-门水平;B-属水平;C-种水平
2.3.3 微生物群落主坐标分析
通过Venn图统计分析不同样本所共有和独有的物种数目,结果如图4所示。在门水平上(图4-A),YY、EY、SY组独有物种数分别为0、0、3个,YY和EY组共有物种1个,YY和SY组共有物种0个,EY和SY组共有物种4个,3组样品共有物种43个。在属水平上(图4-B),YY、EY、SY组独有物种数分别为20、24、59个,YY和EY组共有物种55个,YY和SY组共有物种5个,EY和SY组共有物种81个,3组样品共有物种485个。在种水平上(图4-C),YY、EY、SY组独有物种数分别为72、135和120个,YY和EY组共有物种235个,YY和SY组共有物种17个,EY和SY组共有物种231个,3组样品共有物种1 687个。以上结果表明,发酵中后期共有物种数逐渐增加,这可能是后期发酵环境已趋于稳定,微生物已经形成稳定的群落结构。
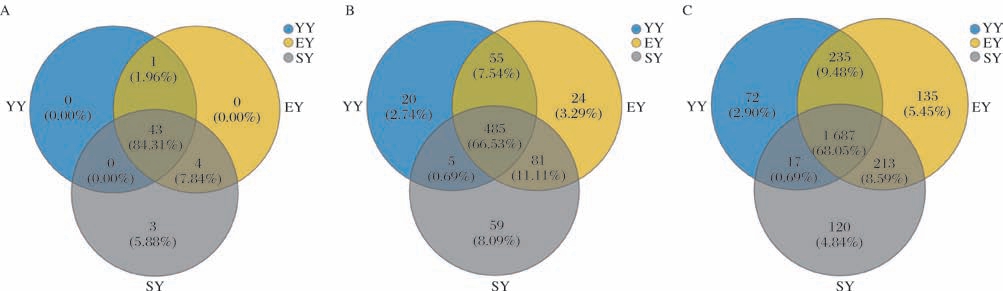
图4 榨菜不同发酵阶段微生物群落Venn分布图
Fig.4 Venn analysis of microbial communities at different fermentation stages of Zhacai
A-门水平;B-属水平;C-种水平
2.3.4 微生物群落组成分析
对榨菜不同腌制阶段微生物分类进行分析,9份样品共注释到52门、1 024属和2 943种,选择丰度前20个物种做堆积图分析物种组成,结果如图5所示。在门水上(图5-A),厚壁菌门(Firmicutes)在整个在发酵过程中一直处为绝对优势菌门,在三腌阶段其相对丰度降低至69.27%;而变形菌门(Proteobacteria)的丰度随着发酵时间的延长而增加,相对丰度从5.02%增长至24.94%。上述结果表明,变形菌门和厚壁菌门主导着涪陵榨菜的发酵,这种变化趋势与刘大群等[18]研究结果基本一致,只是相对丰度值有所不同,这可能腌制工艺、盐浓度和腌制环境不同所导致的。在属水平上(图5-B),布氏乳杆菌属(Latilactobacillus)和明串珠菌属2种乳酸菌属在3个发酵阶段均为优势菌属,随着发酵时间的延迟,布氏乳杆菌属相对丰度先增长后下降,相对丰度由39.92%增长至50.14%,第三阶段降到33.43%;而明串珠菌属相对丰度逐渐下降,由50.35% 降到29.91%,这与LIANG等[19]的研结果一致。另外,肠球菌属(Enterobacter)相对丰度由0.65%增加到15.17%。在种水平上(图5-C),3个腌制阶段的明显优势种均为清酒广布乳杆菌(Latilactobacillus sakei),其次是未分类明串珠菌属(unclassified_g_Leuconostoc)、肠膜明串珠菌(Leuconostoc mesenteroides)、肉色明串珠菌(Leuconostoc carnosum)、弯曲广布乳杆菌(Latilactobacillus curvatus),在三腌阶段,霍氏肠杆菌(Enterobacter hormaechei)的丰度由0.09%增加至15.13%。
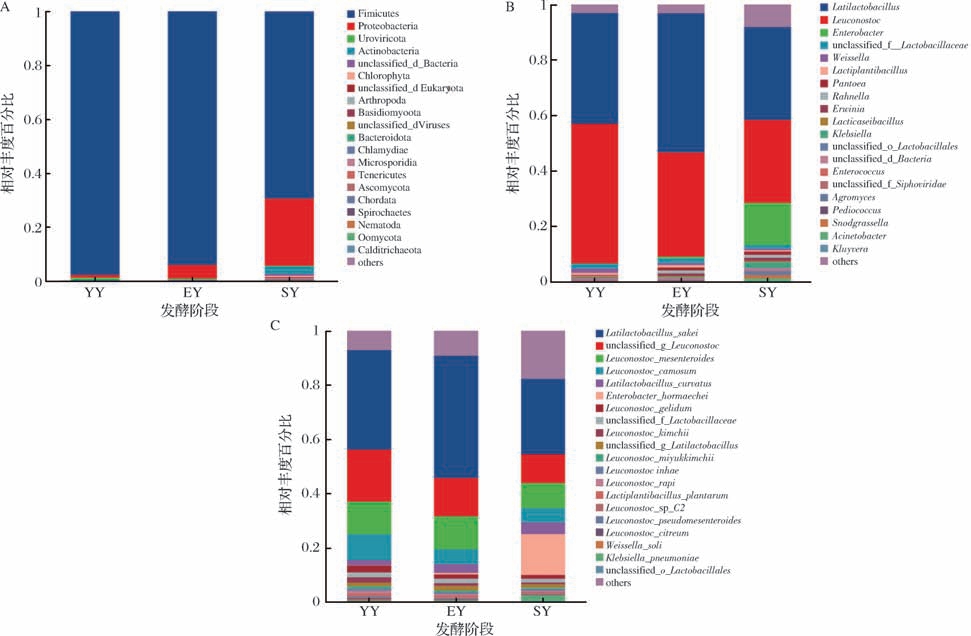
图5 榨菜不同发酵阶段微生物群落组成
Fig.5 Microbial communities at different fermentation stages of Zhacai
A-门水平;B-属水平;C-种水平
上述结果表明,乳杆菌属和明串珠菌属主导涪陵榨菜发酵,这与以往的报道结果非常相似[11-12,19-20],且不同种乳杆菌和明串珠菌的交替变化共同促进涪陵榨菜的发酵。在蔬菜发酵初期和中期阶段起主要作用的是乳酸菌,包括肠膜明串珠菌、短乳杆菌、粪链球菌等,其中肠膜明串珠菌起着重要作用。肠膜明串珠菌属于异型乳酸发酵微生物,可发酵葡萄糖等单糖和双糖,产生二氧化碳、乳酸、乙酸和乙醇,使发酵环境pH下降,从而抑制有害微生物生长。随着乳酸的积累,异型乳酸菌的活动受到抑制,其他乳酸菌按照一定顺序生长繁殖,进入主发酵阶段[21]。另外,乳酸发酵产生的醇和酸发生酯化反应形成不同的酯,增加榨菜的香气。在腌制后期,可发酵性碳水化合物被全部利用,因发酵液pH值降低,乳酸菌的生长繁殖受到抑制,这与本研究中乳杆菌属相对丰度先增长后下降现象一致。
有研究报道称肠杆菌属可以利用糖酵解和戊糖磷酸途径对糖进行分解,进而代谢产生乳酸、乙醇、短链脂肪酸等物质[22],这是榨菜腌制品产生特殊风味的主要途径之一。另外,青菜头内含有特殊的芥子硫苷,压榨使细胞内的芥子酶释放,水解芥子苷,生成具有特殊芳香和特殊刺激味的,这是榨菜产生辛辣味的原因之一。
2.4 物种与功能注释
2.4.1 NR物种注释
对所得序列进行物种分类学注释,通过与NR数据库进行比对,共鉴定出52门、110纲、250目、455科、1 024属和2 943种的微生物。NR注释结果表明,在域水平上,细菌的相对丰度高达95.28%,真菌占4.13%,病毒占0.58%,古细菌仅0.001%。
2.4.2 COG功能注释及差异分析
将9个榨菜发酵液样本DNA测序数据与COG数据库进行比对,共有94 293个基因被注释到25种不同功能单元,其中参与碳水化合物转运与代谢的基因数最多(9 628个),7 514个基因参与氨基酸转运与代谢,7 336个基因参与细胞壁/膜/包膜生物合成,5 888个基因参与转录,5 235个基因参与复制、重组和修复,5 730个基因参与信号转导机制,5 701个基因参与翻译、核糖体结构及合成,4 717个基因参与无机离子运输与代谢,4 556个基因参与翻译后修饰、蛋白质翻转,4 271个基因参与辅酶运输和代谢,4 228个基因参与能源生产和转换(图6-A)。榨菜含有较为丰富的碳水化合物与蛋白质,在榨菜发酵过程中,这些物质也发生了代谢和转化,这是榨菜风味主要来源[23-24],因此参与碳水化合物代谢与氨基酸代谢相关基因也会比较丰富。
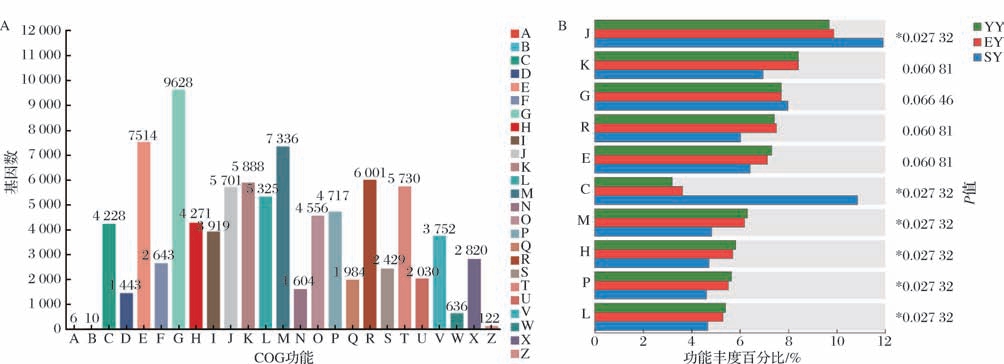
图6 COG功能注释分类图及不同组间注释基因相对丰度图
Fig.6 COG functional annotation classification statistics and relative abundance of annotation genes in different groups
注:A:RNA加工与修饰(RNA processing and modification),B:染色体结构和动力学(chromatin structure and dynamics),C:能量产生和转换(energy production and conversion),D:细胞周期调控、细胞分裂、染色体分配(cell cycle control,cell division,chromosome partitioning),E:氨基酸转运与代谢(amino acid transport and metabolism),F:核苷酸转运与代谢(nucleotide transport and metabolism),G:碳水化合物转运与代谢(carbohydrate transport and metabolism),H:辅酶转运与代谢(coenzyme transport and metabolism),I:脂质转运与代谢(lipid transport and metabolism),J:翻译、核糖体结构和生物合成(translation,ribosomal structure and biogenesis),K:转录(transcription),L:复制、重组和修复(replication,recombination and repair),M:细胞壁/膜/包膜生物合成(cell wall/membrane/envelope biogenesis),N:细胞运动(cell motility),O:翻译后修饰、蛋白质周转(posttranslational modification,protein turnover,chaperones),P:无机离子转运与代谢(inorganic ion transport and metabolism),Q:次生代谢物生物合成、运输和分解代谢(secondary metabolites biosynthesis,transport and catabolism),R:仅用于一般函数预测(general function prediction only),S:function unknown(未知功能),T:信号转导机制(signal transduction mechanisms),U:细胞内运输、分泌和囊泡运输(intracellular trafficking,secretion,and vesicular transport),V:防御机制(defense mechanisms),W:细胞外结构(extracellular structures),X:移动体:噬菌体,转座子(mobilome:prophages,transposons),Z:细胞骨架(cytoskeleton),0.01 <P≤0.05为∗(下同)。
A-COG功能注释分类图;B-不同组间注释基因相对丰度图
图6-B为不同组间的COG功能平均相对丰度(前10)差异情况,结果显示,三腌阶段被注释到参与翻译、核糖体结构及合成、能源生产和转换的基因数量显著高于前2个腌制阶段;而注释到参与细胞壁/膜/包膜生物合成、辅酶运输和代谢、无机离子运输和代谢、复制/重组和修复的基因数量显著低于前2个腌制阶段(P≤0.05)。
2.4.3 KEGG数据库注释及差异分析
将测序结果与KEGG数据库中收录的蛋白序列进行BLAST比对和注释。结果显示,一级分类注释中共包含六类功能通路,分别为新陈代谢、环境信息、遗传信息、人类疾病、细胞过程和有机系统,其中,注释到新陈代谢通路的数量最多,共有32 728 194条;注释到有机系统通路的数量最少(图7-A)。针对二级分类注释,KEGG功能丰度前10的代谢途径包括:全局和总览图、碳水化合物代谢、膜运输、氨基酸代谢、能量代谢、翻译、信号传导、辅酶因子和维生素代谢、核酸代谢、神经退行性疾病,平均相对丰度分别为36.57%、7.99%、4.24%、4.23%、3.94%、3.80%、3.50%、3.12%、2.85%、2.85%(图7-B)。以上结果表明,被注释较多的代谢途径是碳水化合物代谢、氨基酸代谢、膜运输、能量代谢等,推测这些代谢通路可能是微生物群落影响榨菜风味物质形成的重要途径。有研究表明,榨菜在发酵过程中,还原糖含量降低,氨基酸态氮、有机酸和一些鲜味、甜味氨基酸含量增加,氨基酸还可与醇类发生酯化反应产生酯,这些风味物质的产生与乳酸菌Leuconostoc、Lactobacillus、Lactococcus、Debaryomyces hansenii 等有显著相关[11-14]。不同发酵阶段的微生物基因在同一类中注释结果存在差异(图7-B),三腌阶段被注释到能量代谢、翻译、信号转导的代谢途径的基因丰度高于前2个腌制阶段;而被注释到全局和总览图、碳水化合物代谢、膜运输、辅助因子和维生素代谢、核酸代谢的基因丰度低于前2个腌制阶段,这可能与不同发酵阶段优势微生物发生变化有关。
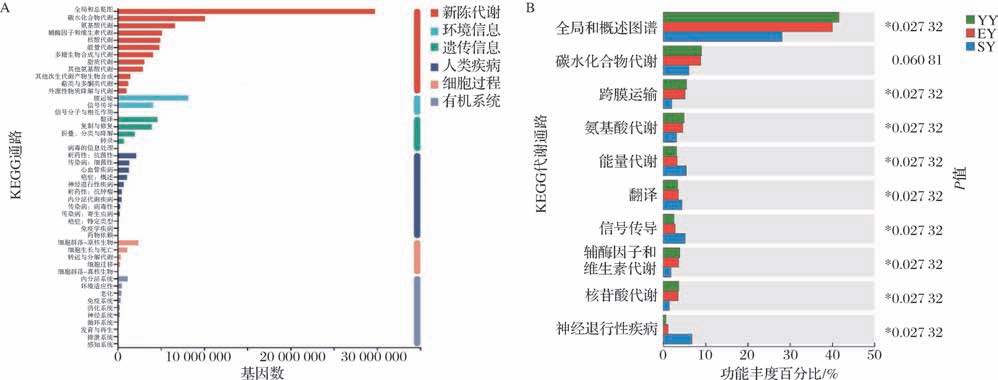
图7 KEGG代谢通路注释图及不同组间注释基因相对丰度图
Fig.7 KEGG metabolic pathway annotations and relative abundance of annotation genes in different groups
A-KEGG代谢通路注释图;B-不同组间注释基因相对丰度图
2.4.4 CAZy数据库注释及差异分析
CAZy数据库注释结果显示(图8-A),在榨菜发酵过程中共注释到9 053个基因,其中糖基转移酶(glycosyl transferases,GTs)和糖苷水解酶(glycoside hydrolases,GHs)是最丰富的CAZy类别,被注释到的基因数分别为3 429、3 171个,分别占比37.88% 和35.03%。然后依次是碳水化合物酯酶(carbohydrate esterases,CEs)、辅助氧化还原酶(auxiliary activities,AAs)、碳水化合物结合模块(carbohydrate-binding modules,CBMs)、糖裂合酶(polysaccharide lyases,PLs),被注释的基因数分别是960、889、336、268个。同一基因功能在不同组间的差异情况见图8-B,AA和GBM的基因丰度在不同发酵阶段存在显著差异(0.01 < P≤0.05),GH、GT、CE、PL的基因丰度在不同发酵阶段差异不显著(P >0.05)。以上结果显示,GHs和GTs是榨菜发酵过程中与碳水化合物代谢相关的主要酶,值得关注的是,GHs通过水解碳水化合物中的糖苷键生成单糖、寡糖或糖复合物,表明GHs和GTs在寡糖、芳香基糖苷的合成、氨基酸和多肽的糖基化方面具有重要作用[25]。而GTs负责催化糖分子与受体分子(如蛋白、寡糖、脂等)连接,参与纤维素、寡糖的分解[26]。本研究结果显示,GHs和GTs是榨菜发酵过程中与碳水化合物代谢相关的主要酶,产生丰富的寡糖与单糖供菌群代谢利用。多项研究表明,榨菜在发酵过程中糖含量逐渐降低[13-14],而糖是微生物生长和繁殖的主要碳源,微生物利用还原糖进行发酵,产生酸、醇、酯和其他风味物质[27]。
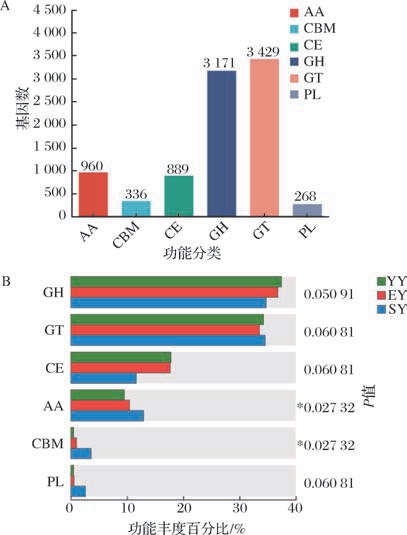
图8 CAZy代谢通路统计及不同组间注释基因相对丰度图
Fig.8 Statistics of the CAZy metabolic pathway and relative abundance of annotation genes in different groups
A-CAZy代谢通路统计;B-不同组间注释基因相对丰度图
3 结论
本研究基于宏基因组学技术分析了不同发酵阶段的涪陵榨菜的微生物多样性和功能基因,得到如下结论:相对丰度大于1.0%的优势菌群在门、属、种水平上分别有52、1 024、2 943个,优势菌群主要来自厚壁菌门、乳杆菌属和明串珠菌属。KEGG数据库注释发现,碳水化合物代谢和氨基酸代谢是注释最多的代谢途径,CAZy数据库注释发现,糖苷水解酶和糖苷转移酶基因数量较多,两者注释到的基因占总基因数目的70.42%。未来研究将分析优势菌群在主要代谢通路中的作用,并进一步探索榨菜微生物与风味物质形成的内在机制,以期为涪陵榨菜生产工艺的改进和品质提升提供理论依据。
[1]杜全模.四川榨菜加工的基本原理及其在生产上的应用[J].调味副食品科技,1984,1: 11-15.DU Q M.The basic principles of Sichuan mustard processing and its application in production[J].China Condiment,1984,1: 11-15.
[2]贺云川,周斌全,刘德君.涪陵榨菜传统工艺概述[J].食品与发酵科技,2013,49(4):57-60.HE Y C,ZHOU B Q,LIU D J.The overview of traditional Fuling Zhacai’s processes[J].Food and Fermentation Technology,2013,49(4):57-60.
[3]ZHANG J M,ZHANG C C,WU W C,et al.Correlation of the bacterial communities with umami components,and chemical characteristics in Zhejiang Xuecai and fermented brine[J].Food Research International,2021,140:109986.
[4]YANG J X,LI F Z,ZHANG Y L,et al.Metagenomic analysis of microbial community succession during the pickling process of Zhacai (preserved mustard Tuber) and its correlation with Zhacai biochemical indices[J].Journal of the Science of Food and Agriculture,2021,101(4):1646-1658.
[5]卢春霞,徐俊豪,余杰,等.HS-SPME-GC-MS/MS结合非靶向代谢组学分析涪陵榨菜发酵过程中挥发性成分[J].食品科学,2024,45(20):206-213.LU C X,XU J H,YU J,et al.Analysis of volatile components in Fuling pickled mustard Tuber during spontaneous fermentation by non-targeted metabolomics based on HS-SPME-GC-MS/MS [J].Food Science,2024,45(20):206-213.
[6]李瑶,余永,陈海,等.低盐榨菜加工中的危害因素分析及控制研究进展[J].食品与发酵工业,2023,49(18):374-380.LI Y,YU Y,CHEN H,et al.Research progress on hazard factors analysis and control of low-salt Tuber mustard processing[J].Food and Fermentation Industries,2023,49(18):374-380.
[7]赵丹,田俊青,程亚娇,等.榨菜脱盐工艺优化及品质分析[J].食品与发酵工业,2017,43(5):167-172.ZHAO D,TIAN J Q,CHENG Y J,et al.Desalting process optimization and quality analysis of Tuber mustard[J].Food and Fermentation Industries,2017,43(5):167-172.
[8]燕平梅,乔宏萍,赵文婧,等.基于PCR-DGGE方法分析榨菜中乳酸菌群落结构[J].食品科学,2016,37(13):136-139.YAN P M,QIAO H P,ZHAO W J,et al.PCR-DGGE analysis of lactic acid bacterial community structure in pickled mustard Tuber[J].Food Science,2016,37(13):136-139.
[9]ZHANG L F,FU G K,ZHANG Z.Electricity generation and microbial community in long-running microbial fuel cell for high-salinity mustard Tuber wastewater treatment[J].Bioelectrochemistry,2019,126:20-28.
[10]WANG J L,ZHOU J,WANG Y M,et al.Efficient nitrogen removal in a modified sequencing batch biofilm reactor treating hypersaline mustard Tuber wastewater: The potential multiple pathways and key microorganisms [ J].Water Research,2020,177:115734.
[11]吴晓红,高生平,蒋彩云,等.榨菜发酵过程中原核微生物群落结构及其理化因子的动态演替[J].食品与发酵工业,2021,47(1):27-34.WU X H,GAO S P,JIANG C Y,et al.Dynamic succession of prokaryotic microbial communities and physicochemical properties during the fermentation of Zhacai[J].Food and Fermentation Industries,2021,47(1):27-34.
[12]郝卓莉.遂宁榨菜发酵过程中细菌群落多样性和基因功能预测分析[J].中国酿造,2021,40(5):59-64.HAO Z L.Bacterial diversity and predictive analysis of gene function during fermentation process of Zhacai in Suining region[J].China Brewing,2021,40(5):59-64.
[13]ZHANG C C,ZHANG J M,LIU D Q.Biochemical changes and microbial community dynamics during spontaneous fermentation of Zhacai,a traditional pickled mustard Tuber from China[J].International Journal of Food Microbiology,2021,347:109199.
[14]LI J,HE Z F,YAN L X,et al.Analysis of the microbial community structure and flavor components succession during salt-reducing pickling process of Zhacai (preserved mustard Tuber)[J].Food Science &Nutrition,2023,11(6):3154-3170.
[15]王玉荣,李文鹏,蔡文超,等.基于宏基因组分箱方法揭示房县黄酒加工用小曲中微生物多样性[J].食品与发酵工业,2023,49(12):209-214.WANG Y R,LI W P,CAI W C,et al.Revealing microbial diversity in Huangjiu Xiaoqu by metagenomic binning approaches[J].Food and Fermentation Industries,2023,49(12):209-214.
[16]牛茵,吴双慧,何济坤,等.基于宏基因组技术分析自然发酵羊肉香肠中微生物多样性及挥发性风味功能基因[J].食品科学,2024,45(2):139-148.NIU Y,WU S H,HE J K,et al.Metagenomic analysis of microbial diversity and functional genes responsible for volatile flavor of naturally fermented mutton sausage[J].Food Science,2024,45(2):139-148.
[17]冼芳莹,赵文鹏,王思宇,等.基于宏基因组测序技术解析高温快速发酵豆豉菌群结构与功能注释[J].食品工业科技,2023,44(2):159-169.XIAN F Y,ZHAO W P,WANG S Y,et al.Analysis of the structure and function of high temperature and rapid fermentation Douchi flora based on macrogenome sequencing technology[J].Science and Technology of Food Industry,2023,44(2):159-169.
[18]刘大群,张程程,童川.基于高通量测序分析不同盐量榨菜坯料中细菌群落多样性[J].中国食品学报,2017,17(12):215-224.LIU D Q,ZHANG C C,TONG C.Analysis of bacterial community diversity in the picked mustard Tuber with different salt content based on high throughput sequencing[J].Journal of Chinese Institute of Food Science and Technology,2017,17(12):215-224.
[19]LIANG H P,CHEN H Y,ZHANG W X,et al.Investigation on microbial diversity of industrial Zhacai Paocai during fermentation using high-throughput sequencing and their functional characterization[J].LWT,2018,91:460-466.
[20]张锐,吴祖芳,沈锡权,等.榨菜低盐腌制过程的微生物群落结构与动态分析[J].中国食品学报,2011,11(3):175-180.ZHANG R,WU Z F,SHEN X Q,et al.Microbial community structure and its dynamic analysis during the processing of low-salinity pickled mustard Tuber[J].Journal of Chinese Institute of Food Science and Technology,2011,11(3):175-180.
[21]施安辉,周波.蔬菜传统腌制发酵工艺过程中微生物生态学的意义[J].中国调味品,2002,27(5):11-15.SHI A H,ZHOU B.The micro-ecological significance of the traditional greenstuff pickling process[J].China Condiment,2002,27(5):11-15.
[22]CHEN M J,QIN Y Y,DENG F M,et al.Illumina MiSeq sequencing reveals microbial community succession in salted peppers with different salinity during preservation[J].Food Research International,2021,143:110234.
[23]李明春.榨菜加工过程中挥发性风味物质的形成及变化研究[D].重庆: 重庆大学,2009.LI M C.Study on the formation and changes of volatile compounds in pickled mustard Tuber during the pickling process [ D].Chongqing: Chongqing University,2009.
[24]刘璞,吴祖芳,翁佩芳.榨菜腌制品风味研究进展[J].食品研究与开发,2006,27(1):158-161.LIU P,WU Z F,WENG P F.Advances of study on flavor of pickled mustard Tuber[J].Food Research and Development,2006,27(1):158-161.
[25]夏亚男,双全.基于宏基因组技术分析固态发酵枣酒酒醅的微生物多样性及关键风味基因[J].食品科学,2022,43(2):192-198.XIA Y N,SHUANG Q.Metagenomic analysis of microbial diversity and key flavor-related genes in solid-state fermented jujube mash for jujube wine[J].Food Science,2022,43(2):192-198.
[26]HUANG Z R,HONG J L,XU J X,et al.Exploring core functional microbiota responsible for the production of volatile flavour during the traditional brewing of Wuyi Hong Qu glutinous rice wine[J].Food Microbiology,2018,76:487-496.
[27]马欢欢,吕欣然,林洋,等.传统东北酸菜自然发酵过程中乳酸菌与营养物质同步分析[J].食品与发酵工业,2017,43(2):79-84.MA H H,LYU X R,LIN Y,et al.Synchronization analysis of lactic acid bacteria and nutrients during fermentation of traditional Northeastern Suancai in China[J].Food and Fermentation Industries,2017,43(2):79-84.