药食同源中药材(medicinal-food homologous Chinese herbal medicines,MFH-CHMs)是中国传统医学与现代营养学结合的产物,指兼具药用价值和食用功能的天然植物、真菌或矿物,是中医药“治未病”理念的重要载体。《神农本草经》中记载了现存最早的中药分类,其按作用和毒性分为上、中、下三品,上药“主养命以应天,无毒,多服久服不伤人”[1],药食同源中药材的雏形已然显现。如今在追求健康的生活理念中,防止与控制疾病、保证身体健康早已成为人们的共识,“饮食养生之道”正慢慢为人们所接受,药食同源中药材迎合了人们的养生理念,其研究和应用也逐渐受到大众的关注。截止2025年6月,我国卫健委已公布包括乌梅、火麻仁、代代花、白果在内的106种既是食品又是中药材的物质(表1),其性质分布见图1。
表1 既是食品又是中药材的物质名单
Table 1 A official list of medicinal-food homologous substances

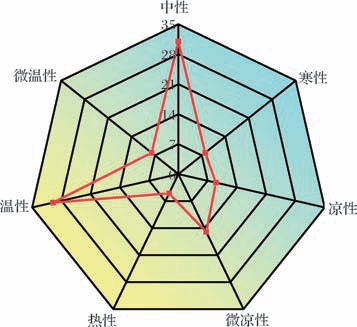
图1 药食同源物的性质分布雷达图
Fig.1 Functional property distribution of medicinal-food homologous substances
炮制是中医药学的特色,通过炮制可以达到减毒、增效、缓性和“生熟异治”的目的[2]。随着炮制技术的不断精进,精准控制下的微生物发酵成为中药炮制的研究热点。微生物在适当的含氧量、温度和湿度条件下发酵草药,产生的水解酶破坏植物细胞壁,使中草药中难以在体内吸收和利用的天然产物转化成易吸收的活性物质,增强或产生新的效果[3-4]。发酵微生物菌种是中药发酵的核心之一,选择合适的菌种既可以减少有毒代谢物积累和其他微生物的污染,又能提高产品的质量和稳定性[5]。乳酸菌是能利用碳水化合物产乳酸的一类细菌的总称,在发酵工业中有悠久的历史[6],常用作各种食品和中药材的发酵剂。越来越多学者已将研究目光投向乳酸菌的中药材发酵。因此,本文归纳了药食同源物质和可用于食品发酵的乳酸菌名单,并从中药材发酵技术、乳酸菌发酵的优势和机理及其发酵前后药食同源中药材活性物质和功效变化等方面进行了系统阐述,旨在为乳酸菌发酵药食同源中药材的深入研究和应用提供较为全面的信息。
1 中药材发酵技术概述及乳酸菌发酵的优势
1.1 发酵技术概述
传统中药发酵技术是依靠环境或植物自身携带的微生物来完成发酵,不需要精确控制发酵温度和湿度,通常靠经验判断发酵终点,难免出现发酵中药疗效、安全性不稳等问题。现代发酵技术整合了微生物生态学、发酵工程和生物工程,从而产生了新的中药发酵技术[3]。现代发酵技术可大致分为固态发酵、液态发酵和药用真菌双向发酵(图2)。
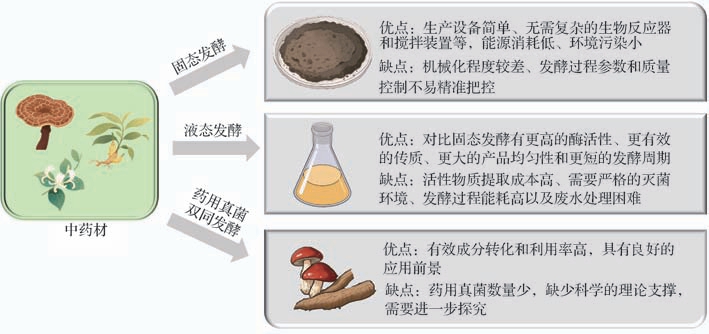
图2 现代发酵技术
Fig.2 Modern fermentation technology
固态发酵是指微生物在不存在或接近不存在游离水的固体基质上进行发酵的生物过程,基质必须具有足以支持微生物生长和代谢的水分[7]。王俊茹[8]筛选出一株鼠李糖乳酪杆菌对金银花进行固态发酵,通过优化确定固态发酵的最佳条件为34 ℃发酵68 h、发酵基质含水量60%以及接菌量10%,且发酵后绿原酸、总黄酮和总多糖含量较发酵前均显著提高,增量分别为8.80、34.62、34.90 mg/g。杨壮等[7]对比7种乳酸菌固态发酵黄精后的多糖得率,发现副干酪乳酪杆菌ATCC 334效果最优,后选用该菌固态发酵黄精研究黄精多糖发酵前后的结构和活性变化,发现发酵后多糖中木糖、核糖、岩藻糖及葡萄糖含量降低而鼠李糖、半乳糖醛酸和半乳糖含量均上升4倍,且发酵多糖结构更疏松、孔隙更致密、保水能力更强,体外抗氧化实验显示发酵多糖自由基清除能力显著高于未发酵多糖。
液态发酵是将活化好的菌种接种到含有药食同源中药材的液体培养基中,并在设定的温度、通气量等条件下发酵产生某些物质的过程。CHUNG等[9]利用乳酸乳球菌KC24液态发酵水培人参,发现发酵12 h和24 h后提取物中总酚含量较未发酵水培人参分别增加了6.1% 和4.1%,DPPH自由基清除能力测定显示24 h发酵提取物的抗氧化活性从32.57%显著提高到41%。王印壮等[10]研究了乳酸菌液态发酵对黄精山楂复合酵素品质的影响,发酵最优工艺为:34 ℃发酵52 h、黄精与山楂质量比5 ∶1及4% 接菌量,在此条件下复合酵素超氧化物歧化酶(superoxide dismutase,SOD)活性较未发酵时翻了一倍、黄酮含量显著提高且口感柔和清爽。
药用真菌双向发酵同时包括了上述2种发酵类型,是药用真菌与药食同源中药材间的双向作用。李慧星等[11]以蛹虫草作发酵真菌、山药作基质进行固态发酵,探究发酵后山药-蛹虫草-代谢物混合物(下称菌质)的抗氧化增效情况及原因,发现菌质的自由基清除率0~2 d缓速上升、2~8 d快速上升、8 d后趋于平稳,发酵后总酚、总皂苷、总黄酮含量均上升,HPLC指纹图谱分析显示,菌质对比山药生成了新成分,扫描电子显微镜(scanning electron microscopy,SEM)分析显示,蛹虫草发酵使山药从褶皱连续且完整变为褶皱减少且呈碎片状形态,傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)结果表明,菌质中产生了更多多酚类物质,表明菌质成分变化、结构变化是抗氧化活性增效的主要原因。雷晓蕾等[12]研究了葛根-茯苓液态发酵产物对2型糖尿病(type 2 diabetes mellitus,T2DM)模型大鼠胰岛素介导的参与机体糖代谢的关键信号通路的影响,结果表明该发酵产物可促进或上调T2DM大鼠肝脏和骨骼肌PI3K、Akt、GLUT4 基因和蛋白的表达,从而改善胰岛素抵抗所导致的T2DM。
1.2 乳酸菌发酵优势
乳酸菌在自然界种类繁多且分布广泛,粮谷、果蔬、蛋奶等食品往往含有多种天然微生物群。传统发酵食品正是利用其中本身携带以及开放环境的微生物群落进行发酵的,如在白酒大曲[13]、贵州酸汤[14]、郫县豆瓣酱[15]等传统发酵食品生产中,乳酸菌是整个或部分发酵阶段的优势菌种,发挥着提供酸性环境、抑杂菌、产酶促代谢、产酸类酯类等风味物质的作用。随着食品工业化的发展,均一的产品质量和可控的生产过程成为追求,新兴工业加工食品通常接种纯种乳酸菌菌株。中药材中接种乳酸菌发酵具有提高原本有效成分含量[16]、缓性减毒[17]、产生新的有效成分[18]和节约中药资源[19]等优点。
乳酸菌是益生菌之一,具有保护肠道、抗菌、降胆固醇、抗氧化和免疫调节等多种健康功效。罗伊氏粘液乳杆菌几乎天然存在于所有脊椎动物和哺乳动物的肠道,其对肠黏膜黏附能力强,能调节肠道菌群分布、拮抗有害细菌的定植,保护肠道健康[20]。加氏乳杆菌可以通过结合胶束脂质抑制膳食脂肪的吸收、缓解高胆固醇饮食引起的高胆固醇血症[21];据报道,上小肠中的加氏乳杆菌可通过影响依赖于ACSL3的脂肪酸感知通路来发挥血糖调节作用[22]。植物乳植杆菌能提高谷胱甘肽过氧化物酶和超氧化物歧化酶的活性,减少脂质过氧化和脱氧核糖核酸损伤,减缓细胞衰老[23]。研究发现,从日本泡菜中分离的植物乳植杆菌和戊糖乳杆菌的免疫调节能力与TagF2 基因密切相关,该基因编码合成聚甘油-3-磷酸盐型磷壁酸的关键酶,可能作为微生物相关分子模式发挥作用[24]。
2 乳酸菌发酵药食同源中药材
2.1 可用于发酵的乳酸菌种类
乳酸菌广泛应用于食品发酵工业。我国食品安全标准与监测评估司发布的2011年第25号、2012年第8号和2022年第4号公告已批准12个属、33个种的乳酸菌应用于食品(表2),其中很多菌种应用在中药材发酵中。除此之外,还有一些未列入名单的乳酸菌菌种也已用于中药发酵的研究,如戊糖乳杆菌[25]、酒类酒球菌[26]等。
表2 可用于食品的乳酸菌
Table 2 Food-grade LAB strains

续表1

注:∗仅限用于1岁以上幼儿的食品;√表示可用于婴幼儿食品。
2.2 乳酸菌发酵机理
乳酸菌与药食同源中药材往往有相互促进的效果。一方面通过乳酸菌发酵作用提升中药材活性物质的含量和功效,另一方面药食同源物质中的活性成分也会利于乳酸菌的增殖。乳酸菌的发酵机理见图3。
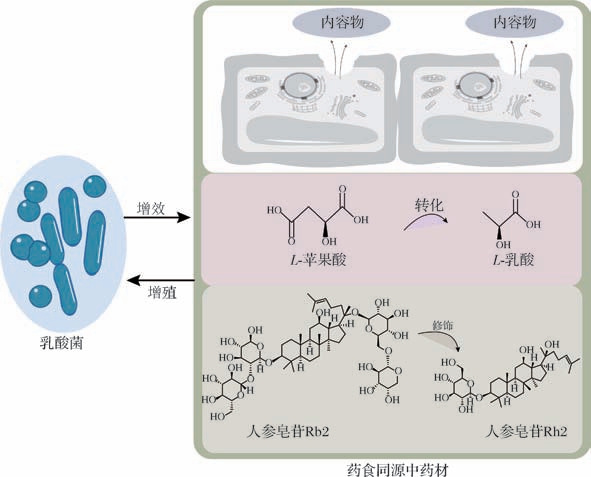
图3 乳酸菌发酵机理
Fig.3 Mechanistic insights into LAB fermentation
乳酸菌的生物转化作用体现在如下3个方面[27]:
(1)乳酸菌自身代谢产生特定酶系,破坏植物细胞壁促使活性成分释放。例如:纤维素酶破坏细胞壁使得内容物溶出从而提升丹参地上茎叶的品质、改善其营养价值[16,28],靳思玉等[29]用乳酸菌发酵斜茎黄芪后测定黄酮含量比对照组增加了约1.45倍。
(2)乳酸菌通过酶作用,将前体物质转化为活性成分。例如:研究发现明串珠菌属、乳杆菌属和足球菌属的乳酸菌能将L-苹果酸转变成L-乳酸[30],既实现生物降酸又改善产品风味;PRATIWI等[31]研究植物乳植杆菌的苹果酸-乳酸发酵,发现在有酿酒酵母存在下,植物乳植杆菌接种量为2%时蛇果醋的总酚含量最高,为106.72 mL GAE/mL,其次是接菌量6%(104.34 mL GAE/mL)和4%(99.17 mL GAE/mL);而抗氧化活性则是4%时最高,为96.46 ppm。
(3)乳酸菌通过酶促作用对活性成分进行修饰,使衍生物的活性更高。例如:乳酸杆菌、明串珠菌和双歧杆菌等可以将主要人参皂苷Rb 1和Rb 2转化为渗透性更强、生物利用度更高的稀有人参皂苷Rh 1、Rh 2、Rg 2、Rg 3等[18];PARK等[32]研究了泡菜中分离的5株乳酸菌的人参皂苷转化能力,发现肠系膜乳杆菌WiKim 19和WiKim 20转化人参皂苷Rb 1为Rg 3的能力约为另外3株菌的5倍。
药食同源中药材的存在有利于乳酸菌的生长、代谢和增效。研究表明,3种药食同源植物紫苏、生姜和花椒的浸提液均有利于乳酸菌的生长[33]。林大成等[34]用添加了药食同源物质(山药)的特制培养基对比普通培养基,研究对嗜酸乳杆菌(Lactobacillus acidophilus,LA)、德氏乳杆菌保加利亚亚种(Lactobacillus delbrueckii subsp. Bulgaricus,LB)、约氏乳杆菌(Lactobacillus johnsonii,LJ) 发酵产胞外多糖(exopolysaccharide,EPS)及抗氧化能力影响,结果表明无论单菌发酵还是混菌发酵,特制培养基效果都明显优于普通培养基,EPS产量和产率规律大致呈现:MIX >LB >LA >LJ,产量较对照组提升2.3~3.2倍,还原力和DPPH自由基清除能力分别提升1.8~2.2倍和1.5~1.8倍。LI等[35]研究发现马齿苋富含酚酸类活性成分,能有效缓解右旋糖酐硫酸钠(dextran sulfate sodium,DSS)诱导的溃疡性结肠炎小鼠的体重减轻、便血、腹泻和结肠缩短症状,体内外实验揭示马齿苋通过NF-κB信号通路抑制炎症相关iNOS和NLRP3蛋白的表达,促进双歧杆菌、嗜酸乳杆菌等有益微生物的生长繁殖、抑制拟杆菌等条件微生物的增殖,表明了马齿苋对肠道健康的有益作用。
3 乳酸菌发酵对药食同源中药材活性物质及功效的影响
药食同源中药材往往富含多种活性物质,但这些物质却不容易直接释放和被人体吸收利用。乳酸菌发酵作用能提高活性成分释放率并会对活性成分产生一定影响,如小分子化、基团修饰等,实现增效作用(图4)。
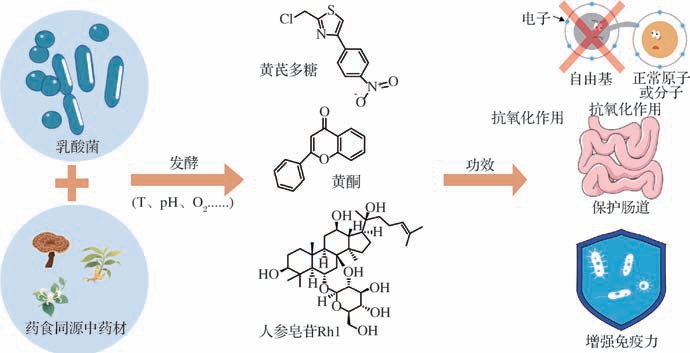
图4 活性成分和功效示意图
Fig.4 Schematic of active compounds and efficacy
3.1 多酚类
多酚类化合物在自然界中储量丰富、种类繁多,包括黄酮类、酚酸和木脂素等。多酚类物质具有抗氧化、抗炎、抗癌等特性,在食品、医药、化妆品等领域应用广泛,但黄酮类、木脂素的低水溶性及酚酸的低亲脂性限制了其在机体的性能[36]。研究发现发酵作用能促进酚类的释放并提高其抗氧化活性,且不同微生物发酵效果往往不同[37]。刘梦培等[38]使用植物乳植杆菌和酿酒酵母分别发酵杜仲雄花,其他发酵条件保持相同,对比未发酵杜仲雄花,发现经植物乳植杆菌发酵后总黄酮含量大幅上升,发酵第5天含量达到峰值6.0 mg/mL,增幅高达70%,而酿酒酵母发酵后总黄酮含量变化不大,发酵峰值出现在第2天,增幅仅为7.5%;发酵使得绿原酸含量小幅度增加,经植物乳植杆菌发酵在第1天达到峰值、增幅为29.4%,酵母则在第6天到达峰值、增幅为27.1%。两相比较显示了植物乳植杆菌的明显优势。研究表明乳酸菌可以通过增加植物的酚类含量来提高抗氧化活性。于中玉等[25]利用戊糖乳杆菌LJ-15发酵薏仁米,发现发酵48 h后总黄酮和总多酚含量均上升,分别从0.035 mg RE/g和0.58 mg GAE/g增加至0.065 mg RE/g和0.81 mg GAE/g,抗氧化能力上升了约1.3倍。陈彦辉等[39]探究了植物乳植杆菌发酵对沙棘多酚类物质的影响,发现发酵的4~8 d乳酸菌处于生长对数期,与此同时游离酚含量显著增加、结合酚含量显著降低、总酚含量保持平稳,这可能是乳酸菌的生长促使结合酚转化为游离酚;发酵0~10 d内,ABTS阳离子自由基和DPPH自由基清除能力均呈现先上升后缓慢下降直至平稳的趋势,且均在第2天达到最高抗氧化水平,乳酸菌发酵提高了沙棘汁的抗氧化特性,这可能是乳酸菌发酵产生β-葡萄糖苷酶将沙棘糖苷水解成了具有更高自由基配基能力的糖苷的原因;UPLC-MS/MS分析及KEGG通路富集分析表明,沙棘多酚转化的重要通路是次生代谢物的生物合成,这可能是沙棘糖苷类多酚向苷元类多酚转化的主要途径,而β-葡萄糖苷酶对促进糖苷转化为苷元有重要作用。李璞钰[40]在宁夏浆水中通过纯培养和耐酸实验分离到一株植物乳植杆菌YHG1-155,用来探究乳酸菌β-葡萄糖苷酶转化沙棘多酚的情况,结果显示发酵产生了五类多酚代谢物,酚酸、黄酮类化合物差异代谢物种类最为丰富,占总产物的70.59%~95.78%,而鞣质、木脂素和香豆素、芪类差异代谢物种类较少,仅为4.22%~29.41%;相关性研究表明,β-葡萄糖苷酶活性与植物乳植杆菌活菌数和部分多酚代谢物含量密切相关。武海丽等[41]的研究表明,沙棘叶多酚具有抑制结肠癌细胞增殖的作用,游离态多酚和结合态多酚的抑制作用均呈现剂量依赖性,但结合态多酚抑制效果更强。此外,有报道表明,肉桂多酚能抑制大鼠肾脏内NLRP3蛋白活化及NLRP3介导的IL-1β 成熟,减轻糖尿病大鼠肾组织的炎症反应,从而对糖尿病肾病大鼠肾脏损伤起到保护作用[42];花椒叶经几种不同有机溶剂提取后的总多酚、总黄酮含量均较水提法翻倍,且抑菌效果显著提升,其中无水乙醇萃取物对金黄色葡萄球菌和大肠杆菌的抑制率均最高[43];黑果枸杞多酚能缓解聚苯乙烯所致生殖毒性,通过DAVID数据库富集分析、分子对接及蛋白质互作网络分析发现,TNF、ESR1、TLR4及EGFR等分子在黑果枸杞多酚对抗聚苯乙烯生殖毒性过程中发挥作用,它们可能是缓解毒性效应的关键[44]。药食同源中药材中的多酚物质的更多功效和作用机制还有待深入研究,与乳酸菌发酵相结合实现功能物质增量增效的研究前景广阔。
3.2 多糖类
多糖是药食同源中药材的重要组成部分,它是不同种类的单糖通过糖苷键结合形成复杂的结构,具有抗氧化、抗菌、降疲劳和提高机体免疫力等功效,其生物活性与多糖的结构密切相关[45]。张心驰等[46]用不同浓度乙醇分级沉淀兰州百合多糖,得到4种多糖产物:BLP-30、BLP-50、BLP-70、BLP-80,它们单糖种类相似,但摩尔分数存在一定的差异,4种多糖产物均富含甘露糖和葡萄糖,推测葡萄糖和甘露糖是兰州百合多糖骨架的主要单糖;体外降血糖实验显示,BLP-50对α-淀粉酶的抑制率提升最多(70.24%),BLP-70对α-淀粉酶的抑制率最高(98.35%),BLP-50和BLP-70对α-葡萄糖苷酶的抑制率分别高达到97.43%和98.36%,综合分析,BLP-70的体外降血糖活性最强。与小分子质量的多糖相比,中药多糖往往具有分子质量大、含量低等特点,使它们的提取、分离、纯化和结构分析更加复杂和更具挑战性[47],而乳酸菌发酵可以提高多糖含量、修饰多糖结构、小分子化多糖分子量以及提高多糖的活性。李嘉懿等[48]将副干酪乳酪杆菌KL1和植物乳植杆菌植物亚种Zhang-LL 1∶1复合后接种于复方中药培养基中,对比发酵前后多糖得率提高了2.51倍。陈晓维等[49]用干酪乳酪杆菌、植物乳植杆菌和鼠李糖乳酪杆菌两两复合发酵红枣浆,发现发酵24 h后,3组混菌发酵的红枣浆多糖含量均明显高于未发酵组,其中,植物乳植杆菌和鼠李糖乳酪杆菌复合发酵的红枣浆中多糖含量最高,约为3.25 mg/g;在抗氧化方面,该混菌组合的DPPH自由基和ABTS阳离子自由基清除能力也显著高于其余2组。HUANG等[50]利用发酵乳杆菌发酵龙眼果肉,对未发酵和发酵龙眼果肉中的多糖进行了分析,发现发酵龙眼多糖的中性糖和糖醛酸含量对比未发酵多糖均降低;此外,龙眼多糖的分子质量随发酵时间显著降低,从(221.63±2.41) kDa降至(109.62±10.66) kDa、溶解度从(42.50±0.21) mg/mL增加到(79.30±0.49) mg/mL,这可能是由于发酵粘液乳杆菌分泌的酶可以降解多糖的分子链,从而导致分子质量下降而溶解度提升;在20 μg/mL质量浓度下,发酵龙眼多糖使IL-6分泌量翻了一倍,增至3.73 pg/mL,且对巨噬细胞产NO具有促进作用,表明发酵龙眼多糖具有增强免疫力的功效。CAO等[51]利用植物乳植杆菌NX-1发酵黄精,发现黄精溶液中多糖含量从19.87 mg/mL增至27.57 mg/mL,这可能是该菌株中含有大量糖苷水解酶和糖基转移酶基因,能有效提高多糖含量;经植物乳植杆菌NX-1发酵后的黄精溶液中,参与胆酸代谢的牛磺胆酸、乙酰胆碱和磷酸胆碱,以及参与亚油酸代谢的(+/-)12,13-二羟基氧代癸酸和13-氧代亚油酸均显著上升。这可能是因为该菌株中含有大量脂质代谢酶基因,能有效提升牛磺胆酸、乙酰胆碱、和D-(+)-甘油酸等活性成分的含量,从而促进脂质代谢。随着研究的深入,关于乳酸菌发酵多糖的机理探索究也越来越多。HUANG等[52]研究发现植物乳植杆菌ATCC 14917发酵能有效促进荔枝果肉中的水不溶性多糖向水溶性多糖转化,且内切葡聚糖酶(包括WP_003644430.1、WP_003643493.1和WP_003643018.1)是水溶性多糖积累的重要因素,水溶性多糖中半乳糖和半乳糖醛酸的释放部分归因于GH42-、GH36-、GH2半乳糖苷酶的表达。
3.3 皂苷类
皂苷类物质是一类由皂苷元(非糖部分)和糖链(糖部分)通过糖苷键结合而成的天然化合物,兼具亲水性和亲油性,广泛存在于植物、某些海洋生物和微生物中,具有抗癌、抗炎、免疫调节等多种生物活性[53]。目前关于皂苷类物质的研究主要集中在微生物作用提高皂苷含量、稀有皂苷的生物转化以及皂苷功效等方面。郑苗等[54]将植物乳植杆菌HZLp-005、干酪乳酪杆菌HZLc-017、鼠李糖乳酪杆菌HZLr-023和嗜酸乳杆菌HZLa-008按1∶1∶1∶1比例混合发酵怀山药块茎,发现薯蓣皂苷元含量在发酵的0~24 h呈现出先下降后升高的趋势,可能是发酵前期乳酸菌利用了部分皂苷元作为营养物质、而后期产生的酶促使怀山药中的薯蓣皂苷水解生成薯蓣皂苷元而加速释放。酸枣仁皂苷A、B是酸枣仁中的特异皂苷,其通过影响下丘脑中蛋白质的表达改变血脑屏障的通透性,从而表现出安神、改善睡眠的功效[55]。张政[56]利用3株植物乳植杆菌发酵酸枣仁汁,发现发酵过程中酸枣仁皂苷A、B呈现先增后降的趋势,在36 h达到最大值,菌株G 1.2和GD 06发酵后皂苷A、B升高量显著高于对照菌株JYLP-326发酵,分别升高了19.16%、3.28% 和20.95%、4.36%;发酵还提高了酸枣仁汁的镇静助眠活性。皂苷类物质中,人参皂苷的研究最为深入,据报道现已分离出620多种人参皂苷,按结构分为三类[57]。植物中天然含有的皂苷大部分为主要人参皂苷Rg 1、Re、Rb 1等,这类皂苷往往含有较多的糖基数目,在体内需要经过肠道微生物代谢为稀有人参皂苷才能发挥药理功效;天然的稀有人参皂苷含量极低,如Rg 3、Rh 1、Rh 2,这类皂苷的糖基数少、分子质量小,更易进入血液循环发挥功效[58-59],因此如何将主要人参皂苷转化为稀有人参皂苷成为研究热点。西洋参中皂苷含量丰富,但稀有皂苷含量很低,其中稀有皂苷P-F11 是西洋参的特异成分[60]。张玉梅[61]筛选出一株植物乳植杆菌,结合超声辅助发酵西洋参,HPLC分析发现发酵后西洋参皂苷的峰面积增加且有新峰产生,高分辨质谱分析初步推断转化峰可能是稀有人参皂苷Rk 1、Rg 5、C-K、Rh 2、F 4;继续对发酵产物进行研究,发现发酵西洋参总皂苷浓度为100 μg/mL时,对HepG 2细胞脂质沉积模型中甘油三酯的清除率达到了55%,对总胆固醇的清除率达到了34.9%,其中低密度胆固醇含量明显降低而高密度胆固醇含量略有上升。这表明植物乳植杆菌发酵的西洋参皂苷具有良好的减脂和降胆固醇功效。金玉洁[62]接种高密度的植物乳植杆菌ZU 018分别发酵Re、Rc、Rb 1三种皂苷底物,发现均能实现生物转化;其中人参皂苷Rb 1的转化效果最好,经菌种ZU 018发酵可转化产生F 2和C-K这2种稀有皂苷。PALANIYANDI等[63]发现副干酪乳酪杆菌耐受性亚种MJM 60396发酵可以将人参皂苷Rb 1转化为Rg 3和Rh 2,HPLC分析显示皂苷转化途径为Rb 1→Rd→Rg 3→Rh 2(Rd作为中间化合物);研究发现,菌株MJM 60396发酵的10 d培养期,Rb 1的浓度持续降低;转化产物Rg 3在第3天出现、在第7天含量达到最高为76.1%,之后开始下降;转化产物Rh 2在第7天出现、到第10天逐渐增加到49.7%。转化后的稀有人参皂苷生物活性显著增强,例如人参皂苷Rg 3可以通过下调miR-216a-5p来减轻糖尿病肾病的进展,减轻肾脏炎症[64]。
3.4 其他
除上述几类主要活性物质外,乳酸菌发酵药食同源中药材也会影响其他活性成分。研究表明,乳酸菌发酵的枣泥中维生素C、β-葡聚糖和β-胡萝卜素含量显著提高,同时草酸、植酸等抗营养物质含量明显低于未发酵的枣泥,提高了枣泥的抗氧化作用、降低了营养拮抗作用[65];乳酸菌发酵酸枣仁汁,在12 h时γ-氨基丁酸含量达到最高,为0.029 mg/mL,较非发酵含量提高了约45%,提高了酸枣仁的安神助眠效果[56]。
4 展望
中药材所含有效成分普遍存在浓度偏低问题,部分组分甚至呈现毒性特征。利用乳酸菌对药材进行发酵处理,不仅能转化生成更易被机体吸收的活性物质,还能显著降低其毒副作用。因此,筛选高效安全的乳酸菌菌种并创新中药发酵工艺具有重要研究价值。当前对药食同源中药材的研究主要聚焦于发酵技术参数优化和发酵过程管控,且研究普遍存在菌种单一化问题。采用多菌种协同发酵模式处理药食同源中药材时,能够显著提升生物酶系的多样性并丰富次级代谢产物谱。这种发酵方式不仅具备更高的底物转化能力,同时在产业化应用层面展现出更广阔的发展空间,成为引领中药现代化发酵技术研究的未来趋势。
尽管乳酸菌本身对人体无害,但其发酵产物仍需进行系统科学的安全性评估。在投入实际应用前,必须制定并完善中药发酵的标准化规范。通过乳酸菌转化药食同源中药材,不仅为揭示天然活性成分生成机制提供了研究平台,更为开发人用和兽用健康产品开辟了新途径。随着合成生物学技术的进步,未来有望构建高效的微生物合成系统来规模化生产药食同源中药材活性成分。
[1]朱姝,王玉芳.论历代本草著作之中药分类方法[J].辽宁中医药大学学报,2012,14(10):157-159.ZHU S,WANG Y F.Analysis of ancient herbal medicine books of traditional Chinese medicine classification[J].Journal of Liaoning University of Traditional Chinese Medicine,2012,14(10):157-159.
[2]汪祺,赵宇新,顾杰,等.基于炮制建立反映中药饮片质量特点的中药标准[J].中国药学杂志,2025,60(2):114-120.WANG Q,ZHAO Y X,GU J,et al.Establishment of traditional Chinese medicine standards reflecting the quality characteristics of Chinese herbal pieces based on processing[J].Chinese Pharmaceutical Journal,2025,60(2):114-120.
[3]LI L,WANG L,FAN W X,et al.The application of fermentation technology in traditional Chinese medicine: A review[J].The American Journal of Chinese Medicine,2020,48(4):899-921.
[4]ZHANG X L,MIAO Q,PAN C X,et al.Research advances in probiotic fermentation of Chinese herbal medicines [J].iMeta,2023,2(2): e93.
[5]陈瑾,吴春颖,王舒玉,等.六神曲两菌协同发酵工艺的优化[J].中华中医药杂志,2022,37(12):7446-7449.CHEN J,WU C Y,WANG S Y,et al.Optimization of fermentation process of Liushenqu by two strains[J].China Journal of Traditional Chinese Medicine and Pharmacy,2022,37(12):7446-7449.
[6]HE X N,CUI Y,JIA Q Y,et al.Response mechanisms of lactic acid bacteria under environmental stress and their application in the food industry[J].Food Bioscience,2025,64:105938.
[7]杨壮,刘怡琳,李隆熙,等.固态发酵制备黄精多糖的工艺优化、理化特性及抗氧化活性[J].食品与发酵工业,2024,50(7):92-98.YANG Z,LIU Y L,LI L X,et al.Process optimization,physicochemical properties,and antioxidant activity of Polygonatum sibiricum polysaccharide prepared by solid-state fermentation[J].Food and Fermentation Industries,2024,50(7):92-98.
[8]王俊茹.鼠李糖乳杆菌固态发酵金银花条件优化及其产物抗病毒效果的初步研究[D].郑州:河南农业大学,2024.WANG J R.Optimization of solid-state fermentation conditions for Lactobacillus rhamnosus on honeysuckle and preliminary study on the antiviral effect of its products[D].Zhengzhou: Henan Agricultural University,2024.
[9]CHUNG Y,PARK J Y,LEE J E,et al.Antioxidant activity and inhibitory effect on nitric oxide production of hydroponic ginseng fermented with Lactococcus lactis KC24[J].Antioxidants,2021,10(10): 1614.
[10]王印壮,费鹏,马艳莉,等.黄精山楂复合酵素发酵工艺优化及品质变化[J].食品研究与开发,2022,43(19):124-133.WANG Y Z,FEI P,MA Y L,et al.Optimization of fermentation process and quality change of Polygonatum sibiricum-hawthorn compound enzyme[J].Food Research and Development,2022,43(19):124-133.
[11]李慧星,周永康,方佩琦,等.山药-蛹虫草双向发酵的抗氧化活性增效性[J].食品科学,2021,42(13):51-56.LI H X,ZHOU Y K,FANG P Q,et al.Enhancement of antioxidant activity of Chinese yam by fermentation with Cordyceps militaris[J].Food Science,2021,42(13):51-56.
[12]雷晓蕾,李津.葛根-茯苓发酵产物对T2DM模型大鼠PI3K/Akt/GLUT4信号通路的影响[J].中国中医基础医学杂志,2025,31(1):49-54.LEI X L,LI J.Effect of fermented products of pueraria-Poria on the PI3K/Akt/GLUT4 signaling pathway in T2DM model rats[J].Chinese Journal of Basic Medicine in Traditional Chinese Medicine,2025,31(1):49-54.
[13]薄涛,吕娜,杨凯环,等.白酒大曲发酵过程中微生物群落及功能研究进展[J].食品科学,2023,44(19):385-393.BO T,LYU N,YANG K H,et al.Recent advances in understanding the composition and functions of microbial community in the fermentation of Baijiu Daqu[J].Food Science,2023,44(19):385-393.
[14]WANG C,ZHANG Q,HE L P,et al.Determination of the microbial communities of Guizhou Suantang,a traditional Chinese fermented sour soup,and correlation between the identified microorganisms and volatile compounds[J].Food Research International,2020,138:109820.
[15]洋汶,徐嘉悦,杨沛树,等.郫县豆瓣发酵微生物与风味物质的研究进展[J].食品工业科技,2025,46(11):21-31.YANG W,XU J Y,YANGPS,et al.Research progress on fermentation microorganisms and flavor compounds in Pixian broad bean paste[J].Science and Technology of Food Industry,2025,46(11):21-31.
[16]LIU J L,LIU M J,SHENG P J,et al.Biotechnological effects of Lactobacillus plantarum,cellulase,and xylanase on nutritional quality and microbial community structure of corn stover silage[J].Fermentation,2025,11(1): 14.
[17]何静阳.白果减毒增效乳酸菌的筛选及功能性饮品的开发[D].南京:南京农业大学,2023.HE J Y.Screening of lactic acid bacteria for reducing toxicity and enhancing efficacy of Baiguo and development of functional beverages[D].Nanjing: Nanjing Agricultural University,2023.
[18]VASQUEZ R,SONG J H,PARK Y S,et al.Application of probiotic bacteria in ginsenoside bioconversion and enhancing its healthpromoting benefits: A review[J].Food Science and Biotechnology,2025,34(8):1631-1659.
[19]赵婵娟,鄢行安,曹立亭,等.复方中药渣发酵物对断奶仔猪生长性能、血清生化指标的影响[J].中国畜牧杂志,2025,61(7):294-298.ZHAO C J,YAN X A,CAO L T,et al.Effects of compound Chinese medicine residue fermentation on growth performance and serum biochemical indexes of weaned piglets[J].Chinese Journal of Animal Science,2025,61(7):294-298.
[20]YOKOTA Y,SHIKANO A,KUDA T,et al. Lactobacillus plantarum AN1 cells increase caecal L.reuteri in an ICR mouse model of dextran sodium sulphate-induced inflammatory bowel disease[J].International Immunopharmacology,2018,56:119-127.
[21]蒋晓晗,阳田恬,李金转,等.加氏乳杆菌的特性与生物学功能及其生产应用[J].饲料工业,2023,44(6):96-100.JIANG X H,YANG T T,LI J Z,et al.Properties of Lactobacillus gasseri and its biological functions[J].Feed Industry,2023,44(6):96-100.
[22]BAUER P V,DUCA F A,ZAVED WAISE T M,et al. Lactobacillus gasseri in the upper small intestine impacts an ACSL3-dependent fatty acid-sensing pathway regulating whole-body glucose homeostasis[J].Cell Metabolism,2018,27(3):572-587.e6.
[23]班世栋,张建星,宗春阳,等.从传统发酵食品到大健康食品:功能微生物的新机遇[J].中国酿造,2025,44(6):8-13.BAN S D,ZHANG J X,ZONG C Y,et al.From traditional fermented foods to health-focused foods: New opportunities in functional microorganism[J].China Brewing,2025,44(6):8-13.
[24]LIU Y T,SAWADA K,ADACHI T,et al.Comparative genome analysis of the immunomodulatory ability of Lactiplantibacillus plantarum and Lactiplantibacillus pentosus from Japanese pickles[J].mSystems,2025,10(5): e01575-e01524.
[25]于中玉,黄佳琪,周凤霞.戊糖乳杆菌LJ-15对薏仁米的发酵特性研究[J].食品科技,2022,47(7):134-140.YU Z Y,HUANG J Q,ZHOU F X.Fermentation characteristics of Coix seed by Lactobacillus pentosus LJ-15[J].Food Science and Technology,2022,47(7):134-140.
[26]李长健.乳酸菌发酵对刺五加叶活性成分的影响及其降糖作用研究[D].哈尔滨:哈尔滨商业大学,2020.LI C J.Effects of lactic acid bacteria fermentation on active components of Acanthopanax leaves and its hypoglycemic activity[D].Harbin: Harbin University of Commerce,2020.
[27]孙慧峰,朱钧溢,国立东,等.乳酸菌生物转化药食同源植物活性成分研究进展[J].食品工业科技,2022,43(7):474-481.SUN H F,ZHU J Y,GUO L D,et al.Research progress on biotransformation of lactic acid bacteria on active ingredients from homologous plants of medicine and food[J].Science and Technology of Food Industry,2022,43(7):474-481.
[28]酆炳森,刘玉珊,刘凌霄,等.乳酸菌与纤维素酶对丹参地上部分青贮品质的影响[J].草地学报,2024,32(10):3313-3319.FENG B S,LIU Y S,LIU L X,et al.Effects of lactic acid bacteria and cellulase on the silage quality of above-ground parts of Salvia miltiorrhiza[J].Acta Agrestia Sinica,2024,32(10):3313-3319.
[29]靳思玉,李苗苗,王立超,等.不同处理对斜茎黄芪青贮发酵品质及黄酮含量的影响[J].黑龙江畜牧兽医,2020(6):107-111.JIN S Y,LI M M,WANG L C,et al.Effects of different treatments on fermentation quality and flavonoid content of Astragalus sinicus silage[J].Heilongjiang Animal Science and Veterinary Medicine,2020(6):107-111.
[30]张春晖,罗耀文,李华.葡萄酒苹果酸-乳酸发酵代谢机理[J].食品与发酵工业,1999,25(5):64-67.ZHANG C H,LUO Y W,LI H.Metabolic mechanism of malolactic fermentation in wine[J].Food and Fermentation Industries,1999,25(5):64-67.
[31]PRATIWI V N,ZUBAIDAH E,WIDYANINGSIH T D,et al.Enhancement of phenolic content and antioxidant activity in snakefruit(Salacca zalacca (Gaerth.)Voss) vinegar by malolactic fermentation with Lactobacillus plantarum[J].Journal of Food Science and Technology,2025: 1-9.
[32]PARK B,HWANG H,LEE J,et al.Evaluation of ginsenoside bioconversion of lactic acid bacteria isolated from kimchi[J].Journal of Ginseng Research,2017,41(4):524-530.
[33]王聪,廖萌,张喆,等.三种药食原料对乳酸菌生长及抗氧化的影响[J].食品工业,2017,38(7):32-35.WANG C,LIAO M,ZHANG Z,et al.The influence of three Chinese medicinal herbs on the growth and antioxidant properties of lactic acid bacteria[J].The Food Industry,2017,38(7):32-35.
[34]林大成,张帆,陈群昌.以中草药促进乳酸菌发酵胞外多糖的抗氧化功能[J].泉州师范学院学报,2017,35(2):45-52.LIN D C,ZHANG F,CHEN Q C.Using Chinese herbal medicine to promote the antioxidant functions of exopolysaccharides fermented by lactic acid bacteria[J].Journal of Quanzhou Normal University,2017,35(2):45-52.
[35]LI Z,CHU T J,SUN X,et al.Polyphenols-rich Portulaca oleracea L.(purslane) alleviates ulcerative colitis through restiring the intestinal barrier,gut microbiota and metabolites[J].Food Chemistry,2025,468:142391.
[36]SALAZAR J,ORTEGA Á,PÉREZ J L,et al.Role of polyphenols in dermatological diseases: Exploring pharmacotherapeutic mechanisms and clinical implications[J].Pharmaceuticals,2025,18(2): 247.
[37]HUR S J,LEE S Y,KIM Y C,et al.Effect of fermentation on the antioxidant activity in plant-based foods[J].Food Chemistry,2014,160:346-356.
[38]刘梦培,李佳,纵伟,等.乳酸菌和酵母菌发酵对杜仲雄花茶汁品质及抗氧化活性的影响[J].中国酿造,2020,39(5):71-76.LIU M P,LI J,ZONG W,et al.Effects of lactic acid bacteria and yeast fermentation on the quality and antioxidant activity of male Eucommia ulmoides flower tea juice[J].China Brewing,2020,39(5):71-76.
[39]陈彦辉,李亚凤,李璞钰,等.植物乳杆菌YHG1-155发酵沙棘汁促糖苷类多酚生物转化[J].中国食品学报,2024,24(11):289-299.CHEN Y H,LI Y F,LI P Y,et al.The biotransformation of glycoside polyphenols in sea buckthorn juice by Lactobacillus plantarum YHG1-155 fermented[J].Journal of Chinese Institute of Food Science and Technology,2024,24(11):289-299.
[40]李璞钰.宁夏浆水微生物中高产β-葡萄糖苷酶乳酸菌筛选及其对沙棘果多酚生物转化的研究[D].银川:宁夏大学,2022.LI P Y.Screening of lactic acid bacteria with high-yield β-glucosidase from Ningxia Jiangshui microbiota and its study on biotransformation of polyphenols in sea buckthorn fruit [D].Yinchuan:Ningxia University,2022.
[41]武海丽,杜锦娥,路洋洋,等.沙棘叶多酚的分离纯化及其活性分析[J].山西大学学报(自然科学版),2023,46(1):236-243.WU H L,DU J E,LU Y Y,et al.Purification and activity analysis of polyphenols from Hippophae rhamnoides leaves[J].Journal of Shanxi University (Natural Science Edition),2023,46(1):236-243.
[42]黄凤,覃田田,黄国栋,等.肉桂多酚抑制炎症小体并改善糖尿病大鼠的肾损伤[J].世界中医药,2025,20(6):932-937.HUANG F,QIN T T,HUANG G D,et al.Cinnamon polyphenols inhibit inflammasome and ameliorate kidney injury in diabetic rats[J].World Chinese Medicine,2025,20(6):932-937.
[43]陈新宇,张雪,谢贞建.花椒叶不同溶剂提取物抗氧化、清除亚硝酸盐及抑菌活性对比研究[J].中国调味品,2025,50(7):84-89;95.CHEN X Y,ZHANG X,XIE Z J.Comparative study on antioxidant,nitrite scavenging and antibacterial activities of different solvent extracts from Zanthoxylum bungeanum leaves[J].China Condiment,2025,50(7):84-89;95.
[44]刘浩然,杨柳,田慧,等.黑果枸杞多酚抗聚苯乙烯生殖毒性机制研究[J].中药新药与临床药理,2025,36(8):1287-1294.LIU H R,YANG L,TIAN H,et al.Mechanism of Lycium ruthenicum polyphenols against polystyrene-induced reproductive toxicity[J].Traditional Chinese Drug Research and Clinical Pharmacology,2025,36(8):1287-1294.
[45]GAO W Y.Exploitation potential and deep-rooted conformational relationships of traditional Chinese medicine polysaccharides[J].Chinese Herbal Medicines,2025,17(1):1-2.
[46]张心驰,惠和平,郭栋费,等.梯度醇沉兰州百合多糖结构及降血糖活性分析[J].精细化工,2023,40(10):2231-2240.ZHANG X C,HUI H P,GUO D F,et al.Analysis on structure and hypoglycemic activity of Lanzhou lily polysaccharides from gradient alcoholic precipitation[J].Fine Chemicals,2023,40(10):2231-2240.
[47]WANG T T,ZHU B J,ZHAO J,et al.Research progress in methods of acquisition,structure elucidation,and quality control of Chinese herbal polysaccharides[J].Chinese Journal of Natural Medicines,2025,23(2):143-157.
[48]李嘉懿,张红星,谢远红,等.益生菌发酵复方中草药产多糖的工艺优化[J].北京农学院学报,2018,33(3):83-87.LI J Y,ZHANG H X,XIE Y H,et al.Optimization of fermentation for producing polysaccharides from Chinese herbal by combined probiotics[J].Journal of Beijing University of Agriculture,2018,33(3):83-87.
[49]陈晓维,温靖,肖更生,等.乳酸菌混合发酵在红枣浆中的发酵特性研究[J].食品与发酵工业,2023,49(17):174-179.CHEN X W,WEN J,XIAO G S,et al.Fermentation characteristics of jujube pulp by mixed fermentation of lactic acid bacteria[J].Food and Fermentation Industries,2023,49(17):174-179.
[50]HUANG F,HONG R Y,ZHANG R F,et al.Physicochemical and biological properties of Longan pulp polysaccharides modified by Lactobacillus fermentum fermentation[J].International Journal of Biological Macromolecules,2019,125:232-237.
[51]CAO W J,LIU Y,ZHANG Z,et al.Lipid-lowering effects and metabolomic investigation of Polygonatum sibiricum fermented by Lactobacillus plantarum NX-1[J].Process Biochemistry,2025,153:102-109.
[52]HUANG G T,SU D X,LEE Y K,et al.Accumulation of water-soluble polysaccharides during lychee pulp fermentation with lactiplantibacillus plantarum involves endoglucanase expression[J].Journal of Agricultural and Food Chemistry,2025,73(6):3669-3679.
[53]GUO R,GUO S C,GAO X,et al.Fermentation of Danggui Buxue Tang,an ancient Chinese herbal mixture,together with Lactobacillus plantarum enhances the anti-diabetic functions of herbal product[J].Chinese Medicine,2020,15(1):98.
[54]郑苗,何佳,吕丹丹,等.怀山药乳酸菌饮品发酵工艺及其活性成分的研究[J].食品科技,2018,43(7):104-110.ZHENG M,HE J,LYU D D,et al.Study on fermentation technology and active components of Chinese yam Lactobacillus beverage[J].Food Science and Technology,2018,43(7):104-110.
[55]WANG W,WANG Y,PEI H Y,et al.The mechanism of simultaneous intake of Jujuboside A and B in the regulation of sleep at the hypothalamic level[J].Aging,2023,15(18):9426-9437.
[56]张政.乳酸菌发酵对酸枣仁营养成分及改善睡眠作用的影响[D].郑州:河南工业大学,2025.ZHANG Z.Effects of lactic acid bacteria fermentation on nutritional components and sleep-improving function of semen zizyphi spinosae [D].Zhengzhou: Henan University of Technology,2025.
[57]ZHENG Y F,TAN H Y,CHAI J Y,et al.Ginseng fruit rare saponins (GFRS) improved inflammatory response: in vitro and in vivo assessment[J].Fitoterapia,2024,179:106244.
[58]苏欣然,刘春莹,王越,等.两种林下参各部位皂苷的组成成分[J].大连工业大学学报,2018,37(1):19-22.SU X R,LIU C Y,WANG Y,et al.Components of ginsenoside in two types of wild ginseng[J].Journal of Dalian Dalian Polytechnic University,2018,37(1):19-22.
[59]叶楠.酿酒酵母异源合成稀有人参皂苷F2[D].天津:天津大学,2021.YE N.Heterologous synthesis of rare ginsenoside F2 by Saccharomyces cerevisiae[D].Tianjin: Tianjin University,2021.
[60]WU G Y,YI J Y,LIU L,et al.Pseudoginsenoside F11,a novel partial PPAR γ agonist,promotes adiponectin oligomerization and secretion in 3T3-L1 adipocytes[J].PPAR Research,2013,2013:701017.
[61]张玉梅.乳酸菌发酵西洋参总皂苷对辅助降脂的影响及饮料的研制[D].沈阳:沈阳农业大学,2024.ZHANG Y M.Effect of lactic acid bacteria fermented Panax quinquefolius total saponins on adjuvant lipid-lowering and development of beverage[D].Shenyang: Shenyang Agricultural University,2024.
[62]金玉洁.乳酸菌高密度培养及其对人参皂苷的发酵转化[D].杭州:浙江大学,2020.JIN Y J.High-density cultivation of lactic acid bacteria and its fermentation transformation of ginsenosides[D].Hangzhou: Zhejiang University,2020.
[63]PALANIYANDI S A,SON B M,DAMODHARAN K,et al.Fermentative transformation of ginsenoside Rb1 from Panax ginseng C.A.Meyer to Rg3 and Rh2 by Lactobacillus paracasei subsp.tolerans MJM60396[J].Biotechnology and Bioprocess Engineering,2016,21(5):587-594.
[64]CHEN Y Z,PENG Y H,LI P,et al.Ginsenoside Rg3 induces mesangial cells proliferation and attenuates apoptosis by miR-216a-5p/MAPK pathway in diabetic kidney disease[J].Aging,2024,16(11):9933-9943.
[65]BOASIAKO T A,BOATENG I D,MA Y K.Valorization of jujube puree using lactic acid bacteria and Acetobacter pasteurianus tri-cultured co-fermentation matrix: Insight into their nutritional,sensory,volatile and non-volatile metabolomics,and physicochemical properties[J].LWT,2025,218:117431.