高氯酸盐(ClO4-)是一种持久有毒的环境污染物,主要由自然和人工2个途径产生。自然环境下,大气中无机氯与臭氧发生光化学反应、紫外线辅助光氧化等过程产生的高氯酸盐会以气溶胶的形式存在大气中,最终通过降水等降到地表[1]。由于高氯酸盐有强氧化性和极其稳定特性,在国防研究、航空航天、漂白和消防设施制造中被广泛应用[2-5]。高氯酸盐极性较大,且易溶于水,会随着地下水和地表水迅速扩散,并通过多种途径进入人体内[6-9]。由于高氯酸盐的电荷和离子半径与碘化物相近,所以它能和碘化物争夺进入甲状腺的机会,进而影响甲状腺功能,阻碍碘化物摄取,间接导致甲状腺激素合成量降低[10-12],进而危及骨骼、大脑、其他腺体及生殖器官,影响人体机能正常运作。
为了保护公众健康,各监管机构设定了相关的安全标准。早在2005年,美国环境保护署(Environmental Protection Agency,EPA)规定了饮用水中高氯酸盐的参考限量为不得超过15 μg/L,这一标准是基于人体每日摄入限量0.000 7 mg/(kg·d)计算得出的[13]。而在2015年,欧洲食品安全局(European Food Safety Authority,EFSA)也更新了其科学意见,指出其在食品中的每日容许摄入量应为0.3 μg/kg[14]。GB 5749—2022《食品安全国家标准 生活饮用水卫生标准》和世界卫生组织(World Health Organization,WHO)[15]规定高氯酸盐限量为70 μg/L。
研究者们就食品中高氯酸盐含量的检测开展了大量工作,结果表明,饮用水、牛奶、啤酒、茶叶、谷物、水果和蔬菜等多种食品中都检出了高氯酸盐[16-23]。同时由于食品中的高氯酸盐浓度低,且基质复杂,干扰因素多,使得样品前处理成为检测的核心步骤,在检测前需对样品进行前处理,富集食品中高氯酸盐,去除干扰检测的物质,以确保检测结果的准确性,同时避免对仪器造成干扰。因此,本文综述了近年来食品样品中高氯酸盐的前处理技术和检测技术,为食品中高氯酸盐的检测及相关研究提供参考。
1 样品前处理技术研究进展
高氯酸盐的强极性、亲水性、化学惰性和热稳定性是其前处理方法设计的核心依据,其高度对称的四面体结构导致电荷高度分散,水合作用极强[2-5],这决定了其最优提取溶剂为高极性介质(如乙腈-水溶液),且在反相色谱系统中保留微弱。高氯酸盐分子结构稳定,难以发生氧化还原反应,这也决定了其在食品体系中的存在状态与分离难度。
有关高氯酸盐与食品基质的相互作用机制,目前暂没有详细地研究其与食品基质的相互作用,但可以从高氯酸盐的性质出发进行推论,因其稳定性和流动性,经自然活动主要分布在地下水、河流土壤中,最终通过灌溉等途径迁移并富集到植物性食品中[1],高氯酸盐更倾向于以自由水合离子的形态存在于含水量高的食品中,这一性质使得采用高极性溶剂(如水、乙腈-水或甲醇-水混合溶液)进行高效提取成为可能。
因碘离子与高氯酸盐的性质相似,且都与甲状腺健康相关,相关研究表明,海带中的碘主要以自由碘离子(I-)的形态存在(占比可达89%以上),而非牢固结合的有机碘,在漂烫、漂洗等加工过程中,碘离子会大量、快速地溶出到水中,其溶出规律符合自由扩散的动力学特征[24]。这有力地证明了碘离子在藻体基质中主要是以游离、可交换的状态存在,而非被紧密锁定。
其中SUN等[25]的研究表明,高氯酸盐在绿茶和红茶的加工(杀青、揉捻、发酵、干燥)过程中干重含量稳定,其在冲泡时具有高迁移率(平均74.1%,最高92.8%),这也支持其以自由离子形态存在,高水溶性、未与其他物质结合的离子才能在热水中快速大量溶出且与海带中碘离子的溶出相似。
综上所述,结合高氯酸盐自身的性质、碘离子在海带中存在方式及其加工溶出和茶叶中高氯酸盐的迁移性等特点,推断出高氯酸盐在食品基质中主要以其自由水合离子的形态存在,这决定了它易于被高极性溶剂提取、在加工过程中稳定以及在冲泡时高效浸出的行为特性。
针对不同基质特性与分析需求,目前已发展出多种前处理技术,主要包括四类方法,表1综合比较了不同前处理方法的优缺点、适用食品基质以及与其匹配的检测技术。
表1 食品中样品前处理技术以及优缺点
Table 1 Sample pretreatment technology and advantages and disadvantages in food

1.1 冷冻诱导液液萃取(cold-induced liquid-liquid extraction,CI-LLE)
CI-LLE是在液液萃取技术上发展起来的一种新方法,这种方法操作简单且不需要使用过多的仪器以及大量的化学试剂和耗材,是一种快速、低成本且环境友好的样品前处理方法。在1996年,这种低温的方法用于沉淀蛋白质和脂肪,是一种作为辅助的纯化方式[26]。其原理为:当温度低于乙腈的临界溶解温度(-1.32 ℃)时,其在水相中的溶解度会降低[27]。因此,使用乙腈和水基质形成均匀的提取物,这种提取物通过CI-LLE预处理进而分离。使用CI-LLE方法,大量的目标分析物高氯酸盐会保留在上层的乙腈相中,此外,乙腈会引起脂肪和蛋白质的凝固与沉淀,使用低温沉淀可将其去除(图1-a下)。经过大量的研究者不断地探索,将这种前处理方法的应用范围进一步扩大,目前已应用于乳及乳制品、茶叶、蜂蜜等样品。LI等[27]通过CI-LLE有效的提取茶和乳制品中的高氯酸盐,减少了潜在的基质干扰。优化前处理条件后,在基质效应和萃取回收率的折衷下,高氯酸盐的富集倍数增加了7.79倍,茶和乳制品中高氯酸盐的加标回收率为78.2%~106.2%,加标回收率高。林强等[28]通过CI-LLE快速检测液态奶中的高氯酸盐。奶样使用乙腈提取,离心取出上清液-20 ℃冷冻30 min,吸取上层液体测定。结果显示高氯酸盐在0.2~100.0 ng/mL范围内线性关系良好,所建立的基于CI-LLE检测高氯酸盐的前处理方法,富集效果好,加标回收率高。此外,也有研究者将CI-LLE成功应用于蜂蜜中高氯酸盐的检测,在蜂蜜样品中加入超纯水,漩涡振荡至完全溶解,加入乙腈,涡旋混合后离心,移至-20 ℃冷冻分层,取上清液进行测定[29]。通过CI-LLE,除去了蜂蜜中的葡萄糖和果糖,富集了样品中的高氯酸盐,方法线性范围好,加标回收率在96.7%~102.3%。
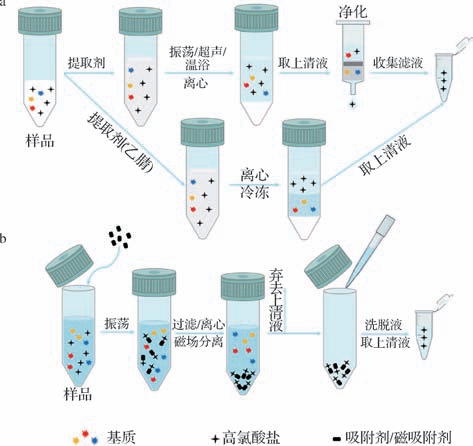
图1 样品前处理流程示意图
Fig.1 Schematic diagram of the sample pretreatment procedure
a-样品除杂净化示意图;b-样品分离提取示意图
选择CI-LLE方法处理乳制品、蜂蜜和茶叶中的高氯酸盐,主要基于以下方面的依据:利用高氯酸盐在乙腈/水中的溶解性差异及水/乙腈的凝固点差异实现分离与富集,可针对性去除不同基质(如乳中的蛋白脂肪、蜜中的糖类)的干扰。
CI-LLE前处理方法是利用水在低温下冻结,而有机相及溶于其中的目标物仍为液体的原理,实现相分离和富集。其主要优势:(1)操作简单快速:避免了复杂的SPE柱活化、上样、淋洗、洗脱等步骤。(2)成本低廉:无需使用SPE小柱。(3)适用于复杂基质:能有效处理像牛奶这样富含蛋白质和脂肪的样品。
但其仍存在一定的局限性,如:(1)净化能力有限:对于极度复杂或高脂的样品,可能需要结合其他净化手段。(2)方法优化需求:冷冻时间、温度、溶剂比例等参数需要针对不同基质进行优化,以确保水相完全凝固和有机相的充分回收。(3)前处理过程耗时较长:相对于使用QuEChERS净化的方法,需要在-20 ℃或低于-20 ℃冷冻较长时间,才能够保证高的回收率。
总之,CI-LLE因其通过物理冷冻实现净化和富集的原理,适合处理像乳制品、果蔬、饮料等高水分复杂食品基质中的高氯酸盐。它能够提供纯净的样品,适合抗干扰能力强的色谱-质谱联用技术[离子色谱-串联质谱法(ion chromatography tandem mass spectrometry,IC-MS/MS)、液相色谱-串联质谱法(liquid chromatography-tandem mass spectrometry,LC-MS/MS)],充分发挥其简单、快速、低成本的优势。
1.2 固相萃取(solid phase extraction,SPE)
SPE技术的核心原理是将液相色谱的固定相填料微型化地装填于一个带有筛板的塑料柱管中,通过模拟色谱分离过程,使样品溶液在真空或压力作用下流经固定相,经历“活化-上样-淋洗-洗脱”的标准流程,利用分析物、干扰物与固定相之间不同的吸附、分配、离子交换等相互作用力,实现目标物的选择性保留、杂质洗脱和目标物洗脱,从而达到净化和富集的目的[30]。SPE尤其适用于高色素、高蛋白或高油脂等复杂食品基质(如茶叶、咖啡、乳制品等)中高氯酸盐的净化。选择其依据在于:SPE可依据填料特性针对性吸附脂质、色素、蛋白质及有机酸等干扰物,从而实现高效净化(图1-a上);也可依据填料特异性选择吸附高氯酸盐,洗脱后收集洗脱液并分析。其吸附原理为:利用离子交换作用,使带负电的高氯酸盐与吸附剂上的正电官能团发生静电结合[31]。ZHANG等[32]在咖啡中高氯酸盐的检测中系统比较了(enhanced matrix removal,EMR)、(graphitized carbon black,GCB)及(mixed-mode cation exchange,MCX)3种SPE柱,最终优选MCX柱作为净化材料,因其在有效去除色素的同时显著降低了基质抑制效应,表现出良好的准确度与重现性,且该方法操作简便、成本较低,已实现商品化,便于实际应用。詹胜群等[33]通过比较初滤液(首1 mL)与续滤液中高氯酸盐的测定结果,发现(hydrophilic lipophilic balance,HLB)小柱在初始阶段对目标物存在可逆吸附,但对最终结果无显著影响,该结果明确了弃去初滤液以保障检测准确性的必要性。在茶叶等色素及多酚含量较高的样品前处理中,多数学者选用GCB小柱进行净化[34-36],主要基于其对色素、黄酮类干扰物的高效保留能力[37]。
SPE可实现净化与分离同步,显著降低基质干扰,被国家标准GB 5009.291—2023《食品安全国家标准 食品中氯酸盐和高氯酸盐的测定》推荐为高氯酸盐测定的前处理方法。其主要优势为:(1)商业化程度高:市面上有各种SPE小柱,如用与净化去除干扰物质的GCB、HLB和C18(bonded silica solid-phase extraction cartridge)等,净化效果好;特异性保留并吸附高氯酸盐的PAX(polymer-based anion exchange)、WAX(weak anion exchange)和SAX(strong anion exchange)等SPE柱。(2)适合各类样品,可针对样品基质选择合适的SPE小柱。然而,使用SPE柱会增加检测费用、多为一次性且通常不可重复使用,在一定程度上增加了检测成本。
该技术与IC-MS/MS和LC-MS/MS匹配度高,净化后的样品能显著降低离子抑制及基质效应,提高检测灵敏度与准确性,是复杂食品样品痕量高氯酸盐检测的理想前处理手段之一。
1.3 QuEChERS与分散固相萃取(dispersive solid phase extraction,DSPE)
在2003年提出的一种Quick Easy Cheap Effective Rugged and Safe(QuEChERS)的制备技术,这种技术快速、简便、廉价、有效、坚固且安全。QuECh-ERS技术最初用于食品农药残留分析[38],然而,为应对样品前处理技术的高通量、低成本的需求,广大研究者开始将改进的QuEChERS技术用于提取不同食品基质中的高氯酸盐。选择这种样品前处理依据为:QuEChERS可根据不同食品基质设计不同前处理方法,选择合适的提取溶剂和吸附剂,可检测的食品种类广泛。QuEChERS解决了SPE核心痛点,主要将前处理过程解构为2个清晰独立的步骤:第一步是萃取与相分离,使用乙腈等有机溶剂作为萃取剂,沉淀蛋白质并高效萃取富集高氯酸盐。第二步是DSPE富集或净化,吸附剂主要分为2个类型,一种方式是使用较多且商业化程度高的,主要作用为除杂净化,其通过涡旋使吸附剂分散并与基质干扰物充分作用,再通过离心去除吸附剂和被吸附的杂质,取上清液即可进行分析。如DONG等[39]以1%甲酸-乙腈溶液作为提取剂对样品进行处理,超声辅助提取后离心,选择(primary secondary amine,PSA)、GCB和C18填料混合使用用于净化,发现PSA效果较差,最终确定使用100 mg C18和40 mg GCB作为吸附剂组合,能有效去除果蔬基质中的干扰物,提高目标离子的回收率,并降低基质效应,满足LC-MS/MS高灵敏度检测的要求。张小刚[40]通过优化乙腈的比例,采用最佳的萃取体积比为V(乙腈)∶V(水)=1∶1,最佳吸附剂组合与用量为100 mg C18和100 mg GCB,检测结果准确。这种方式的核心优势为:(1)操作简便高效:流程简单,省去了传统SPE柱所需的活化、平衡、上样、淋洗、洗脱等繁琐步骤,大大缩短了前处理时间,适用的食品种类广泛。(2)成本低廉:所使用的吸附剂(如C18、GCB)商业化程度高,价格低于单独购买的SPE小柱,适合大规模批量样品检测,降低了单样检测成本。但其最佳吸附剂种类和用量需要根据不同的样品基质进行实验优化,不能一概而论,增加了方法开发的工作量。
另外一种的作用机理为分离提纯,通过振荡的方式使目标分析物与吸附剂结合,再通过过滤或离心分离吸附剂与待测溶液,随后用相对少量的洗脱液洗脱(图1-b)。如韦昱等[41]将茶叶样品使用乙腈提取,以PSA和(polymer-based cation exchange,PCX)为吸附填料吸附高氯酸盐,首先通过涡旋的方式使提取液中的高氯酸盐吸附在吸附剂上,选择5%的氨水溶液洗脱,离心之后取上清液测定。该方法展现出良好的线性关系和高加标回收率,具有操作便捷、成本经济、净化效果显著等优势,适用于茶叶中高氯酸盐的检测。这种“吸附-洗脱”式DSPE是一种更具针对性、选择性和灵敏度的前处理策略,它牺牲了部分操作简便性和通用性,换来了更强的净化能力和富集效果,特别适合用于复杂基质中超痕量特定目标物的检测,尤其适用于LC-MS/MS。
1.4 磁固相萃取(magnetic solid phase extraction,MSPE)
MSPE的原理为:其是一种利用磁性材料作为吸附剂的样品前处理方法,结合了SPE和磁性分离技术的优点。MSPE是DSPE的改进形式,磁性吸附剂在溶液中分布均匀,使吸附剂与目标分析物在摇动的过程中充分接触,并且与DSPE相比,使用磁性分离代替离心或过滤阶段显著减少了样品制备过程所消耗的时间。MSPE适合高离子强度、多干扰物的食品样品(如蔬菜、茶叶、饮料等),选择MSPE的依据在于:磁性吸附剂可通过表面官能团针对性地吸附高氯酸盐,并借助外磁场实现快速分离,有效克服传统离心、过滤中的堵塞和损失问题,大大提高前处理效率。
在基于MSPE的高氯酸盐分析中,多种功能化磁性吸附材料展现出良好的应用潜力。XIE等[42]、KRISHNAN等[43]与SONG等[44]分别研制了交联磁性壳聚糖/聚乙烯醇珠、磁性复合气凝胶及改性磁性生物高分子离子交换树脂,这些材料不仅具有高饱和吸附量,还可借助外部磁场实现快速分离,并能够通过盐溶液再生,具有良好的重复使用性能,尤其适用于环境水样中高氯酸盐的富集与净化。对于茶叶等复杂食品基质,MSPE技术同样适用。ZHAO等[45]合成了季铵化修饰的磁性羧基碳纳米管,用于茶叶中高氯酸盐的萃取净化:样品经1%(体积分数)甲酸溶液均质提取并合并上清液后,加入磁性羧基碳纳米管进行吸附,经磁性分离和洗涤后,采用5% 氨水溶液洗脱,最终使用LC-MS/MS进行分析。该方法在最佳条件下萃取效率高,回收率达85.2%~107.0%,已成功应用于实际茶叶样本的风险监测,表明其在复杂食品体系中也具备良好的适用性与可靠性。
其相对于其他方法的主要优势有:(1)具有高比表面积和高吸附容量,能够有效富集目标物。(2)操作步骤简单,无需复杂的设备;(3)磁性材料可以多次使用,通过简单的再生步骤(如洗脱和干燥)即可恢复其吸附性能,如ZHAO等[43]合成的磁性羧基碳纳米管可重复使用20次,降低了分析成本。但其仍存在局限性:吸附剂的商业化程度较低,多为研究者自制,合成的过程较为繁琐,且需要特定的仪器表征其是否合成成功。
此外,MSPE与LC-MS/MS或IC-MS/MS等高灵敏度、高选择性方法的联用契合度高,磁性材料特异性吸附高氯酸盐能够显著降低基质效应,提升检测准确度和重复性,适合于痕量高氯酸盐的系统分析。
2 食品中高氯酸盐检测方法研究进展
高氯酸盐广泛存在于不同食品样品中,精确检测对于高氯酸盐的毒理学研究、环境及食品安全监管及生命健康保障意义重大。目前,检测食品中高氯酸盐的方法主要包括离子色谱法(ion chromatography,IC)、离子色谱-串联质谱法(IC-MS/MS)、液相色谱-串联质谱法(LC-MS/MS)、表面增强拉曼散射法(surface-enhanced raman scattering,SERS)等[46]。表2为不同方法检测高氯酸盐的比较,总结了不同方法的核心优势及其局限性,同时也概述了其适用场景。
表2 食品中高氯酸盐检测方法总结及优缺点
Table 2 Summary of detection methods and their advantages and disadvantages for perchlorate in food

2.1 离子色谱法
离子色谱法检测高氯酸盐主要基于离子交换原理。高氯酸盐在离子色谱柱中与固定相发生离子交换作用,不同离子因电荷和亲和力差异实现分离。分离后的离子通过电导检测器检测,电导变化与离子浓度成正比,进而实现高氯酸盐的定性和定量分析。无机非金属指标:GB/T 5750.5—2023《生活饮用水标准检验方法》规定了3种检测高氯酸盐的方法,分别为离子色谱法-氢氧根系统淋洗液、离子色谱法-碳酸盐系统淋洗液和超高效液相色谱串联质谱法,其中两种使用离子色谱法检测水中的高氯酸盐。
IC检测水样中高氯酸盐的应用中,研究者通常采用0.22 μm滤膜过滤后直接进样分析,该方法操作简便、结果准确,具有良好的线性范围与加标回收率[47-49]。为进一步提高检测结果的准确性,李婷婷等[50]在饮用水分析中采用Ag柱与H柱去除常见干扰离子,SEILER等[51]则采用OnGuard ⅡBa/Ag/H三层柱去除碳酸盐、氯化物、硫酸盐及金属离子。在蔬菜和水果等复杂基质中,IC法也可通过样品匀浆、提取、离心等前处理步骤实现准确测定,该方法线性良好,回收率达80%~ 120%,灵敏度高,重复性良好,适用于该类食品中高氯酸盐的检测[52-53]。
IC的优势根植于其分离机制——离子交换色谱与化学抑制型电导检测器的联用,对高氯酸盐等阴离子具有天然的高选择性和高灵敏度。其方法开发相对成熟、运行成本低廉,使其成为常规筛查和合规性检测(尤其对于基质简单的饮用水和某些液体食品)的经济高效的方法。其局限性主要来自于电导检测的特异性不足。在复杂食品基质(如牛奶、茶叶、果蔬)中,高浓度的共存离子(如氯酸盐、硝酸盐、硫酸盐等)会对检测造成干扰,即便通过优化色谱柱和淋洗液程序也难以完全分离,这导致其方法检出限在实际样品中显著升高,灵敏度偏低,并存在假阳性的风险。
IC的价值在于其标准化和低成本。然而,当今对食品安全的要求日益苛刻(检测限要求低至μg/kg甚至ng/kg级别)的背景下,IC更适用于:(1)初级筛查:对大量阴性样品进行快速排除。(2)基质简单样品的定量:如瓶装水、饮料等。
2.2 离子色谱-串联质谱法
由于离子色谱法在检测食品有一定的局限性,一些研究者通过串联质谱的多级分析,能够有效减少基质干扰,提高检测的准确性和可靠性。通过离子色谱法的高效的分离特性,可以将样品中的高氯酸盐离子与其他离子分离开,分离后的高氯酸根离子进入质谱检测器,进而实现了高氯酸盐的定性和定量分析。IC-MS/MS检测的食品种类更多,检出限较IC降低明显。
IC-MS/MS在检测水和饮料等样品中的高氯酸盐,前处理方法简单[54-56]。水样一般无需溶剂提取,如碳酸饮料需经过超声处理去除二氧化碳气体,需用预处理柱去除水样的色素,例如Na/H型预处理柱和OnGuard ⅡRP柱。如ZHANG等[57]在测定冲泡后的咖啡样品中,使用乙腈震荡提取,用于沉淀样品中的蛋白质,选择MCX柱用于去除咖啡中的色素,方法线性范围良好,回收率高,适合咖啡制品的检测。
张志敏等[58]在3种色谱柱中选择了分离效果更好AS20色谱柱,提出了使用纯水3次浸泡20 min提取茶叶,可以提取出茶叶中的高氯酸盐,最终取混合后的上清液经OnGuard ⅡRP-1cc柱处理用来排除其他物质的干扰。有良好的线性关系,加标回收率分别为94.6%~133%,定量限为6 μg/kg,该方法应用到不同种类茶叶均可检测出高氯酸盐,重现性好。NOBILE等[59]采用甲醇/1% 甲酸水溶液提取乳中的高氯酸盐,经过涡旋、超声和离心处理后,取上清液过滤,使用离子色谱-高分辨质谱进行分析,通过选择性离子监测模式进行全扫描采集。方法检测限为10 ng/g,线性范围0.5~ 100 ng/g,相关系数大于0.99,可以准确检测生牛乳中的高氯酸盐。多数研究者建立的前处理方法只应用于某一类的食品样品,没有普适性,GARVEY等[60]则建立了牛奶/婴儿配方奶粉、谷物、水果和蔬菜中高氯酸盐的检测方法,依据不同食品基质设计了相应的前处理流程,包括提取、净化和稀释等步骤,高氯酸盐的回收率在82.0%~99.5%,线性范围0.1~200 mg/L,相关系数0.9992,适用于多种食品中高氯酸盐的检测。
IC-MS/MS结合了IC的高效分离能力与MS/MS的定性和定量能力,三重四极杆质谱通过选择反应监测模式,利用母离子-子离子对进行检测,几乎彻底消除了基质干扰,结果准确度高。局限性在于其仪器购置和维护成本高昂、操作复杂以及对技术人员专业技能的要求高。此外,虽然基质效应被大幅抑制,但并未完全消除,仍然需要采用同位素内标法来进行精确校正,这进一步增加了检测成本。
IC-MS/MS是目前广泛用于检测高氯酸盐的方法,主要是应对复杂基质、痕量检测和科研溯源需求的技术。其发展趋势主要体现在:(1)方法的标准化与推广:如何将其从实验室推向更多常规检测机构;(2)前处理流程的优化:开发更快速、更环保、回收率更高的样品前处理方法,以匹配其高速的分析能力。
2.3 液相色谱-串联质谱法
液相色谱-串联质谱法(LC-MS/MS)作为我国GB 5009.291—2023《食品安全国家标准 食品中氯酸盐和高氯酸盐的测定》标准中规定的食品中高氯酸盐检测方法,该方法通过液相色谱系统实现高氯酸盐与基质干扰物的高效分离,再经串联质谱在选择性反应监测模式下对特征母离子-子离子对进行检测,兼具高灵敏度与高选择性,可有效克服复杂食品基质干扰,实现痕量级高氯酸盐的准确定量。
在应用研究中,SUN等[25] 建立了基于PWAX(polymer-based weak anion exchange)固相萃取柱富集、5%氨水-甲醇溶液洗脱的前处理方法,结合LCMS/MS分析了茶叶加工及冲泡过程中高氯酸盐的迁移规律,为茶叶质量安全控制提供科学依据。WANG等[61]则依据食品基质水分含量的不同设计差异化的提取方案,高水分样品使用V(甲醇)∶V(水)=3∶1,低水分样品使用V(甲醇)∶V(水)=3.5∶1进行提取,并借助同位素内标法进行定量,回收率为90.54%~101.80%,RSD低于5.05%,方法稳健,重现性良好。
LC-MS/MS能够检测到极低浓度的高氯酸盐,适用于痕量分析、可以有效区分高氯酸盐与其他干扰物质,确保检测结果的准确性、适用于多种食品基质中高氯酸盐的检测。
然而,也需客观认识到该方法的局限性:(1)仪器设备昂贵、维护成本高,对操作人员专业水平要求较高;(2)尽管SRM模式和同位素内标可显著抑制基质效应,但对于一些极端复杂的样品(如深色酱料、动物内脏等),仍需结合更强效的净化手段或进一步优化色谱分离条件。
2.4 SERS
SERS是一种先进的光谱技术,通过将样品吸附于具有纳米结构的金属表面(例如银、金或铜),能够显著增强拉曼散射信号。当高氯酸盐吸附在这些金属表面时,其拉曼信号可增强104~1015倍。
由于高氯酸盐的对称伸缩振动频率具有拉曼活性,以SERS技术为基础建立的快速定量测定高氯酸盐的方法,灵敏度高、选择性好、检测快速、前处理简单、底物环保。HAO等[62]采用银纳米薄膜基底,实现了对高氯酸盐水溶液的快速SERS检测,其检测限可低至5 μg/L。此外,SERS技术还被成功应用于基质较为复杂的茶叶样品中,GUO等[63]合成了一种结构简单、灵敏、稳定的SERS疏水基底,用于检测茶叶样品。通过合成了银膜/聚二甲基硅氧烷底物,用于SERS测量。茶叶样品粉碎后,加入浓硝酸密封静置后,将混合物进行消解,消解后冷却,清洗,脱气,进行定容用于测定。在激发波长为532 nm的条件下,建立了光谱强度与高氯酸盐浓度之间线性关系,线性关系良好,检出限为0.82 μg/kg,具有很高的灵敏度。
SERS技术与传统方法如IC-MS/MS及LC-MS/MS相比,虽然在前处理简便性和检测速度上具有一定优势,但在定量准确性、方法验证全面性和实验室间重现性方面仍存在较大差距。此外,现有SERS研究多侧重于单一基质或理想条件下的检测性能,缺乏不同基质的验证研究,也尚未建立起统一的SERS方法标准与验证规范。
因此,未来SERS技术在高氯酸盐检测领域的发展应重点关注以下方向:(1)深入研究高氯酸盐与不同SERS基底的相互作用机制及信号增强规律。(2)开发功能化基底材料,提升其抗干扰能力和重现性。(3)明确SERS在不同食品基质中的适用性与局限性,定位其适用范围。
2.5 其他方法
除了上述常用的检测方法外,分光光度法和纸基分析设备也应用于食品中高氯酸盐的检测。SUN等[64]建立了碱性亚甲基蓝和液-液萃取检测水溶液中高氯酸盐的高选择性灵敏方法。依据碱性MB遇高氯酸盐水溶液时,在有机溶剂中会由红变蓝。在最佳条件下,600 nm处紫外-可见吸光度与高氯酸盐浓度在0.002 5~ 0.025 mmol/L范围内呈良好线性(R2=0.994 5),水样和红茶浸液中视觉检测限分别为0.005、0.02 mmol/L,方法经济简便。KUMAR等[65]通过简单的样品处理和基于甲基蓝与高氯酸根离子相互作用的检测原理,开发了一种快速、低成本的纸质微流控平台,用于检测水样中的高氯酸盐。该方法具有良好的线性响应、较低的检测限和定量限,且具有较好的稳定性和特异性,为现场快速检测水中的高氯酸盐提供了一种有效的解决方案。也有荧光探针通过AIE等机制与高氯酸盐发生特异性相互作用,实现了高灵敏度、强抗干扰性的检测,但在复杂食品基质中的应用仍面临挑战[46]。
总体来看,分光光度法和荧光探针检测为高氯酸盐的检测提供了快速、低成本的补充手段,尤其适合现场初筛和大样本筛查。但在实际应用中,仍需结合样品基质复杂程度、准确度要求及设备条件进行方法选择与验证。未来研究可着眼于提高纸基设备的定量性能、开发抗干扰能力更强的识别体系,以及推动多种检测技术的集成化与实用化。
3 总结与展望
高氯酸盐作为一种在食品中广泛存在的持久性污染物,通过食物链进入人体并在体内富集会对人体健康造成潜在危害,因此建立准确、高效的检测方法具有重要意义。本文通过对近年来检测食品中高氯酸盐相关文献进行整理,样品前处理作为食品中高氯酸盐检测的重要部分,影响着检测结果的准确性。当前常用的CI-LLE、QuEChERS和DSPE、SPE及MSPE等技术虽能实现有效的富集与净化,但仍存在一定的局限性:液相萃取有机溶剂消耗量大,存在安全与环境隐患;而固相萃取吸附剂通用性有限,往往需要多种技术联用以提高萃取效率。针对现有技术的不足,提出以下发展方向:
在前处理技术方面,应致力于开发高效、高选择性的新型吸附材料(如针对高氯酸盐具有特异性识别能力的吸附剂),以优化 QuEChERS、DSPE和MSPE等方法的过程效率,减少有机溶剂用量、简化操作流程并提高净化效果。建立针对不同食品基质的标准化前处理程序,有效去除干扰物质,为后续检测提供保障。同时,推进前处理过程的自动化,并开发自动化平台,实现高通量、低成本的样品制备,满足大规模监测需求。
在检测方法方面,应在保证准确性的基础上,提高方法的实用性和经济性。一方面,推动IC-MS/MS和LC-MS/MS等标准检测方法向便捷化、低成本化方向发展;另一方面,重点探索高氯酸盐的快速检测技术路线,深入研究基于特异性识别高氯酸盐的荧光探针检测和纸基分析设备在快速筛查中的应用潜力。通过将优化的前处理程序与这些快速检测技术相结合,最终实现适用于现场快速检测的高氯酸盐试剂盒的开发,建立从样品前处理到检测的一体化、标准化解决方案。
总之,通过发展绿色、高效、自动化的前处理技术,并结合高灵敏、高选择性且易于推广的检测方法,构建适用于复杂食品基质与现场快速筛查不同需求的综合检测方案。特别是通过开发标准化、一体化的快速检测试剂盒,将为食品中高氯酸盐的风险监测与管控提供更加经济、高效、可靠的技术支持,从而为保障食品安全和公众健康提供有效技术保障。
[1]方齐乐,陈宝梁.环境中高氯酸盐的自然来源、形成机制及其归趋行为[J].化学进展,2012,24(10):2040-2053.FANG Q L,CHEN B L.Natural origins,formation mechanisms,and fate of environmental perchlorate[J].Progress in Chemistry,2012,24(10): 2040-2053.
[2]SAI K,SOUNDARAJAN M,SELVARAJ K R,et al.A concise overview of perchlorate sources,contamination,and remediation techniques[J].Bioremediation Journal,2024,28(4):530-540.
[3]NIZIN'SKI P,BŁA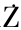 EWICZ A,KON'CZYK J,et al.Perchlorateproperties,toxicity and human health effects: An updated review[J].Reviews on Environmental Health,2021,36(2):199-222.
EWICZ A,KON'CZYK J,et al.Perchlorateproperties,toxicity and human health effects: An updated review[J].Reviews on Environmental Health,2021,36(2):199-222.
[4]KIRK A B.Environmental perchlorate: Why it matters[J].Analytica Chimica Acta,2006,567(1):4-12.
[5]MATAMOROS V,ARIAS C A,NGUYEN L X,et al.Occurrence and behavior of emerging contaminants in surface water and a restored wetland[J].Chemosphere,2012,88(9):1083-1089.
[6]CALDERÓN R,PALMA P,ARANCIBIA-MIRANDA N,et al.Occurrence,distribution and dynamics of perchlorate in soil,water,fertilizers,vegetables and fruits and associated human exposure in Chile[J].Environmental Geochemistry and Health,2022,44(2):527-535.
[7]MAFFINI M V,TRASANDE L,NELTNER T G.Perchlorate and diet: Human exposures,risks,and mitigation strategies[J].Current Environmental Health Reports,2016,3(2):107-117.
[8]CALDERÓN R,GODOY F,ESCUDEY M,et al.A review of perchlorate (ClO4-) occurrence in fruits and vegetables[J].Environmental Monitoring and Assessment,2017,189(2):82.
[9]STEINMAUS C M.Perchlorate in water supplies: Sources,exposures,and health effects[J].Current Environmental Health Reports,2016,3(2):136-143.
[10]PEARCE E N,LEUNG A M,BLOUNT B C,et al.Breast milk iodine and perchlorate concentrations in lactating Boston-area women[J].The Journal of Clinical Endocrinology &Metabolism,2007,92(5):1673-1677.
[11]DOHÁN O,PORTULANO C,BASQUIN C,et al.The Na +/I symporter (NIS) mediates electroneutral active transport of the environmental pollutant perchlorate [J].PNAS2007,104 (51):20250-20255.
[12]周冰洁.高氯酸盐对甲状腺细胞能量代谢的扰动效应研究[D]武汉:武汉轻工业大学,2024.ZHOU B J.Study on the perturbation effect of perchlorate on energy metabolism of thyroid cells[D].Wuhan:Wuhan Polytechnic University,2024.
[13]KUCHARZYK K H,CRAWFORD R L,COSENS B,et al.Development of drinking water standards for perchlorate in the United States[J].Journal of Environmental Management,2009,91(2):303-310.
[14]European Food Safety Authority.Scientific opinion on the risks to public health related to the presence of perchlorate in food,in particular fruits and vegetables[EB/OL](2014-10-17).[2019-11-06].https://doi.org/10.2903/j.efsa.2014.3869.
[15]COTRUVO J A.2017 WHO guidelines for drinking water quality:First addendum to the fourth edition[J].Journal AWWA,2017,109(7):44-51.
[16]LIU Y,SUN H Z,ZHOU L,et al.Quantitative determination and contamination pattern of perchlorate in tea by ultra performance liquid chromatography and tandem mass spectrometry [ J].Food Chemistry,2019,274:180-186.
[17]LIANG Y B,ZHOU L,ZHANG X Z,et al.Uptake,accumulation,translocation,and subcellular distribution of perchlorate in tea (Camellia sinensis L.) plants[J].Journal of Agricultural and Food Chemistry,2021,69(16):4655-4662.
[18]YAO Q H,YAN S N,LIU W J,et al.Perchlorate contamination of tea leaves and a corresponding probabilistic dietary risk assessment using Monte Carlo simulation[J].Food Additives &Contaminants: Part A,2022,39(2):341-350.
[19]KUMAR P,RAGHUNATHAN M.A review on the detection of perchlorate in water and food samples,health impacts,and analytical methods[J].Water,Air,&Soil Pollution,2025,236(3):174.
[20]CHEN Y N,ZHANG H,GE Y M,et al.Perchlorate in foodstuffs from South China and its implication for human dietary exposure[J].Food and Chemical Toxicology,2024,191:114876.
[21]LIU X,HAN H,XU H,et al.Integration of probabilistic exposure assessment and risk characterization for perchlorate in infant formula and supplementary food[J].Food and Chemical Toxicology,2022,168:113347.
[22]黄彬红.婴幼儿配方奶粉中氯酸盐和高氯酸盐污染情况的调查分析[J].中国乳品工业,2024,52(3):30-35.HUANG B H.Investigation analysis of pollution of chlorate and perchlorate in infant formula[J].China Dairy Industry,2024,52(3):30-35.
[23]康婕,陈鸿剑,李媛,等.羊乳制品中高氯酸盐污染来源分析[J].中国乳品工业,2024,52(4):45-49.KANG J,CHEN H J,LI Y,et al.Source analysis of perchlorate pollution in sheep dairy products[J].China Dairy Industry,2024,52(4):45-49.
[24]赵茹月,于源,张雅婷,等.海带漂烫-盐渍加工过程中碘形态含量变化规律[J].食品科学,2024,45(1):75-81.ZHAO R Y,YU Y,ZHANG Y T,et al.Changes of iodine speciation content in kelp during blanching-salting processing[J].Food Science,2024,45(1):75-81.
[25]SUN H Z,LIANG Y B,QI P P,et al.Transfer and risk assessment of perchlorate during green/black tea processing and brewing[J].Food Research International,2025,201:115579.
[26]OENCE D N,GU T Y.Liquid-liquid equilibrium of the acetonitrile-water system for protein purification[J].Separations Technology,1996,6(4):261-264.
[27]LI S H,REN J,ZHANG Y P,et al.A highly-efficient and costeffective pretreatment method for selective extraction and detection of perchlorate in tea and dairy products[J].Food Chemistry,2020,328:127113.
[28]林强,杨超,李美丽,等.冷冻诱导液液萃取-超高效液相色谱-四极杆静电场轨道阱高分辨质谱法检测液态奶中氯酸盐和高氯酸盐[J].食品安全质量检测学报,2022,13(10):3259-3265.LIN Q,YANG C,LI M L,et al.Determination of chlorate and perchlorate in liquid milk by freeze induced liquid-liquid extraction-ultra performance liquid chromatography-quadrupole-orbitrap high resolution mass spectrometry[J].Journal of Food Safety and Quality,2022,13(10):3259-3265.
[29]FEI Z X,SUN M Y,SONG Q,et al.Freezing-assisted sugaringout liquid-liquid extraction coupled with LC-MS/MS for quantitative determination of perchlorate in honey[J].Food Chemistry,2024,435:137604.
[30]MPUPA A,SELAHLE S K,MIZAIKOFF B,et al.Recent advances in solid-phase extraction (SPE) based on molecularly imprinted polymers (MIPs) for analysis of hormones[J].Chemosensors,2021,9(7):151.
[31]MEDINA V F,LARSON S L,EXTINE B,et al.Perchlorate analysis using solid-phase extraction cartridges[J].Journal of Chromatographic Science,2005,43(4):195-200.
[32]ZHANG H,FENG X Q,LIU D Y,et al.A HILIC LC-MS/MS method for the determination of perchlorate and Chlorate in coffee samples[J].Microchemical Journal,2022,181:107822.
[33]詹胜群,张浩,周钧,等.超高效液相色谱-串联质谱法测定婴幼儿配方乳粉中氯酸盐和高氯酸盐[J].食品科技,2022,47(1):312-318.ZHAN S Q,ZHANG H,ZHOU J,et al.Determination of chlorate and perchlorate in infant formula milk powder by UPLC-MS/MS[J].Food Science and Technology,2022,47(1): 312-318.
[34]陈东,范赛,沙博郁,等.超高效液相色谱-串联质谱法测定茶叶中高氯酸盐[J].食品安全质量检测学报,2018,9(4):925-929.CHEN D,FAN S,SHA B,et al.Determination of perchlorate and chlorate in drinks by ultra-performance liquid chromatography-tandem mass spectrometry[J].Journal of Food Safety &Quality,2018,9(4): 925-929.
[35]华永有,李宇翔,林宏琳,等.茶叶中高氯酸盐检测与污染情况分析[J].海峡预防医学杂志,2018,24(1):4-6;12.HUA Y Y,LI Y X,LIN H L,et al.Detection and pollution analysis of perchlorate in tea[J].Strait Journal of Preventive Medicine,2018,24(1):4-6;12.
[36]李雨哲,杨杰,王雨昕,等.同位素稀释-超高效液相色谱-串联质谱法测定茶叶中的高氯酸盐[J].中国食品卫生杂志,2016,28(5):616-619.LI Y Z,YANG J,WANG Y X,et al.Detection of perchlorate in tea by ultra high performance liquid chromatography with tandem mass spectrometry and isotope dilution method[J].Chinese Journal of Food Hygiene,2016,28(5): 616-619.
[37]曾艳,郞红,邵辉,等.茶叶中高氯酸盐检测方法研究进展[J].分析测试技术与仪器,2019,25(3):175-181.ZENG Y,LANG H,SHAO H,et al.Research progress on detection methods of perchlorate in tea[J].Analysis and Testing Technology and Instruments,2019,25(3):175-181.
[38]ANASTASSIADES M,LEHOTAY S J,STAJNBAHER D,et al.Fast and easy multiresidue method employing acetonitrile extraction/partitioning and “dispersive solid-phase extraction” for the determination of pesticide residues in produce[J].Journal of AOAC International,2003,86(2):412-431.
[39]DONG H,XIAO K J,XIAN Y P,et al.A novel approach for simultaneous analysis of perchlorate (ClO4-) and bromate (BrO3-) in fruits and vegetables using modified QuEChERS combined with ultrahigh performance liquid chromatography-tandem mass spectrometry[J].Food Chemistry,2019,270:196-203.
[40]张小刚,徐志华,孙洪峰,等.QuEChERS-超高效液相色谱-串联质谱法测定水果中高氯酸盐[J].食品安全质量检测学报,2021,12(10):4216-4220.ZHANG X G,XU Z H,SUN H F,et al.Determination of perchlorate in fruits by QuEChERS-ultra performance liquid chromatography-tandem mass spectrometry[J].Journal of Food Safety &Quality,2021,12(10):4216-4220.
[41]韦昱,方从容,赵云峰,等.分散微固相萃取/超高效液相色谱-高分辨质谱法测定茶叶中高氯酸盐[J].2021,40(4):583-588.WEI Y,FANG C R,ZHAO Y F,et al.Determination of perchlorate in tea by dispersive micro-solid phase extraction/ultra performance liquid chromatography-high resolution mass spectrometry[J].Journal of Instrumental Analysis,2021,40(4):583-588.
[42]XIE Y H,WU Y L,QIN Y H,et al.Evaluation of perchlorate removal from aqueous solution by cross-linked magnetic chitosan/poly(vinyl alcohol) particles[J].Journal of the Taiwan Institute of Chemical Engineers,2016,65:295-303.
[43]KRISHNAN G R,PRABHAKARAN K,GEORGE B K.Biogenic magnetic nano hydroxyapatite: Sustainable adsorbent for the removal of perchlorate from water at near-neutral pH[J].Journal of Environmental Chemical Engineering,2021,9(6):106316.
[44]SONG W,GAO B Y,GUO Y,et al.Effective adsorption/desorption of perchlorate from water using corn stalk based modified magnetic biopolymer ion exchange resin[J].Microporous and Mesoporous Materials,2017,252:59-68.
[45]ZHAO Y G,ZHANG Y,WANG F L,et al.Determination of perchlorate from tea leaves using quaternary ammonium modified magnetic carboxyl-carbon nanotubes followed by liquid chromatographytandem quadrupole mass spectrometry[J].Talanta,2018,185:411-418.
[46]闵婉妮,李艳妮,安瑜,等.高氯酸盐的快速荧光检测及其食品分析应用进展[J].食品安全质量检测学报,2024,15(18):209-218.MIN W N,LI Y N,AN Y,et al.Rapid fluorescence detection of perchlorate and its application in food analysis[J].Journal of Food Safety &Quality,2024,15(18):209-218.
[47]刘丽菁,杨艳,张文婷,等.离子色谱法测定瓶装水中溴酸盐、氯酸盐和高氯酸盐[J].中国给水排水,2023,39(6):134-138.LIU L J,YANG Y,ZHANG W T,et al.Determination of bromate, Chlorate and perchlorate in bottled water by ion chromatography[J].China Water &Wastewater,2023,39(6):134-138.
[48]张燕娣,蒋才斌.离子色谱法测定饮用水中高氯酸盐方法研究[J].2024(11):106-108.ZHANG Y D,JIANG C B.Study on determination of perchlorate in drinking water by ion chromatography[J].Shanxi Chemical Industry,2024(11):106-108.
[49]李婷婷,周丽,曾文锦,等.离子色谱法同时测定包装饮用水中的6种阴离子[J].生物加工过程,2020,18(4):520-526.LI T T,ZHOU L,ZENG W J,et al.Determination of six kinds of anions in bottled drinking water by ion chromatography[J].Chinese Journal of Bioprocess Engineering,2020,18(4):520-526.
[50]李婷婷,任兴权,周丽,等.离子色谱法同时测定饮用水中的溴酸盐和高氯酸盐[J].食品工业,2020,41(9):325-328.LI T T,REN X Q,ZHOU L,et al.Determination of bromate and perchlorate in drinking water by ion chromatography method[J].The Food Industry,2020,41(9): 325-328.
[51]SEILER M A,JENSEN D,NEIST U,et al.Validation data for the determination of perchlorate in water using ion chromatography with suppressed conductivity detection[J].Environmental Sciences Europe,2016,28(1):18.
[52]张少华,应璐,张书芬,等.超声辅助热水提取-离子色谱法同时测定蔬菜中的硫氰酸盐和高氯酸盐[J].食品工业科技,2019,40(7):224-227.ZHANG S H,YING L,ZHANG S F,et al.Simultaneous determination of thiocyanate and perchlorate in vegetables by ultrasonic-assisted hot water extraction-ion chromatography[J].Science and Technology of Food Industry,2019,40(7):224-227.
[53]RAJSKI Ł,DÍAZ GALIANO F J,CUTILLAS V,et al.Coupling ion chromatography to Q-orbitrap for the fast and robust analysis of anionic pesticides in fruits and vegetables[J].Journal of AOAC INTERNATIONAL,2018,101(2):352-359.
[54]HE X W,GAN W B,YANG J C,et al.Rapid analysis of trace pollutants chlorates,perchlorates,and four xanthates in water based on IC-MS combined technology[J].Microchemical Journal,2024,198:110182.
[55]孙文闪,诸骏杰,董叶箐,等.离子色谱-串联质谱法测定生活饮用水中的高氯酸盐、氯酸盐和溴酸盐[J].食品安全质量检测学报.2020,11(7):2150-2154.SUN W S,ZHU J J,DONG Y Q.et al.Determination of perchlorate,chlorate and bromate in drinking water by ion chromatography-tandem mass spectrometry[J].Journal of Food Safety and Quality,2020,11(7): 2150-2154.
[56]高立红,李仁勇,刘慧,等.离子色谱-串联质谱法检测碳酸饮料中的高氯酸盐[J].环境化学,2017,36(9):2082-2083.GAO L H,LI R Y,LIU H,et al.Determination of perchlorate in carbonated drinks by ion chromatography with tandem mass spectrometry[J].Environmental Chemistry,2017,36(9):2082-2083.
[57]ZHANG H,HUO Z L,LIU H L,et al.A novel ion chromatography tandem mass spectrometry (IC-MS/MS) method for the determination of Chlorate and prechlorate in freshly brewed coffee[J].Microchemical Journal,2021,165:106167.
[58]张志敏,史亚利,王文倩,等.茶叶中高氯酸盐的离子色谱串联质谱分析[J].环境化学,2022,41(2):572-580.ZHANG Z M,SHI Y L,WANG W Q,et al.Analysis of perchlorate in tea by ion chromatography tandem mass spectrometry[J].Environmental Chemistry,2022,41(2):572-580.
[59]NOBILE M,DANESI L,PAVLOVIC R,et al.Presence of Chlorate and perchlorate residues in raw bovine milk from Italian farms[J].Foods,2022,11(18): 2741-2741.
[60]GARVEY J,MARGALIT A,KELLY M,et al.A method for the quantitative analysis of polar anionic pesticides in milk/infant formula,cereals and fruit and vegetables using ion chromatography coupled to tandem mass spectrometry[J].Analytical Methods,2024,16(23):3692-3700.
[61]WANG Y J,DONG J J,CHEN M Y,et al.Dietary exposure and risk assessment of perchlorate in diverse food from Wuhan,China[J].Food Chemistry,2021,358:129881.
[62]HAO J M,HAN M J,LI J W,et al.Surface modification of silver nanofilms for improved perchlorate detection by surface-enhanced Raman scattering[J].Journal of Colloid and Interface Science,2012,377(1):51-57.
[63]GUO Z M,CHEN P,WANG M M,et al.Determination of perchlorate in tea using SERS with a superhydrophobically treated cysteine modified silver film/polydimethylsiloxane substrate[J].Analytical Methods,2021,13(13):1625-1634.
[64]SUN H Z,LIANG Y B,ZHOU L,et al.Visual detection of perchlorate in aqueous solution using alkali methylene blue[J].Analytical Sciences,2022,38(3):525-531.
[65]KUMAR P,KAPOOR A,RAGHUNATHAN M.Rapid and costeffective detection of perchlorate in water using paper-based analytical devices[J].Desalination and Water Treatment,2023,314:130-140.