L-茶氨酸(L-theanine,L-The)作为茶叶特征性非蛋白氨基酸,其分子结构中特有的N-乙基-L-谷氨酰胺基团(图1)赋予独特理化特性,其在酸性环境中稳定性显著优于碱性条件(分解产物为乙胺与谷氨酸)[1]。现代药理学研究揭示其多维度生物活性:a)神经调节方面,通过血脑屏障调控γ-氨基丁酸(γ-aminobutyric acid,GABA)与5-羟色胺(5-hydroxytryptamine,5-HT)水平,介导情绪稳定及认知增强效应;b)代谢调控层面,可抑制血管紧张素转换酶活性,降低收缩压,同时通过激活AMPK通路改善脂质代谢[2-4]。在应用拓展方面,其分子两亲性特征促进开发出缓释微胶囊、纳米脂质体等新型递送系统,广泛应用于功能食品、神经保护制剂及抗肿瘤佐剂[5-10]。基于这些特性,L-茶氨酸已被纳入食品药品监督管理局(Food and Drug Administration,FDA)的一般公认为安全(generally recognized as safe,GRAS)的安全物质清单(1985年),并在我国2014年新食品原料目录中完成注册[11-13]。当前L-茶氨酸的生物制备体系主要涵盖植物提取、酶促合成和微生物发酵三大技术路径,各具特点且存在技术瓶颈。本研究从合成生物学改造、智能化分离纯化、晶体工程优化、干燥包装四大技术进行多维解析,为氨基酸绿色智造提供了系统性解决方案。研究展望了发酵新技术的研究方向,创新性提出“发酵-分离动态耦合”模型,希望能为形成具有自主知识产权的L-茶氨酸绿色可持续生产模式提供科学依据。
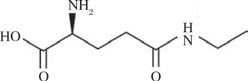
图1 L-茶氨酸结构式
Fig.1 The structure of L-theanine
1 L-茶氨酸生物合成技术进展
1.1 植物源提取技术特征
研究发现,茶叶的风味与其特定次级代谢产物的丰度密切相关,尤其是多酚类和茶氨酸等活性物质。其中,最主要的多酚类化合物是儿茶素,其水溶性较低,而茶氨酸虽然易溶于水,但不易溶于某些有机溶剂[14]。茶氨酸为两性电解质,在水溶液中以带电离子形式存在,而儿茶素则为中性多酚类分子。两者在极性、电荷状态、水溶性以及吸附行为等方面存在显著差异,因此较易实现分离纯化[15]。茶氨酸不仅影响茶汤呈味特性,增强甜度缓解苦涩感,还能与谷氨酸钠协同提升鲜味感知[16]。随着人们对茶氨酸研究的不断深入,发现其含量占茶叶氨基酸总量的一半以上[17],是评判茶叶品质的核心指标[18]。
茶树根尖组织是L-茶氨酸合成的主要部位[19],茶氨酸合成酶能够催化谷氨酸与乙胺缩合生成L-茶氨酸,随后经由特定的转运机制运输至地上器官,并参与一系列代谢过程,对茶树的生长和发芽起到重要促进作用[19-22]。尽管植物提取工艺日趋完善[23-26],但实际生产仍面临多重制约:如干茶叶中茶氨酸的含量较低,仅为1%~2%,无法满足大规模生产需求;原料中存在咖啡因、茶多酚等多组分干扰导致纯化困难;加之茶树生长周期长、生物量有限,导致综合成本居高不下[26]。
1.2 酶催化合成技术的突破
酶法催化合成L-茶氨酸不仅具备操作简便、成本较低的优势,更因酶反应的构型专一性,产物通常为L型的茶氨酸。此外,该方法易于实现规模化生产,已逐渐成为L-茶氨酸工业化制备的主流技术路径,有效弥补了直接提取法产率低及化学合成法选择性差、环境负担重等不足。现有酶系可分为ATP依赖型[如茶氨酸合成酶(theanine synthetase,TS),EC 6.3.1.6[27-28];γ-谷氨酰半胱氨酸合成酶(γ-glutamylcysteine synthetase,γ-GCS),EC 6.3.2.2[28-29];L-谷氨酰胺合成酶(glutamine synthetase,GS),EC 6.3.1.2[27,30-31];γ-谷氨酰甲胺合成酶(γ-glutamylmethylamide synthetase,GMAS),EC 6.3.4.12[32-33];谷氨酸合酶(glutamine oxoglutarate aminotransferase,GOGAT),EC 1.4.1.13[34]和非ATP依赖型[如L-谷氨酰胺酶(glutaminase,GLS),EC 3.5.1.2[27];γ-谷氨酰转肽酶(γ-glutamyl transpeptidase,GGT),EC 2.3.2.2[29,35-36]两大类。TS是茶树中合成茶氨酸的天然酶,在ATP供能下催化谷氨酸和乙胺直接合成L-茶氨酸,但因其结构不稳定且存在逆反应,所以难以实现工业化。因此,目前L-茶氨酸工业合成主要依赖于微生物来源的酶系,尤其是GS、GMAS、GGT和GLS,借助大肠杆菌Escherichia coli、枯草芽孢杆菌(Bacillus subtilis)等微生物体内异源表达催化合成茶氨酸。
研究发现,细菌GS同时具有催化谷氨酰胺和L-茶氨酸的生物学功能。GMAS在ATP供能下催化L-谷氨酸与甲胺或乙胺形成L-茶氨酸,其催化效率明显高于GS。在大肠杆菌中重组表达来源于Methylovorus mays 的GMAS,所获重组菌株的产酶能力为原始菌株的23倍,且其酶学性质与天然酶无显著差异,规模化工业生产潜力巨大。GGT是一种双底物酶,能催化γ-谷氨酰供体裂解并将γ-谷氨酰部分转移至胺类受体,在谷胱甘肽代谢中发挥关键作用。GGT反应时间短,已被用于转肽反应以合成L-茶氨酸[35]。如在谷氨酰胺与铵根存在条件下,GGT可高效生成茶氨酸。此外,尽管某些谷氨酰胺酶表现出γ-谷氨酰转移活性,迄今只有来源于Pseudomonas nitroreducens 的谷氨酰胺酶被明确鉴定具备催化L-茶氨酸合成的能力。利用游离态P. nitroreducens 谷氨酰胺酶,在以谷氨酰胺(γ-谷氨酰供体)和乙胺(受体)为底物的反应体系中,γ-谷氨酰的转移与水解反应可并行发生。实验表明,在0.7 mol/L谷氨酰胺与1.5 mol/L乙胺、0.5 U/mL酶浓度、反应7 h的条件下,可获得高达47 g/L的L-茶氨酸产量。潘力研教授团队选择Bocillus subtilis ATCC 6051Δ5作为表达宿主,创新组合双启动子和双信号肽、信号肽酶的过表达,实现了GGT高水平表达,在L-茶氨酸转化研究中,采用环氧树脂固定化酶,确定了在Bacilluslicheniformis GGT(BlGGT)中连续催化合成L-茶氨酸的最佳反应条件,L-茶氨酸的转化率达到了65.38%[37]。利用工程菌酶促生产L-茶氨酸的主要进展见表1。
表1 利用工程菌酶促生产L-茶氨酸
Table 1 The enzymatic synthesis of L-theanine by engineering bacteria
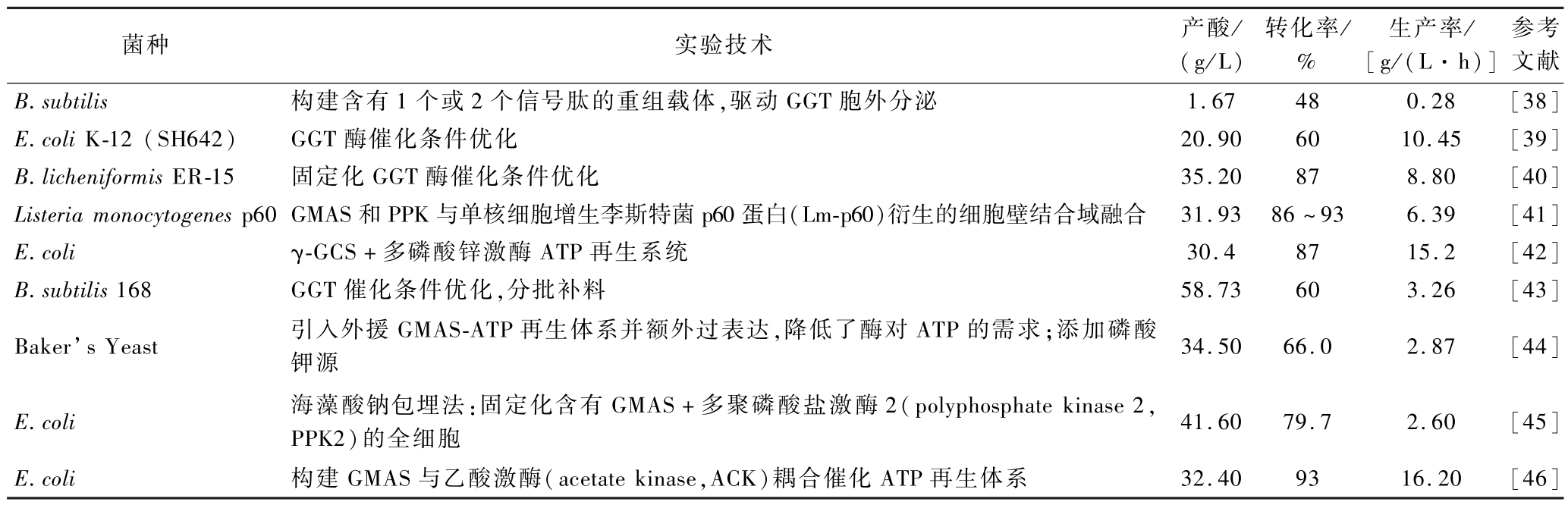
注:多磷酸激酶(poly phosphate kinase,PPK)。
现有文献已证实4种细菌酶均具备茶氨酸合成能力,但酶法技术仍面临多重挑战:双工段增加流程复杂度,原料昂贵、有副产物、乙胺不耐受、ATP依赖型酶等因素导致经济性不足。当前亟需通过大规模筛选手段,建立具有生物多样性的酶资源库;同时从酶特性和工业化应用2个维度开展深度研究:一方面通过酶动力学、热稳定性等参数的系统比对筛选优势酶系;另一方面可以结合酶工程和发酵工程技术参数进行综合评估,定向优化酶的催化机制,通过邻近效应与定向效应提升催化酶和底物结合精度,提高催化效率;利用底物形变诱导契合机制,降低酶催化反应的活化能;对关键酶进行定向改造,利用计算机辅助设计(computer-aided design and drafting,CADD)筛选关键酶的突变体,通过分子动力学模拟优化酶-底物结合能,显著提升酶催化效率;结合新固定化酶技术(如智能响应载体)提高酶的稳定性和底物浓度耐受性,增加酶的循环使用频次等,降低生产成本,筛选出兼具催化效率与产业化适配性的酶制剂。
1.3 发酵法合成L-茶氨酸
微生物发酵生产L-茶氨酸具有原料易得、成本低廉、合成效率高和构型专一性强等优势。其核心在于通过重构微生物代谢通路,使工程菌株将外源原料通过内源代谢高效转化为L-茶氨酸,因此优良生产菌株的筛选与构建至关重要。近年来,随着基因工程与合成生物学技术的迅速发展,L-茶氨酸生产宿主的种类不断拓展,包括E. coli、谷氨酸棒状杆菌、乳酸杆菌、B. subtilis 及短小芽孢杆菌等。其中,E. coli 因其生长周期短、遗传操作体系成熟,已被广泛应用于L-茶氨酸的异源表达与发酵合成[47-51];而谷氨酸棒状杆菌具备GRAS属性,使其更具工业发酵应用潜力[14,52-53]。
研究发现,L-茶氨酸的生物合成受多个代谢系统协同调控,主要包括:a)代谢途径构建;b)关键前体乙胺的高效供应;c)细胞ATP能量的平衡与再生能力;d)发酵工艺参数的精准优化。上述策略的有机结合将为L-茶氨酸的高效、绿色与可持续工业化发酵生产提供坚实基础。
1.3.1 菌种代谢途径构建
微生物发酵菌种在工业发酵中起着至关重要的作用,是工业发酵的动力源头,其稳定性直接决定了发酵产品的质量。研究人员通过基因编辑技术与合成生物学技术相结合,可以定向改造目标菌株的代谢途径,重构微生物的代谢网络,以减少对昂贵原料的依赖,提升发酵效率、优化产物质量和降低成本,这已成为当前氨基酸发酵应用的研究热点。谢希贤教授研究团队[32]对野生型大肠杆菌由糖和乙胺一步发酵生产茶氨酸的代谢途径工程进行了深入研究,对目标菌株进行基因编辑,引入外来基因,切断自身代谢途径,提高了茶氨酸的发酵产量,并在优化发酵条件后,重组菌株TH11发酵产茶氨酸70.6 g/L,产酸率2.72 g/(L·h),糖酸转化率约为42%。季圆清[50]通过系统代谢工程对工程菌THEA3-2做了进一步改造,成功引入乙醛脱氢酶基因和转氨酶基因,构建了乙胺的内源合成代谢途径,在不外源添加乙胺的条件下,实现葡萄糖从头发酵生产茶氨酸,摇瓶发酵L-茶氨酸产量达到了5.91 g/L。姜灏[51]采用多模块代谢工程策略构建了一株茶氨酸从头合成大肠杆菌生产菌株,利用CRISPR/Cas9基因编辑技术进行了一系列基因工程改造,在细胞内构建了乙胺合成通路,能够较为高效地以葡萄糖为唯一碳源从头合成茶氨酸,合成效率为1.92 g/(L·h)。饶志明教授团队通过多策略优化组合,融合了蛋白质理性设计、代谢网络重构与能量调控,系统性突破了L-茶氨酸合成瓶颈,得到谷氨酸棒杆菌突变体E179K/N105R[52]。该团队借助计算机辅助设计进行工程化,不仅提高了酶的热稳定性,增强了酶活力,通过分子模拟揭示了突变增强ATP结合力与局部结构刚性提升催化效率,优化碳通量,使得茶氨酸产量提高36.61%,糖酸转化率57.11%,产率为1.16 g/(L·h),为其工业化提供高效路线。研究者通过结合微生物代谢途径构建和发酵策略已做了诸多的基础科学研究工作,为工业化发酵生产茶氨酸奠定了坚实的理论基础。
1.3.2 关键前体乙胺的高效供应
乙胺作为茶氨酸生物合成的直接氮源和关键前体,其在合成效率和产率上起着决定性作用。目前,微生物发酵主要通过直接外源添加乙胺提高L-茶氨酸的合成速率。然而,由于乙胺沸点较低、易燃且具有细胞毒性,挥发后的气体可能对环境和周围人员造成伤害。外源添加乙胺后,发酵液中乙胺积累,会抑制细胞活性,减少ATP的再生,影响产物的合成[53]。FENG等[49]通过一种生产L-茶氨酸的无细胞蛋白合成(cell-free protein synthesis,CFPS)系统,过表达丙氨酸脱羧酶和谷氨酰胺合成酶,不添加乙胺,得到13.42 μmol/L的L-茶氨酸,验证了不添加乙胺合成L-茶氨酸的可行性。因此,构建微生物内源乙胺生物合成模块实现不依赖外源乙胺补充的L-茶氨酸合成,已成为当前该领域的研究热点。范晓光等[54]在前期研究的基础之上,通过进一步改造L-茶氨酸的代谢途径,构建出工程菌E. coli E12,不添加乙胺,可以直接利用葡萄糖和乙酸双为碳源,发酵33 h产L-茶氨酸70 g/L,糖酸转化率提高到33%,为目前报道的一步法合成L-茶氨酸的最高水平,取得了突破性的进展,工业应用潜力巨大。在发酵合成L-茶氨酸研究过程中,关键前体乙胺的高效供应主要进展如表2、表3所示。
表2 关键前体乙胺的高效供应
Table 2 Efficient supply of key precursor ethylamine

注:“—”表示无相关数据。
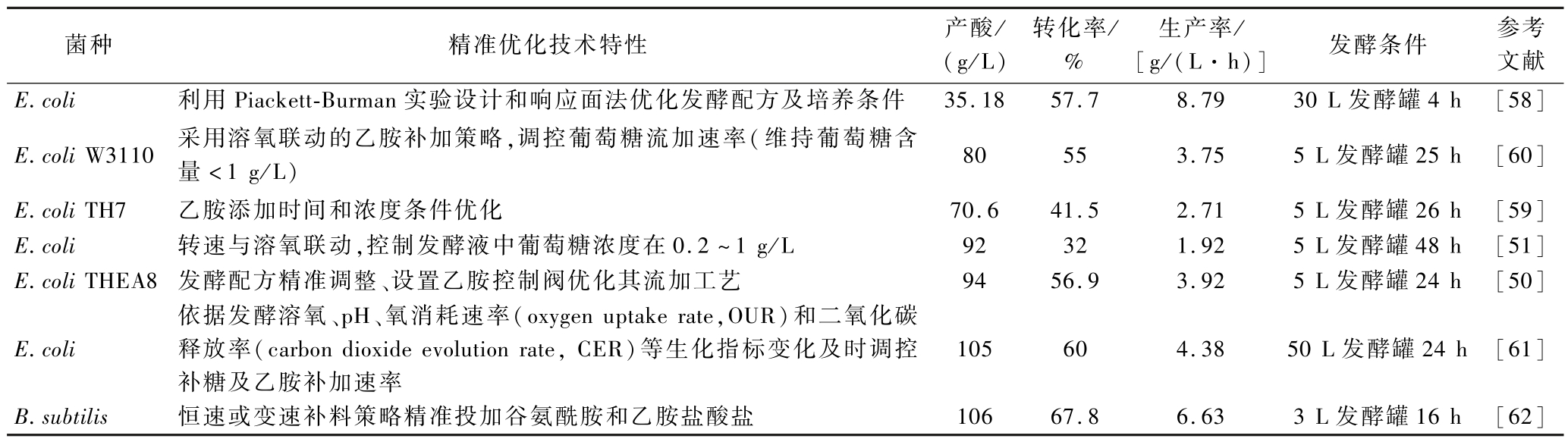
表3 利用工程菌发酵生产L-茶氨酸的精准优化
Table 3 The precise optimization of L-theanine production by fermentation of engineering bacteria
1.3.3 细胞ATP能量的平衡与再生能力
在ATP依赖的合成酶催化过程中,ATP作为辅助因子,进一步参与L-茶氨酸的生产。通过ATP再生,可以显著降低发酵生产成本。目前,已经报道了许多用于ATP再生的酶,如丙酮酸羧化激酶(pyruvate kinase,PK)、肌酸激酶(creatine kinase,CK)、醋酸激酶(acetate kinase,AK)和PPK[56]。FAN等[57]从Mannheimia succiniciproducens 中引入了一种节能的PK,工程菌株E.coli TH11的茶氨酸效价(38.4 g/L)比ATP再生前的TH9菌株提高了7.6%。张迪[14]利用基因工程技术对C. glutamicum 中合成L-茶氨酸的代谢途径进行改造,引入GMASE179K/N105R双突变体和来源Erysipelotrichaceae bacterium 的PPK,胞内ATP水平增加了35.32%,通过分批补加乙胺,最终L-茶氨酸发酵水平达到了44.12 g/L,糖酸转化率为57.11%。
1.3.4 发酵工艺参数的精准优化
在L-茶氨酸的发酵过程中,需通过多参数动态调控与底物策略优化(乙胺、谷氨酰胺、葡萄糖等),结合智能化生物传感系统实现发酵工艺参数的精准控制,以提高目标产物的产量和生产率,最大限度地降低生产成本。
陆文渊[58]结合固定化细胞技术(海藻酸钠-戊二醛交联)提升大肠杆菌对底物的耐受性,L-茶氨酸连续生物合成的平均产量为25.4 g/L,转化率为6.35 g/L。范晓光等[59]通过溶氧联动补料法调控碳源(葡萄糖)流加速率(维持葡萄糖含量<3 g/L)以减少乙酸积累,同时优化乙胺补加时间,L-茶氨酸的产量可达75~ 80 g/L,提升糖酸转化率至52%~55% 。
利用工程菌发酵生产L-茶氨酸的精准优化主要研究进展见表3。傅嘉懿[62]通过对高底物浓度下的L-茶氨酸工艺进行优化,恒速或变速补料策略精准投加谷氨酰胺和乙胺盐酸盐,L-茶氨酸的生成量达到610.1 mmol/L,摩尔转化率达67.8%。
研究指出,微生物发酵体系的构建是核心技术环节,结合优化发酵参数调控、补料分批技术等关键技术节点,如通过精准控制温度、pH值、溶氧等基础参数,结合现代生物工程技术,可显著提升发酵效率与产物质量,以实现发酵过程工艺参数的精准优化,这已成为提升茶氨酸生物合成效率的重要突破口。同时以工业化生产需求为导向,建立从酶资源挖掘到发酵工艺开发的全链条研究体系,通过多学科交叉实现技术路径的迭代升级,结合合成生物学和代谢工程,设计以葡萄糖流向乙胺再到L-茶氨酸的连续代谢路径,通过对发酵技术指标的合理控制,集合发酵设备和智能生物传感系统,可以实现对微生物代谢和产物合成的精确调控,最终实现L-茶氨酸的一步法发酵合成,不仅可以提升合成效率,也为绿色、安全、高效的L-茶氨酸工业化生产提供了新的解决方案。
2 L-茶氨酸的分离纯化
L-茶氨酸发酵体系采用复合培养基设计,包含双相氮源供给系统(无机/有机氮源协同作用)、矿物元素平衡体系及生长因子调控模块。由于发酵体系存在多组分动态平衡特征,包括持续补料的代谢中间体、菌体自溶产物及复合培养基残留物,其分离选择性系数较酶法产物降低42%~65%,这种体系复杂性使得其下游处理相较酶法面临更大的分离困难。基于现有工业实践经验,发酵法生产L-茶氨酸的纯化工程包含4级分离体系:Ⅰ级分离:初级分离;Ⅱ级纯化:脱盐处理;Ⅲ级精制:精制结晶工艺;Ⅳ级成品:干燥与包装[29,63-65]。在工业化应用中,采用四级连续纯化系统可使最终产品纯度达到医药级标准,这一技术路线已通过良好生产规范认证(good manufacturing practice,GMP)。 L-茶氨酸发酵及纯化工艺流程如图2所示。
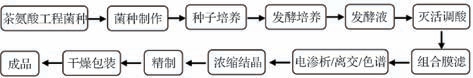
图2 L-茶氨酸发酵及纯化工艺流程
Fig.2 The fermentation and purification process of L-theanine
2.1 Ⅰ级分离
近年来,随着先进膜材料技术的革新,无机陶瓷膜分离工艺在工业分离领域展现出显著优势。该技术凭借其卓越的分离效能、便捷的操作特性、优异的材料稳定性以及环境友好特征,已成为生物发酵产物预处理的首选方案。发酵体系具有高黏度特性,研究证实当浓缩倍数提升时,膜渗透性能呈现指数衰减趋势。工程实践中采用高分子絮凝助剂预处理工艺,通过促进菌体蛋白絮凝聚集以优化物料粒径分布,可有效改善膜面流体动力学特征,维持稳定的通量。在陶瓷膜运行工艺参数调控方面,跨膜压力梯度是影响系统效能的关键变量(推荐范围0.05~0.5 MPa)。压力参数设置需兼顾系统效率与运行稳定性,工程实践表明,采用压力梯度动态适配策略(如脉冲式调节)可延缓膜组件性能衰减,使用寿命延长15%~20%。
在精制分离阶段,创新型分子筛分工艺——纳滤技术展现出独特优势。该技术基于空间位阻效应与道南效应的协同作用,选择性截留分子质量200 Da以上的有机组分及多价态离子,对微生物污染物及热原物质保持高效截留率。特别值得注意的是,荷电型纳滤膜借助静电相互作用机制,可在0.5~1.5 MPa低压条件下实现90% 以上的色素脱除率,相较传统活性炭吸附工艺能耗降低约40%。
针对L-茶氨酸发酵体系的分离提纯,工程实践表明陶滤与纳滤的工艺协同可使初级分离效率提升至新高度。在生产实践过程中,研究人员通过优化两级膜系统的工艺衔接与参数匹配,该集成化方案在工业化应用中实现了L-茶氨酸的平均收得率达到97.3%,分离提取效能显著优于传统工艺。在生物合成领域,这种膜分离技术组合已成为提升产物质量、降低生产成本的关键技术路径。
2.2 Ⅱ级纯化
在发酵工艺优化过程中,辅助盐的引入导致体系盐分富集,传统萃取法因茶氨酸强亲水性难以奏效。现行工业化除盐方案主要依托物理分离技术,其中树脂吸附、电渗析及色谱分离构成三大核心技术体系[28,63-69]。
离子交换树脂法基于茶氨酸两性电解质特性[等电点(isoelectric point,pI)=5.65],通过pH调控实现吸附-解吸动态平衡:酸性条件下阳离子树脂通过静电作用捕获目标物,碱性环境则采用阴离子树脂系统,正确选择离交树脂是实现除盐的关键[70-71]。工艺参数研究表明,流速控制在0.5~1.0 BV/h可平衡交换效率,规避产物渗漏风险[60,72-74],在此条件下,H型732树脂体系可实现95%以上收得率[75-76]。另有研究者对不同阴离子树脂吸附茶氨酸的热力学、吸附性能进行了深入研究,确定阴离子树脂纯化的最佳工艺参数,在后续纯化中得到了纯度较高的茶氨酸产品[66,77-79]。
在除盐工艺中,电渗析分离技术展现独特优势,其通过荷电膜的选择透过性在直流电场中实现离子定向迁移。工程数据显示,该技术对初始电导率适应性良好,脱盐率稳定在85% 水平,茶氨酸纯度可达98%[76-77,80]。相较于树脂法,其优势体现在能耗降低40%、试剂消耗减少70%左右,且具备同步浓缩功能。陈希书等[81]证实该技术在5~15 ms/cm电导率范围内均能保持高效运行,特别适合高盐发酵液的梯级处理。
色谱分离技术作为精密分离代表,利用固定相-流动相分配差异实现分子级纯化。新型钢化玻璃层析柱的应用使茶氨酸纯度突破98.2%,系统回收率达72.5%[82]。该技术核心优势在于:a)梯度洗脱实现零产物损耗;b)填料可再生重复使用;c)与检测系统(如HPLC-MS)无缝对接。尽管设备投资较高,但其自动化程度与分离精度[相对标准偏差(relative standard deviation,RSD) <0.5%]在高端产品制备中具有不可替代性。
技术经济性分析表明,树脂法设备成本最低但运行周期长,污水量大,电渗析综合能耗最优且适合连续生产,色谱法则在超高纯度需求场景占据优势。当前技术发展趋势聚焦于多技术集成,如电渗析-树脂联用系统可降低离交柱污染负荷,而在线色谱监测能实现过程精准控制。未来研究重点应放在新型耐污染膜材料开发及智能化控制系统优化方向。
2.3 Ⅲ级精制
经初级纯化的L-茶氨酸产品(纯度≥98%)需通过深度精制才能满足差异化市场需求。精制工艺的核心在于调控溶液体系相平衡实现产物选择性析出,主要技术路径包括溶剂结晶与晶体优化两类。
溶剂诱导结晶法基于茶氨酸在低介电溶剂(如乙醇/甲醇)中溶解度骤降特性,通过调控溶剂极性诱导晶体定向析出。该工艺兼容常规结晶设备,操作流程简化,但需严格控制溶剂残留量符合相关标准要求。鉴于乙醇溶剂的生物安全性(半数致死量>7 000 mg/kg)显著优于其他有机溶剂,其常在工业生产中优先被作为结晶介质。晶体工程优化技术是通过多级重结晶工艺提升产品物理性能,以获得单分散性良好的晶型产物。虽然溶剂消耗量较初级结晶增加2~3倍,经济性指数下降40% 左右,但是这类高端晶体产品具有卓越的流动性与抗吸湿性(水分活度<0.3),能够满足精密剂型需求,市场溢价空间十分可观,适用于高附加值领域。后续技术发展趋势聚焦于连续结晶反应器开发,结合在线过程分析技术(process analytical technologies,PAT)实现晶体形貌的精准调控。
2.4 Ⅳ级成品
L-茶氨酸作为食品工业中不可或缺的要素,一直以来扮演着重要的角色,其广泛应用于食品、保健品和医药领域。其成品的干燥与包装直接影响产品品质、稳定性及生产成本,近年来围绕高效节能、精准控制、环保安全等方向取得显著进展。
随着新技术的不断突破,氨基酸干燥与包装取得了卓有成效的技术创新,这些新技术手段在L-茶氨酸的干燥与包装工段中得到广泛应用。如节能工艺应用过热蒸汽干燥快速传热且无氧化风险,利用热泵干燥通过余热回收节能30%~50%;智能控制结合微波真空干燥与AI算法动态优化参数,减少茶氨酸的热损伤与结块风险;惰性保护可以采用氮气/氩气环境下干燥,防止产品氧化变色。包装过程中应用纳米复合膜(如石墨烯)等高阻隔材料将透氧率降低90%以上,搭配吸氧/干燥涂层可延长保质期;结合智能监测系统,利用集成温湿度指示标签与射频识别(radio frequency identification,RFID)芯片,实现全程溯源与异常预警;气调包装(modified atmosphere packaging,MAP)技术则是利用充填氮气或二氧化碳抑制微生物生长,保障氨基酸稳定性。
当前氨基酸干燥与包装技术正朝着高效节能、智能精准、绿色低碳方向突破,通过新材料、智能控制与系统集成,推动氨基酸在医药、食品等高附加值领域的应用升级,同时响应全球可持续发展需求。
3 新发酵技术研究方向展望
随着世界新技术的不断突破,特别是AI人工智能技术的爆发式增长,为发酵技术的革新提供了强大的技术支持。如a)动态代谢调控系统构建:开发光控/化学诱导型启动子精确调控乙胺合成模块,实现菌株生长-产物合成两阶段解耦控制。通过基因抑制(clustered regularly interspaced short palindromic repeats interference,CRISPRi)技术动态抑制竞争途径如谷氨酸支路,使碳流定向富集;b)原位分离-发酵耦合工艺:设计具有pH响应特性的智能膜材料,在发酵过程中动态调节膜孔径(5~50 nm可调),实现产物实时分离与菌体循环利用;c)仿生催化界面设计:在工程菌表面固定化茶氨酸转运蛋白,通过构建“细胞膜-纳米纤维”复合催化界面,加速产物外排速率,有效解除胞内积累造成的代谢抑制;d)数字孪生发酵系统:建立包含137个关键参数的发酵过程数字模型,通过机器学习预测最佳补料策略。工业验证表明,该系统使糖酸转化率波动范围从±8%收窄至±1.5%;e)智能化生物传感系统:利用生物活性物质的高度选择性来识别待测生物化学物质,结合AI将其浓度转化为电信号进行检测,能够帮助研究人员迅速识别并筛选出具有高产量和耐受性的突变菌株。智能化生物传感系统的应用使得发酵过程从“黑箱操作”转向“精准调控”,进一步降低了生产成本。新发酵技术体系融合了合成生物学、材料科学与人工智能,构建出“发酵-分离动态耦合”模型,推动L-茶氨酸发酵生产向高效、绿色、智能化升级。
4 总结
综上所述,L-茶氨酸是一种非常重要的营养成分,其具有诸多的生理生化功能。当前微生物发酵法已实现L-茶氨酸工业化生产突破,但仍然面临三大技术瓶颈,如外源乙胺毒性限制菌株代谢活性,产物反馈抑制导致转化率衰减,复杂杂质影响结晶收率。“一步法”发酵技术的关键在于突破乙胺毒性抑制难题,采用代谢途径重构和合成生物学相结合,设计内源性乙胺合成模块的基因回路,实现以葡萄糖为单一碳源的全程自主合成。通过智能化生物传感系统和AI人工智能新技术相结合,持续推动L-茶氨酸生产从“经验驱动”向“理性设计-精准控制”转型,构建“发酵-分离动态耦合”模型,为功能性氨基酸的智能制造提供新范式。
[1]LIU S H,LI J,HUANG J N,et al.New advances in genetic engineering for L-theanine biosynthesis[J].Trends in Food Science &Technology,2021,114: 540-551.
[2]KIM S,JO K,HONG K B,et al.GABA and L-theanine mixture decreases sleep latency and improves NREM sleep[J].Pharmaceutical Biology,2019,57(1): 65-72.
[3]KAHATHUDUWA C N,DASSANAYAKE T L,TISSA AMARAKOON A M,et al.Acute effects of theanine,caffeine and theaninecaffeine combination on attention[J].Nutritional Neuroscience,2017,20(6): 369-377.
[4]张颖,王鑫,刘雅娟,等. L-茶氨酸改善睡眠作用研究进展[J].食品工业科技,2021,42(16):361-366.ZHANG Y,WANG X,LIU Y J,et al.Research progress on improving sleep mechanism of L-theanine[J].Science and Technology of Food Industry,2021,42(16):361-366.
[5]CHEN S N,KANG J X,ZHU H Q,et al. L-theanine and immunity: A review[J].Molecules,2023,28(9):3846.
[6]VUONG Q V,STATHOPOULOS C E,GOLDING J B,et al.Optimum conditions for the water extraction of L-theanine from green tea[J].Journal of Separation Science,2011,34(18):2468-2474.
[7]刘杉,李炜. L-茶氨酸药理作用的研究进展[J].神经药理学报,2020,10(2):24-32.LIU S,LI W.Research progress on pharmacological effects of L-theanine[J].Acta Neuropharmacologica,2020,10(2):24-32.
[8]YOKOGOSHI H,KATO Y,SAGESAKA Y M,et al.Reduction effect of theanine on blood pressure and brain 5-hydroxyindoles in spontaneously hypertensive rats[J].Bioscience,Biotechnology,and Biochemistry,1995,59(4):615-618.
[9]赵丹,王朝旭.茶氨酸的国内外研究现状[J].食品科学,2002,23(5):145-147.ZHAO D,WANG C X.Review on research status of theanine[J].Food Science,2002,23(5):145-147.
[10]李成舰,罗乐,黄春花. L-茶氨酸抗氧化作用的研究进展[J].食品科学技术学报,2018,36(4):69-75.LI C J,LUO L,HUANG C H.Review on antioxidative activities of L-theanine[J].Journal of Food Science and Technology,2018,36(4):69-75.
[11]钟添宇,毛子鋆,吴斌,等.茶氨酸提制及生理功能研究与食品应用进展[J].食品科技,2024,49(10):293-302.ZHONG T Y,MAO Z Y,WU B,et al.Extraction and physiological function of theanine and progress in food application[J].Food Science and Technology,2024,49(10):293-302.
[12]帅玉英,顾钦青,吴晓花,等.新食品原料L-茶氨酸与γ-氨基丁酸的比较[J].食品与药品,2016,18(6): 432-436.SHUAI Y Y,GU Q Q,WU X H,et al.Comparative study of two new food ingredients: L-theanine and γ-aminobutyric acid[J].Food and Drug,2016,18(6): 432-436.
[13]LIU Z W,LI H,LIU J X,et al.Integrative transcriptome,proteome,and microRNA analysis reveals the effects of nitrogen sufficiency and deficiency conditions on theanine metabolism in the tea plant (Camellia sinensis)[J].Horticulture Research,2020,7:65.
[14]张迪.系统代谢改造谷氨棒状杆菌高效生产L-茶氨酸[D].无锡: 江南大学,2024.ZHANG D.Systematic metabolic modification of Corynebacterium glutamicum for efficient production of L-theanine [D].Wuxi:Jiangnan University,2024.
[15]ALLAMEH M,ORSAT V.Effects of time,ultrasonic treatment and pH during extraction on L-theanine and caffeine yields from white tea leaves[J].Future Foods,2024,9: 100304.
[16]LI M Y,LIU H Y,WU D T,et al. L-theanine: A unique functional amino acid in tea (Camellia sinensis L.) with multiple health benefits and food applications[J].Frontiers in Nutrition,2022,9:853846.
[17]CHEN Z,WANG Z,YUAN H Y,et al.From tea leaves to factories: A review of research progress in L-theanine biosynthesis and production[J].Journal of Agricultural and Food Chemistry,2021,69(4): 1187-1196.
[18]刘宝贵,陈致印,张杨玲,等. L-茶氨酸与表没食子儿茶素没食子酸酯预防肥胖及高胆固醇血症的协同调节作用[J].食品工业科技,2022,43(3):341-350.LIU B G,CHEN Z Y,ZHANG Y L,et al.Synergistic moderating effects of L-theanine and EGCG for the prevention of obesity and hypercholesterolemia[J].Science and Technology of Food Industry,2022,43(3):341-350.
[19]FU M Y,TIAN L Y,ZHENG D Q,et al.Visualization of metabolite distribution based on matrix-assisted laser desorption/ionization-mass spectrometry imaging of tea seedlings (Camellia sinensis)[J].Horticulture Research,2024,11(10): uhae218.
[20]FU X M,LIAO Y Y,CHENG S H,et al.Nonaqueous fractionation and overexpression of fluorescent-tagged enzymes reveals the subcellular sites of L-theanine biosynthesis in tea[J].Plant Biotechnology Journal,2021,19(1):98-108.
[21]ZHU Y,HE X,HUANG R,et al.Screening Bacillus subtilis for effective L-theanine production from tea plant rhizosphere soil[J].Applied Biochemistry and Microbiology,2022,58(2):206-212.
[22]WANG Q Y,YU J B,LIN W C,et al. L-theanine metabolism in tea plants: Biological functions and stress tolerance mechanisms[J].Plants,2025,14(3):492.
[23]李学朋,王飞,崔国梁,等.一种连续离子交换技术提取茶氨酸的方法:中国,CN119264007A[P].2024-10-14.LI X P,WANG F,CUI G L,et al.Pathway for extracting theanine by continuous ion exchange technology: China,CN119264007A [P].2024-10-14.
[24]任平红.一种从茶叶中提取茶氨酸的提取设备及提取工艺:中国,CN111848435 A[P].2020-08-21.REN P H.An extraction equipment and process for extracting theanine from tea leaves: China,CN111848435A[P].2020-08-21.
[25]齐崴,何志敏,苏荣欣,等.一种综合提取茶叶中有效成分的方法:中国,CN103242314A[P].2013-04-19.QI W,HE Z M,SU R X,et al.A method for comprehensive extraction of effective components in tea leaves:China,CN103242314A[P].2013-04-19.
[26]鹿洋,齐崴,苏荣欣,等.茶叶中茶多酚的提取纯化及咖啡碱和茶多糖的联产制备[J].食品工业科技,2013,34(20):265-270.LU Y,QI W,SU R X,et al.Extraction and purification of tea polyphenols and simultaneous preparation of caffeine and tea polysaccharides from tea[J].Science and Technology of Food Industry,2013,34(20):265-270.
[27]ASHIHARA H.Occurrence,biosynthesis and metabolism of theanine (γ-glutamyl-L-ethylamide) in plants: A comprehensive review[J].Natural Product Communications,2015,10(5):803-810.
[28]李元,刘珊,祝俊.酶催化合成L-茶氨酸的研究进展[J].食品科学,2017,38(23):298-304.LI Y,LIU S,ZHU J.Process in enzymatic synthesis of L-theanine[J].Food Science,2017,38(23):298-304.
[29]许锦雄,杜阳吉,王钰佳.酶催化合成L-茶氨酸的纯化研究进展[J].农产品加工,2023(1):79-83.XU J X,DU Y J,WANG Y J.Research progress on purification of enzyme-catalyzed synthesis of L-theanine[J].Academic Periodical of Farm Products Processing,2023(1):79-83.
[30]季圆清,周宇航,张通,等. L-茶氨酸生产技术及应用展望[J].食品与发酵工业,2022,48(24):303-311.JI Y Q,ZHOU Y H,ZHANG T,et al.Production technology of L-theanine and its application prospect[J].Food and Fermentation Industries,2022,48(24):303-311.
[31]YAMAMOTO S,WAKAYAMA M,TACHIKI T.Theanine production by coupled fermentation with energy transfer employing Pseudomonas taetrolens Y-30 glutamine synthetase and baker’s yeast cells[J].Bioscience,Biotechnology,and Biochemistry,2005,69(4):784-789.
[32]FAN X G,ZHANG T,JI Y Q,et al.Pathway engineering of Escherichia coli for one-step fermentative production of L-theanine from sugars and ethylamine[J].Metabolic Engineering Communications,2020,11: e00151.
[33]符钟丹.茶叶风味物质茶氨酸的大肠杆菌微生物合成[D].成都: 成都大学,2023.FU Z D.Synthesis of tea flavor substance theanine via Escherichia coli microorganisms[D].Chengdu: Chengdu University,2023.
[34]陈林,张正竹,陈键,等.茶氨酸酶促生物合成研究进展[J].茶叶科学,2011,31(1):1-10.CHEN L,ZHANG Z Z,CHEN J,et al.Review on enzymatic biosynthesis of theanine[J].Journal of Tea Science,2011,31(1):1-10.
[35]张柯铭,罗茜,魏夏森,等.γ-谷氨酰转肽酶的催化特性及其在食品领域应用研究进展[J].食品与发酵工业,2024,50(3):304-313.ZHANG K M,LUO X,WEI X S,et al.Research progress on catalytic properties of γ-glutamyl transpeptidase and its application in food industry[J].Food and Fermentation Industries,2024,50(3):304-313.
[36]马天鸽.异源GGT酶在乳酸乳球菌中的分泌表达及磁性固定化酶的研究[D].合肥: 合肥工业大学,2020.MA T G.Expression of heterologous GGT by Lactococcus lactis and its immobilization of food enzymes[D].Hefei: Hefei University of Technology,2020.
[37]CHEN Q L,WANG B,PAN L.Efficient expression of γ-glutamyl transpeptidase in Bacillus subtilis via CRISPR/Cas9n and its immobilization[J].Applied Microbiology and Biotechnology,2024,108(1):149.
[38]MU D D,LI H W,CHEN Q,et al.Secretion of Bacillus amyloliquefaciens γ-glutamyltranspeptidase from Bacillus subtilis and its application in enzymatic synthesis of L-theanine[J].Journal of Agricultural and Food Chemistry,2019,67(51): 14129-14136.
[39]SUZUKI H,IZUKA S,MIYAKAWA N,et al.Enzymatic production of theanine,an “umami” component of tea,from glutamine and ethylamine with bacterial γ-glutamyltranspeptidase[J].Enzyme and Microbial Technology,2002,31(6):884-889.
[40]BINDAL S,GUPTA R. L-theanine synthesis using γ-glutamyl transpeptidase from Bacillus licheniformis ER-15[J].Journal of Agricultural and Food Chemistry,2014,62(37):9151-9159.
[41]FAN C,QI J K,ZHANG C Z.Biosynthesis of L-theanine via onestep purification and immobilization enzyme system[J].Journal of Applied Microbiology,2025,136(3): lxaf053.
[42]YAO J,LI J,XIONG D D,et al.Development of a highly efficient and specific L-theanine synthase[J].Applied Microbiology and Biotechnology,2020,104(8): 3417-3431.
[43]刘栓英.γ-谷氨酰转肽酶分子改造及其应用[D].无锡: 江南大学,2021.LIU S Y.Molecular modification of γ-glutamyltranspeptidase and its application[D].Wuxi: Jiangnan University,2021.
[44]YANG S Y,HAN Y H,PARK Y L,et al.Production of L-theanine using Escherichia coli whole-cell overexpressing γ-glutamylmethylamide synthetase with bakers yeast[J].Journal of Microbiology and Biotechnology,2020,30(5):785-792.
[45]CHO D H,KIM S,LEE Y,et al.Enhanced theanine production with reduced ATP supply by alginate entrapped Escherichia coli coexpressing γ-glutamylmethylamide synthetase and polyphosphate kinase[J].Enzyme and Microbial Technology,2024,175:110394.
[46]LEE Y,CHO D H,SHIN Y,et al.Use of endogenous acetate kinase for ATP regeneration system of whole-cell L-theanine production catalyzed by γ-glutamylmethylamide synthetase[J].Biotechnology and Bioprocess Engineering,2025,30(1):174-185.
[47]张通,龙科艺,曹华杰,等.利用重组大肠杆菌发酵生产L-茶氨酸[J].食品与发酵工业,2019,45(22): 6-11.ZHANG T,LONG K Y,CAO H J,et al.Production of L-theanine using recombinant Escherichia coli[J].Food and Fermentation Industries,2019,45(22): 6-11.
[48]陈璐.生物催化制备L-茶氨酸及发酵工艺研究[D].开封: 河南大学,2022.CHEN L.Biocatalytic preparation of L-theanine and fermentation process[D].Kaifeng: Henan University,2022.
[49]FENG J C,YANG C,ZHAO Z H,et al.Application of cell-free protein synthesis system for the biosynthesis of L-theanine[J].ACS Synthetic Biology,2021,10(3): 620-631.
[50]季圆清.代谢工程改造大肠杆菌高效合成L-茶氨酸[D].天津: 天津科技大学,2022.JI Y Q.Metabolic engineering of Escherichia coli for efficient synthesis of L-theanine[D].Tianjin: Tianjin University of Science and Technology: 2022.
[51]姜灏.从头合成茶氨酸的大肠杆菌工程菌株的构建[D].天津: 天津科技大学,2023.JIANG Y.Construction of Escherichia coli engineering strain for de novo synthesis of L-Theanine[D].Tianjin: Tianjin University of Science and Technology,2023.
[52]YANG T W,ZHANG D,CAI M M,et al.Combining protein and metabolic engineering strategies for high-level production of L-theanine in Corynebacterium glutamicum[J].Bioresource Technology,2024,394:130200.
[53]马洪坤.谷氨酸棒杆菌生产L-茶氨酸工程菌株的构建[D].天津: 天津科技大学,2021.MA H K.Metabolic engineering of coryneb52acterium glutamicum for L-theanine production[D].Tianjin: Tianjin University of Science and Technology,2022.
[54]范晓光,温昊妍,樊伟明,等.一种提高L-茶氨酸从头发酵产量和转化率的基因工程菌株方法和应用:中国,CN117821356A[P].2024-03-05.FAN X G,WEN H Y,FAN W M,et al.Pathway engineering of Escherichia coli for improving the fermentation yield and conversion rate of L-theanine production by de novo fermentation and its application:China,CN117821356A[P].2024-03-05.
[55]范晓光,季圆清,温昊妍,等.一种利用葡萄糖从头发酵生产L-茶氨酸的基因工程菌方法及应用:中国,CN114874959A[P].2022-04-27.FAN X G,JI Y Q,WEN H Y,et al.Pathway engineering of Escherichia coli for de novo fermentation production of L-theanine by utilizing glucose and its application: China,CN114874959A[P].2022-04-27.
[56]CHEN H G,ZHANG Y P J.Enzymatic regeneration and conservation of ATP: Challenges and opportunities[J].Critical Reviews in Biotechnology,2021,41(1):16-33.
[57]FAN X G,ZHANG T,JI Y Q,et al.Pathway engineering of Escherichia coli for one-step fermentative production of L-theanine from sugars and ethylamine[J].Metabolic Engineering Communications,2020,11: e00151.
[58]陆文渊.茶氨酸生物合成基因工程菌发酵工艺的研究[D].北京: 中国农业科学院,2008.LU W Y.Study on the fermentation process of the genetically engineered Escherichia coli bacteria strain for the biosynthesis of theanine[D].Beijing: Chinese Academy of Agricultural Sciences,2008.
[59]范晓光,季圆清,周宇航,等.一株大肠杆菌基因工程菌及其发酵生产L-茶氨酸的方法:中国,CN202111159099.6[P].2021-09-30.FAN X G,JI Y Q,ZHOU Y H,et al.An Escherichia coli engineering strain and its fermentation method for L-theanine production:China,CN202111159099.6[P].2021-09-30.
[60]张通.高产L-茶氨酸基因工程菌株的构建及其发酵条件优化[D].天津: 天津科技大学,2020.ZHANG T.Construction of high-yield L-theanine producer and optimization of its fermentation conditions[D].Tianjin: Tianjin University of Science and Technology,2020.
[61]谢华丽,孟祥燕,王培,等.一种L-茶氨酸高发酵单位、高糖酸转化率的发酵工艺:中国,CN117210515A[P].2023-10-30.XIE L H,MENG X Y,WANG P,et al.A fermentation process of high unit and conversion rate of L-theanine:China,CN117210515A[P].2023-10-30.
[62]傅嘉懿.Bacillus subtilis γ-谷氨酰转肽酶的发酵及其在L-茶氨酸制备中的应用[D].无锡: 江南大学,2015.FU J Y.Fermentation of γ-glutamyltranspeptidase from Bacillus subtilis and its application in L-theanine production[D].Wuxi:Jiangnan University,2015.
[63]叶朋,陈峰,钟迎东,等.一种制备L-茶氨酸的方法:中国,CN109593799A[P].2019-02-24.YE P,CHEN F,ZHONG Y D,et al.A method for preparing Ltheanine:China,CN109593799A[P].2019-02-24.
[64]李斌水,何连顺.一种微生物发酵制备L-茶氨酸的方法:中国,CN114480522A[P].2021-12-16.LI B S,HE L S.A method for the preparation of L-theanine by microbial fermentation:China,CN114480522A[P].2021-12-16.
[65]冯世红,王飞,刘福玲,等.一种发酵提取茶氨酸的方法:中国,CN114410504A[P].2021-12-15.FENG S H,WANG F,LIU F L,et al.A method for extracting theanine by fermentation: China,CN114410504A [ P].2021-12-15.
[66]张飞,王丽娟,刘寅,等.离子交换法提取酶促转化液中的L-茶氨酸[J].食品工业科技,2012,33 (15):251-253.ZHANG F,WANG L J,LIU Y,et al.Purification of L-theanine from enzymatic catalyzed reaction solution by ion-exchange resins[J].Science and Technology of Food Industry,2012,33 (15):251-253.
[67]袁华,高小红,闫志国,等.沉淀法从茶叶中提取茶氨酸[J].生物学通报,2007,42(5):46-48.YUAN H,GAO X H,YAN Z G,et al.Preparation of L-theanine from Chinese tea by means of precipitation technique[J].Bulletin of Biology,2007,42(5):46-48.
[68]欧阳平凯,汪群慧.电渗析及等电聚焦技术在氨基酸分离与纯化中的应用[J].化工进展,1991,10(2):31-34.OUYANG P K,WANG Q H.Application of electrodialysis and isoelectric focusing technology in separation and purification of amino acids[J].Chemical Industry and Engineering Progress,1991,10(2):31-34.
[69]陈艳,张亚萍,岳明珠.电渗析技术在氨基酸生产中的应用[J].水处理技术,2011,37(11): 10-14;25.CHEN Y,ZHANG Y P,YUE M Z.Application of electrodialysis in the production of amino acids[J].Technology of Water Treatment,2011,37(11): 10-14;25.
[70]马晓娟.酶法生产L-茶氨酸及其结晶与检测[D].南京: 南京师范大学,2014.MA X J.Enzymatic production of L-theanine and its crystallization and detection[D].Nanjing: Nanjing Normal University,2014.
[71]李定忠,沈宗毕.一种膜分离技术结合降温沉析法制备茶多糖、茶多酚、咖啡因和茶氨酸的工艺:中国,CN109251252A[P].2018-07-25.LI D Z,SHEN Z H.A process for the preparation of tea polysaccharides,tea polyphenols,caffeine and theanine by membrane separation technology combined with cooling precipitation method:China,CN109251252A[P].2018-07-25.
[72]林智,杨勇,谭俊峰,等.茶氨酸提取纯化工艺研究[J].天然产物研究与开发,2004,16(5):442-447.LIN Z,YANG Y,TAN J F,et al.Isolation and purification of theanine[J].Natural Product Research and Development,2004,16(5):442-447.
[73]张星海,周晓红,王岳飞.高纯度茶氨酸分离制备工艺研究[J].茶叶,2006,32(4):206-209.ZHANG X H,ZHOU X H,WANG Y F.Study on the preparation craft of high-purity theanine with prep-HPLC[J].Journal of Tea,2006,32(4):206-209.
[74]周兴华,范永军,周丙午.生物固相酶催化合成L-茶氨酸的生产工艺:中国,CN201210006627.9[P].2012-01-11.ZHOU X H,FAN Y J,ZHOU B W.Production process of L-theanine catalyzed by biological solid-phase enzyme: China,CN201210006627.9[P].2012-01-11.
[75]孟佩佩.食用茶氨酸提取精制与质量控制研究[D].广州: 广东药学院,2010.MENG P P.Research on extraction and purification of edibletheanine and quality control[D].Guangzhou: Guangdong Pharmaceutical University,2010.
[76]周楚仪,周文富.离子交换树脂分离茶多酚残液中茶氨酸的工艺研究[J].沈阳大学学报(自然科学版),2013,25(3):198-203.ZHOU C Y,ZHOU W F.Separation of natural theanine from tea polyphenols waste liquids by ion exchange[J].Journal of Shenyang University (Natural Science),2013,25(3):198-203.
[77]崔湘兴,龚雨顺,黄建安,等.717阴离子交换树脂吸附茶氨酸的热力学研究[J].湖南农业大学学报(自然科学版),2008,34(5):601-603.CUI X X,GONG Y S,HUANG J A,et al.Thermodynamics studies on adsorption of theanine on 717 anion exchange resin[J].Journal of Hunan Agricultural University (Natural Sciences),2008,34(5):601-603.
[78]张天明,谢鑫陟,杜守平,等.HZ-202阴离子交换树脂吸附茶氨酸的研究[J].安徽农业大学学报,2013,40(2):254-257.ZHANG T M,XIE X Z,DU S P,et al.Preliminary study on adsorption of L-theanine with anion exchange resin HZ-202[J].Journal of Anhui Agricultural University,2013,40(2):254-257.
[79]李伟,龙伟岸,黄华学.从甜茶中提取茶氨酸以及同时提取甜茶苷和茶多酚的方法:中国,CN108752231A[P].2018-06-28.LI W,YOU W A,HUANG H X.Method for extracting theanine and simultaneous extraction of rubusoside and tea polyphenols from sweet tea:China,CN108752231A[P].2018-06-28.
[80]顾峰.一种从新鲜茶叶中提取高纯度茶氨酸的方法:中国,CN104829486A[P].2015-06-04.GU F.Method for extracting high-purity theanine from fresh tea leaves:China,CN104829486A[P].2015-06-04.
[81]陈希书,张耀武,沈达,等.电渗析处理茶氨酸可行性研究[J].节能与环保,2020(12):77-78.CHEN X S,ZHANG Y W,SHEN D,et al.Feasibility study on theanine treatment by electrodialysis[J].Energy Conservation &Environmental Protection,2020(12):77-78.
[82]高聚霞. L-茶氨酸的一种纯化工艺:中国,CN102850235A[P].2011-06-28.GAO J X.A purification process of L-theanine: China,CN102850235A[P].2011-06-28.