塑料因其化学性质稳定、机械性能优异和易于加工等特性,迅速成为全球产量最高的合成聚合物之一。2024年,全球塑料产量达到了4.14亿t,并且年产量呈逐年递增趋势。尽管塑料为现代社会带来了诸多便利,但其广泛的使用和不当的管理使其在环境和人体中积累[1],给社会带来了严峻的挑战[2-5]。对于塑料的处理,目前普遍采用的物理填埋和化学回收方法不仅经济效益低还造成环境严重污染[6],因此社会对塑料循环经济和技术创新的需求愈发迫切,人类正面临着环境与健康的双重难题。
聚对苯二甲酸乙二醇酯(polyethylene terephthalate,PET)是一种热塑性聚酯,具有透明度高、强度优异、耐化学腐蚀等特性,广泛应用于饮料瓶、纺织纤维及包装材料。该材料于1941年由英国化学家WHINFIELD和DICKSON首次合成,现已成为环境中主要的塑料废弃物之一。PET的合成过程是先由对苯二甲酸(terephthalic acid,TPA)和乙二醇(ethylene glycol,EG)通过酯化反应生成单体对苯二甲酸双羟乙酯(bishydroxyethyl terephthalate,BHET),再通过聚合反应形成线性高分子链。由于其结构中的芳香环具有化学惰性,使得连接TPA和EG的酯键相较于其他塑料(如聚乙烯、聚丙烯、聚氯乙烯等)中的C—C键更易发生水解。
聚对苯二甲酸乙二醇酯水解酶(polyethylene terephthalate hydrolase,PETase)是一类能够催化PET中酯键水解的酶类,早期研究已经解释了PETase的解聚原理[7]为酰化和脱酰基化[8]。目前已被发现的PET水解酶有TfH[9]、 IsPETase[10]、BurPL[11] 和LCC[12]等。最近HAN等[13]还发现了2种新型PET水解酶PpPETase和ScPETase。PET在水解酶的催化下解聚成TPA、对苯二甲酸单羟乙酯(monohydroxyethyl terephthalate,MHET)、BHET和EG,其中TPA和EG为解聚终产物,可循环再利用,因而生物降解具有安全、经济又环保的优点。目前多数PET水解酶在中低温下对PET有解聚活性,且解聚效率低。而有研究表明,在PET玻璃化转变温度(65~70 ℃)左右的高温更有利于PET水解酶的解聚性能[14]。高温条件下PET材料结晶区的结构开始解离,变得更容易被酶分子接近和攻击,使得PET能够更有效地被水解,这极大地拓宽了可被酶法回收PET废料的范围。与此同时,高温环境能够有效抑制大多数杂菌的生长,对于连续的工业化解聚而言,避免了杂菌污染导致的反应效率下降、产物污染等问题,降低了操作复杂性和成本。此外,PET经水解后的终产物在高温下可以实现循环再利用,使得工业化流程中可省去冷却环节,减少能源消耗。耐热酶在高温下有较好的催化活性和稳定性[15],对pH、有机溶剂或重金属离子的耐受性更强,因此成为更理想的PET水解酶。
本研究以PET水解酶晶体结构(PDB:6ILW_A,Chain A)的氨基酸序列为模板,根据NCBI数据库对其进行序列同源性分析,使用ESPript 3.0服务器进行序列保守性分析,并运用新算法——“CLEAN(correlated linkage of enzyme activities and networks)”算法对重组酶实现功能预测。筛选出了来自于苏必利尔湖水华中嗜热菌[16]的疑似PET水解酶,并以其作为目的基因,pET28a(+)质粒作为载体,插入目的基因后转化至大肠杆菌(Escherichia coli)BL21(DE3)中进行可溶性异源表达。对经过Ni2+-NTA亲和层析柱纯化后的纯化酶进行酶学性质的表征,发现其为耐热PET水解酶,研究结果为PET的生物降解微生物或酶的有效开发应用提供了理论依据。
1 材料与方法
1.1 材料与试剂
Thermoleophilaceae bacterium 来源的PET水解酶(GenBank:MBJ7347705.1)的氨基酸序列来自NCBI数据库,由天霖生物科技(无锡)有限公司进行全基因合成;质粒pET28a(+)由天霖生物科技(无锡)有限公司提供;E.coli BL21(DE3)为本实验室保存。
PET颗粒(货号P875573、P885050、P885051)、硫酸卡那霉素(Kana)、异丙基-β-D-硫代半乳糖苷(isopropyl-beta-D-thiogalactoside,IPTG),酯酶底物对硝基苯丁酸酯(4-nitrophenyl butyrate,p-NPB)、对硝基苯己酸酯((4-nitrophenyl hexanoate,p-NPH)和对硝基苯辛酸酯(4-nitrophenyl caprylate,p-NPCa)、BES缓冲液,上海麦克林生化科技股份有限公司;酯酶底物4-硝基苯乙酸酯(4-nitrophenyl acetate,p-NPAc),西格玛奥德里奇(上海)贸易有限公司;铁锤超级裂菌液,南京艾思易生物科技有限公司;180 kDa蛋白预染Marker,一步法PAGE凝胶快速制备试剂盒,诺唯赞生物科技有限公司;TPA、MHET,上海阿拉丁生化科技股份有限公司;其他试剂均为国产分析纯。
LB液体培养基(g/L):酵母提取物5,胰蛋白胨10,氯化钠10,121 ℃高压灭菌20 min。固体培养基在此基础上加入2%(质量分数)的琼脂粉,121 ℃高压灭菌20 min。
1.2 仪器与设备
CF-RXⅡ高速冷冻离心机,日立(中国)有限公司;Spark多功能酶标仪,帝肯(上海)实验器材有限公司;MTC-100恒温金属浴,杭州米欧仪器有限公司;Nano-DSC,美国TA公司;Agilent HPLC 1260,安捷伦科技(中国)有限公司。
1.3 实验方法
1.3.1 酶的筛选与功能预测
1.3.1.1 同源序列检索
以PET水解酶晶体结构(PDB:6ILW_A,Chain A)的氨基酸序列为查询序列,通过NCBI BLASTp工具(参数设置:e-value≤1e-5,矩阵BLOSUM62)在非冗余蛋白数据库中检索嗜热微生物来源的同源序列,筛选标准为序列一致性≥40%,覆盖度≥85%。
1.3.1.2 系统发育分析
由MEGA11软件进行多序列比对和计算遗传距离,从1 000次重复中获得Bootstrap值,以最大似然法(maximum likelihood,ML)构建系统发育树[13],基于p-distance模型计算两两序列间的遗传分化距离,并使用Excel创建序列同一矩阵,生成热图可视化序列相似性矩阵。
1.3.1.3 序列保守性分析
通过ESPript 3.0服务器(https://espript.ibcp.fr)生成序列保守性分析图谱,设置参数:相似性评分阈值60%,参考结构6ILW_A的二级结构元素作为比对基准。
1.3.1.4 功能关联验证
运用CLEAN算法进行功能预测[17],基于酶活性与序列特征的欧氏距离构建功能相关性网络。通过比较候选酶与已知PET水解酶的功能簇分布(阈值设定:Z-score≥2.5,FDR <0.05),借助KEGG服务器(https://www.genome.jp/kegg/)验证其潜在的塑料降解功能。
1.3.2 重组质粒的构建与表达
从NCBI数据库中筛选获得嗜热油菌(Thermoleophilaceae bacterium) 来源的PET水解酶(TbPETase)氨基酸序列hypothetical protein JHC87-03920(MBJ7347705.1),使用Java密码子适应工具(Java Codon Adaptation Tool,JCat)对该氨基酸序列进行密码子优化。以质粒pET28a(+)作为载体骨架,设计BamHⅠ、HindⅢ限制性酶切位点作为克隆位点,委托天霖生物科技(无锡)有限公司合成重组质粒。通过热激法将重组质粒转化至E.coli BL21(DE3)感受态细胞后,选择测序正确的菌株在带有Kana(50 μg/mL)的LB固体培养基上进行划线,37 ℃恒温培养12 h进行单克隆筛选。挑取形态规则的单菌落接种至10 mL含Kana(50 μg/mL)的LB培养基中,于37 ℃、200 r/min条件下振荡预培养8~10 h至对数生长期。随后按2%接种量将菌液转移至150 mL含Kana(50 μg/mL)的LB培养基中,继续在同等条件下扩大培养3 h。当菌体浓度(OD600值)达到0.8~1.0时,加入IPTG,使其终浓度为0.5 mmol/L,16 ℃、200 r/min诱导表达6 h,最终通过离心(8 000 r/min,5 min)收集菌体并贮存于-80 ℃备用。
1.3.3 TbPETase的分离纯化与SDS-PAGE分析
将菌体重悬于含有150 mmol/L NaCl的20 mmol/L Tris-HCl缓冲液(pH值为8.0)中,按比例加入铁锤超级裂菌液(TieChui E. coli Lysis Buffer),于4 ℃恒温搅拌10 min完成细胞裂解。破碎后的菌液经低温离心(12 000 r/min,20 min,4 ℃)后收集上清液用于蛋白纯化。蛋白C端带有6 × His标签,将上清液加载至预平衡的Ni2+-NTA琼脂糖树脂层析柱,依次用含20、50 mmol/L咪唑的洗脱缓冲液梯度去除杂蛋白,最终以100 mmol/L咪唑溶液洗脱目的蛋白。使用截留分子质量为10 kDa的Millipore超滤管,将目的蛋白用20 mmol/L Tris-HCl缓冲液(pH 8.0)置换,并于4 ℃保存备用。产物经SDS-PAGE电泳进行分子质量验证,并采用BCA蛋白质定量试剂盒进行浓度测定。
1.3.4 基质辅助激光解析电离串联飞行时间质谱(matrix-assisted laser desorption-time of flight-mass spectrometry,MALDI-TOF-MS)分析
经SDS-PAGE验证获得单一目标条带后,使用刀片将目的蛋白条带切割成1 mm宽度的凝胶颗粒。依次进行脱色处理、还原烷基化、胶内酶切和肽段萃取,最终将纯化肽段样品点置于MALDI靶板,覆盖基质溶液后使用MALDI-TOF-MS进行检测。
1.3.5 PET水解活性测定
1.3.5.1 测定原理
TbPETase水解PET的原理包括4个基本步骤,分别是Ser-His-Asp催化三联体对底物启动的亲核攻击;酯键的断裂;活性位点水分子的亲和攻击和TbPETase的脱酰化[18]。主要水解产物为TPA和MHET,两者在240 nm处有吸收峰。
1.3.5.2 水解失重法
将PET颗粒经液氮冷冻研磨后过筛,获得PET微粒。使用前将PET微粒依次用0.1%(体积分数)SDS溶液超声清洗及超纯水冲洗3次,60 ℃真空干燥至恒重。称取50 mg(精确到0.1 mg)的预处理PET微粒(记为m1)加入3 mL纯酶(20 mmol/L Tris-HCl缓冲液,pH 8.0,4.5 mg/mL),将混合体系在55 ℃下持续振荡反应48 h。反应结束后通过0.22 μm滤膜分离未降解PET残渣,用10 mL去离子水洗涤滤渣3次,经60 ℃真空干燥24 h至恒重,记录水解后塑料微粒的质量(记为m2)。每个实验组设置3次重复实验。水解率计算如公式(1)所示:
式中:m1,初始PET质量,mg;m2,水解后残留质量,mg。
1.3.5.3 HPLC分析法
水解反应条件与水解失重法中一致。将反应后的水解溶液经0.22 μm滤膜过滤,配制成供试样品。将TPA和MHET分别溶于乙腈,经0.45 μm滤膜过滤,配制成标准品溶液。分离产物所用色谱柱为Discovery HS C18柱,上样量10 μL。分离所用流动相为0.1% (体积分数)的甲酸溶液(A相)和甲醇(B相),以甲醇梯度(30%~90%)进行分离;总流速是0.5 mL/min,检测波长为240 nm,柱温为30 ℃。
1.3.6 TbPETase酶活性测定
采用p-NPAc比色法测定TbPETase酶活性。无色底物p-NPAc在酶催化下水解生成黄色产物对硝基苯酚(4-nitrophenol,p-NP),该产物在404 nm波长处具有特征吸收峰。基于 p-NP浓度与吸光度(A404nm)的线性关系(图1),可以通过监测A404nm 值变化计算酶活性[19]。具体操作步骤如下:在离心管中加入440 μL缓冲液(50 mmol/L BES,pH 7.0)、50 μL p-NPAc(20 mmol/L,溶于乙腈)以及10 μL酶液,混合均匀后于55 ℃温浴5 min,随后立即置于冰上终止反应。取150 μL反应液于酶标板中,使用酶标仪于404 nm处测得吸光度值,以空白反应(不含酶的缓冲液为对照)扣除背景干扰。将吸光度值代入标准曲线得到p-NP浓度即反映酶活性。以上反应均设置3次平行实验。
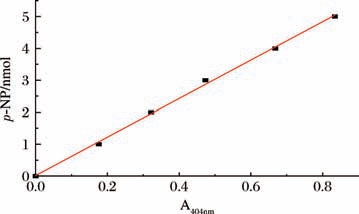
图1 p-NP标准曲线
Fig.1 Standard curve of p-NP
1.3.7 底物选择与反应动力学分析
选取4种硝基苯酯类底物:p-NPAc、p-NPB、p-NPH和p-NPCa,分别配制成20 mmol/L储备液,与酶液在55 ℃下持续反应(间隔7 min,持续35 min),测定酶活性。筛选出相对较优的2种底物进行后续动力学分析。将底物配制成5~45 mmol/L浓度梯度(间隔5 mmol/L)的溶液,在55 ℃下与酶液反应7 min,通过产物p-NP的生成速率计算其初始反应速率,利用Origin软件中的Michaelis-Menten方程进行非线性曲线拟合,得到其Km和Vmax值。
1.3.8 TbPETase的表达优化
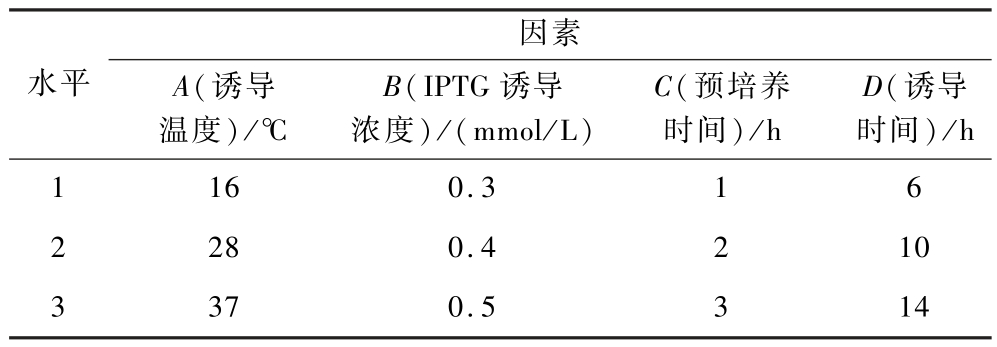
采用L9(34)正交试验设计,以每克菌体经纯化后得到的纯化酶活性为指标,系统考察诱导温度(℃)、IPTG终浓度(mmol/L)、诱导前预培养时间(h)及诱导时间(h)4组关键参数对TbPETase表达的影响,如表1所示。经IBM SPSS分析实验结果,得出最佳诱导培养条件。
表1 L9(34)正交试验因素与水平表
Table 1 Factors and levels of the L9(34) orthogonal design
1.3.9 TbPETase的酶学性质
1.3.9.1 纳米差示扫描热量法(nano-differential scanning calorimetry,nano-DSC)分析
对溶解于缓冲液中的纯化酶(1 mg/mL)进行脱气处理。设定温度为20~100 ℃、升温速率1 ℃/min,先扫描空白缓冲液记录基线,再将酶液注入样品池进行扫描。使用Nano Analyze数据分析软件扣除基线后,通过变性峰顶点确定熔解温度(Tm),积分峰面积并结合校准系数计算焓变值(ΔH)。
1.3.9.2 最适反应温度的测定
将纯化后的TbPETase(20 mmol/L Tris-HCl缓冲液,pH值为8.0,4.5 mg/mL)分装至1.5 mL离心管中,分别在20、30、40、50、60、70 ℃的恒温金属浴中孵育10、20、30 min后测定酶活性,根据p-NP标准曲线计算出p-NP浓度以反映酶活性。
1.3.9.3 半衰期测定
将TbPETase纯化酶(20 mmol/L Tris-HCl缓冲液,pH值为8.0,4.5 mg/mL)置于55 ℃的恒温水浴锅中温浴11 h,每隔1 h进行取样并测定酶活性,将未经热处理的酶的活性设为100%,计算不同时间下的相对酶活性,酶活性衰减至50%所需要的时间,即为此温度下的半衰期。
1.4 数据处理
利用Excel进行“平均值± 标准差”计算,使用Origin 2021进行数据可视化处理,使用SPSS软件进行显著性分析(P <0.05)。
2 结果与分析
2.1 酶的筛选与功能预测
为了筛选与鉴定PET水解酶,使用NCBI数据库进行序列同源性分析(图2-a)并用ESPript 3.0服务器对序列保守性加以分析。从不同种属中选取了31种假定PET水解酶同源蛋白,其中大多数未被记录PET降解能力。为31种候选PET水解酶构建系统发育树,鉴于嗜热酶系在工业处理中的热稳定性优势,最终选定嗜热菌来源的TbPETase进行后续研究。如图2-b所示,借助Discovery Studio软件将TbPETase与PET水解酶晶体结构作序列比对,得到序列一致性为43.2%。使用CLEAN算法进行功能注释,预测出TbPETase的酶学分类号为EC 3.1.1.101,后经KEGG服务器检索确认,EC 3.1.1.101对应功能注释为“PET水解酶”,与目标酶功能一致。因此初步预测TbPETase具有PET水解功能。
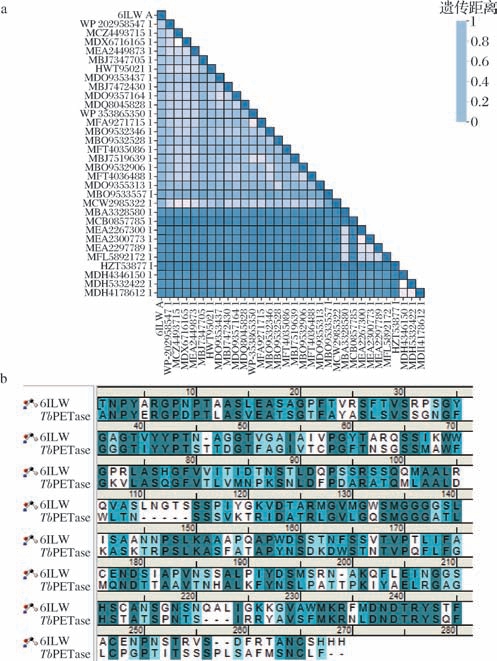
图2 序列相似性与一致性分析
Fig.2 Sequence similarity and identity analysis
a-同源序列相似性矩阵;b-PET水解酶晶体结构与TbPETase序列比对结果
2.2 TbPETase的构建、表达与纯化
使用Java密码子适应工具JCat对该氨基酸序列进行密码子优化[20],消除了某些非必需限制性内切酶识别位点,并且在密码子优化的DNA序列中移除了潜在转录终止信号,同时适配宿主菌E. coli BL21(DE3)密码子偏好性,提高了重组表达效率。如图3-a所示,以质粒pET28a(+)作为载体骨架,设计BamHⅠ、HindⅢ限制性酶切位点作为克隆位点构建出重组质粒。以大肠杆菌作为宿主,利用组氨酸标签对蛋白进行纯化。SDS-PAGE电泳验证结果如图3-b所示,纯化条带单一,说明蛋白纯度较高;分子质量约为28.7 kDa,与理论值相符。MALDI-TOF-MS分析结果如图4所示,5条肽段匹配得分有5个可信度单独超过阈值分数,蛋白得分237分,质谱结果显示纯化得到的重组酶与NCBI数据库中预测的目标酶序列基本相同。综上表明,本实验实现了对TbPETase的成功构建、表达与纯化。
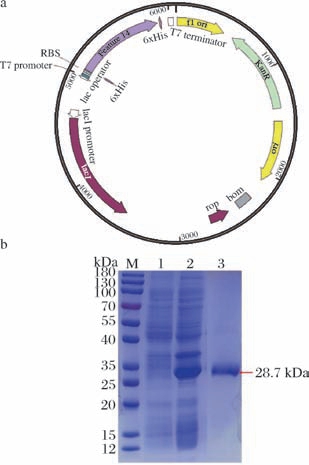
图3 重组质粒的构建与表达
Fig.3 Construction and expression of recombinant plasmids
M-Marker;泳道1-空载;泳道2-重组酶粗酶液;泳道3-纯酶。a-重组质粒构建图谱;b-TbPETase的SDS-PAGE分析
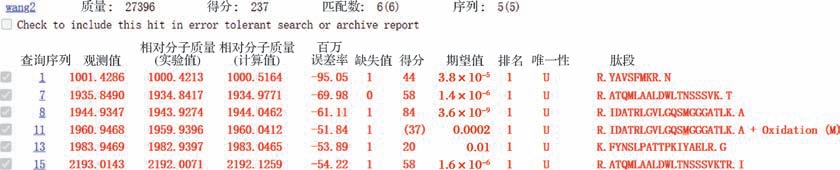
图4 TbPETase的MALDI-TOF-MS分析结果
Fig.4 MALDI-TOF-MS identification of the recombinant TbPETase
2.3 TbPETase的PET水解活性
TbPETase对PET微粒具有酶解作用。取一定质量的PET微粒与TbPETase在55 ℃恒温条件下反应48 h,如图5-a所示,3组实验中,3种不同的PET微粒的质量均有不同程度的损失,水解率约为10%~13%。将反应后的溶液经HPLC检测,结果如图5-b所示,反应液中检测出的吸收峰与TPA和MHET标准品的吸收峰分别对应,由此说明TbPETase对PET微粒能发生水解反应,水解产物为TPA和MHET。
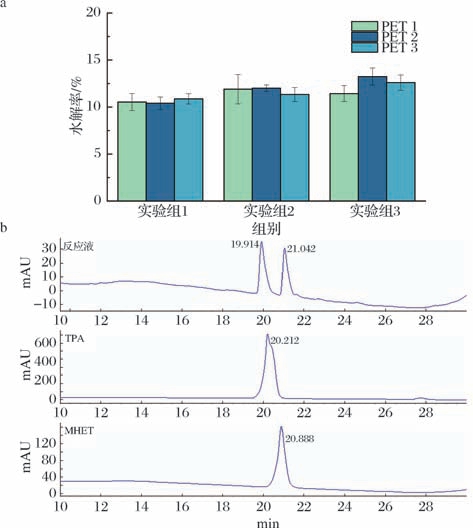
图5 TbPETase的PET水解活性
Fig.5 PET hydrolysis activity of TbPETase
a-三种PET微粒经TbPETase水解48 h失重后测得水解率;b-HPLC分析结果
2.4 TbPETase的底物选择与反应动力学分析
4种硝基苯酯类底物中, p-NPAc是测定TbPETase酶学反应的最适底物。如图6-a所示,在相同的底物浓度下,随着时间的延长,p-NPAc、p-NPB、p-NPH作为反应底物时产物p-NP也不断增加。其中p-NPAc组与p-NPB组的p-NP生成速率优于其他组。分别以p-NPAc、p-NPB作为酶学反应底物测定TbPETase的反应动力学特性,如图6-a、图6-b所示,当不同浓度p-NPAc为底物时,测得米氏方程Y=12.363 59X/(4.225 74 +X),米氏常数Km 为4.226 mmol/L,Vmax 为12.364 mmol/(L·min),Kcat 为818.85 min-1,得Kcat/Km为193 776.729 L/(mol·min);以不同浓度 p-NPB为底物时,测得米氏方程Y=1.424 73X/(22.594 28 + X),米氏常数Km 为22.594 mmol/L,Vmax 为1.425 mmol/(L min),Kcat 为94.36 min-1,计算得Kcat/Km为4 176.321 L/(mol·min)。说明p-NPAc扩散速率较快,与TbPETase的亲和力更强。
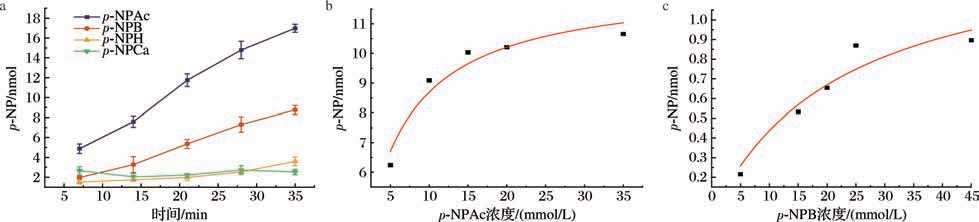
图6 TbPETase的底物选择与反应动力学参数
Fig.6 Substrate selection and kinetic parameters of TbPETase
a-纯酶与不同酯酶底物反应不同时间的酶活性;b-不同浓度的p-NPAc作为底物时的酶反应动力学参数;c-不同浓度的p-NPB作为底物时的酶反应动力学参数
2.5 TbPETase的表达优化
为优化TbPETase在重组菌株中的表达,设计4因素3水平的正交试验,每组设置3次平行实验。IBM SPSS分析实验结果如表2所示。 F 值用于衡量组间方差与组内方差的比值,其数值越大,表明自变量对因变量的影响越显著。结果表明,影响TbPETase表达水平的显著程度依次为:诱导温度>IPTG诱导浓度>诱导时间>预培养时间。经IBM SPSS分析,得出最佳诱导培养条件为:诱导温度16 ℃,IPTG终浓度0.5 mmol/L,预培养时间3 h,诱导时间6 h。以此诱导条件对重组酶进行表达纯化,优化后重组酶活性为8.099 U/mL,相较于未优化表达条件(诱导温度37 ℃,IPTG终浓度0.2 mmol/L,预培养时间2 h,诱导时间7 h)前的重组酶活性(2.125 U/mL)提高了3.81倍。
表2 主体间效应检验结果表
Table 2 Results of the between-subjects effects test
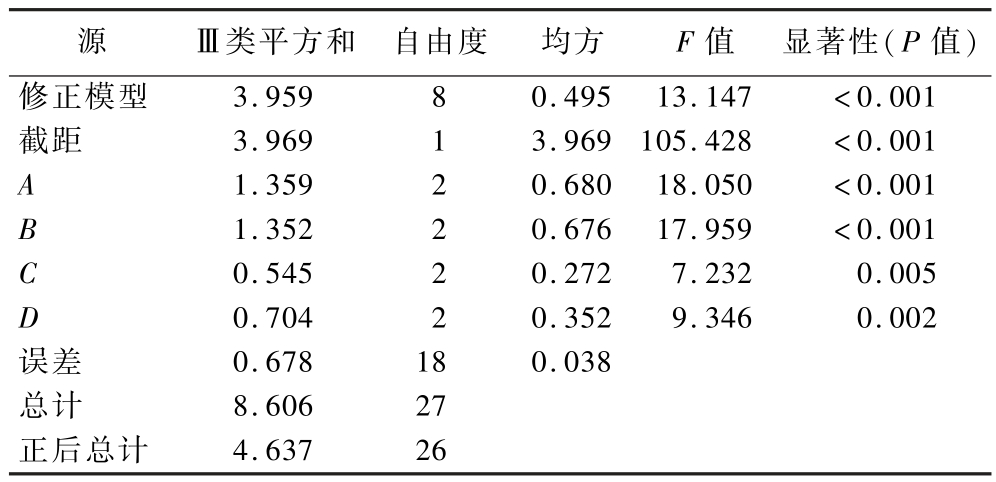
注:F 值,该检验的临界值,高F 值表明组间均值的可变性比组内可变性较大;P 值,反对无效假设的证据,P <0.05意味着有统计学意义。
2.6 TbPETase的酶学性质
2.6.1 TbPETase的熔解温度
通过Nano Analyze软件分析Nano-DSC检测结果,如图7所示,纯化酶的Tm 为64.87 ℃,ΔH 为737 kJ/mol,变性熵(ΔH/Tm)为11.361 kJ/(K·mol)。与已报道的中温型PETase(Tm=58~62 ℃)相比具有显著热稳定性优势,进一步通过Arrhenius方程计算得到活化能(Ea)为289 kJ/mol,证实该酶在工业级PET水解温度下仍保持良好构象稳定性。
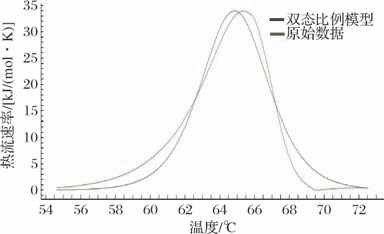
图7 TbPETase的Tm 分 析
Fig.7 Tm of TbPETase
2.6.2 TbPETase的最适反应温度与半衰期
TbPETase的最适温度为55 ℃。如图8-a所示,随着温度的上升,TbPETase与底物的反应速率加快,50~60 ℃时趋于稳定,60 ℃后酶活性开始下降;在同一温度下,温浴时间越长,酶活性越高。由图8-b可知,在最适温度55 ℃下随着时间的延长,TbPETase的残留酶活性缓慢下降,7 h相对酶活性降至50%,说明其半衰期约为7 h。
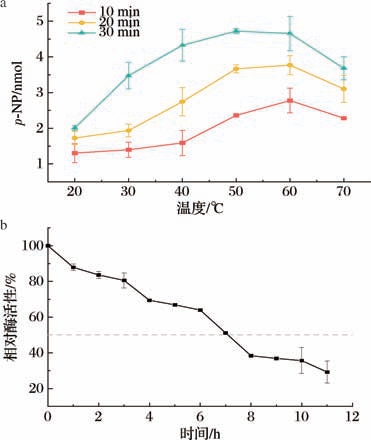
图8 TbPETase的最适反应温度与半衰期
Fig.8 Optimal reaction temperature and half-life of TbPETase
a-TbPETase在不同温度和不同时间下的酶活性;b-TbPETase的半衰期分析
3 结论与讨论
本研究以PET水解酶晶体结构(PDB:6ILW_A,Chain A)的氨基酸序列为基础,筛选出来源于Thermoleophilaceae bacterium 的假定PET水解酶(TbPETase)的基因。使用算法工具对重组酶进行功能预测并完成异源重组表达,发现该酶具有水解PET的功能。初步对重组酶进行功能表征并探究了该酶的酶学性质,研究表明TbPETase的Tm 为64.87 ℃,ΔH为737 kJ/mol。该酶Tm显著高于目前研究最为广泛的、来源于中温菌Ideonella sakaiensis 的IsPETase(Tm=40~55 ℃,易失活),表明其在最适温度下的结构稳定性更优,有效避免了中温酶在较高温度下快速失活的问题。但与其他嗜热菌来源的PETase相比,TbPETase的热稳定性优势并不突出,这限制了其在更高温度(>60 ℃)下的PET水解潜力。 TbPETase在以p-NPAc为底物时,Kcat/Km 为193 776.729 L/(mol·min),其催化效率显著高于野生型IsPETase对p-NPAc的催化效率,这表明TbPETase对酯酶底物具有天然的高催化活性,是该酶一个突出优势,但不及工程化改造后的IsPETase突变体(DuraPETase),表明TbPETase的活性位点仍具有改造潜力。 TbPETase最适反应温度为55 ℃,此温度下的半衰期约7 h,说明该酶可在50~60 ℃下稳定运行反应体系,减少冷却成本。此外,TbPETase对PET微粒的48 h降解率约为10%~13%,对比48 h降解率仅1%的野生型中温水解酶IsPETase,TbPETase水解效率更优,这可能与酶的持续活性或底物通透性有关。虽然该酶与目前已被报道的大部分PET水解酶相比,有较为良好的热稳定性,但与嗜热菌来源的酶相比,其稳定性优势不明显,且其降解效率仍低于部分工程化改造的PET水解酶。例如,一些高度优化的LCC突变体(如FAST-PETase)或IsPETase突变体在温和条件下对PET薄膜或微粒的48 h降解率可达到30%甚至更高水平。因此在生产应用中,该酶的热稳定性与水解效率还有待改善。尽管异源表达的重组酶在应用中具有许多优势,但其催化效率、可溶性表达水平及热稳定性指标仍然不及已成熟的商用酶。针对此项不足之处,后续研究将基于结构与功能的关系理性设计,运用定向改造的手段同步提升该重组酶的热稳定性和水解效率等,以期望获得优势更加全面的PET水解酶,为创造PET生物降解生物催化剂提供更多可能性。
[1]SUN X D,YUAN X Z,JIA Y B,et al.Differentially charged nanoplastics demonstrate distinct accumulation in Arabidopsis thaliana[J].Nature Nanotechnology,2020,15(9):755-760.
[2]JAMBECK J R,GEYER R,WILCOX C,et al.Plastic waste inputs from land into the ocean [J].Science,2015,347(6223):768-771.
[3]ERIKSEN M,LEBRETON L C M,CARSON H S,et al.Plastic pollution in the world’s oceans:More than 5 trillion plastic pieces weighing over 250,000 tons afloat at sea[J].PLoS One,2014,9(12):e111913.
[4]QI Y L,YANG X M,PELAEZ A M,et al.Macro-and micro-plastics in soil-plant system:Effects of plastic mulch film residues on wheat (Triticum aestivum) growth [J].Science of the Total Environment,2018,645:1048-1056.
[5]BORRELLE S B,RINGMA J,LAW K L,et al.Predicted growth in plastic waste exceeds efforts to mitigate plastic pollution [J].Science,2020,369(6510):1515-1518.
[6]ELLIS L D,RORRER N A,SULLIVAN K P,et al.Chemical and biological catalysis for plastics recycling and upcycling [J].Nature Catalysis,2021,4(7):539-556.
[7]HAN X,LIU W D,HUANG J W,et al.Structural insight into catalytic mechanism of PET hydrolase [J].Nature Communications,2017,8(1):2106.
[8]ZHENG M N,LI Y W,DONG W L,et al.Depolymerase-catalyzed polyethylene terephthalate hydrolysis:A unified mechanism revealed by quantum mechanics/molecular mechanics analysis[J].ACS Sustainable Chemistry &Engineering,2022,10(22):7341-7348.
[9]MÜLLER R J,SCHRADER H,PROFE J,et al.Enzymatic degradation of poly(ethylene terephthalate):Rapid hydrolyse using a hydrolase from T.fusca[J].Macromolecular Rapid Communications,2005,26(17):1400-1405.
[10]YOSHIDAS,HIRAGA K,TAKEHANA T,et al.A bacterium that degrades and assimilates poly(ethylene terephthalate) [J].Science,2016,351(6278):1196-1199.
[11]CHEN C C,HAN X,LI X,et al.General features to enhance enzymatic activity of poly(ethylene terephthalate) hydrolysis [J].Nature Catalysis,2021,4(5):425-430.
[12]SULAIMAN S,YAMATO S,KANAYA E,et al.Isolation of a novel cutinase homolog with polyethylene terephthalate-degrading activity from leaf-branch compost by using a metagenomic approach[J].Applied and Environmental Microbiology,2012,78(5):1556-1562.
[13]HAN Z Y,NINA M R H,ZHANG X Y,et al.Discovery and characterization of two novel polyethylene terephthalate hydrolases:One from a bacterium identified in human feces and one from the Streptomyces genus [J].Journal of Hazardous Materials,2024,472:134532.
[14]THOMSEN T B,HUNT C J,MEYER A S.Influence of substrate crystallinity and glass transition temperature on enzymatic degradation of polyethylene terephthalate (PET) [J].New Biotechnology,2022,69:28-35.
[15]ERICKSON E,GADO J E,AVILÁN L,et al.Sourcing thermotolerant poly(ethylene terephthalate) hydrolase scaffolds from natural diversity [J].Nature Communications,2022,13(1):7850.
[16]SHEIK C S,NATWORA K E,ALEXSON E E,et al.Dolichospermum blooms in lake superior:DNA-based approach provides insight to the past,present and future of blooms [J].Journal of Great Lakes Research,2022,48(5):1191-1205.
[17]YU T H,CUI H Y,LI J C,et al.Enzyme function prediction using contrastive learning [J].Science,2023,379(6639):1358-1363.
[18]FENG S S,YUE Y,ZHENG M N,et al. IsPETase-and IsMHETase-catalyzed cascade degradation mechanism toward polyethylene terephthalate[J].ACS Sustainable Chemistry &Engineering,2021,9(29):9823-9832.
[19]JAEGER K E,KOVACIC F.Determination of Lipolytic Enzyme Activities[M].Pseudomonas Methods and Protocols.New York,NY;Springer New York,2014:111-134.
[20]GROTE A,HILLER K,SCHEER M,et al.JCat:A novel tool to adapt Codon usage of a target gene to its potential expression host[J].Nucleic Acids Research,2005,33(WebServerissue):W526-W531.