鱼油作为ω-3多不饱和脂肪酸的重要来源,因其在调节血脂、抗炎及神经保护等方面的显著功效,被广泛应用于功能性食品、医药和营养补充剂领域[1-3]。然而,鱼油的强疏水性导致其体内生物利用度低,且分子中高度不饱和双键结构使其在加工和贮存过程中易发生氧化降解和水解酸败,这不仅会影响鱼油产品的品质,还可能导致潜在的安全性问题[4-5]。因此,开发高效稳定的鱼油递送体系以提高其生物可及性和稳定性,已成为食品科学与营养递送技术领域亟待解决的关键问题。
近年来,自乳化制剂因其能够显著改善水不溶性成分的生物利用度而备受关注[6]。它是通过表面活性剂与油相的协同作用,在温和条件下自发形成纳米或微米级乳滴,大幅增加脂质的比表面积,从而促进油脂与消化酶的接触效率[7-8]。然而,传统自乳化制剂多依赖聚山梨酯等合成表面活性剂,尽管乳化性能优异,但长期摄入可能引发肠道屏障的功能障碍,严重制约其在功能性食品中的应用潜力[9]。
磷脂作为天然两亲性分子,兼具乳化功能与生物相容性,其作为生物膜的主要成分,被认为是具有出色生物相容性的天然表面活性剂,是构建绿色自乳化体系的理想选择[10-13]。磷脂的亲水头部与疏水尾部赋予其双亲性[14],这种结构使其能在油水界面自发组装(亲水头部朝向水相,疏水尾部插入油相),富集于油水界面并降低界面张力,从而促进形成细小且分布均匀的乳液液滴[15]。研究表明,磷脂可通过降低油水界面张力促进乳滴形成,并通过疏水相互作用稳定乳滴结构[16-18]。然而,磷脂的自乳化性能显著受其分子结构(如两亲性、疏水尾部特性、亲水头部基团特性、分子形状等)、浓度以及与其他组分的协同作用影响[19]。当前研究主要集中于使用合成表面活性剂(如Tween系列)构建的自乳化体系。与之相比,磷脂作为天然成分,具有卓越的生物相容性和安全性。此外,磷脂形成的液晶态界面膜通常比传统合成表面活性剂形成的液态膜更具刚性、致密且黏弹性更强,可提供更有效的位阻稳定作用,从而使磷脂基自乳化体系在物理稳定性方面展现出显著优势。然而目前关于天然磷脂在鱼油自乳化过程中的作用效果及其对鱼油体内吸收能力的调控仍缺乏系统研究。
基于此,本研究以鱼油为研究对象,系统构建鱼油-磷脂自乳化体系,并通过流变学、离心稳定性分析、微观结构观察以及药代动力学实验,系统评价不同鱼油-磷脂自乳化体系的稳定性和ω-3多不饱和脂肪酸的体内吸收能力。本研究将为高生物利用度鱼油产品的开发提供新思路。
1 材料与方法
1.1 材料与试剂
鱼油[3种型号:18/12 EE、5/25 EE、18/12 TG,EE为乙酯型鱼油,TG为甘油三酯型鱼油,18/12和5/25代表二十碳五烯酸(eicosapentaenoic acid,EPA) 与二十二碳六烯酸(docosahexaenoic acid,DHA)在鱼油中的含量之比],浙江新维士生物科技有限公司;磷脂,浙江芮立生物技术有限责任公司。
1.2 仪器与设备
LSM710激光共聚焦显微镜,德国Zeiss公司;Mastersizer 3000马尔文微米粒度仪、Malvern ZSP马尔文纳米电位仪,英国马尔文仪器有限公司;LUMi-Sizer稳定性分析仪,德国LUMGmbH有限公司;MCR302流变仪,美国安东帕有限公司;DSA25界面张力仪,德国Krüss GmbH公司。
1.3 实验方法
1.3.1 鱼油-磷脂自乳化液的制备
将磷脂置于85 ℃真空环境中搅拌60 min,待其完全液化(黏度小于500 Pa·s,呈透明均一态)后,将磷脂按照不同剂量(0%、0.5%、3%、6%、10%,质量分数)添加到18/12 EE型鱼油中,然后在85 ℃下以12 000 r/min高速剪切分散5 min,随后在70 ℃下经120 MPa高压微射流循环处理3次,制备得到鱼油-磷脂自乳化液。
1.3.2 鱼油-磷脂自乳化乳液的制备及稳定性观察
将1.3.1节中制备的鱼油-磷脂自乳化液与水按1∶2(质量比)比例混合。首先于自然光下目视评估静态体系的相分离行为及自乳化液的透明度特征;随后对混合体系涡旋振荡处理(30 s,2 500 r/min),形成鱼油-磷脂自乳化乳液并观察其表观形态。通过对比振荡前后体系的表观差异(拍照记录),初步评估磷脂添加量对鱼油-磷脂自乳化乳液稳定性的影响。
1.3.3 界面张力的测定
测试方法参考FENG等[20]的方法并略作修改。将18/12 EE型纯鱼油注入光学透明样品池中,然后将不同浓度的磷脂水溶液滴入含有鱼油的样品池中,利用水滴形状分析软件计算不同浓度磷脂水溶液与鱼油间的界面张力值。
1.3.4 自乳化乳液的流变特性分析
使用流变仪测量鱼油-磷脂自乳化乳液从剪切速率0.01 s-1增加到100 s-1 时的表观黏度变化。将适量乳液均匀添加至流变仪上,等待5 min以达到设定温度。线性黏弹性区通过动态应变扫描得到确认。在0.01~100 rad/s的角频率范围内以0.5%的固定剪切应变值进行频率扫描测试样品的储能模量(G′)和损耗模量(G″)。
1.3.5 共聚焦激光扫描显微镜
将不同的鱼油-磷脂自乳化乳液经尼罗红染色后,制备成样品在共聚焦激光扫描显微镜下进行观察。共聚焦激光扫描显微镜的波长设置为488 nm,观察不同乳液样品的液滴大小以及分布情况。
1.3.6 自乳化乳液的粒径和ζ-电位测定
采用微米粒度仪测定鱼油-磷脂自乳化乳液的液滴尺寸,粒度分布结果来自仪器软件中的激光散射模式。将不同类型的自乳化乳液滴入测量池中,旋涡1 min使液滴均匀分散,直至遮光率达8%~15%,开始测定乳液粒径大小;
将鱼油-磷脂自乳化乳液加水稀释到适当浓度。然后,取样加入到纳米电位仪配套的样品池中,确保样品分布均匀且无气泡存在,随后测定其不同类型自乳化乳液的ζ-电位。
1.3.7 离心稳定性测定
使用稳定性分析仪进行测试。将适量鱼油-磷脂自乳化乳液加入到与仪器相配套的直径为2 mm的样品管中,然后将样品管以1 500 r/min离心15 min,并记录样品透光率曲线变化情况、外观形态和不稳定指数。
1.3.8 18/12 TG和5/25 EE型鱼油关键指标测定
由上述实验确定18/12 EE型鱼油的最适磷脂添加量后,按照此最适磷脂浓度加入18/12 TG和5/25 EE型鱼油,制备自乳化乳液(方法同1.3.1节和1.3.2节)并对乳液外观进行观察。采用共聚焦激光扫描显微镜对不同类型的自乳化鱼油乳液微观结构进行观察(方法同1.3.5节),再测定其粒径、ζ-电位以及离心稳定性(方法同1.3.6节和1.3.7节),并将结果与18/12 EE型鱼油自乳化乳液进行比较。
1.3.9 不同鱼油-磷脂自乳化乳液及其原料鱼油的EPA和DHA体内吸收研究
1.3.9.1 动物实验分组及灌胃
将30只SD大鼠随机分为6组,每组5只(均为雄性),实验前12 h禁食。该研究动物实验已获得湖北工业大学科研伦理与科技安全委员会批准(批准文号:HBUT20250018)。按照质量比1∶2的比例将3种鱼油-磷脂自乳化液与超纯水混合摇匀,形成自乳化乳液后用于大鼠灌胃。以3种类型的原料鱼油为对照,单次灌胃剂量为600 mg/kg鱼油,进行药代动力学评价,所有灌胃样品均现配现用[21]。
1.3.9.2 大鼠血浆的采集
基于前期预实验结果设定大鼠取血时间点,旨在完整表征EPA和DHA在大鼠体内的药代动力学特征。各组大鼠分别于给药前(0 h)及给药后0.5、1、1.5、2、3、4、6、8、10、12和24 h各时间点采血。每个时间点从大鼠尾部静脉采集0.5 mL全血,置于含肝素钠的抗凝管中,轻轻振摇以充分混匀血液与抗凝剂。采集的血样立即置于冰盒中低温避光保存。血样采集后需在30 min内采用冷冻离心机(3 000 r/min,10 min)分离血浆。分离后的血浆迅速转移至冻存管中,存放于-80 ℃冰箱中,供后续GC-MS分析。自血液采集至样品转入-80 ℃冰箱的全过程均控制在1~1.5 h完成。所有血浆样品均于采集后30 d内通过GC-MS方法完成检测,确保样品的稳定性和实验数据的可靠性。
1.3.9.3 大鼠血浆中EPA和DHA的浓度检测
参考孙素玲[22]的方法并作适当修改。
首先对收集的血浆样品进行衍生化处理,在玻璃试管中加入50 μL 1 mg/mL内标溶液(二十三烷酸甲酯),用氮气吹干后加入200 μL待测血浆样品,混匀后加入2 mL含5%的硫酸甲醇溶液,充入氮气密封,混匀后在70 ℃下反应60 min,待反应体系冷却至室温后,加入2 mL 0.9%的生理盐水和1 mL正己烷,涡旋混合5 min,在4 ℃下以5 000 r/min离心5 min,取上层有机相,该萃取步骤重复2次,合并所有正己烷相,用氮气吹干后加入500 μL色谱级正己烷溶解,溶解后的样品过0.22 μm滤头后收集在2 mL棕色进样瓶中用于GC-MS分析。
色谱条件:采用Agilent 7890A/597SC-GCIMSD型色谱柱(30 m ×,0.25 mm,0.25 μm),升温程序为:初始温度设定为200 ℃,保持1 min后,以10 ℃/min的升温速率升至250 ℃,并维持8 min。进样口温度设定为250 ℃,分流比为5∶1。载气为高纯氦气(纯度≥99.999%),流速为1.0 mL/min。进样量为1 μL。质谱条件:采用电子轰击(EI)电离源,离子源温度设定为250 ℃,接口温度为240 ℃。溶剂延迟时间为3 min,扫描模式为选择离子监测模式。监测的特征离子m/z为74.00、79.00、87.00、93.00、119.00和143.00。
1.4 数据分析
所有实验均重复3次,实验结果以“平均值±标准差”表示。使用SPSS 26.0对实验数据进行显著性差异分析(显著水平:P<0.05),用Origin 2024进行绘图。
2 结果与分析
2.1 鱼油-磷脂自乳化乳液外观
如图1-a所示,随着鱼油中磷脂添加量的增加,鱼油自乳化液的颜色不断加深,但整体保持稳定,油相无明显分层现象。经过充分振荡摇匀后,可见未添加磷脂的鱼油无法形成乳液,有明显的分层。磷脂添加量为0.5%的自乳化液形成的乳液出现分层现象,而磷脂添加量为3%、6%、10%的样品组充分振荡后可以形成外观稳定、均一、无分层的自乳化乳液(1-b)。因此,推测这3种(3%、6%、10%)磷脂添加量形成了较为稳定的鱼油-磷脂自乳化体系。

图1 振荡前后鱼油-磷脂自乳液/水体系的外观图
Fig.1 Appearance pictures of fish oil-phospholipid self-emulsifying emulsion
a-振荡前鱼油-磷脂自乳化液/水体系;b-振荡后鱼油-磷脂自乳化液/水体系
2.2 界面张力
由图2可知,所有样品组的油-水界面张力均随吸附时间的延长而逐渐降低。值得注意的是,与未添加磷脂的对照组相比,加入磷脂后油-水间的界面张力显著降低,且随着水相中磷脂质量浓度的增加,油-水界面张力不断下降。这是因为磷脂具有两亲性结构,其疏水尾部可与鱼油相容,而亲水头部倾向于在油水界面定向排列,从而降低油水界面张力。这与YIN等[23]报道的关于不同种类和浓度磷脂对鱼油乳化稳定性的研究结果相似。
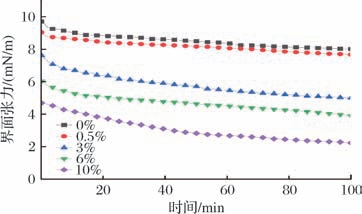
图2 不同浓度磷脂水溶液与鱼油间的界面张力
Fig.2 The surface tension between phospholipids of different concentrations and fish oil
2.3 流变特性
图3-a中的数据显示,鱼油-磷脂自乳化乳液的初始黏度与其磷脂添加量成正比,这可能由于:a)随着磷脂添加量的增加,自乳化乳液的液滴尺寸减小,液滴表面吸附更多的磷脂分子,磷脂分子排列更紧密,形成更厚、更刚性的界面膜,从而导致液滴空间位阻增大,液滴有效体积分数增大,进而提高了自乳化体系的黏度;b)此外,随着磷脂添加量的增加,一部分多余的磷脂在连续相中形成胶束或者囊泡,增大连续相自身的黏度,从而使乳液的初始黏度增大[24]。随着剪切速率的增加,所有乳液的表观黏度逐渐降低,表现出剪切稀化特性,相较于对照组,10%磷脂处理组乳液的黏度下降幅度最大,而6% 处理组适中,0.5%和3%处理组下降幅度最小。这可能是因为鱼油加入磷脂后在低剪切速率下体系的黏性阻力较强;而当剪切速率升高时,外力破坏分子间作用力,导致结构解离或重排,乳液流动性增强,黏度下降,高剪切速率下,密集结构的破坏更显著,因此剪切稀化程度随磷脂浓度增加而更显著[25-26]。
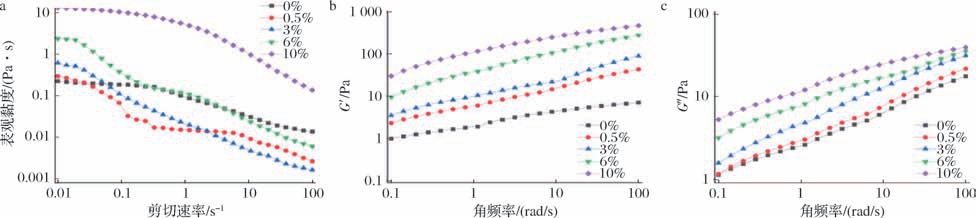
图3 鱼油-磷脂自乳化乳液的流变特性
Fig.3 Rheological properties of fish oil-phospholipid self-emulsifying emulsion
a-表观黏度;b-储能模量;c-损耗模量
如图3-b和3-c所示,G′反映材料的弹性特性,G″反映材料的黏性特性,无论是G′还是G″,均随着角频率的升高而增大,且磷脂含量越高,样品的G′和G″的值越大。这可能是因为在高速角频率下,样品内部变形速率快于松弛时间,导致弹性响应占主导。自乳化乳液形成的液滴结构在高频下无法完全松弛,需贮存更多弹性能量,从而导致G′升高;另一方面,高频振动加剧分子摩擦和能量耗散,磷脂含量越高,网络结构的摩擦阻力越大,因此G″随之升高。较高磷脂浓度(如6% 和10%)下的自乳化乳液的G′ > G″,表现为类固体特性,这意味着鱼油内部的液滴结构能有效抑制液滴聚并和分层,提升乳液的机械稳定性[27]。
2.4 共聚焦激光扫描显微镜图像观察
如图4所示,未添加磷脂的对照组,无法形成自乳化乳液,从共聚焦激光显微图片中可以发现,对照组中的油相以红色连续相为主导,油滴聚集,无法乳化。随着磷脂浓度的增加,自乳化乳液中的油滴粒径不断减小。当磷脂含量增加到3%时,能观察到视野中未出现成片红色油滴的现象,油滴尺寸显著减小,但油滴形状和大小不均一,说明此浓度下磷脂发挥了较好的乳化作用,体系稳定性有所加强,但是由于磷脂含量较低,无法形成紧密的界面膜对抗界面张力。当磷脂添加量大于3% 时,鱼油-磷脂自乳化乳液中液滴数量显著增多,油滴尺寸变得更小更均一,且更趋近于球形,说明当磷脂添加量为6%和10%,可以形成稳定且均一的自乳化乳液。以上结果说明大于3%的磷脂添加量可以促进鱼油-磷脂自乳化乳液形成更规整的结构,并使乳液的稳定性进一步提升。

图4 鱼油-磷脂自乳化乳液的共聚焦激光扫描显微镜图像
Fig.4 Confocal laser scanning microscope images of fish oil-phospholipid self-emulsifying emulsion
2.5 粒径和ζ-电位
如图5所示,随着磷脂浓度的提高,18/12 EE型鱼油-自乳化乳液的粒径呈现下降趋势,6%和10%磷脂样品组中油滴的粒径最小,约在1 μm左右,这印证了2.4节中共聚焦激光显微镜的观察结果。这是因为6% 及以上磷脂添加量能有效降低油水界面张力,形成的液滴更小更均匀,这与HO等[28]的观点一致。研究表明,油滴的表面ζ-电位的绝对值越大,乳液的稳定性越高[29]。由图5可知,自乳化乳液的ζ-电位绝对值随磷脂添加量的增大而提高,这是由于磷脂分子带有电荷,随着浓度增加,更多的磷脂吸附在液滴表面,增加液滴的表面电荷密度,从而增大液滴间的静电斥力,提高了液滴的ζ-电位,这也从侧面证明了6%和10%磷脂添加量的自乳化乳液稳定性较好。
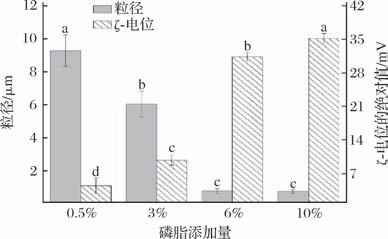
图5 鱼油-磷脂自乳化乳液的粒径和ζ-电位
Fig.5 The particle size and ζ-potential of fish oil-phospholipid self-emulsifying emulsion
注:0%磷脂添加量的鱼油粒径过大无法检出,不同字母表示样品间差异显著(P <0.05)。
2.6 离心稳定性分析
经测试,未添加磷脂的对照组样品油相出现明显上浮,底部透射率随着离心力的增大而增加(图6-a),此时样品的不稳定指数为0.212 7(图6-f);0.5%和3%磷脂样品组底部透射率显著降低(图6-b、图6-c),不稳定指数比对照降低了3.5~5.25倍(图6-f),说明磷脂的添加对鱼油自乳化乳液稳定性有显著促进作用;6%和10%的鱼油-磷脂自乳化乳液离心后未出现上浮(图6-d、图6-e),且不稳定指数接近0.01,这表明这2种自乳化乳液具有良好的离心稳定性。这归因于均匀的粒径分布能减少不同液滴沉降速度的差异,从而使样品在离心过程中分层的过程更为一致,而较高的静电斥力和较低的油水界面张力可以在整个离心过程中保持液滴的分散状态,避免突然的聚并或沉降现象发生[30]。
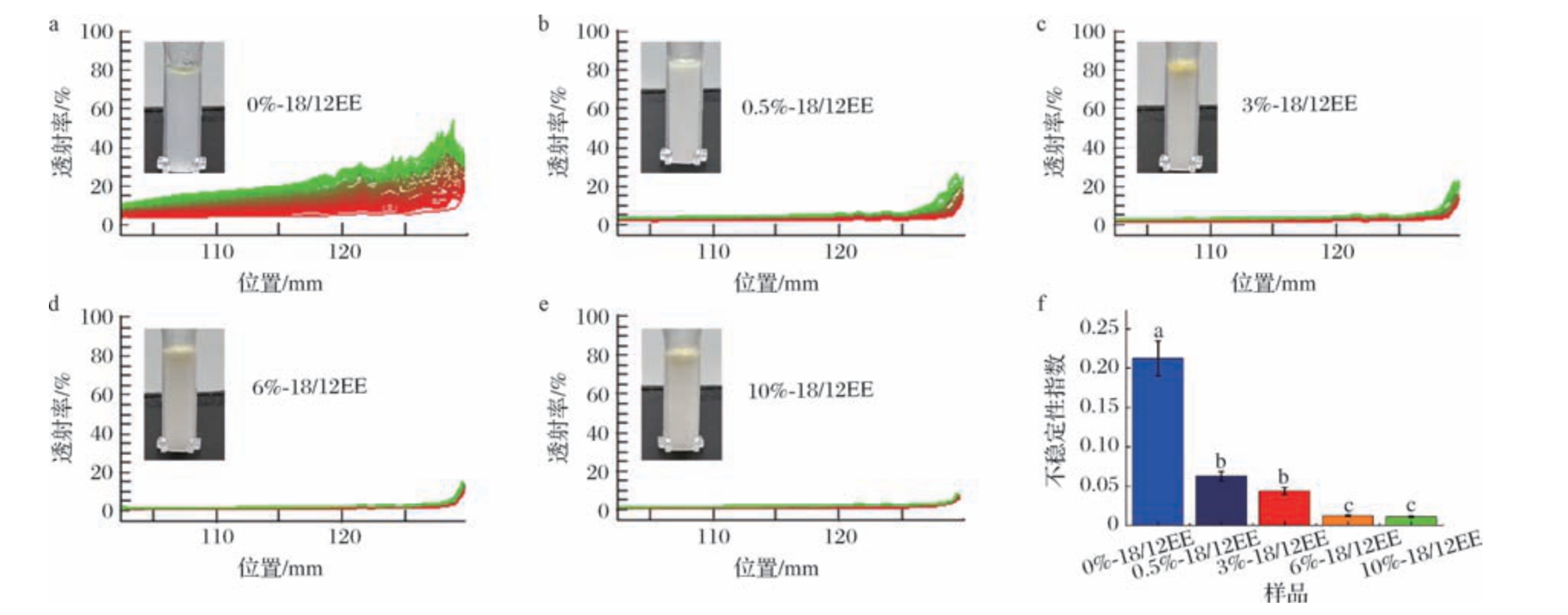
图6 鱼油-磷脂自乳化乳液的离心稳定性
Fig.6 Centrifugal stability spectras of fish oil-phospholipid self-emulsifying emulsion
注:数据标注不同字母表示样品间有显著性差异(P <0.05)。
a~e-离心稳定性;f-不稳定性指数
2.7 18/12 TG和5/25 EE型鱼油添加6%磷脂后的关键指标测定
结合实验结果,6% 与10% 磷脂添加量均能形成理化性质优良的鱼油-磷脂自乳化乳液。然而,根据文献报道[15],当磷脂浓度超过界面饱和吸附阈值时,过量磷脂无法有效锚定于油水界面,转而形成胶束。此类胶束可增溶鱼油中的脂溶性活性成分,与乳化液滴竞争性结合底物,最终导致体系载药效率下降[31]。基于上述机理与成本效益分析(10%磷脂添加量的成本较6% 增加40%),本研究选择6%为最优磷脂添加量。此外,采用该添加量对其余两类鱼油进行关键乳化指标测定,结果发现6%磷脂添加量的自乳化体系对不同类型鱼油均具有普适性增效作用。
如图7-a和图7-b所示,添加了6%磷脂的18/12 TG和5/25 EE型鱼油经充分振荡后形成的自乳化乳液与18/12 EE型鱼油形成的自乳化乳液的外观相似,均未分层且乳液呈现均匀稳定状态;18/12 TG和5/25 EE型鱼油-磷脂自乳化乳液的粒径和电位值与18/12 EE型接近(图7-c);共聚焦激光显微图像显示,18/12 TG和5/25 EE型鱼油-磷脂自乳化乳液在视野中的液滴分布与18/12 EE型鱼油乳液类似,且液滴形状规整,尺寸均一(图7-d~ 图7-f);离心后,18/12 TG和5/25 EE型鱼油-磷脂自乳化乳液均未出现上浮,不稳定指数接近0.012(图8-a~图8-d)。这些结果都证明了6%的磷脂添加量对3种类型鱼油-磷脂自乳化乳液的稳定性有良好的效果,因而沿用此浓度对3种类型鱼油进行药代动力学分析。
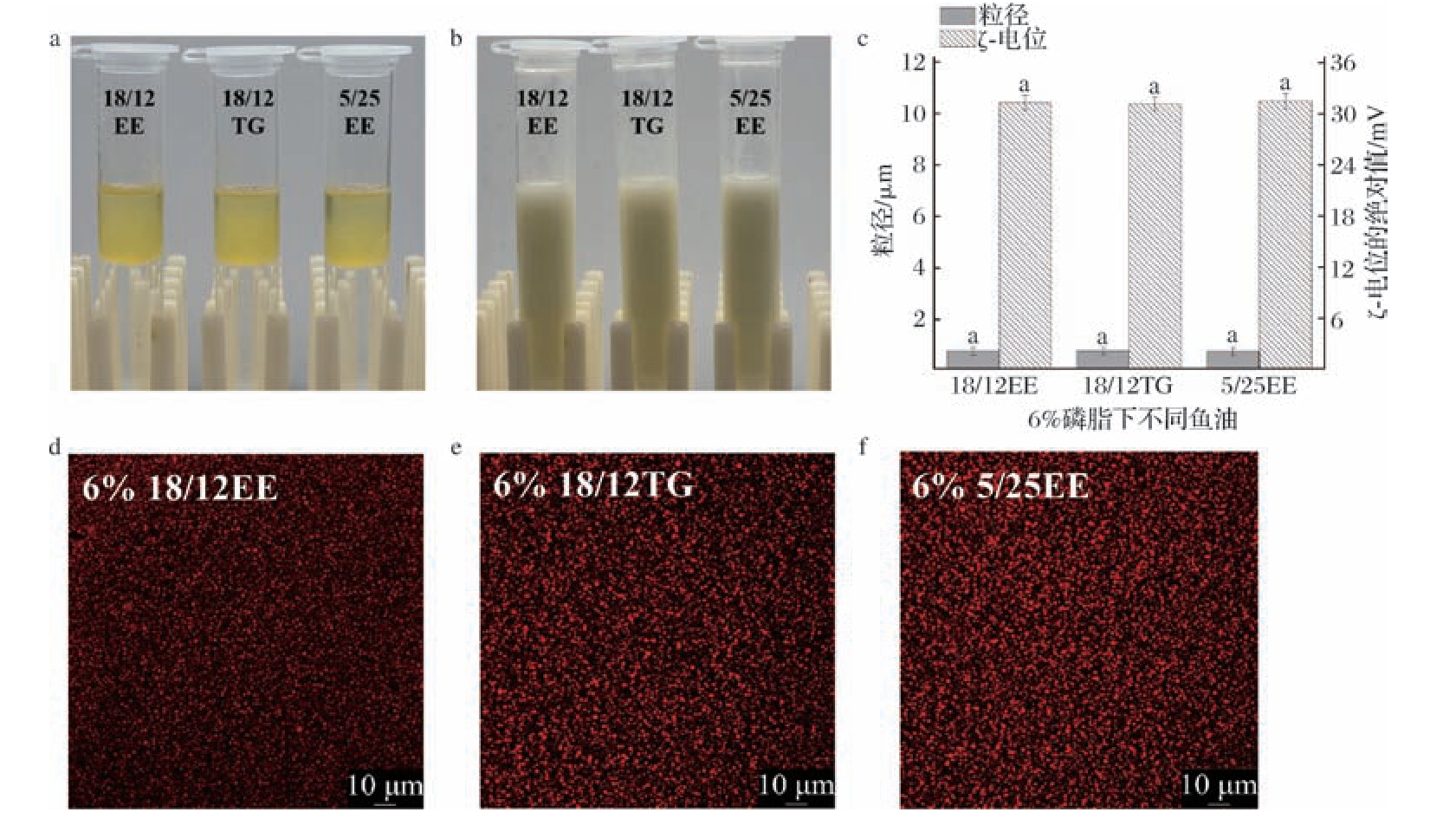
图7 不同类型鱼油-磷脂自乳化乳液的外观、粒径、ζ-电位及共聚焦图像对比
Fig.7 Comparison of appearance,particle size,potential and confocal images of different types of fish oil-phospholipid self-emulsifying emulsion
注:数据标注相同字母表示样品间差异不显著(P >0.05)。
a~b-外观特征;c-粒径及ζ-电位;d~f-共聚焦激光显微镜图像
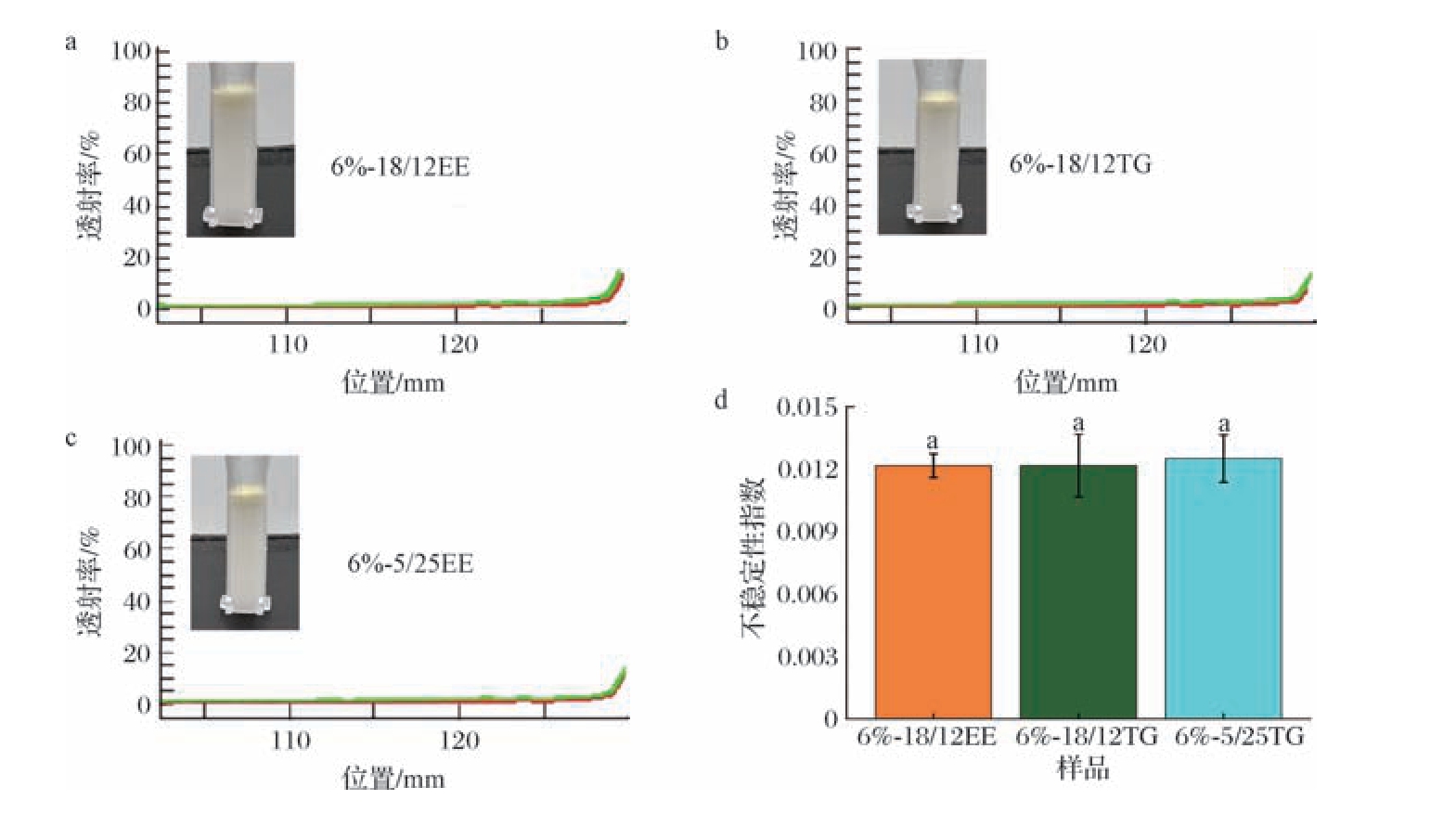
图8 不同类型鱼油-磷脂自乳化乳液的稳定性对比
Fig.8 Comparison of stability of different types of fish oil-phospholipid self-emulsifying emulsion
注:数据标注相同字母表示样品间差异不显著(P >0.05)。
a~c-离心稳定性;d-不稳定性指数
2.8 药代动力学特征分析
研究表明,大鼠和人的血浆脂肪酸组成接近,因而在有关脂质代谢实验中,多选择大鼠为实验动物,以得到与人体实际情况更接近的结果[32]。采用GC-MS测定不同血浆样品中EPA和DHA的含量并绘制大鼠血浆中EPA和DHA浓度-时间曲线,如图9所示,自乳化鱼油组(SE组)中EPA和DHA的浓度在相同取血时间点均高于对应的原料鱼油组(O组),这说明自乳化体系的构建可以显著提高鱼油的体内生物利用度。此外,基于血药浓度-时间曲线的数据,通过Phoenix软件计算出不同鱼油样品的药代动力学参数。由表1可以看出,自乳化体系的构建显著提升了鱼油中EPA/DHA的体内生物利用度,相较于原料鱼油(O组),SE组的Tmax缩短约40%~60%(P <0.05),这说明自乳化可以通过减小鱼油油滴的粒径增强脂质与消化酶的界面接触效率,从而加速脂解进程[33]。此外,灌胃SE-18/12EE、SE-5/25EE和SE-18/12TG后,大鼠血浆中EPA的0~24 h血药浓度-时间曲线下面积(area under the plasma concentration-time curve from time 0 to 24 hours,AUC0-24h) 分别为(14.52± 3.02)、(11.96±6.87)、(15.79±3.72) mg·h/mL,显著高于O-18/12EE、O-5/25EE和O-18/12TG原料鱼油组[分别为(5.46± 3.41)、(3.20± 1.35)、(9.48±6.42) mg·h/mL,P <0.05]。同时,灌胃SE-18/12EE、SE-5/25EE和SE-18/12TG后,大鼠血浆中EPA的AUC0~24h分别为(9.90± 2.53)、(10.71± 3.75)、(10.22±4.43) mg·h/mL,同样显著高于O-18/12EE、O-5/25EE和O-18/12TG对应原料鱼油组[分别为(1.33±0.51)、(1.53±0.42)、(3.19±1.08) mg·h/mL,P<0.05]。SE-18/12EE中EPA和DHA的吸收量分别是原料鱼油O-18/12EE的2.66倍(P <0.05)和7.44倍(P <0.05);SE-5/25EE中EPA和DHA的吸收分别是原料鱼油O-5/25EE的3.74倍(P <0.05)和7.00倍(P <0.05);SE-18/12TG中EPA和DHA的 吸收分别是原料鱼油O-18/12TG的2.89倍(P <0.05)和3.20倍(P <0.05)。
表1 大鼠药代动力学参数比较
Table 1 Comparison of pharmacokinetic parameters in rats
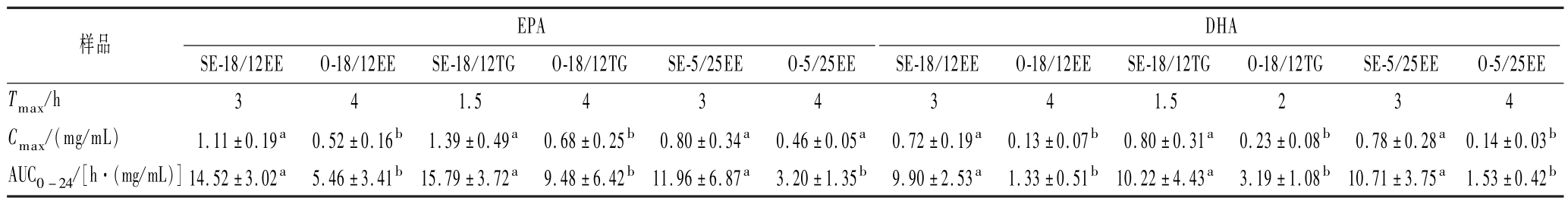
注:相邻两列(自乳化与原料鱼油)数据标注不同字母表示组间有显著性差异(P <0.05)。
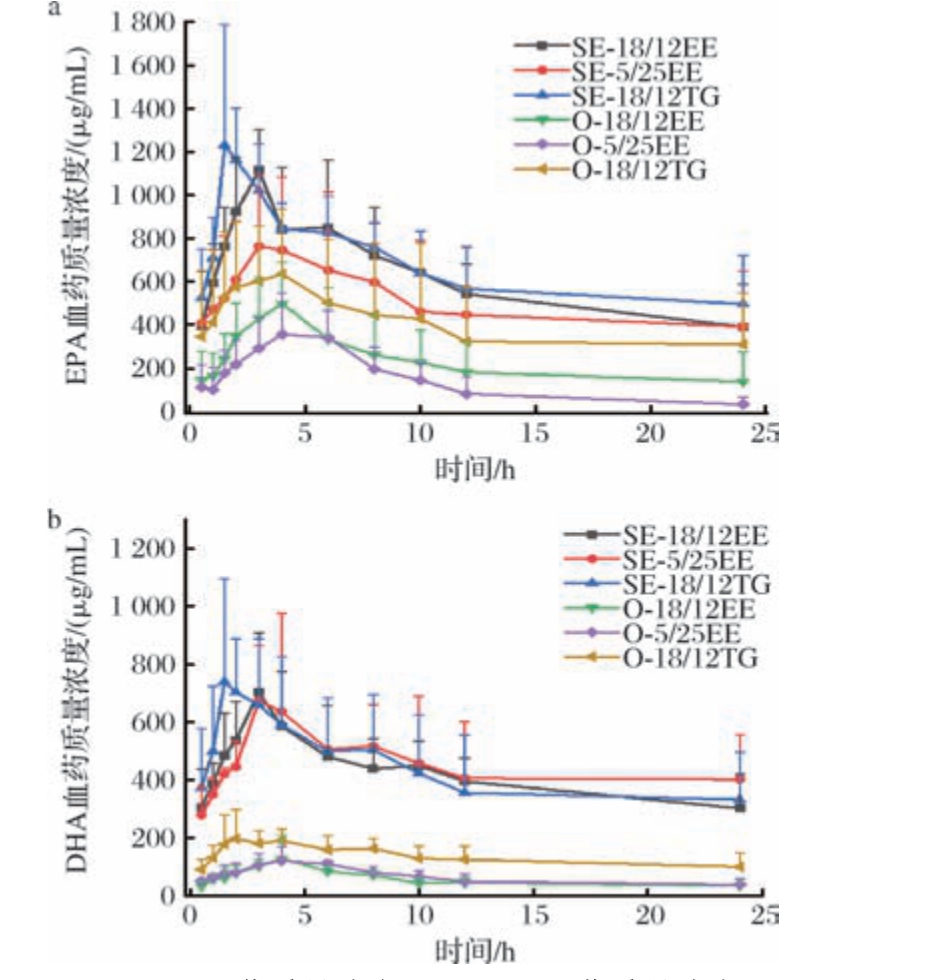
图9 大鼠灌胃各样品后EPA和DHA血药浓度-时间曲线图
Fig.9 The concentration-time curves of EPA and DHA blood drug concentration in rats after intragastric administration of each sample
注:n=5。
a-EPA血药质量浓度;b-DHA血药质量浓度
尽管经自乳化处理后,TG型鱼油中EPA和DHA的吸收率均高于EE型鱼油,但EE型鱼油经自乳化后其体内吸收提升的幅度却更为显著。这一现象可归因于两者消化机制的差异:TG型鱼油主要依赖高效的胰脂肪酶进行水解,而EE型鱼油的水解则主要受限于羧酸酯酶。该酶主要分布于肠道黏膜细胞和肝脏中,在人体肠道腔内浓度较低,且其活性易受胆汁酸浓度、pH等因素影响,导致EE型鱼油的水解速率缓慢。磷脂-自乳化体系的构建有效克服了这一瓶颈:其形成的微细乳滴显著降低了EE型鱼油的粒径,增大了油-水界面比表面积。比表面积的增加直接扩大了羧酸酯酶与EE底物分子的接触机会,从而加速了EE型鱼油的水解速率,促进游离脂肪酸的释放。随后,游离脂肪酸得以在肠黏膜细胞内与甘油重组为甘油三酯,并入乳糜微粒完成吸收[34-35]。
综上所述,磷脂自乳化体系的构建可显著提升3种类型鱼油的体内吸收效率。值得注意的是,其对EE型鱼油的吸收提升作用尤为显著,这主要归因于该体系有效克服了EE型鱼油水解的关键瓶颈,即通过增大油滴比表面积,显著促进了其依赖的限速酶(羧酸酯酶)的接触与催化效率。当然,尽管本研究在大鼠模型中证实了磷脂自乳化体系在提高各类鱼油生物利用度方面的潜力,但种属间的生理差异(如消化酶谱、胆汁分泌、肠道转运等)以及人体胃肠道独特的复杂环境,可能导致该体系在人体内的性能表现与动物实验结果存在一定偏差。因此,未来若推进至人体临床试验,需重点关注人体在吸收效率、代谢途径以及剂量-响应关系等方面的差异。
3 结果与讨论
本研究基于磷脂的优异乳化特性和生物安全性,成功构建了不同类型鱼油(TG/EE)-磷脂自乳化体系,并系统评价了其关键理化性质。结果表明,磷脂的引入可有效形成自乳化乳液,显著降低油滴粒径与油水界面张力,从而提升乳液稳定性。综合理化性能与成本效益分析,6%磷脂添加量为最优选择,其在保证乳液高稳定性(粒径≤1 μm,离心不稳定指数≤0.01)的同时,较10%磷脂添加量可降低约40%的原料成本,为开发高生物利用度鱼油制剂提供了经济高效的解决方案。药代动力学研究进一步证实:鱼油-磷脂自乳化体系能显著促进EPA和DHA的体内吸收。其中,TG型鱼油的生物利用度最高,而EE型鱼油经自乳化改性后,其原本较低的EPA/DHA吸收率得到实质性改善。本研究通过构建鱼油-磷脂自乳化体系,为开发高生物利用度鱼油制剂奠定了理论基础。未来研究可聚焦于界面性质调控、氧化稳定性与酶解效率协同优化、精准剂量设计等方向,以进一步提升该体系在人体复杂胃肠道环境中的长期稳定性与应用效能。
[1]马湖伊杉,潘南,林振宇,等.振动光谱技术在鱼油品质检测中的应用研究进展[J].光谱学与光谱分析,2025,45(2):301-311.MA H Y S,PAN N,LIN Z Y,et al.Research progress on the vibrational spectroscopy technology in the quality detection of fish oil[J].Spectroscopy and Spectral Analysis,2025,45(2):301-311.
[2]YANG T Q,JIANG K Y,LIU S H,et al.The impact of fish oil oxidation on interfacial properties and system stability of cod protein[J].Food Research International,2025,203:115904.
[3]JAMSHIDI A,CAO H,XIAO J B,et al.Advantages of techniques to fortify food products with the benefits of fish oil[J].Food Research International,2020,137:109353.
[4]WANG J K,HAN L X,WANG D Y,et al.Stability and stabilization of omega-3 oils:A review[J].Trends in Food Science &Technology,2021,118:17-35.
[5]MOOMAND K,LIM L T.Oxidative stability of encapsulated fish oil in electrospun zein fibres[J].Food Research International,2014,62:523-532.
[6]DHRITLAHRE R K,PADWAD Y,SANEJA A.Self-emulsifying formulations to augment therapeutic efficacy of nutraceuticals:From concepts to clinic[J].Trends in Food Science &Technology,2021,115:347-365.
[7]UEDA K,UCHIYAMA R,KATO N,et al.Mechanistic insights into drug supersaturation during lipid digestion in self-emulsifying drug delivery systems:A cryo-TEM and NMR study[J].International Journal of Pharmaceutics,2025,674:125425.
[8]BUYA A B,BELOQUI A,MEMVANGA P B,et al.Self-nano-emulsifying drug-delivery systems:From the development to the current applications and challenges in oral drug delivery[J].Pharmaceutics,2020,12(12):1194.
[9]GONÇALVES A,NIKMARAM N,ROOHINEJAD S,et al.Production,properties,and applications of solid self-emulsifying delivery systems (S-SEDS) in the food and pharmaceutical industries[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2018,538:108-126.
[10]LIU Q Q,HUANG H,CHEN H H,et al.Food-grade nanoemulsions:Preparation,stability and application in encapsulation of bioactive compounds[J].Molecules,2019,24(23):4242.
[11]HADDADZADEGAN S,DORKOOSH F,BERNKOP-SCHNÜRCH A.Oral delivery of therapeutic peptides and proteins:Technology landscape of lipid-based nanocarriers[J].Advanced Drug Delivery Reviews,2022,182:114097.
[12]WU H Y,LONG X Y,YUAN F,et al.Combined use of phospholipid complexes and self-emulsifying microemulsions for improving the oral absorption of a BCS class Ⅳcompound,baicalin[J].Acta Pharmaceutica Sinica B,2014,4(3):217-226.
[13]CHEN Z Z,GAO W H,FENG X Q,et al.A comparative study on the preparation and evaluation of solubilizing systems for silymarin[J].Drug Delivery and Translational Research,2024,14(6):1616-1634.
[14]PAN Y,ZHANG L,FU X F,et al.Addition of phospholipids improved the physical stability and fat globule structure of processed milk[J].Foods,2025,14(3):375.
[15]RISSE K,BRIDOT J L,BÄTHER S,et al.Towards tailoring the viscoelasticity of liquid-liquid interfaces in emulsions:Understanding phospholipid-protein interactions at the oil-water interface[J].Food Hydrocolloids.2025,169:111594.
[16]KABALNOV A,WEERS J,ARLAUSKAS R,et al.Phospholipids as emulsion stabilizers.1.interfacial tensions[J].Langmuir,1995,11(8):2966-2974.
[17]谭秀山,张金龙,曹娅.不同乳化剂对油脂乳化稳定性的比较研究[J].农产品加工,2024,(15):33-36;40.TAN X S,ZHANG J L,CAO Y,et al.Comparative study of emulsifying stability of oils and fats with different emulsifiers[J].Farm Products Processing,2024,(15):33-36;40.
[18]DELACOTTE J,GOURIER C,PINCET F.Interfacial pressure and phospholipid density at emulsion droplet interface using fluorescence microscopy [J].Colloids and Surfaces B: Biointerfaces,2014,117:545-548.
[19]FU D W,LI J J,DAI D M,et al.Development and characterization of self-emulsifying high internal phase emulsions using endogenous phospholipids from Antarctic krill oil[J].Food Chemistry,2023,428:136765.
[20]FENG X,DAI H J,YU Y,et al.Adjusting the interfacial property and emulsifying property of cellulose nanofibrils by ultrasonic treatment combined with gelatin addition [J].Food Hydrocolloids,2022,133:107905.
[21]BRODKORB A,EGGER L,ALMINGER M,et al.INFOGEST static in vitro simulation of gastrointestinal food digestion[J].Nature Protocols,2019,14(4):991-1014.
[22]孙素玲.海狗油多不饱和脂肪酸富集及酯化工艺的研究[D].无锡:江南大学,2004.SUN S L.Study on the enrichment and esterification of polyunsaturated fatty acids in seal oil[D].Wuxi:Jiangnan University,2004.
[23]YIN M Y,CHEN M,MATSUOKA R,et al.Effects of phospholipid type and concentration on the emulsion stability and in vitro digestion behaviors of fish oil-loaded emulsions[J].Food Science and Technology,2022,42:e84622.
[24]RISBO J,JØRGENSEN K,SPEROTTO M M,et al.Phase behavior and permeability properties of phospholipid bilayers containing a short-chain phospholipid permeability enhancer[J].Biochimica et Biophysica Acta (BBA)-Biomembranes,1997,1329(1):85-96.
[25]YESILTAS B,GARCÍA-MORENO P J,SØRENSEN A M,et al.Physical and oxidative stability of high fat fish oil-in-water emulsions stabilized with sodium caseinate and phosphatidylcholine as emulsifiers[J].Food Chemistry,2019,276:110-118.
[26]朱皓琛.大豆卵磷脂-薄荷精油乳液的制备工艺优化及在蓝莓汁中的应用[D].武汉:武汉轻工大学,2023.ZHU H C.Preparation and optimization of soybean lecithin-mint essential oil emulsion and its application in blueberry juice[D].Wuhan:WuhanPolytechnic University,2023.
[27]ZHANG Q C,ZHU H,WANG R,et al.Fish oil emulsions stabilized by enzymatic hydrolysis,glycation,and fibrillation of β-Lg:Stability and EPA/DHA bioaccessibility [ J].Food Chemistry,2025,469:142550.
[28]HO T M,RAZZAGHI A,RAMACHANDRAN A,et al.Emulsion characterization via microfluidic devices:A review on interfacial tension and stability to coalescence[J].Advances in Colloid and Interface Science,2022,299:102541.
[29]KRIVOROTOVA T,CIRKOVAS A,MACIULYTE S,et al.Nisinloaded pectin nanoparticles for food preservation[J].Food Hydrocolloids,2016,54:49-56.
[30]冯鑫,马良,戴宏杰,等.食品级Pickering乳液的稳定性及β-胡萝卜素的装载研究[J].食品与发酵工业,2021,47(6):18-25.FENG X,MA L,DAI H J,et al.The study on stability of foodgrade Pickering emulsion and the loading of β-carotene[J].Food and Fermentation Industries,2021,47(6):18-25.
[31]毛相朝,殷成梅,张海洋,等.固定化酶混合胶束体系及其在磷脂合成中的应用: CN118126998A[P].2024-06-04.MAO X C,YIN C M,ZHANG H Y,et al.Fixed enzyme mixed micelle system and its application in phospholipid synthesis: China,CN118126998A[P].2024-06-04.
[32]刘小如,邓泽元,李静,等.从人和动物血浆及红细胞膜脂肪酸谱探讨脂质代谢实验模型动物选取[J].中国实验动物学报,2009,17(2):97-102.LIU X R,DENG Z Y,LI J,et al.Selection of proper animal models for lipid metabolism studies in comparing fatty acids profile of plasma and erythrocyte membrane between healthy adult humans and animals [J].Acta Laboratorium Animalis Scientia Sinica,2009,17(2):97-102.
[33]POUTON C.W.Formulation of poorly water-soluble drugs for oral administration:Physicochemical and physiological issues and the lipid formulation classification system [J].European Journal of Pharmaceutical Sciences,2006,29(3-4):278-287.
[34]DYERBERG J,MADSEN P,MØLLER J M,et al.Bioavailability of marine n-3 fatty acid formulations[J].Prostaglandins,Leukotrienes and Essential Fatty Acids,2010,83(3):137-141.
[35]BREMMELL K E,BRISKEY D,MEOLA T R,et al.A self-emulsifying omega-3 ethyl ester formulation (AquaCelle) significantly improves eicosapentaenoic and docosahexaenoic acid bioavailability in healthy adults[J].European Journal of Nutrition,2020,59(6):2729-2737.