葡萄酒的感官品质与香气特征密不可分,其香气复杂度主要由酿酒酵母(Saccharomyces cerevisiae)在酒精发酵过程中代谢产生的醇、酯、酸等挥发性化合物决定[1]。高级醇可增加葡萄酒香气的复杂性;酯类物质为葡萄酒带来果香、花香等令人愉快的风味;挥发性脂肪酸可保持葡萄酒的平衡感,增加葡萄酒的香气复杂度[1]。近年来,随着“风土”概念的兴起,本土酿酒酵母因其对产区生态的适应性及对地域风味的独特贡献,逐渐成为提升葡萄酒个性化和品质的重要研究方向[2]。例如,孙雅慧[2]在烟台地区从17株本土酵母中筛选出3株果香型菌株(CY2、CY6、CY1),显著提升了葡萄酒的果香特征;刘沛通等[3]在河北地区筛选出高产酯类物质和甘油的菌株60258与菌株60268,优化了酒体的复杂性与口感平衡;杨惠婷[4]和宋佳佳[5]则分别在浙江、苏皖地区发掘出发酵力强且酒体品质优异的菌株HF2与菌株NL1。以上研究表明,本土酵母在提升酿造效率与葡萄酒品质方面具有较好的潜力。值得注意的是,宁夏贺兰山东麓作为我国重要葡萄酒产区,丰富的微生物资源也备受关注。赵海霞等[6]与周桂珍等[7]分别从该地区筛选出多株高产乙醇(Y7、Y28)与发酵风味优良(G14、H3)的本土酵母。然而,宁夏贺兰山东麓产区酵母资源丰富,虽有一定的本土酵母研究基础,但仍有大量兼具高效发酵能力与独特产香潜力的本土酿酒酵母有待继续挖掘,可以为酿造产区特色葡萄酒提供更多的潜在酵母菌株资源。因此,本研究以分离自贺兰山东麓产区的4株本土酿酒酵母(QTX-D7、QTX-D17、YC-E8、YQY-E18)为研究对象,以3株商业酵母(CECA、F33、XR)为对照,测定7株酿酒酵母的生长曲线;通过模拟葡萄汁发酵实验,检测发酵液的CO2失重变化、残糖变化以及发酵结束后的基础理化指标,研究本土酿酒酵母的发酵特性;采用顶空固相微萃取-气相色谱-质谱联用技术(headspace solid phase microextraction-gas chromatography-mass spectrometry,HS-SPME-GC-MS)结合主成分分析(principal component analysis,PCA)与聚类分析,解析不同菌株发酵液中挥发性香气成分的含量、组成及差异。本研究旨在明确本土酿酒酵母的发酵优势与产香特性,为贺兰山东麓产区酿酒微生物资源的开发提供理论依据,并为国产优良酿酒酵母的选育提供参考价值。
1 材料与方法
1.1 材料与试剂
1.1.1 菌种
3株商业酿酒酵母:CECA购自安琪酵母股份有限公司;F33购自拉氟德公司;XR购自诺盟公司。
4株本土酿酒酵母:QTX-D7、QTX-D17、YC-E8和YQY-E18,分离自宁夏贺兰山东麓产区,保藏于宁夏大学葡萄酒与园艺学院实验室。
1.1.2 培养基
YPD液体培养基(g/L):蛋白胨20.0,酵母浸粉10.0,葡萄糖20.0(固体培养基中添加琼脂13.0),加热溶解于1 L蒸馏水中,121 ℃灭菌15 min。
模拟葡萄汁(model synthetic medium,MSM)培养基(g/L):葡萄糖100.0,果糖100.0,酒石酸3.0,柠檬酸0.3,L-苹果酸0.3,七水硫酸镁0.2,磷酸二氢钾2.0,硫酸铵0.3,天冬酰胺0.6,四水硫酸锰0.004,七水硫酸锌0.004,五水硫酸铜0.001,碘化钾0.001,硼酸0.001,四水合钼酸铵0.001,六水合二氯化钴0.000 4,肌醇0.3,生物素0.000 4,维生素B1 0.001,维生素B6 0.001,烟酸0.001,泛酸0.001,对氨基苯甲酸0.001,置于35~40 ℃水浴中,持续搅拌使其完全溶解于1 L的蒸馏水,使用1 mol/L NaOH调节pH值至5.8,使用25 mm ×0.22 μm过滤膜除菌,添加2 mL T2263脂肪酸溶液,购自上海瑞楚生物科技有限公司。
1.2 仪器与设备
SHP-150B生化培养箱,常州诺基仪器有限公司;SW-CJ-2FD超净工作台,苏州安泰空气技术有限公司;LDZX-50FBS高压蒸汽灭菌锅,上海申安医疗器械厂;雷磁PHS-3C pH计,上海仪科学仪器股份有限公司;Multiskan FC酶标仪,赛默飞世尔仪器有限公司;全自动葡萄酒分析仪,Biosystems公司;7890B气相色谱-7000D质谱仪、DB-Wax色谱柱(60 m ×250 μm,0.25 μm),美国Agilent公司。
1.3 实验方法
1.3.1 生长曲线测定
将保藏的7株酿酒酵母甘油菌划线至YPD固体培养基上,28 ℃培养3 d。挑取单菌落接种于3 mL YPD液体培养基中,于28 ℃、180 r/min条件下振荡培养24 h获得种子液。将种子液以1%(300 μL)的接种量分别接种于30 mL YPD液体培养基和MSM培养基中,28 ℃、180 r/min振荡培养,每隔2 h取200 μL菌液于96孔板中,使用酶标仪在600 nm波长处测定菌液的OD值,每个样品重复测定3次。以时间为横坐标,OD值为纵坐标,绘制生长曲线。
1.3.2 模拟葡萄汁发酵实验
将各酵母种子液以1%(500 μL)的接种量接种于50 mL MSM培养基中,于28 ℃静置培养,每个样品设置2个重复。每隔24 h称量CO2 失重并记录,计算单位发酵时间内CO2的释放量,当CO2 累积释放量达到峰值并稳定时,发酵自然停止。以CO2 产生量为纵坐标,发酵时间为横坐标,绘制CO2 失重变化曲线。发酵期间每隔3 d取样,每次取3 mL发酵液,在11 000 r/min条件下离心8 min,取上清液2 mL,用0.45 μm滤膜进行过滤,使用全自动葡萄酒分析仪进行残糖含量测定,绘制残糖动态变化曲线。
1.3.3 发酵液的理化指标测定
发酵结束后,取发酵液测定酒精度、残糖、总酸、甘油、pH。参考GB/T 15038—2006《葡萄酒、果酒通用分析方法》测定酒精度、挥发酸。取3 mL发酵液,在11 000 r/min条件下离心8 min后,取上清液2 mL,用0.45 μm滤膜进行过滤,使用全自动葡萄酒分析仪进行残糖、总酸、甘油含量测定。取20 mL发酵液于离心管中,使用pH计对样品进行pH值测定。
1.3.4 挥发性香气成分分析
采用HS-SPME-GC-MS技术,使用7890B气相色谱-7000D质谱仪、DB-Wax色谱柱(60 m ×250 μm,0.25 μm)对模拟葡萄汁发酵液香气成分进行检测,方法参考周迪等[8]的研究。将5 mL发酵液样品、1.5 g NaCl、10 μL内标4-甲基-2-戊醇(1 g/L)依次加入顶空瓶,后放置于自动进样器上启动检测。色谱条件:进样口温度230 ℃,起始柱温50 ℃,恒温1 min,以3 ℃/min升到220 ℃,保持5 min。载气为高纯氦气(纯度≥99.999%),流速1 mL/min,不分流进样。质谱条件:传输线温度235 ℃,离子源温度230 ℃,电子能量70 eV。通过获得的质谱和保留指数与美国国家标准与技术研究院(National Institute of Standards and Technology,NIST)数据库比对结果,对模拟葡萄汁发酵液中的香气物质进行定性分析,通过内标-标准曲线法对香气成分浓度进行全定量分析。香气物质活度值(odor activity value,OAV)是物质的浓度与其相应嗅觉阈值的比值,用于评价香气物质对葡萄酒整体香气的贡献程度。
1.4 数据处理
使用Microsoft Office 2021软件进行数据统计,SPSS 27软件对数据进行显著性分析,Origin 2022软件进行绘图。
2 结果与分析
2.1 酿酒酵母在YPD和MSM培养基中生长曲线分析
在模拟葡萄汁发酵实验之前,需要对酵母菌株的活性进行检测,以保证模拟发酵实验的可行性与准确性。因此,对3株商业酿酒酵母以及4株本土酿酒酵母进行YPD和MSM培养基中的生长曲线测定,结果如图1所示。由YPD生长曲线可知,7株酿酒酵母的生长情况大致相同,在接种后的0~4 h适应环境,处于生长较为缓慢的迟滞期。从4 h开始,7株酿酒酵母进入生长迅速的对数生长期。14 h后进入稳定期。由MSM生长曲线可知,在初始的0~4 h,3株商业酿酒酵母与4株本土酿酒酵母都处于适应环境的迟滞期。4 h后进入对数生长期。其中F33生长速度明显快于其余6株酿酒酵母,这可能是F33对MSM的生长环境适应性更强。7株酿酒酵母均在30 h后进入稳定期。综上,这7株酿酒酵母在YPD和MSM培养基中生长趋势基本一致,可以用于后续模拟葡萄汁发酵实验。
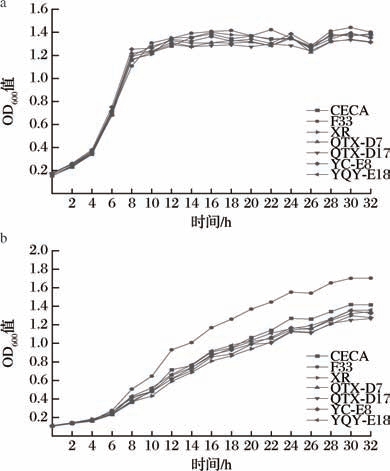
图1 各菌株的生长曲线
Fig.1 Growth curves of each strain
a-YPD生长曲线;b-MSM生长曲线
2.2 模拟葡萄汁发酵动力学测定
在模拟葡萄汁发酵过程中,每隔24 h对发酵液进行称量,绘制CO2失重变化图,如图2-a所示。7株酿酒酵母在接种后第1天即快速启动发酵,其中F33、YC-E8、QTX-D17发酵速度明显更快,有着较为明显的快速发酵时期,在接种后的第13天,CO2 产气量趋于不变,表明发酵接近结束;CECA、XR、QTX-D7发酵速度较为平缓,没有明显的快速发酵时期,在接种后第15天,CO2产气量趋于不变;YQY-E18发酵速度最为缓慢。
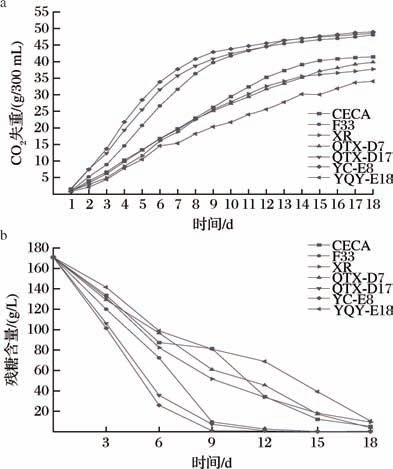
图2 各菌株发酵动力学的测定
Fig.2 Determination of fermentation kinetics of each strain
a-CO2 失重变化;b-残糖变化
在接种酵母的第0、3、6、9、12、15、18天,分别对发酵液中的总糖进行测定,绘制残糖变化图,如图2-b所示。在模拟葡萄汁中接种酿酒酵母之后,均能快速启动发酵。YC-E8、QTX-D17这2株本土酿酒酵母发酵最为迅速,在接种后的0~9 d进入快速发酵时期,模拟葡萄汁中的还原糖大幅度减少,15 d后培养基中的还原糖含量小于1 g/L,发酵基本结束;F33前期0~9 d还原糖消耗速度趋势与YC-E8、QTX-D17一致,但速度略慢,到15 d后培养基中的还原糖含量小于1 g/L;XR、QTX-D7还原糖消耗速度较为平缓,从接种到第15天还原糖的利用速度趋于稳定,后消耗速度放缓,到第18天培养基中的还原糖含量均小于20 g/L;CECA还原糖利用速度基本与XR、QTX-D7一致,但在第6~9天利用速度变缓;YQY-E18在第0~6天还原糖利用速度与其余6株酿酒酵母一致,在第6~12天利用速度明显变缓,第12~18天还原糖利用速度略微加快,但总体速率仍明显低于其余6株酿酒酵母,这表明YQY-E18可能并不适宜用于模拟葡萄汁发酵。
2.3 发酵液基础理化指标分析
由表1可知,商业酿酒酵母F33产乙醇能力最强,为10.11%vol,4株本土酿酒酵母中YC-E8、QTXD17产乙醇更多,分别达到9.63、9.64% vol,三者之间差异不显著;YQY-E18产乙醇最少,为7.1% vol,与其余6株酿酒酵母差异显著,说明YQY-E18难以适应模拟葡萄汁的发酵环境。菌株QTX-D17发酵液总酸最高,为3.05 g/L,菌株XR发酵液总酸最低,为1.85 g/L;总酸从高到低依次为QTX-D17、F33、QTX-D7、YQY-E18、CECA、YC-E8、XR;QTX-D17与XR之间差异显著,与其余5株酿酒酵母差异显著,QTX-D7与F33、QTX-D7与YQY-E18差异不显著,YC-E8、YQYE18、CECA三者之间差异不显著。菌株QTX-D17发酵液中的挥发酸含量最高,为0.38 g/L,菌株F33发酵液中的挥发酸含量最低,为0.22 g/L;挥发酸从高到低依次为QTX-D17、QTX-D7、CECA、YQYQ-E18、XR、YC-E8、F33;QTX-D7和CECA、YC-E8和F33差异不显著,其余菌株之间差异显著。YC-E8、QTX-D17、F33发酵液中残糖含量均低于1 g/L,三者之间差异不显著,与其余4株酿酒酵母差异显著,其中YC-E8发酵能力最强,残糖最少,为0.02 g/L,接近发酵完培养基中所有还原糖;QTX-D7、CECA、XR发酵液中残糖均接近于3.3 g/L,三者之间差异不显著,与其他发酵液差异显著,发酵能力正常;YQY-E18发酵液残糖含量为10.52 g/L,与其他发酵液差异显著,发酵能力较弱。F33产甘油能力最强,为11.73 g/L,但与YC-E8、QTX-D17、CECA相比差异并不显著;YQY-E18和XR产甘油能力较弱,分别为10.36、10.46 g/L,两者之间差异不显著,与上述4株酿酒酵母差异显著。7株酿酒酵母发酵液的pH,最高为XR(pH 4.45),最低为F33(pH 4.37),两者之间差异显著,其余菌株之间差异不显著。
表1 各菌株发酵结束后的发酵液理化指标
Table 1 Physicochemical indexes at the end of fermentation for each strain
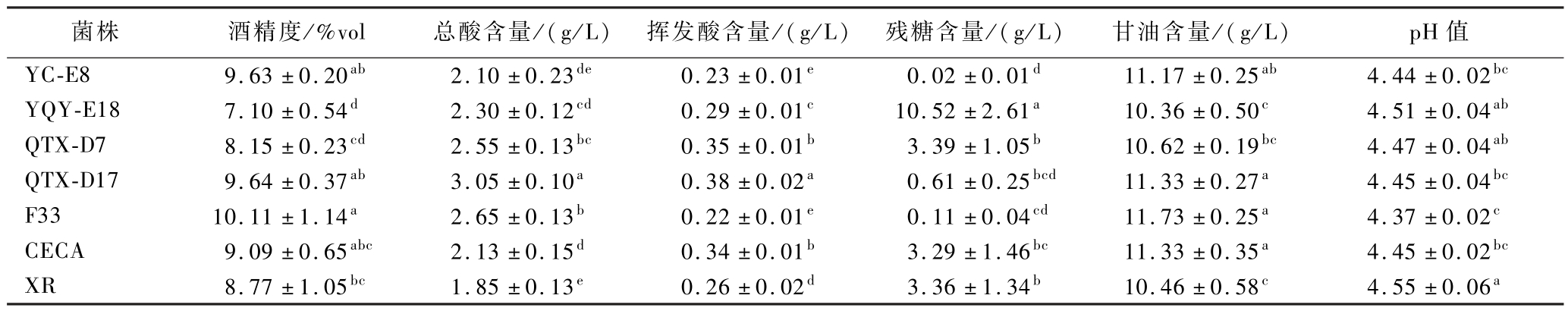
注:同一列中不同小写字母代表有显著差异(P <0.05)。
2.4 挥发性香气成分
如电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.043191)[9-11]所示,发酵液中共检测出44种挥发性化合物,包括酯类14种、醇类13种、醛类7种、酮类5种、酸类4种、其他化合物1种。其中,醇类的含量最高,其次是醛类、酯类、酸类、酮类、其他化合物。
2.4.1 酯类
酯类是酵母在发酵过程中形成的糖代谢次级产物,提供果香和花香。7株酿酒酵母发酵液酯类物质总含量为2 951.93~25 630.34 μg/L,商业酿酒酵母CECA发酵液酯类物质总含量最高,次高的为本土酿酒酵母QTX-D7,总含量12 963.54 μg/L,两者之间差异显著;其余5株菌发酵液酯类物质总含量都在5 000 μg/L以下,与CECA和QTX-D7差异显著。4株本土酿酒酵母发酵液中具有香蕉香气特征的乙酸异戊酯含量均高于商业酿酒酵母F33,其中QTX-D7含量最高为468.95 μg/L。4株本土酵母发酵液中具有成熟香蕉香气特征的正己酸乙酯、具有菠萝和梨香气特征的辛酸乙酯含量均高于XR,其中QTX-D17含量最高,分别为601.77 μg/L和1 095.55 μg/L。QTX-D17发酵液具有果味香气特征的壬酸乙酯含量最高为326.45 μg/L。本土酿酒酵母QTX-D7、QTXD17、YQY-E18发酵液中,具有甜味、坚果、干果、花香气特征的癸酸乙酯,其含量均高于CECA、XR。具有水果香气特征的庚酸乙酯在QTX-D17发酵液中含量最高,为59.39 μg/L。QTX-D17和YC-E8发酵液中具有甜味、花、奶油香气特征的月桂酸乙酯含量均高于XR。QTX-D17发酵液中棕榈酸乙酯含量高于3株商业酿酒酵母,为62.26 μg/L。仅在QTX-D7发酵液中检测出具有玫瑰和梨香气特征的乙酸庚酯。
2.4.2 高级醇
高级醇可增加香气的复杂度。4株本土酿酒酵母发酵液醇类物质总含量高于商业酿酒酵母CECA、XR,本土酿酒酵母QTX-D17与CECA、XR差异显著。QTX-D7发酵液中具有生青味的1-壬醇含量最高,为781.03 μg/L,显著高于CECA;具有橙子和花香气特征的1-癸醇含量最高,为76.01 μg/L,显著高于3株商业酿酒酵母。QTX-D7发酵液中具有生青味、玫瑰、橙子香气特征的2-壬醇,含量为14.77 μg/L,高于对照菌株。QTX-D17发酵液中的苯乙醇含量最高,为36 741.51 μg/L,显著高于商业酿酒酵母CECA。本土酿酒酵母QTX-D7、QTX-D17、YQY-E18发酵液中,具有柑橘、玫瑰香气特征的1-辛醇,其含量均高于3株商业酿酒酵母,其中QTX-D7含量最高,为2 936.84 μg/L。QTX-D7发酵液中具有香草香气特征的正己醇、具有柠檬和橘子香气特征的庚醇含量最高,分别为16 028.62 μg/L和3 160.76 μg/L;具有蘑菇香气特征的1-辛烯-3-醇含量最高,为238.65 μg/L。仅在本土酿酒酵母QTX-D17、YC-E8、YQY-E18发酵液中检测到具有淡甜味和醇香的异丁醇,其中QTX-D17含量最高,为109 894.05 μg/L。
2.4.3 羰基化合物
醛和酮是主要的两类羰基化合物。它们在结构上的区别在于羰基官能团的位置。醛是形成醇的前体,其羰基官能团位于末端碳上,而酮的羰基官能团位于内部碳上。7株酿酒酵母发酵液中共检测到7种醛类(乙醛、己醛、庚醛、正辛醛、壬醛、癸醛、苯甲醛)和5种酮类(2-戊酮、2-庚酮、3-辛酮、仲辛酮、2-壬酮)。本土酿酒酵母QTX-D17、YC-E8、YQY-E18发酵液中总醛含量高于本土酿酒酵母CECA和XR,其中QTX-D7总醛含量最低(31 506.99 μg/L),与含量最高的QTX-D17(78 170.35 μg/L)相比差异显著。4株本土酿酒酵母发酵液中癸醛含量高于商业酿酒酵母F33和XR,其中QTX-D7发酵液含量最高,为30.92 μg/L。QTX-D17、YC-E8、YQY-E18发酵液中具有辛辣、成熟苹果香气特征的乙醛,含量高于商业酿酒酵母CECA、XR,其中QTX-D17发酵液含量最高,为77 584.71 μg/L。本土酿酒酵母QTX-D7和QTX-D17发酵液中具有生青味的壬醛,含量高于3株商业酿酒酵母,分别为240.94、259.62 μg/L。QTX-D7和QTX-D17发酵液中具有柠檬香气特征的正辛醛,含量高于CECA和XR,其中QTX-D17发酵液含量最高,为282.66 μg/L。QTX-D7发酵液中具有苹果、生青味、青草味的己醛,其含量高于XR。YC-E8发酵液中具有杏仁味香气特征的苯甲醛含量最高,为42.98 μg/L。QTX-D7发酵液中总酮含量最高,为1 016.19 μg/L,显著高于3株商业酿酒酵母。仅在QTX-D7、QTX-D17、YQY-E18发酵液中检测到具有花和水果香气特征的2-壬酮,其中QTX-D17发酵液含量最高为72.55 μg/L。QTX-D7和QTX-D17发酵液中具有草本香气特征的3-辛酮,含量高于3株商业酿酒酵母,其中QTX-D7发酵液含量最高为25.67 μg/L。
2.4.4 酸类
挥发性脂肪酸也可增加香气的复杂度。7株酿酒酵母发酵液中共检测出4种酸类物质:己酸、辛酸、壬酸、癸酸。本土酿酒酵母 QTX-D7、QTX-D17、YQY-E18发酵液中挥发酸总含量高于商业酿酒酵母CECA、XR。QTX-D7发酵液中的己酸含量最高,为1 719.43 μg/L。QTX-D17发酵液中的辛酸含量最高,为671.03 μg/L。QTX-D7发酵液中的壬酸和癸酸含量最高,分别为8.91、385.12 μg/L。
2.4.5 PCA
OAV >0.1表示该挥发性香气成分对香气有贡献,因此选择OAV >0.1的香气物质进行PCA。本研究中,OAV较大的化合物是辛酸乙酯、正己酸乙酯等,它们为发酵液贡献主要香气。为了更直观地比较7种发酵液之间的差异,使用Origin 2022软件通过降维处理对数据进行PCA。如图3所示,第一主成分(PC1)的贡献率为41.6%,第二主成分(PC2)的贡献率为22.9%。主成分的累积方差贡献率达到64%,信息损失率为36%。原始指标的信息大部分被保留下来,并作为主成分来分析发酵液。不同酵母的挥发性香气差异明显,CECA出现在左上象限;XR、YC-E8、YQY-E18出现在左下象限;QTX-D7出现在右上象限;F33、QTX-D17出现在右下象限。QTX-D7的位置离其余6株菌都比较远,香气较为独特。
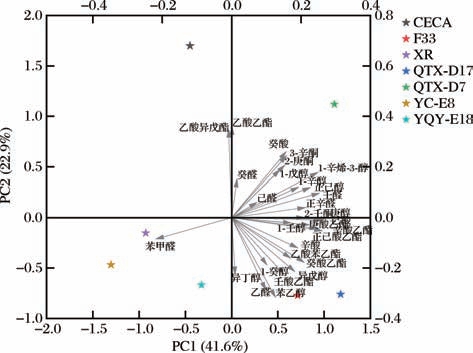
图3 各菌株发酵模拟葡萄汁的挥发性化合物(OAV >0.1)主成分分析载荷图
Fig.3 PCA loadings of volatile compounds (OAV >0.1) in simulated grape juice fermented by each strain
2.4.6 聚类分析
将OAV >0.1的香气物质进行聚类分析,如图4所示,7株酿酒酵母聚为四类(行聚类),第一类包括CECA;第二类包括XR、YC-E8、YQY-E18;第三类包括F33、QTX-D17;第四类包括QTX-D7,与其余三类距离较远,在发酵液挥发性香气成分方面差异较大。香气成分聚为八类(列聚类),第一类包括仅在YCE8、XR发酵液中检测到的苯甲醛;第二类包括在QTX-D7、QTX-D17发酵液中含量较高的癸醛、具有果味和花香的2-壬酮,在QTX-D7发酵液中含量最高的1-壬醇、正己醇、具有柑橘和玫瑰香气特征的1-辛醇、具有果味的1-戊醇;第三类包括在QTX-D7发酵液中含量最高的具有花香特征的乙酸苯乙酯、具有橙子和花香气特征的1-癸醇,在QTX-D17发酵液中含量最高的具有果味的壬酸乙酯,在QTX-D17、F33发酵液中含量较高的苯乙醇,在F33发酵液中含量最高的异戊醇;第四类包括在QTX-D7发酵液中含量最高的己酸、具有柠檬和橘子香气特征的庚醇、1-辛烯-3-醇,在QTX-D17发酵液中含量最高的壬醛;第五类包括在QTX-D17发酵液中含量最高的辛酸、具有菠萝和水果香气特征的庚酸乙酯、具有甜味和花香的癸酸乙酯、具有菠萝和梨香气特征的辛酸乙酯、具有成熟香蕉香气特征的正己酸乙酯;第六类包括在F33发酵液中含量最高的正辛醛、己醛;第七类包括在QTX-D7、QTX-D17发酵液中含量较高的3-辛酮,在QTX-D7、CECA发酵液中含量较高的癸酸、2-庚酮、乙酸异戊酯,在CECA发酵液中含量最高的乙酸乙酯;第八类包括在QTX-D17发酵液中含量最高的异丁醇、乙醛。综上,本土酿酒酵母QTX-D7、QTX-D17发酵液中具有显著性贡献的挥发性香气成分多于其余5株酿酒酵母。
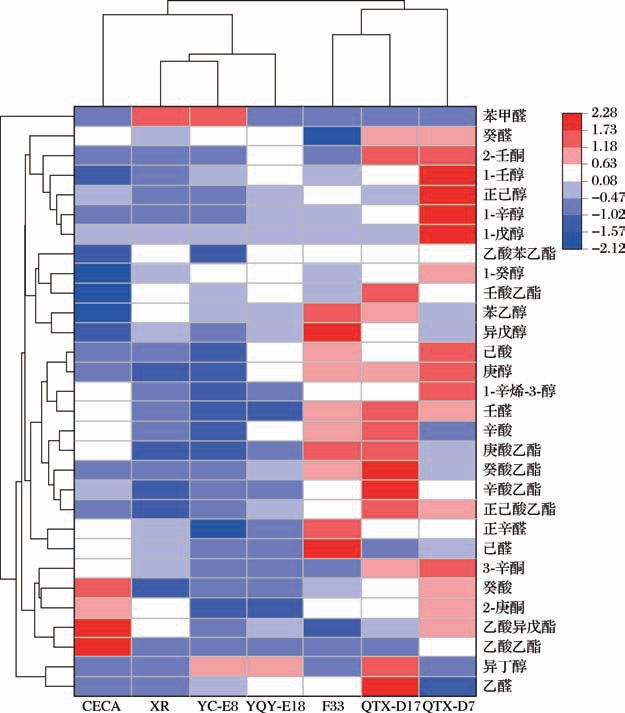
图4 各菌株发酵模拟葡萄汁的挥发性成分(OAV >0.1)聚类分析
Fig.4 Cluster analysis of volatile compounds (OAV >0.1) in simulated grape juice fermented by each strain
3 结论与讨论
优良酿酒酵母菌株应具有生长速度快、发酵平稳、酒精产率高、发酵完全等特性[12]。通过测定在YPD和MSM培养基中的生长曲线发现这7株酿酒酵母的适应能力均较强。通过测定7株酿酒酵母发酵液的CO2产气量及残糖含量发现,QTX-D17、YC-E8的发酵速度明显更快,有较为明显的快速发酵时期,优于3株商业酿酒酵母。合适的酵母发酵剂除了要避免发酵迟缓和卡滞,还必须实现快速发酵,这意味着可以显著节省时间和成本,从而优化酒厂的工艺[13]。因此,本土酿酒酵母QTX-D17和YC-E8有潜力用于葡萄酒酿造,可以快速完成发酵。发酵结束后,对这7株酿酒酵母发酵液的5种基础理化指标进行了测定。结果表明,QTX-D17、YC-E8有较强的产乙醇能力,优于商业酿酒酵母CECA、XR。总酸度是葡萄酒口感协调的标志之一,在成品酒中,总酸度不应超过10 g/L,最理想的值为4~6 g/L[14]。本研究中7种酿酒酵母发酵液的总酸度为1.8~3.1 g/L,本土酿酒酵母QTX-D17的产酸能力最强,发酵液的总酸度最接近理想的总酸度。QTX-D7和QTX-D17发酵液中挥发酸的含量高于3株商业酿酒酵母。QTX-D17、YC-E8的还原糖利用率较高,优于商业酿酒酵母CECA、XR。YC-E8、QTX-D17产甘油能力较强,优于商业酿酒酵母XR,可以使葡萄酒的口感圆润。4株本土酿酒酵母发酵液pH值相近,与商业酿酒酵母CECA的pH值差异不显著。由以上发酵特性可知,本土酿酒酵母QTX-D17、YC-E8发酵液的发酵速度、产乙醇能力、产酸能力、还原糖利用率、产甘油能力优于商业酿酒酵母,具有优良酿酒酵母的特质。
本研究对7株酿酒酵母发酵液进行挥发性香气成分分析。对比7株酿酒酵母发酵液的酯类物质发现,4株本土酿酒酵母发酵液中乙酸异戊酯、正己酸乙酯、辛酸乙酯、壬酸乙酯、十一酸乙酯能够带来果香的酯类物质,其含量高于部分商业酿酒酵母。其中,乙基酯类中的正己酸乙酯、辛酸乙酯含量最高,能够带来成熟的香蕉、菠萝、梨的香气特征,与CARPENA等[15]的研究结果一致;发酵液中乙酸异戊酯的含量,QTX-D7可达商业酿酒酵母F33的4.5倍,QTX-D17可达商业酿酒酵母F33的2.8倍,能够带来香蕉的香气特征;发酵液中壬酸乙酯的含量,QTX-D7可达商业酿酒酵母CECA的2.3倍,QTX-D17可达商业酿酒酵母CECA的3.3倍,能够带来水果的香气特征。有研究表明,乙酸乙酯质量浓度低于150 mg/L时会散发出理想的香气[16]。本土酿酒酵母QTX-D7发酵液中有乙酸乙酯,且质量浓度低于150 mg/L,带来了令人愉快的果香和甜味。乙酸庚酯是本土酿酒酵母QTX-D7发酵液中的特异性香气物质,能够带来玫瑰般的香气特征。巩丽莉等[17]在本土酿酒酵母QTXD17发酵液中检测到了一种特异性香气物质2-己烯酸乙酯;杨惠婷[4]在本土酿酒酵母发酵液中检测到十一酸乙酯等特异性香气物质。可见,本土酿酒酵母QTX-D7和QTX-D17可以产生比商业酵母更多的酯类物质,并且还能产生具有菌株特异性的酯类物质。对比7株酿酒酵母发酵液的醇类物质发现,4株本土酿酒酵母发酵液中高级醇的质量浓度均低于330 mg/L,能够产生积极的芳香贡献;能够带来积极香气特征的醇类物质中,1-壬醇、1-癸醇的含量高于3株商业酿酒酵母,苄醇的含量高于商业酿酒酵母CECA、F33,苯乙醇的含量高于商业酿酒酵母CECA。其中,QTX-D7发酵液中1-壬醇的含量可达商业酿酒酵母CECA的2.6倍,能够带来生青味;1-癸醇的含量可达商业酿酒酵母CECA的2.1倍,能够带来橙子和花的香气特征;苄醇的含量可达商业酿酒酵母F33的4倍,能够带来杏仁味;苯乙醇的含量可达商业酿酒酵母CECA的1.6倍,UGLIANO等[18]认为苯乙醇的存在是比较理想的,是花香特征的潜在贡献者,尽管检测到的苯乙醇浓度低于阈值,但其仍能与其他挥发性物质一起对香气做出贡献[19]。另外,QTX-D7发酵液中异戊醇的含量最低,DE-LA-FUENTE-BLANCO等[20]发现异戊醇会抑制果香和木香,对葡萄酒的香气质量起负面作用,因此,QTX-D7发酵液中较低的异戊醇含量可能意味着对香气的负面影响相对较弱。对比7株酿酒酵母发酵液的醛类物质发现,QTX-D7和QTX-D17这2株本土酿酒酵母菌株产生的乙醛有显著差异,乙醛可能是这2株本土酿酒酵母发酵液的关键挥发性化合物之一。乙醛与其他化合物具有较高的反应活性,对葡萄酒香气轮廓具有直接影响和间接影响[21-22]。低浓度的乙醛赋予了令人愉悦的果香;当其浓度较高时,会产生青草般的异味[23]。QTX-D7发酵液的乙醛含量低于QTX-D17,在此方面,QTX-D7优于QTX-D17。对比7株酿酒酵母发酵液的酸类物质发现,4株本土酿酒酵母的酸类物质含量均未超过700 mg/L,不会为发酵液带来不愉快的香气特征[24]。由以上香气成分分析可知,相较于3株商业酿酒酵母,本土酿酒酵母QTX-D7和QTX-D17能够产生更多具有积极香气特征的香气物质,可用于酿造风味独特的葡萄酒。综上所述,本土酿酒酵母QTX-D17、YC-E8的发酵特性及QTX-D7、QTX-D17的挥发性香气物质合成能力优于商业酿酒酵母,具有作为葡萄酒优良发酵剂的潜能,可为宁夏贺兰山东麓产区的酿酒微生物资源开发提供参考。
[1]SWIEGERS J H,BARTOWSKY E J,HENSCHKE P A,et al.Yeast and bacterial modulation of wine aroma and flavour[J].Australian Journal of Grape and Wine Research,2005,11(2):139-173.
[2]孙雅慧.优质果香型本土酿酒酵母的筛选[D].烟台:烟台大学,2023.SUN Y H.Screening of high-quality fruit-flavored indigenous Saccharomyces cerevisiae[D].Yantai:Yantai University,2023.
[3]刘沛通,丁子元,于庆泉,等.优良本土酿酒酵母的酿造特性研究[J].中国食品学报,2023,23(1):204-215.LIU P T,DING Z Y,YU Q Q,et al.Studies on oenological characteristics of high-quality Chinese indigenous Saccharomyces cerevisiae strains[J].Journal of Chinese Institute of Food Science and Technology,2023,23(1):204-215.
[4]杨惠婷.浙江地区酿酒酵母的优选鉴定及发酵特性的研究[D].呼和浩特:内蒙古农业大学,2022.YANG H T.Optimization identification and fermentation characteristics of Saccharomyces cerevisiae in Zhejiang province[D].Hohhot:Inner Mongolia Agricultural University,2022.
[5]宋佳佳.苏皖地区酿酒酵母的筛选鉴定及其发酵特性研究[D].呼和浩特:内蒙古农业大学,2022.SONG J J.Screening and identification of Saccharomyces cerevisiae and research on fermentation characteristics in Jiangsu and Anhui regions[D].Hohhot:Inner Mongolia Agricultural University,2022.
[6]赵海霞,王晓蕾,张琇.贺兰山东麓鲜食葡萄优良本土酿酒酵母的筛选和发酵特性研究[J].中国酿造,2025,44(1):73-79.ZHAO H X,WANG X L,ZHANG X.Screening and fermentation characteristics of superior indigenous Saccharomyces cerevisiae from table grapes in the eastern foothills of Helan Mountain[J].China Brewing,2025,44(1):73-79.
[7]周桂珍,杨伟明,杨建兴,等.宁夏贺兰山东麓葡萄酒酵母菌的筛选及应用[J].微生物学通报,2023,50(2):553-572.ZHOU G Z,YANG W M,YANG J X,et al.Screening and application of wine yeasts at the eastern foot of Helan Mountain in Ningxia Hui Autonomous Region[J].Microbiology China,2023,50(2):553-572.
[8]周迪,卢玲,王岚.贺兰山东麓产区非酿酒酵母筛选及发酵特性研究[J].食品与发酵工业,2025,51(1):72-80.ZHOU D,LU L,WANG L.Screening and fermentation characteristics of non-Saccharomyces yeasts from eastern foot of Helan Mountain[J].Food and Fermentation Industries,2025,51(1):72-80.
[9]CULLERÉ,ESCUDERO A,CACHO J,et al.Gas chromatographyolfactometry and chemical quantitative study of the aroma of six premium quality Spanish aged red wines[J].Journal of Agricultural and Food Chemistry,2004,52(6):1653-1660.
[10]HU K,JIN G J,MEI W C,et al.Increase of medium-chain fatty acid ethyl ester content in mixed H. uvarum/S. cerevisiae fermentation leads to wine fruity aroma enhancement[J].Food Chemistry,2018,239:495-501.
[11]ZEA L,MOYANO L,MORENO J,et al.Discrimination of the aroma fraction of Sherry wines obtained by oxidative and biological ageing[J].Food Chemistry,2001,75(1):79-84.
[12]VATS P,BANERJEE U C.Studies on the production of phytase by a newly isolated strain of Aspergillus niger var teigham obtained from rotten wood-logs[J].Process Biochemistry,2002,38(2):211-217.
[13]ANDORRÀ I,MIRÓ G,ESPLIGARES N,et al.Wild Yeast and Lactic Acid Bacteria of Wine[M].Peixoto Basso T.Yeasts in Biotechnology.IntechOpen,2019.
[14]CIOCH-SKONECZNY M,SATORA P,SKONECZNY S,et al.Physicochemical characterization of wines produced using indigenous yeasts from cold climate grapes[J].European Food Research and Technology,2021,247(1):201-209.
[15]CARPENA M,FRAGA-CORRAL M,OTERO P,et al.Secondary aroma:Influence of wine microorganisms in their aroma profile[J].Foods,2021,10(1):51.
[16]PADILLA B,GIL J V,MANZANARES P.Past and future of non-Saccharomyces yeasts:From spoilage microorganisms to biotechnological tools for improving wine aroma complexity[J].Frontiers in Microbiology,2016,7:411.
[17]巩丽莉,周迪,卢玲,等.贺兰山东麓优良本土酿酒酵母筛选及发酵特性分析[J].微生物学通报:2023,50(9):4021-4044.GONG L L,ZHOU D,LU L,et al.Screening and fermentation of excellent indigenous Saccharomyces cerevisiae strains from eastern foothills of Helan Mountains[J].Microbiology China:2023,50(9):4021-4044.
[18]UGLIANO M,HENSCHKE P.Yeasts and Wine Flavour[M].Wine Chemistry and Biochemistry,2009:313-392.
[19]ZHU J C,NIU Y W,XIAO Z B.Characterization of the key aroma compounds in Laoshan green teas by application of odour activity value (OAV),gas chromatography-mass spectrometry-olfactometry(GC-MS-O) and comprehensive two-dimensional gas chromatography mass spectrometry (GC × GC-qMS) [J].Food Chemistry,2021,339:128136.
[20]DE-LA-FUENTE-BLANCO A,SÁENZ-NAVAJAS M P,FERREIRA V.On the effects of higher alcohols on red wine aroma[J].Food Chemistry,2016,210:107-114.
[21]STYGER G,PRIOR B,BAUER F F.Wine flavor and aroma[J].Journal of Industrial Microbiology &Biotechnology,2011,38(9):1145-1159.
[22]LIU S Q,PILONE G J.An overview of formation and roles of acetaldehyde in winemaking with emphasis on microbiological implications[J].International Journal of Food Science &Technology,2000,35(1):49-61.
[23]TEKARSLAN-SAHIN S H.Adaptive laboratory evolution of yeasts for aroma compound production [ J].Fermentation,2022,8(8):372.
[24]LAI Y T,HSIEH C W,LO Y C,et al.Isolation and identification of aroma-producing non-Saccharomyces yeast strains and the enological characteristic comparison in wine making[J].LWT,2022,154:112653.