丙酸为重要的三碳有机酸,广泛应用于药物合成、饲料防腐和生物基纤维制造。1984年,美国食品和药物管理局(Food and Drug Administration,FDA)和世界卫生组织(World Health Organization,WHO)批准丙酸为食品安全防腐剂[1],人体最高摄入可达3 000 mg/kg[2]。因此,丙酸及丙酸钙在食品和农产品保鲜领域中需求增加迅速。丙酸及其盐类的全球市场规模从2022年46.325万t逐年增长,估计到2030年达到60.31万t,2023年我国丙酸产量达到8.12万t,2024年9.0万t,丙酸产量年增长10.84%。
目前丙酸主要来源于石化合成,以石油为原料合成丙酸用于食品防腐剂存在安全隐患,因此,急需以微生物发酵法替代化学合成法获得丙酸[3]。丙酸为生物还原代谢末端产物,合成丙酸的微生物主要为厌氧或兼性厌氧菌,其中丙酸杆菌属中的产酸丙酸杆菌(Acidipropionibacterium acidipropionici)为最常见的丙酸生产菌,该菌为兼性厌氧菌,无运动,一般呈杆状、不形成孢子,可利用葡萄糖、甘油、乳酸、乳酸钠、木糖和纤维素水解物等多种碳源生产丙酸[4-6],其合成代谢途径主要经糖酵解途径和Wood-Werkman途径[7]。LIU等[8]以产酸丙酸杆菌ATCC 4965为发酵菌种,于5 L发酵罐以葡萄糖和甘油为混合碳源发酵丙酸,产量达到21.90 g/L;YANG等[9]以果糖为碳源,获得26.5 g/L的丙酸产量;马永良[10]利用产酸丙酸杆菌FS1171,分批补料发酵17 d获得86.65 g/L的丙酸产量。目前,产酸丙酸杆菌发酵丙酸存在发酵周期长、丙酸浓度低、副产物乙酸、琥珀酸和乳酸多等问题,导致工业化生产丙酸成本居高不下。
产酸丙酸杆菌具有独特的细胞壁成分和细胞内强限制性修饰系统[11],使该菌的遗传改造非常困难,同时应用基因工程改造菌株所产丙酸及丙酸钙,无法通过安全认证用于食品添加剂,因此,以多重叠加诱变的方法[12],配合高效筛选路径,获得高产丙酸的微生物菌株势在必行。本文对本实验室保藏的产酸丙酸杆菌PA8进行微波超声联合诱变复合常温常压等离子体(atmospheric room temperature plasma,ARTP)诱变,以透明圈与菌落直径比值进行大量菌株筛选,该方法实现85% 以上正向突变,然后以血清瓶发酵丙酸复筛,最终获得一株高产丙酸的突变株,为工业化生产丙酸提供了高产丙酸的生产菌,以及诱变筛选方法。
由于产酸丙酸杆菌PA8分离于天然酸乳,存在多种维生素和氨基酸合成缺陷,找到适合该菌生长和发酵丙酸的培养基组成,是实现其工业化发酵丙酸的必要条件。酵母提取物因富含氨基酸和维生素B族,可为产酸丙酸杆菌生长提供必需的维生素和氨基酸,进而显著提高发酵丙酸产率,但其高昂成本限制了工业应用[13-15],发酵丙酸的低成本氮源替代物成为热点,YANG等[9]利用大豆糖蜜与玉米浆混合氮源,将丙酸生产成本降低70%。因此,本研究开发酵母细胞裂解液和玉米浆替代酵母提取物,大幅度降低发酵培养基成本。此外,金属离子Fe2+、Zn2+、Mn2+和Co2+对丙酸合成途径中的关键酶具有显著调控作用,尤其Co2+是丙酸代谢关键酶甲基丙二酰-CoA变位酶的辅因子,其浓度直接影响碳代谢流合成丙酸和副产物生成[16-17]。因此,本研究对诱变筛选获得高产丙酸菌株的发酵关键组成进行优化,在降低培养基成本的同时,获得较好发酵丙酸的结果。
综上所述,本文旨在通过微波联合超声诱变复合ARTP诱变产酸丙酸杆菌PA8,以透明圈/菌落直径的方法大量筛选突变株,获得一株稳定遗传的高产丙酸的产酸丙酸杆菌,对其发酵丙酸培养基中氮源种类和金属离子等关键组分进行单因素和响应面分析优化,最终在10 L发酵罐中验证了高产菌株和优化培养基的有效性,结果使丙酸产量提高了21.44%,发酵周期缩短了42 h。本研究可为丙酸工业化生产奠定基础,同时为丙酸高产菌株的获得提供有价值的策略和方法。
1 材料与方法
1.1 材料
1.1.1 菌种
产酸丙酸杆菌PA8,保藏于本实验室。
1.1.2 试剂
蛋白胨、酵母粉,Oxoid公司;乳酸钠,天津科密欧化学试剂有限公司;胰蛋白胨大豆肉汤(trypticase soy broth TSB),海博生物技术有限公司;丙酸,天津市津东天正精细化学试剂厂;葡萄糖、硫酸镁、磷酸氢二钾,福晨(天津)化学试剂有限公司;玉米浆,酵母抽提物,山东阳城生物科技有限公司。
1.1.3 培养基
基本培养基(g/L):TSB 10,酵母粉10,乳酸钠10;(固体基本培养基另加18琼脂粉)。
初筛培养基(g/L):TSB 10,酵母粉10,葡萄糖20,碳酸钙1,琼脂粉18,pH 7.0。
复筛发酵培养基(g/L):蛋白胨10,酵母粉5,葡萄糖45,磷酸氢二钾1,硫酸镁0.5,pH 7.0。
发酵培养基(g/L):葡萄糖70、蛋白胨18、玉米浆10、酵母抽提物6、磷酸氢二钾1、硫酸镁0.5、硫酸铁0.1、硫酸锌0.08、氯化钴0.1、硫酸锰0.1,初始pH 6.0。
1.2 仪器与设备
KM-23C超声波清洗机,北京赛智创业科技有限公司;Mandela型多功能等离子体诱变系统,北京艾德豪克仪器生物有限公司;G80F23CN2P-B5(R0)微波炉,广州格兰仕微波生活电器制造有限公司;SBA-40E物传感分析仪,山东省科学院生物研究所;Agilent 1200高效液相色谱仪,安捷伦科技有限公司;AminexHPX-87H色谱柱,伯乐生命医学产品(上海)有限公司。
1.3 实验方法
1.3.1 诱变菌悬液制备
出发菌株PA8于固体基本培养基中划线活化,挑取单菌落于液体基础培养基中30 ℃厌氧培养48 h,以4%接种量至基础培养基,30 ℃培养36 h。取1 mL菌液,12 000 r/min离心5 min,菌体离心洗涤2次后用1 mL生理盐水重悬,并稀释100倍(OD600 值为0.07~0.09,菌落数为3~5 ×108个/mL)备用。
1.3.2 微波-超声联合诱变方法
微波诱变[18]:取稀释好的菌液5 mL置于50 mL锥形瓶中,微波功率800 W,每8 s取出,冰浴15 s,以消除热效应,累计诱变不同时间。
超声诱变:取稀释好的菌液5 mL置于10 mL无菌EP管中,置于40 kHz的低频率超声处理,每9 s取出,冰浴5 s,消除热效应,累计诱变不同时间。
微波-超声联合诱变[19]:取稀释好的菌液5 mL置50 mL锥形瓶中,微波单独诱变100 s,将菌液置于10 mL无菌EP管中于40 kHz的低频率超声处理,每9 s取出,冰浴降温处理5 s,消除热效应,累计诱变不同时间。
1.3.3 ARTP诱变方法
取稀释好的菌悬液10 μL置于ARTP育种仪配套的金属载片上,按照ARTP生物育种仪的操作流程,以高纯氦气为气源,设定功率为100 W,氮气流量10 SLM,载片与气流端口距离为2 mm,诱变不同时间,诱变结束后立刻将金属载片置于1 mL无菌生理盐水中,避光培养[20]。
1.3.4 诱变后平板初筛方法
将诱变后菌悬液稀释至10-2,取100 μL涂布于初筛培养基平板,30 ℃厌氧培养,120 h测定计算透明圈直径比菌落直径,挑选圈径比值高的菌株进行复筛。
1.3.5 诱变菌株复筛方法
将初筛菌株在血清瓶液体发酵培养基体系进行复筛。一级种子培养:斜面菌苔接种于液体基本培养基的血清瓶中,30 ℃厌氧培养36 h;二级种子培养:一级种子以4%接种于液体基本培养基的血清瓶中,30 ℃厌氧培养48 h;二级种子以10%接种量接种于液体发酵培养基中,发酵168 h,其中第24、72 h补加2 mL 100 g/L碳酸钙母液。于96、168 h分别取样,进行有机酸和残糖检测。
HPLC检测丙酸及其他主要有机酸[21]:
a)标准溶液的制备:丙酸标准溶液20 g/L用5 mmol/L硫酸分别稀释至0.5、1.0、1.5、2.0、2.5 g/L;将乳酸及琥珀酸定容标准溶液20 g/L,分别用5 mmol/L硫酸相稀释至0.2、0.4、0.6、0.8、1.0 g/L。
b)样品处理:将样品于8 000 r/min离心5 min,吸取1 mL上清液置于10 mL容量瓶中,使用流动相定容至10 mL;0.22 μm滤器过滤待测。
c)检测条件:色谱柱AminexHPX-87H、流动相为5 mmo/L的硫酸、流速0.8 mL/min、柱温30 ℃、加样量10 μL,紫外检测波长215 nm。
d)标准曲线:以浓度为横坐标、峰面积为纵坐标,建立丙酸、琥珀酸、乳酸浓度与检测峰面积的回归曲线,在检测浓度范围内,3种有机酸线性范围均良好,回归方程分别为:丙酸(y=0.916 +346.43x,R2=0.999 4);琥珀酸(y=0.58 +334.79x,R2=0.999 8);乳酸(y=9.689 +493.04x,R2=0.999 2)。
1.3.6 发酵培养基优化
1.3.6.1 发酵丙酸有机氮源的优化
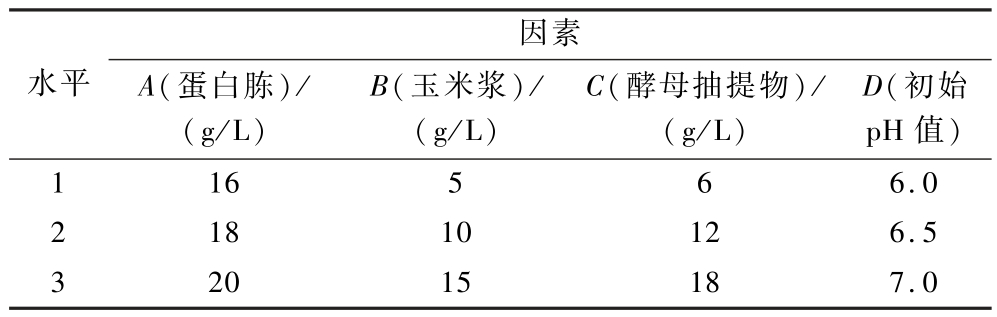
为了适应工业化生产需要,以玉米浆替代部分有机氮源,酵母抽提物替代酵母粉,选择蛋白胨(A)、玉米浆(B)、酵母抽提物(C)、初始pH(D)为考察因素,以168 h丙酸产量为评价指标,设计L9(34)正交试验如表1所示,以优化发酵培养基组分。发酵与检测方法按1.3.5节中方法进行。
表1 氮源正交试验设计
Table 1 Orthogonal experimental design of nitrogen sources
1.3.6.2 发酵丙酸金属离子的优化
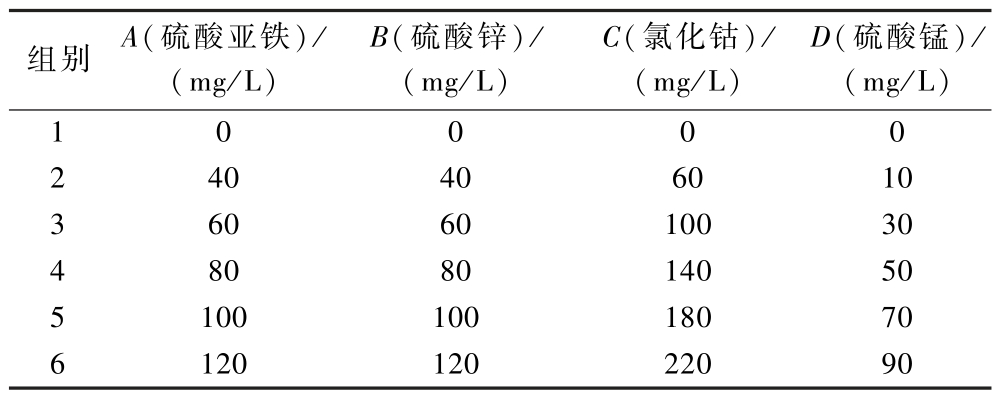
根据DERMAN等[15]的研究,金属离子对于产酸丙酸杆菌的丙酸产量有积极的效果,选择硫酸亚铁、硫酸锌、氯化钴、硫酸锰4种金属离子对发酵培养基进行单因素试验;在氮源优化后培养基的基础上,分别添加硫酸亚铁、硫酸锌、氯化钴、硫酸锰进行发酵实验,添加金属离子水平如表2所示。
表2 金属离子对发酵丙酸的影响设计
Table 2 The design of the influence of metal ions on fermentative propionic acid production
根据单因素试验结果以硫酸亚铁(A)、硫酸锌(B)、氯化钴(C)、硫酸锰(D) 为考察因素,以168 h丙酸产量为评价指标,设计L9(34)正交试验如表3所示,以优化发酵培养基组分。发酵与检测方法按1.3.5节中方法进行。
表3 金属离子正交试验设计
Table 3 Orthogonal experimental design of metal ions

1.3.7 10 L罐发酵验证方法
一二级种子培养与1.3.5节所示方法一致,二级种子液按10%接种量至10 L发酵罐中,使用优化后的发酵培养基,32 ℃厌氧培养,自动流加150 g/L氢氧化钙调节pH值为5.3,残葡萄糖降低到1 g/L结束发酵。
1.4 数据分析
试验数据采用Excel、SPSS进行处理,Origin 2018软件进行图形的绘制。
2 结果与分析
2.1 微波-超声联合诱变
2.1.1 微波诱变及超声诱变致死率
以PA8菌株为出发菌株,采用1.3.2节所述方法进行微波诱变,微波处理时间设定为40、60、80、100、120、150、200 s。经诱变处理后的菌悬液稀释涂布于基本培养基上,厌氧培养72 h。以存活菌落数量计算致死率,实验结果如图1所示,随着诱变时间的延长,致死率呈现上升趋势,到120 s时致死率到达80%。但随后150 s致死率略有下降,随后上升,到200 s时,致死率与120 s时相当。故选择在致死率下降之前的一个时间点,即100 s(致死率为65.81%)作为微波联合超声诱变的微波诱变剂量。
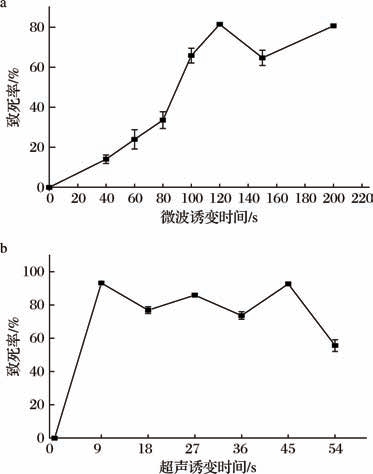
图1 微波诱变及超声诱变致死率曲线
Fig.1 Lethality curves of microwave mutagenesis and ultrasonic mutagenesis
a-微波诱变;b-超声诱变
以PA8菌株为出发菌株,采用1.3.2节所述方法,菌体经超声波处理,时间分别为9、18、27、36、45、54 s,诱变处理后稀释涂布于基本培养基,厌氧条件下培养72 h。以菌落数绘制致死率曲线如图1所示。菌株PA8对超声波诱变极其敏感,9 s超声波处理即达到90%的致死率,但随后延长超声诱变时间,致死率呈现逐渐下降趋势,超声波处理54 s时,致死率回落至较低水平。
根据上述致死率结果,鉴于PA8菌株对不同诱变条件的响应特性,本研究选择在微波诱变100 s后连续进行9 s的超声诱变,以期实现更为有效的遗传变异筛选。
2.1.2 微波-超声联合诱变及菌株筛选
以PA8菌株为出发菌株,通过微波-超声联合诱变之后,采用1.3.4节所述方法进行平板筛选(图2),在基本平板上选择60株生长速度快,菌落直径大的菌株点种至初筛平板上,并命名为LH1-LH59,同时以点种出发菌株PA8作为对照,在120 h时记录菌株圈径比,具体数据见电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.043146,下同)。
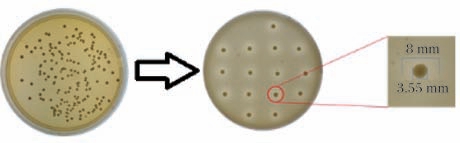
图2 平板筛选方法示意
Fig.2 Schematic diagram of the plate screening method
通过诱变后菌株与出发菌株的圈径比挑选出13株圈径比大于PA8菌株(2.70)且生长旺盛的菌株,进行下一步血清瓶发酵筛选,所挑选菌株分别为:LH1 (3.50)、LH2(3.00)、LH3(3.00)、LH5(4.00)、LH37(3.00)、LH38 (4.60)、LH41 (3.14)、LH44(3.00)、LH45(3.33)、LH52(3.00)、LH54(3.67)、LH56 (4.33)、LH57(3.33)。
2.1.3 联合诱变菌株复筛
对上一节筛选出13株菌以1.3.5节方法进行液体发酵,从中筛选出丙酸产量及丙酸占总酸比例最高的菌株。结果如图3所示,与出发菌株PA8(12.63 g/L丙酸产量)相比,11株菌在丙酸产量以及丙酸占总酸比率均优于PA8菌株,其正向筛选率85%,表明该平板透明圈筛选方法具有较好的适用性。其中菌株LH5(14.15 g/L)、LH54(14.46 g/L)丙酸产量提高均在10%以上,LH54丙酸占比总酸达到71.08%,LH5达到62.24% 较出发菌株(59.39%) 分别提高了2.85%、11.69%。在工业中,丙酸占总酸比率的提高有利于后续对丙酸的提取和纯化,有效降低丙酸生产的成本,选择丙酸产量和丙酸占比最高的LH54进行后续的ARTP诱变,以期获得更加优势的菌株。
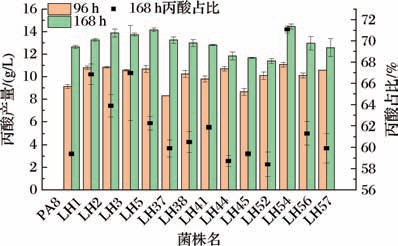
图3 微波-超声联合诱变复筛菌株发酵结果及丙酸占比
Fig.3 Fermentation results of microwave-ultrasonic combined mutagenesis re-screened strains and propionic acid proportion
2.2 ARTP诱变获得高产丙酸菌
2.2.1 ARTP诱变致死率曲线绘制及诱变
以LH54为出发菌株,采用1.3.3节所述方法进行ARTP诱变,诱变时间分别为15、30、45、60、75、90、105、120 s。经诱变处理后的菌株稀释涂布于基本培养基上,并在厌氧条件下培养72 h,计算菌体致死率,结果如图4所示。
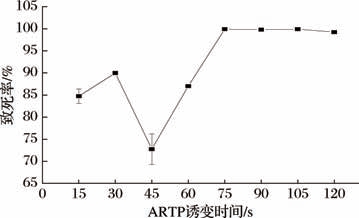
图4 ARTP诱变致死率曲线
Fig.4 ARTP mutagenesis lethality curve
LH54菌体的致死率呈现先增加然后突然降低,随后再次上升并稳定到致死率近乎100%。ARTP处理的前30 s内,随着诱变时间的延长,致死率显著提升至89.99%,但诱变时间延长到45 s时,致死率骤然降低,随后诱变延长到75 s致死率达到98%呈现出致死率急速增加趋势,75~ 120 s致死率达到100%。如图5所示结果,本文选择30 s为ARTP诱变处理时间。
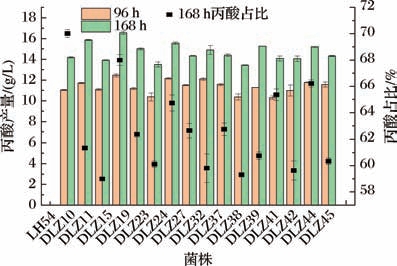
图5 ARTP诱变复筛菌株发酵结果及丙酸占比
Fig.5 Fermentation results of ARTP mutagenesis re-screened strains and propionic acid proportion
产酸丙酸杆菌PA8经过微波-超声波复合诱变后叠加ARTP诱变3种物理诱变过程,均出现初始诱变计量致死率急剧增加,随后致死率下降,然后又增加的波动现象。本文推测该现象与PA8菌株自身的DNA修复能力相关,其细胞内具有较强的SOS修复系统等DNA修复机制[22],当细菌受到环境压力刺激后,启动细胞内SOS修复系统,胞内能量与分配倾向于DNA修复,延缓菌体分裂使部分菌体存活。已有研究指出高剂量胁迫下,细菌可能优先分配资源至修复而非生长[23],因此在相对低剂量损伤压力范围,PA8菌株胞内的修复机制未被完全激活,DNA复制受到外来物理能量破坏,导致菌体大量死亡;随后诱变计量增加达到一定阈值后,胞内的修复机制被全部激活,菌体内优先分配能量至DNA修复,同时细胞分裂减弱使损伤致死率突然短暂下降;但继续增加诱变剂量后引发细胞内DNA修复机制的紊乱,反而减少有效修复[24],表现为菌体死亡快速增加直至致死率100%。本文所选择的诱变剂量均为诱变致死率第一轮高峰时点,此时菌体细胞未完全激活DNA修复机制,有利于获得更高的突变率。
2.2.2 ARTP诱变平板筛选
对LH54菌株进行30 s ARTP诱变后,以1.3.4节方法进行菌株平板初筛。于初筛平板上点种45株菌,命名为DLZ1~DLZ45,以出发菌株LH54做对照,在120 h时记录菌株圈径比,具体数据见附表2。
通过对比出发菌株与诱变后菌株的圈径比及菌株在平板上的生长状况,挑选其中15株圈径比大于出发菌株LH54(2.73)或生长旺盛的菌株进行下一步筛选,分别为:DLZ10 (3.33)、DLZ11 (2.67)、DLZ15(3.33)、DLZ19(3.33)、DLZ23(2.67)、DLZ24(3.00)、DLZ27(2.67)、DLZ32(2.67)、DLZ37(4.00)、DLZ38(2.67)、DLZ39(3.00)、DLZ41(3.00)、DLZ42(2.67)、DLZ44(2.67)、DLZ45(2.67)。
2.2.3 ARTP诱变菌株复筛
通过初筛获得的15株突变菌株,以1.3.5节方法进行液体发酵实验。发酵结果如图5所示。
产酸透明圈直径比菌落直径,比值超过出发菌株LH54的突变菌株发酵产酸均有提高,此筛选方法正确率达100%;其中突变株DLZ10(15.87 g/L丙酸产量)和DLZ15(16.57 g/L丙酸产量)分别比出发菌株LH54(丙酸产量14.19 g/L)丙酸产量提高11.86%和16.79%,将DLZ15和DLZ10菌株进行传代稳定性验证,两菌株斜面转接10代,其0、2、4、6、8、10代斜面菌体发酵产丙酸没有差异,这表明诱变筛选出的菌株具有较高的遗传稳定性,对比2株突变株的丙酸产量,最终选择DLZ15菌株进行发酵培养基优化实验。
2.3 发酵工艺优化
2.3.1 丙酸发酵中有机氮源的优化
在前期实验的基础上结合工业生产实际,选择不同的氮源组合对发酵培养基进行进一步优化,以获得最适突变菌株DLZ15的发酵方案。由于培养基中引入玉米浆和酵母抽提物,对发酵初始pH存在较大影响,故本次优化中对培养基的初始pH进行同时优化,根据软件正交设计助手设计正交试验,按照实验方案进行发酵实验,实验结果如表4所示。
表4 氮源正交试验结果
Table 4 Orthogonal experiment results of nitrogen sources
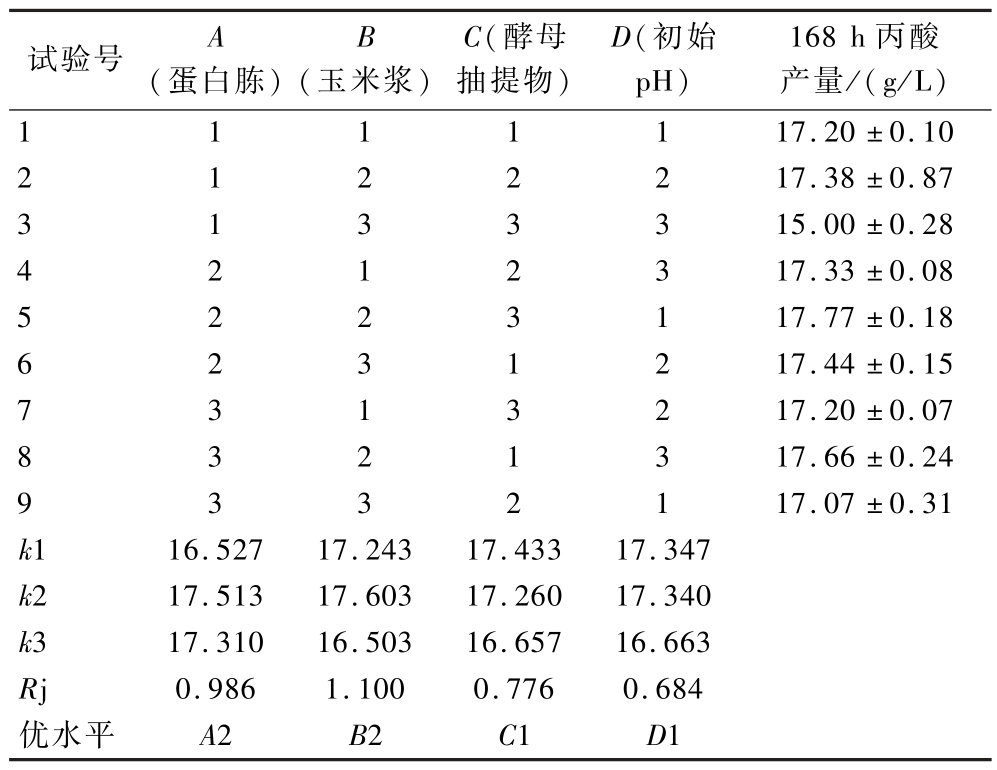
由表4可知,以丙酸产量作为指标,最优组合为A2B2C1D1,即蛋白胨18 g/L、玉米浆10 g/L、酵母粉0.6 g/L、初始pH值为6.0。对于丙酸产量的影响大小顺序为:玉米浆>蛋白胨>酵母抽提物>初始pH值。根据方差分析(附表3),本次正交试验所设计的因素对丙酸产量的影响均显著(P <0.05),3种氮源的影响极为显著(P <0.01)。方差分析与极差分析结果一致。
选择发酵培养基为(g/L):蛋白胨18、玉米浆10、酵母抽提物6、葡萄糖45、磷酸氢二钾1、硫酸镁0.5,初始pH值6.0与初始培养基进行对比,结果如图6-a所示,优化后培养基在96、168 h时丙酸产量均有所提升,其中168 h丙酸产量由16.80 g/L提高到18.16 g/L,产量提高了8.10%;160 h丙酸占比从69.70%提高至73.92%,提高了4.22%。
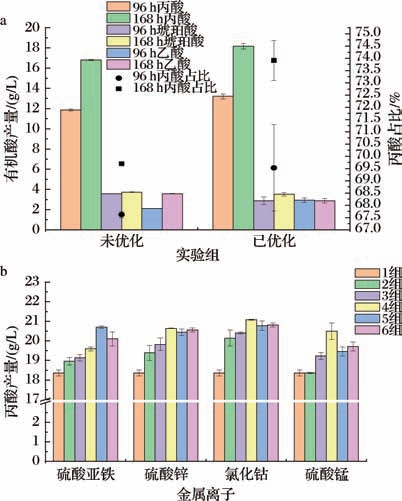
图6 氮源正交试验结果验证及金属离子单因素试验结果
Fig.6 Verification of the orthogonal experiment results for nitrogen sources and orthogonal experiment results of nitrogen sources
a-氮源正交试验结果验证;b-金属离子单因素试验结果
2.3.2 丙酸发酵中金属离子单因素试验和正交试验优化
2.3.2.1 金属离子单因素试验
金属离子作为辅因子参与丙酸代谢过程,其中亚铁离子、锌离子、钴离子和锰离子对丙酸的发酵存在较显著的作用[11]。在氮源优化培养基的基础上,进行硫酸亚铁、硫酸锌、氯化钴和硫酸锰进行单因素试验,结果如图6-b所示。分别添加不同浓度各金属离子,发酵丙酸均优于未添加金属离子的对照组。
其中硫酸亚铁100 mg/L、硫酸锌80 mg/L、氯化钴140 mg/L、硫酸锰50 mg/L为各金属离子添加最优质量浓度,丙酸产量分别为20.69、20.63、21.08、20.48 g/L。DISHISHA等[25]发现,添加0.1 g/L硫酸亚铁可使费氏丙酸杆菌(Propionibacterium freudenreichii)的丙酸产量提高30%,与本论文结果一致;报导同时指出费氏丙酸杆菌在Zn2+质量浓度超过0.05 g/L时被抑制生长,本文Zn2+ 质量浓度达到0.08 g/L时发酵丙酸产量最佳,高于0.08 g/L质量浓度对发酵产丙酸无显著影响,推测由于菌种具有差异,产酸丙酸杆菌对Zn2+质量浓度不敏感,马永良[10]也发现用产酸丙酸杆菌FS1171菌株发酵丙酸时,分别加入硫酸亚铁12 mg/L,硫酸锰16 mg/L,丙酸产量分别达20.7、20.8 g/L,与本文结果相当。
2.3.2.2 金属离子正交试验
以2.3.2.1节中产量最优的各金属离子浓度作为正交试验的中间水平进行金属离子正交试验。根据软件正交设计助手设计正交试验,按照实验方案进行发酵实验,实验结果如表5所示。
表5 金属离子正交试验结果
Table 5 Orthogonal experiment results of metal ions
由表5可知,金属离子的最优组合为A2B2C2D3,即硫酸铁100 mg/L、硫酸锌80 mg/L、氯化钴140 mg/L、硫酸锰100 mg/L。对于丙酸产量的影响大小顺序为:硫酸锰>氯化钴>硫酸铁>硫酸锌。根据方差分析(附表4),仅硫酸锰对丙酸产量的影响均显著(P <0.05)。极差分析结果一致。最终发酵培养基确定为(g/L):葡萄糖45、蛋白胨18、玉米浆10、酵母抽提物6、磷酸氢二钾1、硫酸镁0.5、硫酸铁0.1、硫酸锌0.08、氯化钴0.1、硫酸锰0.1,初始pH值为6.0。
2.4 10 L生物反应器发酵验证
以葡萄糖质量浓度70 g/L其他组分与优化后发酵培养基相同,分别进行DLZ15、PA8 10 L发酵罐丙酸发酵实验,结果如图7所示。突变株DLZ15发酵150 h产丙酸达到(42.49±1.56) g/L,残葡萄糖降低到1 g/L以下,出发菌株PA8发酵至192 h,残糖降低到1 g/L以下,最终产丙酸仅为(38.37±0.36) g/L。DLZ15菌株发酵丙酸产量比出发菌株PA8提高10.74%,同时发酵时间缩短42 h,其发酵强度达到0.297 g/(L·h),而PA8菌株发酵强度仅为为0.200 g/(L·h),突变株较出发菌株提高48.5%。同时,突变株DLZ15发酵丙酸纯度为86.05%,较PA8(80.14%)提高了5.91%;其中琥珀酸占比基本一致(10.36%、10.21%),而DLZ15发酵中,乙酸的生成较少,相对提高了丙酸纯度,推测在突变株中代谢流发生改变。
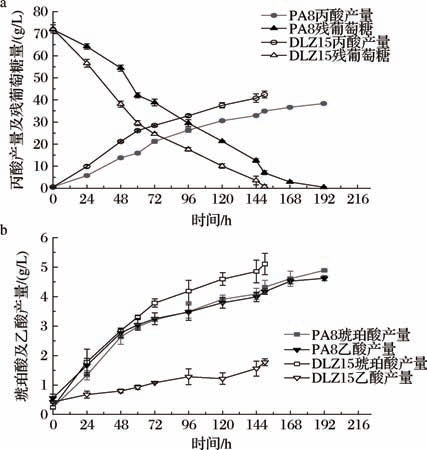
图7 两株菌10 L发酵罐发酵情况对比
Fig.7 Comparison of fermentation performance of two strains in a 10 L fermenter
a-丙酸生成及碳源消耗情况;b-副产物生成情况
通过此发酵罐验证实验,说明经复合诱变和产酸透明圈筛选后,显著增加产酸丙酸杆菌的发酵丙酸速度和葡萄糖转化丙酸的能力。由于丙酸发酵属于产物抑制性发酵过程,同时,产丙酸代谢为厌氧过程,所以发酵周期较长,使丙酸发酵过程电耗较高,设备周转期太长,缩短丙酸发酵是其工业化的瓶颈。该突变菌株显著缩短发酵周期,提高丙酸发酵强度,增加丙酸纯度,具有较好的工业生产价值。
3 结论
本论文针对产酸丙酸杆菌发酵丙酸周期长,丙酸生产率低等问题,通过微波-超声复合诱变叠加ARTP诱变,经透明圈法筛选和血清瓶发酵验证后得到产酸丙酸杆菌突变株DLZ15,该菌株实验室丙酸产量较出发菌株提高了31.20%,丙酸占比较出发菌株提高了8.6%,传代实验证明其具有遗传稳定性较高的特性。
本论文以高产丙酸突变菌株DLZ15为研究对象,对其发酵培养基中氮源和金属离子进行了优化,最终确定了最优培养基配方为(g/L):葡萄糖45、蛋白胨18、玉米浆10、酵母抽提物6、磷酸氢二钾1、硫酸镁0.5、硫酸铁0.1、硫酸锌0.08、氯化钴0.1、硫酸锰0.1,初始pH值为6.0。以此发酵培养基,分别进行突变株DLZ15与出发菌株PA8的10 L发酵丙酸实验,结果表明突变株DLZ15于150 h时丙酸产量为(42.49±1.56) g/L,发酵周期缩短了42 h,发酵强度达到0.297 g/(L·h)。比出发菌株PA8提高48.5%。而本论文诱变筛选的高产菌株DLZ15在丙酸生产性能方面展现出显著优势,具备良好的工业应用潜力。
[1]ZIDWICK M J,CHEN J S,ROGERS P.Organic acid and solvent production: Propionic and butyric acids and ethanol[J].The Prokaryotes.Berlin,Heidelberg: Springer,2013:135-167.
[2]TUNGKIJANANSIN N,ALAHMAD W,NHUJAK T,et al.Simultaneous determination of benzoic acid,sorbic acid,and propionic acid in fermented food by headspace solid-phase microextraction followed by GC-FID[J].Food Chemistry,2020,329:127161.
[3]ABDEL-AZEEM A M,ABO NOUH F A,GEZAF S A,et al.Propionic Acid Chemistry and Production[M].Valorization of Biomass to Bioproducts.Amsterdam: Elsevier,2023:3-15.
[4]BARBIRATO F,CHEDAILLE D,BORIES A.Propionic acid fermentation from glycerol: Comparison with conventional substrates[J].Applied Microbiology and Biotechnology,1997,47(4):441-446.
[5]BOYAVAL P,CORRE C.Production of propionic acid[J].Le Lait,1995,75(4-5):453-461.
[6]JIN Z,YANG S T.Extractive fermentation for enhanced propionic acid production from lactose by Propionibacterium acidipropionici[J].Biotechnology Progress,1998,14(3):457-465.
[7]WOOD H G.Metabolic cycles in the fermentation by propionic acid bacteria[J].Current Topics in Cellular Regulation,1981,18:255-287.
[8]LIU Y,ZHANG Y G,ZHANG R B,et al.Glycerol/glucose co-fermentation: One more proficient process to produce propionic acid by Propionibacterium acidipropionici[J].Current Microbiology,2011,62(1):152-158.
[9]YANG H,WANG Z Q,LIN M,et al.Propionic acid production from soy molasses by Propionibacterium acidipropionici: Fermentation kinetics and economic analysis[J].Bioresource Technology,2018,250:1-9.
[10]马永良.产酸丙酸杆菌FS1171丙酸发酵优化[D].福州: 福建师范大学,2017.MA Y L.Fermentation optimization of propionic acid production by Propionibacterium acidipropionici FS1171 [D].Fuzhou: Fujian Normal University,2017.
[11]诸葛鑫.代谢工程改造詹氏丙酸杆菌和过程优化提高丙酸产量[D].无锡: 江南大学,2014.ZHUGE X.Metabolic engineering of Propionibacterium jensenii and process optimization for enhanced propionic acid production[D].Wuxi: Jiangnan University,2014.
[12]HOFFMAM Z B,SOARES L B,DE MORAIS E R,et al.Evolutionary engineering and chemical mutagenesis of Propionibacterium acidipropionici for improved propionic acid production from sugarcane-derived saccharides[J].Process Biochemistry,2023,130:584-594.
[13]KAGLIWAL L D,SURVASE S A,SINGHAL R S,et al.Wheat flour based propionic acid fermentation: An economic approach[J].Bioresource Technology,2013,129:694-699.
[14]QUESADA-CHANTO A,DA COSTA J P C L,SILVEIRA M M,et al.Influence of different vitamin-nitrogen sources on cell growth and propionic acid production from sucrose by Propionibacterium shermanii[J].Acta Biotechnologica,1998,18(3):267-274.
[15]DERMAN Ü C,ERDEM A,ALEMDAR F,et al.Kinetics of fermentative production of propionic acid on a range of carbon and nitrogen sources using Acidipropionibacterium acidipropionici [ J].Food Bioscience,2024,57:103507.
[16]GUAN N Z,LI J H,SHIN H D,et al.Metabolic engineering of acid resistance elements to improve acid resistance and propionic acid production of Propionibacterium jensenii[J].Biotechnology and Bioengineering,2016,113(6):1294-1304.
[17]LIU L,ZHUGE X,SHIN H D,et al.Improved production of propionic acid in Propionibacterium jensenii via combinational overexpression of glycerol dehydrogenase and malate dehydrogenase from Klebsiella pneumoniae[J].Applied and Environmental Microbiology,2015,81(7):2256-2264.
[18]朱建茹,朱娜,刘丽华,等.诱变筛选Vc二步伴生菌[J].煤炭与化工,2024,47(4):149-152.ZHU J R,ZHU N,LIU L H,et al.Mutagenesis screening Vc twostep companion bacteria[J].Coal and Chemical Industry,2024,47(4):149-152.
[19]高紫君,毕付提,蒋水星,等.曲酸高产菌的复合诱变选育[J].食品研究与开发,2021,42(2):186-190.GAO Z J,BI F T,JIANG S X,et al.Compound mutagenesis of strain with high yield of kojic acid[J].Food Research and Development,2021,42(2):186-190.
[20]周旭波,陈瑜琦,丁鼎,等.常压室温等离子诱变选育L-色氨酸高产菌株[J].食品与发酵工业,2022,48(3):44-49.ZHOU X B,CHEN Y Q,DING D,et al.Breeding of L-tryptophan high-yield strain by ARTP mutagenesis[J].Food and Fermentation Industries,2022,48(3):44-49.
[21]杨海朋,王自强,王云山,等.丙酸发酵过程中四种有机酸快速、简便的分析方法[J].中国酿造,2016,35(5):107-110.YANG H P,WANG Z Q,WANG Y S,et al.Fast and convenient determination method of four organic acids during propionic acid fermentation[J].China Brewing,2016,35(5):107-110.
[22]SUWANNAKHAM S,HUANG Y,YANG S T.Construction and characterization of ack knock-out mutants of Propionibacterium acidipropionici for enhanced propionic acid fermentation[J].Biotechnology and Bioengineering,2006,94(2):383-395.
[23]GHOSH S,ORMAN M A.Exploring the links between SOS response,mutagenesis,and resistance during the recovery period[J].Antimicrobial Agents and Chemotherapy,2024,68(5):e01462-e01423.
[24]GAO B,LIANG L,SU L,et al.Structural basis for regulation of SOS response in bacteria[J].PNAS,2023,120(2): e2217493120.
[25]DISHISHA T,IBRAHIM M H A,CAVERO V H,et al.Improved propionic acid production from glycerol: Combining cyclic batchand sequential batch fermentations with optimal nutrient composition[J].Bioresource Technology,2015,176:80-87.