酿酒酵母(Saccharomyces cerevisiae)是食品发酵工业的核心菌种,良好的发酵性能直接决定着酒类产品的品质与产量[1];其优良的发酵效率和遗传稳定性,使其成为葡萄酒、啤酒等酒精饮品生产的关键微生物[2]。然而,传统菌株在极端环境条件下的胁迫性、原料利用率及风味物质合成能力较差,无法满足生产需求。随着原生质体融合技术的出现,为酿酒酵母遗传性能的优化提供了革命性的解决方案[3]。
原生质体融合技术通过去除细胞壁形成原生质体,利用高温灭活或者紫外灭活,并在促融剂作用下实现跨物种遗传物质重组[4-6];相较于传统诱变育种,其优势显著:可突破生殖隔离,实现不同物种优势性状的精准组合;通过多轮融合策略,构建具有复杂代谢网络的工程菌株,并显著缩短育种周期[7-8]。
许多研究已充分展示了原生质体融合技术在提升酵母菌株性能方面的显著成效。例如,XIN等[9]通过原生质体融合技术将酿酒酵母菌株L与发酵菌株Q融合,成功获得融合子Q/L-f 2,其乙醇耐受体积分数达14%,较亲本菌株Q的耐受阈值(10%)提升40%,彰显了原生质体技术形成的融合子对极端发酵环境中的强适应性及遗传稳定性。此外,还有运用原生质体融合技术成功选育出的耐酸絮凝性酿酒酵母,该菌株在30 ℃及35 ℃、pH值为2.2条件下能高效发酵葡萄糖产乙醇,且糖消耗速率和基于糖消耗的乙醇收率相比亲本菌株显著提高,表明原生质体融合技术也是快速获取耐酸絮凝性酿酒酵母的有效途径[10]。JETTI等[11]利用原生质体融合技术将酿酒酵母与树干毕赤酵母进行杂交,成功培育出SP2-18杂交菌株,其底物利用率、酒精产量及耐受性均得到显著提升。同时,WANG等[12]借助原生质体融合技术,成功构建出由酿酒酵母与假丝酵母组成的新型重组融合酵母,该酵母在酿造香气醇厚的低酒精度苹果酒领域展现出可观的应用前景。
基于以上研究背景,本研究拟采用酿酒酵母GY-1(高效发酵)与根霉K1(强糖化能力)为亲本,旨在构建兼具淀粉糖化与乙醇发酵能力的新型融合菌株。通过解析融合子代谢网络重构机制,可为工业菌种设计提供理论依据,推动酿酒行业向高效、低碳、风味可控的现代化方向转型。后续研究将聚焦融合子规模化发酵工艺优化及风味代谢组学解析,为产业应用奠定基础。
1 材料与方法
1.1 材料与试剂
1.1.1 实验材料
马铃薯,红葡萄,呈贡区吴家营农贸市场;酿酒酵母GY-1和根霉K1,由云南师范大学生命科学学院微生物实验室分离并保存;纤维素酶(生物技术级),上海源叶生物科技有限公司;溶菌酶,北京索莱宝科技有限公司;蜗牛酶,北京普西唐生物科技有限公司。
磷酸缓冲液(phosphate buffer,PB):87.7 mL 0.2 mol/L NaH2PO4和12.3 mL 0.2 mol/L Na2HPO4,pH 6.0,121 ℃灭活20 min。
高渗磷酸缓冲液(phosphate buffer saline,PBS):PB加1 mol/L山梨醇。
0.2 %(体积分数)β-巯基乙醇溶液:β-巯基乙醇200 μL,蒸馏水100 mL,0.45 μm有机膜过滤除菌。
原生质体促融剂:现配PBS加35%(质量分数)聚乙二醇6000。
复合酶液:添加蜗牛酶、纤维素酶、溶菌酶1.5%(质量分数)于高渗PBS,0.45 μm有机膜过滤除菌。
1.1.2 培养基
霉菌培养基:蛋白胨5 g,葡萄糖10 g,磷酸二氢钾13 g,硫酸镁0.25 g,溶于1 000 mL超纯水中,自然pH。固体培养基加20 g/L琼脂,121 ℃高压蒸汽灭菌20 min。
YPD培养基:酵母膏10 g,蛋白胨20 g,葡萄糖20 g,溶于1 000 mL超纯水中,自然pH。固体培养基加20 g/L琼脂,121 ℃灭菌20 min。
再生培养基:YPD加0.8 mol/L KCl,0.5 mol/L蔗糖,1 mol/L山梨醇,自然pH,121 ℃灭菌20 min。
1.2 仪器与设备
UV-5100紫外分光光度计,上海元析仪器有限公司;LDZM-60L-I立式高压蒸汽灭菌器,上海申安医疗器械厂;CP1502电子天平,奥豪斯仪器有限公司;CX23LEDRFS1C生物显微镜,仪景通光学科技有限公司;CM2000显微镜相机,凯诺公司;PHS-2C精密酸度计,上海雷磁仪器厂;TGL-16B高速离心机,上海安亭科学仪器厂;SW-CH-1F洁净工作台,苏州安泰空气技术有限公司;ZHWY-111B恒温培养振荡器,上海智城分析仪器制造公司;BWS-20恒温水槽与水浴锅,上海一恒科学仪器有限公司;2W019766阿贝折射仪,上海光学;K5600C超微量分光光度计,北京凯奥科技发展有限公司。
1.3 实验方法
1.3.1 酿酒酵母、根霉生长曲线绘制及耐热性测定
用光密度法(OD600)测定各菌株的生长曲线[13]。取对数生长期酿酒酵母配制细胞浓度为1 ×107 CFU/mL,取0.1 mL;取根霉K1的对数生长期菌丝离心研磨,收集根霉菌丝体0.01 g;放置在60 ℃的水浴锅中水浴保温,取水浴15、20、25、30 min后的菌液涂布,观察其生长情况[14]。
1.3.2 原生质体融合子制备、融合、再生
通过离心收集新鲜培养的酵母细胞和根霉菌丝体,并利用无菌研钵分别对其研磨。以PBS溶解研磨液,各取1 mL上述研磨液,与4 mL复合酶液混匀后,30 ℃恒温水浴酶解2 h,然后60 ℃水浴30 min进行灭活。
将酿酒酵母GY-1与根霉K1的灭活原生质体以1∶1(体积比)等比例振荡混合均匀,4 000 r/min离心5 min,添加0.2% (体积分数)β-巯基乙醇溶液预处理10 min,将沉淀物重新悬浮在原生质体促融剂中,添加0.5 mol/L KCl和10 mmol/L CaCl2,调节pH值为6.5,置于35 ℃水浴40 min,再用高渗PBS离心洗涤3次,并在3 500 r/min离心10 min,收集细胞后重新悬浮在高渗PBS溶液中涂布到高渗再生培养基上,在30 ℃下培养3 d等待融合子出现,以只灭活的不添加原生质体促融剂处理的细胞作为对照[15]。
1.3.3 融合子检出
利用DNA提取试剂盒对亲本及融合子进行DNA粗提取,利用超微量分光光度计对其DNA含量进行定量测定[16],选择符合原生质体融合子条件的细胞做后续实验。
1.3.4 融合子的鉴定及系统发育
利用引物ITS1与ITS4将1.3.3节得到的DNA提取样品进行扩增。将扩增产物进行测序,拼接,形成融合子的碱基序列与GenBank核酸数据库进行相似性比对,MEGA7.0软件进行系统发育树分析。
ITS1:5′-TCCGTAGGTGAACCTGCGG-3′
ITS4:5′-TCCTCCGCTTATTGATATGC-3′
1.3.5 发酵性能测试
将4株杂合子、1株亲本及混菌种子液分别按0.1%(体积分数)的接种量接种于葡萄汁培养基中,在30 ℃、180 r/min条件下摇床培养4 d,随后于30 ℃静置发酵4 d。最后室温放置至连续2 d质量不再发生变化时停止发酵。并对以下含量进行测定:失重、乙醇含量[17]、可溶性总糖[18]、pH值。
1.3.6 碳水化合物活性酶种类对比
通过发酵实验,以乙醇产量为指标筛选产乙醇能力最优的融合子与亲本GY-1及其他融合子进行性能对比。对乙醇产量最高的融合子和亲本菌株进行全基因组测序,采用碳水化合物活性酶数据库(carbohydrate-active enzymes database,CAZy)对编码基因进行功能注释,统计各酶家族的种类与数量并进行差异化分析。
1.3.7 KEGG数据库注释对比
对亲本以及原生质体融合子进行全基因组测序后,使用KEGG数据库进行代谢通路解析,对比二者的代谢通路差异。
2 结果与分析
2.1 生长曲线及耐热性
由图1可知酿酒酵母GY-1在8~16 h为生长对数期,此时细胞内基因表达模式高度一致,特定基因的表达水平稳定,适合用于基因表达分析。根霉K1在OD600处吸光度呈先上升后下降趋势,其原因为在0~14 h时,根霉K1生长旺盛,处于生长对数期;在14~20 h时,根霉繁殖生成大量菌丝,出现结团现象,导致吸光度下降。选择培养12 h时的酿酒酵母和培养12 h的根霉作为原生质体使用材料。
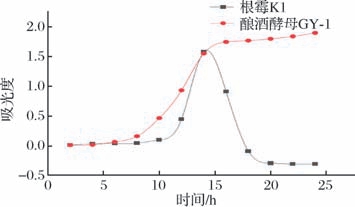
图1 根霉与酵母的生长曲线
Fig.1 Growth curves of Rhizopus and S.cerevisiae
对经酶解制备的对数生长期酵母及根霉原生质体开展灭活分析,由图2-A可知,根霉原生质体在60 ℃下灭活20 min后,已无生长活性。图2-B显示,酿酒酵母在60 ℃灭活20 min后仍有少部分酿酒酵母存活。综上,选择60 ℃ 灭活25 min作为根霉K1原生质体的灭活条件;选择60 ℃灭活30 min,作为酿酒酵母原生质体的灭活条件。
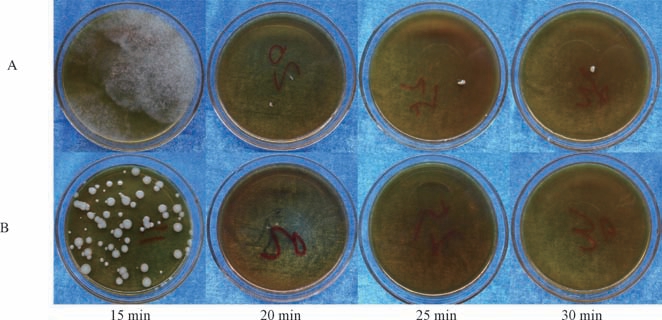
图2 亲本灭活情况分析
Fig.2 Analysis of parental strain inactivation
A-K1灭活情况;B-GY-1灭活情况
2.2 融合子制备
光学显微镜放大400倍对原生质融合子进行观察,如图3-A所示,2个原生质体膜接触、黏连,随后膜结构逐渐模糊,最终形成单一、连续的细胞膜包裹着细胞,表明原生质体融合成功。对原生质体融合子经过三代划线后,其形态已不再发生改变,表型为酵母型态,如图3-B所示。
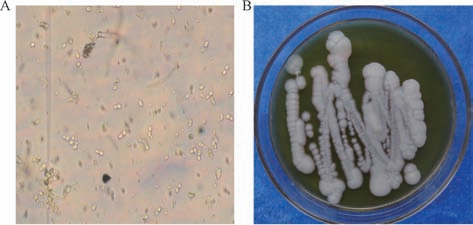
图3 融合子的菌落形态
Fig.3 Colony morphology of fusant
A-400倍镜下原生质体融合子;B-菌落形态
2.3 融合子的检出
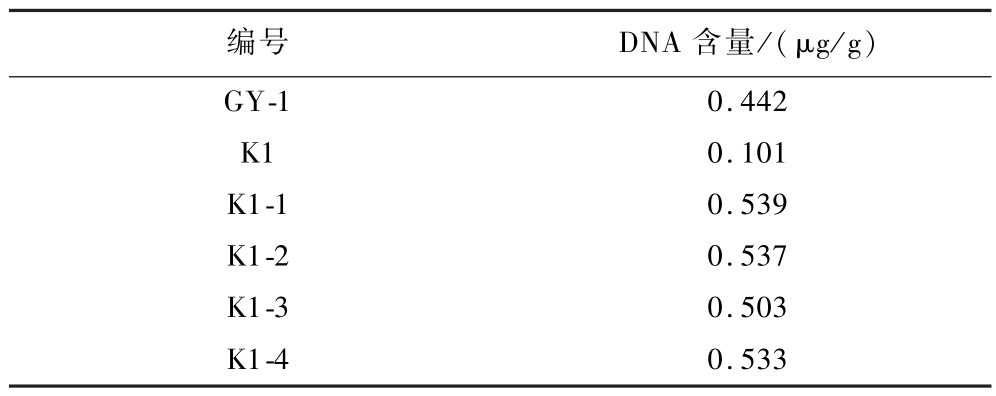
在5个再生培养基中共选择出10株生长旺盛的原生质体融合子,经过2次纯化后获得菌株,提取DNA后对其DNA含量进行定量检测。选取DNA大于任意双亲但是小于双亲DNA含量之和的菌种作为目标菌种[15]。最终结果如表1所示,获得4株原生质体融合子,这些融合子的DNA含量符合原生质体融合子遗传规律。
表1 菌株DNA含量
Table 1 DNA content of strains
2.4 系统发育分析
系统进化树结果如图4所示,系统进化树图清晰地展示了K1-1、K1-2、K1-3、K1-4之间的亲缘关系和进化历程,这4个分支都从一个更高级别的共同节点分出,这意味着它们彼此之间也存在一定的亲缘关系。K1-1、K1-2、K1-3、K1-4四个融合子没有聚在同一个分支上,表明四者之间的基因有一定的差异。通过分析它们在系统进化树中的位置和连接关系,推断出它们之间的进化关系有差异,但有共同的祖先,表明该原生质体融合成功。
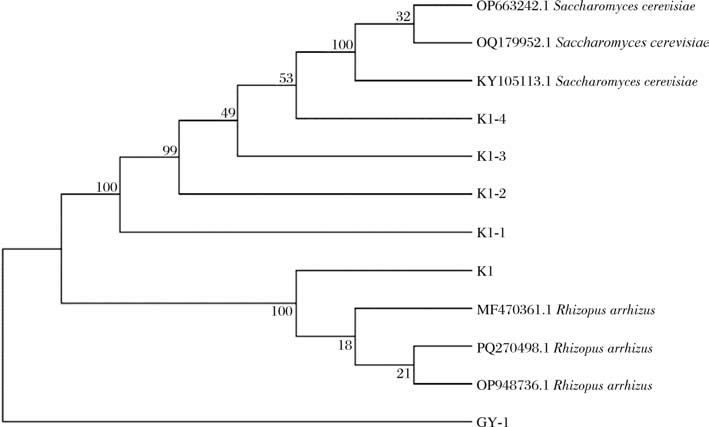
图4 融合子的系统发育树
Fig.4 Phylogenetic tree of fusant
2.5 葡萄酒发酵实验
由于单一菌株根霉K1在葡萄酒发酵中存在不产酒精及葡萄汁利用率低的问题,后续实验未设其为对照,采用发酵瓶失重法(CO2 失重量)评估酒精产量及发酵性能。图5-A显示,相同条件下融合子K1-1、K1-3发酵能力最优(CO2 失重量最大),其次为混合菌株,亲本GY-1最差,表明融合子碳源转化乙醇能力显著优于亲本;图5-B表明,K1-1、K1-2、K1-3乙醇含量较GY-1分别提升15.61%、8.96%、12.36%。低于混合菌但高于单一亲本,推测融合子通过代谢协同作用提高乙醇生成效率;图5-C显示,GY-1发酵液pH值最高(3.49),与其他组差异显著,K1-1、K1-2、K1-3 pH值相近(3.40~3.43),混合菌与K1-4 pH值较低(3.35~3.36);图5-D表明,所有发酵产物均为半干型葡萄酒(残糖5.05~5.9 g/L),K1-1残糖量最高(5.9 g/L)、糖代谢能力弱于混合体系,K1-4残糖量最低(4.8 g/L)、糖分利用效率优于亲本。综上,融合子在乙醇产量和发酵能力上优于单一亲本,K1-1表现最优,后续可通过优化发酵条件或筛选菌株进一步提升其工业应用潜力。
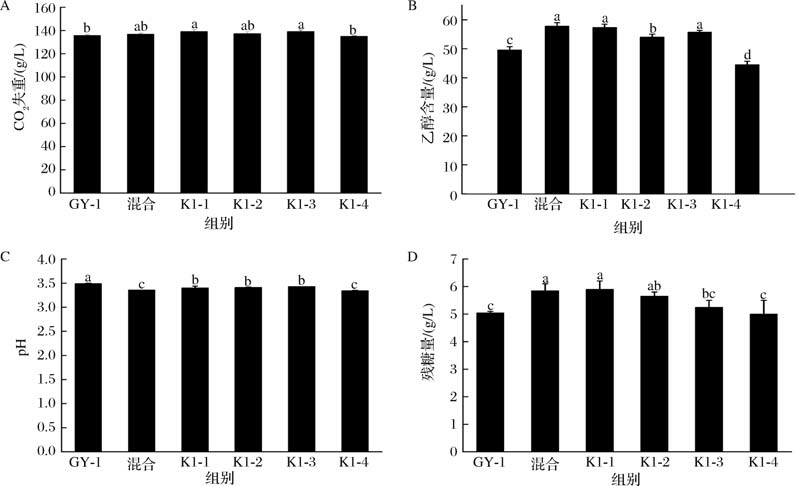
图5 葡萄酒发酵各参数变化分析
Fig.5 Analysis of changes in various parameters during wine fermentation
注:图中不同字母表示差异显著(P <0.05)。
A-CO2 失重;B-乙醇含量;C-pH;D-残糖量
2.6 碳水化合物活性酶种类对比
经过发酵实验筛选,融合子K1-1具有良好的发酵性能,且产乙醇能力比亲本以及其他融合子更强。将亲本以及K1-1菌株进行全基因组测序,进行碳水化合物活性酶种类对比,结果如图6所示。GY-1共有1 019条酶基因,可产生碳水化合物活性酶268种;K1-1有1 045条酶基因,能产生碳水化合物活性酶269种;K1有4 290个酶基因,可产生碳水化合物活性酶有1 105种。GY-1与K1-1在糖苷水解酶类(glycoside hydrolases,GH)、多糖裂解酶类(polysaccharide lyases,PL)、碳水化合物酯酶类(carbohydrate esterases,CE)、辅助活性酶类(auxiliary activities,AA)和碳水化合物结合模块(carbohydrate-binding modules,CBM)在种类上并不存在差异,只有在数量上存在差异;而糖基转移酶类(glycosyltransferases,GT)K1-1比GY-1多一种,为GT76。在K1中也存在糖基转移酶GT76,且只有3个基因可以进行编码。
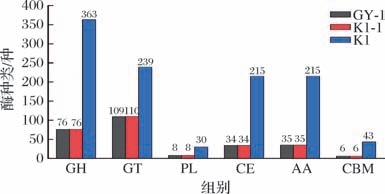
图6 碳水化合物活性酶种类对比
Fig.6 Comparison of carbohydrate-active enzyme types
糖基转移酶与单糖和多糖的生物合成密切相关[19],菌株K1-1相较于亲本GY-1,新增了一种糖基转移酶GT76。糖基转移酶介导的天然产物糖基化是次级代谢产物生物合成中最广泛存在的修饰方式之一,其核心功能是将糖基从一个化合物转移至另一个化合物,催化活化单糖转移并连接到蛋白、核酸、寡糖、脂类和小分子等不同受体分子上,完成后者的糖基化加工。例如甜叶菊来源的二萜糖基转移酶SrUGT76G1,够识别多种二萜及其他小分子化合物,催化生成相应的糖基化产物[20]。糖基转移酶GT76基因的引入不仅扩展了菌株的代谢网络,赋予其执行新糖基化反应的能力,还可能通过糖基化修饰改善抗生素的溶解性、稳定性和生物活性,进而提升抗生素合成潜力;同时,该特征可能增强菌株对渗透压、氧化应激等环境压力的适应性,并优化多糖合成通路以提高胞外多糖产量,拓展其工业应用价值。
GY-1和K1-1在酶系上存在部分重叠,即两者具有部分相同的酶系,但它们所含酶的种类数量有着明显差异。具体而言,GY-1相较于K1-1,多出了AA3、AA3.1、GT41、GT66这4个酶系家族,这些家族总共涉及5个基因;K1-1相较于GY-1,多出了24个酶系家族,包括 CE7、GH13、GH13.1-GH13.40 (其中GH13.1-GH13.40包含GH13.1、GH13.2等17个亚型)、GH33、GH74、GH93、GT53,这些家族涵盖的基因数量多达30个。
GH是水解糖苷键的一类重要酶,包含与淀粉液化、糖化及纤维素降解相关的酶[21]。这些酶系差异深刻影响着菌株的代谢特性:GY-1更多的AA3、AA3.1、GT41与GT66(糖基转移酶系),可能在特定底物的氧化修饰及糖链合成中发挥作用,参与某些特殊次级代谢产物的生成;而K1-1富集的CE7、GH13、GH33等酶系,显著增强了其对多糖、酯类等复杂底物的降解能力。例如,GH13家族广泛参与淀粉液化与糖化[22],使K1-1在淀粉利用上更具优势;GH33家族可水解唾液酸糖苷键,拓展了菌株对特殊糖源的利用范围[23]。这种酶系组成的分化,最终导致两菌株在代谢通路、底物谱及产物合成上的差异,为解析其功能特性与应用潜力提供了关键线索。
K1-1通过GH酶系的数量扩增、GT76的代谢流定向调控及AA3酶的减少,实现了从多糖降解到乙醇合成的全流程优化。这一发现不仅揭示了菌种融合在代谢工程中的潜力,也为工业菌株的理性设计提供了新的靶点。
2.7 KEGG注释结果对比
根据KEGG通路注释结果(图7)发现酿酒酵母GY-1、原生质体融合子K1-1及根霉K1的基因组特征与代谢网络呈现显著差异。亲本菌株中,酿酒酵母GY-1(5 453个基因)的代谢通路基因占比31.6%(1 725个);而丝状真菌根霉K1(8 947个基因)代谢基因富集度高达40.2%(3 595个),凸显其复杂次级代谢潜力。原生质体融合子K1-1的基因总数(5 466个)仅比GY-1多13个,代谢通路基因仅微增1个(1 726个),其余功能基因数量与GY-1高度接近(如遗传信息处理基因941 vs 944),表明异源基因组整合呈现高度选择性。这种非加性整合机制可归因于两方面:第一,根霉作为多核丝状真菌,其复杂染色体结构在融合后因核不兼容性难以稳定保留[24];第二,工业菌株在人工选择压力下倾向于基因组精简,淘汰冗余基因(如与酵母功能重叠的根霉代谢基因),仅保留可能增强胁迫响应或底物利用的关键基因[25]。该结果表明,远缘真菌原生质体融合更易触发基因组排斥与适应性筛选,而非简单的遗传物质叠加。
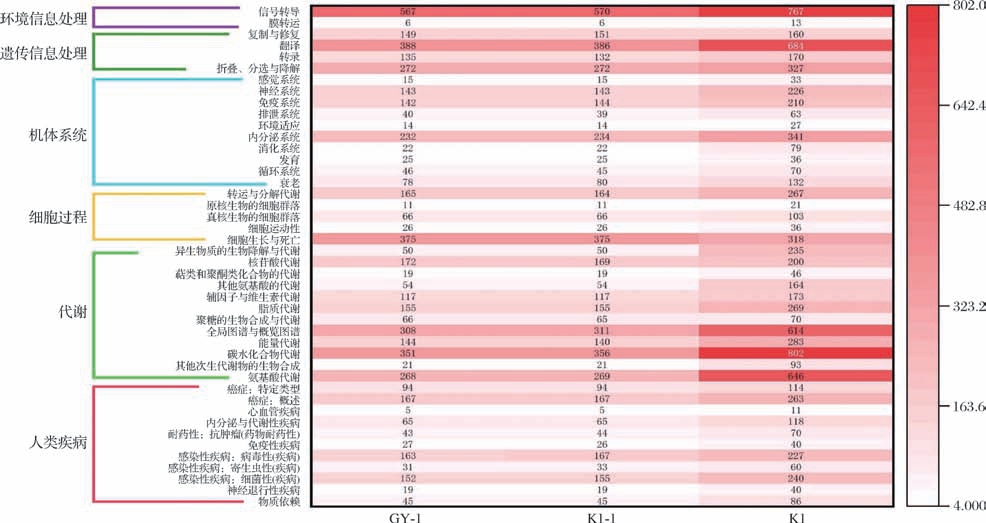
图7 KEGG通路注释对比图
Fig.7 Comparative analysis of KEGG pathway annotations
聚焦酿酒酵母菌株比较,K1-1与GY-1在核心代谢通路中呈现细微差异:碳水化合物代谢通路中,K1-1基因数为356个,较GY-1(351个)增加5个,提示其可能通过提升葡萄糖转运蛋白或糖酵解酶基因表达加速葡萄糖摄取,进而强化乙醇发酵效率,适用于高糖工业发酵场景;能量代谢通路中,K1-1基因数(140个)较GY-1(144个)减少4个,GY-1的能量代谢基因略多,可能在标准培养条件下维持更高基础代谢率,更适合需菌体生物量积累的应用(如单细胞蛋白生产);核苷酸代谢通路中,K1-1基因数(169个)较GY-1(172个)减少3个,但两者DNA/RNA合成关键基因无显著缺失,不影响细胞增殖及遗传稳定性。
GY-1与K1-1有关乙醇代谢相关的通路信息如图8所示。二者差异最大的是氧化磷酸化。根据“巴斯德效应”,高效的氧化磷酸化会抑制低效的乙醇发酵代谢:当氧化磷酸化的基因数量增多时,相应的酶表达量会提升,电子传递链的效率也会随之增强,此时NADH会优先参与氧化磷酸化过程,而非用于乙醇发酵。而GY-1氧化磷酸化的基因数量62个高于K1-1的氧化磷酸化数量58个。综上结果可知K1-1的乙醇产量会高于GY-1。
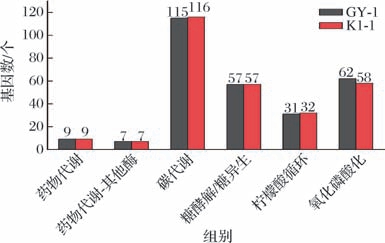
图8 乙醇相关代谢途径基因数量分布对比图
Fig.8 Comparative analysis of gene abundance in ethanol-related metabolic pathways
尽管存在上述差异,两菌株在氨基酸代谢(268/269个基因)、脂质代谢(均为155个基因)、辅酶与维生素代谢(均为117个基因)等基础代谢通路中表现高度保守,表明其核心代谢功能一致,遗传背景具有较强相似性。K1-1的碳水化合物代谢优化使其在高糖环境下的底物消耗速率和乙醇产率更具优势,而GY-1的能量代谢特性则支持其在标准培养条件下的稳定生长。根霉K1的代谢通路基因数显著高于酵母,反映出丝状真菌在次级代谢及复杂物质分解能力上的天然特性,但与酵母的工业应用方向(如单细胞发酵产物)差异显著。
综上,酿酒酵母GY-1与K1-1的代谢通路差异主要体现在碳代谢效率与能量分配策略,可根据发酵目标(如产物类型、环境胁迫)选择适配菌株,两者的代谢保守性则为遗传操作及功能研究提供了稳定基础。根霉K1的代谢复杂性提示其在酶制剂、次级代谢产物合成等领域的应用潜力,但需结合丝状真菌特性开展针对性研究。
3 讨论
尽管本研究已取得了一系列重要成果,但仍有许多问题值得进一步探讨。首先,本研究仅对融合子K1-1进行了初步分析,未来可对其他融合子进行深入研究,以揭示其发酵性能及遗传背景的多样性。其次,本研究虽然发现了糖基转移酶GT 76在K1-1发酵性能提升中起着重要作用,但其具体作用机制仍需进一步阐明。此外,混合发酵体系在本研究中表现出优于单一融合子的发酵性能,这提示未来可探索混合发酵体系中不同菌种间的相互作用机制,以期进一步提高乙醇产量。
最后,随着合成生物学和代谢工程技术的不断发展,未来可尝试通过基因编辑手段对融合子进行定向改造,以进一步优化其发酵性能。
[1]窦帅伟,程思远,余永建,等.朗姆酒发酵中酵母相互作用及其对风味品质影响的研究进展[J].食品科学,2025,46(6):381-391.DOU S W,CHENG S Y,YU Y J,et al.Research progress in yeastyeast interactions and their effect on flavor quality during rum fermentation[J].Food Science,2025,46(6):381-391.
[2]范婷婷,王慕瑶,李俊,等.酵母生物多样性开发及工业应用[J].生物工程学报,2021,37(3):806-815.FAN T T,WANG M Y,LI J,et al.Exploration of yeast biodiversity and development of industrial applications[J].Chinese Journal of Biotechnology,2021,37(3):806-815.
[3]郑贻丹,袁先铃.育种技术在酒用酵母中的应用研究进展[J].中国酿造,2023,42(4):29-34.ZHENG Y D,YUAN X L.Research progress on application of breeding technology in wine yeasts[J].China Brewing,2023,42(4):29-34.
[4]LI N,LU J,WANG Z R,et al.Improving the regeneration rate of deep lethal mutant protoplasts by fusion to promote efficient L-lysine fermentation[J].BMC Biotechnology,2023,23(1):22.
[5]WANG Y L,WANG Y C,CHEN X,et al.Protoplast fusion between Blakeslea trispora 14,271 (+) and 14,272 (-) enhanced the yield of lycopene and β-carotene[J].World Journal of Microbiology and Biotechnology,2021,37(4):58.
[6]WAWRO A.Improvement of acetic acid tolerance in Saccharomyces cerevisiae by novel genome shuffling[J].Applied Biochemistry and Microbiology,2021,57(2):180-188.
[7]罗丽蓉.乳酸菌融合体构建及发酵泡椒性能评价[D].贵州大学,2023.LUO LR.Construction of lactic acid bacteria fusants and evaluation of their performance in fermented pickled peppers[D].Guizhou:Guizhou University,2023.
[8]张子栋,常胜合,董湘熔,等.原生质体融合技术在遗传育种中的应用[J].河南农业科学,2010,39(6):156-159.ZHANG Z D,CHANG S H,DONG X R,et al.Application of protoplast fusion technology in genetic breeding[J].Journal of Henan Agricultural Sciences,2010,39(6):156-159.
[9]XIN Y,YANG M,YIN H,et al.Improvement of ethanol tolerance by inactive protoplast fusion in Saccharomyces cerevisiae[J].BioMed Research International,2020:1979318.
[10]苟敏,杨白雪,汤岳琴,等.利用原生质体融合技术构建耐酸絮凝性产乙醇酿酒酵母[J].生物技术通报,2016,32(11):115-123.GOU M,YANG B X,TANG Y Q,et al.Construction of acid-tolerant and flocculating Saccharomyces cerevisiae strain for ethanol production by protoplast fusion[J].Biotechnology Bulletin,2016,32(11):115-123.
[11]JETTI K D,GNS R R,GARLAPATI D,et al.Improved ethanol productivity and ethanol tolerance through genome shuffling of Saccharomyces cerevisiae and Pichia stipitis[J].International Microbiology,2019,22(2):247-254.
[12]WANG Z L,XU K D,CAI R,et al.Construction of recombinant fusant yeasts for the production of cider with low alcohol and enhanced aroma [ J].European Food Research and Technology,2020,246(4):745-757.
[13]杨昳津,林祥娜,夏永军,等.不同营养添加物对黄酒酵母的乙醇耐受及发酵性能的影响[J].食品与发酵工业,2018,44(1):37-43.YANG Y J,LIN X N,XIA Y J,et al.Effects of different nutrition additives on ethanol tolerance and fermentation performance of Chinese rice wine yeast[J].Food and Fermentation Industries,2018,44(1):37-43.
[14]张亚萌,王金晶,钮成拓,等.基因组重排选育优良发酵性能的高浓酿造啤酒酵母[J].食品与发酵工业,2023,49(19):97-104.ZHANG Y M,WANG J J,NIU C T,et al.Breeding brewing yeast with improved fermentation performance in high-gravity beer fermentation by genome shuffling[J].Food and Fermentation Industries,2023,49(19):97-104.
[15]徐奎栋.原生质体融合选育低醇增香苹果酒酵母[D].陕西:西北农林科技大学,2017.XU KD.Constructing hybrid yeasts through protoplast fusion for lowering ethanol and enhancing aroma[D].Shanxi:Northwest A&F University,2017.
[16]林路成,徐志伟,张建泽,等.原生质体融合结合基因编辑技术显著提高酿酒酵母2-苯乙醇产量[J].食品与发酵工业,2023,49(5):18-24.LIN L C,XU Z W,ZHANG J Z,et al.Protoplast fusion combined with gene editing technology significantly improves the ability of Saccharomyces cerevisiae to produce 2-phenylethanol[J].Food and Fermentation Industries,2023,49(5):18-24.
[17]刘忠义,欧昌荣,汤海青,等.3,5-二硝基水杨酸法测定葡萄酒中总糖含量的条件优化[J].核农学报,2013,27(11):1717-1723.LIU Z Y,OU C R,TANG H Q,et al.Optimization of conditions for determination of total sugar contents in wine by 3,5-dinitrosalicylic acid method[J].Journal of Nuclear Agricultural Sciences,2013,27(11):1717-1723.
[18]杨柳,钱京都,杨金雨,等.葡萄酒酿造过程CO2 的生成规律及回收探究[J].中国酿造,2024,43(8):209-217.YANG L,QIAN J D,YANG J Y,et al.CO2 generation and recovery in wine brewing process[J].China Brewing,2024,43(8):209-217.
[19]KIM J H,AN H J,GARRIDO D,et al.Proteomic analysis of Bifidobacterium longum subsp.infantis reveals the metabolic insight on consumption of prebiotics and host glycans[J].PLoS One,2013,8(2):e57535.
[20]LIU Z F,LI J X,SUN Y W,et al.Structural insights into the catalytic mechanism of a plant diterpene glycosyltransferase SrUGT76G1[J].Plant Communications,2020,1(1):100004.
[21]GRAEBIN N G,DA N SCHÖFFER J,DE ANDRADES D,et al.Immobilization of glycoside hydrolase families GH1,GH13,and GH70:State of the art and perspectives[J].Molecules,2016,21(8):1074.
[22]段绪果,吴敬.微生物GH13家族淀粉脱支酶研究进展[J].微生物学报,2013,53(7):648-656.DUAN X G,WU J.Advances in studying microbial GH13 starch debranching enzyme-a review [J].Acta Microbiologica Sinica,2013,53(7):648-656.
[23]CAO X T,YANG X,XIAO M,et al.Molecular dynamics simulations reveal the conformational transition of GH33 sialidases[J].International Journal of Molecular Sciences,2023,24(7):6830.
[24]COVO S.Genomic instability in fungal plant pathogens[J].Genes,2020,11(4):421.
[25]STEENSELS J,SNOEK T,MEERSMAN E,et al.Improving industrial yeast strains:Exploiting natural and artificial diversity[J].FEMS Microbiology Reviews,2014,38(5):947-995.