高温大曲作为酱香型白酒酿造的糖化剂、发酵剂及生香剂[1],提供水解酶、功能微生物及风味前体物质[2],在白酒酿造中,酱香型白酒所用曲量最多(曲粮比约1∶1),高温大曲质量直接影响酱香型白酒独特风味形成和品质提升[3]。目前,大部分企业依靠感官评价(外观、断面与香气等)将高温大曲分级(如特级、优级和一级),但不同等级大曲品质差异的物质基础和形成机制尚不清晰,限制了对大曲品质的深入理解。因此,深入剖析不同等级高温大曲的代谢物特性及理化、酶活性质,对大曲品质评价和改进具有重要意义。
当前众多研究聚焦于不同等级大曲的微生物组成及挥发性风味化合物探索。微生物研究表明,优质大曲细菌、酵母菌、特定微生物丰度均较高[4],对大曲品质形成有一定影响。王高伟等[5]通过对挥发性化合物分析,揭示高等级大曲中含有较多的吡嗪类(2,3-二甲基吡嗪等)、酚类(愈创木酚等)等特征香气成分;TANG等[3]进一步发现优质大曲富含酸类(乙酸、丙酸等)、酯类(丙酸乙酯等)、醛酮类(苯乙醛等)、醇类(苯乙醇等)等。然而,极少研究关注到不同等级高温大曲的不挥发性化合物(糖、糖醇、氨基酸、有机酸等),其作为微生物生长营养源和挥发性风味物质前体[6],是大曲质量形成的重要物质基础。氨基酸既是微生物代谢的氮源,亦是高级醇和吡嗪类的重要前体——苏氨酸促进吡嗪类物质的产生,亮氨酸、苯丙氨酸分别作为异戊醇、2-苯乙醇的前体[7]。此外,氨基酸在大曲形成过程贡献呈味特性,并参与调控大曲香型[8]与色泽[9]。糖类可以与氨基酸在高温下发生美拉德反应,产生大曲特征香气化合物[8]。乳酸、柠檬酸等有机酸则是大曲及白酒中酯类香气成分的前体物质[10]。因此,分析不同等级高温大曲的不挥发性化合物差异,对于深入理解经验分级背后的科学本质具有重要意义。目前,常用核磁共振[11]、超高效液相色谱[7]、液相色谱-质谱[9]、GC-MS[8]检测大曲的不挥发性化合物,其中衍生化-GC-MS技术表现出独特优势,通过化学衍生化(如硅烷化、烷基化、酰基化等)处理,可有效提高极性不挥发化合物的挥发性和热稳定性,实现对低丰度代谢物的精确定量[12],为全面解析大曲中不挥发性化合物组成提供了技术支撑。典型衍生化策略包括:N,O-双三甲基硅烷三氟乙酰胺(N,O-bistrimethylsilyltrifluoroacetamide, BSTFA)衍生糖类,N-甲基-N-叔丁基二甲基硅烷三氟乙酰胺(N-methyl-N-tert-butyldimethylsilyltrifluoroacetamide, MTBSTFA)衍生有机酸等。
本研究以不同等级高温大曲(特级、优级、一级)为研究对象,在分析其理化性质和酶活力特性基础上,采用化学衍生化-GC-MS技术表征和定量不挥发性化合物谱,通过化学计量学工具筛选不同等级高温大曲关键差异化合物,旨在从多角度揭示不同等级大曲的品质差异特征,为进一步控制和提高高温大曲的品质提供了理论依据。
1 材料与方法
1.1 材料与试剂
样品:特级、优级和一级酱香型高温大曲来自贵州某酱香型酒厂。
不同等级大曲样品评定:大曲的等级由10位具备丰富经验的员工从外观、断面和曲香等方面进行评定[4]。
取样方法:经评定后获得了特级(P1-P3)、优级(S1-S3)和一级(N1-N3)这3个等级高温大曲样品。4 ℃冰箱存放测理化性质样品,测不挥发性化合物样品置于-80 ℃冰箱存放,每个样品做3次平行分析。
C6~C30 正构烷烃以及用于定性及定量的标准品均为色谱纯,焦谷氨酸、脯氨酸、丙氨酸、亮氨酸、缬氨酸、苏氨酸、苯丙氨酸、谷氨酸、酪氨酸、异亮氨酸、丝氨酸、天冬氨酸、谷氨酰胺、色氨酸、天冬酰胺、赖氨酸、高丝氨酸、甘氨酸、组氨酸、2-氨基丁酸、半胱氨酸、5-氨基戊酸、乳酸、葡糖酸、甘油酸、尿酸、乳清酸、苯乙酸、羟基丙酸、柠檬酸、丙二酸、棕榈酸、富马酸、琥珀酸、苹果酸、油酸、肉豆蔻酸、羟基乙酸、亚油酸、3-羟基-3-甲基丁二酸、草酸、2-羟基-3甲基丁酸、酒石酸、硬脂酸、哌啶酸、2-糠酸、衣康酸、亚氨基二乙酸、3-苯基乳酸、戊二酸、2-羟基异己酸、曲酸、2-羟基丁酸、葡萄糖、果糖、木糖、阿拉伯糖、核糖、半乳糖、蔗糖、海藻糖、麦芽糖、龙胆二糖、纤维二糖、蜜二糖、乳糖、甘露糖醇、核糖醇、阿拉伯糖醇、赤藓糖醇、肌肌醇、木糖醇、苏糖醇、半乳糖醇、山梨糖醇、鲨肌醇、磷酸、硼酸、甘油、葡糖酸内酯、2,3-丁二醇、乙二醇、阿拉伯糖酸内酯、木糖酸内酯、甘油醛、3-羟基吡啶、次黄嘌呤、乙醇胺、乙腈、吡啶、DL-正亮氨酸(内标1)、水杨苷(内标2)、BSTFA及MTBSTFA,Sigma-Aldrich公司;葡糖胺,麦克林公司;鲨肌醇、鸟氨酸氨酸,阿拉丁公司;甲硫氨酸、山梨酸、甲基丁二酸、2-羟基苯乙酸、尿素,TCI公司;浓盐酸,中国医药集团有限公司;超纯水采用Milli-Q纯化系统制备。
1.2 仪器与设备
7890A-5975C型GC-MS,美国安捷伦公司;粉碎机,上海塞耐机械进出口有限公司;氮吹仪,上海安谱实验科技股份有限公司;Milli-Q 超纯水系统,河北碧思源恒通水处理工程有限公司;超声波清洗仪,深圳市洁盟清洗设备有限公司;高速冷冻离心机,长沙维尔康湘鹰离心机有限公司;电热鼓风干燥箱,上海博讯实业有限公司医疗设备厂。
1.3 实验方法
1.3.1 理化及酶活力分析
大曲理化(水分、酸度、淀粉含量、氨基氮含量)参照QB/T 4257—2011《酿酒大曲通用分析方法》进行分析;蛋白含量采用凯氏定氮法测定;酸性蛋白酶、中性蛋白酶、糖化酶、液化酶活力均采用试剂盒(如电子版增强出版附表1所示,https://doi.org/10.13995/j.cnki.11-1802/ts.044122,下同)测定。
表1 不同等级高温大曲的理化和酶活力特性比较
Table 1 Comparison of physicochemical and enzymatic activity properties of high-temperature Daqu of different grades
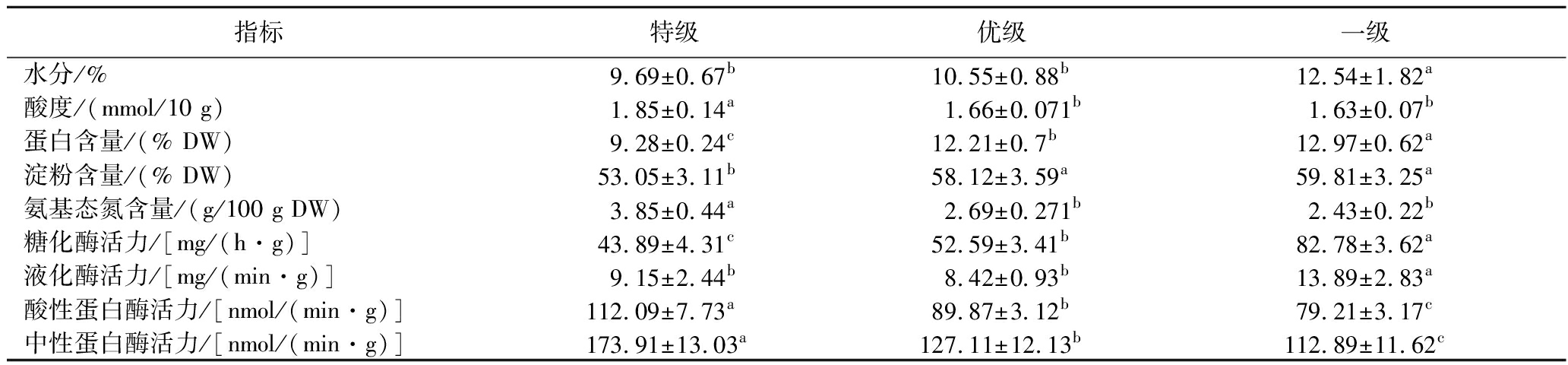
指标特级优级一级水分/%9.69±0.67b10.55±0.88b12.54±1.82a酸度/(mmol/10 g)1.85±0.14a1.66±0.071b1.63±0.07b蛋白含量/(% DW)9.28±0.24c12.21±0.7b12.97±0.62a淀粉含量/(% DW)53.05±3.11b58.12±3.59a59.81±3.25a氨基态氮含量/(g/100 g DW)3.85±0.44a2.69±0.271b2.43±0.22b糖化酶活力/[mg/(h·g)]43.89±4.31c52.59±3.41b82.78±3.62a液化酶活力/[mg/(min·g)]9.15±2.44b8.42±0.93b13.89±2.83a酸性蛋白酶活力/[nmol/(min·g)]112.09±7.73a89.87±3.12b79.21±3.17c中性蛋白酶活力/[nmol/(min·g)]173.91±13.03a127.11±12.13b112.89±11.62c
注:同行不同小写字母表示差异显著(P<0.05)。
1.3.2 上清液制备
参考并改进石亚林等[8]的方法,取5 g高温大曲样品于100 mL棕色瓶中,用25 mL 0.1 mol/L HCl溶液溶解,冰浴超声1 h,定性滤纸过滤。用0.1 mol/L HCl溶液洗涤至总体积为25 mL。
1.3.3 衍生化
1.3.3.1 有机酸和氨基酸等衍生化
取上述上清液200 μL于1.5 mL离心管中,加入乙腈300 μL,于4 ℃下,10 000 r/min离心5 min,沉淀蛋白。取离心后的上清液100 μL放入2 mL液相色谱瓶中,加入DL-正亮氨酸溶液10 μL(内标,1 000 μg/mL,溶于0.1 mol/L HCl溶液),氮气吹干后将50 μL的MTBSTFA和50 μL的乙腈加入2 mL液相色谱瓶中,混合均匀。然后在100 ℃烘箱中反应1 h,24 h内用GC-MS分析。
1.3.3.2 糖和糖醇等衍生化
取上述上清液100 μL,装在2 mL的液相色谱瓶中,加入100 μL 500 μg/mL的水杨苷(内标),氮气吹干。然后在液相色谱瓶中加入50 μL BSTFA溶液(含质量分数1%的三甲基氯硅烷)和50 μL吡啶。在70 ℃烘箱反应2 h。取1 μL上清液,GC-MS分析。
1.3.4 GC-MS分析
GC条件:HP-5色谱柱(30 m×0.25 mm,0.25 μm);进样口温度:280 ℃;氦气以1 mL/min的流速流动;升温程序为:65 ℃保温2 min,然后以6 ℃/min的速度升温至300 ℃,保温15 min;质谱条件为:EI电离源,电离能70 eV,扫描范围50~650 amu,离子源温度300 ℃。
采用全扫描模式进行检测,依据保留时间和保留指数对化合物进行定性分析。定量分析通过构建标准曲线实现:使用0.1 mol/L HCl溶液配制混合标准溶液,随后进行2倍梯度稀释。各浓度梯度标准溶液的衍生化及分析流程与样品处理程序保持一致。以标准品与内标物的峰面积比值为横坐标,标准品与内标物的质量浓度比值为纵坐标,绝对质量浓度按公式(1)计算:
目标化合物质量浓度![]() 内标质量浓度
内标质量浓度
(1)
1.4 统计学分析
所有实验结果用“平均值±标准差”表示。采用SPSS 20.0进行单因素方差分析,以P<0.05为差异有统计学意义。采用SIMCA 14.0软件进行偏最小二乘判别分析(partial least squares-discriminant analysis,PLS-DA)。使用TBtools 1.082绘制韦恩图。使用Origin 2024和GraphPad prism 9.5.1软件绘制柱状图等。
2 结果与分析
2.1 不同等级高温大曲理化和酶活力差异分析
如表1所示,特级、优级与一级大曲在理化和酶学特性上存在显著差异。特级大曲水分含量最低(9.69%),显著低于一级(12.54%),但均满足白酒酿造所用成熟大曲的水分含量小于13%的标准[9]。在高温高湿环境下,氨基酸和糖等发生美拉德反应,能得到较高质量的低水分大曲[3],而高水分含量的大曲在贮存过程中容易发生霉变,导致曲块的品质下降。同时,特级大曲总酸度(1.85 mmol/10 g)显著高于优级大曲(1.66 mmol/10 g)与一级大曲(1.63 mmol/10 g),与丁芳等[11]研究一致。乳酸菌等产酸微生物分解脂肪、淀粉和蛋白质产生有机酸是导致酸度升高的主要原因[13],而较高的酸度可抑制杂菌生长,并为有益微生物提供生化反应前体及生存条件[10]。特级曲的蛋白质含量最低,氨基态氮含量最高,可能源于其较高的蛋白酶活力加速了蛋白质降解,生成更多氨基酸类前体物质。此外,淀粉是大曲中的主要物质之一,大曲的淀粉含量反映的是其在贮存发酵过程中酶分解淀粉水平,糖化酶和液化酶驱动淀粉转化为葡萄糖。本研究中3个等级大曲中淀粉含量占比为53.05%~59.81%,其中一级大曲淀粉含量显著高于特级,反映微生物对碳源的利用效率低下。研究表明未发酵好的大曲表现出高糖化酶和液化酶活力[14],一级大曲糖化酶和液化酶活力较高可能也指示其发酵不充分,而残留的大量淀粉底物促进贮存期酶的作用[15],呈现显著高于特级的糖化酶、液化酶活力。
2.2 不同等级高温大曲理化和酶活力差异分析
为进一步阐明高温大曲等级异质性,采用衍生化-GC-MS联用技术分析高温大曲中的游离态不挥发性化合物,共鉴定105种化合物,其中97种绝对定量、8种相对定量(表2为不同等级高温大曲重要不挥发化合物定量结果的部分数据,105种不挥发化合物定量结果见附表2),包括25种氨基酸及其衍生物、15种糖类(含1种糖苷)、10种糖醇、37种有机酸、2种无机酸以及16种其他化合物。结果显示,不同等级高温大曲中多数不挥发性化合物的含量存在显著性差异(P<0.05)。其中乳清酸、曲酸、N-乙酰-L-丙氨酸、甘油葡糖苷等18种化合物系首次在酱香型高温大曲中被鉴定(表2)。葡萄糖、木糖、甘露糖醇、核糖醇、赤藓糖醇、焦谷氨酸、脯氨酸、乳酸等20种化合物为不同等级高温大曲共有高含量不挥发化合物(大于1 mg/g)。
表2 不同等级高温大曲重要不挥发化合物定量结果 单位:μg/g
Table 2 Quantitative results of important non-volatile compounds in high-temperature Daqu of different grades
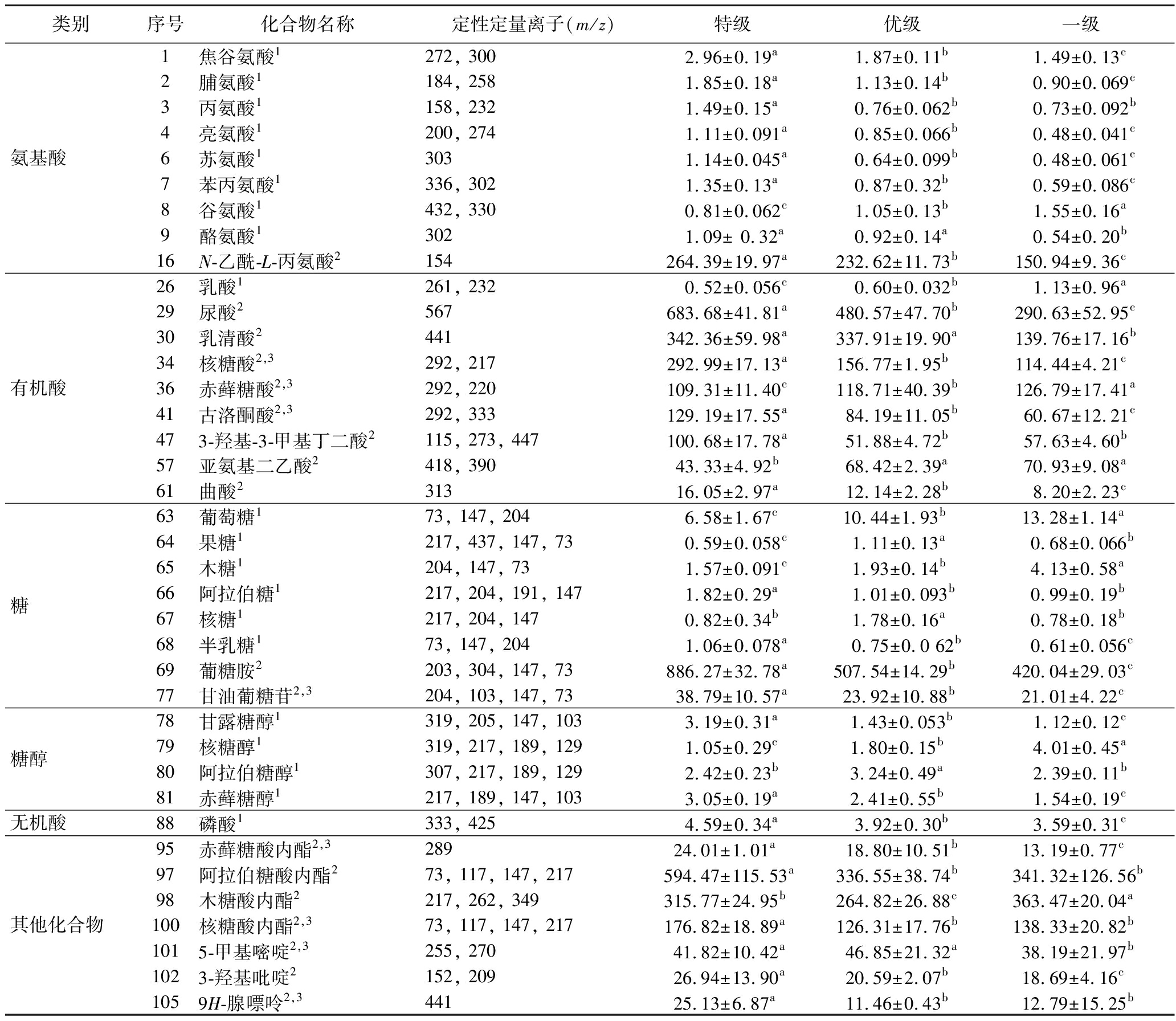
类别序号化合物名称定性定量离子(m/z)特级优级一级氨基酸1焦谷氨酸1272, 3002.96±0.19a1.87±0.11b1.49±0.13c2脯氨酸1184, 2581.85±0.18a1.13±0.14b0.90±0.069c3丙氨酸1158, 2321.49±0.15a0.76±0.062b0.73±0.092b4亮氨酸1200, 2741.11±0.091a0.85±0.066b0.48±0.041c6苏氨酸13031.14±0.045a0.64±0.099b0.48±0.061c7苯丙氨酸1336, 3021.35±0.13a0.87±0.32b0.59±0.086c8谷氨酸1432, 3300.81±0.062c1.05±0.13b1.55±0.16a9酪氨酸13021.09± 0.32a0.92±0.14a0.54±0.20b16N-乙酰-L-丙氨酸2154264.39±19.97a232.62±11.73b150.94±9.36c有机酸26乳酸1261, 232 0.52±0.056c 0.60±0.032b1.13±0.96a29尿酸2567683.68±41.81a480.57±47.70b290.63±52.95c30乳清酸2441342.36±59.98a337.91±19.90a139.76±17.16b34核糖酸2,3292, 217292.99±17.13a156.77±1.95b114.44±4.21c36赤藓糖酸2,3292, 220109.31±11.40c118.71±40.39b126.79±17.41a41古洛酮酸2,3292, 333129.19±17.55a84.19±11.05b60.67±12.21c473-羟基-3-甲基丁二酸2115, 273, 447100.68±17.78a51.88±4.72b57.63±4.60b57亚氨基二乙酸2418, 39043.33±4.92b68.42±2.39a70.93±9.08a61曲酸231316.05±2.97a12.14±2.28b8.20±2.23c糖63葡萄糖173, 147, 2046.58±1.67c10.44±1.93b 13.28±1.14a 64果糖1217, 437, 147, 730.59±0.058c1.11±0.13a0.68±0.066b65木糖1204, 147, 731.57±0.091c1.93±0.14b4.13±0.58a66阿拉伯糖1217, 204, 191, 1471.82±0.29a1.01±0.093b0.99±0.19b67核糖1217, 204, 1470.82±0.34b1.78±0.16a0.78±0.18b68半乳糖173, 147, 2041.06±0.078a0.75±0.0 62b0.61±0.056c69葡糖胺2203, 304, 147, 73886.27±32.78a507.54±14.29b420.04±29.03c77甘油葡糖苷2,3204, 103, 147, 7338.79±10.57a23.92±10.88b21.01±4.22c糖醇78甘露糖醇1319, 205, 147, 1033.19±0.31a1.43±0.053b1.12±0.12c79核糖醇1319, 217, 189, 1291.05±0.29c1.80±0.15b4.01±0.45a80阿拉伯糖醇1307, 217, 189, 1292.42±0.23b3.24±0.49a2.39±0.11b81赤藓糖醇1217, 189, 147, 1033.05±0.19a2.41±0.55b1.54±0.19c无机酸88磷酸1333, 4254.59±0.34a3.92±0.30b3.59±0.31c其他化合物95赤藓糖酸内酯2,328924.01±1.01a 18.80±10.51b13.19±0.77c 97阿拉伯糖酸内酯273, 117, 147, 217594.47±115.53a336.55±38.74b341.32±126.56b98木糖酸内酯2217, 262, 349315.77±24.95b264.82±26.88c363.47±20.04a100核糖酸内酯2,373, 117, 147, 217176.82±18.89a126.31±17.76b138.33±20.82b1015-甲基嘧啶2,3255, 27041.82±10.42a46.85±21.32a38.19±21.97b1023-羟基吡啶2152, 20926.94±13.90a20.59±2.07b18.69±4.16c1059H-腺嘌呤2,344125.13±6.87a11.46±0.43b12.79±15.25b
注:组间不同小写字母表示差异显著(P<0.05);表中化合物右上角数字1表示含量单位为mg/g,数字2表示酱香型高温大曲首次鉴定的化合物,数字3表示相对定量结果;表中数据为“平均值±标准差”(n=9)。
在本研究新鉴定的18种化合物中,尿酸为微生物嘌呤代谢产生的关键有机酸[16];曲酸则能高效抑制酪氨酸酶活力、阻遏黑色素生成[17];乳清酸是嘧啶核糖核苷酸从头生物合成途径的中间产物,具有延缓细胞衰老,促进新陈代谢等功效[18];甘油葡糖苷是由曲霉的α-葡萄糖苷酶催化甘油发生糖基化反应产生,在日本清酒和甜米酒中含量约0.1%~0.5%,与酒曲使用密切相关[19],以上新发现的化合物均在特级大曲含量较高,可能对大曲中品质形成存在一定的影响。
如图1-b所示,氨基酸(19%~28%)、糖类(25%~41%)及糖醇(20%)构成不同等级高温大曲不挥发化合物主体成分,特级大曲的不挥发性成分总量在3个样品中居于首位(图1-a)。其中氨基酸含量在特级中达17.42 (mg/g)(图1-a),含量随等级提升而显著升高(P<0.05),表现为特级>优级>一级,这与丁芳等[11]研究结论一致。特级大曲中焦谷氨酸(2.96 mg/g)、脯氨酸(1.85 mg/g)、丙氨酸(1.49 mg/g)等呈味氨基酸的含量最高,对大曲风味特征形成分别贡献焦香味、苦味和甜味,并对微生物群落的代谢调控具有重要贡献[7]。
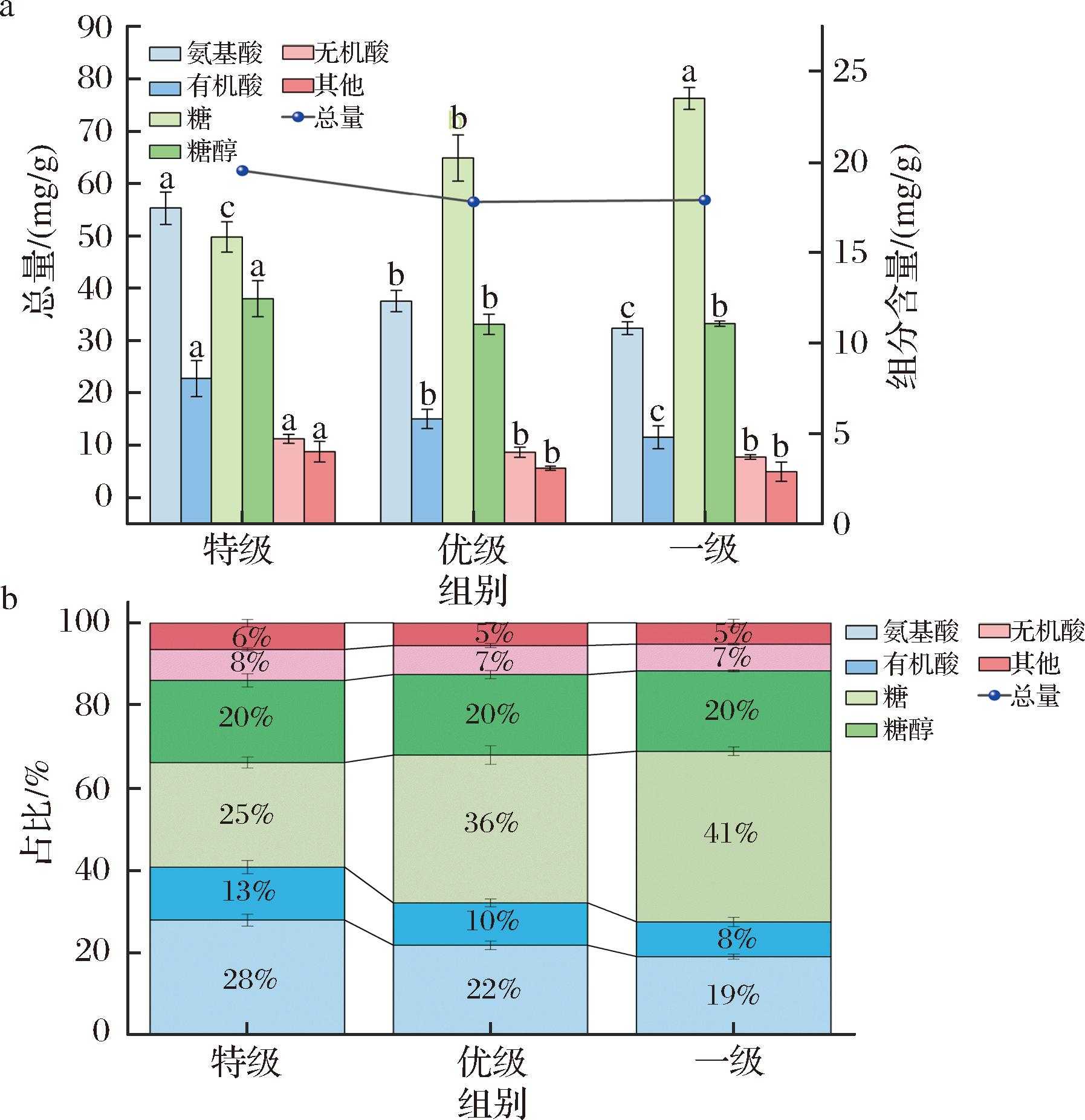
a-含量;b-占比
图1 不同等级高温大曲不挥发性化合物组分比较
Fig.1 Comparison non-volatile compounds of high-temperature Daqu of different grades
注:不同小写字母表示差异显著(P<0.05)。
糖类含量随等级增加而降低(特级<优级<一级),一级大曲的糖类含量最高(23.50 mg/g),葡萄糖(13.28 mg/g)与木糖(4.13 mg/g)含量最高,且其在一级大曲中的含量显著高于特级大曲和优级大曲(表2)。特级大曲中糖醇总含量更高,以甘露糖醇(3.19 mg/g)、阿拉伯糖醇(2.42 mg/g)、赤藓糖醇(3.05 mg/g)构成糖醇主要成分。
有机酸总量较少,占比为8%~13%,在特级和优级的含量显著高于一级大曲,但乳酸作为含量最高的不挥发有机酸,在一级最高(1.13 mg/g)。无机酸仅检出磷酸[特级(4.59 mg/g);各等级均>3 mg/g]和硼酸,目前对无机酸研究极少,仅有石亚林等[8]在大曲中准确定量。
综上,特级大曲以高含量氨基酸、有机酸、糖醇和无机酸为特征,一级大曲则以高糖含量为标志。
2.3 不同等级高温大曲关键差异不挥发性化合物解析
2.3.1 主成分分析
主成分分析表明,105种不挥发性化合物可明显区分特级、优级和一级高温大曲(图2-a),前2个主成分累计解释83.8%差异(PC1=69.8%,PC2=14.0%)。空间分布显示特级与一级大曲分离最远,特级与优级较近(与图2-b聚类结果一致),说明特级和一级组分差异大。此外,如图2-c所示,大多数不挥发性化合物分布集中在特级大曲附近,驱动特级大曲的形成与分布[8];高含量的糖和糖醇驱动一级大曲分布;优级曲样品位于主成分分布中间位置,主要富含少量糖和有机酸。
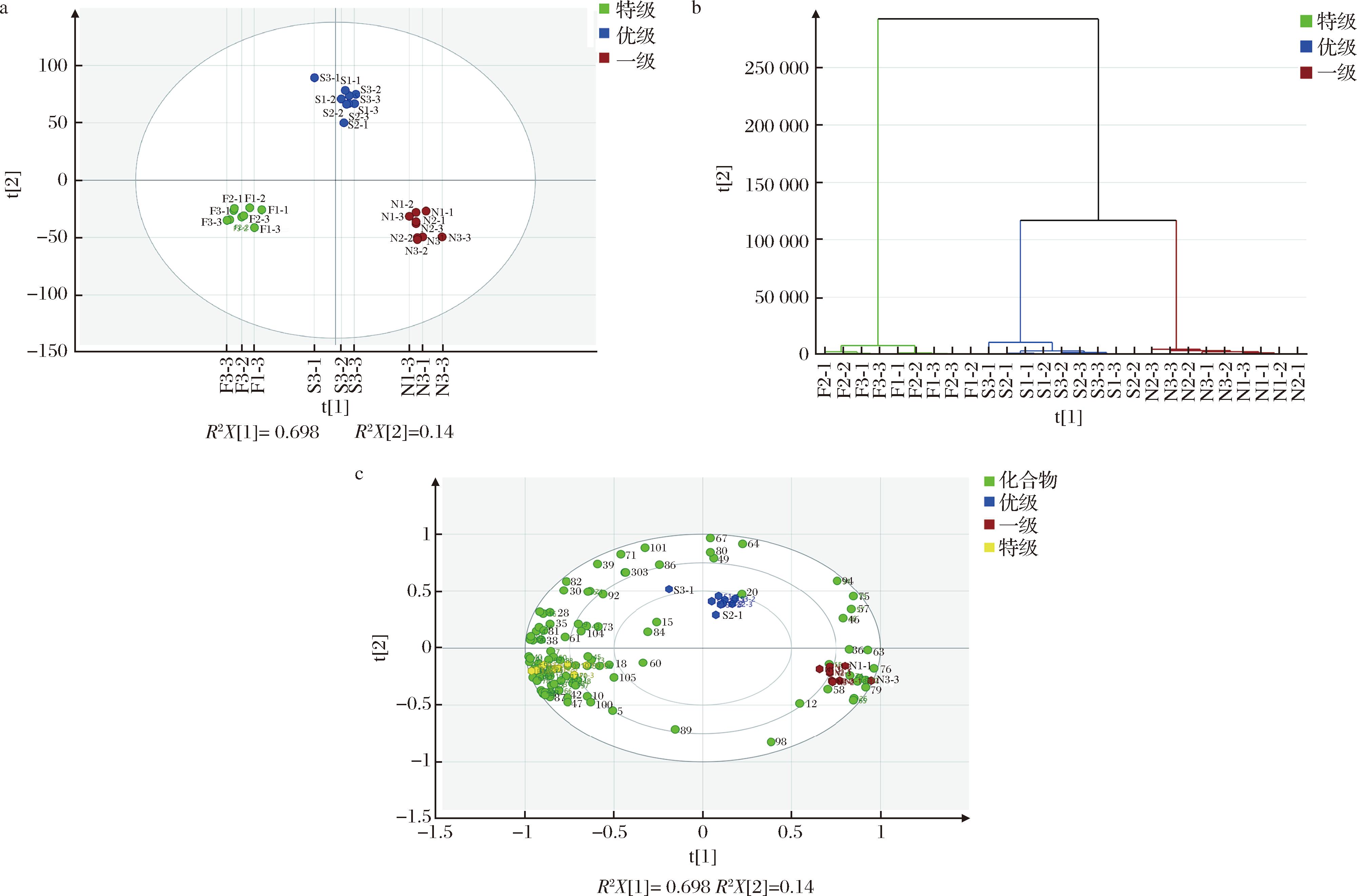
a-主成分分析;b-聚类分析;c-载荷图分析
图2 不同等级高温大曲及105种不挥发性化合物的无监督分析
Fig.2 Unsupervised analysis of high-temperature Daqu of different grades and 105 non-volatile compounds
注:序号1-105对应化合物如电子版增强出版附表2所示。
2.3.2 PLS-DA
基于PLS-DA筛选高温大曲等级分化的关键不挥发性化合物[9](图3-a),模型展现出优异的分级能力(Q2=0.98>0.5),通过置换检验(n=200)进一步验证了模型的可靠性(图3-b)。采用变量投影重要性(variable importance in the projection,VIP>1)、极组间差异倍数|log2FC|≥1和显著性(P<0.05)来识别特级、优级、一级曲的关键不挥发性化合物(生物标志物)[20]。结果表明24种化合物VIP>1(电子版增强出版附图1),49种化合物|log2FC|≥1(电子版增强出版附图2),通过韦恩图筛选出3个等级高温大曲17种关键差异化合物(图3-c)。
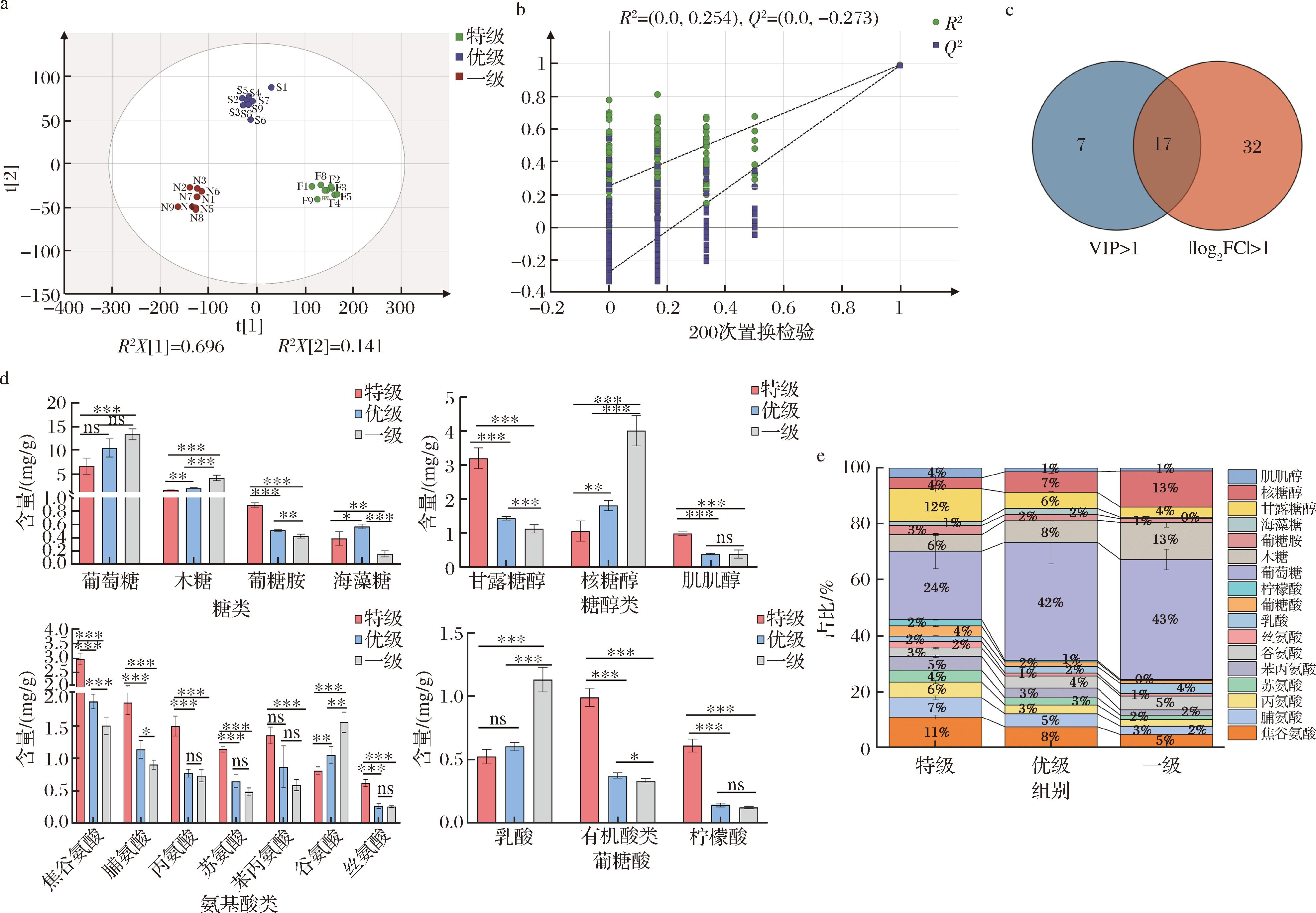
a-PLS-DA图;b-置换检验结果;c-Veen图分析;d-17种关键不挥发性化合物含量显著性分析;e-17种关键不挥发性化合物占比变化分析
图3 基于PLS-DA识别不同等级高温大曲的关键差异化合物
Fig.3 Identification of key compounds for high-temperature Daqu of different grades based on PLS-DA
注:ns表示P>0.05;*表示P<0.05;**表示P<0.01;***表示P<0.001。
糖类中的葡萄糖、木糖、海藻糖、葡糖胺为关键差异化合物,葡萄糖(VIP=4.56,|log2FC|=1.02),在特级曲中其含量显著低于一级(P<0.001,图3-d),一级占比43%,较特级增加19%(图3-e),其作为微生物核心碳源,驱动代谢过程并促进酯类、醛类等风味化合物合成[21]。木糖亦在一级大曲显著积累,其含量高出特级7%(图3-e),可能与制曲原料纤维杂质含量高及微生物利用木糖效率低下相关[22];海藻糖在优级大曲显著高于一级,具有稳定、抗逆等作用[23],可由葡萄糖、麦芽糖等产生。首次定量检出的葡糖胺(在特级中3%)可由果糖与氨和氨基酸反应生成。该物质是食品中颜色、风味和香气的关键前体,可转化形成非挥发性吡嗪(如糖嗪与脱氧果糖嗪,在烤花生和酱油中检测到)[24]。
核糖醇、甘露糖醇和肌肌醇含量在特级与一级大曲间均呈现显著差异(图3-d)。一级大曲中核糖醇显著富集(|log2FC|=1.93),占比13%(图3-e),推测可能由于其脱氢酶活性受阻,限制了向关键前体D-核酮糖的转化[25]。特级大曲中甘露糖醇和肌肌醇含量分别为一级的2.85和2.63倍,分别增加8%和3%(图3-e),这可能源于发酵过程其经历的高渗透压环境诱导耐高渗酵母积累多元醇,以抵御细胞脱水并保护结构完整性[26],此外,糖醇在加热过程中有助于维持大曲色泽稳定[27]。
焦谷氨酸、脯氨酸、丙氨酸、苏氨酸、丝氨酸、苯丙氨酸和谷氨酸为关键差异氨基酸。焦谷氨酸(VIP=1.83)是对分级影响最大的氨基酸,特级曲(11%)中含量显著高于一级(图3-d),有助于高温大曲产生特有的“焦糊香”,可以由谷氨酸转化产生[7]。特级曲中苏氨酸含量显著高于优级和一级(图3-d),研究指出其代谢物2,5-二甲基吡嗪与酱香风味的浓郁度呈正相关[28]。如果食品中谷氨酸的浓度高于约1 mmol/L的味觉阈值,则会赋予鲜味[29]。谷氨酸在一级中含量更高(5%),可能对一级大曲鲜味有一定作用。
有机酸中葡糖酸和柠檬酸的含量在特级大曲显著高于一级(图3-d)。葡糖酸具有抑制杂菌,平衡糖化与发酵效率的作用[30];柠檬酸的高含量表明三羧酸循环在特级大曲可能更加活跃,促进糖和有机酸的分解利用。乳酸可由三羧酸循环代谢或酯化形成乳酸乙酯等香气化合物,使得乳酸在特级曲含量显著低于一级。
综上,不同等级高温大曲的关键不挥发化合物呈现明显的差异化分布:特级大曲的焦谷氨酸、脯氨酸、丙氨酸、苏氨酸、丝氨酸、苯丙氨酸、甘露糖醇、肌肌醇、葡糖酸、柠檬酸、葡糖胺含量显著高于一级,伴随糖类(葡萄糖、木糖)和乳酸的显著降低,反映了高效的生物转化和物质变化,一级大曲则以糖类物质和部分中间代谢物(核糖醇、谷氨酸、乳酸)的积累为主要特征,优级曲含有更多的海藻糖。这17种关键差异化合物的分布特征为理解大曲质量差异提供了代谢物质层面的客观依据。
3 结论与展望
本研究解析了不同等级高温大曲的理化性质与酶活力差异,特级、优级与一级大曲在理化和酶学特性上存在显著差异。基于化学衍生化结合GC-MS技术对特级、优级和一级高温大曲共表征并定量了105种不挥发性化合物,特级大曲不挥发化合物总量最高,氨基酸和糖占比最大。化学计量学分析得到,主成分分析可以实现特级、优级和一级大曲有效区分,进一步通过PLS-DA筛选出特级,优级和一级大曲的17种关键差异不挥发性化合物(生物标志物),特级大曲的焦谷氨酸等11种化合物含量显著高于一级,伴随糖类(葡萄糖、木糖)和乳酸的显著降低,为深入解析不同等级高温大曲的品质差异和提升大曲质量奠定了重要理论基础。本研究为高温大曲品质形成和评价体系的优化提供了重要的理论依据。然而,本研究仍存在若干局限性,主要体现在样本数量相对有限,且对特定非挥发性化合物的具体功能特征尚未进行深入解析。未来研究可进一步探究高温大曲中非挥发性风味物质谱系,结合挥发性成分解析建立基于成分分析为导向的大数据高温大曲分级系统,以完善大曲质量控制与提升。
[1] 范文来, 徐岩.蒸馏酒工艺学[M].北京:中国轻工业出版社, 2023.FAN W L, XU Y.Distilled Spirits Technology[M].Beijing:China Light Industry Press, 2023.
[2] YANG L, FAN W L, XU Y.Qu-omics elucidates the formation and spatio-temporal differentiation mechanism underlying the microecology of high temperature Daqu[J].Food Chemistry, 2024, 438:137988.
[3] TANG P, WANG L Q, ZHAO Q, et al.Characterization of key aroma compounds and relationship between aroma compounds and sensory attributes in different quality of high temperature Daqu[J].LWT, 2024, 194:115801.
[4] WANG X D, BAN S D, QIU S Y.Analysis of the mould microbiome and exogenous enzyme production in Moutai-flavor Daqu[J].Journal of the Institute of Brewing, 2018, 124(1):91-99.
[5] 王高伟, 曹润洁, 陈双, 等.采用顶空固相微萃取结合全二维气相色谱飞行时间质谱解析不同等级中高温大曲的挥发性组分差异特征[J].食品与发酵工业, 2025, 51(2):285-292.WANG G W, CAO R J, CHEN S, et al.Analysis of volatile compounds differences in different grades medium-high temperature Daqu by headspace solid-phase microextraction with comprehensive two-dimensional gas chromatography time-of-flight mass spectrometry[J].Food and Fermentation Industries, 2025, 51(2):285-292.
[6] LUO S, ZHANG Q L, YANG F, et al.Analysis of the formation of sauce-flavored Daqu using non-targeted metabolomics[J].Frontiers in Microbiology, 2022, 13:857966.
[7] 乔敏莎, 王凡, 山其木格, 等.超高效液相色谱质谱法测定酱香型酒曲原料中氨基酸含量[J].食品与发酵工业, 2023, 49(12):278-284.QIAO M S, WANG F, SHAN Q, et al.Direct determination of 19 amino acids in raw materials of Moutai-flavor Jiuqu by ultra performance liquid chromatography-tandem mass spectrometry[J].Food and Fermentation Industries, 2023, 49(12):278-284.
[8] 石亚林, 范文来, 徐岩.不同香型白酒大曲及其发酵过程中游离态糖和糖醇的研究[J].食品与发酵工业, 2016,42(7):188-192.SHI Y L, FAN W L, XU Y. Profiles of free sugars and alditols in Chinese Daqu by silylation coupled with GC-MS[J]. Food and Fermentation Industries, 2016, 42(7):188-192.
[9] YANG L, FAN W L, XU Y.GC×GC-TOF/MS and UPLC-Q-TOF/MS based untargeted metabolomics coupled with physicochemical properties to reveal the characteristics of different type Daqus for making soy sauce aroma and flavor type Baijiu[J].LWT, 2021, 146:111416.
[10] 杨会. 白酒中不挥发呈味有机酸和多羟基化合物研究[D].无锡:江南大学,2017.YANG H.Characterization of non-volatile gustatory organic acids and polyhydroxy compounds in Chinese liquors[D].Wuxi:Jiangnan University, 2017.
[11] 丁芳, 张原頔, 蒋英丽, 等.不同等级高温大曲微生物群落和代谢物的特征分析[J].中国酿造, 2022, 41(11):24-30.DING F, ZHANG Y D, JIANG Y L, et al.Microbial communities and metabolites characteristics of high temperature Daqu with different grades[J].China Brewing, 2022, 41(11):24-30.
[12] 范文来. 白酒及其发酵过程中内源产生的不挥发性有机化合物综述[J].酿酒, 2020, 47(6):4-14.FAN W L.Review of nonvolatile endogenous metabolism in Chinese liquor(Baijiu) and fermentation process[J].Liquor Making, 2020, 47(6):4-14.
[13] ZHANG Z D, RAN X X, GUO Z, et al.Microbial diversity, functional properties, and flavor characteristics of high-temperature Daqu with different colors[J].Food Research International, 2025, 212:116406.
[14] WEI Y H, WEN Z, YAO S J, et al.Tempo-spatial dynamics of physicochemical properties and microbial communities in high-temperature Daqu during the fermentation process[J].Food Chemistry:X, 2025, 29:102815.
[15] 孙海彦. 生淀粉糖化酶高产菌的选育及产酶机理的研究[D].海口:海南大学, 2016.SUN H Y.Breeding of high-yielding raw-starch-digesting-glucoamylase producer and study on its mechanism for producing this enzyme[D].Haikou:Hainan University, 2016.
[16] 李杰, 李霜, 张鹏霞, 等.发酵食品中具有潜在降尿酸功能乳酸菌的筛选及特性分析[J].食品研究与开发, 2024, 45(7):174-180.LI J, LI S, ZHANG P X, et al.Screening and characteristics analysis of lactic acid bacteria with potential function of reducing uric acid from fermented foods[J].Food Research and Development, 2024, 45(7):174-180.
[17] 方婧杰, 陈建, 陈雅娟, 等.曲酸提取工艺优化及其对酪氨酸酶抑制作用的分子机制[J].食品与机械, 2023, 39(12):9-17.FANG J J, CHEN J, CHEN Y J, et al.Optimization of the extraction process and molecular mechanism of inhibition on tyrosinase of kojic acid[J].Food &Machinery, 2023, 39(12):9-17.
[18] 李长庚, 龚雨, 宗媛, 等.B族维生素对大肠杆菌发酵生产乳清酸的影响[J].食品与发酵工业, 2023, 49(13):56-63.LI C G, GONG Y, ZONG Y, et al.Effect of B vitamins on the production of orotic acid by fermentation of Escherichia coli[J].Food and Fermentation Industries, 2023, 49(13):56-63.
[19] LUO Q, DUAN Y K, LU X F.Biological sources, metabolism, and production of glucosylglycerols, a group of natural glucosides of biotechnological interest[J].Biotechnology Advances, 2022, 59:107964.
[20] NIU J L, LI W W, DU B H, et al.Temporal heterogeneity of microbial communities and flavor metabolism during storage of high-temperature Daqu[J].Food Chemistry, 2025, 464:141577.
[21] WEN Z, WEI Y H, HAN D Y, et al.Deciphering the role of traditional flipping Crafts in medium-temperature Daqu fermentation:Microbial succession and metabolic phenotypes[J].Current Research in Food Science, 2025, 10:101063.
[22] 王倩, 高教琪, 周雍进.葡萄糖和木糖高效共利用代谢工程研究进展[J].生物工程学报, 2024, 40(8):2710-2730.WANG Q, GAO J Q, ZHOU Y J.Metabolic engineering for the efficient co-utilization of glucose and xylose[J].Chinese Journal of Biotechnology, 2024, 40(8):2710-2730.
[23] 王晨晶, 范文来, 徐岩, 等.豉香型传统工艺饼曲及机械化麸曲中的糖和糖醇[J].食品与发酵工业, 2018, 44(6):235-239.WANG C J, FAN W L, XU Y, et al.Sugars and sugar alcohols in traditional bingqu and mechanical-making moldy bran(Fuqu) for Chixiang aroma type liquor[J].Food and Fermentation Industries, 2018, 44(6):235-239.
[24] DHUNGEL P, HRYNETS Y, BETTI M.Sous-vide nonenzymatic browning of glucosamine at different temperatures[J].Journal of Agricultural and Food Chemistry, 2018, 66(17):4521-4530.
[25] SINGH R, SINGH R, KIM I W, et al.An efficient ribitol-specific dehydrogenase from Enterobacter aerogenes[J].Enzyme and Microbial Technology, 2015, 72:56-64.
[26] 于点, 郭卫冷, 丁炀, 等.肌醇代谢在植物响应非生物胁迫中的作用[J].植物遗传资源学报, 2024, 25(2):162-170.YU D, GUO W L, DING Y, et al.The role of myo-inositol metabolism in plants response to abiotic stress[J].Journal of Plant Genetic Resources, 2024, 25(2):162-170.
[27] MART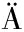 U G A, COMAN V, VODNAR D C.Recent advances in the biotechnological production of erythritol and mannitol[J].Critical Reviews in Biotechnology, 2020, 40(5):608-622.
U G A, COMAN V, VODNAR D C.Recent advances in the biotechnological production of erythritol and mannitol[J].Critical Reviews in Biotechnology, 2020, 40(5):608-622.
[28] 李雯. 苏氨酸对酱香风味的影响[D].贵阳:贵州大学, 2020.LI W.Effect of threonine on Maotai flavor[D].Guiyang:Guizhou University, 2020.
[29] ZHAO C J, SCHIEBER A, G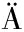 NZLE M G.Formation of taste-active amino acids, amino acid derivatives and peptides in food fermentations-A review[J].Food Research International, 2016, 89:39-47.
NZLE M G.Formation of taste-active amino acids, amino acid derivatives and peptides in food fermentations-A review[J].Food Research International, 2016, 89:39-47.
[30] HU H B, LI J W, JIANG W K, et al.Strategies for the biological synthesis of D-glucuronic acid and its derivatives[J].World Journal of Microbiology and Biotechnology, 2024, 40(3):94.