玫瑰茄(Hibiscus sabdariffa L.)是锦葵科木槿属的一年生草本植物,又名洛神花,洛神果、山茄等,其作为一种经济作物在福建、广东、广西、云南等地均有广泛种植[1-2]。玫瑰茄的营养价值在于其花萼中富含多酚类色素花色苷,含量可达其花萼干重的1.7%~2.5%[3]。玫瑰茄花色苷(Hibiscus sabdariffa L.anthocyanins,HSA)主要以飞燕草素-3-桑布双糖苷为主,还含有矢车菊素-3-O-半乳糖苷,飞燕草素-3-O-半乳糖苷,矢车菊素-3-桑布双糖苷和飞燕草素-3-O-葡萄糖苷等花色苷[4]。有较多研究表明,玫瑰茄中的花色苷等活性成分具有抗氧化、降血压、降血脂,降血糖以及抗肿瘤等生理功效和健康益处[5-8]。然而,花色苷稳定性差,在不利的酸碱、氧、亲核剂、酶、金属离子、温度、光照等因素的作用下,其生物活性损失较大[9]。保护花色苷的稳定性并减少生物活性损失成为花色苷加工利用的重要研究内容。
微胶囊化技术可以通过壁材包埋和递送需要保护的芯材,既能够提高芯材的稳定性也能提高特定芯材的生物效能。YOUNESI等[10]通过喷雾干燥法利用麦芽糊精和乳清蛋白粉将玫瑰茄花色苷微胶囊化,减少了花色苷的损失并使花色苷的抗氧化性得到更好的保护。与未包埋的玫瑰茄花色苷相比,经喷雾干燥微胶囊化后的花色苷在Cu2+和 Zn2+中稳定性更高[11]。DE MOURA等[12]采用离子凝胶滴注法制备玫瑰茄花色苷微胶囊(Hibiscus sabdariffa L. anthocyanin microcapsules,HSAM),模拟胃液消化后发现微胶囊能更好地在肠内保护花色苷的生物活性。也有研究指出锐孔法制备玫瑰茄花色苷微胶囊在体外释放实验中花色苷的缓释性更好[13]。由于微胶囊化技术方法和包埋壁材的多样性,不同包埋剂和包埋方法下玫瑰茄花色苷的包埋率、稳定性和微胶囊特征均有较大差异,探究不同工艺下玫瑰茄花色苷微胶囊的加工条件和粉体特性有重要意义。
本研究采用喷雾干燥法制备HSAM,在优化微胶囊加工工艺条件的基础上,采用激光粒度仪、粉体测试仪表征微胶囊理化特性,并考察玫瑰茄花色苷微胶囊化前后的稳定性,以期为玫瑰茄花色苷的合理加工利用提供理论参考。
1 材料与方法
1.1 材料与试剂
玫瑰茄花色苷(pH差示法测得原料中的总花色苷含量为26.51 mg矢车菊素-3-O-葡萄糖苷当量/g提取物),广东君道营养科技有限公司;阿拉伯胶,食品级,广东兴达食品配料有限公司;乳清蛋白,食品级,江苏荣创生物工程有限公司;壳聚糖盐酸盐,食品级,西安冠诚生物科技有限公司。
1.2 仪器与设备
ZY-8000喷雾干燥仪,上海紫裕生物科技有限公司;TM3030扫描电子显微镜,日本株式会社日立高新技术那珂事业所;LS-POP(9)激光粒度分析仪,珠海欧美克仪器有限公司;Multiskan GO酶标仪、Nicolet IS20傅里叶变换红外光谱仪,赛默飞世尔科技公司;ZWS-21 W紫外灯,苏州市相城区创新照明电器厂;GJ03-09粉体综合特性测试仪,白山市玖久仪器仪表有限公司;STA449热重分析仪,德国耐驰仪器制造有限公司;MiniFlex600X射线粉末衍射仪,日本理学(Rigaku)公司。
1.3 实验方法
1.3.1 不同喷雾干燥加工条件单因素试验
根据预实验和原料特性,本研究利用微胶囊包埋材料阿拉伯胶、乳清蛋白和壳聚糖盐酸盐按照5∶5∶1(质量比)混合作为复合包埋壁材,包埋材料的比例根据材料与花色苷粉结合程度选择确定。微胶囊制备方法参考已发表的方法制作[14]。以花色苷微胶囊的包埋率和含水率为指标进行单因素研究。壁材浓度单因素条件为:1%、2%、3%、4%、5%(质量分数),芯壁比1∶3,进料速率67%(流速8 mL/min),进风温度170 ℃的条件下。芯壁比单因素条件为:1∶1、1∶2、1∶3、1∶4、1∶5(g∶g),壁材浓度3%,进料速率67%,进风温度170 ℃。进料速率单因素条件为:63%(流速8 mL/min)、65%(流速11 mL/min)、67%(流速14 mL/min)、69%(流速17 mL/min)、71%(流速21 mL/min),在壁材浓度3%,芯壁比1∶3,进风温度170 ℃。进风温度单因素研究条件为:150、160、170、180、190 ℃,壁材浓度3%,芯壁比1∶3,进料速率67%。
1.3.2 响应面优化试验
在单因素试验的基础上,选取壁材浓度(X1)、芯壁比(X2)和进风温度(X3)3个因素,采用Design-Expert 13软件设计了3因素3水平Box-Behnke中心组合实验,具体因素水平和实验点设计见表1,其中芯壁比为芯材质量(g)和壁材质量(g)的比值。在-1、0、1的水平下3个因素对应的参数分别为:X1(1%、2%、3%)、X2(1∶2、1∶3、1∶4)、X3(170、175、180 ℃)。以花色苷包埋率作为响应值,以含水率为参考值进行测定。
表1 实验设计及响应值结果
Table 1 Box-Behnken design and response values
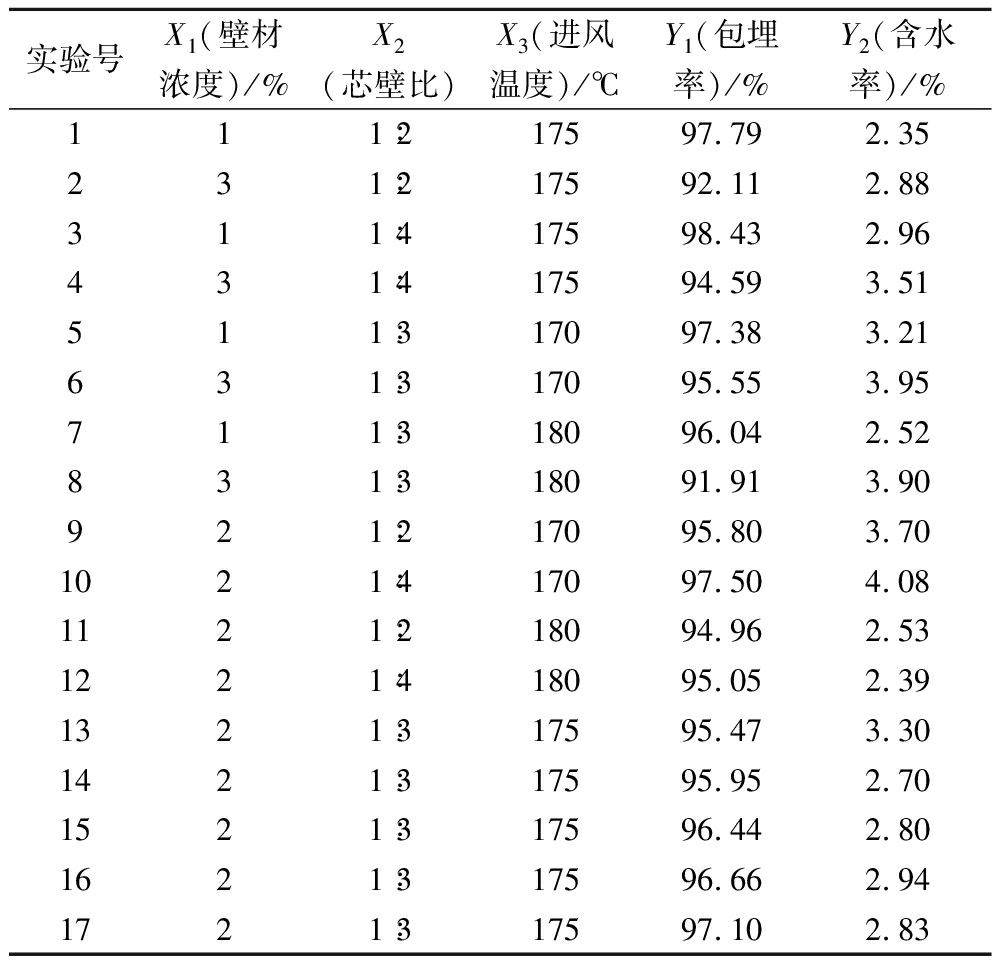
实验号X1(壁材浓度)/%X2(芯壁比)X3(进风温度)/℃Y1(包埋率)/%Y2(含水率)/%111∶217597.792.35231∶217592.112.88311∶417598.432.96431∶417594.593.51511∶317097.383.21631∶317095.553.95711∶318096.042.52831∶318091.913.90921∶217095.803.701021∶417097.504.081121∶218094.962.531221∶418095.052.391321∶317595.473.301421∶317595.952.701521∶317596.442.801621∶317596.662.941721∶317597.102.83
1.3.3 微胶囊花色苷含量测定和包埋率计算
微胶囊总花色苷含量参考已报道方法并调整后进行测定[15]。取0.2 g样品加入体积分数为60%的乙醇溶液10 mL,超声波细胞粉碎仪破碎1 min,过滤后取1 mL滤液分别与pH 1.0的缓冲液和pH 4.5的缓冲液4 mL混合,充分振荡后放入10 ℃冰箱中静置20 min,分别测定其在510 nm和700 nm波长条件下的吸光度,样品平行测定5组。
微胶囊表面花色苷含量测定:取0.2 g微胶囊粉体,加入10 mL无水乙醇,振荡后4 000 r/min,离心10 min。取1 mL上清液分别与pH值为1.0的缓冲液和pH值为4.5的缓冲液4 mL混合,充分振荡后放入10 ℃冰箱中静置20 min,用酶标仪分别测定其在510 nm和700 nm波长条件下的吸光度,样品平行测定5组。按照花色苷含量计算公式[16]计算微胶囊表面花色苷含量。
喷雾干燥微胶囊包埋率的计算[9]如公式(1)所示:
包埋率![]()
(1)
1.3.4 微胶囊含水率测定
采用自动水分测定仪测定HSAM含水率。记录称样皿质量W0,称取HSAM样品大约0.5 g放在称量盘上,记录干燥前样品质量W1,记录烘干后质量W2,最后按公式(2)计算含水率[17]:
含水率![]()
(2)
1.3.5 微胶囊特性表征
傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FT-IR)分析:取少量HSA与HSAM样品分别与溴化钾混合,研磨均匀后在干燥条件下压片,再将制备好的压片样品置于红外光谱室中进行扫描,测试条件为:扫描范围为4 000~400 cm-1,光谱分辨率为1 cm-1,扫描次数为64次。
热重分析:使用热重分析仪评估壁材和微胶囊的热稳定性。称取适量样品放入氧化铝杯中,设置热扫描范围为30~700 ℃,设置N2为冲洗气体,流速20 mL/min,升温速率 10 ℃/min [18]。
X-射线衍射(X-ray diffraction,XRD)分析:将微胶囊颗粒以表面无裂纹状态平铺于样品板中,以Cu-Ka射线作为激发源,测定样品的结晶度,电压40 kV,电流15 mA,衍射角范围5°~80°(2θ),步长以0.02 °/min进行扫描[19]。
扫描电镜观察:将一层导电胶带粘贴到样品架上,将微胶囊均匀地铺在导电胶带上,并进行喷金处理后,用扫描电子显微镜观察微胶囊的微观形态。测量条件为电压15 kV[20],在一定放大倍数下拍照。
微胶囊粒径及分布情况测定:将0.2 g微胶囊样品溶于100 mL无水乙醇,搅拌至混匀,用激光粒度分析仪在遮光比为10%~20%时测量微胶囊的粒径及分布。每个样品由仪器自动3次重复测定,统计仪器测定粒径和数量百分百比数据。粒径的多分散系数(polydispersity index, PDI)的计算,PDI=(D90-D10)/D50,其中D10、D50、D90分别表示样品中直径为10%、50%、90%的颗粒直径。
微胶囊粉体特性测定:采用粉体综合特性测试仪测量微胶囊(成品)的休止角、崩溃角、差角、松装密度、振实密度、压缩度、分散度等基本物理特性[1]。
1.3.6 微胶囊稳定性评价
温度对微胶囊稳定性影响处理条件:分别取0.5 g最优条件下包埋的HSAM粉末和HSA粉于称量皿中,置于电热恒温干燥箱中,在70、80、90 ℃下分别加热4、8、12 h,对比测定样品中花色苷含量。
紫外光照射对微胶囊稳定性的影响[21]:分别取0.5 g最优条件下包埋的HSAM粉末和HSA粉平铺于称量皿中,紫外光下分别照射处理8、10、12 h后取出,分别测定样品中花色苷含量。
以处理前后的花色苷保留率为指标评价微胶囊在不同条件下的稳定性,花色苷保留率计算如公式(3)所示:
花色苷保留率![]()
(3)
1.4 数据处理
所有实验重复至少3次,采用DesignExpert software 13进行实验响应面试验设计、数据处理及统计分析;其它实验数据用SPSS 27进行分析,显著性水平设定为P<0.05,数据用Excel和Origin软件处理并绘图。
2 结果与分析
2.1 不同条件下HSAM的包埋情况
花色苷微胶囊粉体水分含量不仅影响粉体的黏结性和流动性等加工性能,还会影响微胶囊的溶解性和保质期等。不同喷雾干燥条件对HSAM包埋率和含水率的影响见图1。由图1-A可知,在芯壁比固定,壁材浓度为2%时,花色苷包埋率达到最高值98.11%;而在壁材浓度最高5%时,花色苷的包埋率最低(92.42%)。这可能与壁材浓度的增加而溶液黏性升高有关,溶液的高黏性导致喷雾包埋效果下降。有研究表明亲水性胶体比例增加能够因自身的胶联而降低花色苷包埋率[22]。氢键是花色苷与各种乳清蛋白分子之间链接的主要结合力,直接使壁材复合物形成包埋胶囊[23],而本研究中高比例的乳清蛋白和高壁材浓度可能影响了这种氢键的形成。不同壁材浓度对HSAM含水率没有显著影响(P>0.05)。
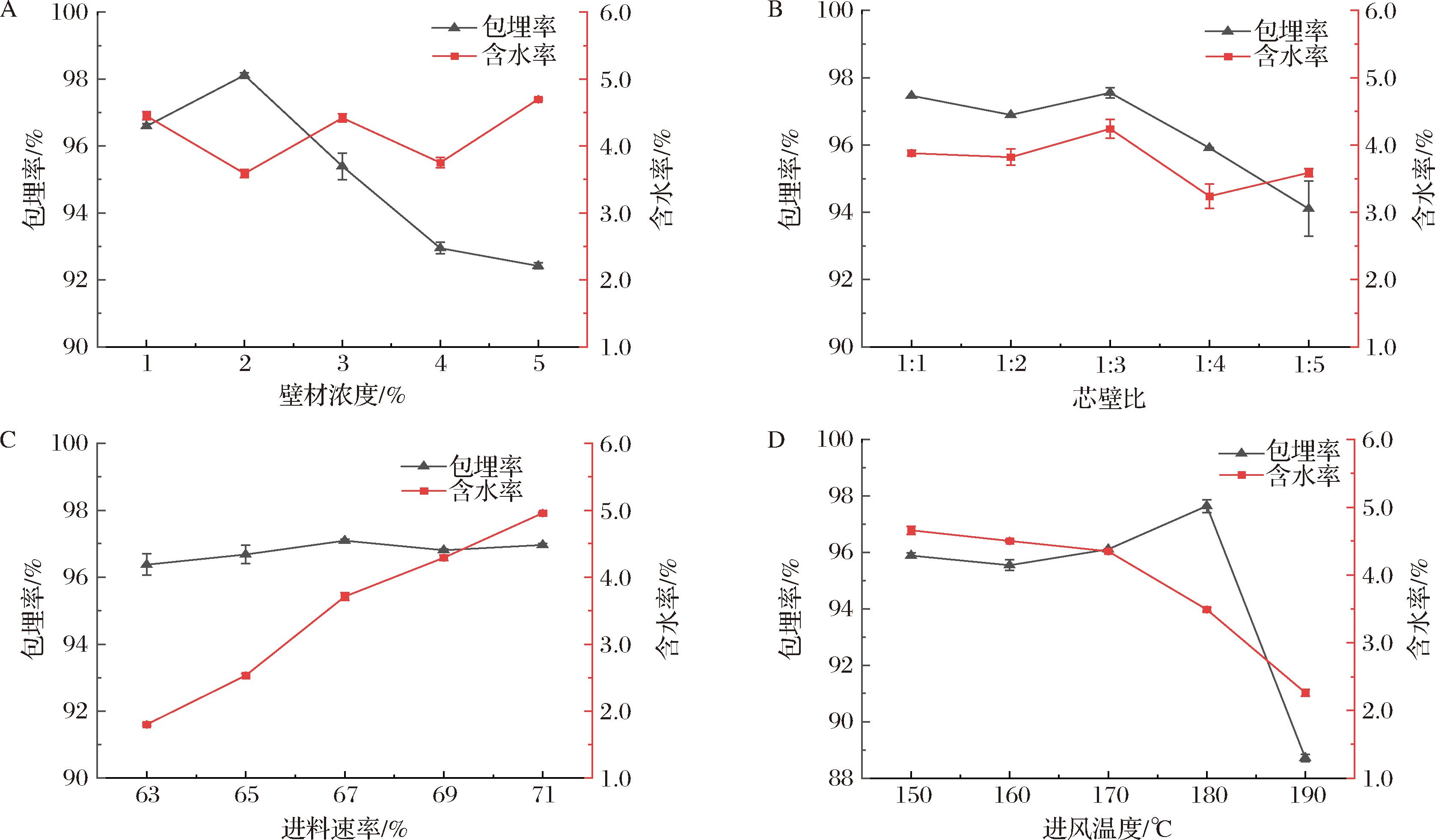
A-壁材浓度组;B-芯壁比组;C-进料速率组;D-进风温度组
图1 不同条件对花色苷微胶囊包埋率和含水率的影响
Fig.1 The influence of different factors on the encapsulation efficiency and moisture content of anthocyanin microcapsules
芯壁比对HSAM包埋率的影响见图1-B。在3%的壁材浓度下,芯壁比为1∶3时,包埋率最高为97.55%。芯壁比为1∶4和1∶5时,随花色苷芯材比例的降低包埋率显著降低(P<0.05),可能是因为在芯材比例较低的情况下,壁材之间的胶连增强而无法将芯材有效包埋。这与已报道研究结果一致[11,24],但有研究发现使用麦芽糊精作为单一包埋剂对玫瑰茄花色苷进行喷雾干燥包埋时,随着麦芽糊精比例的增加花色苷包埋率提高[25],这可能与壁材的不同特性有关。芯壁比对微胶囊含水率的影响趋势与包埋率类似,芯壁比在1∶4或1∶5时微胶囊含水率均低于4%。
不同进料速率对HSAM包埋率的无显著影响(P>0.05),见图1-C。这种不显著的变化与同类研究结果基本一致[26]。而微胶囊含水率则随进料速率的升高而显著增加(P<0.05),在进料速率为63%时微胶囊含水率最低为1.80%,在进料速率为71%时微胶囊含水率最高为4.96%。这是因为进料速率提升,喷雾干燥热加工过程中物料水分蒸发速率降低,微胶囊干燥不充分而含水量增加。
进风温度对HSAM包埋的率影响见图1-D。随着进风温度从150 ℃升至180 ℃,包埋率逐渐缓慢升高,并在180 ℃是达到最高值97.64%;当进风温度达到190 ℃时,包埋率陡然降低至88.70%。这可能是在190 ℃高温下花色苷因不耐高温而损失较多,导致包埋率降低。随着进风温度提高,喷雾干燥的干燥效能提升,HSAM的含水率呈下降趋势。
2.2 不同喷雾加工条件对HSAM粒径的影响
不同喷雾加工条件对HSAM粒径的影响如图2所示。不同条件下,HSAM的粒径主要分布在0~125 μm。当微胶囊的小粒径颗粒占比较高且分布较均匀集中时,喷雾干燥加工出的微胶囊较好。在所有测试因素中,不同壁材浓度的变化对HSAM的粒径影响差异较大,其他3个因素组间无显著差异。在壁材浓度为2%时最佳,所得微胶囊粒径在0~10 μm的占比达到43.23%,粒径在25 μm以下的微胶囊占比为85.27%;而壁材浓度为5%时,所得微胶囊粒径在0~10 μm的占比为17.14%,粒径在25 μm以下的微胶囊占比为66.82%。喷雾干燥法的微胶囊粒径大小主要受喷雾喷嘴大小、喷嘴位置、液体输送速率、雾化压力和溶液浓度的影响[27]。有研究指出较高的进风口温度下得到的花色苷微胶囊更小[28],但本研究未发现这种现象。综合以上结果,结合花色苷包埋率、含水率和微胶囊粒径变化规律,确定在进料速率为66%的条件下,对壁材浓度、芯壁比和进风温度3个因素进行响应面优化研究。
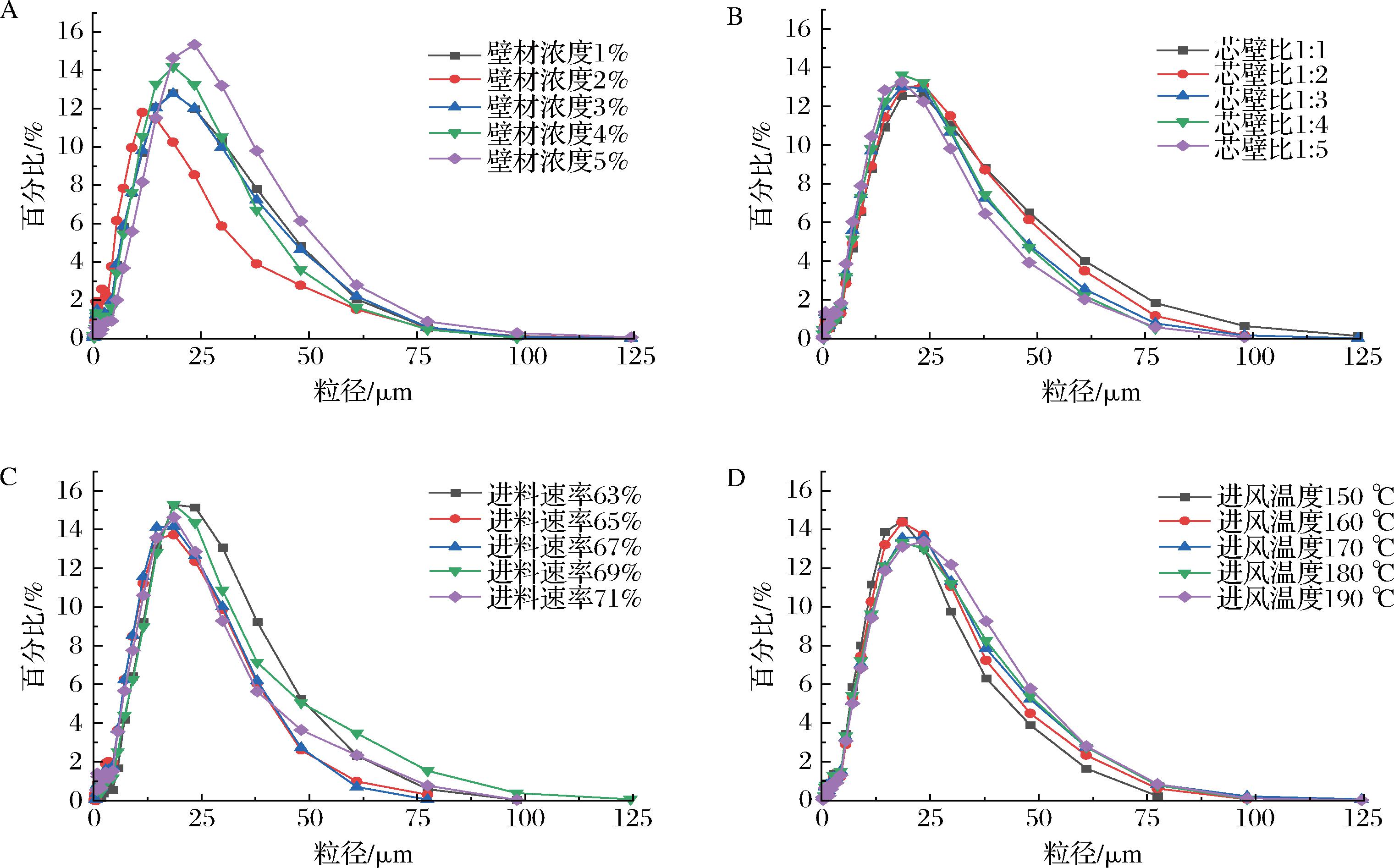
A-壁材浓度组;B-芯壁比组;C-进料速率组;D-进风温度组
图2 不同条件下花色苷微胶囊粒径分布图
Fig.2 Particle size distribution of anthocyanin microcapsules under different conditions
2.3 HSAM包埋条件的响应面优化
2.3.1 响应面结果与分析
花色苷微胶囊的响应面实验设计和结果如表1所示。结果表明,花色苷微囊的包埋率分布在91.91%~98.43%,水分含量在2.35%~4.08%。将HSAM包埋率作为响应值,进一步对结果进行回归分析,分析得到二次回归方程为:Y1=-5.66+0.19X1+0.14X2+0.07X3+0.007X1X2-0.007X1X3-0.001X2X3-![]()
对上述模型进行显著检验与方差分析,所建立的二次多项式模型极显著(P<0.01),模型的失拟项较大(P=0.285 2>0.05),说明该模型不失拟;模型决定系数R2为0.926 3,模型调整系数为![]() 这表明该模型与实验数据的拟合性较好[22],回归方程代表性较好,其响应值的变化有92.63%来自所选变量;可以通过这个回归模型对HSAM喷雾干燥工艺进行优化和预测。
这表明该模型与实验数据的拟合性较好[22],回归方程代表性较好,其响应值的变化有92.63%来自所选变量;可以通过这个回归模型对HSAM喷雾干燥工艺进行优化和预测。
方差分析结果中的F值可以反映因素对响应值影响程度,F值越大则影响程度越高[23],模型F值可以判断出各因素对包埋率影响的强度。分析结果表明,X1,X3对花色苷微囊含量的影响均达到了极显著水平,X2对其含量的影响较大,而X1X2、X1X3、X2X3和![]() 对其含量影响较小。各显著性以上的因素对花色苷微囊包埋率的影响程度大小的顺序是:壁材浓度(X1)>进风温度(X3)>芯壁比(X2)。
对其含量影响较小。各显著性以上的因素对花色苷微囊包埋率的影响程度大小的顺序是:壁材浓度(X1)>进风温度(X3)>芯壁比(X2)。
2.3.2 响应面模型验证
根据所得模型预测,各因素的最优参数组合为:壁材浓度1.247%、芯壁比1∶4、进风温度170.02 ℃;在此工艺条件下预计喷雾干燥所得HSAM的包埋率可达98.2%。为验证模型预测条件的可靠性,并考虑在生产实际及喷雾工艺对粉体含水率的影响,将验证参数调整为:壁材浓度1.2%、芯壁比1∶4和进风温度171 ℃,结果(图3-B)发现:HSAM包埋率可达(98.17±1.03)%,含水率为(3.24±0.18)%,与预测值吻合度较高。这表明该模型及优化后的条件适合用于HSAM的喷雾干燥加工。
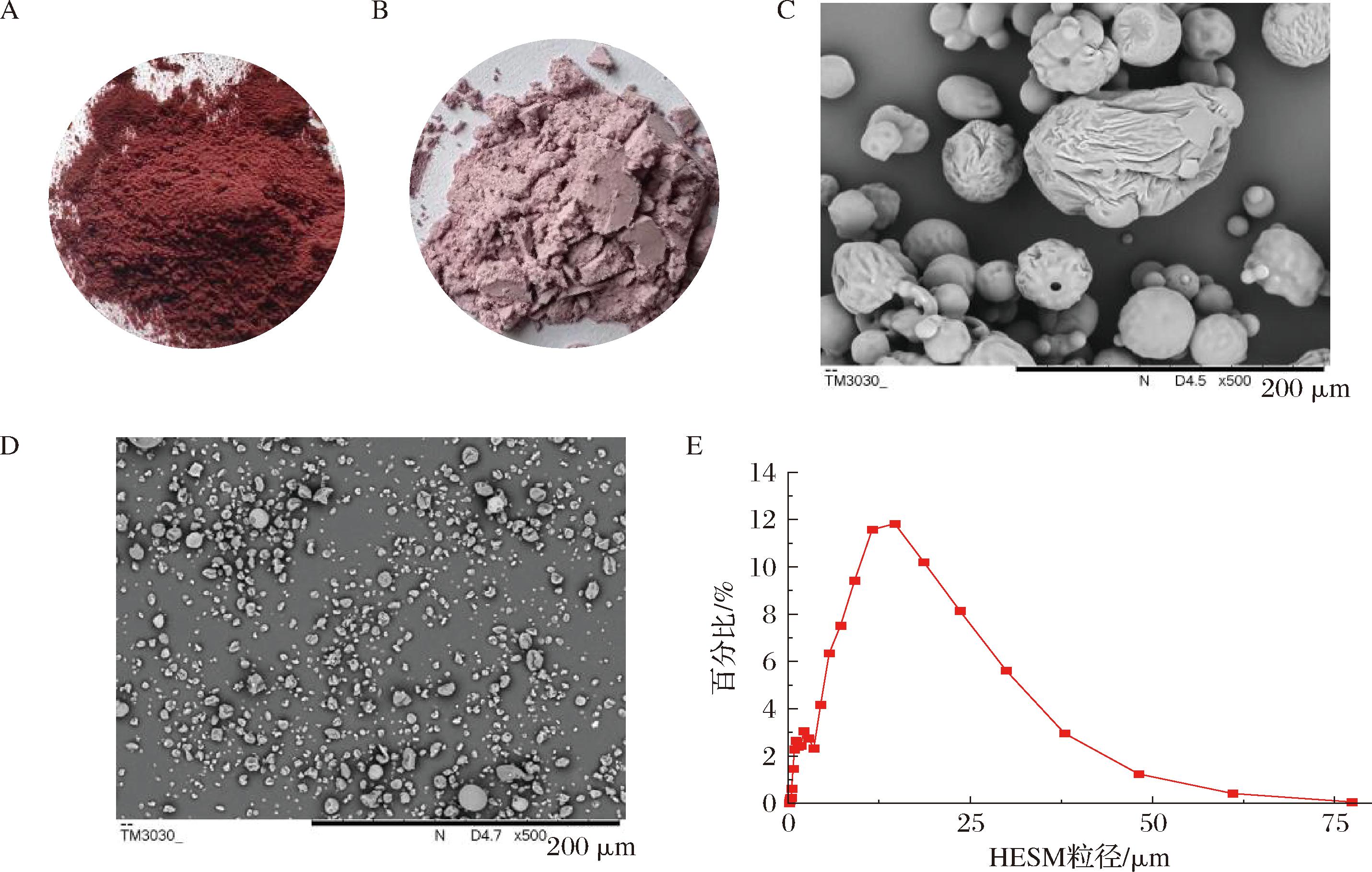
A-未包埋的HSA粉;B-最优条件下HSAM粉;C-HSA粉扫描电镜图;D-HSAM扫描电镜图;E-HSAM粒径分布图
图3 未包埋的HSA和最优条件下HSAM的样品形态和粒径图
Fig.3 Morphology and particle size distribution of unencapsulated HSA and encapsulated HSAM under optimal conditions
2.4 HSAM特性表征
2.4.1 HSAM的扫描电镜观察和粒度分析
分别对未包埋的HSA(图3-A)和最优条件下制备的HSAM(图3-B)进行扫描电镜观察发现,未包埋的HSA颗粒不均匀(图3-C),且粒径远大于HSAM的粒径(图3-D)。HSAM大小均匀,呈表面有褶皱的多面体状。这种形态是由于干燥过程中,壁材包裹花色苷后,在干燥过程中内部失水萎缩而出现的特征。这种褶皱状态时喷雾干燥法制备微胶囊的正常现象[29],与较多同类微胶囊微观结构类似[9]。未发现微胶囊有破裂损伤等形态,这表明壁材较好地包埋了花色苷,并在干燥过程中起到了支撑和保护作用。本研究的包埋材料中含有了乳清蛋白和壳聚糖,以乳清蛋白联合多糖为壁材的微胶囊能高效包封花色苷[30],这有助于支持微胶囊结构的稳定性。
通过激光粒度仪分析颗粒的散射光强,可以测定纳米微胶囊粒度及分布规律[16]。测定结果发现,HSAM的粒径主要范围在0~80 μm(图3-E);其中粒径30 μm以下的HSAM占比达到95.34%,0~20 μm粒径的HSAM占比达到81.59%,0~10 μm粒径的HSAM占比达到47.98%,0~1 μm粒径的微胶囊占比达到7.57%。代表颗粒分布均匀程度PDI达到0.43,表明颗粒较均匀。HSAM的粒度分析结果与扫描电镜的观察结果一致,表明HSAM微胶囊具有较小的粒径。
2.4.2 HSAM的粉体特性
干燥方法和包封条件对花色苷粉体的多种物理性能有显著影响[31]。对最优喷雾干燥条件下HSAM进行粉体综合特性测定发现(表2),所得HSAM的松装密度0.259 g/cm3, 振实密度0.516 g/cm3。这2个参数是反映粉体轻重的重要物理值,取决于粉体的粒度分布、温度、湿度等。有研究指出粉体堆积密度随着粒径的增加而减小[32]。所得HSAM的休止角为(44±0.5)°,崩溃角(23±0.5)°,说明得到的微胶囊粉体摩擦力小,黏度小,流动性较好,适合粉体管道化加工。还发现所得微胶囊的压缩度较大,为49.8%;而分散度较小,为19.6%;这说明粉体喷流性、飞溅性适中。
表2 最优条件下HSAM粉体综合特性
Table 2 Powder characteristics of HSAM under optimal conditions
休止角/°崩溃角/°差角/°松装密度振实密度压缩度/%分散度/%45.0±0.523.0±0.522.0±1.80.259±0.0120.516±0.03449.8±2.119.6±1.6
2.4.3 HSAM的FT-IR分析
如图4所示,HSA在3 436.53 cm-1处宽频带吸收峰对应花色苷 O—H 键伸缩振动产生,对应HSAM的吸收波长为3 399.89 cm-1。HSA在2 942.84 cm-1 处的峰来自 C—H 键伸缩振动,对应HSAM的吸收波长为2 931.27 cm-1。HSA在1 617.98 cm-1处的峰表示芳香烃骨架 C![]() C 伸缩,对应HSAM的吸收波长为1 602.56 cm-1。HSA在1 066.44 cm-1 处的峰来自酚类的 C—O 伸缩,对应HSAM的吸收波长为1 079.94 cm-1。以上都属于花色苷所属的黄酮类物质的典型特征峰。
C 伸缩,对应HSAM的吸收波长为1 602.56 cm-1。HSA在1 066.44 cm-1 处的峰来自酚类的 C—O 伸缩,对应HSAM的吸收波长为1 079.94 cm-1。以上都属于花色苷所属的黄酮类物质的典型特征峰。
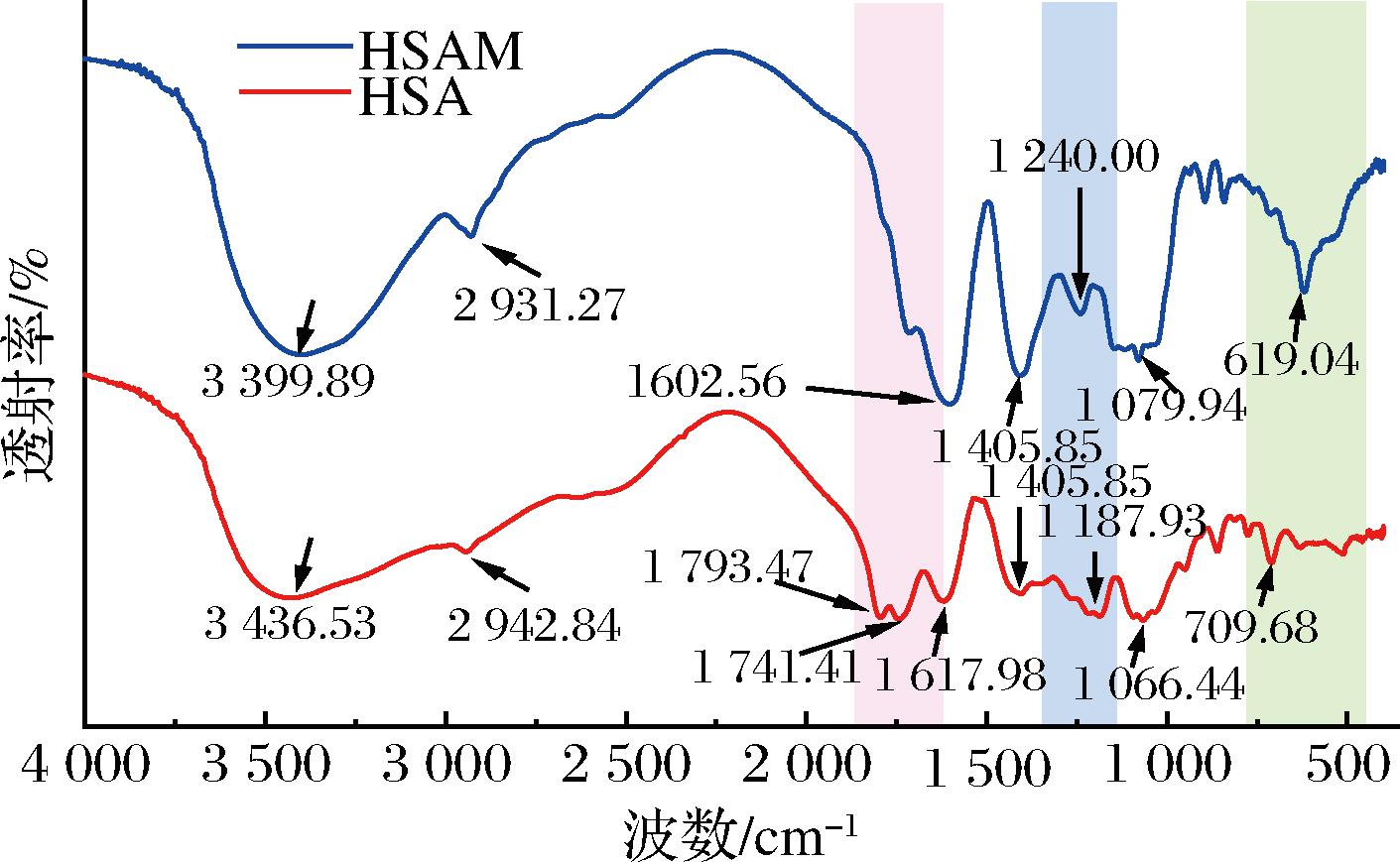
图4 未包埋的HSA和最优条件下HSAM的傅里叶变换红外光谱图
Fig.4 FT-IR spectra of unencapsulated HSA and encapsulated HSAM under optimal conditions
如图4中有底纹处的光谱图所示,微胶囊化后,HSA在1 793.47 cm-1和1 741.41 cm-1处的C—O 伸缩吸收峰,以及在1 187.93 cm-1处的酚类O—H吸收峰在HSAM对应的位置消失,说明壁材和花色苷之间结合形成了一定的氢键作用,包埋效果较理想。这与卡拉胶包埋玫瑰茄花色苷前后的红外图谱变化类似[24]。包埋后HSAM在619.04 cm-1处出现新的HN2面外摇吸收峰,并使HSA在709.68 cm-1的吸收峰消失,这可能是乳清蛋白粉中的HN2呈现出来的,说明复合包埋剂将花色苷包裹在内而自身暴露在外层而屏蔽了HSA对应的吸收峰,证明微胶囊化效果较好。
2.4.4 HSAM的XRD图谱分析
未包埋的HSA和微胶囊化后HSAM的XRD图谱如图5所示。2个样品在2θ=20°附近都出现了一个宽大衍射峰,表明两者都处于非晶相[33],而且所使用的的包埋剂不会导致峰位置的剧烈变化。这与紫薯花色苷包埋前后XRD图谱类似[34]。花色苷包埋前后其 XRD 衍射峰发生了偏移,HSA的衍射峰位于大约19.22°,HSAM的衍射峰峰大约位于21.46°;同时HSAM在31.96°出现了新的衍射峰。这表明包埋剂和花色苷之间发生了一定相互作用导致了新晶体结构的形成,包埋剂的添加对 HSA的晶体结构有一定影响,但不会影响胶囊粉末的结晶度。这与HSA经麦芽糖糊精包埋后的XRD图谱和结果有一定相似性,新形成的非晶态材的分子运动性、热力学特性和溶解性得到提高和改善[35]。
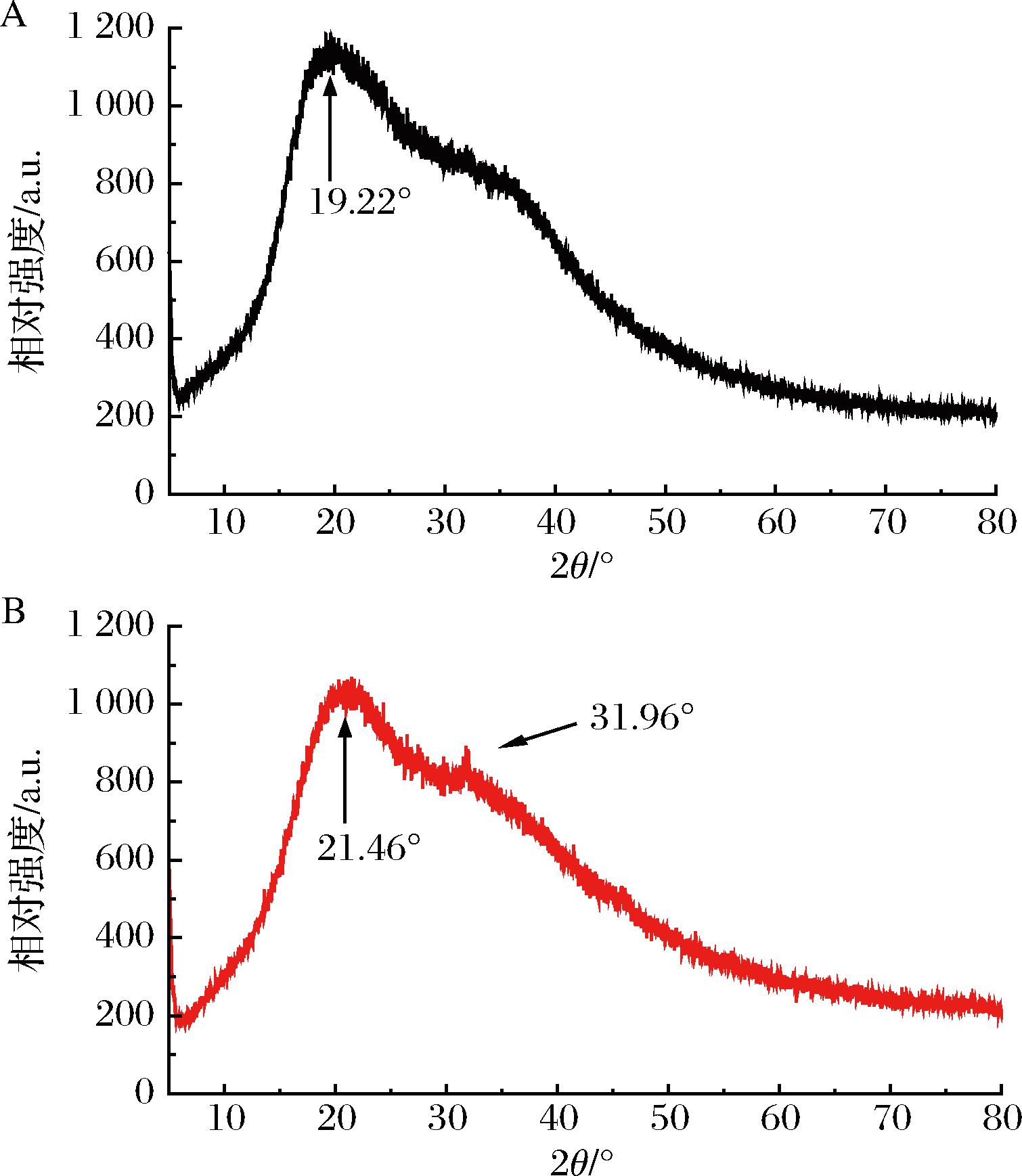
A-HSA;B-HSAM
图5 未包埋的HSA和最优条件下HSAM的X射线衍射图
Fig.5 XRD patterns of unencapsulated HSA and encapsulated HSAM under optimal conditions
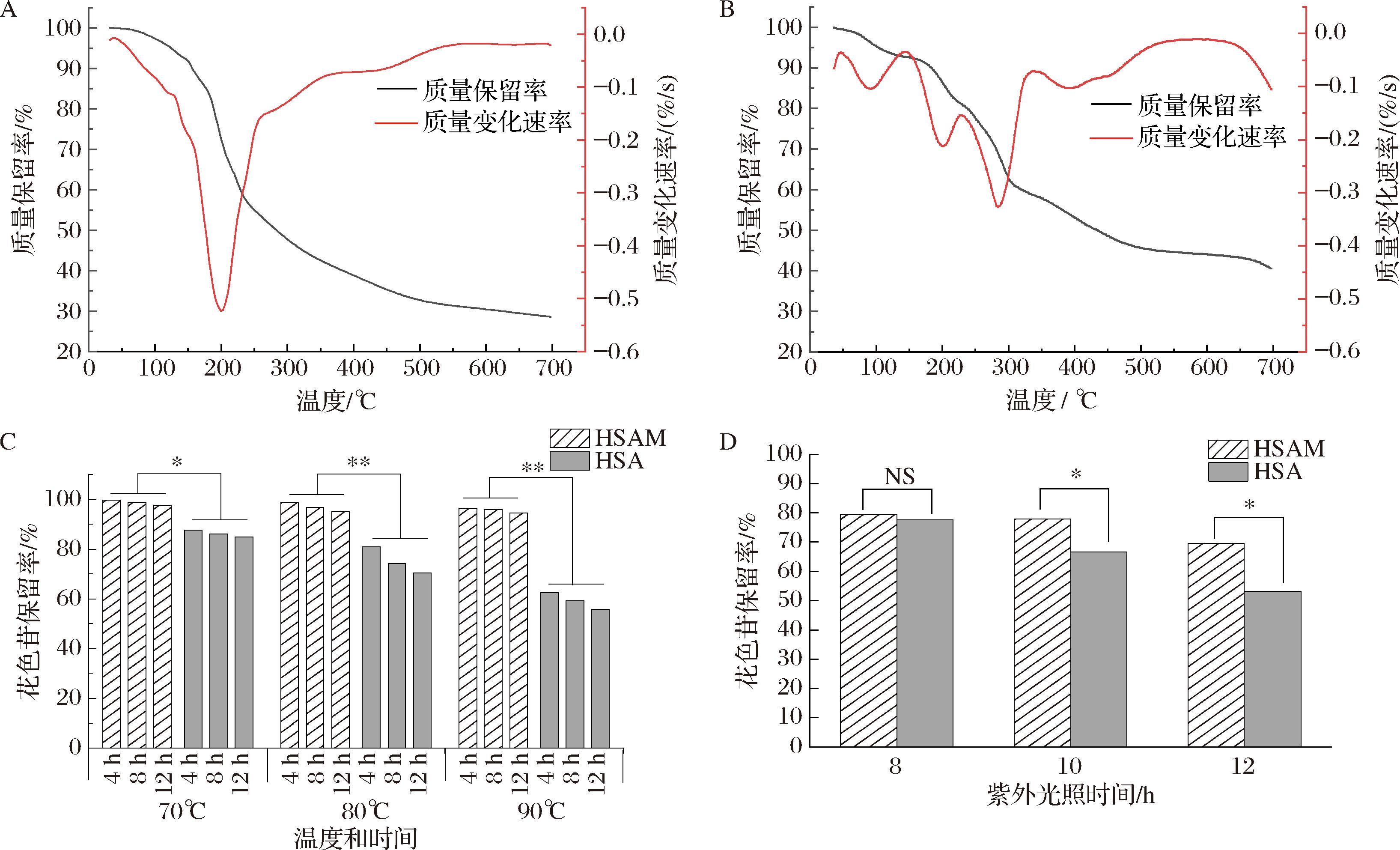
A-HSA热重分析图;B-HSAM热重分析图;C-温度对样品稳定性影响;D-紫外光光照对样品稳定性影响
图6 未包埋的HSA和最优条件下HSAM的稳定性分析图
Fig.6 Stability analysis of unencapsulated HSA and encapsulated HSAM under optimal conditions NS:P>0.05;*:P<0.05;**:P<0.01。
2.5 HSAM的热重分析和稳定性
热重分析可以通过测定样品在升温过程中的质量变化和降解情况反映样品的稳定性。未包埋的HSA在加热过程质量保留率曲线急剧下降(图6-A),在150~200 ℃时质量下降速率最快,表明HSA的质量在此阶段快速损失。这是因为玫瑰茄花色苷在高温下被加热分解[21]。与未包埋的HSA相比,包埋后的HSAM的质量保留率曲线下降较缓慢(图6-B),这表明包埋后的HSAM热稳定性更高。HSAM在升温过程中,质量变化速率曲线程波动下降趋势,在75~100 ℃、150~200 ℃和250~300 ℃有3个快速下降阶段,且第3个阶段下降速率最快,但低于HSA的最大下降速率。可能与复合包埋材料中的乳清蛋白分解进而导致花色苷暴露而分解[36]。这表明复合壁材在不同加热阶段逐渐分解,延缓了花色苷的质量损失速度,提高了花色苷的热稳定性。综合分析,HSAM在150 ℃以下热稳定性好,适于食品加工生产操作。
在低于100 ℃的温度下,随加热时间延长,HSA和HSAM中的花色苷保留率均有下降(图6-C),但HSAM组花色苷损失少,保留率更高。HSA组在70 ℃热处理4 h和12 h后,花色苷保留率分别为87.7%和84.9%,90 ℃的温度下加热4 h和12 h后,其花色苷保留率分别为62.6%和55.7%,极显著低于HSAM组(P<0.01)。HSAM组在70 ℃热处理4 h和12 h后,花色苷保留率为分别为99.7%和94.98.8%;在90 ℃的温度下加热4 h和12 h后,花色苷保留率为分别为96.3%和94.6%,无显著差异(P>0.05)。这表明微胶囊化的花色苷在较高的温度以及较长时间的加热处理条件下更稳定,这与葡萄花色苷微胶囊的稳定性结果一致[37]。这也表明玫瑰茄花色苷经混合壁材包埋、喷雾干燥加工成的HSAM稳定性高于HSA。
紫外光稳定性测试结果表明(图6-D),HSA组的花色苷保留率随紫外光照时间延长迅速下降,而HSAM中的花色苷保留率变化较小,具有较好的稳定性。在紫外光照射10 h和12 h后,HSAM中的花色苷保留率均显著(P<0.05,P<0.05)高于HSA组。这表明HSAM在紫外光下更稳定,花色苷损失率低。
3 结论
本研究以复配的阿拉伯胶、乳清蛋白和壳聚糖盐酸盐作为复合包埋壁材包埋花色苷,对喷雾干燥加工条件中的壁材浓度、芯壁比、进料速率和进风温度等因素进行了研究和响应面优化。发现各因素对花色苷微囊包埋率影响程度大小的顺序是:壁材浓度>进风温度>芯壁比。喷雾干燥法制备HSAM的最佳工艺条为:芯壁比1∶4、壁材浓度1.2%(质量分数)、进风温度171 ℃。在此条件下得到的HSAM包埋率为(98.17±1.03)%,含水率(3.24±0.18)%,且扫描电镜下粒径均匀,粒径低于10 μm的比例达到47.98%。所得HSAM的松装密度为0.259 g/cm3, 振实密度为0.516 g/cm3;且休止角为(44±0.5)°,黏度小,流动性较好,适合粉体管道化加工。花色苷被包埋后部分红外光谱消失,说明复合壁材较好地使原料微胶囊化。微胶囊的最大XRD衍射峰发生偏移,在31.96°出现了新的衍射峰,复合包埋剂与玫瑰茄花色苷形成了更稳定的新的粉晶体结构。热重分析和光热稳定性研究表明,微胶囊化后的玫瑰茄花色苷耐热性更好,在紫外光作用下更稳定。
本研究通过蛋白-胶体-多聚糖复合壁材制备的玫瑰茄花色苷微胶囊特性表征清晰,粒径均匀,具有较好的粉体加工特性和稳定性。所探索的玫瑰茄花色苷微胶囊的制备工艺条件、理化性质和稳定性,为玫瑰茄花色苷深加工提供了新的理论参考,有利于经济作物玫瑰茄进一步高值加工利用。
[1] CHEW L Y, TENG S K, NEO Y P, et al.The potential of Roselle (Hibiscus sabdariffa) plant in industrial applications:A promising source of functional compounds[J].Journal of Oleo Science, 2024, 73 (3):275-292.
[2] 李秀芬, 朱建军, 高照亮, 等.氮肥与磷钾肥对玫瑰茄生长及开花结果的影响[J].浙江农业科学, 2022, 63(11):2595-2597.LI X F, ZHU J J, GAO Z L, et al.The impact of nitrogen, phosphorus, and potassium fertilizers on the growth, flowering, and fruiting of Hibiscus Sabdariffa L.[J].Journal of Zhejiang Agricultural Sciences, 2022, 63(11):2595-2597.
[3] DA-COSTA-ROCHA I, BONNLAENDER B, SIEVERS H, et al.Heinrich Hibiscus sabdariffa L.—A phytochemical and pharmacological review[J].Food Chemistry, 2014, 165:424-443.
[4] 田美玲, 陈沁雯, 刘斌雄, 等.玫瑰茄花青素纯化、鉴定及抗氧化活性评价[J].现代食品科技, 2024, 40(7):155-165.TIAN M L, CHEN Q W, LIU B X, et al.Purification, identification, and antioxidant activity of anthocyanins from Roselle[J].Modern Food Science and Technology, 2024, 40(7):155-165.
[5] ALMAJID A, BAZROON A, ALAHMED A, et al.Exploring the health benefits and therapeutic potential of Roselle (Hibiscus sabdariffa) in human studies:A comprehensive review[J].Cureus, 2023,15(11):e49309.
[6] SAPIAN S, ALI IBRAHIM MZE A, JUBAIDI F F, et al.Therapeutic potential of Hibiscus sabdariffa Linn.in attenuating cardiovascular risk factors[J].Pharmaceuticals (Basel), 2023, 16(6):807.
[7] NAIDOO K, KHATHI A.The potential role of gossypetin in the treatment of diabetes mellitus and its associated complications:A review[J].International Journal of Molecular Sciences, 2023, 24(24):17609.
[8] JAMROZIK D, BORYMSKA W, ![]() I.Hibiscus sabdariffa in diabetes prevention and treatment-does it work an evidence-based review[J].Foods.2022,11(14):2134.
I.Hibiscus sabdariffa in diabetes prevention and treatment-does it work an evidence-based review[J].Foods.2022,11(14):2134.
[9] HUANG Y, ZHOU W B.Microencapsulation of anthocyanins through two-step emulsification and release characteristics during in vitro digestion[J].Food Chemistry, 2019, 278:357-363.
[10] YOUNESI M, PEIGHAMBARDOUST S H, SARABANDI K, et al.Application of structurally modified WPC in combination with maltodextrin for microencapsulation of Roselle (Hibiscus sabdariffa) extract as a natural colorant source for gummy candy[J].International Journal of Biological Macromolecules, 2023, 242(3):124903.
[11] 赵彦巧, 王月, 孟翔宇, 等.喷雾干燥法制备玫瑰茄花色苷微胶囊条件优化[J].福建农业学报, 2021, 36(1):104-114.ZHAO Y Q, WANG Y, MENG X Y, et al.Optimized preparation of spray-dried anthocyanins microcapsules[J].Fujian Journal of Agricultural Sciences, 2021, 36(1):104-114.
[12] DE MOURA S C S R, BERLING C L, GARCIA A O, et al.Release of anthocyanins from the hibiscus extract encapsulated by ionic gelation and application of microparticles in jelly candy[J].Food Research International, 2019,121:542-552.
[13] 孟翔宇, 赵彦巧, 李钰琨, 等.玫瑰茄花色苷微胶囊的制备及其稳定性与释放性的评价[J].食品工业科技, 2019, 40(14):174-181.MENG X Y, ZHAO Y Q, LI Y K, et al.Preparation of anthocyanin from Hibiscus sabdariffa microcapsules and evaluation of stability and release[J].Science and technology of food Industry, 2019, 40(14):174-181.
[14] MILLINIA B L, MASHITHAH D, NAWATILA R, et al.Microencapsulation of Roselle (Hibiscus sabdariffa L.) anthocyanins:Effects of maltodextrin and trehalose matrix on selected physicochemical properties and antioxidant activities of spray-dried powder[J].Future Foods, 2024, 9:100300.
[15] IDHAM Z, MUHAMAD I I, SARMIDI M R.Degradation kinetics and color stability of spray-dried encapsulated anthocyanins from Hibiscus sabdariffa L.[J].Journal of Food Process Engineering, 2012, 35(4):522-542.
[16] LIU Y J, CHEN F X, GUO H H.Optimization of bayberry juice spray drying process using response surface methodology[J].Food Science and Biotechnology, 2017, 26(5):1235-1244.
[17] 王闯, 宋江峰, 李大婧, 等.叶黄素微胶囊化研究[J].食品科学, 2011, 32(2):43-47.WANG C, SONG J F, LI D J, et al.Study on the microencapsulation of lutein[J].Food Science, 2011, 32(2):43-47.
[18] 孟梓怡,罗子阳,段翰英,等.杨梅果汁蛋白粉稳定性及其花色苷生物利用率[J].食品与发酵工业, 2023, 49(3):197-204.MENG Z Y, LUO Z Y, DUAN H Y, et al.Stability and anthocyanin bioavailability of red bayberry juice protein powder[J].Food and Fermentation Industries, 2023, 49(3):197-204.
[19] 赵洪源,杨倩倩,冯歆怡,等.不同壁材组成对文冠果油微胶囊理化性质与稳定性的影响 [J].食品与发酵工业, 2025,51(18):143-149.ZHAO H Y, YANG Q Q, FENG X Y, et al.Influence of wall composition on physical chemical properties and stability of Xanthoceras sorbifolium Bunge oil microcapsules[J].Food and Fermentation Industries, 2025,51(18):143-149.
[20] 李海龙,马子龙,米帅,等.黑果腺肋花楸花色苷纳米微胶囊的制备及其表征[J].中国食品学报, 2022, 22(12):191-199.LI H L, MA Z L, MI S, et al.Preparation and characterization of anthocyanin nano-microcapsules of Sorbus melanocarpa[J].Journal of Chinese Institute of Food Science and Technology.2022, 22(12):191-199.
[21] CHEN B Y, CHEN L, LI C, et al.Ultrasound-assisted glycosylation of ovalbumin and dextran conjugate carrier for anthocyanins and their stability evaluation[J].Ultrasonics Sonochemistry, 2024, 109:107024.
[22] 刘云海, 曹小红, 刘瑛.天然色素花青素的微胶囊化研究[J].食品科技, 2004, 29(11):18-20.LIU Y H, CAO X H, LIU Y.Study on microencapsulation of anthocyanins[J].Food Science and Technology, 2004, 29(11):18-20.
[23] WU G, HUI X D, LIANG J X, et al.Combination of rehydrated whey protein isolate aqueous solution with blackcurrant concentrate and the formation of encapsulates via spray-drying and freeze-drying:Alterations to the functional properties of protein and their anticancer properties[J].Food Chemistry, 2021, 355:129620.
[24] 王丽霞,肖辉民,吴浈浈,等.喷雾干燥玫瑰茄花色苷微胶囊化效果及其性质[J].食品工业, 2021, 42(6):6-10.WANG L X, XIAO H M, WU Z Z, et al.The encapsulation effect and the properties of spray-dried microencapsulated Roselle anthocyanins[J].Food Industry, 2021, 42(6):6-10.
[25] NGUYEN Q D, DANG T T, NGUYEN T V L, et al.Microencapsulation of roselle (Hibiscus sabdariffa L.) anthocyanins:Effects of drying conditions on some physicochemical properties and antioxidant activities of spray-dried powder[J].Food Science &Nutrition, 2022, 10(1):191-203.
[26] GAO X B, ZHU D H, LIU Y J, et al.Physicochemical properties and anthocyanin bioaccessibility of downy rose-myrtle powder prepared by superfine grinding[J].International Journal of Food Properties.2019, 22(1):2022-2032.
[27] MAHDAVI S A, JAFARI S M, GHORBANI M, et al.Spray-drying microencapsulation of anthocyanins by natural biopolymers:A review[J].Drying Technology, 2014, 32(5):509-518.
[28] JAFARI S M, GHALEGI GHALENOEI M, DEHNAD D.Influence of spray drying on water solubility index, apparent density, and anthocyanin content of pomegranate juice powder[J].Powder Technology, 2017, 311:59-65.
[29] NAMBIAR R B, SELLAMUTHU P S, PERUMAL A B.Microencapsulation of tender coconut water by spray drying:Effect of Moringa oleifera gum, maltodextrin concentrations, and inlet temperature on powder qualities[J].Food and Bioprocess Technology, 2017, 10(9):1668-1684.
[30] 吴越, 杨军, 王琦, 等.贮藏时间和温度对蓝莓花色苷微胶囊品质的影响[J].农业工程学报, 2017,33(8):301-308.WU Y, YANG J, WANG Q, et al.Effects of storage time and temperature on quality of blueberry anthocyanin microcapsules[J].Transactions of the Chinese Society of Agricultural Engineering, 2017, 33(8):301-308.
[31] ![]() C, KESKIN O,
C, KESKIN O, ![]() H, et al.Encapsulation and drying methods in the production of powdered red cabbage (Brassica oleracea L.):Chemometrics and Fourier transform infrared spectroscopy[J].Food Science and Technology International, 2024, 5:10820132241238261.
H, et al.Encapsulation and drying methods in the production of powdered red cabbage (Brassica oleracea L.):Chemometrics and Fourier transform infrared spectroscopy[J].Food Science and Technology International, 2024, 5:10820132241238261.
[32] CAPARINO O A, TANG J, NINDO C I, et al.Effect of drying methods on the physical properties and microstructures of mango (Philippine‘Carabao’ var.) powder[J].Journal of Food Engineering, 2012, 111(1):135-148.
[33] NGUYEN Q D, DANG T T, NGUYEN T V L, et al.Microencapsulation of Roselle (Hibiscus sabdariffa L.) anthocyanins:Effects of different carriers on selected physicochemical properties and antioxidant activities of spray-dried and freeze-dried powder[J].International Journal of Food Properties, 2022, 25(1):359-374.
[34] 贺禧,赵涛,雷激,等.紫薯粗提物微胶囊的制备、表征及其生物活性研究[J].食品与发酵工业,2025,51(21):286-297.HE X, ZHAO T, LEI J, et al.Preparation, characterization and biological activity study of purple sweet potato crude extract microcapsules[J].Food and Fermentation Industries, 2025,51(21):286-297.
[35] KARTINI K, HUDA M B, HAYATI Z M, et al.Scaling up stirring-assisted extraction and transformation of Roselle anthocyanins into dried powder using spray-drying and oven-drying[J].Applied Food Research, 2023, 3(2):100357.
[36] WANG Y, YANG C, ZHANG J, et al.Interaction between whey protein isolate and rose anthocyanin extracts at different pHs:Structure, emulsification and digestibility of complexes[J].Food Bioscience, 2022, 49:101888.
[37] 毛莹, 帅晓艳, 王惠玲, 等.基于内源乳化法和喷雾干燥优化制备花色苷微胶囊及其稳定性分析[J].食品科学, 2020, 41(2):267-275.MAO Y, SHUAI X Y, WANG H L, et al.Preparation and stability evaluation of anthocyanin microcapsules by emulsification/internal gelation with optimized spray drying[J].Food Science, 2020, 41(2):267-275.