黄嘌呤氧化酶 (xanthine oxidase, XOD) 是生物体内催化活性氧 (reactive oxygen species,ROS) 生成的唯一酶类,在嘌呤代谢途径中催化次黄嘌呤氧化为黄嘌呤,并最终生成尿酸[1]。当前降尿酸治疗策略主要包括抑制XOD活性以减少尿酸生成,以及使用促尿酸排泄药物[2]。现有药物如XOD抑制剂(别嘌呤醇)和促尿酸排泄剂(苯溴马隆)虽具疗效,但存在肝肾毒性、超敏反应等副作用,导致长期用药依从性降低。因此,兼具安全性与疗效的药食同源中草药成为研究热点。
葛根 (Pueraria lobata) 作为传统药食两用资源,富含葛根素、黄豆苷元等黄酮类化合物,其降尿酸作用已在动物模型中得到初步验证[3]。然而,现有的XOD抑制剂筛选技术(如紫外分光光度法、电化学法、固定化酶亲和筛选、虚拟筛选)普遍存在以下局限:难以从复杂天然提取物中快速定位活性成分;筛选与结构鉴定环节分离,导致研究周期冗长;缺乏对活性成分与靶酶相互作用机制的深入解析[4]。因此,亟需开发一种集活性成分捕获、高效鉴定及作用机制验证于一体的筛选方法。近年来,超滤技术、平衡透析法以及功能化磁性纳米颗粒 (magnetic nanoparticles, MNPs) 与高效液相色谱联用技术,已被证明是筛选天然产物活性化合物的简便且高效的工具[5]。
MNPs 因其固有的磁性分离能力及纳米结构优势而备受关注[6-7]。随着纳米技术的发展,核壳结构磁性纳米颗粒因其内层Fe3O4核心提供的基础磁性和外层赋予的附加功能特性,已成为研究热点[8]。二氧化硅作为最常用的壳层材料之一,具有生物相容性高、易于表面功能化修饰、并能有效防止核心磁性材料的氧化和团聚等显著优势[9-10]。此外,核壳型磁性二氧化硅纳米颗粒还能显著提高固定化过程中酶的负载量和稳定性[11]。基于酶与配体之间的特异性亲和作用,固定化于磁性二氧化硅纳米颗粒上的酶可用于从复杂天然产物中高效、选择性地捕获其结合配体[12]。
1 材料与方法
1.1 材料与试剂
葛根,购买自陕西商洛秦岭,经课题组鉴定确为葛根;分析纯无水乙醇、分析纯氨水,天津欧博凯化工有限公司;黄嘌呤[(xanthine,XA),纯度:98%,批号:M06GB140821]、别嘌醇(allopurinol,纯度:98%,批号:X27 J10Y91606),上海源叶生物科技有限公司;XOD(50 U/mg),上海麦克林生化科技股份有限公司。
1.2 仪器与设备
多功能粉碎机,永康市红太阳机电有限公司;RE-2000B真空旋转蒸发器,上海亚荣生化仪器厂;LGJ-12A真空冷冻干燥机,北京四环起航科技有限公司;T2600紫外可见分光光度计,上海佑科仪器仪表有限公司;先行者电子天平,奥豪斯仪器(常州)有限公司;Smart Lab9 KW X射线衍射(X-ray diffraction,XRD)仪,日本Rigaku公司;JSM-IT200扫描电子显微镜(scanning electron microscope,SEM),日本电子株式会社;Vertex70红外光谱仪,德国布鲁克公司;超高效液相色谱串联傅里叶变换质谱,赛默飞公司。
1.3 实验方法
1.3.1 固定化XOD的制备
参考DENG等[13]的方法并稍作改动:量取1 mL Fe3O4分散液于952 mL乙醇和278 mL水中,超声均匀后加入30 mL氨水,再加入12 mL正硅酸四乙酯,室温下搅拌8 h后,将产物磁分离,用超纯水洗涤产物数次,冷冻干燥得样品Fe3O4@SiO2。
随后称取Fe3O4@SiO2磁性纳米颗粒139 mg,超声10 min使Fe3O4@SiO2完全分散于280 mL无水乙醇中,再加入2.8 mL 3-氨基丙基三乙氧基烷硅,室温下搅拌6 h后,将产品进行磁分离,用超纯水洗涤数次后,冷冻干燥得氨基化Fe3O4@SiO2磁性纳米颗粒。将130 mg氨基官能化后的Fe3O4@SiO2磁性纳米颗粒悬浮于130 mL戊二醛溶液中活化1 h,磁吸,弃上清液;用PBS洗涤3次,磁分离,弃上清;加入56 mL XOD溶液(50 μg/mL)到磁珠中在室温下搅拌2 h将XOD固定在磁性 Fe3O4@SiO2 固体载体上,最后磁分离,用PBS洗涤3次,磁分离得样品Fe3O4@SiO2-XOD,置于PBS中4 ℃保存。
1.3.2 磁珠固定化酶的结构表征
1.3.2.1 XRD分析
将空白磁珠和样品磁珠在扫描范围5~90°,电压40 VA,管电流为200 mA的条件下用Smart Lab9 KW XRD仪进行检测[14]。
1.3.2.2 SEM分析
将空白磁珠和样品磁珠粘到导电胶上[15],用GVC-1 200喷金仪喷金,随后直接用JSM-IT200扫描电子显微镜拍摄样品。
1.3.2.3 傅里叶变换红外光谱(Fourier transform infrared spectroscopy,FTIR)
采用KBr压片法制样,对空白磁珠和磁珠固定化酶进行官能团表征分析,测试波数为4 000~400 cm-1[15]。
1.3.3 实际样品垂钓
1.3.3.1 葛根溶液制备
根据课题组前期工作[16],将葛根中药材清洗烘干,粉碎成末,过40~60目筛,制得葛根粗粉;称取粗粉,添加固液比1∶20(g∶mL)的40%(体积分数)乙醇溶液,80 ℃恒温水浴分别提取2次,合并滤液。将滤液在真空旋转蒸发仪中进行浓缩,得到葛根提取物;再将蒸发浓缩后的提取物在真空冷冻干燥机中进行冷冻干燥,得到葛根提取物粉末。
1.3.3.2 样品垂钓
参考DENG等[13]的方法并作改动:将5 mg Fe3O4@SiO2-XOD磁性纳米颗粒添加到配制好的葛根提取物溶液中,在恒温振荡培养器中180 r/min、30 ℃的条件下孵育30 min,磁分离,PBS清洗磁性纳米颗粒3次;然后向磁性纳米材料配体络合物中添加3 mL甲醇(99.9%),同上步条件下孵育1 h,磁分离,吸取上清液至离心管中;将葛根提取物溶液和靶向垂钓后的甲醇洗脱液用0.22 μm微孔滤膜过滤,送至美吉生物用超高效液相色谱-四极杆飞行时间质谱联用(ultra-performance liquid chromatography-quadrupole-time-of-flight-mass spectrometry, UPLC-Q-TOF-MS)仪进行分析。
1.3.4 色谱及质谱条件
色谱分析参数:采用HSS T3 反向色谱柱(100 mm×2.1 mm, 1.8 μm),柱温箱温度设定为40 ℃,流动相流速0.40 mL/min,进样体积3 μL,流动相体系由以下组分构成:A相为体积分数为0.1%的甲酸-水-乙腈混合溶液(体积比为95∶5),B相为体积分数为0.1%的甲酸-乙腈-异丙醇-水三元溶剂体系(体积比为47.5∶47.5∶5),实施梯度洗脱程序。
质谱检测条件:采用电喷雾电离源(electrospray ionization,ESI)正负离子双模式扫描,质量扫描范围设定为m/z:70~1 050。离子源参数优化如下:离子源温度为400 ℃,碰撞室能量动态调节(20~60 V),正离子模式喷雾电压+3 400 V,负模式离子喷雾电压-2 800 V,去簇电压50 V,雾化气与辅助加热气均为50 psi,气帘气30 psi。
在上述条件下,对葛根提取物溶液及靶向垂钓后的甲醇洗脱液使用UPLC-Q-TOF-MS仪进行鉴定分析。
1.3.5 分子对接
分子对接研究通常用于揭示天然物质的最强结合方式[17]。此外,分子对接算法通过数值估算结合能,能够根据配体-受体相互作用的结合潜力对对接化合物进行排序。计算方法在化学与生物学中的整合,在现代靶向药物的研发过程中发挥了重要作用。对筛选所得化合物与XOD之间的分子对接模拟,具体方法如下:
受体蛋白结构准备:从UniProt数据库检索黄嘌呤氧化酶(XOD;UniProt ID:P47 989)通过RCSB PDB数据库筛选该UniProt ID对应的晶体结构,优先选择分辨率≤2.0 Å且含钼辅因子(Mo-co)的复合物结构(如PDB ID:1FIQ)下载PDB文件后移除水分子、辅酶及原始配体,保留完整酶结构采用PyMOL 2.5进行去溶剂化处理,并通过AutoDockTools执行质子化优化最终保存为预处理PDB格式文件;配体分子预处理:从PubChem数据库获取葛根活性成分(如刺芒柄花素Formononetin, CID:5 280 378)的2D SDF结构使用Chem3D 20.0进行构象搜索与MMFF94力场能量最小化输出为带电荷参数的Mol 2格式文件;分子对接与可视化:利用AutoDockTools定义活性口袋(Grid box:60×60×60 Å, spacing=0.375 Å)采用AutoDock Vina 执行半柔性对接(Exhaustiveness=32)对接结果导入PyMOL生成三维相互作用图(键距阈值≤3.5 Å)复合物经Discovery Studio构建二维相互作用图谱。
2 结果与分析
2.1 磁性纳米颗粒结构表征
2.1.1 XRD分析
XRD结果表明(图1),所制备的复合纳米颗粒在2θ=18.3°、30.1°、35.4°、43.1°、53.4°、56.9°、62.5°处呈现特征衍射峰,分别归属于(111)、(220)、(311)、(400)、(422)、(511)、(400)晶面,所有峰位与磁铁矿(Fe3O4, PDF#19-0629)的标准衍射数据高度吻合(误差小于0.2°),明确证实纳米颗粒内核为面心立方尖晶石结构(空间群Fd-3 m),这与吴江渝等[14]的研究结果相似。同时值得注意的是,图谱中未检测到归属于SiO2的特征衍射峰,表明材料中的Si组分主要以非结晶态形式存在,这很可能对应于包裹在磁性内核表面的非晶二氧化硅壳层;最外层修饰的XOD作为一种生物大分子蛋白质,其非晶态特性不会在 XRD 图谱中产生额外的布拉格衍射峰,因此XRD结果主要反映了内核Fe3O4/SiO2复合结构的晶体学特征[18]。该尖晶石结构的成功形成是材料具备超顺磁或铁磁性能的关键结构基础。
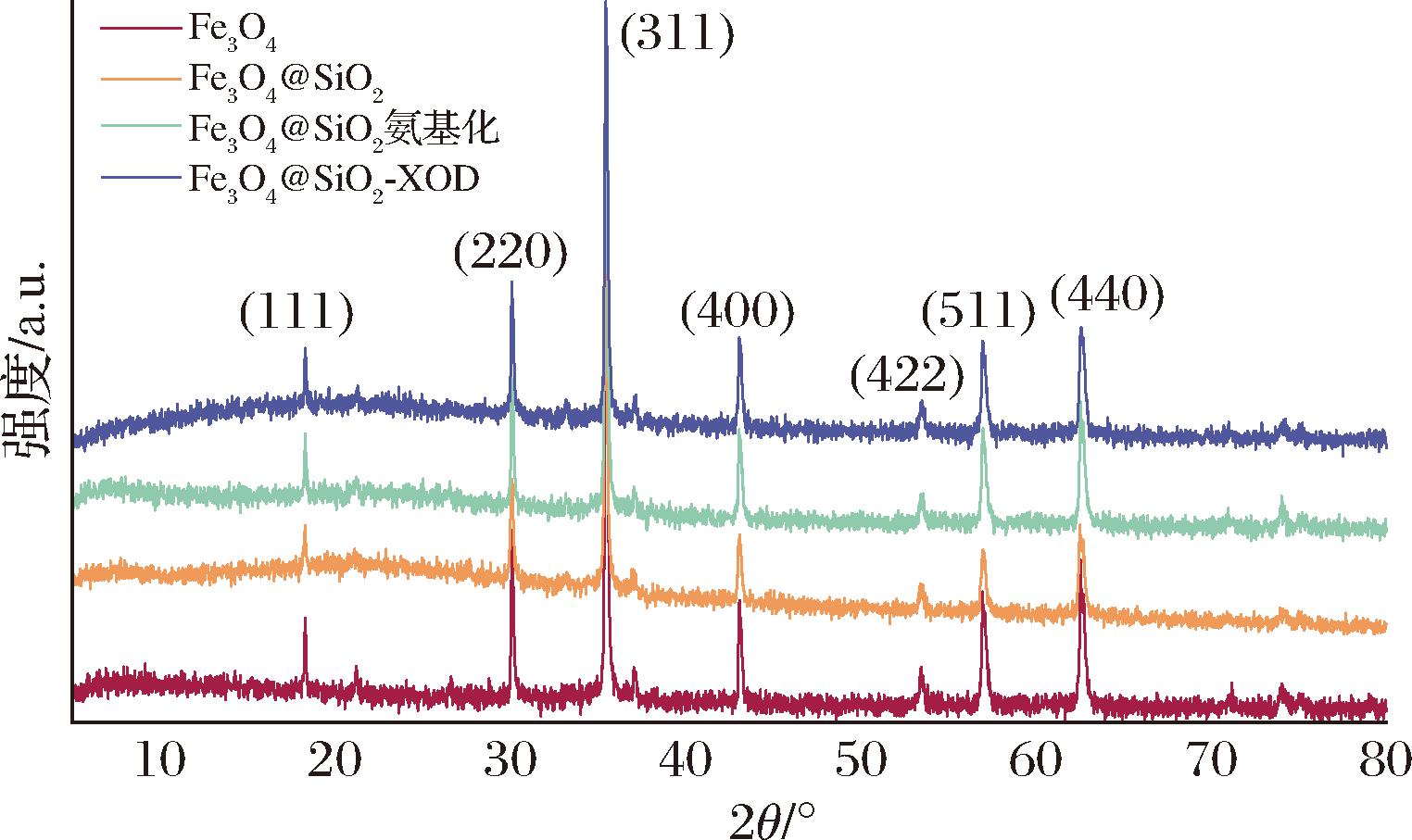
图1 Fe3O4、Fe3O4@SiO2、Fe3O4@SiO2氨基化、Fe3O4@SiO2-XOD的XRD图谱
Fig.1 XRD patterns of Fe3O4, Fe3O4SiO2, aminated Fe3O4@SiO2, and XOD-immobilized Fe3O4@SiO2
2.1.2 SEM表征
SEM表征结果如图2所示,可以发现经过SiO2包裹后的Fe3O4粒径均匀,呈球形,表面凹凸不平,通过与图2-a对比能够发现其表面有一层壳聚包裹物,说明SiO2已经修饰在表面,但XOD是否被修饰上还不明确,需要结合其他表征分析确定[18]。

a-Fe3O4;b-Fe3O4@SiO2;c-Fe3O4@SiO2氨基化;d-Fe3O4@SiO2-XOD
图2 Fe3O4、Fe3O4@SiO2、Fe3O4@SiO2氨基化、Fe3O4@SiO2-XOD的SEM表征图
Fig.2 SEM micrographs of Fe3O4,Fe3O4@SiO2, aminated Fe3O4@SiO2, and XOD-immobilized Fe3O4@SiO2
2.1.3 红外光谱分析
图3是其红外图谱,在580 cm-1处的峰是由Fe3O4中Fe—O—Fe键的伸缩振动引起,是Fe3O4的特征吸收峰;经过正硅酸四乙酯表面修饰的Fe3O4磁性纳米颗粒在1 091.3 cm-1处出现新的吸收峰,这是由于二氧化硅层中Si—O—Si不对称伸缩振动引起的,且756.3 cm-1和848.1 cm-1为Si—O—Si对称收缩振动,478.4 cm-1为SiO2的弯曲振动峰,说明SiO2层已成功涂布于磁性颗粒表面;加入3-氨基丙基三乙氧基烷硅在Fe3O4@SiO2磁性纳米颗粒修饰上—NH2后在3 100 cm-1处吸收峰变宽,在1 592.1 cm-1处吸收峰增强,这是由于C—N伸缩振动和N—H弯曲振动引起,表明功能性氨基已连接到磁性纳米颗粒上,固定了XOD之后,1 640 cm-1为—OH的弯曲伸缩振动峰,表明XOD包覆在材料表面,这与宋敏杰[19]研究结果相似。
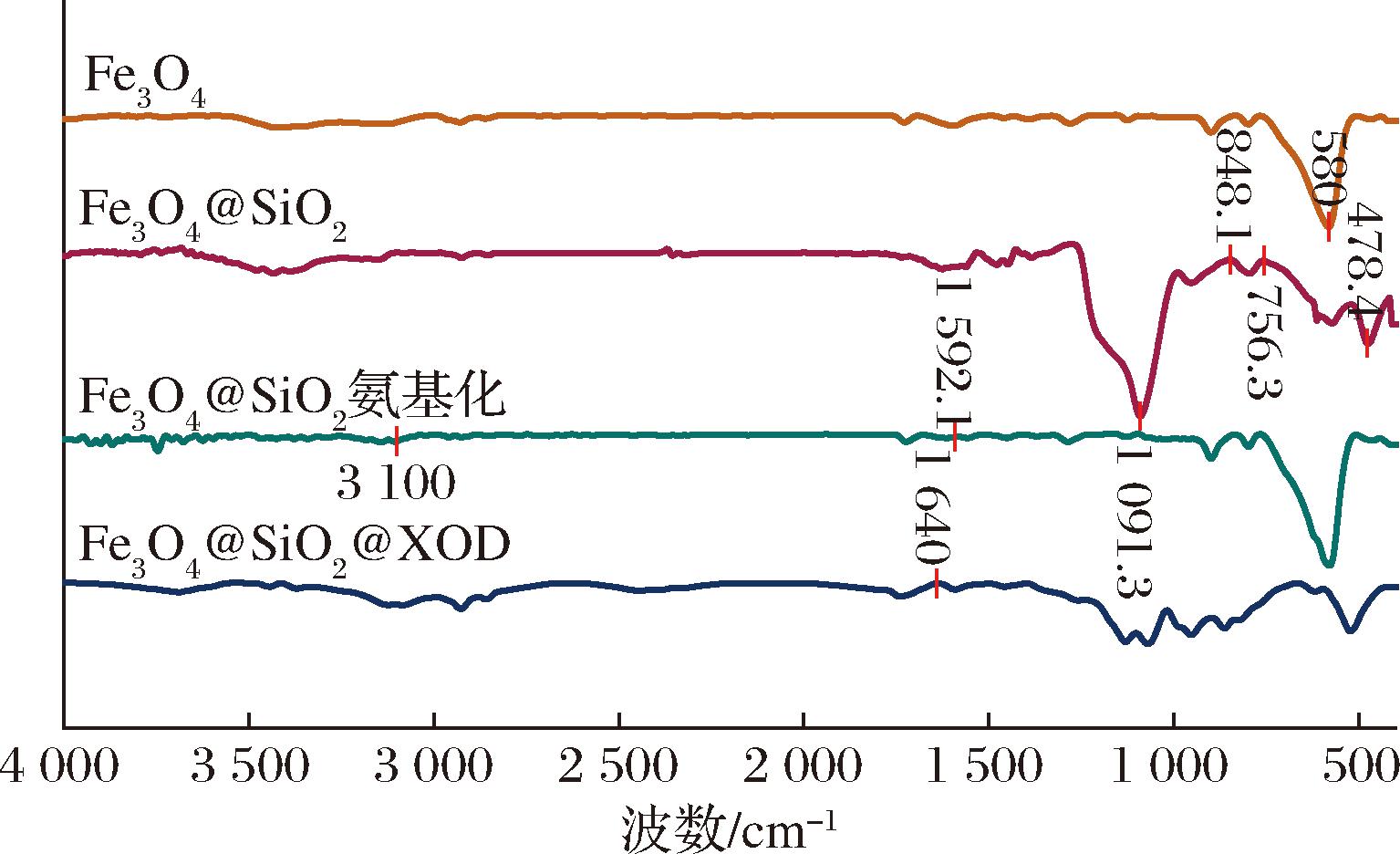
图3 Fe3O4、Fe3O4@SiO2和Fe3O4@SiO2-XOD红外光谱图
Fig.3 FTIR spectra of Fe3O4, Fe3O4@SiO2, and XOD-immobilized Fe3O4@SiO2
2.2 活性成分筛选结果
对葛根提取液以及经XOD靶向垂钓提取甲醇洗脱液样品进行分析,得到质谱在正离子及负离子模式下的总离子色谱图(total ion chromatogram,TIC),将葛根提取液与XOD靶向垂钓洗脱液进行对比,如图4所示。正离子模式下,葛根提取液检出30个显著色谱峰[保留时间(retention time,RT):0.0~8.0 min],主要归属为异黄酮类(如葛根素、大豆苷)及生物碱,XOD靶向垂钓洗脱液检出8个特异性富集峰;负离子模式下,葛根提取液检出32个显著色谱峰,对应有机酸类化合物;XOD靶向垂钓洗脱液检出7个高选择性峰,能够看到经XOD垂钓后的色谱峰明显减少,说明垂钓有效。最终确定这15个化合物信息见表1,其中异黄酮类化合物9个、酚酸类化合物3个、植物甾醇2个以及脂肪酸类化合物1个。
表1 葛根中与降尿酸相关性较大的化学成分
Table 1 Chemical components of Pueraria lobata with high correlation with lowering uric acid
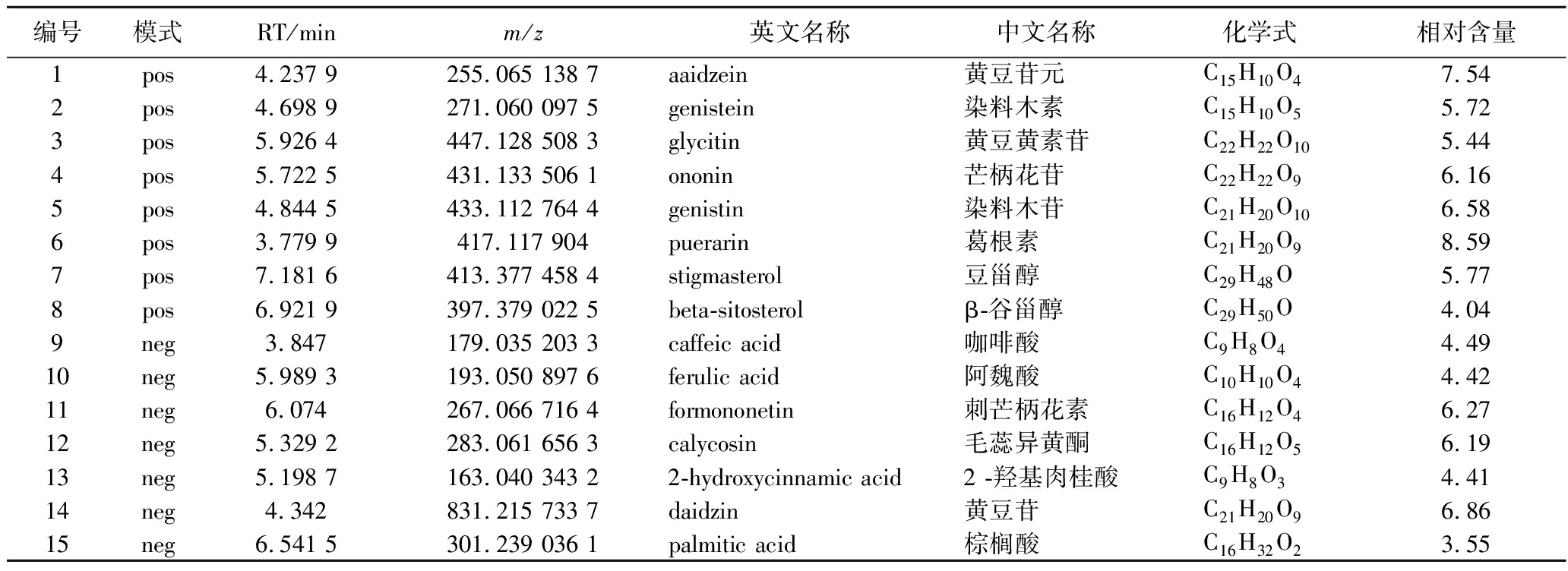
编号模式RT/minm/z英文名称中文名称化学式相对含量1pos4.237 9255.065 138 7aaidzein黄豆苷元C15H10O47.542pos4.698 9271.060 097 5genistein染料木素C15H10O55.723pos5.926 4447.128 508 3glycitin黄豆黄素苷C22H22O105.444pos5.722 5431.133 506 1ononin芒柄花苷C22H22O96.165pos4.844 5433.112 764 4genistin染料木苷C21H20O106.586pos3.779 9417.117 904puerarin葛根素C21H20O98.597pos7.181 6413.377 458 4stigmasterol豆甾醇C29H48O5.778pos6.921 9397.379 022 5beta-sitosterolβ-谷甾醇C29H50O4.049neg3.847179.035 203 3caffeic acid咖啡酸C9H8O44.4910neg5.989 3193.050 897 6ferulic acid阿魏酸C10H10O44.4211neg6.074267.066 716 4formononetin刺芒柄花素C16H12O46.2712neg5.329 2283.061 656 3calycosin毛蕊异黄酮C16H12O56.1913neg5.198 7163.040 343 22-hydroxycinnamic acid2 -羟基肉桂酸C9H8O34.4114neg4.342831.215 733 7daidzin黄豆苷C21H20O96.8615neg6.541 5301.239 036 1palmitic acid棕榈酸C16H32O23.55
注:pos代表正离子模式,neg代表负离子模式。
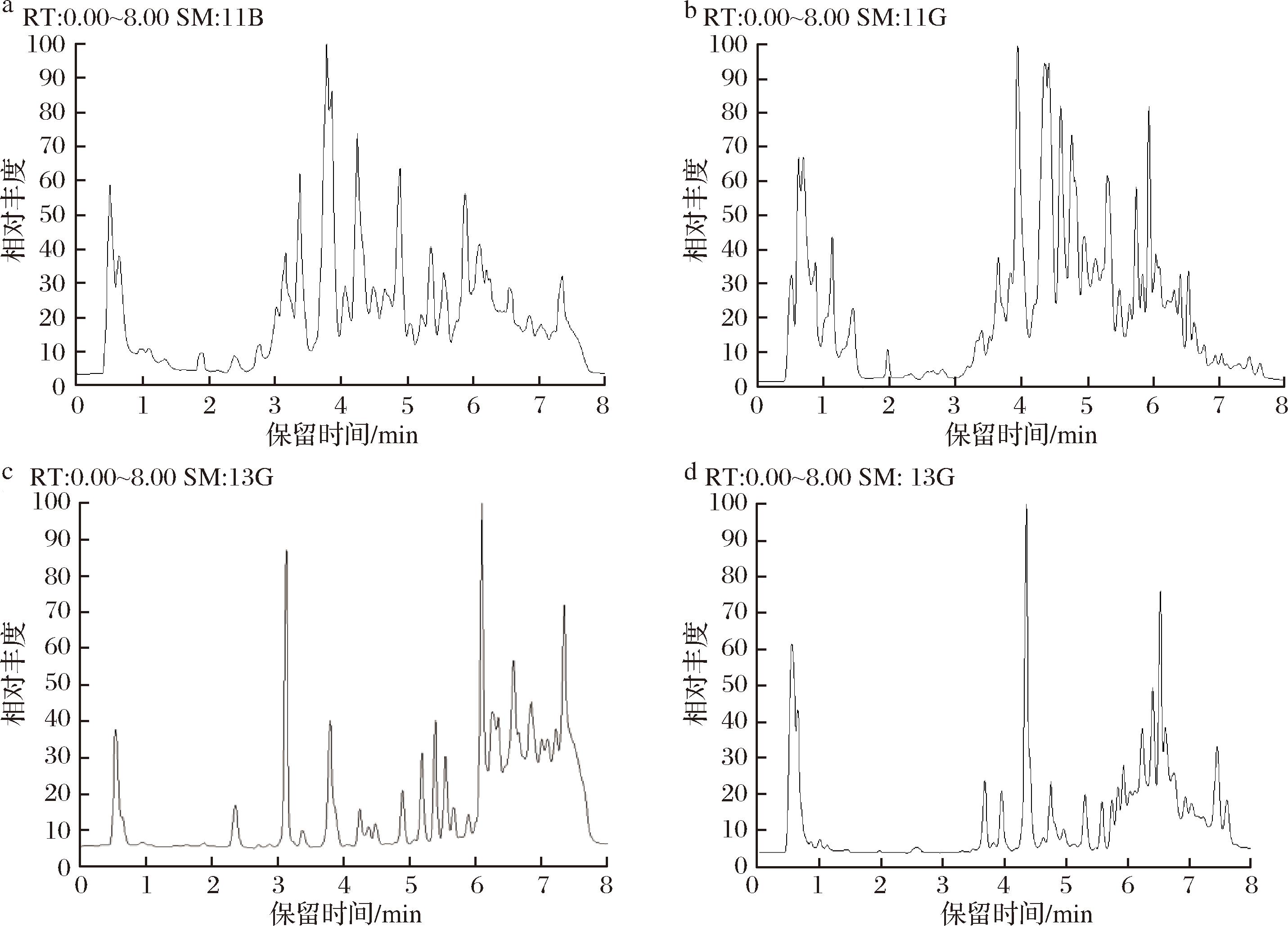
a-葛根提取液正离子模式;b-葛根提取液负离子模式;c-葛根垂钓洗脱液正离子模式;d-葛根垂钓洗脱液负离子模式
图4 葛根提取液及垂钓洗脱液总离子流图
Fig.4 TIC of Pueraria lobata root extract and ligand fishing eluate samples
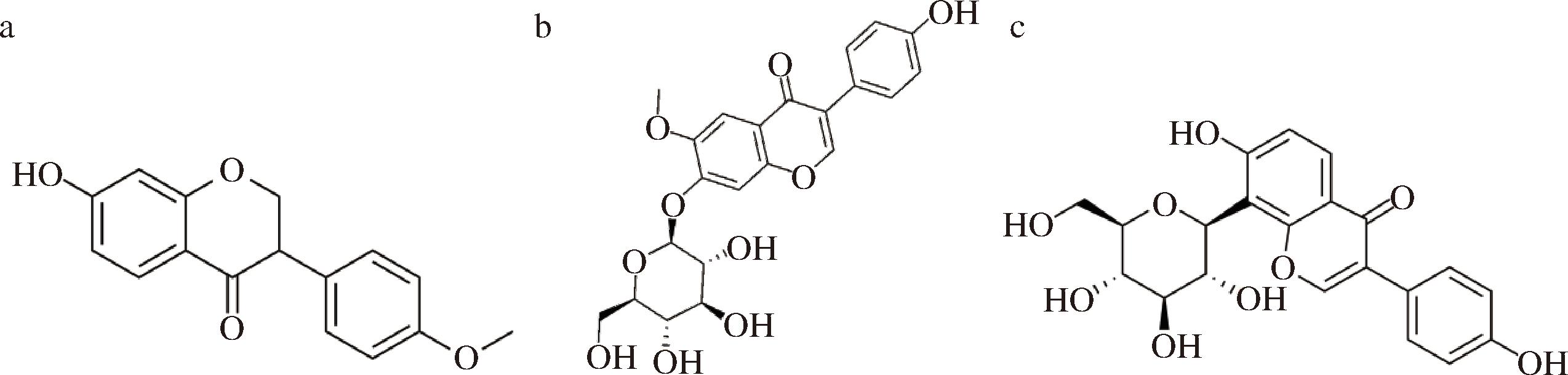
a-刺芒柄花素;b-黄豆黄素苷;c-葛根素
图5 刺芒柄花素、黄豆黄素苷、葛根素的分子结构
Fig.5 Molecular structures of formononetin, glycitin, and puerarin
2.3 分子对接结果
将生成尿酸的底物黄嘌呤、次黄嘌呤[20],阳性对照药别嘌呤醇以及筛选所得化合物与XOD进行分子对接模拟,通常结合能小于0 kcal/mol表明结合过程可自发进行,结合能小于-5.0 kcal/mol表明配体与受体之间存在较强的结合亲和力[21],结合能越低表明结合过程中释放的能量越多,说明其具备更强的结合亲和力[22]。对接结果如表2所示,图6为部分分子对接可视图。
表2 分子对接结果表
Table 2 Table of molecular docking results

配体蛋白结合能/(kcal/mol)氢键疏水相互作用H-π共轭刺芒柄花素-9.9LYS:1 045、ALA:1 078、SER:1 080、THR:1 083ALA:910、ARG:912、GLN:1 040、ALA:1 078—黄豆黄素苷-9.8ASN:272、THR:609、HIS:683、ASN:830PHE:270、ASN:830、ARG:1 222、HIS:683、THR:609PHE:270、ARG:1 222芒柄花苷-9.8ARG:32、THR:25、CYS:73、ARG:233、GLU:23、GLU:676、HIS:683、ASN:272THR:25、MET:268、LYS:269、ASN:272、ARG:680LYS:269、MET:268、ARG:680、ARG:233染料木素-9.7PHE:798、LYS:1045、SER:1 080、THR:1 083、GLY:1 260—GLN:1 040、SER:1 080染料木苷-9.6GLU:23、THR:25、ARG:32、ARG:233、LYS:269、ASN:272、GLU:676LYS:269、ASN:272、ARG:680、VAL:684、GLU:23、ARG:233、GLU:676HIS:683、ARG:680、ARG:233、LYS:269黄豆苷-9.6ALA:338、THR:354、LYS:422、SER:425、LYS:1 228PHE:337、ALA:338、ASN:351、LYS:1 228PHE:337β-谷甾醇-9.4—LYS:57、ASP:59、ILE:66、HIS:82、PRO:224、TRP:283、ASN:288—豆甾醇-9.3ALA:304、SER:307ASP:59、ILE:66、PRO:224、TRP:283、ASN:288、TYR:58、HIS:82—葛根素-9.1GLU:23、ARG:32、ARG:233、LYS:269、ARG:680LEU:27、ALA:28、LEU:41、GLU:676—黄豆苷元-9.0PHE:798、MET:1 038、ALA:1 079、GLN:1 194、GLU:1 261PHE:798、ALA:1 078、GLU:1 261—毛蕊异黄酮-8.6ARG:880、THR:1 010、GLU:1 261、GLU:802LEU:648、LEU:873、PHE:914、VAL:1 011、LEU:1 014、ALA:1 079PHE:1 009、PHE:914、ALA:1 079、LEU:648、LEU:873、LEU:1 014咖啡酸-8.4ARG:880、THR:1 010、VAL:1 011ALA:1 079、GLU:1 261、PHE:914、PHE:1 009ALA:1 079、PHE:914、PHE:1 009阿魏酸-7.6THR:1 010、VAL:1 011LEU:873、PHE:914、LEU:1 014、ALA:1 078ALA:1 079、PHE:1 009、PHE:914棕榈酸-7.0ARG:880、THR:1 010PHE:798、ARG:912、PHE:914、PHE:1 009、ALA:1 078、GLU:1 261—别嘌呤醇-6.9ARG:880、THR:1 010、GLU:802PHE:914, PHE:1 009, ALA:1 079PHE:914黄嘌呤-6.8GLU:802、ARG:880、THR:1 010、ALA:1 079PHE:914、VAL:1 011、LEU:1 014VAL:1 011、OHE:1 009、PHE:9142-羟基肉桂酸-6.6ARG:912、SER:1 080、ALA:1 079PHE:798、GLU:1 261ARG:912次黄嘌呤-6.2GLY:797、PHE:798、MET:1 038、GLN:1 194PHE:798、MET:1 038ARG:912、PHE:798、CYS:150、MET:1 038
注:—表示无数据。

a-黄嘌呤与XOD的分子对接及二维图谱;b-次黄嘌呤与XOD的分子对接及二维图谱;c-刺芒柄花素与XOD的分子对接及二维图谱;d-黄豆黄素苷与XOD的分子对接及二维图谱;e-芒柄花苷与XOD的分子对接及二维图谱;f-染料木素与XOD的分子对接及二维图谱
图6 部分分子对接图及二维作用图谱
Fig.6 Partial molecular docking pose visualization and 2D ligand-protein interaction diagrams
2.3.1 别嘌呤醇的抑制机制
分子对接分析表明,黄嘌呤、次黄嘌呤和阳性对照药别嘌呤醇与XOD的结合能分别为-6.8、-6.2、-6.9 kcal/mol,其中别嘌呤醇表现出最强的结合亲和力。因此,别嘌呤醇优先与XOD结合,从而竞争性抑制黄嘌呤、次黄嘌呤与XOD结合,从而降低尿酸生成。三者的结合机制均依赖氢键、疏水作用及H-π共轭的协同效应,但关键结合残基及模式存在显著差异:黄嘌呤与别嘌呤醇均通过与XOD活性位点的关键催化残基GLU:802和ARG:880形成氢键网络而实现结合,此外二者与PHE:914残基间的疏水作用及H-π共轭效应亦是稳定其复合物构象的共同特征;而次黄嘌呤则通过独特残基(如PHE:798和MET:1 038)实现结合,其较弱结合能可能与疏水界面较小及非保守氢键参与有关;别嘌呤醇与XOD的结合能高于黄嘌呤与XOD的结合能,充分表明其能有效抑制尿酸生成。别嘌呤醇对XOD活性位点具有更高的亲和力,其通过与天然底物黄嘌呤(-6.8 kcal/mol)和次黄嘌呤(-6.2 kcal/mol)竞争性地结合酶的催化中心,从而有效抑制了由黄嘌呤至尿酸的酶促反应,从源头阻断了尿酸的生成。
2.3.2 异黄酮类成分的抑制机制
分子对接结果显示,异黄酮类化合物与XOD的结合能(-8.6~-9.9 kcal/mol)均显著低于别嘌呤醇(-6.9 kcal/mol),其中刺芒柄花素结合能最低(-9.9 kcal/mol),抑制潜力最强。这些化合物通过差异化的结合模式与XOD相互作用:刺芒柄花素和染料木素主要结合于钼蝶呤辅因子附近的LYS:1 045、SER:1 080区域,可能直接阻断催化中心;而芒柄花苷、染料木苷等则通过糖基介导的多元氢键与ARG:32、ASN:272等入口通道残基结合,形成更广泛的相互作用网络。此外,疏水空腔(如PHE:270、337)和H-π共轭(如黄豆黄素苷与PHE:270)的协同作用进一步稳定了复合物结构。
总结其构效规律,葛根提取物抑制XOD活性的构效关系揭示了多层级的作用机制,其核心在于苯并吡喃-4-酮母核结构、氢键位点以及糖基化位置三者的精密协同。根据刺芒柄花素、黄豆黄素苷以及葛根素的分子结构来看(图5),刺芒柄花素凭借其A环的7-羟基与C环的4-羰基,可与Glu:802、Thr:1 010和Arg:880形成稳定的氢键网络,其活性显著高于糖基化屏蔽了羟基的葛根素;恰当的糖基化,如黄豆黄素苷在C7位连接糖基可通过与Asn:768产生额外氢键增强结合,但取代位点不当,如葛根素在C8位连接糖基,此位置深处于母核平面附近,庞大的糖基会产生显著的空间位阻,干扰了异黄酮母核理想地嵌入疏水口袋的路径,从而导致其结合能力被大幅削弱。
2.3.3 植物甾醇类成分的抑制机制
β-谷甾醇与豆甾醇的结合能分别为-9.4、-9.3 kcal/mol,分子对接结果表明,该类化合物主要通过疏水相互作用,高效抑制XOD活性。该类分子以其刚性甾环结构,精准嵌入由XOD中ASP:59、ILE:66、PRO:224、TRP:283、ASN:288和HIS:82等残基共同围成的疏水结合口袋,通过显著的空间匹配和疏水相互作用实现高稳定性结合。特别地,豆甾醇在疏水结合的基础上,还借助ALA:304与SER:307残基形成氢键,进一步强化了结合的位点选择性;而β-谷甾醇则完全经由疏水作用实现优异的亲和力,成为一类典型的疏水驱动型抑制剂。
该结合特性阐明了一类区别于别嘌呤醇等传统竞争性抑制剂的新型变构抑制机制。由于植物甾醇的结合位点远离钼蝶呤催化中心的疏水区域,提示其可能通过诱导XOD构象变化,以变构调控方式间接影响底物通道或催化微环境,进而阻断尿酸生成。这一发现不仅从分子层面揭示了植物甾醇降尿酸的作用机理,也为以变构抑制为核心的新一代XOD抑制剂的筛选奠定了科学基础。不仅提供了具有潜力的先导分子,更在药物设计思路上开辟了新途径,有望克服现有疗法中普遍存在的耐药性及毒副作用问题。
2.3.4 酚酸类成分的抑制机制
植物酚酸类化合物通过其特有的结构特征与XOD活性区域发生多模式相互作用,从而实现抑制酶活性和发挥降尿酸的作用。从分子对接结果来看,咖啡酸表现出最强的结合能力(-8.4 kcal/mol),其抑制机制主要通过酚羟基和羧基与ARG:880、THR:1 010和VAL:1 011形成关键氢键网络,同时其苯乙烯基骨架与PHE:914、PHE:1 009和ALA:1 079产生显著的疏水作用和H-π堆叠效应;阿魏酸(-7.6 kcal/mol)在咖啡酸结构基础上引入甲氧基,虽一定程度上增强疏水作用,但可能因位阻效应略微降低氢键结合能力,导致总体结合能弱于咖啡酸;2-羟基肉桂酸(-6.6 kcal/mol)仅具单酚羟基结构,其氢键相互作用较少(仅与ARG:912、SER:1 080等结合),疏水作用和H-π效应也较弱,因此结合能相对最低。
总体而言,这类化合物的抑制效能与其酚羟基数量、取代基类型及共轭体系密切相关:邻二酚羟基结构(如咖啡酸)可形成更强氢键网络,且共轭骨架与PHE:914、1 009等芳香残基的H-π堆叠是维持高亲和力的关键。这些化合物均直接结合于XOD的底物催化区域,表明其可能作为竞争性抑制剂阻断黄嘌呤的氧化过程,从而从源头上减少尿酸生成。该发现不仅揭示植物酚酸类降尿酸的作用机理,也为基于天然酚酸结构优化开发新型XOD抑制剂提供了重要依据。
2.3.5 脂肪酸类成分抑制机制
分子对接结果表明,棕榈酸通过亲水片段结合与疏水尾部协同抑制机制有效抑制XOD。其羧基与活性中心关键残基ARG:880和THR:1 010形成氢键,实现特异性结合;C16烷烃链则与PHE:914、PHE:1 009及ALA:1 078等疏水残基产生广泛疏水作用,共同使其结合能(-7.0 kcal/mol)优于别嘌呤醇(-6.9 kcal/mol),表明棕榈酸可以作为一种竞争性XOD抑制剂。
该机制不仅阐明长链脂肪酸通过占据活性中心减少尿酸合成的结构基础,也为新型抑制剂设计提供了策略方向。例如,可将高效抑制基团与柔性烷链耦合,协同优化氢键与疏水效应,从而开发具有高亲和力和成药性的新一代降尿酸先导化合物。
2.3.6 配体垂钓技术有效性验证
综合分析表明,配体垂钓技术成功地从葛根提取物中富集到一系列与XOD具有超强结合能力的活性成分,其结合能整体显著优于底物及阳性对照药物别嘌呤醇,充分验证了该筛选方法的高效性和可行性。分子对接结果不仅揭示葛根是极具开发潜力的XOD抑制剂宝库,其中刺芒柄花素、黄豆黄素苷和芒柄花苷等成分表现出卓越的结合亲和力,预示它们可能是远超别嘌呤醇的新型高效抑制剂先导化合物,而且为后续研究提供了明确方向:这些高活性成分应优先进行体外酶活性抑制验证、细胞模型测试及体内药效学评价。本研究最终证实,配体垂钓技术能够高效锁定葛根中的强效XOD结合成分,该策略不仅为抗高尿酸血症功能食品或药物的开发提供了坚实的理论依据和重要的先导化合物线索,同时也凸显了配体垂钓技术在中药现代化研究中具有重要的应用价值。
3 讨论
本研究通过合成固定化XOD的MNPs,实现了XOD活性基团配体在磁性金属纳米粒子表面的修饰。通过系统性的结构表征,证实了所合成的MNPs可有效应用于XOD抑制剂的筛选。利用该平台对葛根提取液进行筛选,成功鉴定出15种潜在XOD抑制剂成分。并对底物黄嘌呤、次黄嘌呤,阳性对照药物别嘌呤醇及筛选所得化合物与XOD进行分子对接研究。结果表明,这些活性成分能够有效结合于XOD的活性位点,且结合能均优于底物黄嘌呤、次黄嘌呤以及阳性对照药物别嘌呤醇。
研究结果揭示了葛根提取物中活性成分抑制XOD活性的构效关系与分子机制:高效抑制剂需具备苯并吡喃-4-酮母核及多位游离酚羟基等关键药效特征,其活性依赖于氢键网络、疏水作用和H-π堆叠的协同效应。进一步阐明葛根提取物中活性成分存在2种抑制机制:一类为基于活性中心结合的竞争性抑制(如异黄酮类、酚酸类、棕榈酸);另一类为新型变构抑制(如植物甾醇),通过结合远端疏水空腔间接调控酶活性。该发现不仅揭示了天然产物的降尿酸本质,更为开发兼具高亲和力与新作用机制、能够克服现有药物耐药性问题的新一代XOD抑制剂提供了关键理论基础和结构设计方向。
这些发现为XOD抑制剂的结构优化及靶向设计提供了分子层面的理论依据,同时也为葛根资源的高效利用奠定了理论基础。与常规方法相比,本研究成功建立了一种快速、简便的分析方法,通过将固定化XOD与UPLC-Q-TOF-MS/MS联用,实现了XOD抑制剂的鉴定与表征。所制备的MNPs与XOD的偶联物展现出良好的选择性和稳定性。该方法被证明可有效从复杂天然产物混合物中鉴定生物活性化合物,因此具有应用于新型XOD抑制剂及其他修饰药物制剂鉴定的潜力。
[1] CRAWLEY W T, JUNGELS C G, STENMARK K R, et al. U-shaped association of uric acid to overall-cause mortality and its impact on clinical management of hyperuricemia[J]. Redox Biology, 2022, 51:102271.
[2] YU W C, LIU J R, BARANENKO D, et al. The role of dietary polysaccharides in uric acid regulation: Mechanisms and benefits in managing hyperuricemia[J]. Trends in Food Science &Technology, 2025, 157:104902.
[3] GA Y, WEI Y Y, ZHAO Q Y, et al. Puerariae Radix protects against ulcerative colitis in mice by inhibiting NLRP3 inflammasome activation[J]. Food Science and Human Wellness, 2024, 13(4):2266-2276.
[4] 任玲玲, 张迟, 曾金祥, 等. 降尿酸中药药效物质筛选方法学研究进展[J]. 中国实验方剂学杂志, 2019, 25(18):227-234.REN L L, ZHANG C, ZENG J X, et al. Methodology for screening effective substances of Chinese herbal medicine for reducing serum uric acid level[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2019, 25(18):227-234.
[5] QIN Y, YAN Y, ZHOU J, et al. Advancements in screening systems for active ingredients in traditional Chinese medicines using ligand fishing technique[J]. TrAC Trends in Analytical Chemistry, 2024, 180:117983.
[6] ZHU H E, TAO J, WANG W H, et al. Magnetic, fluorescent, and thermo-responsive Fe3O4/rare earth incorporated poly(St-NIPAM) core-shell colloidal nanoparticles in multimodal optical/magnetic resonance imaging probes[J]. Biomaterials, 2013, 34(9):2296-2306.
[7] WAGSTAFF A J, BROWN S D, HOLDEN M R, et al. Cisplatin drug delivery using gold-coated iron oxide nanoparticles for enhanced tumour targeting with external magnetic fields[J]. Inorganica Chimica Acta, 2012, 393:328-333.
[8] TANG Y T, FENG F, XU G H, et al. Providing insight into exchange coupling within nanomagnetism: Mechanism, micromagnetic simulation, synthesis and biomedical application[J]. Science China Materials, 2024, 67(10):3049-3082.
[9] JIANG F Y, FU Y, ZHU Y, et al. Fabrication of iron oxide/silica core-shell nanoparticles and their magnetic characteristics[J]. Journal of Alloys and Compounds, 2012, 543:43-48.
[10] BU M, MA W Z. Study on core-shell-shell structured nanoparticles with magnetic and luminescent features: Construction, characterization and oxygen-sensing behavior[J]. Journal of Luminescence, 2013, 141:80-86.
[11] PASTUKH O, ADAMEK M, LASKOWSKA M, et al. Surface anchoring of Mn12-stearate single-molecule magnets on variable-diameter silica nanospheres: Implications for magnetic signal amplification[J]. Applied Surface Science, 2026, 715:164550.
[12] WANG T, LI D P, YU B Y, et al. Screening inhibitors of xanthine oxidase from natural products using enzyme immobilized magnetic beads by high-performance liquid chromatography coupled with tandem mass spectrometry[J]. Journal of Separation Science, 2017, 40(9):1877-1886.
[13] DENG X, SHI S Y, LI S M, et al. Magnetic ligand fishing combination with high-performance liquid chromatography-diode array detector-mass spectrometry to screen and characterize cyclooxygenase-2 inhibitors from green tea[J]. Journal of Chromatography. B, Analytical Technologies in the Biomedical and Life Sciences, 2014, 973C: 55-60.
[14] 吴江渝, 许谦, 李竹, 等. 磁性二氧化硅纳米粒子的制备及性能[J]. 武汉工程大学学报, 2014, 36(7):43-47.WU J Y, XU Q, LI Z, et al. Preparation and properties of magnetic silica nanoparticles[J]. Journal of Wuhan Institute of Technology, 2014, 36(7):43-47.
[15] 邹惠亮, 陈柯, 王新财, 等. 土茯苓中黄嘌呤氧化酶抑制剂筛选鉴定研究[J]. 中成药, 2024, 46(5):1558-1564.ZOU H L, CHEN K, WANG X C, et al. Screening and identification of xanthine oxidase inhibitors from Smilax glabra[J]. Chinese Traditional Patent Medicine, 2024, 46(5):1558-1564.
[16] 龚频, 翟鹏涛, 张梦璇, 等. 野葛总黄酮的提取工艺优化及抗氧化活性研究[J]. 中国酿造, 2022, 41(10):172-176.GONG P, ZHAI P T, ZHANG M X, et al. Optimization of extraction process of total flavonoids from Pueraria lobata and its antioxidant activity[J]. China Brewing, 2022, 41(10):172-176.
[17] SONG D N, ZHAO H H, WANG L L, et al. Ethanol extract of Sophora japonica flower bud, an effective potential dietary supplement for the treatment of hyperuricemia[J]. Food Bioscience, 2023, 52:102457.
[18] 张帆, 王薇, 曹颖, 等. 基于配体垂钓技术筛选三七叶中环氧合酶-2抑制剂[J]. 色谱, 2024, 42(12):1126-1135.ZHANG F, WANG W, CAO Y, et al. Screening of cyclooxygenase-2 inhibitors in Panax notoginseng leaves based on ligand fishing technique[J]. Chinese Journal of Chromatography, 2024, 42(12):1126-1135.
[19] 宋敏杰.基于配体垂钓筛选蓝点马鲛鱼肉蛋白中的黄嘌呤氧化酶抑制肽[D]. 锦州: 渤海大学,2020.SONG M J. Screening of xanthine oxidase inhibitor peptides from Scomberomorus niphonius protein based on ligand fishing[D]. Jinzhou: Bohai University,2020.
[20] GROVE A. The delicate balance of bacterial purine homeostasis[J]. Discover Bacteria, 2025, 2(1):14.
[21] YANG M, LIU J C, GUO T, et al. Exploration of the mechanism of Tripterygium wilfordii in the treatment of myocardial fibrosis based on network pharmacology and molecular docking[J]. Current Computer-Aided Drug Design, 2023, 19(1):68-79.
[22] NEETHA S, SANTHOSH C, VINAY KUMAR D C, et al. Synthesis, structure elucidation, DFT, molecular docking studies, and antioxidant activities of thiazole derivative: A combined experimental and computational study[J]. Journal of Molecular Structure, 2025, 1348:143430.