乳液是由2种不相容的液体组成的分散体系,在化妆品、食品和制药等领域有着广泛的研究应用,因此乳液的稳定性对于维持其性能具有至关重要的作用。传统乳液依赖于表面活性剂进行稳定,易受环境条件(如pH、温度和离子强度)的影响[1],这在一定程度上限制了其实际应用[2]。皮克林乳液是一种新型的乳液体系,其以固体颗粒作为稳定剂吸附在油水界面形成一层致密的膜,产生较大的空间位阻,具有比传统乳液更高的稳定性[3]。
目前皮克林乳液的稳定剂主要为二氧化硅和氧化锌等无机颗粒,易造成食品安全的问题[4]。因此,开发天然、环保、可生物降解的食品级颗粒作为皮克林乳液的稳定剂具有重要意义。现阶段,多糖基颗粒、蛋白基颗粒和脂肪晶体颗粒已得到广泛的研究和应用[5],其中常见的食品级蛋白基颗粒主要来源于玉米醇溶蛋白、大豆球蛋白、豌豆蛋白和乳清蛋白等[4,6-9],对利用蛋清蛋白(egg-white proteins,EWP)制备皮克林乳液的研究较少。EWP因其均衡的必需氨基酸组成、高消化率以及优异的凝胶特性和乳化特性成为食品科学领域的研究热点[10-11]。EWP独特的两亲性结构和优良的乳化特性,使其能够有效吸附于油-水界面,形成稳定的界面膜[12-14],但其在极端条件下易发生蛋白质的解折叠,导致界面的吸附能力下降,因此需要经过改性修饰以增强分子相互作用力与改善内部结构。碱诱导能促进蛋白质三级结构的展开,暴露出包裹在蛋白质内部的疏水基团,从而增强蛋白质表面疏水性,赋予其在油水界面良好的稳定性[15]。近年来,多酚介导的蛋白质交联策略为调控蛋白纳米结构提供了新思路[16],但对于不同碱结合多酚在蛋清颗粒制备及其乳液稳定机制中的应用尚未深入探索。
本研究基于NaOH诱导结合Ca(OH)2与茶多酚(tea polyphenol,TP)制备蛋清凝胶微颗粒,通过测定蛋清凝胶微颗粒平均粒径、zeta电位、表面疏水性和内源性荧光等表征其理化特性及结构变化。将所制备的蛋清凝胶微颗粒用于稳定皮克林乳液,并评价了其对乳液的稳定性。本研究为基于蛋清凝胶微颗粒的皮克林乳液设计提供新思路,推动其在功能性食品和抗氧化方面的应用,为EWP的加工和食品产业的创新发展提供了新方向。
1 材料与方法
1.1 材料与试剂
新鲜鸭蛋,质量55~65 g,广州市长湴市场;TP,纯度(>98%),上海梦泽生物科技有限公司;NaOH、Ca(OH)2、HCl、Na2HPO4,分析纯,广州化学试剂厂;8-苯氨基-1-萘磺酸铵盐(ammonium salt of 8-phenylamino-1-naphthalene sulfonate,ANS),分析纯,美国Sigma-Aldrich公司;尿素(CON2H4),分析纯,天津化学试剂厂;考马斯亮蓝G-250生化试剂,上海伯奥生物技术有限公司;NaH2PO4,分析纯,天津市大茂化学试剂厂。
1.2 仪器与设备
RF-5301PC荧光分光光度计、UV-2600紫外分光光度计,日本岛津公司;ZETASIZER NANO ZSP纳米粒度电位仪,英国Malvern Instruments公司;MCR301流变仪,奥地利Anton Paar公司;DGJ-10C真空冷冻干燥机,上海博登生物科技有限公司;KYKY-EM8000扫描电镜,北京中科科仪股份有限公司;scientz-150高压均质机,宁波新芝生物科技股份有限公司。
1.3 实验方法
1.3.1 蛋清凝胶微颗粒和皮克林乳液的制备
新鲜鸡蛋洗净后将蛋清和蛋黄分离,其中蛋清溶液用磁力搅拌器分散15 min。测定EWP含量,调整蛋白质质量分数至10%。称取20 g蛋清,分别加入0.57% NaOH、0.57% NaOH+0.015% Ca(OH)2、0.57% NaOH+0.04% TP、0.57% NaOH+0.015% Ca(OH)2+0.04% TP制备蛋清凝胶(均为质量分数)。将制备好的蛋清凝胶捣碎,并按照料液比1∶3(g∶mL)混合蒸馏水后,用分散机在6 000 r/min下分散3 min,调整蛋白质质量分数为2%,并加入质量分数为0.02%的叠氮钠在10、30、50 MPa下均质循环3次。将处理得到的蛋清凝胶微颗粒置于4 ℃冰箱中贮藏备用,按照上述凝胶顺序制备的蛋清凝胶微颗粒分别命名为NA-P-10、NA-P-30、NA-P-50、CA-P-10、CA-P-30、CA-P-50、TP-P-10、TP-P-30、TP-P-50,TC-P-10、TC-P-30、TC-P-50。
将质量分数为2%的凝胶微颗粒用蒸馏水稀释至1.0%,然后将在50 MPa下均质得到的蛋清凝胶微颗粒与玉米油按照1∶1的体积比混合,使用配备12 mm直径探头的分散机在10 000 r/min下分散2 min,制备好的乳液在4 ℃条件下贮存,并依次命名为NA-PE、CA-PE、TP-PE、TC-PE。
1.3.2 蛋清凝胶微凝胶颗粒粒径和zeta电位的测定
将凝胶微颗粒浓度用蒸馏水稀释至1%(粒度分布,质量分数)和0.1%(zeta电位,质量分数),收集数据前在仪器内平衡120 s,25 ℃下至少连续读数12次。平行测定3次后计算zeta电位和平均粒径。
1.3.3 蛋清凝胶微凝胶颗粒浊度的测定
参考CHANG等[17]的方法,将制备的凝胶微颗粒用50 mmol/L PBS(pH 7.0)稀释至1 mg/mL,测定其在500 nm处的吸光度,将凝胶微颗粒分别用1 mol/L NaCl、30 mmol/L二硫苏糖醇(dithiothreitol,DTT)、0.017 3 mol/L十二烷基硫酸钠(sodium dodecyl sulfate,SDS)、6 mol/L尿素溶液稀释至蛋白质质量浓度为1 mg/mL静置10 min后再测定其透光率。
1.3.4 蛋清凝胶微凝胶颗粒内源性荧光的测定
参照邵贝贝等[18]的方法,使用荧光分光光度计测定凝胶微颗粒的内源性荧光。将样品质量浓度用PBS稀释至1 mg/mL,激发波长分别设置为295 nm与258 nm,发射波长为300~450 nm,狭缝宽度设定为5 nm,扫描速度为120 nm/s,扫描温度为25 ℃。
1.3.5 蛋清凝胶微凝胶颗粒表面疏水性的测定
采用AI等[19]研究中描述的方法测定凝胶微颗粒的表面疏水性。将样品质量浓度用PBS稀释成0.1 mg/mL,荧光光度计在280 nm激发波长下扫描300~500 nm的内源性荧光光谱,扫描速度为5 nm/s,狭缝矫正5 nm。
1.3.6 蛋清凝胶微凝胶颗粒的扫描电子显微镜
参照许瑞[20]的方法,使用扫描电子显微镜对蛋清凝胶微颗粒的形貌进行观察。取稀释后的微颗粒分散体滴在硅片上,用氮气吹干。用导电胶将硅片固定在样品台上,喷金后利用扫描电镜观察微颗粒的微观形态。
1.3.7 皮克林乳液粒径的测定
制备好的乳液通过粒度分析仪测定粒径。其参数如下所示:颗粒吸收率为0.001,颗粒折射率为1.470,分散剂折射率为1.330,分散剂为蒸馏水。实验结果采用体积平均直径D4,3和面积平均直径D3,2来表示,设置样品自动测试3次。
1.3.8 皮克林乳液外观和微观结构的测定
通过观察乳液液滴在贮存0 d和15 d的界面(乳液层与水层)位置变化情况,表征乳液的乳析稳定性。将新鲜制备的乳液注入样品瓶中,室温下贮存15 d拍摄乳液外观变化。将各乳液样品适当稀释,然后取一滴稀释乳液滴在载玻片上,使用光学显微镜观察记录。
1.3.9 皮克林乳液流变特性的测定
皮克林乳液黏度的测定使用探头为CP50(直径为50 mm),吸取1 mL乳液样品滴于测试平台上,使探头缓慢下降完全覆盖样品。黏度扫描条件如下:剪切速率为0.1~100 rad/s,温度为25 ℃,振幅γ设置为2%。频率扫描条件如下:在线性黏弹范围内进行,扫描范围为1~100 rad/s,应变为0.2%。
1.4 数据分析
所有测试均进行3次,结果以“平均值±标准差”报告。根据单因素方差分析(analysis of variance,ANOVA),采用Duncan’s multiple range test来确定均值之间的差异,显著性设定为P<0.05。
2 结果与分析
2.1 蛋清凝胶微颗粒的粒径分布变化
粒径是影响皮克林乳液稳定性的一个重要因素[6]。蛋清凝胶在不同均质压力下所制备微颗粒的粒径分布如图1所示,所制备的蛋清凝胶通过化学作用力交联,均质后形成不同粒径大小的微颗粒,除CA-P-10、TP-P-50、TC-P-50出现了2个峰以外,所有的微颗粒粒径均呈现单峰分布。值得注意的是,随着均值压力增大,微颗粒粒径变小,且微颗粒的粒径分布峰变宽。均质压力的增大会产生高剪切应力,破坏蛋白肽键的连接,影响蛋白质之间的相互作用,导致蛋白质聚集体分散成更小的微颗粒[21-22],这也是TP-P-50和TC-P-50的粒径分布出现2个峰的原因。相比之下,低压均质形成的颗粒尺寸较均一,高压均质会产生强烈的空化剪切效应,诱导部分凝胶微颗粒进一步破碎为更小的颗粒,导致微颗粒的粒径分布峰变宽[23]。
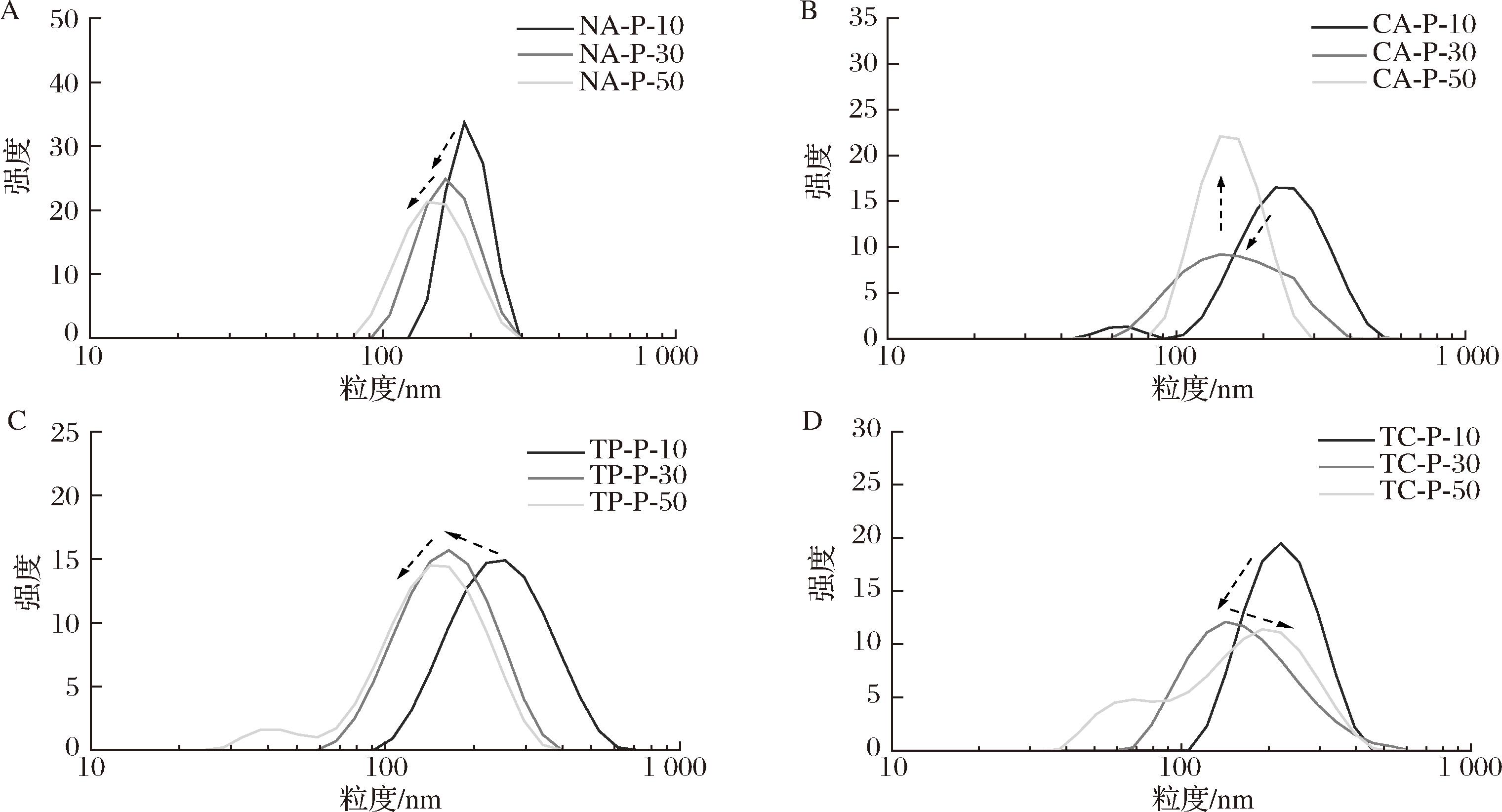
A-NA-P组的粒径分布;B-CA-P组的粒径分布;C-TP-P组的粒径分布;D-TC-P组的粒径分布
图1 不同蛋清凝胶微颗粒的粒度分布
Fig.1 Particle size distribution of different EWG microparticles
2.2 蛋清凝胶微颗粒的zeta电位和平均粒径的变化
图2显示了不同蛋清凝胶制备的微颗粒的zeta电位和平均粒径的变化。如图2-A所示,所有微颗粒的zeta电位绝对值均大于30 mV,表明微颗粒均能很好地抵抗静电吸引以维持其稳定性[24]。在30 MPa的均质压力下,微颗粒的电位变化不显著(P>0.05)。在50 MPa的均质压力下,与NA-P组相比,CA-P组、TP-P组和TC-P组的zeta电位绝对值显著降低(P<0.05),且TC-P组的zeta电位绝对值大于TP-P组(P<0.05)。高压均质后暴露出蛋白质表面的羧酸基团(如天冬氨酸、谷氨酸的侧链),其与Ca2+结合中和了部分负电荷,导致CA-P组的zeta电位绝对值显著低于NA-P组。而TP-P组和TC-P组蛋白质表面的负电荷被部分屏蔽或重新分布,从而导致zeta电位绝对值较低。
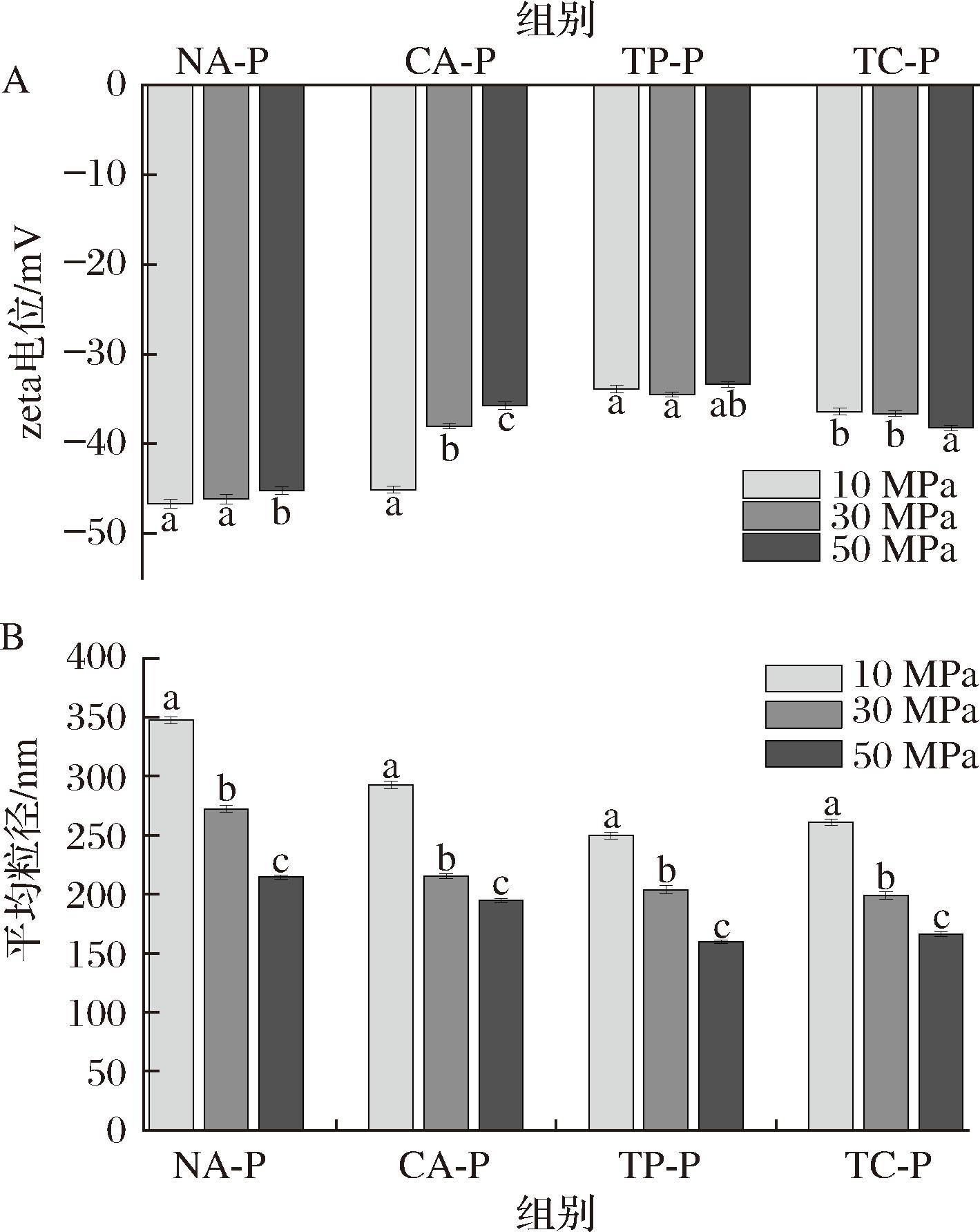
A-不同蛋清凝胶微颗粒的zeta电位;B-不同蛋清凝胶微颗粒的平均粒径
图2 不同蛋清凝胶微颗粒的zeta电位和平均粒径
Fig.2 The zeta potential and average particle size of different EWG microparticles
注:不同小写字母表示差异显著(P<0.05)(下同)。
凝胶微颗粒的平均粒径变化如图2-B所示。所有样品的平均粒径随着均质压力的增大而变小,其中NA-P组的平均粒径最大,CA-P组、TC-P组、TP-P组的平均粒径依次降低,最小值为159.53 nm。与仅添加了NaOH的凝胶微颗粒相比,Ca(OH)2的添加会在凝胶微颗粒中产生非特异性交联。而Ca(OH)2和TP同时加入到蛋清凝胶时,Ca2+会限制TP与蛋白质结合,高压均质能打破非特异性交联与醌和蛋白质之间的相互作用,导致平均粒径变小。此外,在TP-P组中,TP容易氧化生成醌类化合物,再与蛋白质结合形成较弱的网络结构[25],导致该网络结构对外力的抵抗能力较弱,高压均质后形成粒径更小的颗粒。综上所述,在50 MPa的均质压力下所制备的蛋清凝胶微颗粒较小且分布均匀,因此,本研究选择50 MPa的均质压力用于制备皮克林乳液。
2.3 蛋清凝胶微颗粒的浊度变化
通过浊度来测定蛋清凝胶微颗粒分子间作用力如图3所示。NaCl、SDS、尿素、DTT可以依次破坏离子键、疏水相互作用、氢键和二硫键[26-27]。实验结果表明,NA-P组经SDS、尿素和DTT处理后浊度显著下降(P<0.05),表明仅添加NaOH形成的凝胶微颗粒的稳定性主要依靠氢键、疏水相互作用和二硫键。CA-P组经NaCl处理后浊度显著上升(P<0.05),而经SDS、尿素处理后又显著下降(P<0.05),表明CA-P组的稳定性由离子键、疏水相互作用和氢键主导,其中离子键主要是由Ca2+与蛋白质表面的羧基等带电氨基酸残基形成的,这进一步影响蛋白质构象,使疏水基团暴露并通过疏水相互作用聚集,进一步增强蛋白质分子之间的相互作用。TP-P组和TC-P组经SDS、尿素、DTT处理后,浊度均显著下降(P<0.05),表明TP-P组和TC-P组的微颗粒稳定性主要依赖于氢键、疏水相互作用和二硫键。然而,与TP-P组相比,TC-P组离子键占比更高,疏水相互作用占比更少,原因可能是TP和Ca(OH)2两者同时存在时会相互竞争与蛋白质的结合位点,而蛋白质优先与Ca2+结合,从而导致更多的离子键形成。综上所述,蛋清凝胶微颗粒的稳定性由多类化学作用力协同维持,其中CA-P组高度依赖离子键,而NA-P组、TP-P组、TC-P组均由氢键、疏水相互作用和二硫键作用力共同维持。
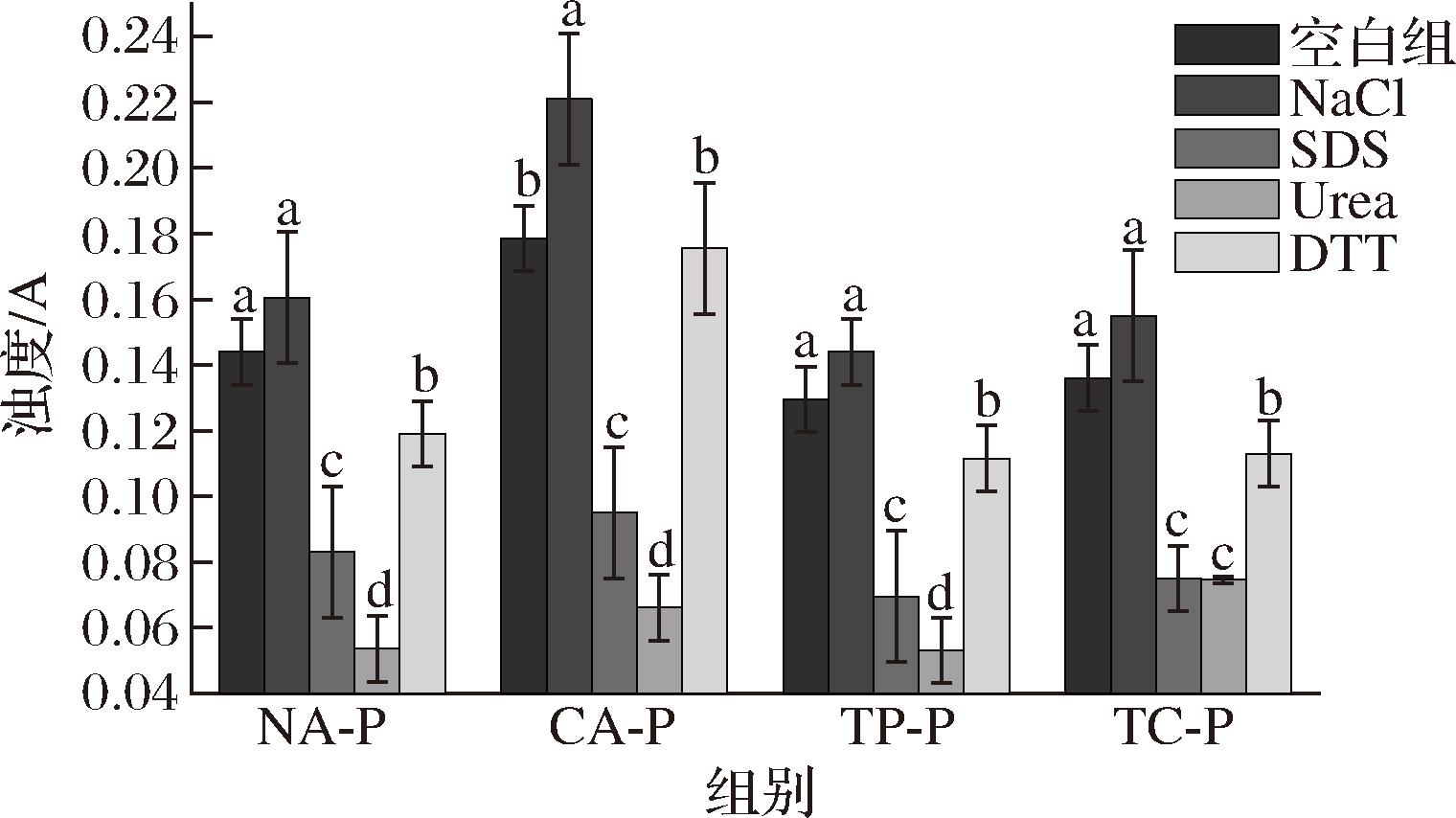
图3 不同蛋清凝胶微颗粒的浊度
Fig.3 Turbidity of different EWG microparticles
2.4 蛋清凝胶微颗粒的SEM
不同处理组凝胶微颗粒(NA-P、CA-P、TP-P、TC-P)在300×放大倍数下的微观结构如图4所示,NA-P组微颗粒显示出粗糙的网络和较大的孔隙,CA-P组微颗粒结构较紧凑均匀,这是由于Ca2+可与蛋白质表面的羧基等带负电基团发生桥联,增强蛋白质之间相互作用,从而形成较均匀网络结构。相比之下,TP容易氧化生成醌类化合物,再与蛋白质结合形成较弱的网络结构,导致TP-P组的结构较松散[28]。值得注意的是,TC-P组中,Ca(OH)2的强交联效应仍占主导,可部分抵消TP对蛋白质交联的干扰,故其微颗粒孔隙结构相较于TP-P组致密,这表明Ca(OH)2能够部分抵消TP对蛋白交联的干扰。

A-NA-P组的微观结构;B-CA-P组的微观结构;C-TP-P组的微观结构;D-TC-P组的微观结构
图4 不同蛋清凝胶微颗粒的微观结构(300×)
Fig.4 Microstructure of different EWG microparticles (300×)
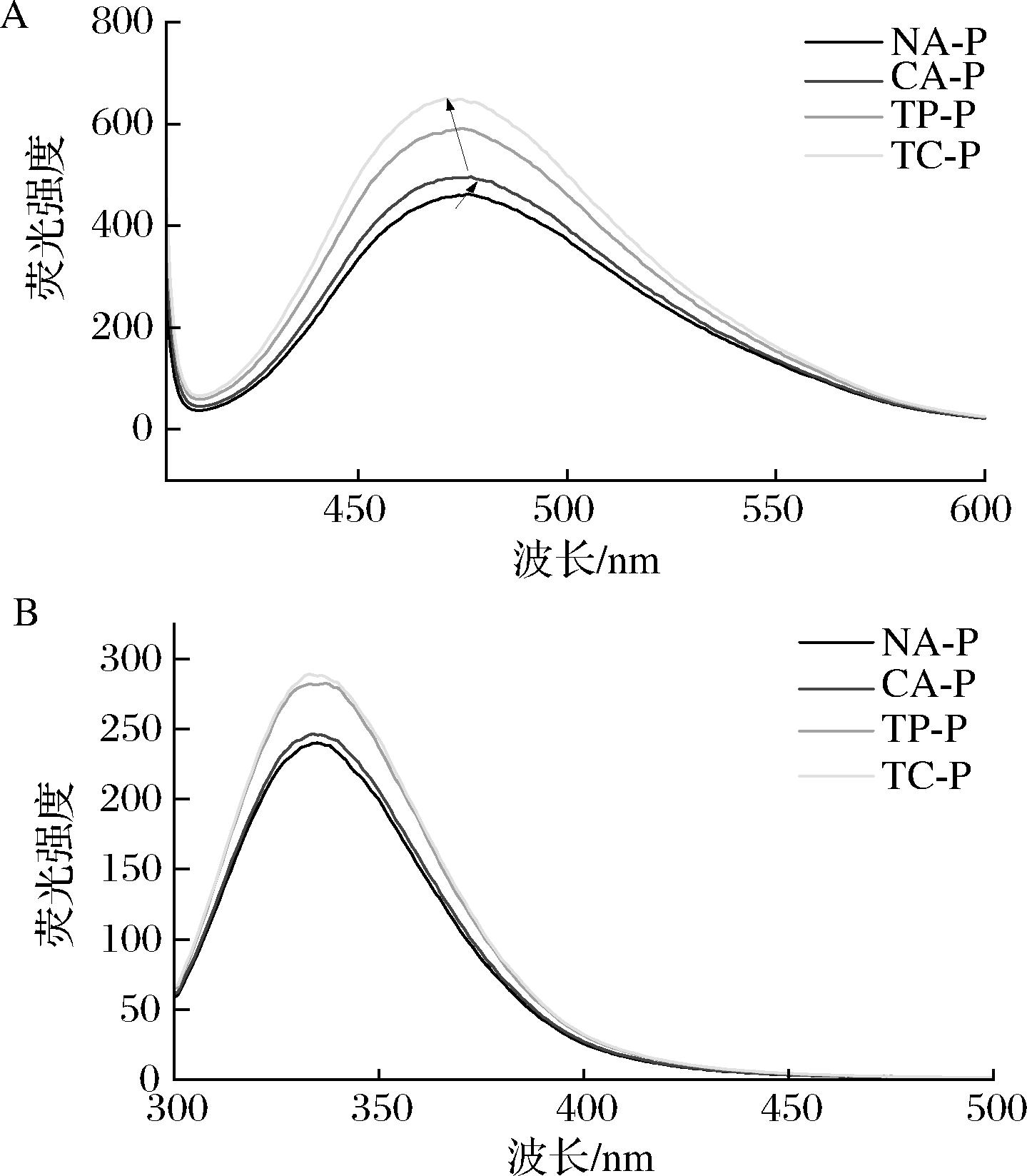
A-不同蛋清凝胶微颗粒的表面疏水性;B-不同蛋清凝胶微颗粒的内源性荧光
图5 不同蛋清凝胶微颗粒的表面疏水性和内源性荧光
Fig.5 Surface hydrophobicity and intrinsic fluorescence of different EWG microparticles
2.5 蛋清凝胶微颗粒的表面疏水性和内源性荧光
不同处理组凝胶微颗粒(NA-P、CA-P、TP-P、TC-P)的表面疏水性变化如图5-A所示,表面疏水性能够反映蛋白质空间结构的变化。单独添加Ca(OH)2和TP均提高了微颗粒的表面疏水性,且两者同时加入时,其表面疏水性峰值达到最高。原因是高压均质会破坏Ca2+与疏水性氨基酸残基之间的相互作用,并促使Ca2+与OH-形成离子键,导致原本被Ca2+覆盖的疏水性氨基酸残基暴露于蛋白质表面。此外,TP易氧化形成醌类化合物,其与蛋白质共价结合暴露出疏水基团导致表面疏水性增强[25]。TC-P组表面疏水性最强,表明Ca(OH)2和TP间存在协同调控作用,使其微颗粒暴露出更多疏水位点。
蛋清凝胶微颗粒的内源性荧光结果如图5-B所示,蛋白质内源性荧光主要来源于芳香族氨基酸,包括色氨酸(Trp)、酪氨酸(Tyr)与苯丙氨酸(Phe)。荧光强度由高到低依次为TC-P组>TP-P组>CA-P组>
NA-P组。NA-P组荧光强度最低,说明仅添加NaOH形成的凝胶网络不稳定,在高压均质下易发生颗粒间团聚,造成荧光物质包埋于内部,暴露程度降低,导致内源性荧光最弱[29]。CA-P组引入Ca2+后,其荧光强度略有提升。根据纪雪花等[30]的研究,Ca2+与蛋白质通过桥联作用形成更稳定的网络结构,这导致其能抵抗剪切造成的团聚,在均质后形成更小的颗粒,增加荧光物质暴露的表面积,从而提高荧光强度。TC-P组和TP-P组的荧光峰值显著大于CA-P组和NA-P组,表明TP与蛋白质相互作用,诱导微颗粒内部的蛋白质构象改变,使更多Trp暴露在亲水环境,增强其荧光强度。TC-P组的结构稳定性较强,均质后形成更均匀的分散体系,暴露出更多的荧光物质,故TC-P组的荧光强度略高于TP-P组。
2.6 皮克林乳液的外观和微观
不同凝胶微颗粒制备的皮克林乳液的外观形貌和微观结构如图6所示。贮存0 d制备的皮克林乳液均出现乳析现象,其中NA-PE和TC-PE的乳析现象较弱,其他组差异不明显。将上层乳液分离后贮存15 d,皮克林乳液均未出现分层,表明利用蛋清凝胶微颗粒制备的皮克林乳液具有较好的贮藏稳定性。在光学显微镜的观察下,TC-PE和TP-PE的乳液液滴较小、分布的较均匀并形成较厚的界面膜。TC-PE和TP-PE颗粒较小,易被吸附到油和水之间的界面上,从而形成致密的界面膜,有利于防止液滴聚结[31]。相反,CA-PE和NA-PE的乳液液滴尺寸较大、分布不均匀且形成的界面膜较薄。据报道,较大的粒径会减小界面覆盖率[32],导致微颗粒未能完全覆盖均质过程中形成的所有液滴,部分液滴相互结合,聚集形成了更大的液滴,并且出现了联结的现象,不利于乳液的稳定。
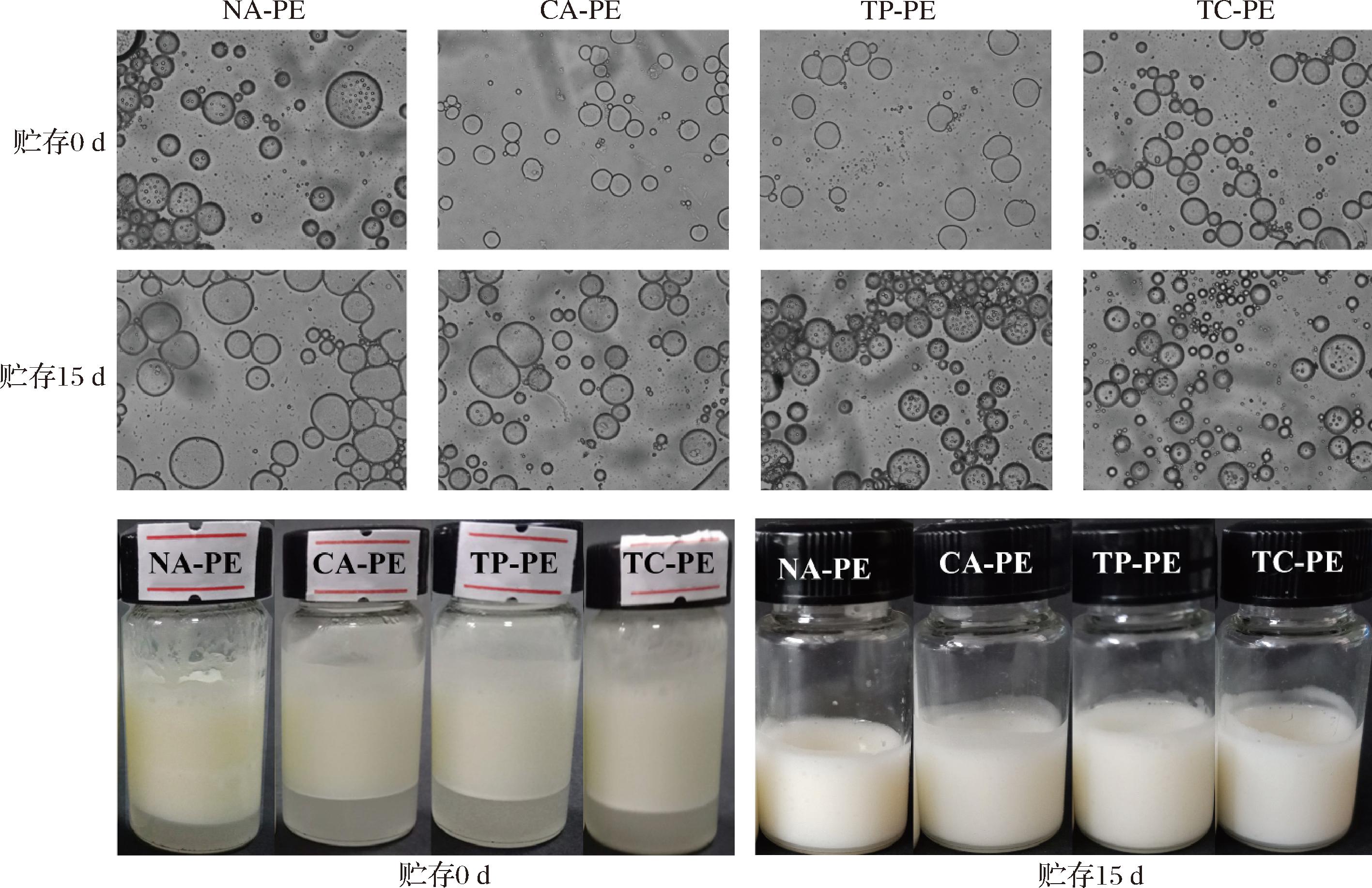
图6 不同蛋清凝胶微颗粒制备的皮克林乳液贮存0 d和15 d的微观和外观结构
Fig.6 Microscopic and macroscopic structures of Pickering emulsions stabilized by different EWG microparticles after 0 and 15 days of storage
2.7 皮克林乳液的粒径
平均粒径能反映乳液体系的稳定性,粒径越小乳液越稳定[33]。不同凝胶微颗粒制备的皮克林乳液贮藏0 d和15 d的平均粒径变化如图7所示。贮存0 d制备的乳液中,TP-PE和TC-PE的粒径较小,分别为19.9 μm和20.2 μm,其次为CA-PE和NA-PE。贮存15 d后,除了TP-PE的粒径出现增大的现象,其他乳液粒径均显著下降(P<0.05),其中TC-PE的粒径减小了24.25%。TP-P组和TC-P组的微颗粒具有较小的粒径,易快速吸附到油水界面形成稳定的界面膜[34],表现为小粒径液滴。在贮存期间,TP氧化生成的醌类物质与蛋白形成二硫键[35],Ca2+可与蛋白交联诱导蛋白质构象变化[28],进一步暴露疏水基团,增强与油相的相互作用。TP与Ca2+协同作用促使界面膜收缩,导致液滴体积减小,粒径显著下降。
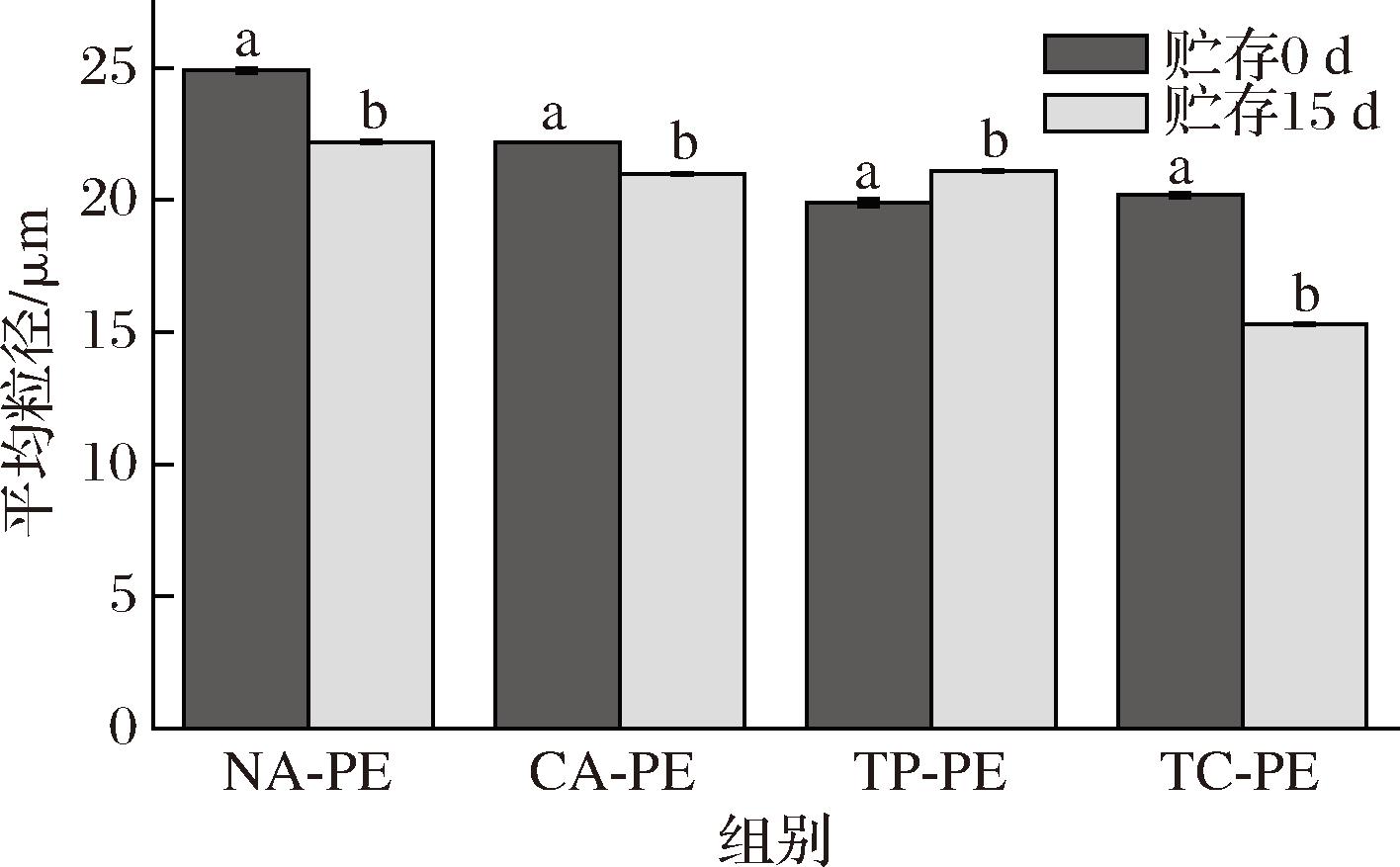
图7 不同蛋清凝胶微颗粒制备的皮克林乳液粒度分布
Fig.7 Particle size distribution of Pickering emulsions prepared from different EWG microparticles
2.8 皮克林乳液的流变特性
2.8.1 皮克林乳液的表观黏度
乳液稳定性与乳液表观黏度紧密相关。如图8-A所示为皮克林乳液的黏度扫描结果,所有乳液表观黏度均随剪切速率上升呈下降趋势,呈现剪切稀化现象,其中黏度最大的是CA-PE,表明所制备皮克林乳液均为假塑性流体[36]。剪切速率增加破坏了乳液体系内部分子间相互作用从而导致其表观黏度降低,CA-P可以较完全地覆盖油滴,并形成较厚的表层,提供强大的空间位阻稳定性,从而获得更好的乳液抗剪切性。贮藏15 d后,所有乳液表观黏度均显著增加,其中TC-PE的黏度最大(图8-B)。TC-PE的粒径显著降低且分散更均匀,形成较厚的界面膜,这有利于提高乳液的抗剪切性。
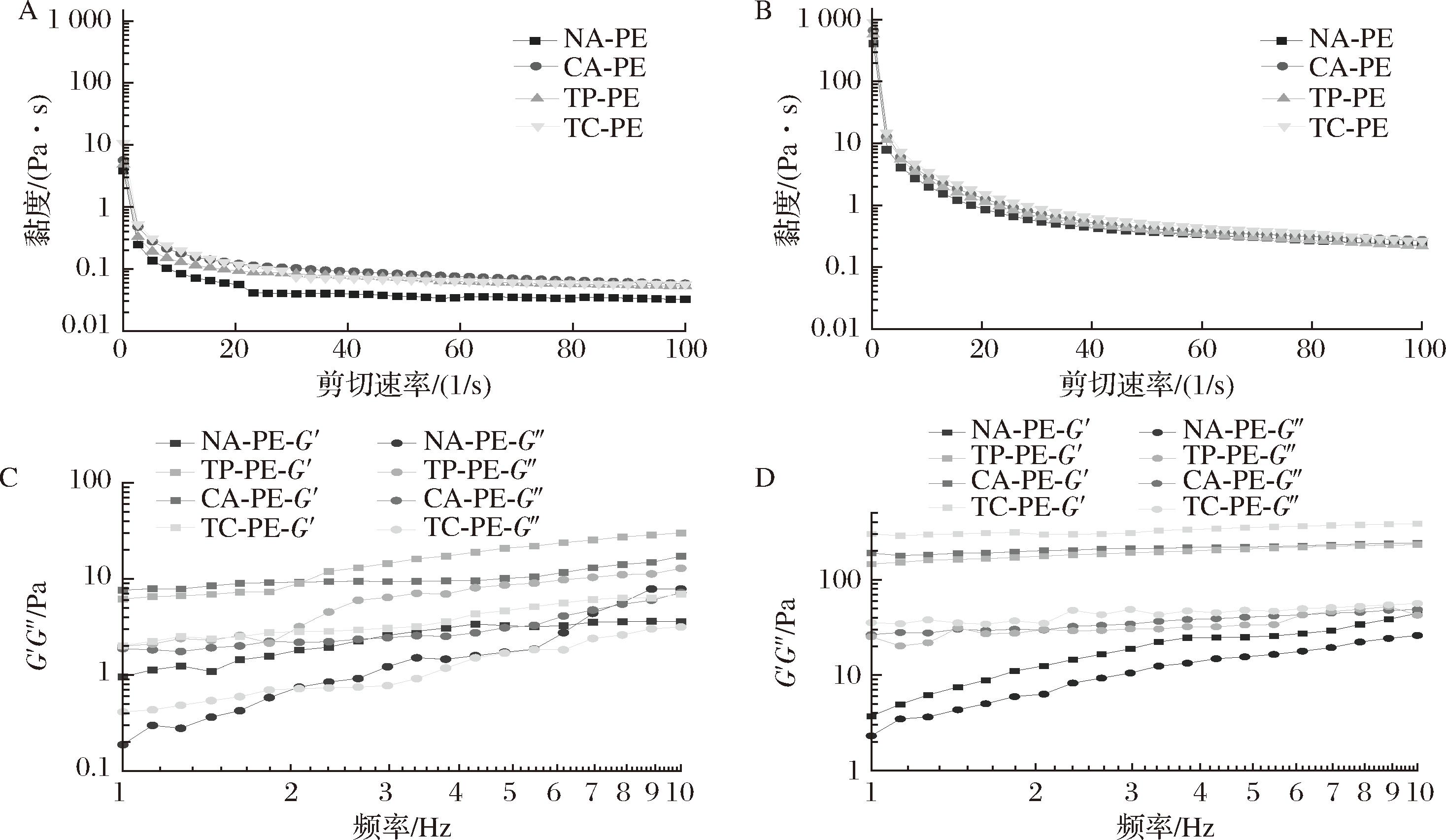
A-贮存0 d;B-贮存15 d;C-贮存0 d;D-贮存15 d
图8 不同蛋清凝胶微颗粒制备的皮克林乳液的流变特性
Fig.8 Rheological properties of Pickering emulsions prepared from different EWG microparticles
2.8.2 皮克林乳液的频率扫描
如图8-C和图8-D分别为贮存0 d和贮存15 d的皮克林乳液频率扫描的结果。G′与G″均随着角频率的增加而升高,表明皮克林乳液的G′与G″均呈频率依赖性。此外,对于所有乳液,在特定的频率(0.1~10 rad/s)时,G′大于G″,即乳液的弹性特性占主导地位,说明该乳液表现出黏弹性固体行为。贮存15 d后,G′与G″均提高且G′始终大于G″,这表明该皮克林乳液具有较好的稳定性。此外,TC-PE的G′显著高于其他组别,原因可能是TC组在体系内部较高的分子相互作用协同下,赋予了TC-PE更强的抵抗剪切应力的特性,导致乳液复合模量整体上升,与表观黏度结果整体一致。综上所述,所制备的皮克林乳液均表现出黏弹性固体行为,贮存0 d的皮克林乳液中CA-PE和TP-PE表现出较高的弹性特性,贮存15 d后TC-PE表现出较好的稳定性,表明可通过化学修饰增强分子间相互作用以提高乳液体系稳定性。
3 结论与讨论
本实验探究差异化诱导形成的蛋清凝胶制备的微颗粒物理化学性质与微结构差异,并考察蛋清凝胶微颗粒稳定皮克林乳液的性能。高压均质导致蛋清凝胶颗粒化形成微颗粒,粒径最小为159.23 nm。与NA-P组和CA-P组相比,TP-P组和TC-P组微颗粒暴露更多疏水性基团,表现为更小的粒径和更紧密的网络微结构。TC-PE组的液滴粒径最小且分布均匀,形成较厚的界面膜。此外,贮存0 d的皮克林乳液TC-PE组表现出较高的表观黏度和弹性模量,贮存15 d后表现出最高黏度和最佳稳定性。综上所述,单独添加Ca(OH)2或TP以及同时添加均能改善凝胶微颗粒的性质,并提升皮克林乳液的稳定性。其中,同时添加Ca(OH)2和TP所制备的微颗粒制成的乳液表现出最佳稳定性。本研究结果可为开发抗氧化和天然蛋白基皮克林乳液的研究提供理论依据。但TP的化学结构与蛋白质的相互作用模式、可能形成新的作用力还有待进一步阐明。
[1] ZHANG Y J, ZHOU X, ZHONG J Z, et al.Effect of pH on emulsification performance of a new functional protein from jackfruit seeds[J].Food Hydrocolloids, 2019, 93:325-334.
[2] LV P F, WANG D, CHEN Y L, et al.Pickering emulsion gels stabilized by novel complex particles of high-pressure-induced WPI gel and chitosan:Fabrication, characterization and encapsulation[J].Food Hydrocolloids, 2020, 108:105992.
[3] 李尚霖. 两亲性蛋清蛋白基Pickering乳液构建及应用研究[D].长春:吉林大学, 2024.LI Sh L.Construction and application research of amphiphilic egg white protein-based Pickering emulsions[D].Changchun:Jilin University, 2024.
[4] 高俊炉, 韩雪儿, 虎梦吉, 等.蛋白质纳米笼稳定Pickering乳液及其在食品领域研究进展[J].食品研究与开发, 2023, 44(20):199-206.GAO J L, HAN X E, HU M J, et al.Protein nanocage-stabilized Pickering emulsion and its application in food field:A review[J].Food Research and Development, 2023, 44(20):199-206.
[5] 张莹. 豆渣纤维固体乳化剂的制备及其对皮克林乳液稳定性的影响[D].长春:吉林农业大学, 2022.ZhANG Y.Preparation of soybean dreg fiber solid emulsifier and its effect on the stability of Pickering emulsion[D].Changchun:Jilin Agricultural University, 2022.
[6] 张兆熙. 氧化淀粉-玉米醇溶蛋白复合颗粒稳定的皮克林乳液制备及应用[D].无锡:江南大学, 2024.ZHANG Z X.Preparation and application of Pickering emulsions stabilized by oxidized starch/zein complex particles[D] Wuxi:Jiangnan University, 2024.
[7] YANG H, SU Z W, MENG X H, et al.Fabrication and characterization of Pickering emulsion stabilized by soy protein isolate-chitosan nanoparticles[J].Carbohydrate Polymers, 2020, 247:116712.
[8] ZHU X F, ZHANG N, LIN W F, et al.Freeze-thaw stability of Pickering emulsions stabilized by soy and whey protein particles[J].Food Hydrocolloids, 2017, 69:173-184.
[9] EUSTON S R, FINNIGAN S R, HIRST R L.Aggregation kinetics of heated whey protein-stabilized emulsions[J].Food Hydrocolloids, 2000, 14(2):155-161.
[10] 李嘉宜, 丁义文, 艾民珉.光谱检测技术在禽蛋品质评价中的应用研究进展[J].食品安全质量检测学报, 2024, 15(2):185-195.LI J Y, DING Y W, AI M M.Research progress on the application of spectroscopic detection technology in the quality evaluation of poultry eggs[J].Journal of Food Safety and Quality, 2024, 15(2):185-195.
[11] 吕远奇. 基于大豆分离蛋白的混合凝胶体系构建及其在植物基肉制品中的应用[D].无锡:江南大学, 2023.LYU Y Q.Construction of mixed gel system based on soybean protein isolate and its application in plant based meat[D].Wuxi:Jiangnan University, 2023.
[12] 郝梦, 毛书灿, 汪兰, 等.食品中动物蛋白形成皮克林乳液的研究进展[J].中国食品学报, 2023, 23(6):420-430.HAO M, MAO S C, WANG L, et al.Research progress on formation of Pickering emulsion from animal protein in food[J].Journal of Chinese Institute of Food Science and Technology, 2023, 23(6):420-430.
[13] 李曼, 刘立增, 刘爱国, 等.蛋白质对冰淇淋品质影响及其在冰淇淋中应用的研究进展[J].食品工业科技, 2024, 45(24):416-426.LI M, LIU L Z, LIU A G, et al.Research progress on the influence of protein on ice cream quality and its application in ice cream[J].Science and Technology of Food Industry, 2024, 45(24):416-426.
[14] 向聪, 钟梦真, 霍嘉颖, 等.贮藏条件对溏心蛋清凝胶特性影响及机制[J].食品科学, 2025, 46(5):281-291.XIANG C, ZHONG M Z, HUO J Y, et al.Effects of storage conditions on gel characteristics of soft-boiled egg white and underlying mechanisms[J].Food Science, 2025, 46(5):281-291.
[15] ZHAO Y, CHEN Z Y, LI J K, et al.Formation mechanism of ovalbumin gel induced by alkali[J].Food Hydrocolloids, 2016, 61:390-398.
[16] CHEN Y, YAO M Y, PENG S, et al.Development of protein-polyphenol particles to stabilize high internal phase Pickering emulsions by polyphenols’ structure[J].Food Chemistry, 2023, 428:136773.
[17] CHANG C H, NIU F G, GU L P, et al.Formation of fibrous or granular egg white protein microparticles and properties of the integrated emulsions[J].Food Hydrocolloids, 2016, 61:477-486.
[18] 邵贝贝, 刘丽莉, 张楠, 等.银耳多糖对蛋清蛋白凝胶性质及结构的影响[J].食品与发酵工业, 2025, 51(8):119-124.SHAO B B, LIU L L, ZHANG N, et al.Effect of Tremella fuciformis polysaccharide on gel properties and structure of egg white protein[J].Food and Fermentation Industries, 2025, 51(8):119-124.
[19] AI M M, XIAO N, ZHOU Q, et al.The relationship between acylation degree and gelling property of NaOH-induced egg white gel:Efficient is better?[J].Food Research International, 2022, 160:111668.
[20] 许瑞. 负载肉桂醛纳米颗粒复合水凝胶在肉制品中对鼠伤寒沙门氏菌的抑制作用[D].镇江:江苏大学, 2023.XU R.Inhibitory effect of composite hydrogel loaded with cinnamaldehyde nanoparticles on salmonella typhimurium in meat products[D].Zhenjiang:Jiangsu University, 2023.
[21] SHIRSATH S R, SONAWANE S H, GOGATE P R.Intensification of extraction of natural products using ultrasonic irradiations:A review of current status[J].Chemical Engineering and Processing:Process Intensification, 2012, 53:10-23.
[22] ZHOU Y Y, YUE W T, LUO Y M, et al.Preparation and stability characterization of soybean protein isolate/sodium alginate complexes-based nanoemulsions using high-pressure homogenization[J].LWT, 2022, 154:112607.
[23] LUO L, CHENG L R, ZHANG R J, et al.Impact of high-pressure homogenization on physico-chemical, structural, and rheological properties of quinoa protein isolates[J].Food Structure, 2022, 32:100265.
[24] XU W, JIN W P, LI Z S, et al.Synthesis and characterization of nanoparticles based on negatively charged xanthan gum and lysozyme[J].Food Research International, 2015, 71:83-90.
[25] WANG Z Y, XIAO N, GUO S G, et al.Tea polyphenol-mediated network proteins modulate the NaOH-heat induced egg white protein gelling properties[J].Food Hydrocolloids, 2024, 149:109514.
[26] OLDFIELD D J, SINGH H, TAYLOR M W, et al.Heat-induced interactions of β-lactoglobulin and α-lactalbumin with the casein micelle in pH-adjusted skim milk[J].International Dairy Journal, 2000, 10(8):509-518.
[27] LIU K S, HSIEH F H.Protein-protein interactions in high moisture-extruded meat analogs and heat-induced soy protein gels[J].Journal of the American Oil Chemists’ Society, 2007, 84(8):741-748.
[28] AI M M, ZHOU Q, GUO S G, et al.Effects of tea polyphenol and Ca(OH)2 on the intermolecular forces and mechanical, rheological, and microstructural characteristics of duck egg white gel[J].Food Hydrocolloids, 2019, 94:11-19.
[29] AI M M, ZHOU Q, XIAO N, et al.Enhancement of gel characteristics of NaOH-induced duck egg white gel by adding Ca(OH)2 with/without heating[J].Food Hydrocolloids, 2020, 103:105654.
[30] 纪雪花, 杜启伟, 苏琪皓, 等.基于油-水界面行为解析蛋白质乳液絮凝机制及其控制方法研究进展[J].食品科学, 2021, 42(13):281-288.JI X H, DU Q W, SU Q H, et al.Mechanisms for and control strategies against the flocculation of protein-stabilized emulsion based on oil-water interface behavior:A review[J].Food Science, 2021, 42(13):281-288.
[31] LIANG Q F, ZHOU C W, REHMAN A, et al.Improvement of physicochemical properties, microstructure and stability of lotus root starch/xanthan gum stabilized emulsion by multi-frequency power ultrasound[J].Ultrasonics Sonochemistry, 2023, 101:106687.
[32] PEI X P, ZHAI K K, LIANG X C, et al.Interfacial activity of starch-based nanoparticles at the oil-water interface[J].Langmuir, 2017, 33(15):3787-3793.
[33] 赵国瑜, 范方宇, 黄瑾, 等.纳米SiO2改性4种大分子材料的乳液制备及性质[J].食品科学, 2022, 43(8):22-28.ZHAO G Y, FAN F Y, HUANG J, et al.Preparation and properties of emulsions stabilized with four kinds of nano-SiO2-modified macromolecular material[J].Food Science, 2022, 43(8):22-28.
[34] 卢筠梦, 赵雪, 徐幸莲.蛋白界面膜及其评价方法研究进展[J].食品与发酵工业, 2021, 47(1):285-292.LU J M, ZHAO X, XU X L.Recent progress in protein interfacial film and its evaluation methods[J].Food and Fermentation Industries, 2021, 47(1):285-292.
[35] 周绪霞, 陈婷, 吕飞, 等.茶多酚改性对蛋清蛋白凝胶特性的影响及机理[J].食品科学, 2018, 39(16):13-18.ZHOU X X, CHEN T, LYU F, et al.Effect and mechanism of modification with tea polyphenols on the gel properties of egg white protein[J].Food Science, 2018, 39(16):13-18.
[36] 杨刚. 非牛顿流体的剪切稀化特性及其对微通道内两相流动力学特性的影响[D].大连:大连海事大学, 2024.YANG G.Shear -thinning characteristics of non-Newtonian fluid and its influence on flow dynamics of two-phase flow in microchannels[D].Dalian:Dalian Maritime University, 2024.