芋头(Colocasia esculenta(L.) Schott)是天南星科芋属热带、亚热带作物,广泛分布于非洲、大洋洲、亚洲和美洲[1],我国芋头种植以珠江流域为主,且品种繁多而公认品质最好的芋头都在两广地区[2]。两广地区芋头多在每年9月至次年4月均可收获,其余时间主要以带泥的方式进行贮藏(10~15 ℃)后销售。然而,由于贮藏期的温度和湿度控制不准、包装方式不明确、带泥贮藏时携带微生物较多、采收时的机械损伤、子芋脱落形成伤口等多种因素导致芋头贮藏2~3月腐烂率即可达30%~50%,甚至整库腐烂,造成严重的经济损失。此外,目前芋头以带泥方式流通,进入消费市场,但该种方式对消费者不友好、难以进入大型商超提升商品价值。可见,由于上述因素造成了荔浦芋头贮藏期腐烂率高、销售周期短、销售方式不友好、销售区域窄等问题,严重影响商品价值,制约产业发展。因此,开发适应现代消费方式的贮藏保鲜包装技术尤为重要。
芋头多生长在湿地环境中,携带病原微生物较多;且芋头在高温潮湿的贮藏环境容易发霉而失去商业价值,为采后贮藏保鲜带来挑战[3]。李学智等[4]分别研究了4、12、25 ℃下贮藏芋头质量损失速率、芋头干物质、蔗糖、淀粉、色泽等品质变化,发现芋头贮藏于12 ℃品质最好。田方[5]用1-甲基环丙基(1-methylcyclopropyl,1-MCP)结合不同的气调方式及贮藏温度对奉化产芋艿种球进行保鲜实验,发现2~7 ℃结合充氮能较好的维持芋头品质。MODI等[6]通过研究南非芋采后贮藏,发现芋头的品质和贮藏环境的温度、湿度有关,芋头球茎贮藏在35~40 cm深度的坑中表现较好,3个月芋头的腐烂率为2%~4%。魏秋羽等[7]通过研究不同包装方式对香荷芋贮藏品质的影响,发现纳米包装可自发调节包装袋内的湿度,保持芋头的贮藏品质。以上研究表明,芋头的贮藏品质与贮藏温度、湿度及包装方式有关。目前,国内外学者的研究主要集中在芋头带泥贮藏销售,而关于芋头去泥贮藏的保鲜技术鲜有报道。芋头采后清洗不利于机械损伤、芋子脱落等造成的伤口愈合,且贮藏期易受到病原微生物侵染,引起芋头球茎腐烂。在前期研究中,通过探索不同的愈伤方式,发现芋头经清洗去泥后,30 ℃热空气处理2 d,芋头损伤处可明显形成愈伤组织,抵御微生物侵染[8]。但关于贮藏期的包装方式尚需进一步研究。本文以荔浦芋头为实验材料,研究芋头经清洗杀菌、愈伤后在不同包装处理下发霉率、失重率、维生素C、可溶性蛋白、淀粉、可溶性糖等主要品质指标的变化规律;分析活性氧、抗氧化物质及抗氧化活性之间的联系;明确适合荔浦芋头贮藏保鲜包装方式;旨在为芋头的贮藏技术体系提供生产指导及理论依据。
1 材料与方法
1.1 材料与试剂
2024年1月,新鲜荔浦芋头采收于广西荔浦九道生命种源科技研发有限公司并运回实验室,挑选约1 000 g,且无机械损伤、无病虫害的芋头作为实验对象。淀粉含量测试盒、可溶性糖含量测试盒、超氧阴离子测试盒、过氧化氢(H2O2)测试盒、过氧化氢酶(catalase,CAT)测试盒、超氧化物歧化酶(superoxide dismutase,SOD)测试盒、总抗氧化能力(DPPH)测试盒,苏州科铭生物科技有限公司;其余试剂均为国产分析纯,上海阿拉丁生化科技股份有限公司。
1.2 仪器与设备
恒温恒湿箱,上海龙跃仪器设备有限公司;UV-1800P紫外-可见分光光度计,上海美谱达仪器有限公司;JW-1042高速冷冻离心机,安徽嘉文仪器装备有限公司;906-ULTS超低温冰箱,上海浦西华家用电器有限公司;HH-3A数显恒温水浴锅,国华(常州)仪器制造有限公司;Synergy LX多功能酶标仪,美国伯腾仪器有限公司;Telaire-7001 CO2气体检测仪,美国GE公司;DDS-307A电导率仪,上海仪电科学仪器股份有限公司;PAL-BX/ACID F5糖酸,日本ATAGO公司。
1.3 实验方法
1.3.1 材料处理
参考孙志栋等[9]的方法并对其进行优化。去除芋头表面泥块等杂物,用清水洗涤1次,再用蒸馏水温和冲洗1次,于0.067%(体积分数)咪鲜胺溶液浸泡2 min后捞起并用风扇吹干。参考前期研究方法于30 ℃恒温箱愈伤2 d[8],愈伤处理的芋头分别采用不包装、普通包装袋[市售聚乙烯(polyethylene,PE)保鲜袋,规格为29.5 cm×20 cm×15 μm]、透湿包装袋[透湿包装袋开设4个直径为3 mm的小孔,其材质为聚乙烯醇(polyvinyl alcohol,PVA),规格为32 cm×19 cm×15 μm,水蒸气透过率为149.8 g/(m2·d)]封口包装,置于10 ℃、相对湿度80%~85%下贮藏180 d。贮藏期间每隔30 d进行观察取样1次,随机取5个芋头,测定表观品质指标。取下芋头中间部分并切成粒状,液氮冷冻后粉碎,-80 ℃冰箱保存,用于测定生理指标。
1.3.2 芋头呼吸强度的测定
参考CALEB等[10]的方法并对其进行优化。随机抽取5个大小均匀的芋头与CO2检测仪一同置于带盖玻璃容器中,密封,静置5 min后开始记录初始数值,连续记录7 min,1 min记录1次,计算结果。
1.3.3 芋头失重率的测定
参考BARMAN等[11]的差重法并对其进行优化。芋头经包装后立即称重并记录初始质量m0,取样时记录最终重量m1,计算结果。
1.3.4 芋头相对电导率(relative electrolytic leakage,REL)的测定
参考SHUAI等[12]的方法并作修改进行测定。从每个处理中随机取出20 g芋头并切成约2 mm的末状,称取2 g芋末置于50 mL试管,加入30 mL蒸馏水清洗2次,最后加入20 mL蒸馏水,常温静置40 min,测定初始电导率(E1), 煮沸5 min后冷却至室温,测定最终电导率(E2)。REL的计算如公式(1)所示:
(1)
1.3.5 芋头可溶性固形物(total soluble solid,TSS)含量的测定
参考TAVARINI等[13]的方法并作修改进行测定。每次分别从每个处理组中随机称取20 g鲜切芋头,榨汁,用3层纱布过滤,用蒸馏水调零,将收集的滤液直接滴糖酸仪上测量TSS含量,每组处理测定10次,去除最大最小值,求取平均值。单位为oBrix。
1.3.6 芋头维生素C的测定
参考李志英等[14]的方法并对其进行优化。每个处理组分别称取0.5 g液氮速冻样品于10 mL试管,加入5 mL 2%(质量分数)的草酸溶液、0.2 g活性炭,混匀,4 ℃、10 000×g离心10 min,收集上清液并稀释1.5倍。另取2支10 mL试管,空白组加入1 mL稀释液,1 mL 30 g/L硼酸-250 g/L乙酸钠;实验组加入1 mL稀释液,1 mL 250 g/L乙酸钠。常温避光20 min后2组均加入1 mL 0.2 g/L邻苯二胺,常温避光40 min,在激发波长355 nm、发射波长425 nm处测定荧光强度并计算维生素C含量。
1.3.7 芋头可溶性蛋白的测定
参考ZHANG等[15]的考马斯亮蓝G250(Coomassie brilliant blue G250,CBBG)染色法并作修改进行测定。称取0.5 g样品于10 mL试管,加入5 mL蒸馏水,均质,4 ℃、10 000×g离心20 min并收集上清液。取1 mL上清液于10 mL试管,加入5 mL CBBG染料,静置2 min,在波长595 nm测定吸光度并计算可溶性蛋白的含量。
1.3.8 芋头可溶性糖的测定
采用试剂盒(蒽酮比色法)测定芋头可溶性糖的含量,糖类物质在酸性条件下与蒽酮试剂反应,生成蓝绿色的糠醛衍生物,其在620 nm处有最大的吸光度。芋头可溶性糖含量的单位为mg/g。
1.3.9 芋头还原糖的测定
参考孔祥佳等[16]的3,5-二硝基水杨酸法并作修改进行测定芋头还原糖的含量。将0.1 g样品加入到3 mL蒸馏水中,80 ℃水浴30 min,25 ℃、8 000×g离心20 min并收集上清液。吸取2 mL上清液加入1.5 mL 3,5-二硝基水杨酸试剂中,沸水加热5 min,冷却至室温,于波长540 nm处测得最大吸光值。计算结果以质量分数(%)表示。
1.3.10 芋头淀粉的测定
采用试剂盒(蒽酮比色法)测定芋头淀粉的含量,淀粉在酸的作用下被分解为葡萄糖,葡萄糖与蒽酮试剂反应生成蓝绿色的化合物,其在620 nm处有最大的吸光度,芋头淀粉含量的单位为mg/g。
1.3.11 芋头淀粉酶活性的测定
参考黄秋伟等[17]的方法并作修改进行测定。称取0.5 g样品于5 mL试管,加入3 mL蒸馏水,均质,20 ℃提取20 min,20 ℃、8 000×g离心20 min并收集上清液。另取2支10 mL试管,空白组加入0.5 mL上清液,1 mL 3,5-二硝基水杨酸溶液;实验组加入0.5 mL上清液。2组均在40 ℃保温10 min后加入0.5 mL 10 g/L的淀粉液,再在40 ℃保温5 min后于实验组加入1 mL 3,5-二硝基水杨酸溶液。2组沸水浴5 min后取出冷却,加6 mL蒸馏水并于540 nm下比色测定吸光值。
1.3.12 芋头活性氧(reactive oxygen species,ROS)及相关酶活性的测定
采用试剂盒测定芋头超氧阴离子自由基![]() H2O2含量。
H2O2含量。![]() 的反应液在530 nm处有最大的吸光度,最终结果以nmol/g表示。H2O2的反应液在 415 nm 处有最大的吸光度,最终结果以μmol/g表示。
的反应液在530 nm处有最大的吸光度,最终结果以nmol/g表示。H2O2的反应液在 415 nm 处有最大的吸光度,最终结果以μmol/g表示。
SOD、CAT、DPPH自由基活性采用试剂盒测定,SOD的反应液在560 nm处有最大的吸光度,酶活力单位为U/g。CAT的反应液在405 nm处有最大的吸光度,酶活性单位为U/g。DPPH的反应液在515 nm处有最大的吸光度,以自由基清除率(%)表示。
过氧化物酶(peroxidase,POD)、多酚氧化酶(polyphenol oxidase,PPO)活性测定参考JIANG等[18]的方法并对其进行优化。称取0.5 g样品加入到3 mL 0.05 mol/L磷酸盐缓冲液(pH值=7.8,含0.2 g聚乙烯吡咯烷酮)中,混合均匀,于4 ℃、10 000×g下离心10 min,收集上清液,冰浴保存。将1.8 mL 0.05 mol/L磷酸盐缓冲液(pH值=7)、0.5 mL 0.05 mol/L愈创木酚、0.5 mL 2%(体积分数)H2O2、0.2 mL上清液依次加入5 mL新离心管中,立即在紫外分光光度计470 nm处测定吸光度,每分钟记录1次,连续记录3 min,计算POD活性。将2.3 mL 0.05 mol/L磷酸盐缓冲液(pH值=7)、0.5 mL 0.01 mol/L邻苯二酚、0.2 mL上清液依次加入5 mL新离心管中,立即在紫外分光光度计398 nm处测定吸光度,每分钟记录1次,连续记录1 min,计算PPO活性。POD和PPO的活性单位定义为每克样品每分钟吸光度增加1,即为1个活性单位。POD和PPO的活性均以U/g表示。
1.3.13 芋头苯丙烷代谢产物及相关酶活性的测定
总酚、类黄酮含量测定参考曹建康等[19]的方法并对其进行优化。将0.3 g样品与3 mL 4 ℃预冷的1%(体积分数)HCl-CH3CH2OH溶液混合均匀,于4 ℃避光反应20 min(每隔5 min涡旋1次),4 ℃、10 000×g离心10 min,收集上清液,冰浴保存。取0.2 mL上清液于紫外光(ultra violet,UV)板上,在280、325 nm波长处分别测定总酚、类黄酮的吸光值。总酚含量用OD280nm/g表示,类黄酮含量用OD325nm/g表示。
苯丙氨酸解氨酶(phenylalanine ammonia lyase,PAL)活性测定参考程双等[20]的方法并对其进行优化。将0.5 g样品与5 mL提取液[含5 mmol/L ß-巯基乙醇、2 mmol/L EDTA、40 g/L聚乙烯吡咯烷酮(polyvinyl pyrrolidone,PVP)]混合均匀,离心,冰浴保存上清液。将3 mL 50 mmol/L硼酸缓冲液和0.5 mL 20 mmol/L L-苯丙氨酸加入5 mL新试管中,37 ℃恒温箱中预热10 min,加入0.5 mL上清液,立即于290 nm处测定初始值OD0值,反应60 min后测定终止值OD1值,计算结果。每克样品在1 h内吸光度值提升0.01为1个活性单位。
1.4 数据统计分析
所有实验均进行3次重复。数据处理借助Microsoft Excel 2021完成,图表绘制借助Origin 2021完成,处理组间显著性分析借助SPSS 25.0软件完成。*表示同一贮藏时间不包装组与透湿包装组间差异显著(P<0.05),**表示同一贮藏时间不包装组与透湿包装组间差异极显著(P<0.01)。
2 结果与分析
2.1 不同包装方式对芋头外观的影响
不同包装对芋头外观的影响如图1所示,不包装及透湿包装均不发霉,而普通包装的芋头在第30天均发霉,失去商业价值。这可能是由于市售的普通包装袋透水率较低,内部易形成水蒸气,而芋头自身携带的微生物在适宜的温度湿度下大量繁殖,引起芋头头部长霉,最终失去商业价值。这也与李静[21]的研究结果一致,芋头喜干不喜湿,潮湿的环境下容易长霉。可见,选择合适的包装对芋头长期贮藏至关重要。因此,在后期的贮藏实验中均则围绕芋头不包装及透湿包装2种方式开展。

图1 不同包装对芋头外观品质的影响
Fig.1 Effect of different packaging on the appearance quality of taro
2.2 不同包装对芋头呼吸强度、失重率、相对电导率、TSS含量的影响
呼吸代谢对于采后果蔬的生理品质具有重要影响,较高的呼吸强度会加速营养物质消耗,从而引发一系列品质劣变问题的出现[22]。如图2-A所示,在10 ℃贮藏期间,2组的呼吸强度均呈先降后升的变化规律。30 d时降至3.71、4.37 μg/(kg·s),不包装组120 d后迅速上升,第180天升至11.90 μg/(kg·s);而透湿包装组在30~150 d贮藏期间的呼吸强度变化不大,维持在4.03~5.43 μg/(kg·s)。2组的呼吸强度在前30 d迅速降低可能是由于芋头刚在30 ℃完成愈伤,促进了呼吸代谢;完成愈伤转入10 ℃贮藏后,芋头的代谢减慢,呼吸强度迅速下降。贮藏期间,2组的失重率均呈上升趋势,不包装组的上升趋势明显大于透湿包装组(P<0.01)(图2-B)。贮藏至第180天时,不包装组的失重率升至36.85%,透湿包装组的失重率为24.08%。这可能是透湿包装袋一定程度阻隔了芋头水分的散失,更有利于芋头水分、营养物质的保持[23]。呼吸强度增大,失重率上升,会促进果蔬细胞膜透性增大,而相对电导率能反映果蔬细胞膜通透性的情况[24]。贮藏期间,2组的相对电导率呈上升趋势(图2-C)。第90天后,不包装组的增长速度明显大于透湿包装组。此外,2组的TSS含量的变化趋势与相对电导率的相似,均呈上升趋势(图2-D)。贮藏第90天后,不包装组的增长速度显著大于透湿包装组。可见,随着贮藏时间的延长,失重率上升,细胞膜通透性增大,细胞液外渗,同时呼吸强度增加,淀粉在淀粉酶等的作用下被分解为糖类等,导致TSS含量增大[25]。综上所述,贮藏期间,透湿包装较不包装更能减缓呼吸强度、失重率、相对电导率、可溶固形物的上升,保持芋头的贮藏品质。
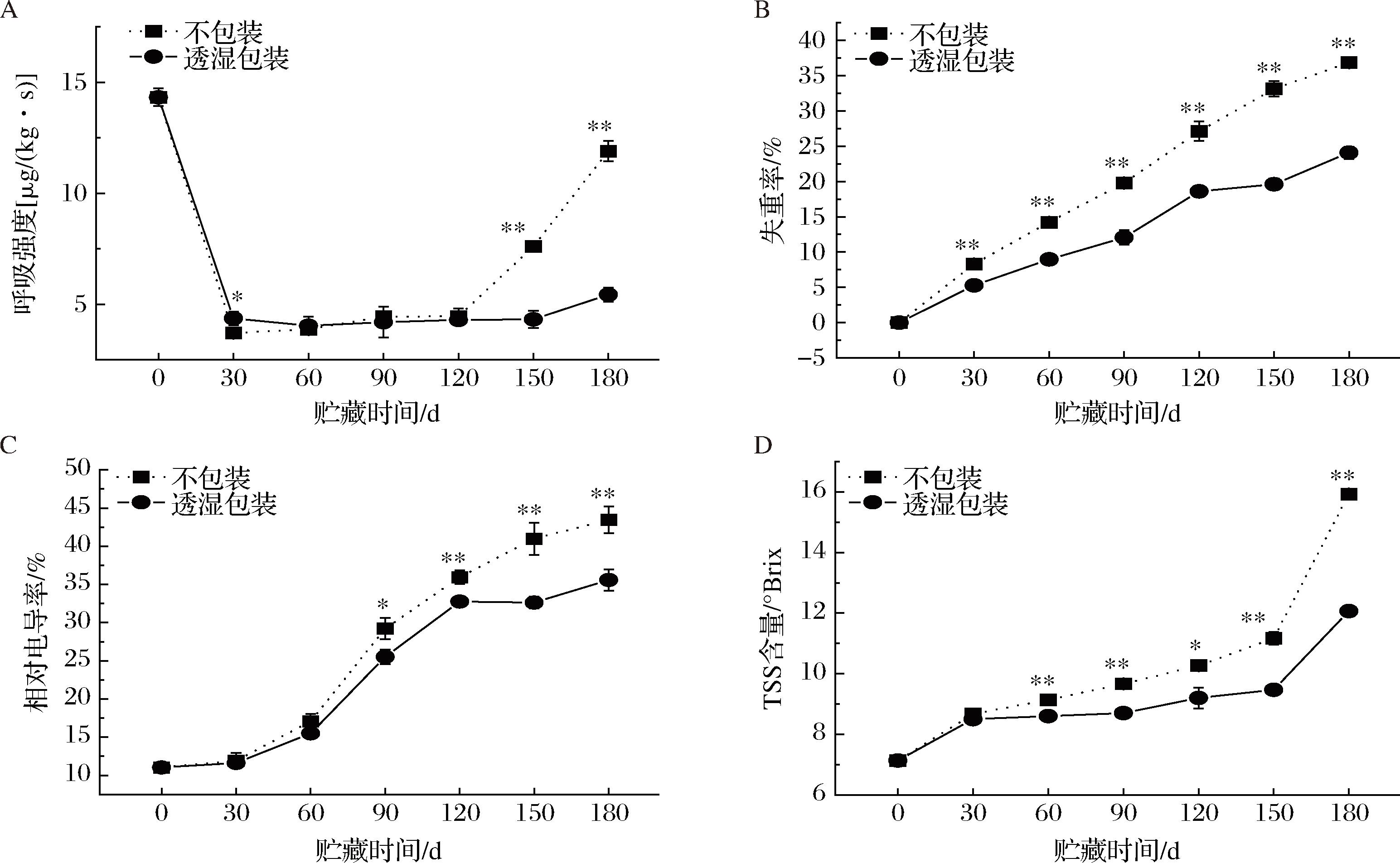
A-呼吸强度;B-失重率;C-相对电导率;D-TSS含量
图2 不同包装对芋头呼吸强度、失重率、相对电导率、TSS含量的影响
Fig.2 Effect of different packaging on respiratory intensity, weight loss, relative electrical conductivity and TSS content of postharvest taro
注:*表示同一贮藏时间不包装组与透湿包装组间差异显著(P<0.05),**表示同一贮藏时间不包装组与透湿包装组间差异极显著(P<0.01)(下同)。
2.3 不同包装对芋头营养物质及相关酶活性的影响
贮藏期间,芋头的生理代谢活动消耗了大量的营养物质,如维生素C、可溶性蛋白、淀粉等。如图3-A所示,2组芋头的维生素C含量呈下降的变化趋势。贮藏期间,不包装组在第180天时降至6.22 mg/100 g,而透湿包装组保持在6.75 mg/100 g。2组芋头的可溶性蛋白含量的变化趋势与维生素C含量的相似,呈下降趋势(图3-B)。不包装组在180 d时降至96.97 mg/100 g;而透湿包装组在整个贮藏期仅下降了6.47 mg/100 g,第180天依然保持在102.13 mg/100 g;不包装组整个贮藏期间的可溶性蛋白含量均显著低于透湿包装组(P<0.05)。2组芋头的淀粉含量的变化趋势与维生素C含量的相似,呈下降趋势(图3-C),不包装组在180 d时降至234.34 mg/g,透湿包装组保持在250.81 mg/g;不包装组整个贮藏期间淀粉含量均显著低于透湿包装组(P<0.01)。贮藏期间,2组芋头的淀粉酶活性呈下降的变化趋势(图3-D),不包装组淀粉酶活性在第180天降至0.087 mg/(min·g),透湿包装组淀粉酶活性在第180天降至0.089 mg/(min·g);不包装组在整个贮藏期的淀粉酶活性均比透湿包装组同期大,这一结论与彭丽桃等[26]的研究结果一致。贮藏期间,淀粉被淀粉酶分解为葡萄糖、麦芽糖等可溶性糖,为芋头的生理活动提供能量。
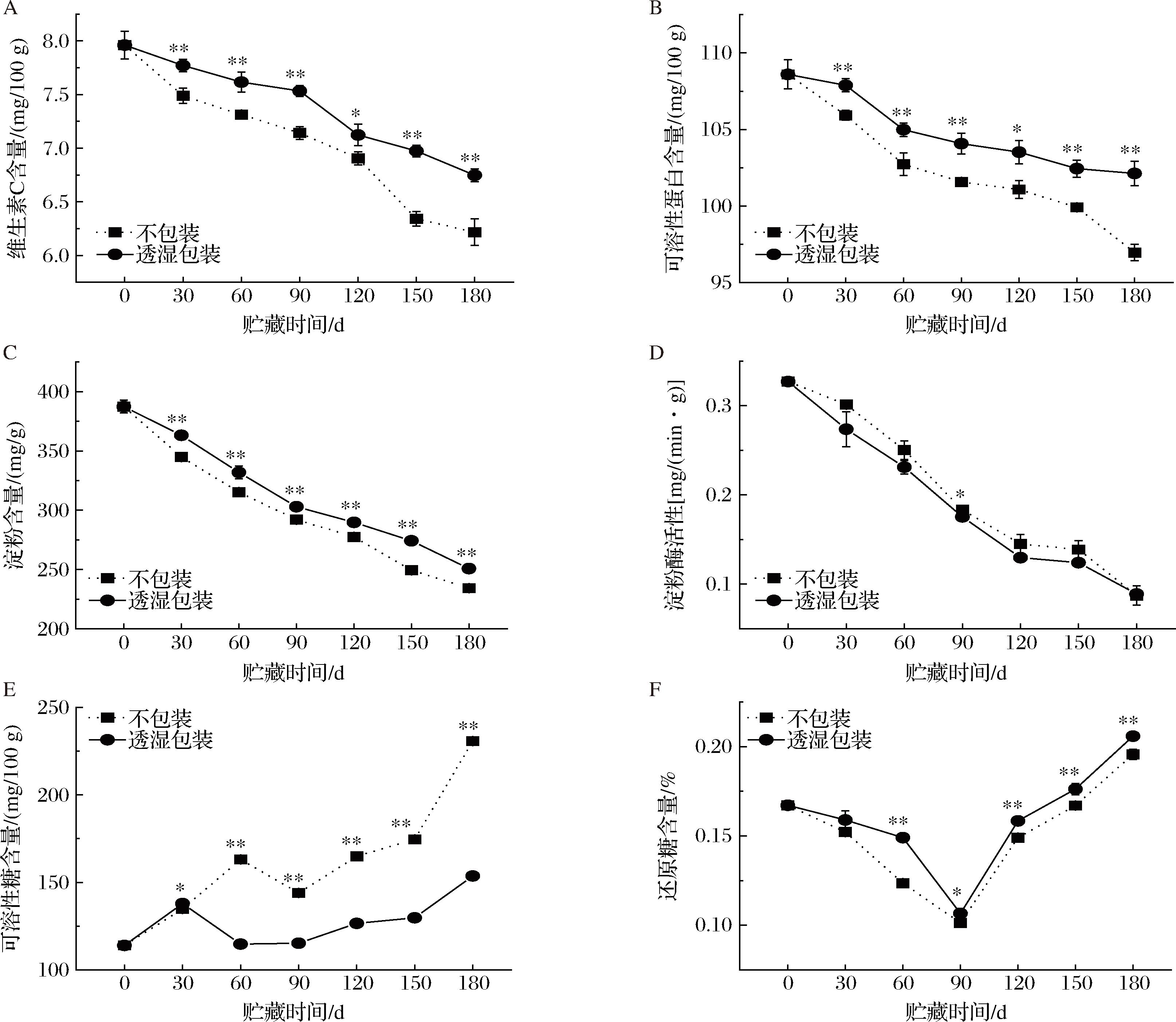
A-维生素C含量;B-可溶性蛋白含量;C-淀粉含量;D-淀粉酶活性;E-可溶性糖含量;F-还原糖含量
图3 不同包装对芋头维生素C含量、可溶性蛋白含量、淀粉含量、淀粉酶活性、可溶性糖含量、还原糖含量的影响
Fig.3 Effects of different packaging on vitamin C content, soluble protein content, starch content, amylase activity, soluble sugar content and reducing sugar content of postharvest taro
芋头中淀粉含量很高,富含多糖类物质,食用风味独特,烹饪后口感软糯香甜可口[27],但贮藏期间由于受生理代谢调节,均会出现动态变化。如图3-E所示,2组芋头的可溶性糖含量呈先升后降再升的变化趋势。不包装组在180 d时升至230.74 mg/100 g,而透湿包装组在整个贮藏期仅上升了39.66 mg/100 g,第180天保持在153.63 mg/100 g。2组芋头的还原糖含量呈先降后升的变化趋势(图3-F)。不包装组、透湿包装组均在第90天后降至最低点分别为0.10%、0.11%,后迅速上升,第180天分别为0.20%、0.21%。综上所述,贮藏期间,芋头在酶的作用下分解营养物质为自身的生理活动提供能量,透湿包装较不包装更能维持维生素C、可溶性蛋白、淀粉等营养物质含量,保持贮藏品质。
2.4 不同包装对芋头ROS及相关酶活性的影响
ROS是生物体内含氧自由基的总称,具有强氧化性,主要包括![]() 等。当生物体受到胁迫时,线粒体释放大量ROS,使ROS在细胞内积累,最终氧化损伤细胞膜。如图4-A所示,贮藏期间,2组芋头
等。当生物体受到胁迫时,线粒体释放大量ROS,使ROS在细胞内积累,最终氧化损伤细胞膜。如图4-A所示,贮藏期间,2组芋头![]() 的含量均呈先升后降再升的变化趋势。不包装组的
的含量均呈先升后降再升的变化趋势。不包装组的![]() 含量在第90天积累到峰值为29.06 nmol/g,随后下降;而透湿包装组的
含量在第90天积累到峰值为29.06 nmol/g,随后下降;而透湿包装组的![]() 含量在第90天达到最高点15.84 nmol/g。同时,2组芋头H2O2含量的变化规律与
含量在第90天达到最高点15.84 nmol/g。同时,2组芋头H2O2含量的变化规律与![]() 含量的相似,呈先升后降再升的变化趋势(图4-B)。不包装组在贮藏期间的H2O2含量均显著大于透湿包装组(P<0.05)。
含量的相似,呈先升后降再升的变化趋势(图4-B)。不包装组在贮藏期间的H2O2含量均显著大于透湿包装组(P<0.05)。
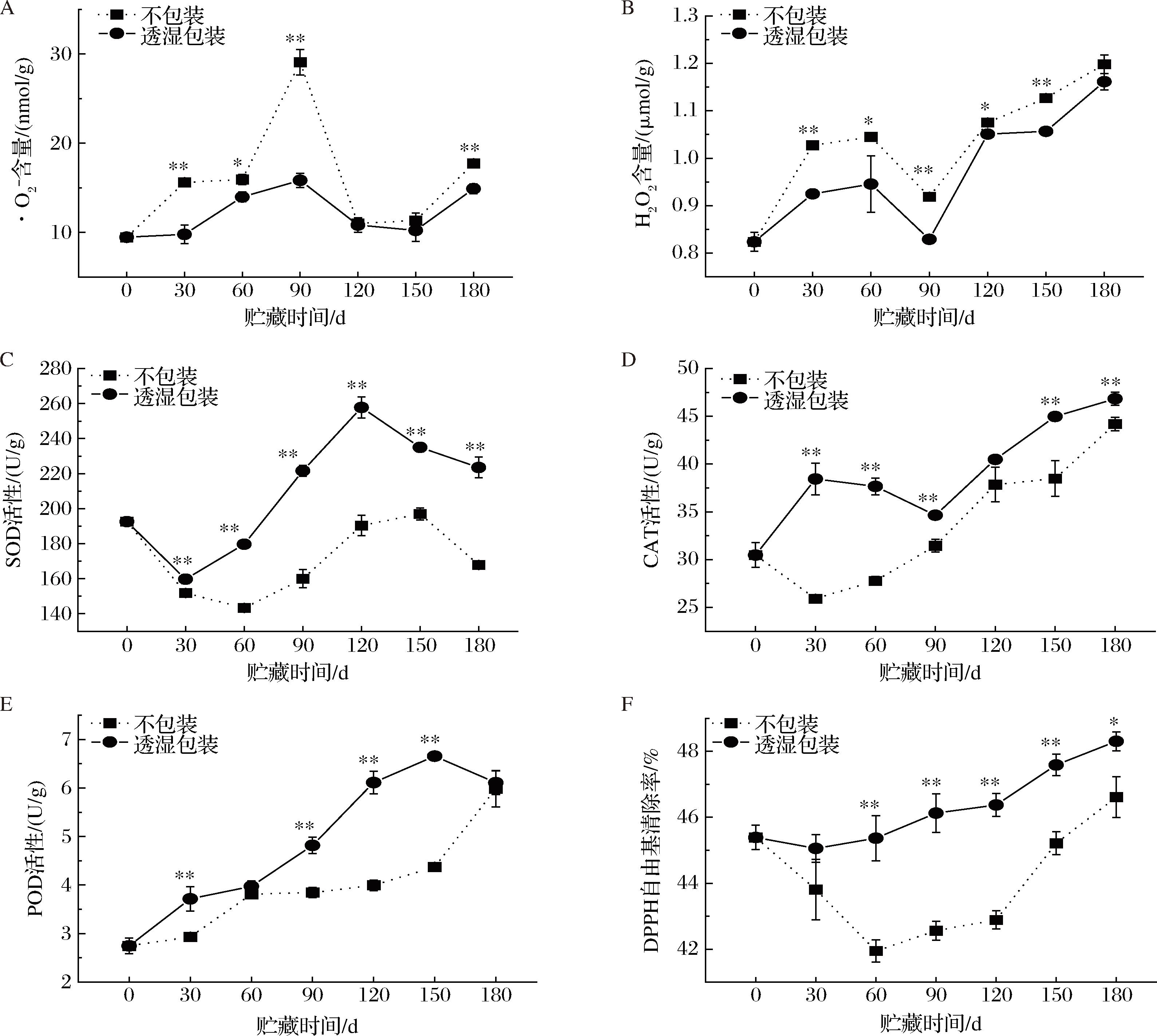
![]() 含量;B-H2O2含量;C-SOD活性;D-CAT活性;E-POD活性;F-DPPH自由基清除率
含量;B-H2O2含量;C-SOD活性;D-CAT活性;E-POD活性;F-DPPH自由基清除率
图4 不同包装对芋头![]() 含量、H2O2含量、SOD活性、CAT活性、POD活性、DPPH自由基清除率的影响
含量、H2O2含量、SOD活性、CAT活性、POD活性、DPPH自由基清除率的影响
Fig.4 Effect of different packaging on ![]() content, H2O2 content, SOD activity, CAT activity, POD activity and DPPH free radical scavenging rateof postharvest taro
content, H2O2 content, SOD activity, CAT activity, POD activity and DPPH free radical scavenging rateof postharvest taro
果蔬受到胁迫时,会诱导体内活性氧物质的快速积累,而SOD、CAT、POD等酶能分解ROS,从而增加果蔬抗氧化性。由图4-C可知,贮藏期间,2组芋头SOD活性均呈先降后升再降的变化趋势。不包装组SOD活性在第0天为最高点192.61 U/g,第180天为167.92 U/g;而透湿包装组的SOD活性在第120天达到最高点257.79 U/g,第180天为223.51 nmol/g;不包装组在贮藏期间的SOD活性均显著低于透湿包装组(P<0.01)。由图4-D可知,2组芋头CAT活性呈不同的变化趋势,不包装组的CAT活性呈先降后上升的变化趋势,于第30天达最低值25.91 U/g,第180天达到峰值44.19 U/g;透湿包装组的CAT活性呈先升后降再升的变化趋势,于第180天达到峰值46.84 U/g。由图4-E可知,2组芋头POD活性呈不同的变化趋势,不包装组的POD活性呈不断上升的变化趋势,于第180天达到峰值5.98 U/g;透湿包装组的POD活性呈先升后降的变化趋势,于第150天达到峰值6.66 U/g后降至第180天6.11 U/g;不包装组在贮藏期间的POD活性均显著低于透湿包装组同期(60、180 d除外)(P<0.01)。2组芋头DPPH自由基清除率均呈先降后上升的变化趋势(图4-F),不包装组的DPPH自由基清除率于第60天降至最低值41.95%,第180天达到峰值46.61%;透湿包装组的DPPH自由基清除率于第30天降至最低值45.06%,第180天达到峰值48.31%。综上所述,透湿袋包装有助于激活芋头抗氧化酶的活性,清除ROS的积累。
2.5 不同包装对芋头苯丙烷代谢的影响
酚类物质具有较强的抗脂质过氧化功能,能提高果蔬的抗氧化活性[28]。因此,酚类物质的积累对芋头的品质尤为重要。由图5-A可知,2组芋头总酚含量的变化趋势不同,不包装组的总酚含量呈不断上升的变化趋势,于第180天达到峰值6.20 OD280nm/g;透湿包装组的总酚含量呈先升后降再升的变化趋势,于第180天达到峰值7.55 OD280nm/g;透湿包装组在贮藏期第60天后的总酚含量均显著高于不包装组同期(P<0.01)。贮藏期间,2组芋头的类黄酮含量均呈上升的变化趋势(图5-B),不包装组的类黄酮含量在第180天达到峰值0.86 OD325nm/g;透湿包装组的类黄酮含量在第180天达到峰值1.02 OD325nm/g,明显比不包装组高(P<0.01)。酚类的积累与苯丙烷代谢、酶促褐变有关,PAL能影响酚类物质的合成。由图5-C可知,2组芋头的PAL活性均呈先升后降的变化趋势,且均在第90天分别达到峰值38.99、41.59 U/g。PPO在氧气下将酚类物质氧化为醌类物质,调节果蔬体内的酚类物质。由图5-D可知,2组芋头PPO活性的变化趋势不同,不包装组的PPO活性呈先升后降的变化趋势,于第120天达到峰值7.60 U/g后下降;而透湿包装组则呈先降后升再降的变化趋势,于第90天降至4.61 U/g;不包装组在贮藏期前150 d的PPO活性均显著高于透湿包装组(P<0.05)。综上所述,透湿包装较不包装更能抑制芋头PPO的活性,积累酚类物质,提高芋头的抗氧化能力。
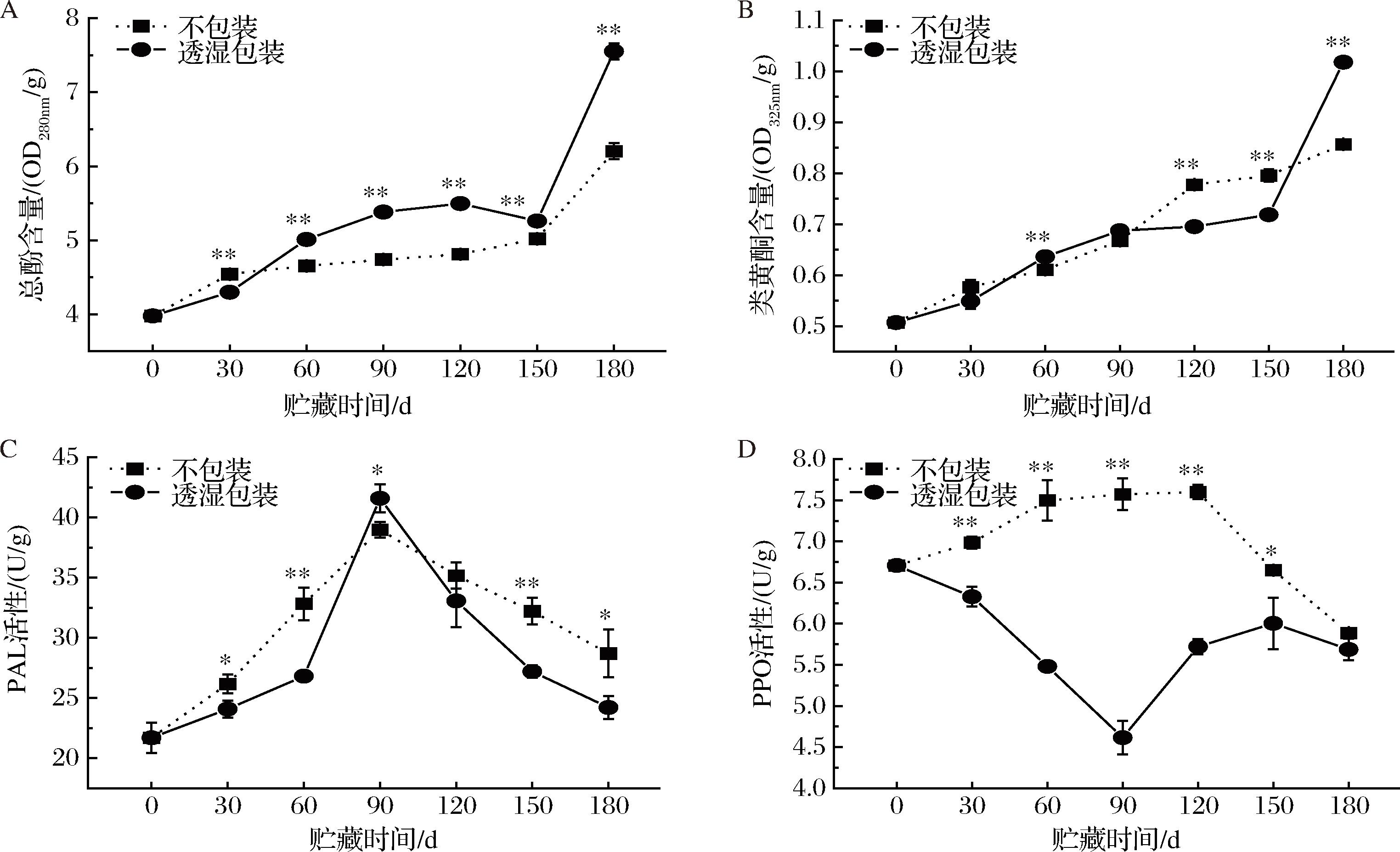
A-总酚含量;B-类黄酮含量;C-PAL活性;D-PPO活性
图5 不同包装对芋头总酚含量、类黄酮含量、PAL活性、PPO活性的影响
Fig.5 Effect of different packaging on total phenol content, flavonoid content, PAL activity and PPO activity of postharvest taro
3 讨论与结论
芋头在采后贮藏过程中容易受外界温湿度的影响及病原微生物的侵扰,而引起失重、发霉、腐烂等现象。本文研究不包装、普通包装袋包装、透湿包装袋包装对芋头品质的影响,发现不同包装对芋头外观品质、营养品质均有影响。普通包装袋包装的芋头贮藏30 d时,所有芋头头部均长白霉。有研究报道芋头表面出现白霉主要为腐皮镰孢菌,该菌株喜欢生长在湿度条件较高的环境[29],普通包装袋因透水能力较差,由于受到呼吸作用等影响袋内易凝聚大量水珠,为腐皮镰孢菌等提供了适宜的生存环境,引起芋头发霉,失去商业价值。而本研究选用的透湿包装,透水率较高[149.8 g/(m2·d)],可及时降低袋内的湿度,保持芋头表面干爽,不易长霉。不包装虽不出现上述情况,但后期失水率显著上升,不利于品质维持。这与魏秋羽等[7]的研究结论一致,芋头的贮藏品质与温度、湿度有关。以上结论表明,不包装及透湿包装均能有效防止芋头发霉。
呼吸是采后果蔬的唯一能量来源,采后果蔬通过呼吸作用分解营养物质为自身的新陈代谢提供能量[30]。因此,随着贮藏时间的延长,芋头的失重率上升。但第30~120天2处理组的呼吸强度差异并不明显,而2组间同期的失重率差异极显著(P<0.01),表明透湿包装较不包装更能保持芋头的水分。随着水分的流失,果蔬组织内部的细胞壁水、细胞质水、液泡水间发生水分迁移,造成失重率上升,失重率与细胞膜通透性呈正相关[31]。因此,相对电导率也随着芋头贮藏时间的延长而上升。相对电导率上升,细胞膜通透性增大,大量的细胞液外渗,引起TSS含量上升[32]。芋头的失重率、相对电导率、TSS含量均随贮藏时间的延长而上升,与以上结论相符。芋头水分的流失、细胞膜通透性的改变会引起其营养物质的变化。维生素C、可溶性蛋白、淀粉含量等营养指标均呈下降的变化趋势。贮藏期间,透湿包装组的维生素C、可溶性蛋白、淀粉含量均高于不包装同一时间的含量;透湿包装组的淀粉酶活性低于不包装同期,但2组的淀粉酶活性在贮藏期间均呈下降趋势,这可能是因为淀粉酶活性与芋头的水分含量有关。随着贮藏时间的延长,由于呼吸作用及蒸腾作用等,芋头的水分含量降低,而淀粉酶活性与水分含量呈正相关[33],淀粉酶活性随水分含量降低而降低。这与DOGAN[34]的研究结论一致,高淀粉作物贮藏期间的淀粉酶活性与水分含量有关。综上所述,透湿包装较不包装更能保护芋头细胞膜结构的完整性,延缓失重率、相对电导率、使TSS含量上升,保持较高的营养品质。
果蔬的衰老、冷害、机械损伤和病虫害会促进ROS的合成,ROS能诱发膜脂不饱和脂肪酸发生过氧化反应,促进脂肪酸分解,产生脂质过氧化物,破坏细胞膜结构,引起果蔬腐烂[35]。研究表明,果蔬在受到胁迫时,自身会作出应激反应并产生大量的![]() 被SOD歧化为H2O2,H2O2被CAT、POD等酶分解为H2O和O2[36]。本研究发现,不同的包装也能影响芋头ROS代谢,进而影响芋头的贮藏品质。芋头贮藏期间,不包装组的
被SOD歧化为H2O2,H2O2被CAT、POD等酶分解为H2O和O2[36]。本研究发现,不同的包装也能影响芋头ROS代谢,进而影响芋头的贮藏品质。芋头贮藏期间,不包装组的![]() 含量均比透湿包装组同一时期的含量高;而透湿包装组的SOD、CAT、POD活性均比不包装组同一时期的活性高。因此,透湿包装较不包装更能维持ROS代谢平衡,保护细胞膜的完整性,维持较低的相对电导率,降低芋头失重率、腐烂率。果蔬的贮藏品质也与其抗氧化物质有关,酚类是重要的抗氧化物质,而贮藏期间酚类的积累主要来源于果蔬的苯丙烷代谢[37]。透湿包装组的苯丙烷类代谢途PAL酶活性仅在第90天强于不包装组,但透湿包装组的PPO活性显著大于不包装组同一贮藏时期的酶活性(第180天除外),透湿包装组的总酚含量在贮藏期第60天后均显著高于不包装组同一时期(P<0.01),透湿包装组的DPPH自由基清除率在贮藏期30 d后显著高于不包装组同一时期的总抗氧化能力(P<0.05)。综上所述,透湿包装较不包装更有利于提高芋头抗氧化物质的含量、抗氧化酶活性,及时清除其体内的ROS,构建ROS代谢平衡。
含量均比透湿包装组同一时期的含量高;而透湿包装组的SOD、CAT、POD活性均比不包装组同一时期的活性高。因此,透湿包装较不包装更能维持ROS代谢平衡,保护细胞膜的完整性,维持较低的相对电导率,降低芋头失重率、腐烂率。果蔬的贮藏品质也与其抗氧化物质有关,酚类是重要的抗氧化物质,而贮藏期间酚类的积累主要来源于果蔬的苯丙烷代谢[37]。透湿包装组的苯丙烷类代谢途PAL酶活性仅在第90天强于不包装组,但透湿包装组的PPO活性显著大于不包装组同一贮藏时期的酶活性(第180天除外),透湿包装组的总酚含量在贮藏期第60天后均显著高于不包装组同一时期(P<0.01),透湿包装组的DPPH自由基清除率在贮藏期30 d后显著高于不包装组同一时期的总抗氧化能力(P<0.05)。综上所述,透湿包装较不包装更有利于提高芋头抗氧化物质的含量、抗氧化酶活性,及时清除其体内的ROS,构建ROS代谢平衡。
本文通过研究不包装、普通包装、透湿包装对荔浦芋头贮藏品质的影响,发现普通包装袋因透水能力较差,袋内湿度大,易长霉,不利于芋头的贮藏。在长期贮藏期间,透湿包装较不包装更能减小芋头的呼吸作用和失重率,保持更高的维生素C、可溶性蛋白、淀粉含量;提高总酚等抗氧化物含量及SOD、CAT、POD等抗氧化酶活性,增强芋头的总抗氧化能力,清除芋头体内积累的ROS,保护细胞膜的完整性,维持较高的贮藏品质。透湿包装袋通过适时调节袋内环境湿度,平衡水分蒸发的动态过程,既能有效抑制有害微生物的滋生,又能延缓芋头生理代谢速率。该透湿包装袋能维持适度的微环境湿度,有效避免高湿度引发的结露现象,同时防止过度失水导致品质下降,这种自发式湿度调控作用显著降低了ROS对细胞膜的过氧化损伤,并通过优化贮藏微环境使芋头始终处于低代谢休眠状态,实现延长保鲜期至180 d以上。
[1] 向华, 吴曼, 胡志山, 等.世界芋头生产布局与贸易格局分析[J].世界农业, 2018(10):144-150.XIANG H, WU M, HU Z S, et al.Analysis of the global taro production layout and trade pattern[J].World Agriculture, 2018(10):144-150.
[2] 郭巨先, 尹艳, 唐康, 等.芋种质资源研究进展与展望[J].广东农业科学, 2021, 48(9):81-90.GUO J X, YIN Y, TANG K, et al.Research progress and prospect of Colocasia esculenta germplasm resources[J].Guangdong Agricultural Sciences, 2021, 48(9):81-90.
[3] 吴通礼. 芋头常见病害的识别及综合防治技术[J].江西农业, 2012(3):40-41.WU T L.Identification and integrated control techniques of common diseases of taro[J].Jiangxi Agriculture, 2012(3):40-41.
[4] 李学智, 吕家龙, 李洪浩, 等.温度对芋贮藏效果的影响[J].中国蔬菜, 2003(3):38-39.LI X Z, LYU J L, LI H H, et al.Effect of temperature on storage of taro[J].China Vegetables, 2003(3):38-39.
[5] 田方. 奉化芋艿营养成分分析及其加工保鲜技术研究[D].宁波:宁波大学, 2013.TIAN F.Study on analysis of nutritional contents and technologies for processing and fresh-keeping of fenghua taro[D].Ningbo:Ningbo University, 2013.
[6] MODI A T, BORNMAN C H.Short-term preservation of maize landrace seed and taro propagules using indigenous storage methods[J].South African Journal of Botany, 2004, 70(1):16-23.
[7] 魏秋羽, 李大婧, 宋江峰, 等.不同包装方式对1-MCP处理香荷芋贮藏品质的影响[J].江苏农业学报, 2018, 34(1):194-199.WEI Q Y, LI D J, SONG J F, et al.Influence of different packing methods on storage quality of 1-MCP-treated Xianghe taro[J].Jiangsu Journal of Agricultural Sciences, 2018, 34(1):194-199.
[8] 陈道业, 陈于陇, 戴凡炜, 等.不同愈伤处理方式对芋头采后愈伤层形成及代谢的影响[J].食品科学, 2025, 46(7):264-272.CHEN D Y, CHEN Y L, DAI F W, et al.Effects of different treatments on postharvest callus formation and metabolic mechanisms in taro[J].Food Science, 2025, 46(7):264-272.
[9] 孙志栋, 田方, 张仁杰, 等.1-MCP和温度处理对采后芋头贮藏品质的影响[J].核农学报, 2015, 29(9):1730-1736.SUN Z D, TIAN F, ZHANG R J, et al.Effects of 1-MCP and temperature treatment on postharvest storage quality of taros[J].Journal of Nuclear Agricultural Sciences, 2015, 29(9):1730-1736.
[10] CALEB O J, MAHAJAN P V, OPARA U L, et al.Modelling the respiration rates of pomegranate fruit and arils[J].Postharvest Biology and Technology, 2012, 64(1):49-54.
[11] BARMAN K, ASREY R, PAL R K.Putrescine and carnauba wax pretreatments alleviate chilling injury, enhance shelf life and preserve pomegranate fruit quality during cold storage[J].Scientia Horticulturae, 2011, 130(4):795-800.
[12] SHUAI L, XUE P Y, LIAO L Y, et al.Methyl jasmonate suppressed the pericarp browning in postharvest longan fruit by modulating membrane lipid and energy metabolisms[J].Postharvest Biology and Technology, 2024, 209:112681.
[13] TAVARINI S, DEGL'INNOCENTI E, REMORINI D, et al.Antioxidant capacity, ascorbic acid, total phenols and carotenoids changes during harvest and after storage of Hayward kiwifruit[J].Food Chemistry, 2008, 107(1):282-288.
[14] 李志英, 薛志伟, 张海容.用荧光光度法测定饮料中的Vc含量[J].商丘师范学院学报, 2007,23(9):60-62.LI Z Y, XUE Z W, ZHANG H R.Spectrofluorimetry method for determining ascorbic acid in soft drink[J].Journal of Shangqiu Normal University, 2007,23(9):60-62.
[15] ZHANG Y T, LI S L, DENG M Y, et al.Blue light combined with salicylic acid treatment maintained the postharvest quality of strawberry fruit during refrigerated storage[J].Food Chemistry:X, 2022, 15:100384.
[16] 孔祥佳, 沈洁, 赵峰, 等.胁迫性和非胁迫性低温贮藏番石榴果实糖代谢差异分析[J].保鲜与加工, 2024, 24(12):36-42.KONG X J, SHEN J, ZHAO F, et al.Differential analysis of sugar metabolism in guava fruits under stress and non-stress low temperature storage[J].Storage and Process, 2024, 24(12):36-42.
[17] 黄秋伟, 龙凌云, 罗小杰, 等.贮藏温度对板栗果仁糖类物质含量和质地的影响[J].粮食与油脂, 2024, 37(9):63-69.HUANG Q W, LONG L Y, LUO X J, et al.Add to favorite effect of storage temperature on the carbohydrates content and texture of chestnut kernels[J].Cereals &Oils, 2024, 37(9):63-69.
[18] JIANG A L, TIAN S P, XU Y.Effects of controlled atmospheres with high-O2 or high-CO2 concentrations on postharvest physiology and storability of “Napoleon” sweet cherry[J].Acta Botanica Sinica, 2002, 44(8):925-930.
[19] 曹建康, 姜微波, 赵玉梅.果蔬采后生理生化实验指导[M].北京:中国轻工业出版社, 2007:44-45.CAO J K, JIANG W B, ZHAO Y M.Experiment Guidance of Postharvest Physiological and Biochemical of Fruits and Vegetables[M].Beijing:China Light Industry Press, 2007:44-45.
[20] 程双, 胡文忠, 马跃, 等.鲜切果蔬酶促褐变发生机理的研究[J].食品工业科技, 2010, 31(1):74-77;80.CHENG S, HU W Z, MA Y, et al.Study on the enzymatic browning mechanism of fresh-cut fruits and vegetables[J].Science and Technology of Food Industry, 2010, 31(1):74-77;80.
[21] 李静. 芋头贮藏法[J].农村新技术, 2009(20):72.LI J.Storage method of taro[J].New Rural Technologies, 2009(20):72.
[22] 唐建新, 王佳莉, 英丽美, 等.果蔬采后生理代谢变化及调控机制研究进展[J].包装工程, 2022, 43(5):91-99.TANG J X, WANG J L, YING L M, et al.Advances in physiological metabolism changes and regulation mechanism of harvested fruits and vegetables[J].Packaging Engineering, 2022, 43(5):91-99.
[23] 郑鹏蕊, 李东立, 付亚波, 等.一种自发气调包装袋对杨梅果实采后品质的影响[J].保鲜与加工, 2022, 22(6):28-34.ZHENG P R, LI D L, FU Y B, et al.Effects of a spontaneous modified atmosphere packaging bag on postharvest qualities of bayberry (Myrica rubra) fruits[J].Storage and Process, 2022, 22(6):28-34.
[24] 林毅雄, 林艺芬, 陈莲, 等.解偶联剂DNP处理对采后龙眼果实呼吸作用和细胞膜透性的影响[J].中国食品学报, 2018, 18(2):191-196.LIN Y X, LIN Y F, CHEN L, et al.Effects of uncouple agent 2,4-dinitrophenol (DNP) treatment on respiration and cellular membrane’ permeability in harvested longan fruit[J].Journal of Chinese Institute of Food Science and Technology, 2018, 18(2):191-196.
[25] LIU Q, HAN R, YU D, et al.Characterization of thyme essential oil composite film based on soy protein isolate and its application in the preservation of cherry tomatoes[J].LWT, 2024, 191:115686.
[26] 彭丽桃, 杨书珍, 任小林, 等.采后两种不同果肉类型油桃软化相关酶活性的变化[J].热带亚热带植物学报, 2002,10(2):171-176.PENG L T, YANG S Z, REN X L, et al.Changes in softening-related enzymes in melting- and nonmelting-flesh nectarines after harvest[J].Journal of Tropical and Subtropical Botany, 2002,10(2):171-176.
[27] 袁晓, 杨盼迪, 王斌.AOS1基因克隆及其在鲜切芋头褐变中的表达模式分析[J].广东农业科学, 2023, 50(9):198-206.YUAN X, YANG P D, WANG B.Analysis on cloning of AOS1 gene and its expression pattern during the browning process in fresh-cut taros[J].Guangdong Agricultural Sciences, 2023, 50(9):198-206.
[28] 管玉格, 王怡, 袁宁, 等.鲜切果蔬酚类物质生物合成机制及抗氧化活性研究进展[J].中国食品学报, 2024, 24(2):397-406.GUAN Y G, WANG Y, YUAN N, et al.Biosynthetic mechanism of phenolic substances and their antioxidant activity in fresh-cut fruits and vegetables:A review[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(2):397-406.
[29] 宗积林. 新鲜江西毛芋头贮藏期霉变微生物鉴定及保鲜技术研发[D].武汉:华中农业大学, 2023.ZONG J L.Identification of moldy microorganisms and development of preservation technology for fresh Jiangxi taro during storage[D].Wuhan:Huazhong Agricultural University, 2023.
[30] 薛智超. 低温胁迫下甘薯采后呼吸代谢的变化及转录组分析[D].杭州:浙江农林大学, 2024.XUE Z C.Changes and transcriptome analysis of postharvest respiratory metabolism in sweetpotato tuberous roots under lowtemperature[D].Hangzhou:Zhejiang A&F University, 2024.
[31] 梅成铭. 鲜切菠萝蜜常温和低温贮藏期间品质变化研究[D].海口:海南大学, 2020.MEI C M.Study on quality changes of fresh-cut jackfruit during ordinary and low temperature storage[D].Haikou:Hainan University, 2020.
[32] 乔沛, 李慧星, 罗建成, 等.外源褪黑素对采后西梅的贮藏品质及软化相关基因表达的影响[J].食品工业科技, 2025, 46(9):340-351.QIAO P, LI H X, LUO J C, et al.Effect of exogenous melatonin on postharvest storage quality and softening-related gene expression of Prunus domestica[J].Science and Technology of Food Industry, 2025, 46(9):340-351.
[33] 陈裕鸿. 白玉菇真空冷却过程中的水分迁移原位观测及其品质变化规律[D].广州:华南理工大学, 2022.CHEN Y H.In situ observation of water migration during vacuumcooling and quality change of white hypsizygus marmoreus[D].Guangzhou:South China University of Technology, 2022.
[34] DOGAN I S.Alpha amylases:The effect of storage conditions on cereal alpha amylases, a rapid method for measuring fungal alpha amylases, and their effects on dough rheological properties and francala (a hearth bread) production[D].Manhattan:Kansas State University, 1996.
[35] 刘馨怡, 吴珂, 徐丹, 等.油梨蒂腐病菌对油梨果实活性氧代谢的影响[J].分子植物育种, 2022, 20(18):6145-6151.LIU X Y, WU K, XU D, et al.Lasiodiplodia theobromae-induced alteration on ROS metabolism in avocado fruits[J].Molecular Plant Breeding, 2022, 20(18):6145-6151.
[36] LV J Y, ZHANG J H, HAN X Z, et al.Genome wide identification of superoxide dismutase (SOD) genes and their expression profiles under 1-methylcyclopropene (1-MCP) treatment during ripening of apple fruit[J].Scientia Horticulturae, 2020, 271:109471.
[37] 李如新, 郭媛媛, 解春艳, 等.茉莉酸甲酯处理对鲜切甜瓜贮藏期间苯丙烷代谢的影响[J].食品工业科技, 2023, 44(15):354-361.LI R X, GUO Y Y, XIE C Y, et al.Effect of methyl jasmonate treatment on phenylpropanoid pathway in fresh-cut melon during storage[J].Science and Technology of Food Industry, 2023, 44(15):354-361.