酱香型白酒是中国传统发酵蒸馏酒的典型代表之一,生产工艺复杂且周期漫长,历经2次投料、9次蒸煮、8次发酵和7次取酒,酿造出不同风格特征与感官特性的轮次基酒,基酒品质特点是决定成品酒质量的核心要素[1]。一、二轮次基酒粮香、酸香、酸涩味突出;三至五轮次基酒整体香气结构协调,曲香、酱香、花香和水果香突出;六、七轮次基酒糊香、苦味和后味突出,这些差异取决于酒体风味化合物的组成及量比[2]。多位研究者利用液液微萃取、顶空固相微萃取、气相色谱质谱等技术从酱香轮次基酒中准确定性、定量出上百种挥发性风味化合物,结果表明,酯类、醇类、酸类、醛酮类等物质是决定酒体感官差异的主体风味化合物[3-5]。其中,酸类物质是白酒中重要的呈味化合物,同时兼具抗氧化、维持肠道微生态平衡等益生功能[6]。在白酒勾调工艺中,科学调控酒体酸类物质的比例,不仅可优化白酒风味轮廓,还能赋予其健康功能属性[7]。当前,针对酱香轮次基酒中酸类物质的研究已有相关报道,孙优兰等[2]对基酒的风味化合物进行检测,其中酸类化合物含量为1.56~3.32 g/L,占总含量的12.80%~26.51%,以乙酸、乳酸、异戊酸、丙酸、丁酸及异丁酸为主。酸香是一轮次基酒的主要特征风味,并随轮次递增呈逐渐减弱的趋势[5]。唐维川等[8]以同一窖池7个轮次的酱香型基酒为对象,使用气相色谱法对样品风味物质进行定量检测,结合主成分分析法进行分析,确定各轮次基酒中总酸含量随轮次数增加而减小,一轮次酒总酸含量最高,达2.94 g/L。
可见,目前的研究主要聚焦于不同轮次基酒中酸类物质的含量变化,对其来源解析仍显不足。白酒酿造过程中酸类物质生成与微生物群落演替密不可分[9],堆积发酵前期,糖化堆温度升高和溶氧量增加显著促进了微生物的生命活动,特别是产酸细菌(如醋酸菌、芽孢杆菌等)的增殖与代谢,从而加速了有机酸的积累;堆积后期有机酸(如乳酸、乙酸)与乙醇在微生物酯酶催化作用下生成酯类化合物,部分有机酸被消耗[10-11]。窖池发酵阶段,随着酸度快速升高,以乳酸菌、乳杆菌等为代表的产酸和耐酸微生物逐渐成为窖内优势菌属,通过降解脂肪、淀粉和蛋白质等大分子物质持续生成有机酸[12]。此外,氨基酸是生成有机酸的重要前体物质之一,在微生物代谢活动下,氨基酸发生脱氨基或转氨基反应后生成α-酮酸,再通过糖酵解或三羧酸(tricarboxylic acid,TCA)循环进一步生成有机酸[13-14]。微生物与氨基酸共同调控着有机酸的合成过程,影响酸类物质的积累与转化,但其中复杂的相互作用关系尚未明晰。因此,本研究以一轮次基酒的特征酸香为切入点,聚焦其生产来源的下、造沙轮次,以高粱、母曲、母糟及糟醅为研究对象,利用气相色谱、高效液相色谱、高通量测序等技术,并结合多元统计方法,从氨基酸与微生物层面系统解析有机酸的变化规律及来源,为酱香型一轮次基酒酸香风味的形成机制提供理论数据,以期提升轮次基酒品质。
1 材料与方法
1.1 材料与试剂
实验所用的高粱、母曲、糟醅样品均采自贵州省遵义市某酱香型车间2025生产年度;氯化钠(分析纯)、盐酸(分析纯)、无水乙醇(色谱纯)、磷酸二氢钾(分析纯),国药集团化学试剂有限公司;乳酸、乙酸、丙酸、异丁酸、丁酸、异戊酸、戊酸、辛酸、2-乙基丁酸(均为色谱纯),上海安谱实验科技股份有限公司;甲醇(色谱纯),德国默克股份有限公司;钾钠缓冲液、固体茚三酮、氨基酸标准液,赛卡姆(北京)科学仪器有限公司。
1.2 仪器与设备
GC-8890气相色谱火焰离子化检测器(gas chromatography-flame ionization detector,GC-FID)、1260高效液相色谱仪,美国Agilent公司;MIKRO 220R台式高速冷冻离心机,德国Hettich公司;Aquaplore3S超纯水系统,美国艾科浦公司;TND03-H-H混匀型干式恒温器,深圳托能达科技有限公司;AR2130/C电子天平,奥豪斯上海公司;S-433Dup全自动氨基酸分析仪,赛卡姆(北京)科学仪器有限公司。
1.3 实验方法
1.3.1 样品采集
高粱等样品:随机从生产现场各取200 g下、造沙轮次的高粱、母曲、母糟样品共5份,包括下沙高粱(GL-XS)、下沙母曲(MQ-XS)、下沙母糟(MZ-XS)、造沙高粱(GL-ZS)、造沙母曲(MQ-ZS)。
糟醅样品:取下、造沙轮次堆积发酵和窖池发酵样品共18份,下沙(XS)、造沙(ZS)轮次糟醅样品分别包括完堆糟醅(WD-XS、WD-ZS)、堆积中期糟醅(DZ-XS、DZ-ZS)、入窖糟醅(RJ-XS、RJ-ZS),窖池发酵7 d糟醅(J7-XS、J7-ZS)、窖池发酵14 d糟醅(J14-XS、J14-ZS)、窖池发酵21 d糟醅(J21-XS、J21-ZS)、窖池发酵结束28 d出窖上层糟醅(CS-XS、CS-ZS)、出窖中层糟醅(CZ-XS、CZ-ZS)及出窖下层糟醅(CX-XS、CX-ZS)。固定追踪同一个糖化堆进行采样,堆积发酵阶段如图1-a所示,在糖化堆对应的表层及中心a、b、c、d、e、f点等量取样,混合均匀为一个样品;窖内发酵阶段如图1-b所示,在窖池内上层、中层、下层中心及边角h、i、j、k1、l1、m1点等量取样,混合均匀为一个样品;出窖阶段如图1-b所示,在窖池上层h、k1、k2、k3、k4点等量采样,混合均匀后得到出窖上层糟醅;在窖池中层i、l1、l2、l3、l4点等量采样,混合均匀后得到出窖中层糟醅;在窖池下层j、m1、m2、m3、m4点等量采样,混合均匀后得到出窖下层糟醅。
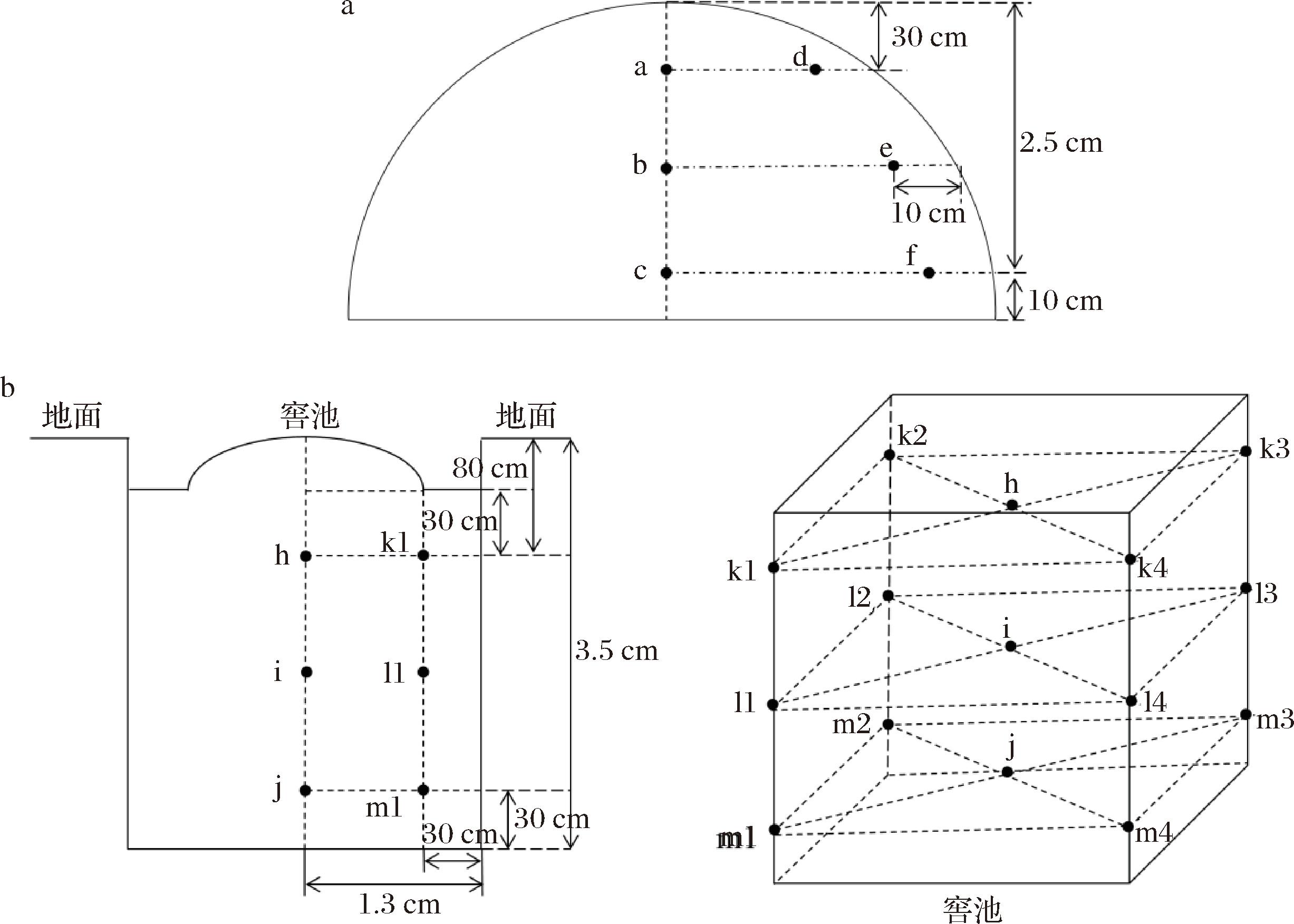
a-堆积发酵;b-窖池发酵
图1 堆积发酵和窖池发酵取样示意图
Fig.1 Schematic diagram of sampling for heap fermentation and pit fermentation
1.3.2 有机酸检测分析
样品的乳酸、乙酸含量通过高效液相色谱仪进行测定,丙酸、异丁酸、丁酸、异戊酸、戊酸及辛酸含量通过GC-FID进行测定,每个样品平行检测3次。
样品前处理:称取(10±0.5) g样品于50 mL离心管中,加入20 mL体积分数为53%的乙醇水溶液,20 ℃条件下超声30 min,5 000 r/min条件下离心3 min,取上清液1.5 mL,过0.22 μm滤膜后进行GC-FID及高效液相色谱检测,根据标准品色谱峰的保留时间确定样品中各物质的色谱峰,以及根据标准曲线确定各物质的含量(以糟醅质量计μg/g)。
GC-FID条件:采用DB-WAX色谱柱(30 m×0.25 mm×0.25 μm);进样口温度240 ℃;进样量:1 μL;分流比:30∶1;载气∶氮气(纯度≥99.999%);柱流量:1 mL/min;升温程序:起始30 ℃,保持3 min,3 ℃/min升温至90 ℃,不保持,5 ℃/min升温至180 ℃,保持25 min;FID检测器温度250 ℃。
高效液相色谱条件:采用C18色谱柱;流动相:0.02 mol/L 磷酸二氢钾溶液;流速:0.8 mL/min;检测波长:208 nm;进样量:1 μL;柱温:30 ℃。
1.3.3 游离氨基酸测定
根据GB 5009.124—2016《食品安全国家标准 食品中氨基酸的测定》,取样品(2±0.1) g,置于氨基酸水解管中,加入10 mL 6 mol/L的盐酸,充分浸润,摇匀;将水解管置于(110±10) ℃烘箱中,加热20 h,取出冷却至室温,将反应液转移至50 mL容量瓶中,以超纯水定容;滤纸过滤反应液,取1 mL置于烧杯中,以电热板(40~50 ℃)进行赶酸处理,重复2~3次,最后以超纯水定容至10 mL;取适当溶液过0.22 μm微孔滤膜置于进样小瓶,利用全自动氨基酸分析仪进行检测,每个样品平行检测3次。
1.3.4 高通量测序
利用E.Z.N.ATM Mag-Bind Soil DNA Kit试剂盒提取样品微生物总基因组DNA。DNA的浓度和纯度用紫外可见光谱比值法评估。参考本课题组方法[15]对细菌16S rRNA基因的V3~V4区域进行PCR扩增,采用Illumina Miseq测序平台,对细菌16S rRNA基因V3~V4区进行高通量测序分析,样本的建库和测序由上海生物工程有限公司完成。
1.4 数据处理
采用Excel、SPSS 22.0软件进行数据处理,柱状图及桑基图利用Origin 2022进行绘制;热图-柱状图、STAMP图等利用OmicShare tools及联川生物云平台进行绘制。
2 结果与分析
2.1 下、造沙轮次酿造过程中有机酸的组成情况
下、造沙轮次,高粱、母曲、母糟及糟醅中均含有机酸,但组成存在差异,其中乳酸、乙酸及丙酸在糟醅中含量较高,异丁酸在母曲中含量较高,丁酸、辛酸、戊酸、异戊酸在母糟中含量较高。下、造沙轮次中,糟醅样品的乳酸含量分别为2 933.62~15 859.97 μg/g和6 103.83~24 707.50 μg/g,乙酸含量分别为309.67~5 367.54 μg/g和1 347.15~4 316.00 μg/g,堆积发酵过程中,糟醅的乳酸和乙酸呈动态波动,经过窖池发酵后,出窖糟醅中的含量有所提升,且随生产轮次的推进呈递增趋势(图2)。与黄廷财等[16]研究结果类似,酿造过程中,乳酸及乙酸含量显著高于其他有机酸。其次是丙酸,丙酸在下沙轮次窖池发酵后期的糟醅中逐渐生成,出窖时下层糟醅中的含量达到峰值为406.84 μg/g;造沙轮次中,丙酸含量有所下降,但整体变化较为稳定。此外,辛酸在酿造发酵过程中含量最低,下沙和造沙轮次糟醅中的平均含量分别为0.27、1.02 μg/g。丁酸、辛酸、戊酸、异戊酸和异丁酸均是酱香型白酒中的重要风味物质,呈酸味,并且随着直链碳链的延长,戊酸、己酸、辛酸等还具有一定的脂肪味[17]。
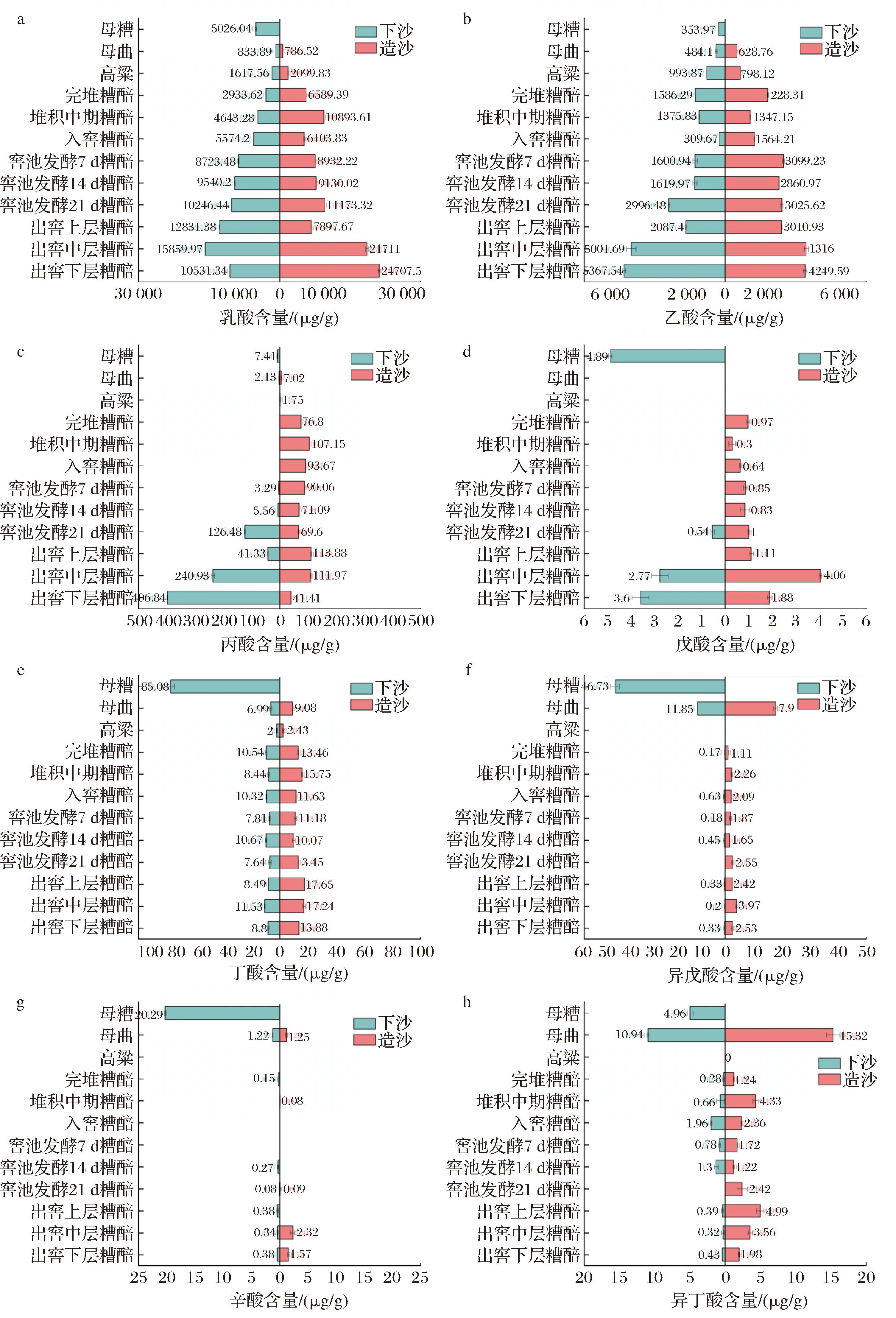
a-乳酸;b-乙酸;c-丙酸;d-戊酸;e-丁酸;f-异戊酸;g-辛酸;h-异丁酸
图2 下、造沙轮次酿造过程中的有机酸组成
Fig.2 Composition of organic acids during the Xiasha and Zaosha round brewing process
2.2 下、造沙轮次酿造过程中有机酸的溯源分析
如图3可知,母糟是有机酸的主要来源,含量为5.53 μg/g,高于母曲和高粱;堆积发酵阶段,下、造沙轮次糟醅中的有机酸含量均呈先升高后降低的变化趋势,在堆积中期达到峰值,下沙和造沙轮次中分别为6.03、12.37 μg/g;窖池发酵阶段,糟醅有机酸含量随发酵时间延长呈缓慢上升趋势,分别在10.34~13.38μg/g(下沙轮次)和12.14~14.29 μg/g(造沙轮次)之间;到开窖取醅阶段,窖内不同空间位置的糟醅中有机酸含量存在显著差异(P<0.05),其中上层糟醅的有机酸含量始终低于其他位置糟醅。综上,下、造沙酿造过程中,酿酒原料及糟醅的有机酸含量呈整体上升的动态变化趋势,且下沙至造沙轮次有明显积累。
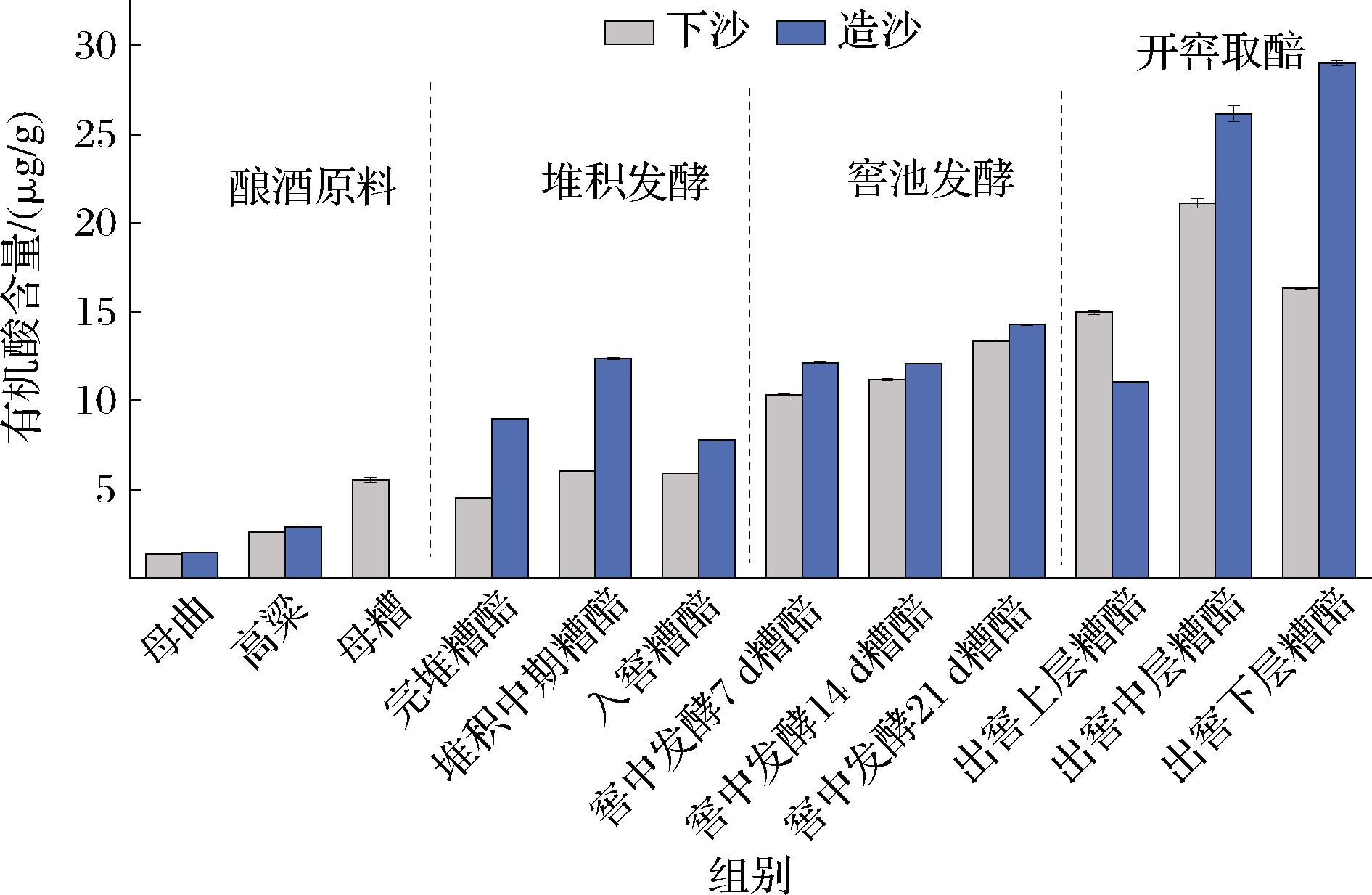
图3 下、沙造沙轮次酿造过程中原料及糟醅的有机酸含量变化
Fig.3 Changes in organic acid contents in raw materials and fermented grains during the Xiasha and Zaosha round brewing process
进一步对高粱、母曲、母糟及糟醅中有机酸来源进行分析,如图4所示,约95%的有机酸在堆积和窖池发酵过程产生,且随发酵推进,有机酸含量不断提高。其中,乳酸及乙酸的主要来源是出窖中层及下层糟醅,表明这2种酸在窖内发酵阶段得到大量生成与积累,这与窖池密闭无氧条件下发生的乳酸菌代谢密切相关[18],乳酸菌代谢包括丙酮酸代谢、糖酵解代谢、氨基酸代谢等多途径,代谢产物包括乳酸、乙酸、游离氨基酸等,其中高含量的乳酸和氨基酸结合被证明在发酵体系中可提升食品的营养价值及绵酸柔和的口感品质,且两者具有显著相关性[19]。
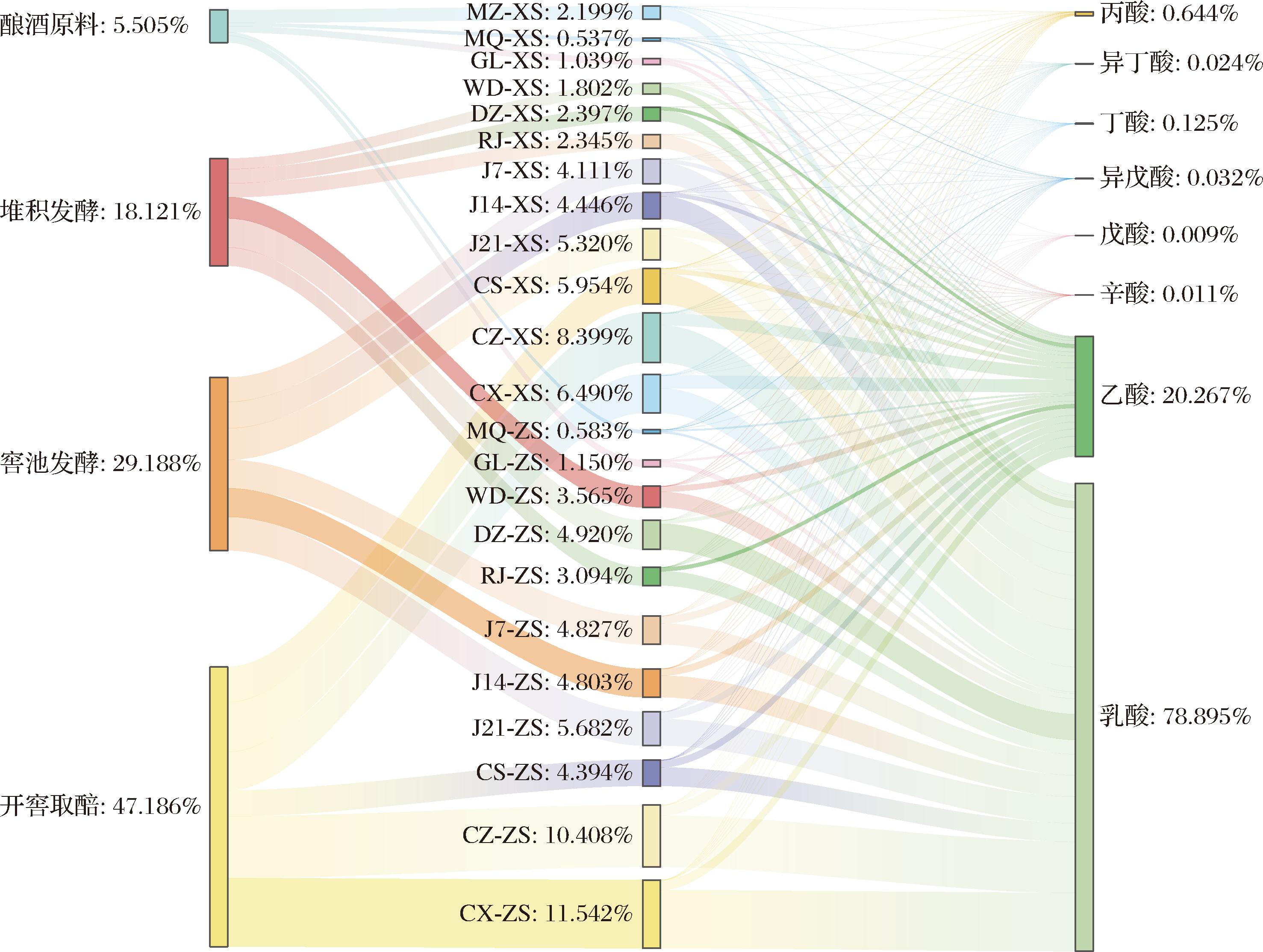
图4 下、造沙轮次酿造过程中有机酸溯源分析
Fig.4 Source tracing analysis of organic acids in raw materials and fermented grains during the Xiasha and Zaosha round brewing process
2.3 下、造沙轮次酿造过程中游离氨基酸的组成分析
对下、造沙轮次酿造过程中高粱、母曲、母糟及糟醅中游离氨基酸进行分析,如图5所示,共检测出17种游离氨基酸,其总量为0.87~481.97 mg/g,除母曲样品外,其他样品中的氨基酸含量均较为丰富,其中高粱(GL-XS、GL-ZS)含量最高,母糟(MZ-XS)次之,表明高粱、母糟是下、造沙轮次游离氨基酸的主要来源,并在后续酿造过程中被分解。已有研究报道,氨基酸经微生物分解代谢会衍生出短链脂肪酸、含硫化合物、芳香族化合物、多胺、氨等物质,而酱香型白酒酿造是一个多菌种相互作用的自发发酵过程,期间伴随大量复杂的微生物动态演变、能量传递及物质转化,这极可能是下、造沙轮次酿造过程中糟醅的游离氨基酸含量逐渐下降,同时有机酸含量逐渐升高的关键原因[20-21]。丁晨红等[22]研究表明依照分子中所含氨基(—NH2)和羧基(—COOH)的数目配比,可将检测出的17种氨基酸划分为酸性和非酸性两大类别,其中酸性氨基酸包括谷氨酸和天冬氨酸,其余15种氨基酸均为非酸性氨基酸。谷氨酸、丙氨酸、天冬氨酸、亮氨酸和脯氨酸在各样本中含量突出,是下、造沙轮次酿造过程中的优势氨基酸。其中,天冬氨酸和谷氨酸呈酸味特征,占各样本氨基酸总量的26.85%(MQ-ZS)~44.61%(MZ-XS),丙氨酸和脯氨酸呈甜味特征,占各样本氨基酸总量的15.46%(MQ-XS)~29.52%(CZ-XS),亮氨酸呈苦味特征,占氨基酸总量的7.23%(MQ-XS)~11.50%(GL-XS)。以上数据表明,酸性氨基酸在酿造过程中占主导地位,极有可能是构成酱香一轮次酒酸香特征的重要前体物质之一。
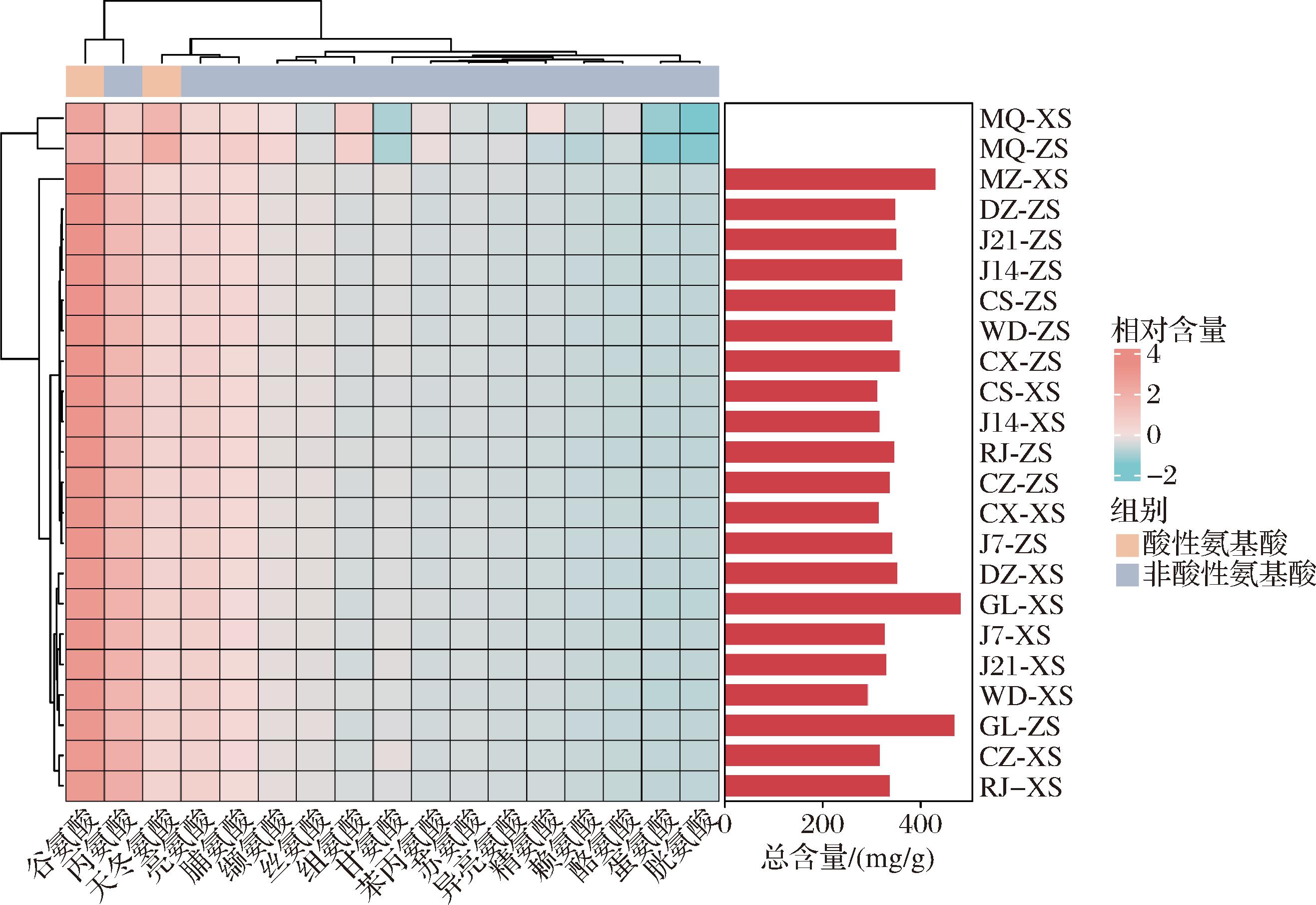
图5 下、造沙轮次酿造过程中原料及糟醅中游离氨基酸热图-柱状图
Fig.5 Heatmap-column chart of free amino acids in raw materials and fermented grains during the Xiasha and Zaosha round brewing process
2.4 下、造沙轮次酿造过程中细菌群落的多样性分析
细菌是白酒酿造过程中有机酸的主要微生物来源[23],对下、造沙轮次发酵过程中高粱、母曲、母糟及糟醅中细菌多样性进行16S rRNA基因扩增子测序分析,共获得2 141 917条原始序列。经去除引物接头序列、序列拼接与质量过滤等处理后,得到1 903 076条有效序列,平均长度为425.96 bp。如表1所示,所有样本的测序覆盖率均达到0.99以上,表明测序数据合理可靠,能够真实反映样本中的微生物群落组成特征。
表1 下、造沙轮次酿造过程中原料及糟醅的细菌群落多样性
Table 1 Bacterial community diversity in raw materials and fermented grains during the Xiasha and Zaosha round brewing process
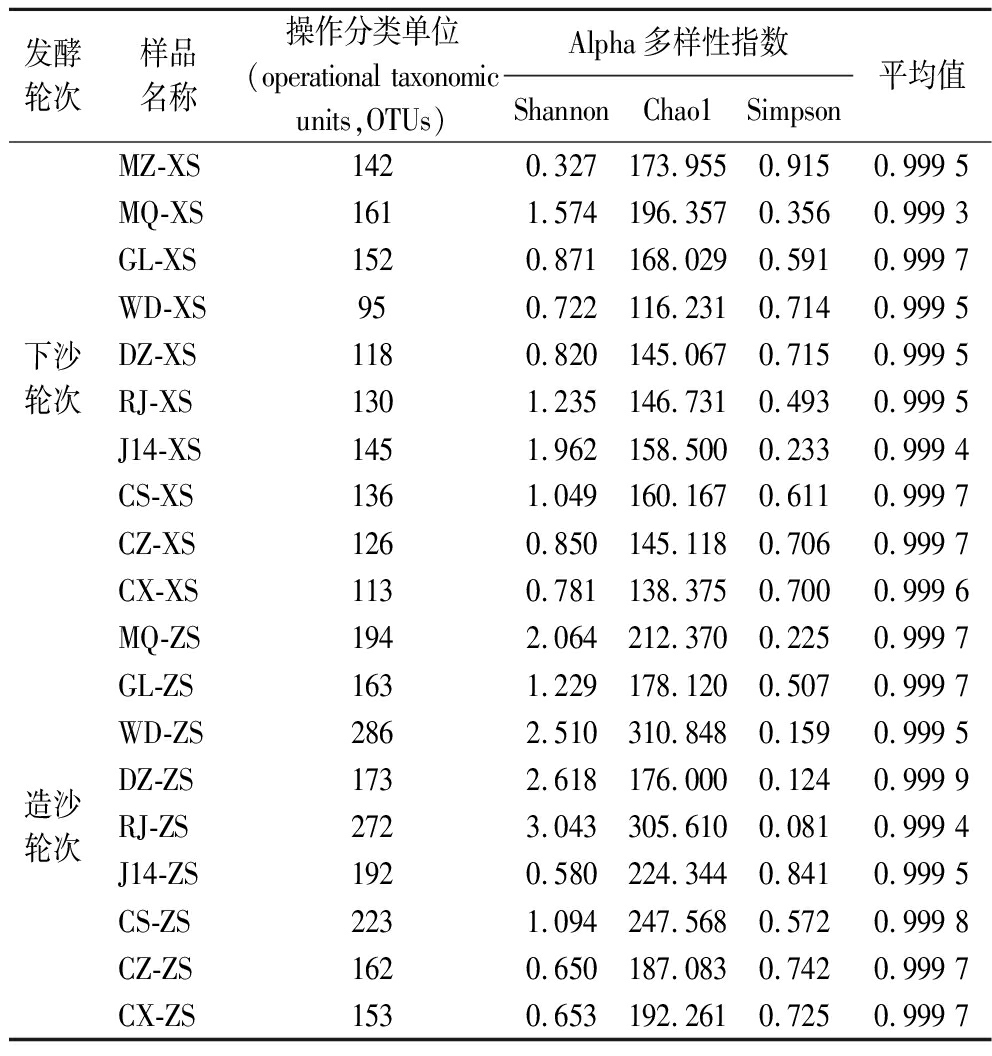
发酵轮次样品名称操作分类单位(operational taxonomicunits,OTUs)Alpha多样性指数ShannonChao1Simpson平均值下沙轮次MZ-XS1420.327173.9550.9150.999 5MQ-XS1611.574196.3570.3560.999 3GL-XS1520.871168.0290.5910.999 7WD-XS950.722116.2310.7140.999 5DZ-XS1180.820145.0670.7150.999 5RJ-XS1301.235146.7310.4930.999 5J14-XS1451.962158.5000.2330.999 4CS-XS1361.049160.1670.6110.999 7CZ-XS1260.850145.1180.7060.999 7CX-XS1130.781138.3750.7000.999 6造沙轮次MQ-ZS1942.064212.3700.2250.999 7GL-ZS1631.229178.1200.5070.999 7WD-ZS2862.510310.8480.1590.999 5DZ-ZS1732.618176.0000.1240.999 9RJ-ZS2723.043305.6100.0810.999 4J14-ZS1920.580224.3440.8410.999 5CS-ZS2231.094247.5680.5720.999 8CZ-ZS1620.650187.0830.7420.999 7CX-ZS1530.653192.2610.7250.999 7
2.5 下、造沙轮次酿造过程细菌组成及演替规律解析
筛选属水平上相对丰度>1%的优势细菌属,以解析下、造沙轮次酿造过程中高粱、母曲、母糟及糟醅的细菌群落特征,如图6所示。高粱的优势菌属是叶绿体门未分类菌属(norank_Chloroplast);母糟的优势菌属为未分类乳杆菌属(unclassified_Lactobacillaceae);而母曲的优势菌属是枝芽孢杆菌属(Virgibacillus)与克罗彭斯特德氏菌属(Kroppenstedtia)。据报道,乳杆菌属(Lactobacillus)可以通过发酵糖产生有机酸和二乙酰,为乳酸乙酯等酯类的生成提供前体物质,还可以通过调节发酵环境的pH值,抑制发酵前期部分腐败微生物的生长。枝芽孢杆菌属在黄色大曲中占比最高,与多种酶活性和风味物质关联[24],克罗彭斯特德氏菌属在黑色大曲中占比最高,与氨基酸、脂质、有机酸等风味底物代谢有关[25-26]。
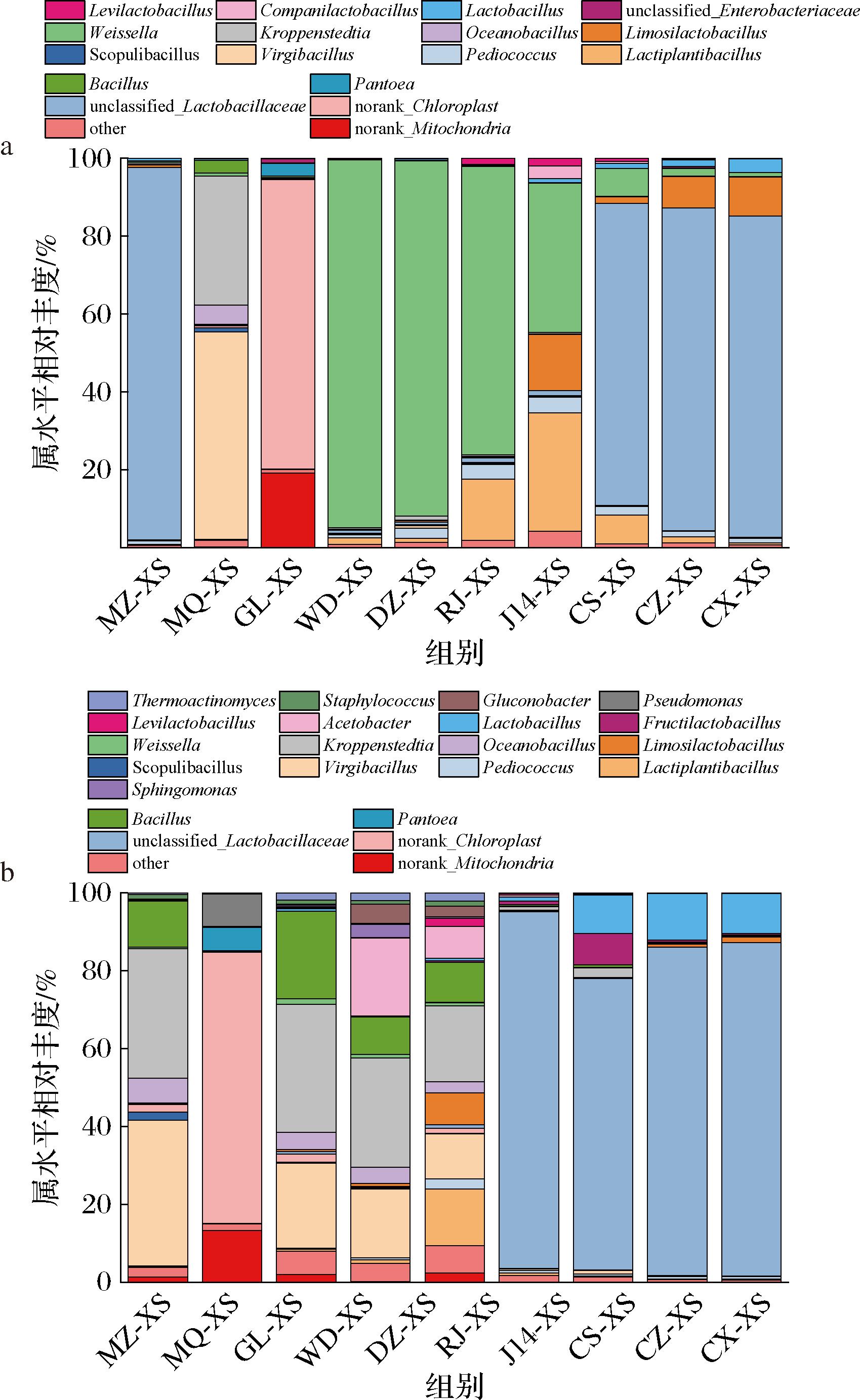
a-下沙;b-造沙
图6 下沙和造沙轮次酿造过程中原料及糟醅的属水平的细菌群落组成
Fig.6 Bacterial community composition at the genus level in raw materials and fermented grains during the Xiasha and Zaosha rounds of brewing
糟醅样品中,下沙轮次堆积发酵环节以魏斯氏菌属(Weissella)为主,并且其相对丰度随堆积发酵逐渐递减,魏斯氏菌属是乳酸菌的一种,在白酒酿造过程中主要作用为产酸,可产生蛋白酶、脂肪酶和纤维素酶等酶类,为发酵提供酸性环境[27-28]。造沙轮次堆积发酵环节的细菌群落构成更为复杂,以克罗彭斯特德氏菌属(19.54%~32.93%)、枝芽孢杆菌属(11.51%~21.88%)及芽孢杆菌属(Bacillus)(9.69%~22.56%)为主,该组成特征与原料母曲的菌群结构较为接近。芽孢杆菌属能够在发酵过程中产生蛋白酶、淀粉酶、糖化酶等关键酶类,水解原料中的大分子物质,还可通过美拉德反应等促进吡嗪类、酸类等对酱香风味贡献显著的风味物质生成[5]。此外,下、造沙轮次出窖糟醅的细菌群落结构较为接近,并与原料母糟呈现高度相似性。
2.6 下、造沙轮次酿造过程中细菌群落的功能性分析
进一步分析下、造沙轮次酿造过程中细菌群落的功能特征,不同轮次样品的KEGG代谢途径差异如图7所示。结果显示,2组样本的代谢途径组成及比例整体相近,丰度排名前五的代谢途径按由高到低顺序排列,依次为碳水化合物代谢、氨基酸代谢、辅因子与维生素代谢、萜类和聚酮类化合物代谢及脂质代谢,其中碳水化合物代谢、氨基酸代谢、及脂质代谢均与酸类化合物的生成有关[29-30]。研究表明碳水化合物的分解代谢(如糖酵解、三羧酸循环等)是有机酸(如丙酮酸、乳酸、柠檬酸等)生成的核心途径,通过一系列酶促反应将糖类物质转化为各类有机酸,是微生物代谢中有机酸的直接来源[9]。与其相比,氨基酸代谢则是有机酸的间接来源,蛋白质在蛋白酶的作用下水解为多种游离氨基酸,其中部分氨基酸可在脱氨基或转氨基反应后生成α-酮酸,再通过糖酵解或三羧酸循环进一步代谢,如丙氨酸可转化为丙酮酸,天冬氨酸可代谢为草酰乙酸,谷氨酸则可生成α-酮戊二酸等,这些中间代谢物不仅参与能量生成,也为有机酸的合成提供关键底物[31-32]。
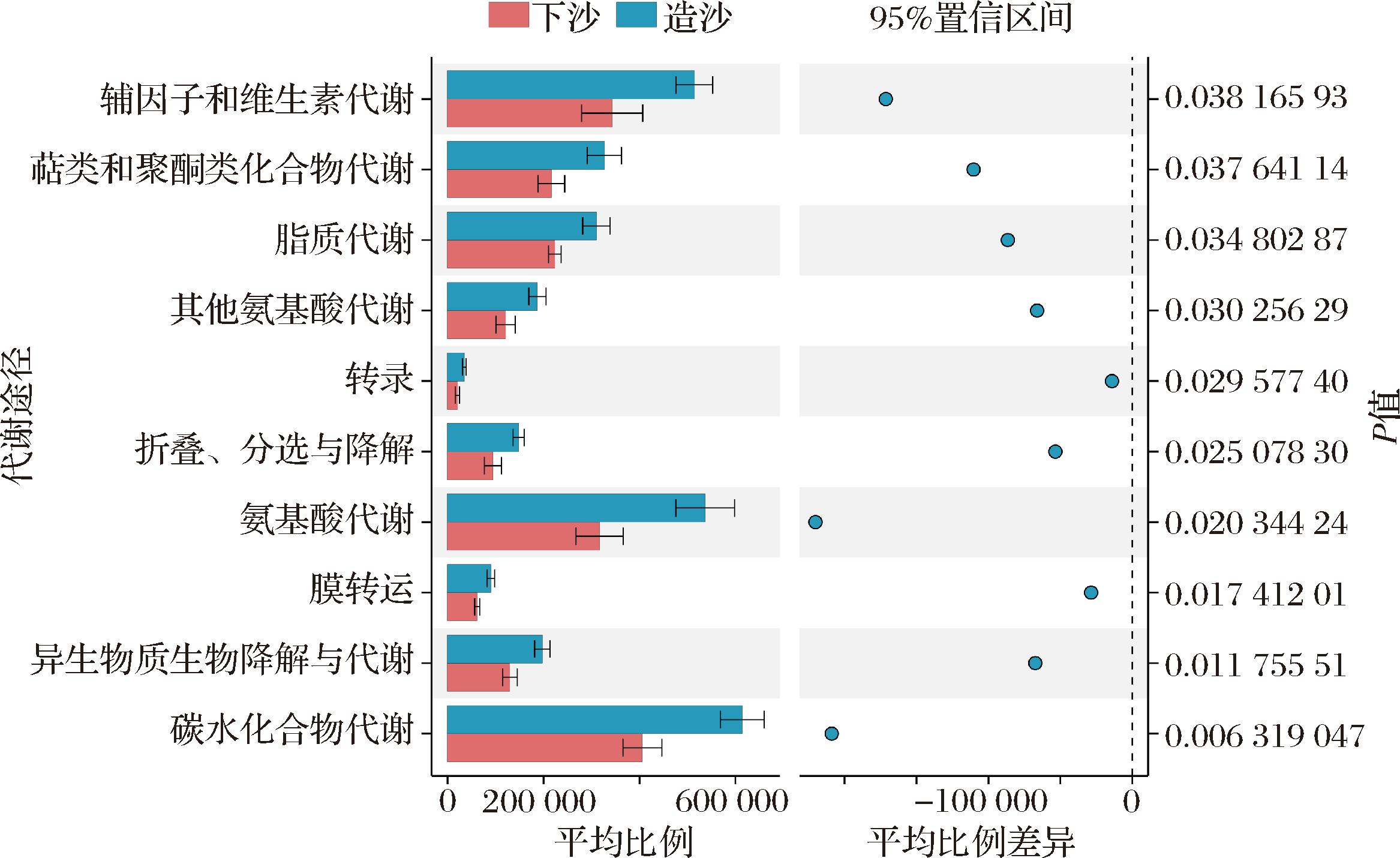
图7 下、造沙轮次酿造过程中原料及糟醅的细菌群落功能性分析STAMP图
Fig.7 STAMP diagram of functional analysis of bacterial communities in raw materials and fermented grains during the Xiasha and Zaosha round brewing process
注:图中左侧为不同功能在2组样本中的丰度,中间为95%置信区间内的功能丰度差异,右侧为t检验的P值。
2.7 下、造沙轮次酿造过程中有机酸转化关联性分析
白酒酿造过程中原料的氨基酸可通过参与微生物的生命代谢活动生成有机酸,“氨基酸-微生物-有机酸”的转化过程存在复杂的关联机制。氨基酸与微生物关联分析结果如图8所示。高粱、母曲、母糟及糟醅中的游离氨基酸与部分优势菌属存在显著相关性,并以负相关为主,其中除胱氨酸与蛋氨酸外,所有氨基酸均与枝芽孢杆菌属、海洋芽孢杆菌属(Oceanobacillus)和克罗彭斯特菌属等呈显著负相关关系。WEI等[14]研究证实,在酱香型白酒发酵中,枝芽孢杆菌属的丰度与亮氨酸、异亮氨酸等支链氨基酸含量呈负相关,其代谢活动可能通过生成异丁酸等短链脂肪酸消耗底物氨基酸。海洋芽孢杆菌属是高温大曲的常见菌属,已被证实涉及糖酵解、糖异生等代谢途径,糖酵解是细胞能量代谢的核心过程之一,主要通过将葡萄糖转化为丙酮酸,生成的丙酮酸还可以转化为乙酰辅酶A供三羧酸循环使用,或通过乳酸脱氢酶转化为乳酸,其糖酵解途径与氨基酸代谢的协同作用可能推动有机酸生成[33]。
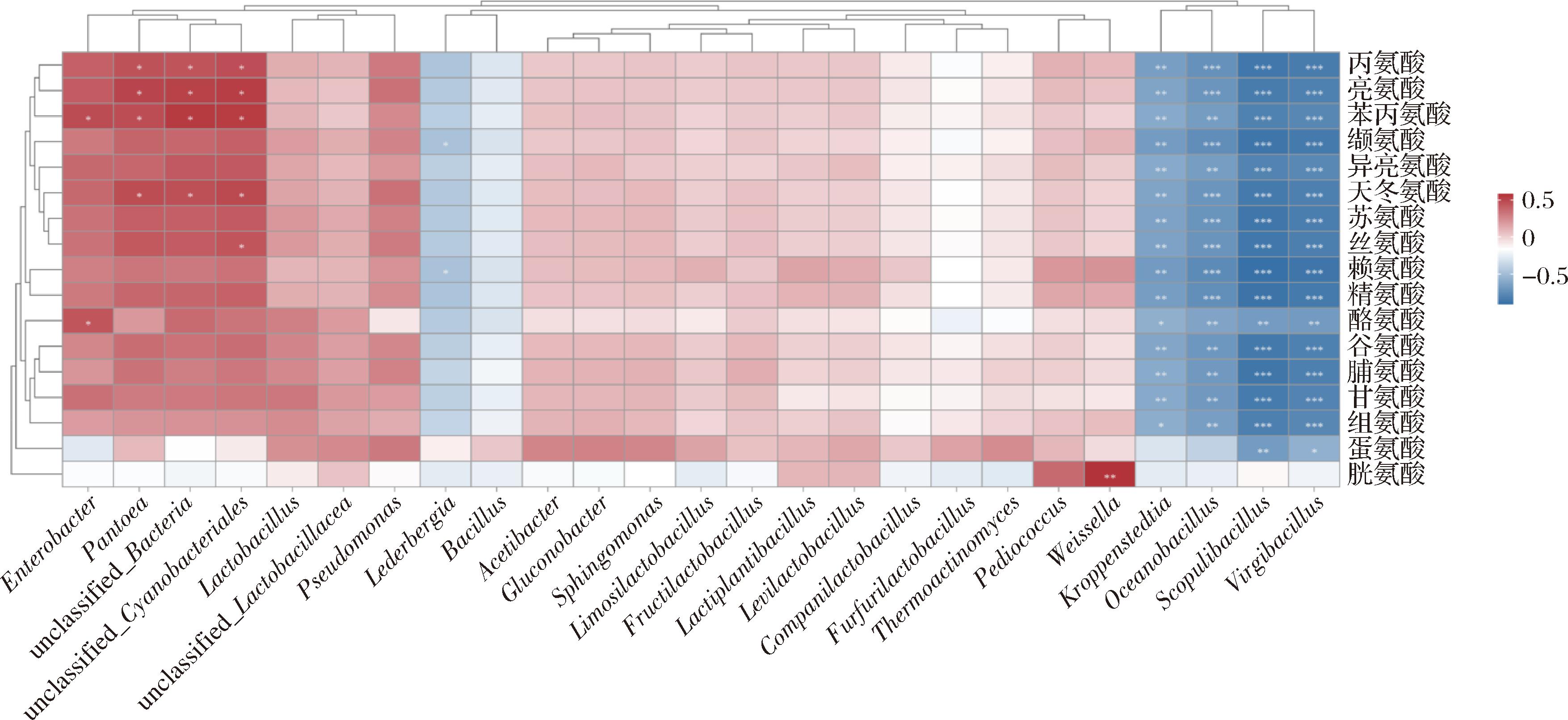
图8 下、造沙轮次所用原料以及糟醅中游离氨基酸与细菌群落结构间的相关性
Fig.8 Correlation between free amino acids and bacterial community structure in raw materials and fermented grains used in the Xiasha and Zaosha round brewing process
进一步对微生物与有机酸进行关联分析,如图9所示,多种有机酸与酿造过程中的优势细菌属呈现出显著的正相关关系。其中,乳杆菌属与乳酸、乙酸、丙酸及戊酸等多种有机酸均存在显著相关性,是酿造过程中主要的产酸菌属。此外,其他细菌属也展现出一定的产酸能力。例如,未分类乳杆菌属(unclassified_Lactobacillaceae)与乳酸、乙酸正相关;粘液乳杆菌属(Limosilactobacillus)与丙酸正相关;火山渣芽孢杆菌属(Scopulibacillus)与异戊酸、异丁酸正相关。不仅如此,异丁酸还与克罗彭斯特菌属、莱德伯格氏菌属(Lederbergia)、海洋芽孢杆菌属、枝芽孢杆菌属等多种细菌属呈现出显著的正相关性。
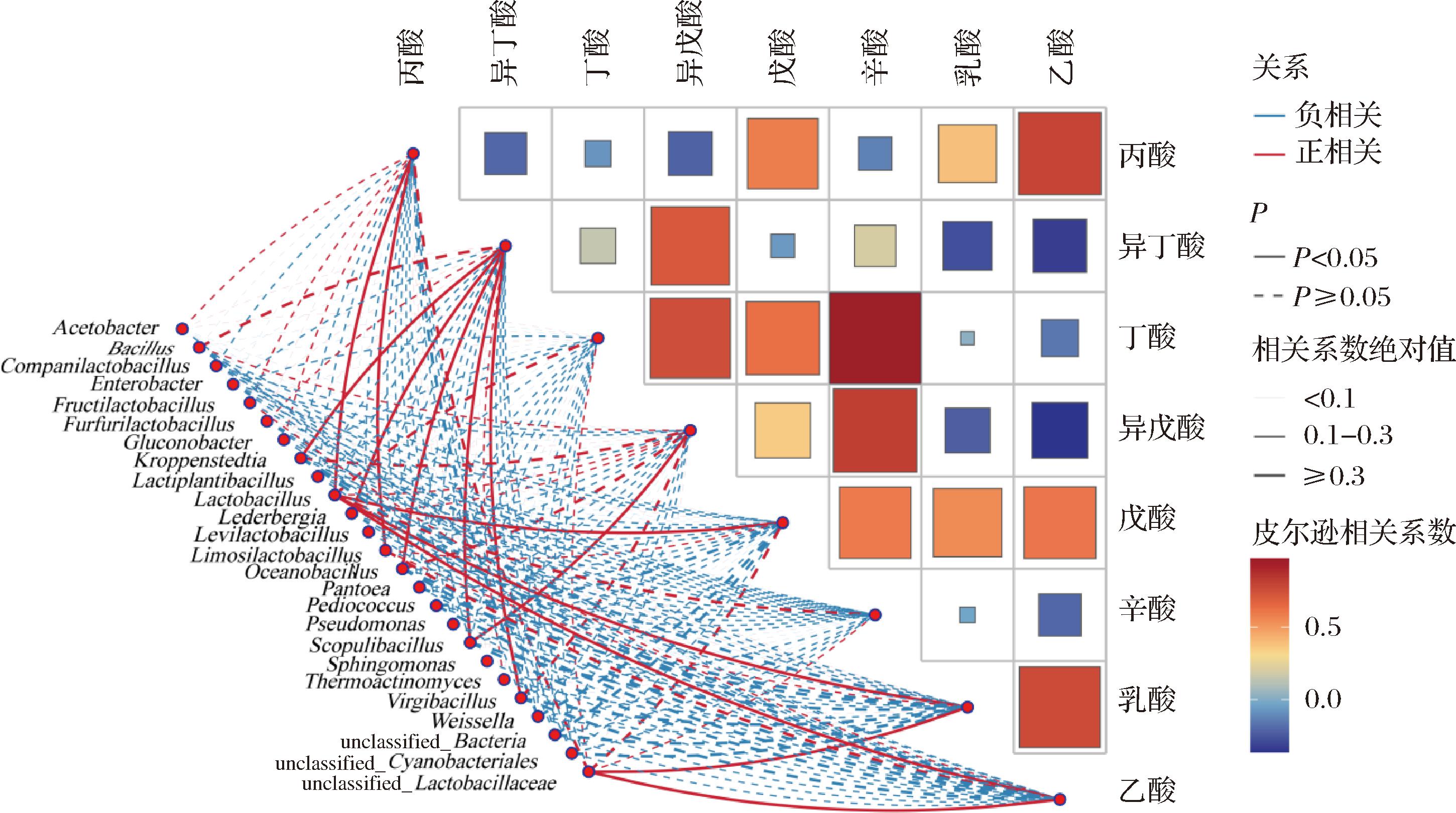
图9 下、造沙轮次所用原料以及糟醅中细菌群落结构与有机酸的相关性
Fig.9 Correlation between bacterial community structure and organic acids in raw materials and fermented grains used in the Xiasha and Zaosha round brewing process
3 结论
本研究利用气相色谱、高效液相色谱、高通量测序等技术,并结合多元统计分析方法,系统分析了酱香型白酒下、造沙轮次酿造过程母糟、母曲、高粱及糟醅的有机酸、游离氨基酸及细菌群落等方面的变化规律及关联作用。结果表明酿造过程有机酸主要来源于酿造发酵阶段,且随发酵推进和轮次演替,有机酸含量不断提高,其中,乳酸、乙酸含量显著高于其他有机酸,并主要在窖池发酵阶段生成。有机酸的生成与氨基酸及微生物间存在复杂的转化关系,氨基酸层面,原料中的氨基酸较酿造过程中的更为丰富,其中酸性氨基酸天冬氨酸和谷氨酸在酿造原料及糟醅中占主导地位,极有可能是构成酱香一轮次酒酸香特征的重要前体物质;微生物层面,高通量测序结果表明,未分类乳杆菌属、枝芽孢杆菌属等是酿造原料中的优势菌属,魏斯氏菌属、克罗彭斯特菌属、枝芽孢杆菌属等是酿造发酵阶段的优势菌属。此外,关联性分析发现,原料及糟醅中的大部分游离氨基酸与酿造过程中的优势菌属枝芽孢杆菌属、海洋芽孢杆菌属和克罗彭斯特菌属存在显著负相关关系;同时酿造过程中的优势菌属亦与多种有机酸显著正相关,如乳杆菌属与乳酸、乙酸、丙酸以及戊酸的生成相关,克罗彭斯特菌属、莱德伯格氏菌属、海洋芽孢杆菌属、枝芽孢杆菌属等与异丁酸的生成相关。本研究揭示了碳水化合物代谢和氨基酸代谢是酱香型白酒酿造过程中微生物代谢的主要途径,“氨基酸-微生物-有机酸”之间存在复杂关联,本研究为一轮次基酒酸香风味的形成机制提供了理论依据。
[1] LIU H L, SUN B G.Effect of fermentation processing on the flavor of Baijiu[J].Journal of Agricultural and Food Chemistry, 2018, 66(22):5425-5432.
[2] 孙优兰, 骆红波, 王金龙, 等.酱香型白酒不同轮次基酒风味特征分析[J].食品与发酵工业, 2024, 50(17):343-352.SUN Y L, LUO H B, WANG J L, et al.Analysis of flavor characteristics of different rounds base liquor for Jiangxiangxing Baijiu[J].Food and Fermentation Industries, 2024, 50(17):343-352.
[3] 余小斌, 黄张君, 刘小刚, 等.酱香型不同轮次及等级基酒的感官和风味成分特征分析[J].中国酿造, 2024, 43(8):61-73.YU X B, HUANG Z J, LIU X G, et al.Analysis of sensory and flavor components characteristics of sauce-flavor Baijiu base liquor with different rounds and grades[J].China Brewing, 2024, 43(8):61-73.
[4] 石馨, 范宸铭, 张方利, 等.酱香型轮次原酒特征风味与感官特性的差异性分析[J].中国酿造, 2025, 44(1):92-99.SHI X, FAN C M, ZHANG F L, et al.Analysis on the difference of characteristic flavor and sensory characteristics of sauce-flavor rounds original liquor[J].China Brewing, 2025, 44(1):92-99.
[5] 何东梅. 基于风味组学对贵州酱香轮次基酒风味结构的解析[D].贵阳:贵州大学, 2021.HE D M.The analysis of flavor structure in Guizhou sauce-flavor base liquors from different fermentation rounds based on flavoromics[D].Guiyang:Guizhou University, 2021.
[6] GAO W J, FAN W L, XU Y.Characterization of the key odorants in light aroma type Chinese liquor by gas chromatography-olfactometry, quantitative measurements, aroma recombination,and omission studies[J].Journal of Agricultural and Food Chemistry, 2014, 62(25):5796-5804.
[7] 云敏, 周洪楷.有机酸在酱香型白酒酿造过程的调控作用[J].酿酒科技, 2011(7):44-46.YUN M, ZHOU H K.Regulating roles of organic acids in the production process of Maotai-flavor liquor[J].Liquor-Making Science &Technology, 2011(7):44-46.
[8] 唐维川, 孔祥凯, 王婷, 等.基于主成分分析法评价酱香型白酒的不同轮次基酒[J].现代食品科技, 2021, 37(7):269-277;268.TANG W C, KONG X K, WANG T, et al.Evaluation of different rounds of Moutai-flavor Baijiu based on principal component analysis[J].Modern Food Science and Technology, 2021, 37(7):269-277;268.
[9] YANG L, XIAN C, LI P, et al.The spatio-temporal diversity and succession of microbial community and its environment driving factors during stacking fermentation of Maotai-flavor Baijiu[J].Food Research International, 2023, 169:112892.
[10] SHI W, CHAI L J, ZHAO H, et al.Deciphering the effects of different types of high-temperature Daqu on the fermentation process and flavor profiles of sauce-flavor Baijiu[J].Food Bioscience, 2024, 61:104917.
[11] 宋娟, 张霁红, 康三江, 等.乙酸-2-苯乙酯的合成途径与调节研究[J].西南大学学报(自然科学版), 2018, 40(8):25-31.SONG J, ZHANG J H, KANG S J, et al.A study on the synthetic pathways and regulation of acetic acid-2-phenyl ethyl ester[J].Journal of Southwest University (Natural Science Edition), 2018, 40(8):25-31.
[12] 杨康丽, 苏伟, 母应春, 等.洞酿酱香型白酒下沙轮次微生物多样性与理化品质相关性分析[J].中国食品添加剂, 2025, 36(5):33-42.YANG K L, SU W, MU Y C, et al.Correlation analysis of microbial diversity and physicochemical properties during Xiasha rounds of Dongniang Maotai-flavor Baijiu[J].China Food Additives, 2025, 36(5):33-42.
[13] SANCEDA N G, SUZUKI E, KURATA T.Development of normal and branched chain volatile fatty acids during the fermentation process in the manufacture of fish sauce[J].Journal of the Science of Food and Agriculture, 2001, 81(10):1013-1018.
[14] WEI J L, LU J, NIE Y, et al.Amino acids drive the deterministic assembly process of fungal community and affect the flavor metabolites in Baijiu fermentation[J].Microbiology Spectrum, 2023, 11(2):e02640-e02622.
[15] 朱安然, 汪地强, 胡建锋, 等.酱香型白酒一轮次糟醅微生物群落结构及溯源分析[J].食品科学, 2025, 46(4):117-125.ZHU A R, WANG D Q, HU J F, et al.Microbial community structure and traceability in fermented grains for Jiang-flavor Baijiu during the first round of fermentation[J].Food Science, 2025, 46(4):117-125.
[16] 黄廷财, 柴丽娟, 时伟, 等.酱香型白酒第2、3轮次堆积发酵有机酸代谢规律与菌群结构及其相关性解析[J].食品科学, 2024, 45(18):106-115.HUANG T C, CHAI L J, SHI W, et al.Microbial community structure and organic acid metabolism and their correlation in the second and third rounds of stacking fermentation of sauce-flavor Baijiu[J].Food Science, 2024, 45(18):106-115.
[17] 倪兴婷, 孙细珍, 严玲, 等.白酒中重要风味物质的味觉阈值测定[J].食品与发酵工业, 2025,51(22):376-381.NI X T, SUN X Z, YAN L, et al.Determination of taste threshold of important flavor substances in Baijiu[J].Food and Fermentation Industries, 2025,51(22):376-381.
[18] 邱显平, 黄桥, 杨静, 等.浓香型白酒在新、老窖池发酵过程中酒醅微生物群落结构差异分析[J].中国酿造, 2024, 43(1):50-56.QIU X P, HUANG Q, YANG J, et al.Differences of microbial community structure in fermented grains during strong-flavor Baijiu fermentationin new and old pits[J].China Brewing, 2024, 43(1):50-56.
[19] 罗珍岑, 杨宗朋, 赵艳军, 等.乳酸菌对固态发酵食醋品质提升的研究进展[J].食品研究与开发, 2024, 45(21):217-224.LUO Z C, YANG Z P, ZHAO Y J, et al.Research progress on quality improvement of solid-state fermented vinegar using lactic acid bacteria[J].Food Research and Development, 2024, 45(21):217-224.
[20] 何艾莲, 冯珊, 程华峰, 等.酱香型白酒酿造过程中微生物的多样性研究[J].中国食品工业, 2024(19):137-139.HE A L, FENG S, CHENG H F, et al.Study on microbial diversity in the brewing process of Maotai-flavor Liquor[J].China Food Industry, 2024(19):137-139.
[21] 刘正, 秦培军, 卢延想, 等.酱香型白酒酿造过程中微生物多样性及代谢过程研究进展[J].中国酿造, 2022, 41(6):6-11.LIU Z, QIN P J, LU Y X, et al.Research progress of microbial diversity and metabolic process during the fermentation of sauce-flavor Baijiu[J].China Brewing, 2022, 41(6):6-11.
[22] 丁晨红, 王英, 王威利, 等.鱼粉中酸碱性氨基酸及呈味氨基酸含量特点研究[J].饲料工业, 2018, 39(16):49-52.DING C H, WANG Y, WANG W L, et al.Study on the contents of acidic and basic amino acids and flavor amino acids in fish meal[J].Feed Industry, 2018, 39(16):49-52.
[23] WANG L Q, TANG P, ZHAO Q, et al.Difference between traditional brewing technology and mechanized production technology of Jiangxiangxing Baijiu:Micro ecology of Zaopei, physicochemical factors and volatile composition[J].Food Research International, 2024, 192:114748.
[24] 张英, 胡景辉, 张娇娇, 等.基于微生物组学技术探究不同大曲品质与酿造性能的相关性[J].食品工业科技, 2026,47(6):150-159.ZHANG Y, HU J H, ZHANG J J, et al.Based on microbiome technology, the correlation between quality and brewing performance of different Daqu was explored[J].Science and Technology of Food Industry, 2026,47(6):150-159.
[25] DONG W W, YU X, WANG L Y, et al.Unveiling the microbiota of sauce-flavor Daqu and its relationships with flavors and color during maturation[J].Frontiers in Microbiology, 2024, 15:1345772.
[26] DU Y K, XIN W, XIA Y, et al.Analysis of fermentation control factors on volatile compounds of primary microorganisms in Jiang-flavor Daqu[J].Journal of Food Biochemistry, 2022, 46(10):e14277.
[27] FUSCO V, CHIEFFI D, FANELLI F, et al.The Weissella and Periweissella genera:Up-to-date taxonomy, ecology, safety, biotechnological, and probiotic potential[J].Frontiers in Microbiology, 2023, 14:1289937.
[28] 谢铃, 刘双平, 刘甜甜, 等.辣蓼草对酒药关键微生物与品质的影响研究[J].食品与发酵工业, 2024, 50(23):53-61.XIE L, LIU S P, LIU T T, et al.Effects of Polygonum hydropiper L. on key microorganisms and quality in Jiuyao[J].Food and Fermentation Industries, 2024, 50(23):53-61.
[29] GUAN T, LIU B, WANG R, et al.The enhanced fatty acids flavor release for low-fat cheeses by carrier immobilized lipases on O/W Pickering emulsions[J].Food Hydrocolloids, 2021, 116:106651.
[30] 王三, 周姝芯, 汤凯, 等.新疆哈萨克奶酪特征风味物质与微生物群落结构解析[J].食品与发酵工业, 2026,52(4):143-152.WANG S, ZHOU S X, TANG K, et al.Comprehensive analysis of characteristic flavor compounds and microbial community composition in Xinjiang Kazak cheese[J].Food and Fermentation Industries, 2026,52(4):143-152.
[31] 圣群航, 王俊麟, 彭东, 等.襄阳地区中温大曲细菌多样性及其滋味品质解析[J].食品与发酵工业, 2026,52(5):186-194.SHENG Q H, WANG J L, PENG D, et al.Analysis of bacterial diversity and taste quality of medium-temperature Daqu from Xiangyang, China[J].Food and Fermentation Industries, 2026,52(5):186-194.
[32] 陈群群, 邓洋, 杨珍珠, 等.酸肉发酵过程中碳源代谢对其品质的影响研究进展[J].食品与发酵工业, 2026,52(2):412-420.
CHEN Q Q, DENG Y, YANG Z Z, et al.Recent advances in the effects of carbon source metabolism on the quality of sour meat during fermentation[J].Food and Fermentation Industries, 2026,52(2):412-420.
[33] WU S L, DU H, XU Y.Daqu microbiota adaptability to altered temperature determines the formation of characteristic compounds[J].International Journal of Food Microbiology, 2023, 385:109995.