葡萄的品质对葡萄酒的风味起着决定性作用[1],而葡萄的风味品质又深受其糖酸代谢的调控[2],其中糖分和有机酸的积累与平衡直接决定了果实的甜度、酸度以及整体的风味口感。葡萄中的糖主要由葡萄糖(glucose,Glu)、果糖(fructose,Fru)和蔗糖(sucrose,Suc)组成。当蔗糖含量较低时,葡萄糖和果糖占主导地位,但蔗糖是葡萄中的主要转运糖[3]。据研究表明,蔗糖代谢是葡萄糖分积累的关键途径,它不仅为浆果生长提供碳源和能量,而且还能增加葡萄果实中的糖浓度并改善风味品质[4]。此外,葡萄中的有机酸以苹果酸(malic acid,MA)和酒石酸(tartaric acid,TA)为主,其中酒石酸含量虽高但不参与主要代谢过程,而柠檬酸(citric acid,CA)的含量相对较低[5]。因此,在葡萄的生长发育过程中,苹果酸发挥着至关重要的作用。其中烟酰胺腺嘌呤二核苷酸-苹果酸脱氢酶(nicotinamide adenine dinucleotide-malic dehydrogenase,NAD-MDH)、烟酰胺腺嘌呤二核苷酸磷酸-苹果酸酶(nicotinamide adenine dinucleotide phosphate-malic enzyme,NADP-ME)和磷酸烯醇式丙酮酸羧化酶(phosphoenolpyruvate carboxylase,PEPC)作为调控苹果酸合成与分解的关键酶[6-7],其基因表达水平可能受到微量元素供给的影响。然而,目前关于喷施微量元素对酿酒葡萄有机酸代谢相关酶基因(NAD-MDH、NADP-ME、PEPC)表达的调控机制尚缺乏系统研究。
焉耆盆地地处北纬41°~42°,与法国波尔多纬度相近,属中温带干旱大陆性气候;该地区光热资源丰富,年均日照时数超过3 100 h,昼夜温差大,能为酿酒葡萄栽培提供良好的自然条件[8]。但长期以来,氮磷钾肥的过量使用导致土壤中锰(Mn)、锌(Zn)、硼(B)、钼(Mo)、铜(Cu)等微量元素匮乏,造成葡萄糖酸比例失调,严重影响品质与产量。因此,为改善葡萄品质,应及时补充微量元素肥料。叶面肥是一种专为叶片表面设计的液体肥料,可通过叶表皮与气孔等通道迅速吸收;与土壤施肥相比,叶面施肥展现出简便易行、环境风险低、用量小、养分利用率高及吸收迅速等显著优势[9]。不同植物对各类肥料的浓度需求存在显著差异。若施用浓度过低,喷施后难以达到预期的施肥效果;反之,若浓度过高,则极易引发肥害现象。因此,应在确保不引发肥害及毒素症的前提下,精准把控叶面肥的最佳施用浓度。常用叶面肥用量为硫酸锰1~3 g/L、硫酸锌1~4 g/L、硫酸铜0.1~0.2 g/L、钼酸铵0.2~1 g/L、硼砂2 g/L左右[10]。果树常用叶面喷施微量元素肥包括硼酸或硼砂、硫酸锰、硫酸铜、硫酸锌等,一般喷施质量浓度为1~5 g/L。适宜的微量元素供给对植物生理代谢具有关键调控作用,其能激活酶系统、维持细胞代谢活性,从而使葡萄品质得到改善。八硼酸钠可调控草莓糖酸代谢,提高蔗糖代谢相关酶活性并降低有机酸含量[11];硼锌铜复合肥能增强芹菜的抗氧化酶活性[12]。
本试验中以马瑟兰酿酒葡萄为试材,进行不同浓度的微量元素混合液(Mn、Zn、Cu、Mo、B)叶面喷施处理,测定不同生育期果实糖酸组分含量、相关代谢酶活性及微量元素含量。同时,检测了NAD-MDH、NADP-ME和PEPC基因表达的变化。从而筛选出最佳处理浓度,并探究微量元素的调控机理,为优化葡萄栽培管理、提升果实品质提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
马瑟兰葡萄采自新疆焉耆县乡都酒庄,采摘后立即置于冰盒中转运至实验室,经液氮速冻后,转移至-80 ℃超低温箱备用。
1.1.2 试剂
葡萄糖、蔗糖、果糖、酒石酸、苹果酸、草酸(oxalic acid,OA)、CA对照品均购于上海甄准生物科技有限公司;色谱乙腈、色谱三乙胺购于德国Merck公司;磷酸、蒽酮、硫酸锰、七水合硫酸锌、五水合硫酸铜、四水合钼酸铵、十水合四硼酸钠购于国药集团化学试剂有限公司;蔗糖合成酶合成方向(sucrose synthase synthetic direction,SS-ss)、蔗糖合成酶分解方向(sucrose synthase decomposition direction,SS-sc)、蔗糖磷酸合成酶(sucrose phosphate synthase,SPS)、酸性转化酶(acid invertase,AI)、中性转化酶(neutral invertases,NI)、NADP-ME、PEPC、柠檬酸合酶(citrate synthase,CS)、NAD-ME试剂盒均购于北京索莱宝科技有限公司;线粒体乌头酸酶(mitochondrial aconitase,Mit-ACO)、细胞质乌头酸酶(cytoplasmic aconitase,Cyt-ACO)及烟酰胺腺嘌呤二核苷酸-异柠檬酸脱氢酶(nicotinamide adenine dinucleotide-isocitrate dehydrogenase,NAD-IDH)试剂盒购于上海依赫生物科技有限公司。
1.2 仪器与设备
XH-C涡旋混合器,金坛区白塔新宝仪器厂;Agilent 126 0 Infinity Ⅲ高效液相色谱仪,美国安捷伦科技公司;SpectraMax 190全波长酶标仪,美谷分子仪器有限公司;TG-16G台式高速冷冻离心机,湖南凯达科学仪器有限公司;ABI 7500实时荧光定量PCR仪,Applied Biosystems;NexION 1000G电感耦合等离子体质谱仪,珀金埃尔默股份有限公司。
1.3 实验方法
1.3.1 采前处理
设置3个浓度梯度,T1、T2、T3[其化合物名称和浓度见电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.044706,下同)所示],以清水为对照(CK)。每个处理于开花期、坐果期、膨大期和转色期进行叶面喷施,每次喷施至叶片完全湿润滴液,选风力不大的傍晚,以延缓雾滴风干,便于离子渗透。每个处理6株,3次重复,所选用的肥料为Mn肥、Zn肥、Cu肥、Mo肥和B肥混合叶面肥。实验分别于果实坐果期、膨大期、转色期(处理后第5天)及成熟期进行采样。
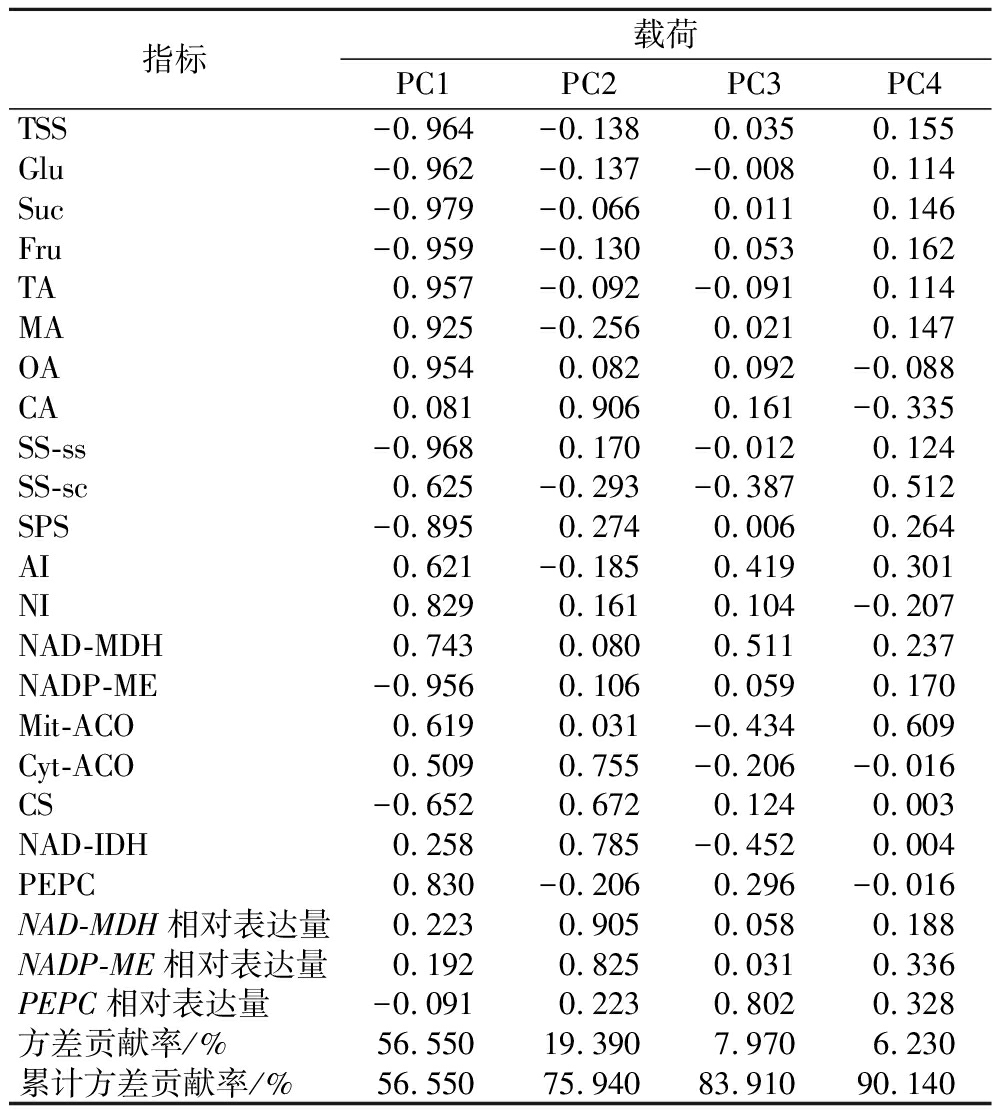
表1 葡萄果实糖酸、相关酶活以及酸代谢关键基因主成分载荷矩阵与方差贡献率
Table 1 Principal component loadings matrix and variance contribution of sugar and acid, related enzyme activities, and key genes in acid metabolism of grape fruits
指标载荷PC1PC2PC3PC4TSS-0.964-0.1380.0350.155Glu-0.962-0.137-0.0080.114Suc-0.979-0.0660.0110.146Fru-0.959-0.1300.0530.162TA0.957-0.092-0.0910.114MA0.925-0.2560.0210.147OA0.9540.0820.092-0.088CA0.0810.9060.161-0.335SS-ss-0.9680.170-0.0120.124SS-sc0.625-0.293-0.3870.512SPS-0.8950.2740.0060.264AI0.621-0.1850.4190.301NI0.8290.1610.104-0.207NAD-MDH0.7430.0800.5110.237NADP-ME-0.9560.1060.0590.170Mit-ACO0.6190.031-0.4340.609Cyt-ACO0.5090.755-0.206-0.016CS-0.6520.6720.1240.003NAD-IDH0.2580.785-0.4520.004PEPC0.830-0.2060.296-0.016NAD-MDH相对表达量0.2230.9050.0580.188NADP-ME相对表达量0.1920.8250.0310.336PEPC相对表达量-0.0910.2230.8020.328方差贡献率/%56.55019.3907.9706.230累计方差贡献率/%56.55075.94083.91090.140
1.3.2 果实可溶性总糖(total soluble solid,TSS)、葡萄糖、果糖、蔗糖含量及代谢相关酶活性测定
可溶性总糖含量的测定采用蒽酮试剂法,标准曲线为:y=209.932 7x-0.303 2,R2=0.998 1。葡萄糖、果糖、蔗糖的含量使用高效液相色谱仪测定[13]。色谱柱条件:Waters XBridge Amide(4.6 mm×150 mm,5 μm),柱温:35 ℃,流动相为30%(体积分数)乙腈-水溶液和80%乙腈-水溶液,流速1 mL/min,进样量为10 μL,检测波长254 nm。葡萄糖、果糖、蔗糖的标准曲线分别为:y=1.074x+0.720 7(R2=0.998 6)、y=1.205 5x+0.463 1(R2=0.996 9)、y=1.121 9x+0.706 7(R2=0.999 1)。
根据试剂盒方法测定蔗糖代谢相关酶活性。称取液氮研磨的马瑟兰葡萄组织0.1 g,分别加入1 mL相应提取液,冰浴匀浆。SS-ss、SS-sc及SPS提取液于4 ℃、8 000×g离心10 min;AI及NI提取液于4 ℃、12 000×g离心10 min。收集各上清液,置于冰上备用待测。所有指标的测定均严格依照试剂盒说明书进行操作,并设置3次重复实验,实验结果依据说明书提供的方法进行计算与表述。
1.3.3 果实有机酸含量及代谢相关酶活性的测定
苹果酸、酒石酸、草酸和柠檬酸的含量使用高效液相色谱仪测定[5],色谱柱条件为:Waters XSelect HSS T3(250 mm×4.6 mm,3.5 μm),柱温:35 ℃,流动相为0.02 mol/L NH4H2PO4水溶液(pH=2.7),流速为0.9 mL/min,进样量为10 μL,检测波长210 nm。苹果酸、酒石酸、柠檬酸、草酸的标准曲线分别为,y=0.544x+1.42(R2=0.999 5)、y=1.221x+0.452 1(R2=1)、y=0.779 8x-2.051 5(R2=1)、y=4.202 3x+13.833(R=0.999 1)。
有机酸代谢相关酶活性依据相应试剂盒说明书测定。取液氮研磨的马瑟兰葡萄果实组织,NAD-ME称取0.5 g,其余酶(NADP-ME、PEPC、CS)均称取0.1 g,各加入1 mL提取液冰浴匀浆。NAD-MDH、NADP-ME和PEPC的匀浆液于4 ℃、8 000×g离心10 min后取上清待测;CS的匀浆液经4 ℃、600×g离心5 min 后,取上清再于4 ℃、11 000×g离心10 min,收集上清待测。Mit-ACO、Cyt-ACO及NAD-IDH的活性采用ELISA法测定,具体提取方法参照牛冬青[13]的方法。
1.3.4 果实微量元素含量测定
称取冻干葡萄粉末0.1 g于聚四氟乙烯消解内罐,加硝酸5 mL浸泡过夜。盖好内盖,旋紧不锈钢外套,放入恒温干燥箱,80 ℃保持2 h,120 ℃保持2 h,再升至160 ℃保持4 h,在箱内自然冷却至室温,打开后加热赶酸至近干,将消化液洗入25 mL或者10 mL容量瓶中,用少量硝酸(1%,体积分数)洗涤内罐和内盖3次,洗液合并至容量瓶中并用1%硝酸定容至刻度,混匀备用。同时做空白实验。试液上机测定各元素含量。
1.3.5 酸代谢相关基因表达量的测定
总RNA的提取使用SteadyPure 通用型RNA提取试剂盒Ⅱ。RNA浓度和纯度通过全波长酶标仪测定,使用全氏金生物反转录试剂盒(AE311-02)将RNA反转录为cDNA。目的基因的引物由上海生工生物工程技术服务有限公司合成,具体序列如附表2所示。使用M5 HiPer SYBR® Premix Es TaqTM试剂盒及LightCycler 96®实时荧光定量PCR系统进行qPCR扩增,以测定基因表达水平。以β-actin作为内参基因,靶基因表达水平根据2-ΔΔCT方法计算。设置3个生物重复序列。
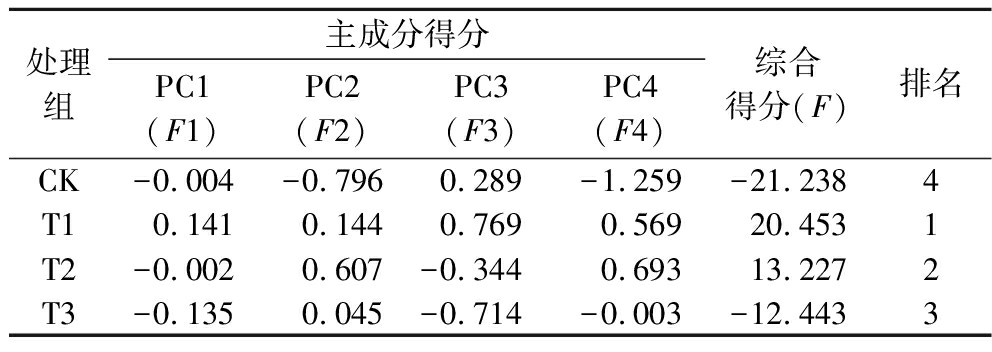
表2 微量元素喷施处理对马瑟兰葡萄主成分得分表
Table 2 Principal component scores of muscat grape under trace element foliar application treatments
处理组主成分得分PC1(F1)PC2(F2)PC3(F3)PC4(F4)综合得分(F)排名CK-0.004 -0.796 0.289 -1.259 -21.238 4T10.141 0.144 0.769 0.569 20.453 1T2-0.002 0.607 -0.344 0.693 13.227 2T3-0.135 0.045 -0.714 -0.003 -12.443 3
1.4 数据分析
待测样品均需进行3次平行测定,采用Excel软件处理数据,利用SPSS 19.0统计软件对数据进行方差分析、多重比较和相关性分析,使用Origin 2021绘图。
2 结果与分析
2.1 微量元素对葡萄果实可溶性总糖及糖组分含量的影响
如图1所示,在葡萄果实发育过程中,可溶性总糖、葡萄糖、蔗糖和果糖含量总体呈上升趋势,并在成熟期达到最高。不同发育阶段糖分积累存在明显差异:坐果期至膨大期增幅较小,而转色期至成熟期糖分迅速积累,表明转色期为关键时期。不同处理中,T2处理在多数时期表现出最佳的糖积累促进效果,尤其在成熟期,其可溶性总糖、蔗糖和果糖含量显著高于其他处理(P<0.05)。T1处理对糖积累也有积极影响,转色期和成熟期葡萄糖与果糖含量显著高于CK(P<0.05)。相比之下,T3处理对糖积累表现为抑制作用,其可溶性总糖、葡萄糖和果糖在成熟期显著低于CK及其他处理(P<0.05)。T1与T2处理对糖分积累的促进作用可能与锌和硼元素的协同作用有关。锌作为多种关键酶的辅因子,在增强植物光合能力和调控糖酵解途径中起重要作用[14];硼则主要促进光合产物(蔗糖)在韧皮部的运输[9,15]。二者协同作用促进了糖分的高效供应与积累。而T3处理对糖积累的抑制作用,可能由于喷施浓度过高,导致元素失衡,阻碍糖分的运输、转化与贮存。
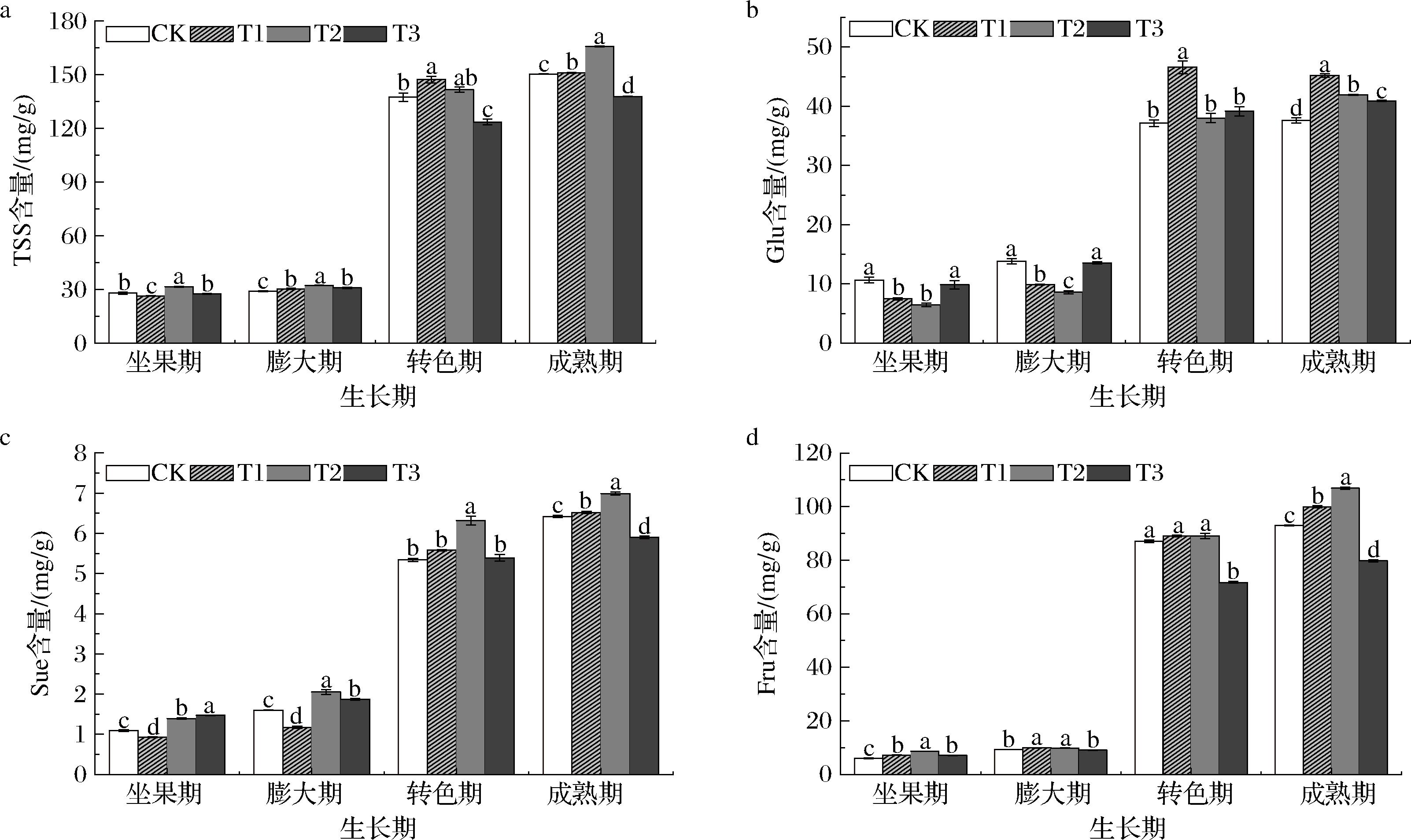
a-TSS含量;b-Glu含量;c-Suc含量;d-Fru含量
图1 喷施微量元素对葡萄果实可溶性总糖及糖组分含量的影响
Fig.1 Effects of spraying trace elements on the content of total soluble sugar and sugar components in grape fruit
注:不同小写字母表示组间存在显著差异(P<0.05)(下同)。
2.2 微量元素对葡萄果实糖代谢相关酶活性的影响
叶面喷施5种微量元素对马瑟兰葡萄果实蔗糖代谢相关酶活性有显著影响(图2)。如图2-a与图2-c所示,SS-ss和SPS活性在果实发育过程中总体呈上升趋势。两者作为蔗糖合成的限速酶[16],SS-ss可催化二磷酸核苷葡萄糖与果糖合成蔗糖[17],而SPS则调控蔗糖-6-磷酸的合成,促进蔗糖的积累与转化。T1、T2、T3处理的酶活性在各个生育期均显著高于CK处理组(P<0.05)。其中,T2处理对SS-ss和SPS活性的促进作用最为显著:在坐果期、膨大期、转色期和成熟期,SS-ss活性分别较CK提高了1.76、0.70、0.21、0.39倍;SPS活性分别提高了1.36、0.81、0.45、0.40倍。这些结果表明,叶面喷施微量元素混合液可以有效提升蔗糖代谢途径中SS-ss和SPS的活性,可能与锌元素的补充有关[14]。
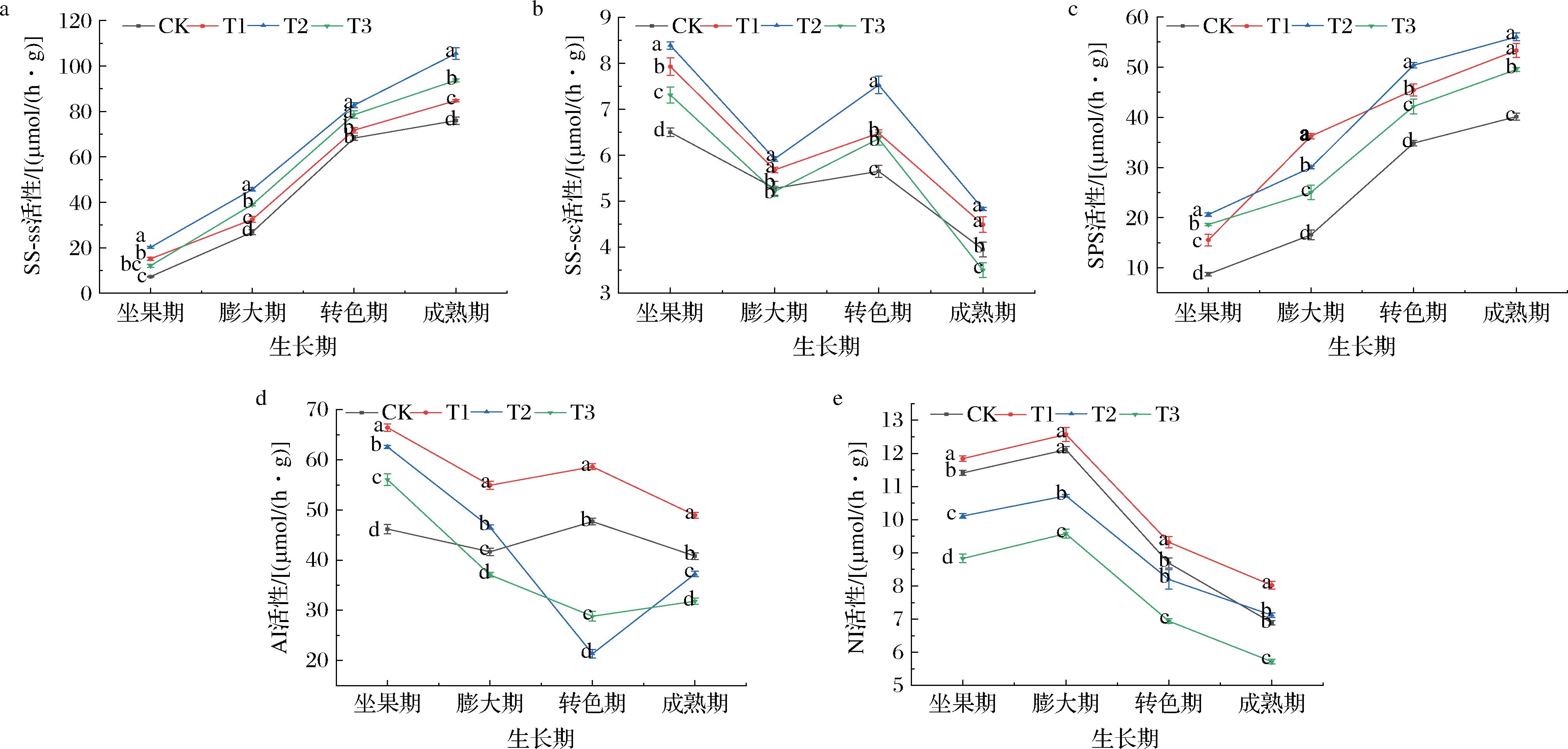
a-SS-ss活性;b-SS-sc活性;c-SPS活性;d-AI活性;e-NI活性
图2 喷施微量元素对葡萄果实糖代谢相关酶活性的影响
Fig.2 Effect of foliar application of trace elements on the activities of enzymes related to sugar metabolism in grape fruits
SS-sc(图2-b)活性呈波动变化趋势,坐果期开始缓慢下降,膨大期逐渐上升,随后再次下降,并在成熟期达到最低。在整个生长过程中,T2处理效果最佳,坐果期、膨大期、转色期和成熟期的活性分别较CK提高了29.08%、12.12%、33.27%、22.28%。该结果与闫玉静[18]的研究结论一致,表明T2处理中的适宜锌浓度可能通过稳定酶活性中心的构象、促进酶蛋白的合成,并在成熟期有效调控蔗糖分解与积累的动态平衡,从而实现对蔗糖代谢的关键调控作用。
AI活性在不同处理下表现出显著的阶段性差异(图2-d)。T1处理组的AI活性在整个发育期内呈下降趋势,但与对照相比,4个时期的酶活性仍分别显著提高(P<0.05)了43.79%、31.79%、22.91%、19.94%。表明适宜微量元素处理能持续增强AI活性[19],可能是通过促进蔗糖分解为果糖和葡萄糖,从而为果实发育提供更直接的碳源。T2和T3处理则显著(P<0.05)抑制了AI活性,其变化趋势总体表现为先下降后上升。说明喷施高浓度的微量元素可能会抑制AI活性,干扰其正常功能。
NI活性在果实发育过程中呈现动态变化(图2-e)。在坐果期缓慢上升,从膨大期至转色期逐渐下降,到成熟期NI活性达到最低。T1处理效果最佳,与CK相比,坐果期、膨大期、转色期及成熟期分别提高了3.77%、3.80%、7.25%、16.40%。相反,T3处理显著降低(P<0.05)了其活性,4个时期分别较对照降低了29.22%、26.41%、25.22%、20.45%。该结果与张妍妍[11]研究中硼处理可提高柑橘NI活性的结论相一致,表明T1处理对酶活的促进可能主要得益于适宜硼浓度通过维持细胞膜完整性及促进糖代谢底物运输实现的积极作用;而T3处理中过量硼元素则可能通过干扰酶构象或代谢反馈机制显著抑制NI活性。
2.3 微量元素对葡萄果实有机酸组分含量的影响
马瑟兰葡萄果实的有机酸主要由酒石酸和苹果酸构成,柠檬酸和草酸含量较低(图3)。在果实发育过程中,酒石酸和苹果酸含量总体呈递减趋势,苹果酸在成熟期降至最低,表明其代谢消耗最为显著。不同处理中,T2处理对有机酸积累效果最为显著。在酒石酸方面,T2处理在坐果期和成熟期的含量分别显著高于CK(P<0.05),提升了8.99%和13.77%。苹果酸在成熟期的含量以T2处理最高,比CK提高15.81%。草酸在果实发育早期含量较高,转色期开始下降,至成熟期略有上升,成熟期T2>T1>CK>T3,T2处理组草酸含量最高,为0.96 mg/g,显著高于其他处理组(P<0.05)。柠檬酸呈“N”型动态变化,T2处理在坐果期、膨大期和成熟期的含量分别提高了28.21%、38.96%、21.82%,显著高于CK(P<0.05)。T1处理在膨大期和成熟期的柠檬酸含量也显著高于CK组(P<0.05)。T1和T2处理有效减少了有机酸的消耗,可能是由于适宜浓度的锰促进了三羧酸循环的运行,作为关键酶的辅因子,锰的充足供应保证了有机酸的正常合成与转化,从而维持酸代谢平衡。相反,T3处理可能由于高浓度锌抑制了锰的吸收与转运,导致三羧酸循环中关键酶活性降低,从而阻碍了有机酸的合成[20]。
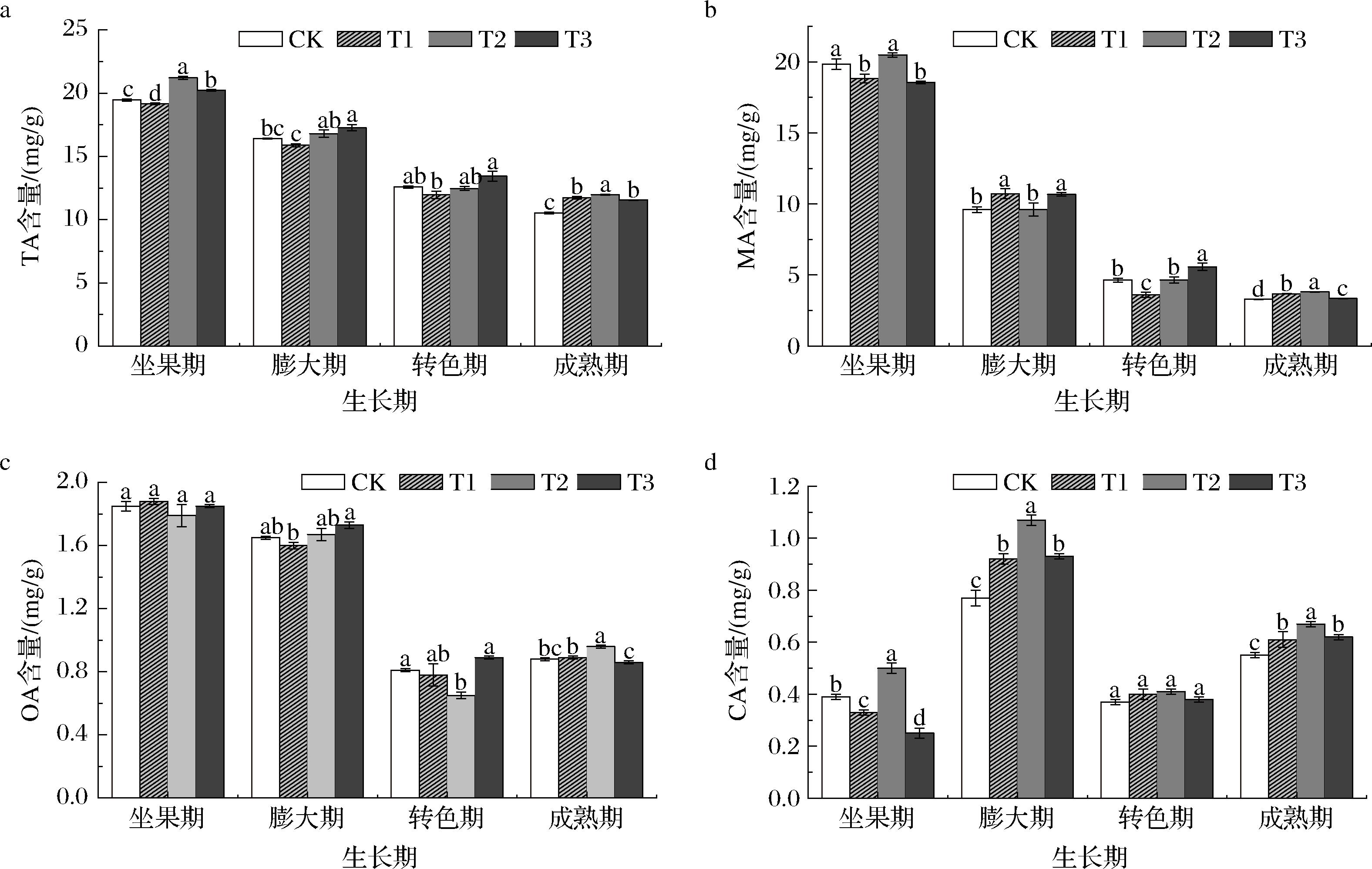
a-TA含量;b-MA含量;c-OA含量;d-CA含量
图3 喷施微量元素对葡萄果实酸组分含量的影响
Fig.3 Effect of foliar application of trace elements on the acid composition content of grape fruits
2.4 微量元素对葡萄果实有机酸代谢相关酶活性的影响
叶面喷施5种微量元素能有效影响马瑟兰葡萄果实的有机酸代谢相关酶的活性(图4)。如图4-a所示,各处理组中NAD-MDH活性在整个果实发育期间的变化趋势基本一致,其中T1和T2处理组的酶活性显著高于(P<0.05)CK。成熟期时,T1处理组的酶活性达到66.10 U/min/g,较CK提高了25.47%。在T1处理下NAD-MDH活性达到最高,而T3处理组酶活性显著低于(P<0.05)CK,可能是因为硼元素的作用,适量硼通过促进碳水化合物转运与代谢[20],为NAD-MDH催化的苹果酸合成提供了充足的底物与能量保障,而过量硼则可能会直接抑制NAD-MDH活性[11]。
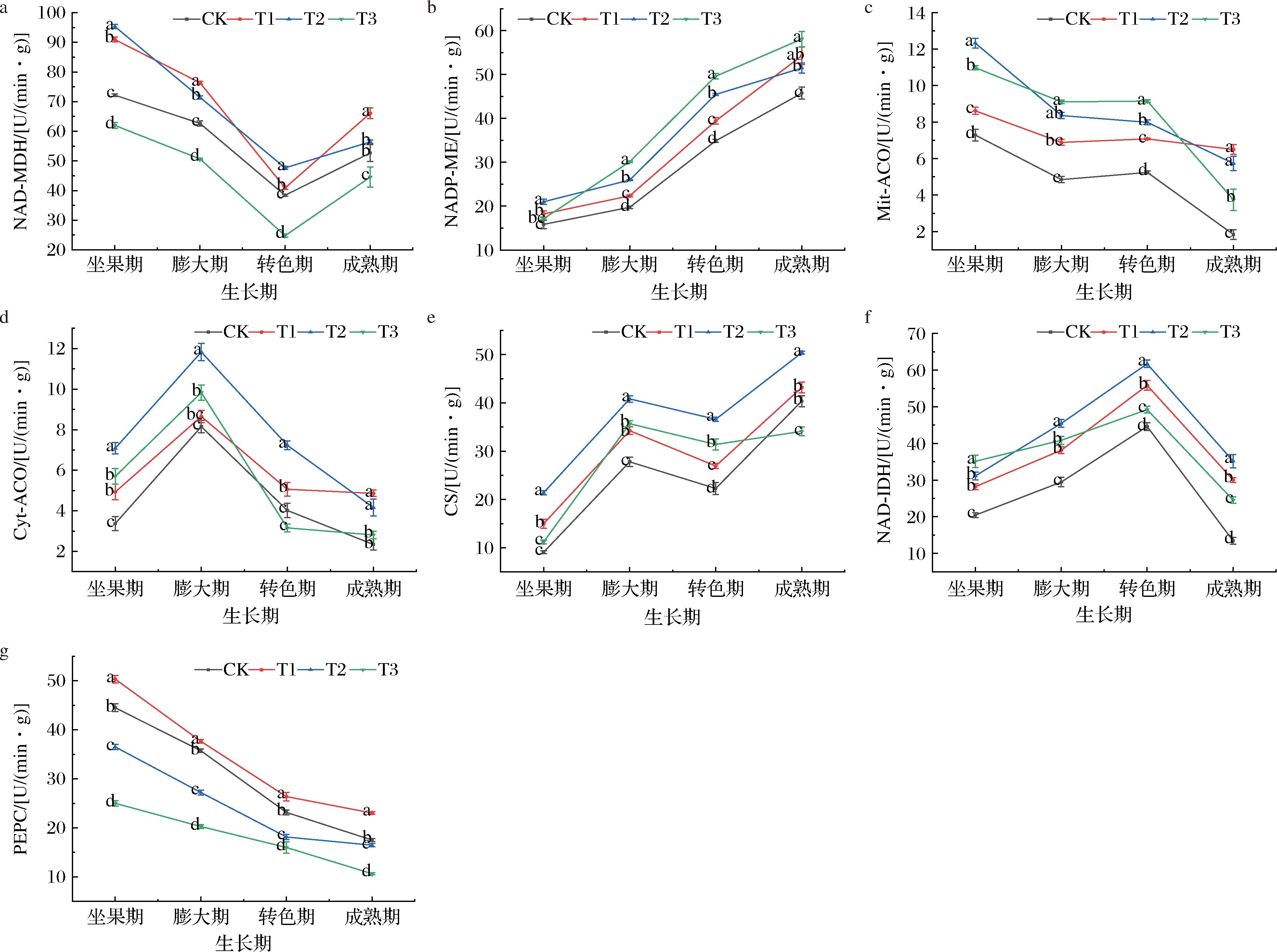
a-NAD-MDH活性;b-NADP-ME活性;c-Mit-ACO活性;d-Cyt-ACO活性;e-CS活性;f-NAD-IDH活性;g-PEPC活性
图4 喷施微量元素对葡萄果实酸代谢相关酶活性的影响
Fig.4 Effect of foliar application of trace elements on the activity of enzymes related to acid metabolism in grape fruits
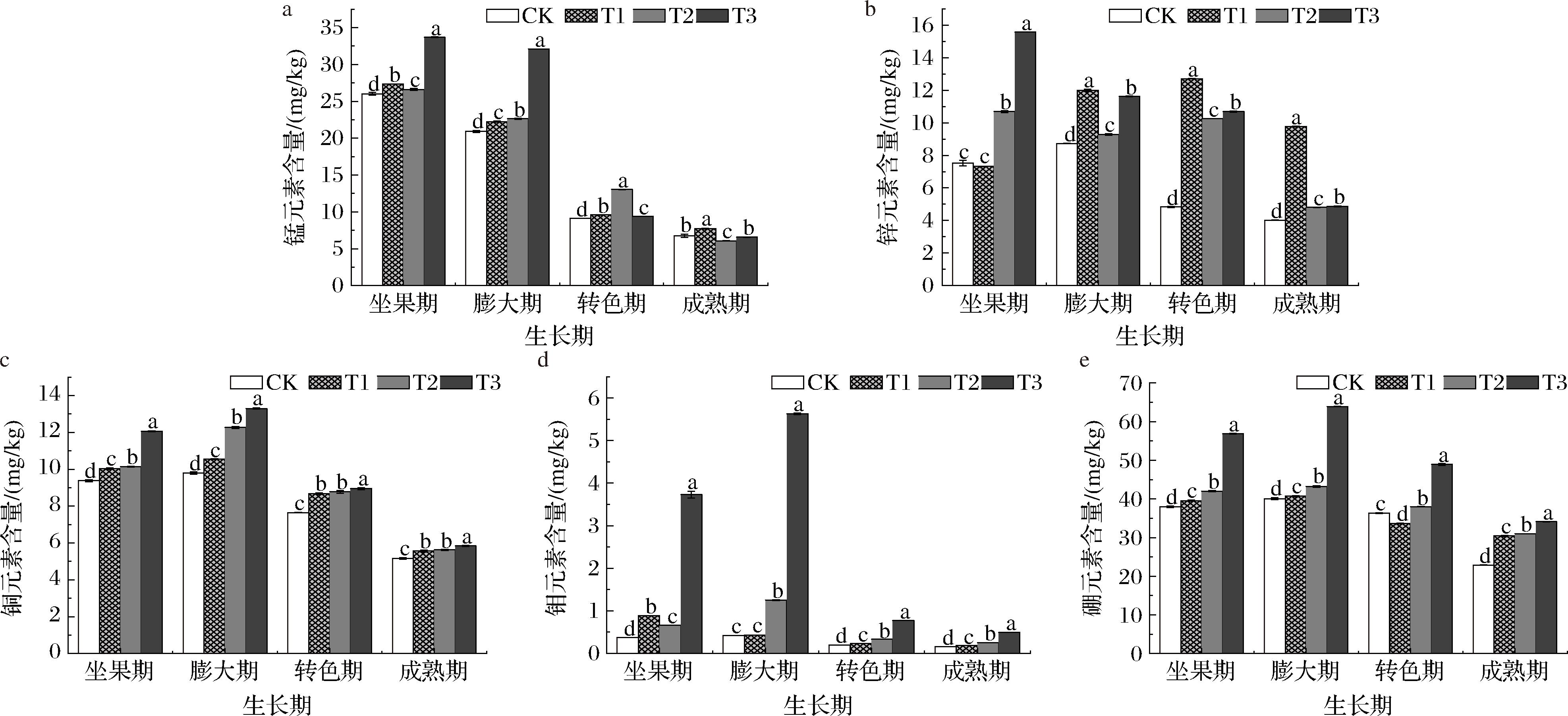
a-锰元素含量;b-锌元素含量;c-铜元素含量;d-钼元素含量;e-硼元素含量
图5 喷施微量元素对葡萄果实相应元素含量的影响
Fig.5 Effect of foliar application of trace elements on the corresponding element content in grape fruits
如图4-b所示,从坐果期至成熟期,各处理组NADP-ME活性总体呈持续上升趋势。在整个发育过程中,T1和T2处理组的酶活性始终显著高于(P<0.05)CK;T3处理自膨大期起酶活性显著高于(P<0.05)CK,并持续至成熟期。至成熟期时,各处理组酶活性达到最高,其中T3处理活性最高,为58.09 U/(min·g)。以上表明,T3处理下的NADP-ME活性最高,可能是因为叶面喷施浓度过高,促进了细胞代谢。
如图4-c所示,在葡萄生长发育阶段T1、T2、T3处理组的Mit-ACO的活性显著高于(P<0.05)CK。至葡萄成熟期时,酶活性表现为T1>T2>T3>CK,其中T1处理组活性最高为6.50 U/(min·g),CK酶活性最低为1.84 U/(min·g)。在较低浓度配比下的T1处理能使Mit-ACO活性达到最高,可能是各元素之间的协同作用,并且低浓度硼可辅助维持线粒体膜完整性[21],为Mit-ACO提供稳定的催化环境,因此酶活性达到峰值。
如图4-d所示,在整个果实发育期间,T1和T2处理组的Cyt-ACO活性均显著高于(P<0.05)CK处理组。其中,T2处理在4个时期的酶活性分别较CK提高了110.09%、45.15%、79.85%、77.78%,其提升幅度总体高于T1处理。此外,在转色期,T3处理组的酶活性为3.16 U/min/g,显著低于(P<0.05)对照,降幅达21.4%。这表明可能适度的微量元素处理能够有效激活三羧酸循环关键酶活性,促进有机酸代谢与能量供应;而喷施浓度过高可能在转色期引发代谢抑制或离子平衡失调,反而抑制了Cyt-ACO的活性。
如图4-e所示,CS活性在果实发育过程中呈现动态变化:自坐果期起快速上升,于膨大期达到阶段性高峰后开始下降,转色期再次升高,并在成熟期达到峰值。在整个发育阶段,T1和T2处理组的酶活性始终显著高于(P<0.05)CK组。至成熟期时,T2处理的酶活性最高为50.38 U/(min·g),显著高于(P<0.05)CK 40.35 U/(min·g);而T3处理组的酶活性为34.11 U/(min·g),则显著低于(P<0.05)CK。推测可能是因适宜的锌和铜元素供应可激活酶蛋白或提供必需的辅因子[22],有效促进了三羧酸循环的代谢效率;而微量元素喷施浓度过高可能会破坏酶结构或干扰底物供应,导致酶活性下降。
NAD-IDH活性在葡萄生长过程中总体呈先升后降趋势(图4-f),并在转色期达到峰值。各处理组的酶活性在整个生育期均显著高于CK(P<0.05)。成熟期时,各组酶活性表现为T2>T1>T3>CK,其中T2处理组最高,达35.19 U/(min·g),显著高于CK(P<0.05);T1与T3处理组分别为30.03、24.57 U/(min·g),也显著高于CK(P<0.05)。NAD-IDH是三羧酸循环的关键限速酶[23],其在转色期活性峰值与果实有机酸转化和能量代谢需求的增强密切相关。成熟期T2处理组酶活性最高,说明适宜浓度的微量元素配比可有效促进该酶活性,优化有机酸代谢过程。
PEPC活性总体呈下降趋势(图4-g)。整个生长阶段T1处理组显著高于(P<0.05)CK,而T2和T3处理组的酶活性在整个发育期均显著低于(P<0.05)CK。T1处理下较高的PEPC活性,可能是由于锰元素发挥了作用,锰是PEPC活性中心的关键辅因子[24],可稳定酶蛋白空间结构并增强其与底物的结合能力,从而维持酶催化效率。相比之下,T2和T3处理下酶活性显著受到抑制则可能与铜元素过量有关,过量的Cu2+可能通过竞争酶活性中心位点或引发氧化胁迫等方式,干扰PEPC的正常功能[22]。
2.5 叶面喷施对葡萄果实微量元素的影响
如图5-a所示,葡萄果实中锰含量在整个发育期内总体呈下降趋势。在坐果期与膨大期,T3处理效果最为显著,其锰含量分别较CK处理组显著提高(P<0.05)29.49%与10.62%;至转色期,T2处理效果最佳;而在成熟期,T1处理的锰含量最高,达7.73 mg/kg。以上表明,葡萄果实锰含量随生育进程总体呈下降趋势,这可能与果实发育前期对锰的需求较高有关,如参与光合作用、酶系统激活等[20],而后期葡萄果实的发育重心转向糖分等有机物的积累,从而导致锰元素含量下降。
如图5-b所示,坐果期时,T3处理组的锌含量为15.58 mg/kg,效果最佳。膨大期至成熟期,T1处理组效果较好,与CK相比,锌含量分别提高了0.37、1.63、1.43倍。在坐果期,T3处理效果较好,可能是由于高浓度的锌通过角质层被光合叶片直接吸收,满足了细胞分裂和代谢对锌的需求[25-26]。随着外源锌浓度的增加,植株各器官中的锌含量总体上升,叶片作为主要吸收和贮存器官,其锌含量最高,提供了充足的锌营养[20]。膨大期开始,T1处理优于T3处理,可能是高浓度锌影响了离子平衡[14],导致T3处理在膨大期后锌吸收效率下降,难以满足果实需求;而T1处理通过保持适宜的锌水平,维持了离子平衡,并促进了锌与其他元素的协同作用,确保了较高的锌含量,显著高于CK。
如图5-c~图5-e所示,铜、钼、硼元素在葡萄生育期内均呈现先升高后下降的趋势,且经叶面喷施微量元素处理后,表现为T3>T2>T1>CK。成熟期,T3处理组的铜含量比CK提高了11.64%。T3处理效果最佳,推测由于其较高的喷施浓度,更能充分补充植株铜储备,并持续为果实发育提供铜,最终在成熟期显著提升(P<0.05)铜含量。T3处理下,钼元素在成熟期较坐果期下降了86.86%,可能与葡萄生长需求变化有关。坐果期钼参与氮素同化,需求较高[9];而成熟期氮代谢减弱,钼需求下降并可能向营养器官再分配,导致钼含量大幅下降。在成熟期,T3处理下硼元素含量比CK提高了49.1%。相较于T1、T2处理,T3喷施的硼浓度更高,硼作为葡萄生长初期的重要元素,参与细胞壁构建,并协同氮素代谢与光合产物合成[21]。前期充足的硼供给不仅满足了葡萄坐果和幼果发育的需求,还在植物体内贮存了一定的硼,进入成熟期后,硼的生理需求重心可能转移,但前期积累的硼仍持续存在于果实中,最终使T3处理在成熟期维持较高的硼含量。
2.6 相关性分析
由图6-a可知,可溶性总糖、葡萄糖、蔗糖和果糖含量与SS-ss、SPS呈极显著正相关(P<0.01),与NI呈极显著负相关(P<0.01);蔗糖含量与AI呈显著负相关(P<0.05)。表明SS-ss和SPS通过促进蔗糖合成正向调控糖分积累,NI与AI通过催化蔗糖分解负向调控。
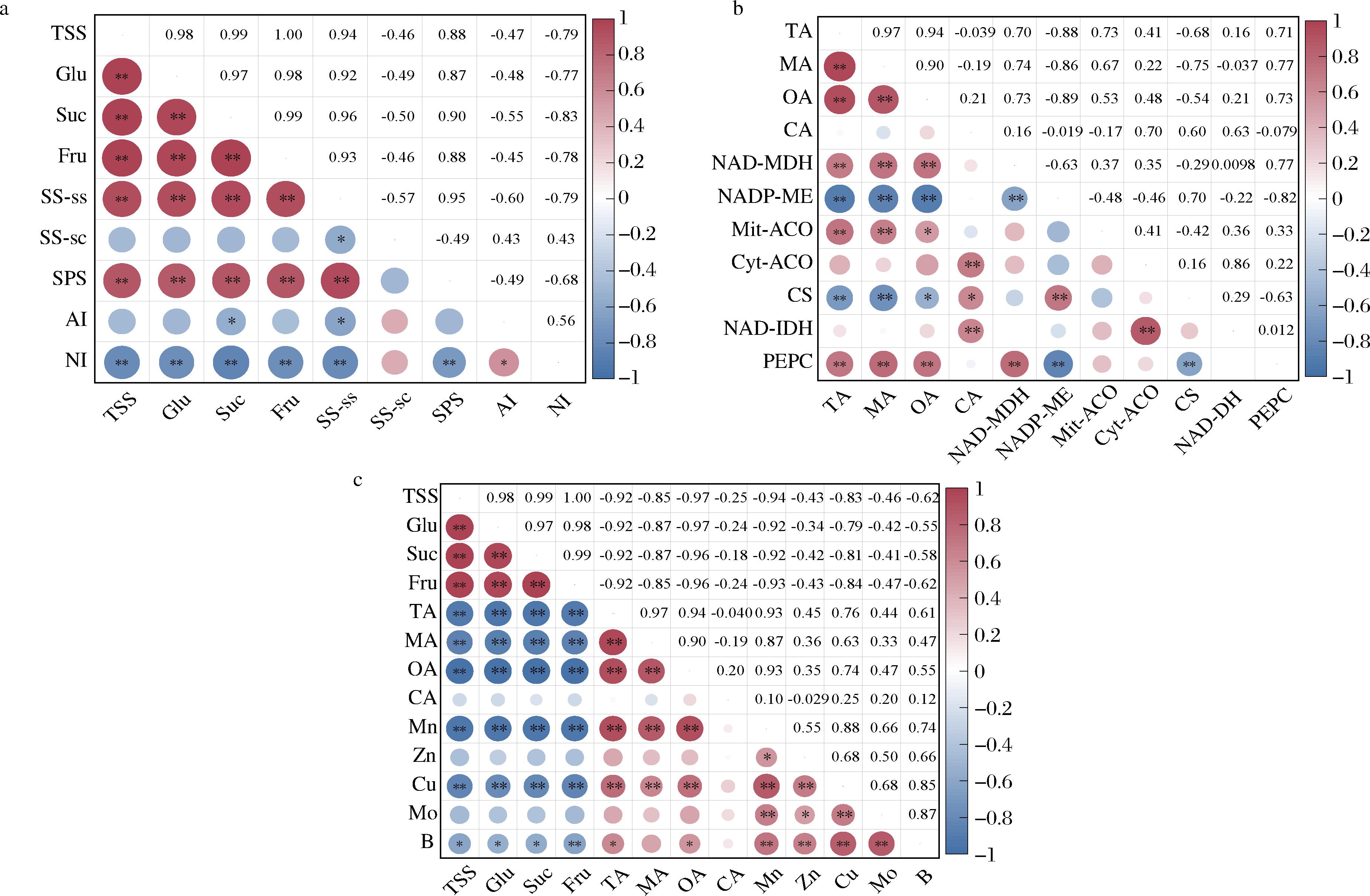
a-糖与糖酶相关性分析;b-酸与酸酶相关性分析;c-微量元素与糖酸相关性分析
图6 相关性分析热图
Fig.6 Correlation analysis heat map
注:不同的符号代表处理之间的显著差异,*表示P<0.05,**表示P<0.01。
由图6-b可知,酒石酸和苹果酸含量与NAD-MDH、Mit-ACO和PEPC呈极显著正相关(P<0.01),与NADP-ME和CS呈极显著负(P<0.01)相关;草酸含量与NAD-MDH和PEPC呈极显著正相关(P<0.01),与NADP-ME呈极显著负相关(P<0.01);柠檬酸含量与Cyt-ACO和NAD-IDH表现出极显著正相关(P<0.01)。NAD-MDH与PEPC共同调控酒石酸、苹果酸和草酸的合成积累,而柠檬酸代谢则依赖于Cyt-ACO与NAD-IDH的协同作用。
由图6-c可知,可溶性总糖、葡萄糖、蔗糖和果糖与酒石酸、苹果酸和草酸呈极显著负相关(P<0.01)。糖组分与有机酸作为构成果实风味的关键品质性状,坐果期至膨大期,果实同步启动糖与有机酸合成以支撑细胞分裂与体积增大[27],进入成熟期后,代谢重心发生转变,表现为糖分的持续积累与有机酸的逐步降解,从而形成适宜的糖酸比,让葡萄果实具有独特的风味。锰和铜元素与可溶性总糖、葡萄糖、蔗糖和果糖呈极显著负相关(P<0.01),而与酒石酸、苹果酸和草酸呈极显著正相关(P<0.01)。表明这2种元素更倾向参与有机酸代谢途径,这可能是由于锰和铜元素作为多种关键酶的辅因子,在三羧酸循环及有机酸合成与积累中发挥着重要作用[28]。硼元素与可溶性总糖、葡萄糖和蔗糖呈显著负(P<0.05)相关,与果糖呈极显著负相关(P<0.01),与酒石酸和草酸呈显著正相关(P<0.05)。一方面,硼可能通过影响糖转运蛋白活性,阻碍糖分向果实运输与积累的过程[9];另一方面,硼还可能通过间接调控有机酸代谢关键酶活性[29],参与有机酸代谢的调控过程。以上表明锰、铜和硼元素通过不同的作用机制参与调控果实糖酸代谢,共同影响葡萄果实风味品质的形成。
2.7 微量元素对葡萄果实中酸代谢相关基因表达的影响
如图7-a所示,在葡萄整个生长发育期间,CK处理组NAD-MDH的表达呈下调趋势。与对照组相比,T1、T2、T3处理均显著(P<0.05)促进了NAD-MDH的表达,表明不同处理均对NAD-MDH的表达有上调作用。T2处理组NAD-MDH的表达量在膨大期、转色期和成熟期达到最大值,分别是对照组的2.16、0.46、0.83倍,这样既保证有机酸适度留存,又避免过度积累。果实发育期间,CK组NADP-ME的表达水平低于T1、T2、T3处理组(图7-b)。T1处理NADP-ME在坐果期达到峰值,可通过早期激活苹果酸降解,避免幼果期有机酸过量对细胞代谢的干扰;T2处理NADP-ME在转色期和成熟期达到峰值,此时通过促进有机酸降解,与糖分积累形成平衡。如图7-c所示,CK处理组PEPC表达量在整个发育过程中变化较小,保持相对稳定。经T2处理显著提高(P<0.05)了PEPC的表达量,并在成熟期达到峰值。而PEPC作为苹果酸合成的关键酶[13],其表达上调可能通过增强草酰乙酸的供应为有机酸合成提供更多碳骨架,进而调控果实成熟阶段的酸度平衡。
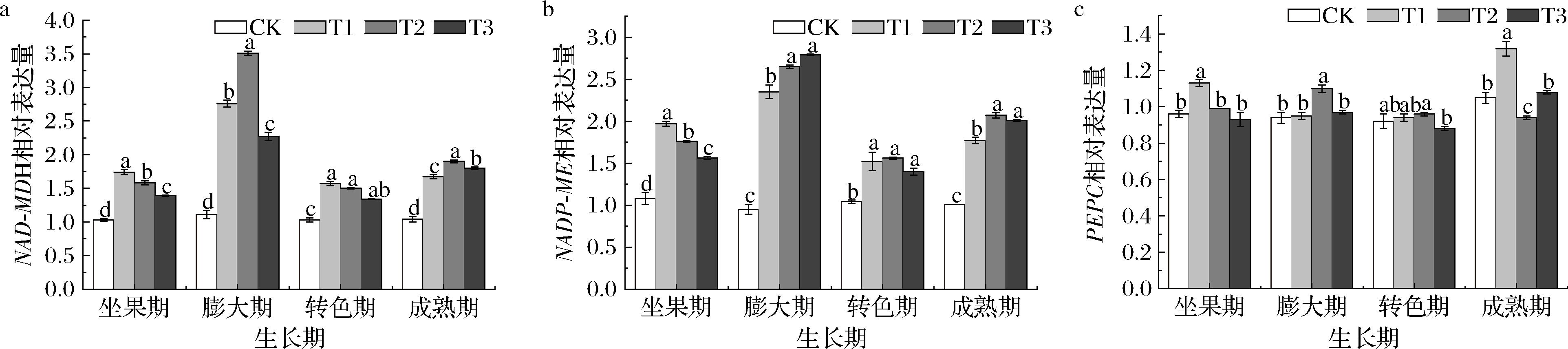
a-NAD-MDH相对表达量;b-NADP-ME相对表达量;c-PEPC相对表达量
图7 微量元素对葡萄有机酸代谢关键基因相对表达量的影响
Fig.7 Effect of trace elements on the relative expression of key genes involved in organic acid metabolism in grapes
2.8 主成分分析
通过对糖酸含量等23项相关指标(表1)进行主成分综合分析,最终提取出特征值大于1的4个主成分(PC1、PC2、PC3、PC4),方差贡献率分别为56.55%、19.39%、7.97%、6.23%,累计方差贡献率达到90.14%,符合分析要求。PC1中,酒石酸、AI、NAD-MDH、NADP-ME相对表达量等14项指标有较大正向量值,可溶性总糖、葡萄糖、蔗糖、果糖等9项指标有较大负向量值;PC2中,草酸、柠檬酸、SS-ss、NI等14项指标有较大正向量值,而可溶性总糖、酒石酸、苹果酸、PEPC等9项指标有较大负向量值;PC3中,可溶性总糖、蔗糖、果糖、苹果酸等16项指标有较大正向量值,葡萄糖、酒石酸、Cyt-ACO、Mit-ACO等7项指标有较大负向量值;PC4中除了草酸、柠檬酸、NI、Cyt-ACO、PEPC表现出负向量值外,其余18项均表现出正向量值。
综合得分由4个主成分(累计方差贡献率为90.14%)及其贡献率加权计算得出。由表2可知,不同处理的综合得分排名为T1>T2>T3>CK。此结果证明,T1处理对提高果实品质效果最佳。
3 结论与讨论
本研究深入讨论了叶面喷施微量元素对马瑟兰葡萄果实糖代谢与有机酸代谢的调控作用,从代谢关键酶活性、基因表达及物质积累等多维度揭示了其影响规律,为葡萄品质调控提供了理论依据与技术支撑。在糖代谢方面,适宜浓度的微量元素通过精准调控蔗糖代谢关键酶的活性与方向,推动糖分高效积累[30]。蔗糖合成酶作为双功能酶,能可逆催化蔗糖的合成与分解,而SPS和转化酶(AI、NI)分别主导蔗糖合成与水解的不可逆途径[13]。喷施微量元素处理显著上调(P<0.05)了SS-ss活性与SPS活性,同时抑制了AI和NI的表达,促使光合产物更多地向蔗糖合成分配,进而实现了果实中可溶性总糖、葡萄糖、蔗糖和果糖的协同积累。在有机酸代谢方面,微量元素处理显著降低(P<0.05)了酒石酸、苹果酸、草酸与柠檬酸的含量。该过程主要涉及3条协同调控路径:锰、锌等元素作为辅助因子激活NADP-ME等关键酶,促进有机酸脱羧与呼吸消耗[31-32];同时,PEPC基因表达的上调增强了草酰乙酸的生成潜力,为酸代谢提供更活跃的底物周转;而柠檬酸合酶与NADP-ME活性的提升,则进一步优化了三羧酸循环与苹果酸代谢流的平衡,共同促使有机酸含量下降。
综合来看,对马瑟兰葡萄叶面喷施适宜浓度的微量元素能有效调控其糖酸代谢,并改善果实品质。其中,T1处理(0.025 g/L Mn、0.04 g/L Zn、0.016 g/L Cu、0.025 g/L Mo、0.075 g/L B)效果最为显著。通过喷施微量元素能提升SS-ss与SPS活性,显著增加(P<0.05)了果实中可溶性总糖、葡萄糖、蔗糖及果糖的含量;同时果实中NADP-ME和CS的活性被提高,而NAD-MDH、NAD-IDH、PEPC、Cyt-ACO及Mit-ACO的活性则受到抑制,进而导致酒石酸、苹果酸、草酸与柠檬酸含量的下降。此外,该处理还促进了果实对锌元素的积累,并显著上调了PEPC的基因表达。
[1] RUSTIONI L, ALTOMARE A, SHANSHIASHVILI G, et al. Microclimate of grape bunch and sunburn of white grape berries: Effect on wine quality[J]. Foods, 2023, 12(3):621.
[2] ALEM H, RIGOU P, SCHNEIDER R, et al. Impact of agronomic practices on grape aroma composition: A review[J]. Journal of the Science of Food and Agriculture, 2019, 99(3):975-985.
[3] WALKER R P, BONGHI C, VAROTTO S, et al. Sucrose metabolism and transport in grapevines, with emphasis on berries and leaves, and insights gained from a cross-species comparison[J]. International Journal of Molecular Sciences, 2021, 22(15): 7794.
[4] WANG C N, WANG L N, YE J B, et al. Fruit quality of Vitis vinifera: How plant metabolites are affected by genetic, environmental, and agronomic factors[J]. Scientia Horticulturae, 2022, 305:111404.
[5] 牛生洋, 刘崇怀, 刘强, 等. 葡萄种质果实有机酸组分及其含量特性[J]. 食品科学, 2022, 43(12):228-234.NIU S Y, LIU C H, LIU Q, et al. Composition and contents of organic acids in different grape germplasms[J]. Food Science, 2022, 43(12):228-234.
[6] LIAO H Z, LIN X K, DU J J, et al. Transcriptomic analysis reveals key genes regulating organic acid synthesis and accumulation in the pulp of Litchi chinensis Sonn. cv. Feizixiao[J]. Scientia Horticulturae, 2022, 303:111220.
[7] JIANG B, FANG X J, FU D Q, et al. Exogenous salicylic acid regulates organic acids metabolism in postharvest blueberry fruit[J]. Frontiers in Plant Science, 2022, 13:1024909.
[8] 吴晓琳. 焉耆盆地葡萄酒产业价值链提升对策[J]. 合作经济与科技, 2024(18):47-49.WU X L. Countermeasures for upgrading the value chain of wine industry in Yanqi basin[J]. Co-Operative Economy &Science, 2024(18):47-49.
[9] 谢和缘. 叶面营养对红美人柑橘产量品质及养分利用的影响[D]. 武汉: 华中农业大学, 2023.XIE H Y. Effects of foliar nutrition on yield, quality and nutrient utilization of Hongmeiren citrus[D]. Wuhan: Huazhong Agricultural University, 2023.
[10] 杨相, 宋庆燕, 崔洁, 等. 黄芪叶片营养吸收特点与专用叶面肥研究进展[J]. 辽宁中医药大学学报, 2018, 20(4):144-146.YANG X, SONG Q Y, CUI J, et al. Progress in characteristics of nutrient uptake of Astragalus leaves and special foliar fertilizer[J]. Journal of Liaoning University of Traditional Chinese Medicine, 2018, 20(4):144-146.
[11] 张妍妍. 八硼酸钠调控“章姬”草莓果实糖酸比及叶片光合特性的生理机制[D]. 新乡: 河南科技学院, 2022.ZHANG Y Y. Physiological mechanism of sodium octaborate regulating fruit sugar-acid ratio and leaf photosynthetic characteristics of ‘Zhangji’ strawberry [D]. Xinxiang : Henan Institute of Science and Technology, 2022.
[12] MA J Z, ZHANG M, LIU Z G, et al. Copper-based-zinc-boron foliar fertilizer improved yield, quality, physiological characteristics, and microelement concentration of celery (Apium graveolens L.)[J]. Environmental Pollutants and Bioavailability, 2019, 31(1):261-271.
[13] 牛冬青. 整形方式和砧木对酿酒葡萄果实糖酸代谢及有机酸相关基因表达的影响[D]. 太原: 山西农业大学, 2019.NIU D Q. Effects of shaping methods and rootstocks on sugar and acid metabolism and expression of organic acid-related genes in wine grape berries[D]. Taiyuan : Shanxi Agricultural University, 2019.
[14] 宋长征. 锌元素对梅鹿辄葡萄果实与葡萄酒质量及幼苗生长的影响[D]. 咸阳: 西北农林科技大学, 2018.SONG C Z. Effects of zinc on fruit and wine quality and seedling growth of Merlot grape[D]. Xianyang: Northwest A &F University, 2018.
[15] 苏静, 祝令成, 刘茜, 等. 果实糖代谢与含量调控的研究进展[J]. 果树学报, 2022, 39(2):266-279.SU J, ZHU L C, LIU (Q /X), et al. Research progress on sugar metabolism and concentration regulation in fruit[J]. Journal of Fruit Science, 2022, 39(2):266-279.
[16] 王玮, 程远, 叶青静, 等. 植物蔗糖合酶生理生化功能研究进展[J]. 华北农学报, 2023, 38(S1):261-270.WANG W, CHENG Y, YE Q J, et al. Advances in physiological and biochemical functions of plant sucrose synthase[J]. Acta Agriculturae Boreali-Sinica, 2023, 38(S1):261-270.
[17] FIGUEROA C M, ASENCI N DIEZ M D, KUHN M L, et al. The unique nucleotide specificity of the sucrose synthase from Thermosynechococcus elongatus[J]. FEBS Letters, 2013, 587(2):165-169.
N DIEZ M D, KUHN M L, et al. The unique nucleotide specificity of the sucrose synthase from Thermosynechococcus elongatus[J]. FEBS Letters, 2013, 587(2):165-169.
[18] 闫玉静. 根外喷锌对苹果果实激素含量和糖代谢酶活性的影响[D]. 泰安: 山东农业大学, 2015.YAN Y J. Effects of root spraying zinc on hormone content and sugar metabolism enzyme activity of apple fruit[D]. Tai ’an : Shandong Agricultural University, 2015.
[19] 李明. 不同施肥处理对纽荷尔和红肉脐橙果实糖积累的影响[D]. 武汉: 华中农业大学, 2013.LI M. Effects of different fertilization treatments on sugar accumulation in fruits of Newhall and Cara Cara navel orange[D]. Wuhan: Huazhong Agricultural University, 2013.
[20] 马琦琦, 李丽君, 王斌, 等. 微肥对植物生长作用及施用技术的研究进展[J]. 安徽农业科学, 2022, 50(13):4-6.MA Q Q, LI L J, WANG B, et al. Research progress on the effects of micro-fertilizers on plant growth and application techniques[J]. Journal of Anhui Agricultural Sciences, 2022, 50(13):4-6.
[21] 金天, 徐月美, 邝冠翎, 等. 缺硼胁迫对枳幼苗根系生长及线粒体功能的影响[J]. 园艺学报, 2024, 51(1):121-132.JIN T, XU Y M, KUANG G L, et al. Effect of boron deficiency on the root growth and mitochondrial function of trifoliate orange seedlings[J]. Acta Horticulturae Sinica, 2024, 51(1):121-132.
[22] 彭雅萍. 喷施铜硼肥对忍冬生长生理影响及代谢组学研究[D]. 南京: 南京农业大学 ,2022.PENG Y P. Effects of spraying copper and boron fertilizer on the growth physiology and metabolomics of Lonicera japonica[D]. Nanjing: Nanjing Agricultural University, 2022.
[23] JIN L F, YUE Y, LIU F, et al. Identification of the grapefruit (Citrus paradisi) isocitrate dehydrogenase gene and functional analysis of CpNADP-IDH1 in citric acid metabolism[J]. Horticulturae, 2025, 11(6): 598.
[24] 陶雨朝. 玉米苗对锰亏缺的生理响应及基因型差异[D]. 哈尔滨: 东北农业大学, 2023.TAO Y C. Physiological responses and genotypic differences of maize seedlings to manganese deficiency[D]. Harbin: Northeast Agricultural University, 2023.
[25] KAUR H, GARG N. Zinc toxicity in plants: A review[J]. Planta, 2021, 253(6):129.
[26] BHANTANA P, RANA M S, SUN X C, et al. Arbuscular mycorrhizal fungi and its major role in plant growth, zinc nutrition, phosphorous regulation and phytoremediation[J]. Symbiosis, 2021, 84(1):19-37.
[27] 孙肖瑞, 谢兆森, 尤佳玲, 等. 葡萄果实中糖转运、代谢与调控研究进展[J]. 植物生理学报, 2021, 57(3):542-550.SUN X R, XIE Z S, YOU J L, et al. Research progress on sugar transport, metabolism and regulation in grape (Vitis vinifera) berry[J]. Plant Physiology Journal, 2021, 57(3):542-550.
[28] 管庆林, 朴晟源, 秦艳青, 等. 中微量元素配施对雪茄烟叶中性致香成分及非挥发性有机酸含量的影响[J]. 山东农业科学, 2023, 55(2):110-118.GUAN Q L, PIAO S Y, QIN Y Q, et al. Effects of combined application of medium and trace elements on neutral aroma components and non-volatile organic acid content of cigar leaves[J]. Shandong Agricultural Sciences, 2023, 55(2):110-118.
[29] 杨兴华. GABA对柑橘缺硼胁迫的响应及对根系发育和代谢的调控作用[D]. 赣州: 赣南师范大学, 2022.YANG X H. Response of GABA to boron deficiency stress in citrus and its regulation on root development and metabolism[D]. Ganzhou : Gannan Normal University, 2022.
[30] KAUR H, KAUR H, KAUR H, et al. The beneficial roles of trace and ultratrace elements in plants[J]. Plant Growth Regulation, 2023, 100(2):219-236.
[31] 顾梅花. 酿酒葡萄养分吸收规律及喷施镁锰铁肥对其产量品质的影响[D].银川: 宁夏大学, 2024.GU M H. The law of nutrient absorption of wine grape and the effect of spraying magnesium manganese iron fertilizer on its yield and quality[D]. Yinchuan: Ningxia University, 2024.
[32] 周敏. 刺葡萄矿质营养变化规律与钾对果实糖分积累的影响研究[D]. 长沙: 湖南农业大学, 2017.ZHOU M.Study on the change rule of mineral nutrition and the effect of potassium on fruit sugar accumulation in Vitis davidii Foex[D]. Changsha: Hunan Agricultural University, 2017.