高胆固醇血症引发的动脉粥样硬化、冠心病、脑中风等心脑血管疾病,已成为威胁人类健康的“第一杀手”,研究表明[1-2],血清总胆固醇(total cholesterol,TC)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)水平的升高与冠心病发病风险的增加密切相关,TC水平每降低1%,能将患冠心病的风险降低2~3倍,在积极预防心血管疾病方面,具有降胆固醇作用的益生菌显得尤为重要。发酵马乳保留着许多优良特性的乳酸菌资源,乳酸菌作为人及动物肠道中极为重要的菌群之一,与机体的许多生理功能有着密切的联系。大量实验表明乳酸菌在体内和体外均有降解胆固醇作用,这对益生菌市场产生了积极的影响[3-4]。
目前有关益生菌通过调节肠道微生态平衡和改善脂质代谢发挥降胆固醇作用的研究日趋增多,其中以乳杆菌属为代表的功能菌株已被证实可在肠道定植,并通过糖的发酵、胆汁酸的生物转化以及调节肠道菌群丰度与组成,预防高脂血症并降低心血管疾病风险[5-6]。寻找品质优良、性能稳定、安全有效的降胆固醇的乳酸菌菌种并用于功能性乳酸菌和制品的开发,具有重要的意义。
酸马奶是一种以鲜马奶为原料,经传统发酵方式得到的乳制品。新疆作为人类最早驯化马匹的发源地之一,其传统马乳制品中保留了种类丰富的发酵菌资源。根据国际前沿研究对肠道菌群深入了解,富含益生菌的食品在人类慢性代谢性疾病方面得到很大关注,传统发酵马乳也是如此。自然发酵地域菌种组成具有显著差异,致使所含微生物资源独具特色。由于工业化的推进[7],传统发酵菌资源濒临灭绝,新疆远离城市的牧区,尚保留了传统发酵菌种。菌种资源具有稀缺性,本课题组深入牧区采集传统发酵马乳收集发酵菌(调研民间收集效果显著的发酵马乳),共分离、筛选得到29株乳酸菌和酵母菌(传统发酵中这两种微生物是共存的),课题组通过体外生长特性、益生特性及体外降胆固醇能力,筛选出4株乳酸菌。
本课题组研究结果表明,传统发酵牛乳、驼乳和马乳均存在多菌混合生长现象,初步对其相互作用进行研究,结果提示复合益生菌制剂可能通过菌株间的协同作用发挥其特定作用。自然发酵食品中的微生物可能以群体形式存在,其通过代谢互补与生态互作增强整体功能;另一方面,已有研究证实复合菌在降低胆固醇、改善肠道屏障及调节免疫等方面的表现出优于单一菌株的效果,体现出“集团军作战”的优势[8]。基于此,本研究通过体外实验,分别评估了单一菌和复合菌的降胆固醇能力。实验结果证实,复合菌降胆固醇效果优于单一菌株[9]。本研究利用从同一发酵乳中分离筛选出的4株具高效降胆固醇能力的乳酸菌制备复合益生菌制剂,考察了其在大鼠高脂血症模型中的调节血脂作用及机制为益生菌辅助或替代治疗高脂血症提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株来源与实验动物
实验所用菌株均由本课题组分离自新疆伊犁哈萨克自治州尼勒克县牧区牧民家庭的传统发酵马乳,鉴定为植物乳植杆菌(Lactiplantibacillus plantarum),菌株编号分别为Ni2A、Ni2B、Ni2C、Ni2D。
实验动物选用6周龄SPF级雄性SD大鼠40只,购自新疆医科大学动物实验中心,体质量为180~200 g。生产许可证号:SCXK(新)2023-0001,使用许可证号SYXK(新)2023-0004,本实验方案经过新疆医科大学实验动物伦理委员会审核,符合国家实验动物福利伦理的相关规定,伦理审查批号为:IACUC-20250720-01。饲养条件为温度20~26 ℃,湿度40%~70%,12 h/12 h光暗循环,自由摄食饮水,垫料每周更换2次。
1.1.2 试剂
MRS(man rogosa sharpe)肉汤培养基、MRS琼脂培养基,北京索莱宝科技有限公司;胆汁酸试剂盒,上海优选生物科技有限公司;总胆固醇、甘油三酯(triglyceride,TG)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol, HDL-C)和低密度脂蛋白胆固醇试剂盒,深圳迈瑞生物医疗电子股份有限公司;磷酸盐缓冲液(phosphate-buffered saline,PBS)、二甲苯、乙酸乙酯、基础培养基、Caco-2细胞专用培养基(GZ10818)、阿托伐他汀钙片(H20051408),立普妥公司;乙酸(A875975)、丙酸(P816182)、正丁酸(B802730),麦克林公司;2-乙基丁酸(E105669),阿拉丁公司。
1.2 仪器与设备
电子分析天平,上海梅特勒-托利多仪器有限公司;SX-500蒸汽灭菌锅,Tomy Digital Biology 公司;HYQX-Ⅲ 厌氧培养箱,上海新诺仪器集团有限公司;CHT210R 大容量高速台式冷冻离心机,湖南湘仪实验室仪器开发有限公司;Multiskan GO酶标仪,赛默飞世尔科技有限公司;BS-120全自动生化分析仪,深圳迈瑞生物;GC 2010plus,岛津公司。
1.3 实验方法
1.3.1 菌株活化
将4种乳酸菌菌株分别划线接种于MRS琼脂培养基,37 ℃恒温培养48 h,挑取单个菌落接种至MRS肉汤中,37 ℃培养48 h,活化3代,备用。
1.3.2 自聚集性能的测定
参照肖春进等[10]的方法,将活化后的4株菌液分别于4 ℃、3 444×g离心10 min,收集各菌体沉淀。用PBS缓冲液洗涤,加入PBS缓冲液重悬调整菌悬液浓度为1×108 CFU/mL,酶标仪测OD600nm处的吸光度值(Ai)。随后,取4 mL菌悬液分装于离心管中,于37 ℃恒温培养。分别于0、1、2、4、24 h取上清液,测定其OD600nm处的吸光度值(At),每个菌株平行做3组重复实验取平均值,按公式(1)计算自聚集率:
自聚集率![]()
(1)
式中:A0为0 h的OD600nm,At分别代表1、2、4、8、24 h处的OD600nm。
1.3.3 表面疏水性的测定
同1.3.2节方法制备菌悬液,随后取3 mL菌悬液,分别加入1 mL二甲苯和乙酸乙酯混匀,酶标仪测OD600nm处的吸光度(Ci),于37 ℃恒温静置2 h分层,取水相,测定其OD600nm处的吸光度值(Ci),每个菌株平行做3组重复实验取平均值,按公式(2)计算表面疏水率:
表面疏水率![]()
(2)
式中:C0为0 h的OD600nm,Ci为2 h的OD600nm。
1.3.4 Caco-2细胞的黏附率测定
检测其对Caco-2细胞的黏附性,进一步评估益生菌胃肠道定植潜力。参照陈大卫等[11]的方法:将Caco-2细胞以1×105 cells/mL接种于12孔板,37 ℃、5%(体积分数)CO2培养至单层。PBS洗涤2次后,每孔加入0.5 mL菌悬液(基础培养基重悬,108 CFU/mL),每个菌株设3个复孔。37 ℃孵育2 h,PBS洗涤去除未黏附菌,加胰酶消化,随后加入完全培养基终止消化,吹打收集细胞,梯度稀释后涂板计数,按公式(3)计算细胞黏附率:
细胞黏附率![]()
(3)
1.4 动物实验
1.4.1 复合益生菌制备及动物分组
将4种乳酸菌分别于MRS肉汤培养基中37 ℃恒温培养48 h,离心,生理盐水洗涤2次、重悬,通过平板菌落计数法计算菌悬液中的活菌数,将4株菌的浓度均调整为:1×1010 CFU/mL和1×108 CFU/mL,随后按相同比例进行配制。高剂量复合益生菌:含同一样品分离出的4株乳酸菌(1×1010 CFU/mL),低剂量复合益生菌:含同一样品分离出的4株乳酸菌(1×108 CFU/mL),用于灌胃。
将SD大鼠适应性喂养1周后随机分为正常(normal control,N)组和高脂饮食(high fat diet,HFD)组。N组饲喂基础生长繁殖饲料,HFD组给予高脂饲料(D12492)。当HFD组血清TG、TC、LDL-C水平显著高于N组(P<0.05)时,视为造模成功。将造模成功的大鼠随机分为模型(model control,M)组、阳性药物[positive control(PC),阿托伐他汀钙片,8 mg/kg)]组、复合益生菌高剂量组(Ni-G)、复合益生菌低剂量组(Ni-D),每组8只,N组和M组灌胃等量生理盐水,持续8周。
大鼠给药8周后,禁食过夜,称重后腹腔注射麻药麻醉,腹主动脉采血。室温静置2 h,以861×g离心15 min,血清分离后分装于无菌离心管内。取完血后立即取出完整肠道,于无菌操作台迅速取出其内容物,置于冻存管液氮速冻,转移至-80 ℃冰箱保存。
1.4.2 生化指标
用全自动生化分析仪检测血清TC、TG、LDL-C、HDL-C水平,酶联免疫吸附法(enzyme-linked immunosorbent assay,ELISA)测定血清与粪便中总胆汁酸(total bile acids,TBA)含量。
1.4.3 粪便短链脂肪酸(short-chain fatty acids,SCFAs)含量检测
气相色谱法测定粪便SCFAs含量,称取0.1 g粪便,于液氮中快速研磨均匀,立即转至离心管中,随后加入2-乙基丁酸作为内标(终浓度为2 mmol/L)和0.4 mL甲醇混匀。用HCl调节pH值至1,室温静置10 min。在13 776×g、15 min离心,取上清液经0.2 μm有机滤膜过滤,现配现用[12]。
1.4.4 肝脏病理学
实验结束后解剖摘取大鼠肝脏,拍照并称重,按公式(4)计算肝脏指数,观察各组肝脏变化。取肝组织进行苏木精-伊红(hematoxylin and eosin,H&E)染色:经4%多聚甲醛固定、石蜡包埋、切片及H&E染色,光学显微镜下观察肝组织病理学变化。
肝脏指数![]()
(4)
1.4.5 肠道微生物的宏基因测序分析
大鼠粪便样本的基因组DNA采用FastPure Stool DNA Isolation Kit(Magnetic bead)试剂盒提取。提取完成后,检测DNA的浓度与纯度,并通过1%琼脂糖凝胶电泳评估DNA完整性。通过Covaris M220进行片段化,并筛选约350 bp的片段用于构建配对末端(PE)文库。使用Illumine NovaSeqTM X Plus测序平台进行宏基因组测序(上海美吉生物医药科技有限公司)。基于Majorbio云平台进行生物信息学分析,对原始数据进行质控,随后,对高质量数据进行组装并构建非冗余基因集,对基因集进行物种注释后,通过R软件(Version 3.3.1)计算α多样性,基于Bray-Curtis距离矩阵进行主坐标分析(principal co-ordinates analysis,PCoA),以可视化样本间的β多样性。使用非冗余基因集与NR数据库进行比对,计算各物种(门、属、种水平)的相对丰度。为筛选组间差异菌群,进行了多组间物种差异比较,并采用线性判别分析[(linear discriminant analysis,LDA),LDA分数>3,P<0.05]的效应量(linear discriminant analysis effect size,LEfSe)分析筛选肠道菌群差异物种。采用斯皮尔曼相关性分析对显著富集的肠道菌群与相关指标进行相关性分析。最后,基于KEGG数据库对肠道菌群功能代谢通路进行注释与富集分析。
1.5 统计学方法
应用SPSS 26.0软件进行统计分析,计量资料以“平均值±标准差”表示。若数据符合正态分布,方差齐,则2组间采用t检验,多组间比较采用单因素方差分析;若数据不符合正态分布,采用非参数秩和检验。
2 结果与分析
2.1 复合益生菌益生特性
益生菌的胃肠道黏附与定植能力是其发挥益生作用的先决条件[13-14],本研究通过自聚集性、表面疏水性及Caco-2细胞黏附率综合评估4株乳酸菌的肠道定植潜力(图1)。结果显示,4株乳酸菌均表现出良好的自聚集性能:2 h时自聚集率均超过10%,4 h时均超过25%,24 h时均超过90%(图1-a)。研究结果与宋莺丽等[15]的研究一致,即菌株自聚集性随时间延长而增强,培养24 h后自聚集率均超过90%且上清液澄清,表明4株乳酸菌具备肠道定植的潜力。采用二甲苯和乙酸乙酯检测4株乳酸菌的表面疏水性,结果见图1-b。由图可知,4株乳酸菌对二甲苯(23.38%~31.59%)的疏水性高于乙酸乙酯(8.01%~11.41%),可能与其表面结构差异有关。4株乳酸菌对Caco-2细胞的黏附率见图1-c,其黏附率为(2.66%~10.00%),与徐晶晶等[16]从母乳中筛选的4株植物乳植杆菌的黏附率水平相当,该研究以L.rhamnosusGG(LGG)作为对照组,其黏附率为5.38%,本研究中菌株Ni2B的黏附率[(5.27±0.24)%]与LGG相近,而菌株Ni2D的黏附率[(10±0.38)%]则高于LGG对照组,表明4株乳酸菌具有较好的细胞黏附率。综上,4株乳酸菌具备在肠道定植的潜力,从而发挥其益生作用,为后续体内实验奠定了基础。
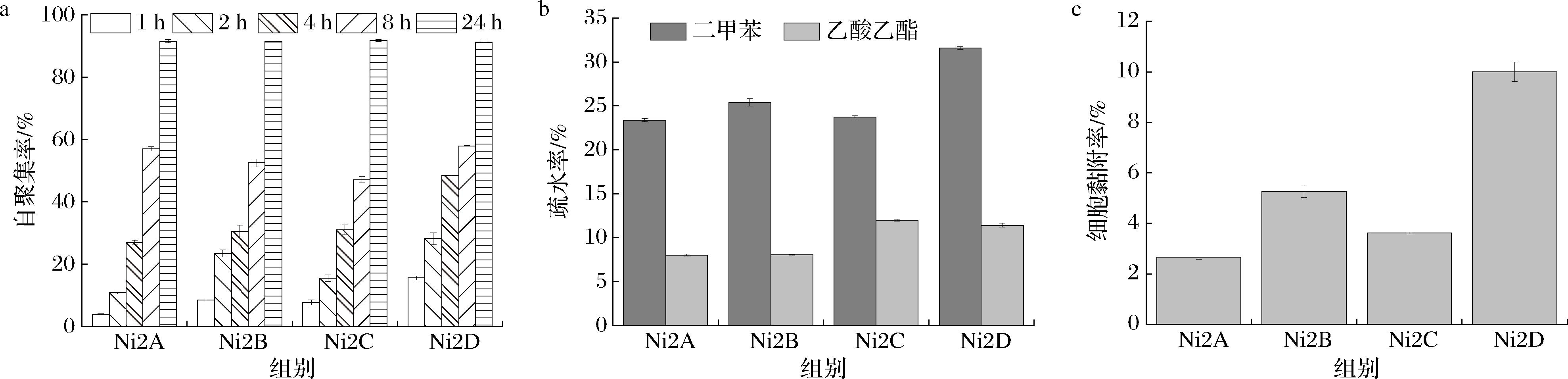
a-自聚集率;b-疏水率;c-细胞黏附率
图1 四株乳酸菌的定植性能
Fig.1 The colonization performance of four strains of lactic acid bacteria
2.2 复合益生菌对HFD大鼠的调血脂作用
2.2.1 大鼠体重变化
观察发现,N组大鼠活动活跃,体质量增长平稳,毛色光泽良好,摄食量与饮水量正常;M组大鼠随体质量增长活动量减少,体质量增长迅速,进食量增大;经干预后,大鼠体质量增长减缓,活动量较模型组增加。如图2所示,M组大鼠体质量显著高于N组(P<0.01)。经干预后,PC组和复合益生菌组体质量增长减缓。至实验第3周末,PC组和复合益生菌组体质量均低于M组(P<0.05),表明发酵马乳源复合益生菌可有效抑制高脂饮食诱导的大鼠体质量过度增长。
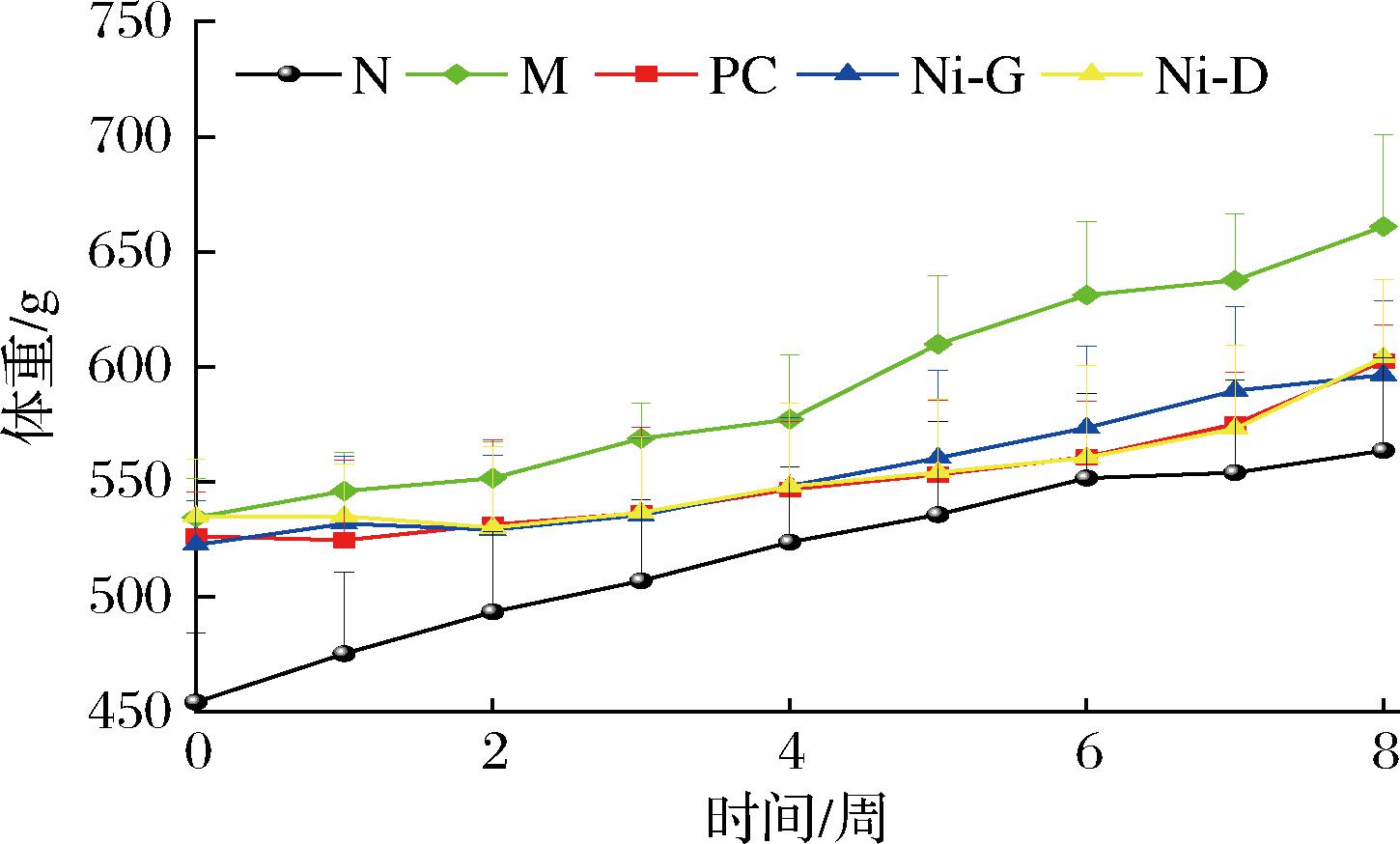
图2 大鼠体质量变化
Fig.2 Changes in body mass of rats
2.2.2 复合益生菌对HFD大鼠血脂的影响
益生菌可以预防和缓解脂质代谢相关的疾病[17-18],本研究通过体内实验,评估复合益生菌对高脂血症大鼠血脂的作用。由图3可知,干预8周后,与N组比较,M组大鼠TC、TG和LDL-C水平显著升高(P<0.01),与M组相比,PC组TC、TG、LDL-C水平显著降低(P<0.01);复合益生菌组TC、LDL-C水平显著降低(P<0.01),血清TG水平有所降低,但无统计学意义(P>0.05),表明发酵马乳源益生菌能够有效改善高脂血症大鼠的血脂异常,特别是显著降低TC和LDL-C水平。ZIAEI等[19]研究发现食用含有双歧杆菌的发酵乳制品可有效使血清中TC、LDL-C的水平降低更加明显,这与本研究结果一致。
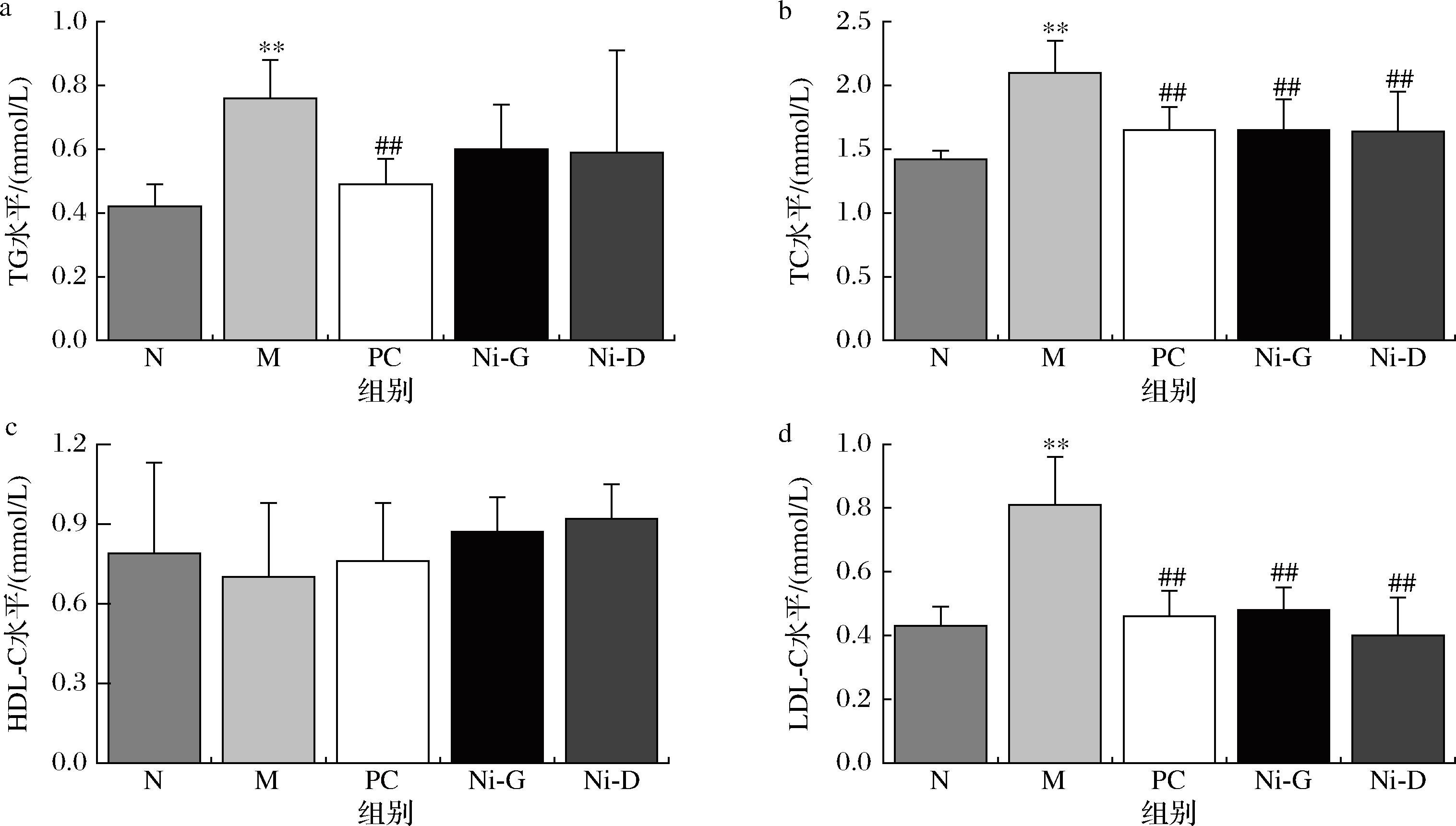
a-TG水平;b-TC水平;c-HDL-C水平;d-LDL-C水平
图3 复合益生菌对血脂的影响
Fig.3 Effects of compound probiotics on blood lipid levels
注:与N组相比:**表示P<0.01;与M组相比:##表示P<0.01(下同)。

a-肝脏H&E染色;b-肝脏指数
图4 光学显微镜下观察肝组织苏木精-伊红染色图(200×)和肝脏指数
Fig.4 Hematoxylin-eosin staining images of liver tissues observed under light microscope (200×) and liver index
2.2.3 复合益生菌对肝脏病理学的影响
各组肝组织形态如图4-a所示,N组肝细胞肝小叶结构清楚,肝细胞索排列整齐、肝细胞形态正常、无脂肪颗粒沉积、未见变性、坏死等改变。M组大部分肝细胞脂肪变性,肝细胞呈小泡性脂肪变性,大部分受累肝细胞呈泡沫状。干预后与M组相比,PC组可见少部分肝细胞脂肪变性,Ni-G组肝细胞结构基本正常,少部分肝细胞脂肪变性,Ni-D组可见部分肝细胞脂肪变性,脂质空泡变性呈大小泡混合型。肝指数显示(图4-b),M组较N组大鼠肝脏指数升高,差异有统计学意义(P<0.01);与M组相比,干预后,各组肝脏指数降低,差异有统计学意义(P<0.01)。上述结果表明,高脂饮食成功诱导了大鼠肝脏脂质代谢紊乱,导致肝细胞脂肪变性和肝脏指数升高,提示肝脏损伤。肝脏作为维持全身脂质代谢稳态的核心器官,其胆固醇吸收、合成、分解及脂蛋白转运的协同调控对脂质平衡至关重要[20]。高脂饮食可促进肝内脂肪滴异常积聚,引发脂肪肝。本研究发现,PC组及复合益生菌组均能有效减轻肝脏脂肪沉积,改善肝组织病理损伤并显著降低肝脏指数。
2.2.4 复合益生菌对大鼠肠道菌群的影响
2.2.4.1 肠道菌群多样性变化
Alpha多样性反映肠道内物种丰富度与多样性,本研究采用Chao指数评估物种丰富度(指数值越高,丰富度越高),Shannon指数评估物种多样性(指数值越高,多样性越高),如图5-a所示,与N组相比,M组大鼠肠道菌群的物种丰富度降低,表明HFD导致物种丰富度下降。干预后,各组物种丰富度呈现升高趋势;各组间物种多样性无显著差异(图5-b),表明各组对物种多样性影响不大。另外,通过主坐标分析(principal coordinate analysis,PCoA)评估样本间群落结构差异(图5-c)。如图所示,N组和M组间显著分离,表明高脂饮食显著改变菌群结构,同时各干预组分布趋近于N组,表明干预后可逆转高脂饮食引起的菌群紊乱;N组与干预组样品组内距离小,反映实验重复性良好且菌群结构稳定,而M组组内离散度高,表明其个体间菌群差异较大,可能与高脂饮食导致代谢差异有关。
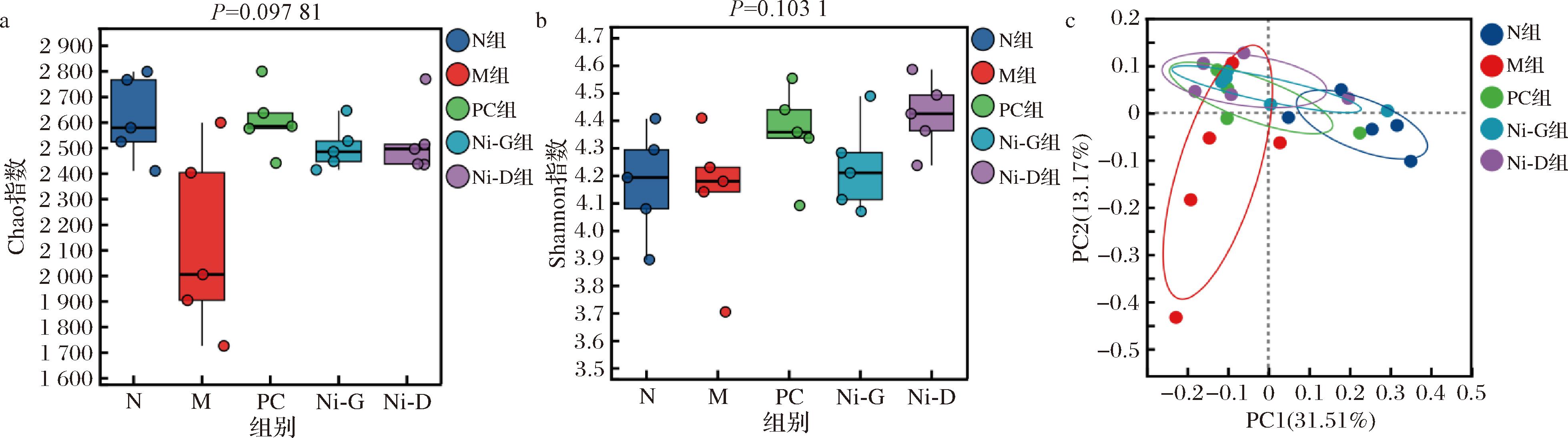
a-Chao指数;b-Shannon指数;c-PCoA分析
图5 肠道菌群多样性
Fig.5 Diversity of gut microbiota
2.2.4.2 肠道菌群物种丰度变化
门水平上肠道群落的分布情况,如图6-a所示,在门水平上厚壁菌门(Bacillota)、拟杆菌门(Bacteroidota)、螺旋体菌门(Spirochaetota)等为优势菌门。Bacillota/Bacteroidota比值是衡量肠道菌群稳态的重要指标之一,Bacillota能够增加宿主能量获取效率从而诱导肥胖,而Bacteroidota则参与调节免疫,高脂膳食会影响宿主的免疫系统和肠道屏障功能,间接抑制Bacteroidota生长[21-22]。本研究结果显示,与N组相比,M组Bacillota/Bacteroidota比值上升,经干预后各组比值下降,表明PC和复合益生菌可有效调节菌群稳态。由图6-b可知,属水平优势菌属包括真杆菌属(Eubacterium)、梭菌属(Clostridium)、瘤胃球菌属(Ruminococcus)等;由图6-c可知,种水平优势菌包括Eubacterium_sp.、Ruminococcus_sp.、Clostridium_sp.等,而经复合益生菌干预后,Ruminococcus_sp.、颤螺菌属(Oscillibacter_sp.)、劳森菌属(Lawsonibacter_sp.)和候选食粪泥弧菌(Candidatus_Limivicinus_faecipullorum)等菌显著上升,表明复合益生菌摄入增加了肠道中有益菌的丰度,从而改善高脂饮食引起的肠道菌群紊乱。
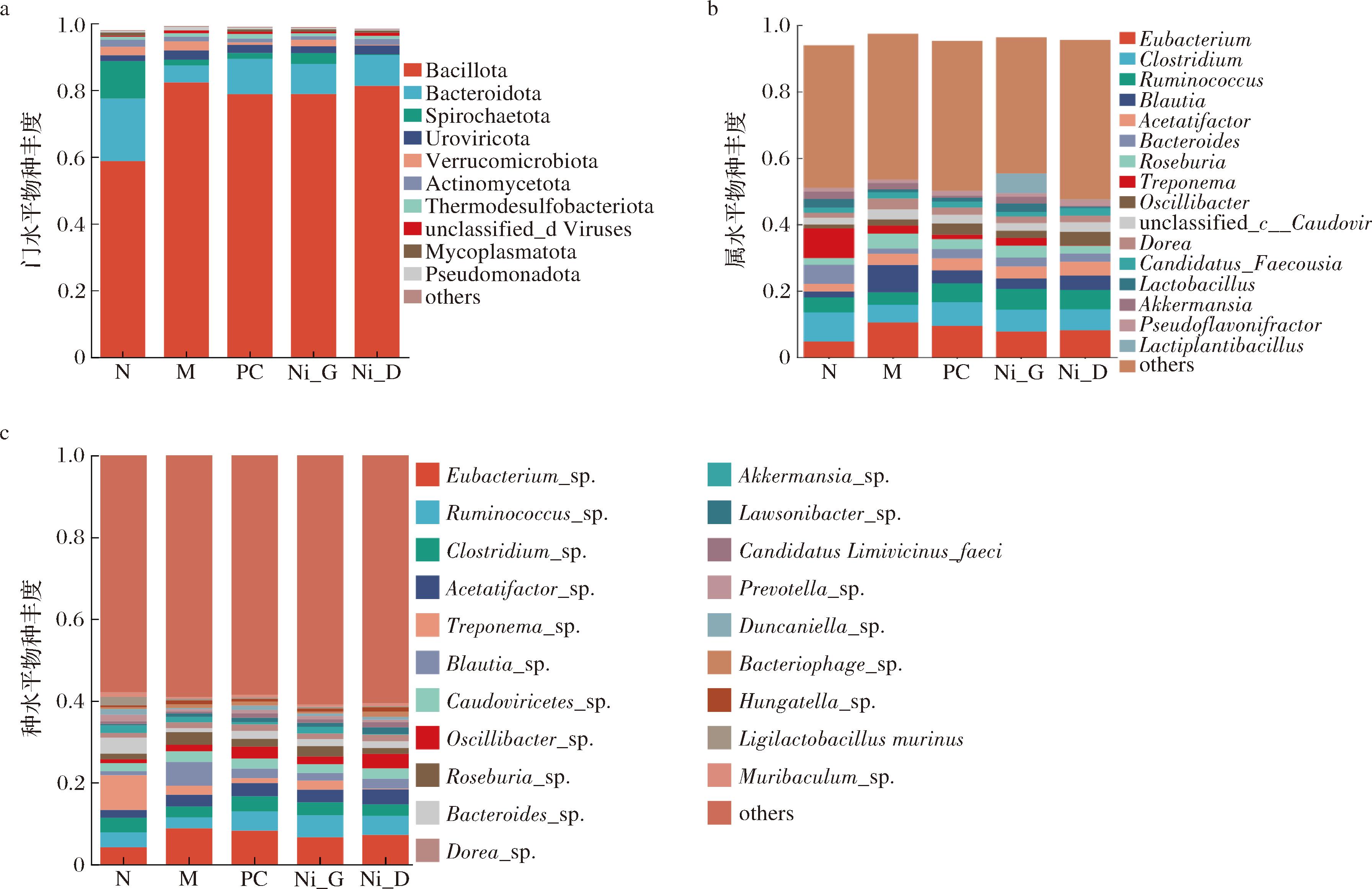
a-门水平物种丰度;b-属水平物种丰度;c-种水平物种丰度
图6 复合益生菌对大鼠肠道菌群丰度的影响
Fig.6 Effects of compound probiotics on the abundance of gut microbiota in rats
2.2.4.3 肠道菌群物种差异变化
为进一步探究肠道微生物组成的差异,通过多物种差异检验图在种水平进行差异菌群检验,如图7-a所示,Ruminococcus_sp.、Blautia_sp.、Roseburia_sp.、Lactiplantibacillus plantarum、Lactiplantibacillus_sp.等菌在各组中具有显著性差异。使用LEfSe分析确定干预前后各组显著富集微生物,以LDA分数>3为筛选标准,结果显示(图7-b),N组显著富集g_Lactobacillus等,M组显著富集毛螺菌科(Lachnospiraceae)、布劳特氏菌属(Blautia)等,Ni-G组显著富集芽孢杆菌纲(Bacilli)、乳杆菌科(Lactobacillaceae)等,Ni-D组显著富集梭菌纲(Clostridia)、颤螺菌科(Oscillospiraceae)等。进化分支图显示(图7-c),这些差异微生物主要聚集在c_Clostridia、支原体科(Mycoplasmataceae)和放线菌门(Actinomycetota)的分支上。研究表明Lactobacillus、Oscillibacter和Lactiplantibacillus等菌属与脂代谢调控相关,高脂饮食可降低其丰度[23-25]。以上结果表明,复合益生菌能通过调节菌群丰度而调节肠道菌群稳态。
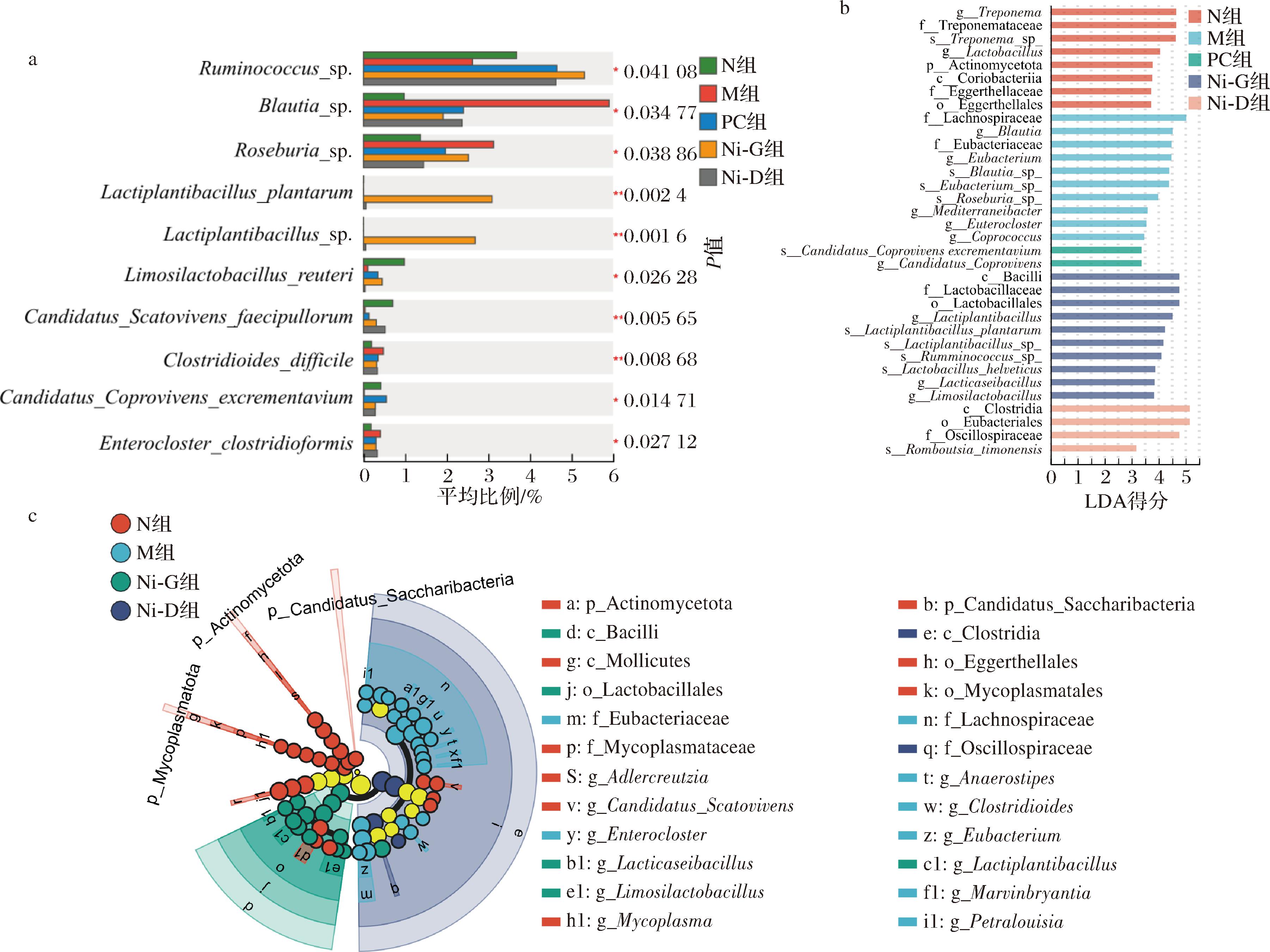
a-物种差异检验图;b-LDA图;c-进化分支图
图7 物种差异分析图
Fig.7 Analysis of species differences
2.2.4.4 肠道菌群与脂质代谢指标的相关性分析
基于Spearman相关性分析在种水平进行临床因子的相关性分析,对肠道显著富集菌与脂质代谢参数进行关联分析(图8)。结果显示,Blautia_sp.与TC、TG及血清胆汁酸呈显著正相关(P<0.05),而与丙酸、乙酸及总SCFAs呈显著负相关(P<0.05)。Lactobacillus_intestinalis与胆汁酸呈显著负相关(P<0.05),与丙酸、丁酸、乙酸和总SCFAs呈正相关(P<0.05);候选食粪栖粪菌(Candidatus_Scatovivens_faecipullorum)与TC、TG呈负相关(P<0.05),与乙酸、总SCFAs呈正相关(P<0.05)。此外,丁酸弧菌属 sp.(Butyrivibrio_sp.)、异味杆菌属 sp.(Dysosmobacter_sp.)、Oscillibacter_sp.和Lawsonibacter_sp.与LDL-C之间均呈负相关(P<0.05)。
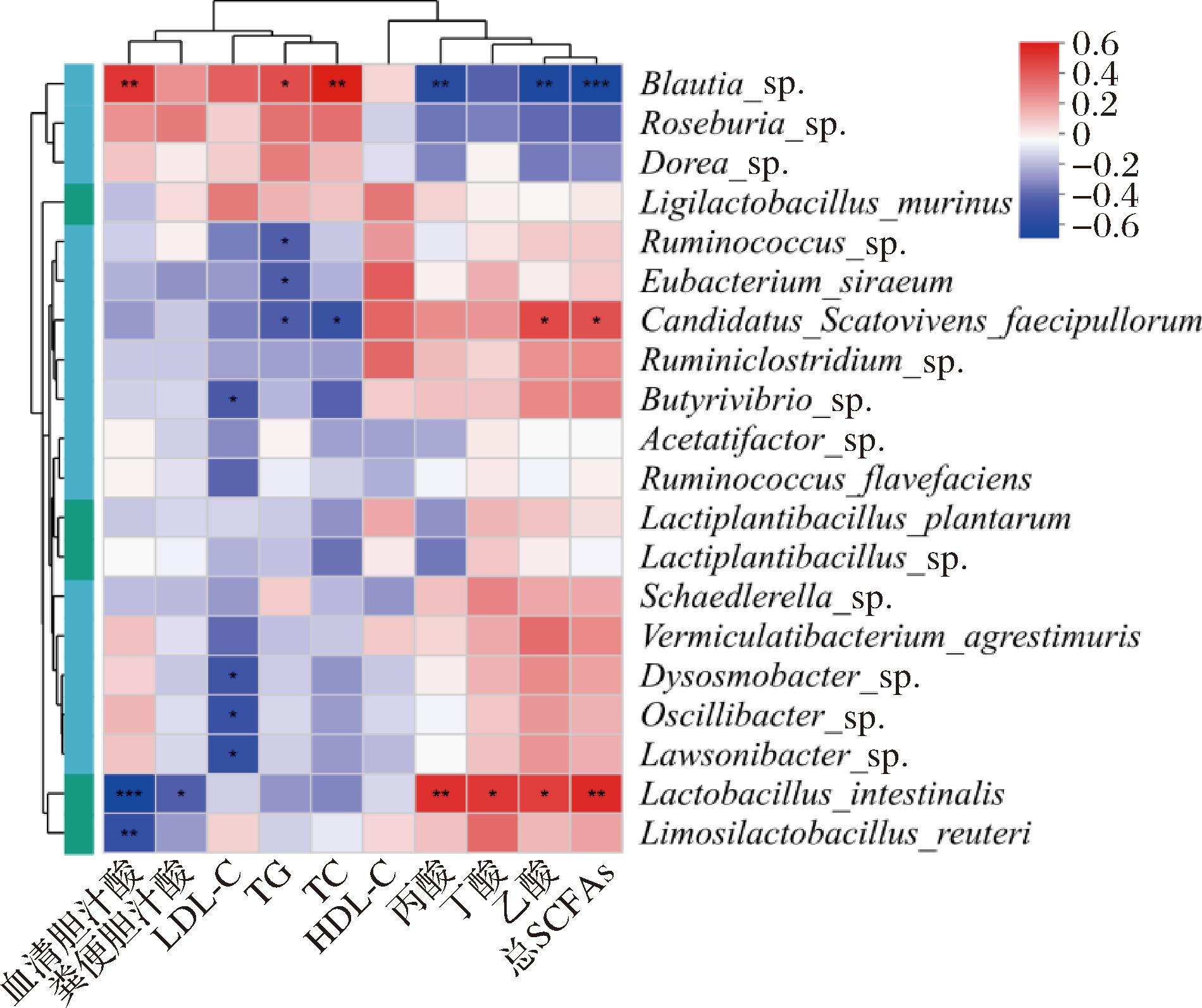
图8 肠道关键微生物菌与脂质代谢参数之间的相关性热图
Fig.8 Heatmap of the correlation between key intestinal microbial genera and lipid metabolism parameters
2.2.4.5 肠道菌群功能代谢差异变化
通过KEGG一级代谢通路进行分析,主要为代谢环境信息处理等。进一步通过KEGG二级代谢通路进行差异分析(图9),与N组相比,M组聚糖生物合成与代谢,翻译、复制与修复及内分泌系统等相关代谢通路注释显著下降(P<0.05);与M组相比,PC组复制与修复,萜类和聚酮类代谢和心血管疾病等代谢通路注释显著上升(P<0.05);复合益生菌组内分泌系统,心血管疾病和转录等相关代谢通路注释显著上升(P<0.05)。这种代谢功能重塑与菌群结构改变如Lactobacillus、Ruminococcus、Oscillibacter等升高相关,共同构成益生菌改善脂质代谢的核心机制。
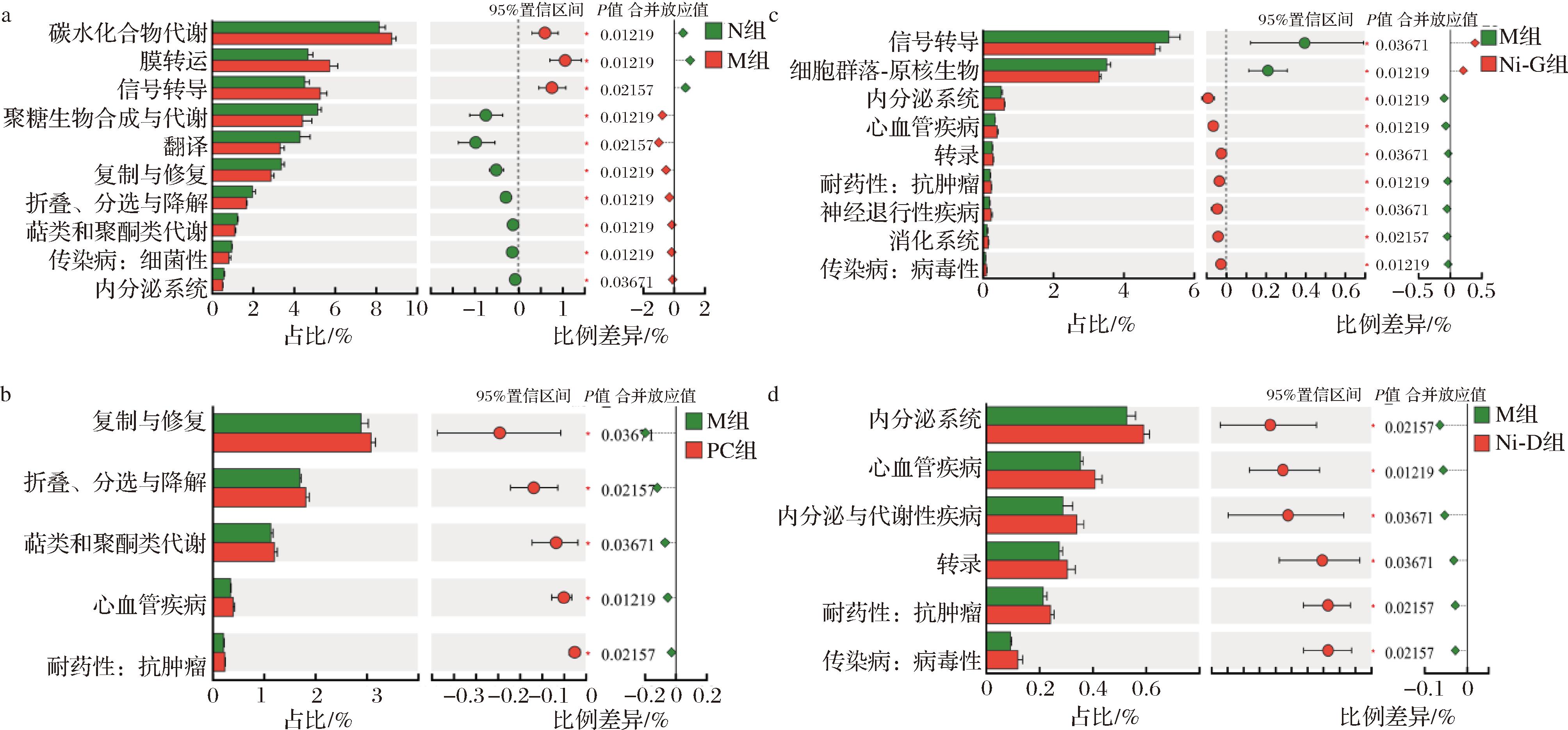
a-N组与M组功能差异图;b-M组与PC组功能差异图;c-M组与Ni-G组功能差异图;d-M组与Ni-D组功能差异图
图9 肠道菌群功能代谢差异图
Fig.9 Functional metabolic differences of intestinal microbiota
2.2.6 复合益生菌对SCFAs含量影响
SCFAs是膳食纤维经肠道菌群发酵产生的主要代谢物,主要存在于结肠,其可通过调节胆固醇、游离脂肪酸及葡萄糖代谢,减少体内脂肪积累[26],发酵马乳源复合益生菌对高脂血症大鼠粪便SCFAs含量的影响见图10。由图可知,M组粪便中乙酸、丙酸和丁酸含量显著下降(P<0.01),可能源于肠道菌群整体功能受损。经益生菌干预后,PC组和Ni-G组乙酸含量显著升高。此外,复合益生菌组丁酸含量升高但无统计学差异(P>0.05),虽然SCFAs通常通过结合G蛋白偶联受体GPR41、GPR43,调节食欲和体重,并抑制肝脏脂肪生成,但在高碳水化合物饮食诱导的肥胖状态下,这一保护性机制可能被削弱,导致肠道能量吸收增加和肝脏脂肪生成加剧[27]。
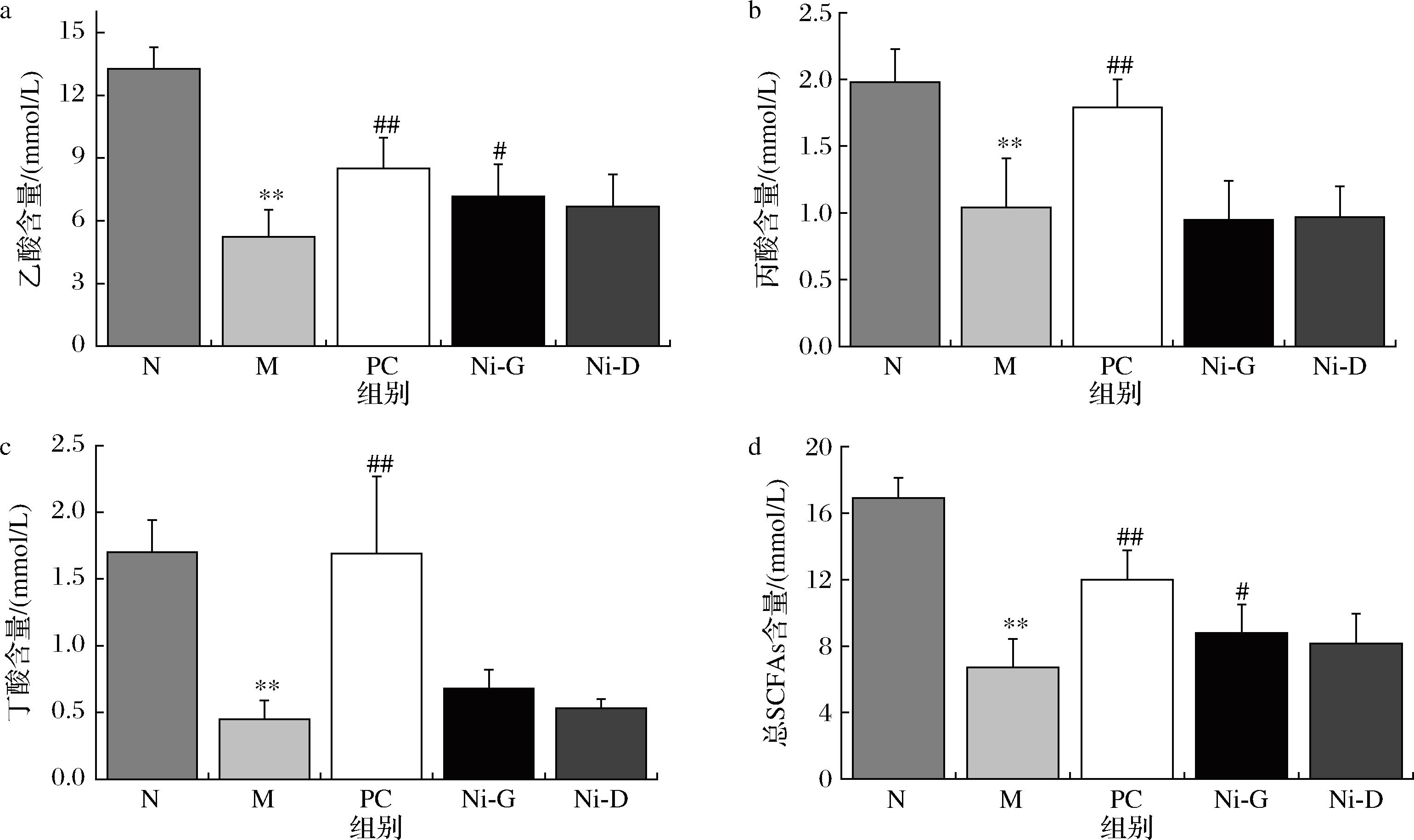
a-乙酸含量;b-丙酸含量;c-丁酸含量;d-总SCFAs含量
图10 复合益生菌对SCFAs含量影响
Fig.10 The effect of composite probiotics on SCFAs content
注:与M组相比,#表示P<0.05。
2.2.7 复合益生菌对TBA含量的影响
图11为发酵马乳源复合益生菌对高脂血症大鼠TBA含量的影响。由图可知,与N组比较,M组大鼠血清和粪便中TBA含量显著上升(P<0.01),表明高脂饮食导致大鼠TBA代谢稳态失衡,这种失衡可能源于高脂负荷下肝脏TBA合成增加、肠道重吸收效率改变或排泄途径变化。与M组相比,PC组和Ni-G组血清中TBA含量显著下降(P<0.05)。经干预后,PC组、Ni-G组和Ni-D组粪便中TBA水平显著降低,表明益生菌可能通过调节TBA肠肝循环或影响肝脏TBA合成,促进TBA代谢恢复正常,从而调节血脂水平。
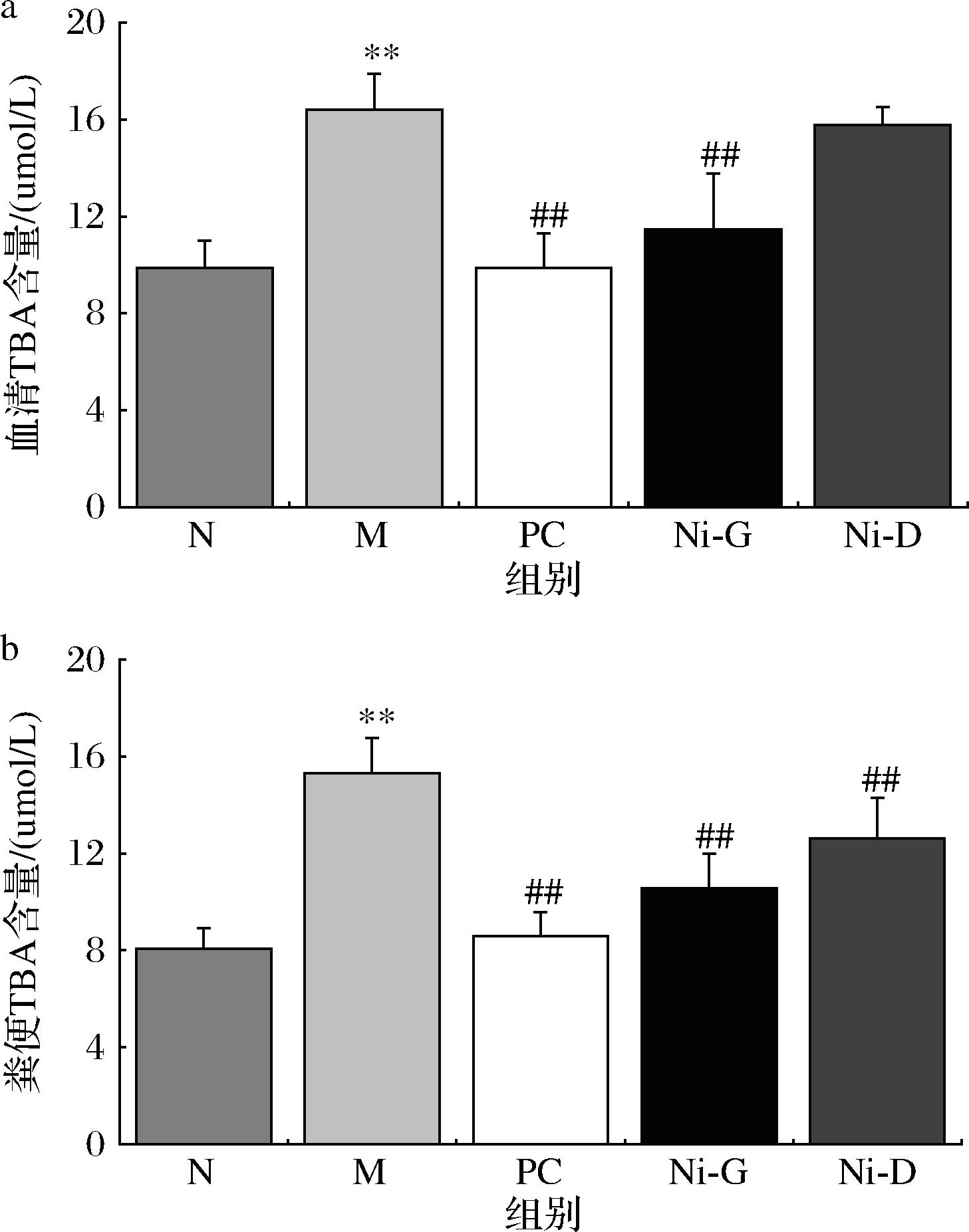
a-血清胆汁酸;b-粪便胆汁酸
图11 复合益生菌对胆汁酸含量的影响
Fig.11 The effect of composite probiotics on bile acid content
3 讨论
本研究从新疆传统发酵马乳中分离出4株植物乳植杆菌,体外实验证明复合菌的效果优于单一菌株,这一优势可能与菌株在生长过程中的相互促进、共生关系的形成以及降胆固醇机制的叠加或协同作用有关[9]。在天然发酵体系中,微生物通过代谢互补、群体感应与生态分工形成稳定的功能共同体。本研究所用菌株均来自同一发酵样品,通过实验室制备复合益生菌,主要目的是考察其调节血脂肠道菌群的作用和机制,复合益生菌降胆固醇代谢涉及胆盐解离、细菌吸附同化及胆汁酸酶活性调节等多个环节[28]。单一菌株通常作用于单一通路,而复合菌则可能通过“多靶点、多机制”协同作用,共同提升降胆固醇作用。基于此,本研究进一步通过动物实验验证该复合益生菌在体内的降胆固醇作用,并深入探讨其潜在机制。
益生菌的胃肠道黏附与定植能力是其发挥益生效应的重要基础。本研究结果显示,所选用的4株益生菌均具备良好的胃肠道黏附与定殖潜力,而这一特性是其能够在宿主肠道内存留并进一步发挥益生作用的重要基础。4株菌自聚集率均高于90%,这表明它们能在肠道内通过形成聚集体来抵抗机械清除作用,为定植提供物理屏障;对二甲苯的疏水率为23.38%~31.59%,对Caco-2细胞的黏附率为2.66%~10.00%,表明其具备良好的肠道滞留和定植潜力。
动物实验结果显示,HFD诱导大鼠出现体重显著增加和脂代谢紊乱,复合益生菌干预显著抑制体重增长,降低血清TC和LDL-C水平(P<0.01),TG亦呈下降趋势但未达显著性。肝脏病理学分析显示,益生菌干预显著减轻肝细胞脂肪变性及肝脏指数上升,表明其在缓解肝脏脂质蓄积和保护肝组织结构功能方面具有积极作用。作为脂代谢的核心器官,肝脏功能的改善与全身脂质稳态的恢复密切相关。上述结果与乳杆菌FZU0713调节血脂作用的研究一致[2]。此外,多项荟萃分析指出[29],益生菌能够有效降低血清TC和LDL-C水平,进而减少动脉粥样硬化性心血管疾病及其他相关心血管病变的风险。
宏基因组学分析显示,HFD导致肠道菌群Chao指数下降及肠道菌群群落结构紊乱,益生菌干预可逆转上述变化,恢复菌群结构。在门水平上,Bacillota/Bacteroidota比值显著降低;属水平上,Lactobacillus、Ruminococcus和Oscillibacter等菌属丰度上升;种水平上,Ruminococcus_sp.、Oscillibacter_sp.等菌株丰度升高。Spearman相关分析提示Blautia_sp.与脂代谢参数呈正相关,与SCFAs呈负相关,表明其在高脂模型中丰度升高可能与代谢异常有关[8]。Lactobacillus_intestinalis和Candidatus_Scatovivens_faecipullorum与脂代谢参数呈负相关,与SCFAs呈正相关,表明其可降低胆固醇、增强肠道屏障功能,通过调控微生态组成增强肠道代谢功能,进而系统影响宿主的脂质代谢过程[2,8,27]。此外,益生菌干预可能通过影响胆汁酸代谢,抑制初级胆汁酸重吸收,使初级胆汁酸能够进入结肠,并在结肠内通过特定肠道微生物群进一步代谢为次级胆汁酸,参与胆固醇稳态调节。本研究结果显示,复合益生菌能够降低血清总胆汁酸含量。因此,本文推测复合植物乳植杆菌可通过调节胆汁酸代谢功能,调节脂质代谢。
KEGG功能富集分析表明,差异菌群与代谢物主要富集于内分泌系统和心血管疾病相关通路。表明马乳源益生菌的降脂机制可能与多系统、多靶点调控密切相关。因此,复合益生菌可能通过协同调控菌群-SCFAs-胆汁酸轴,进而影响下游内分泌及心血管相关通路,最终实现降脂效应。
5 结论
本研究通过评价4株乳酸菌的肠道定植特性并制备复合益生菌制剂,系统探究其对高脂血症大鼠血脂及肠道菌群的作用及机制。结果表明,4株乳酸菌具有良好的肠道定植能力,且马乳源益生菌干预可显著改善高脂血症症状,具体表现为:降低体重增长(P<0.01)、降低血清TC和LDL-C水平(P<0.01)、改善肝指数及减轻肝组织脂质沉积。肠道菌群测序结果显示,马乳源益生菌能够上调Lactobacillus、Ruminococcus、Oscillibacter等水平,有效改善高脂饮食诱导的肠道菌群失调,同时能够提高粪便中乙酸、丁酸含量,降低血清胆汁酸水平(P<0.01),表明复合益生菌可通过通重塑肠道菌群结构、改善SCFAs代谢和调控胆汁酸稳态改善高脂血症大鼠的脂代谢紊乱。KEGG通路分析表明,上述调控作用与内分泌系统及心血管系统功能密切相关,提示复合益生菌可通过多靶点、多通路协同发挥降脂作用。综上,马乳源复合益生菌可有效改善高脂血症大鼠的血脂代谢异常,为发酵乳源益生菌防治代谢性疾病及开发新型益生菌制剂提供了理论和实验依据。
[1] 王增武, 郭远林. 中国血脂管理指南(基层版2024年)[J]. 中国循环杂志, 2024, 39(4):313-321.WANG Z W, GUO Y L. Chinese guideline for lipid management(primary care version 2024)[J]. Chinese Circulation Journal, 2024, 39(4):313-321.
[2] FAN X Y, ZHANG Q, GUO W L, et al. The protective effects of Levilactobacillus brevis FZU0713 on lipid metabolism and intestinal microbiota in hyperlipidemic rats[J]. Food Science and Human Wellness, 2023, 12(5):1646-1659.
[3] DING Z T, HANI A, LI W Y, et al. Influence of a cholesterol-lowering strain Lactobacillus plantarum LP3 isolated from traditional fermented yak milk on gut bacterial microbiota and metabolome of rats fed with a high-fat diet[J]. Food &Function, 2020, 11(9):8342-8353.
[4] ZAFAR H, SAIER M H Jr. Gut Bacteroides species in health and disease[J]. Gut Microbes, 2021, 13(1):1848158.
[5] KIM S J, PARK S H, SIN H S, et al. Hypocholesterolemic effects of probiotic mixture on diet-induced hypercholesterolemic rats[J]. Nutrients, 2017, 9(3): 293.
[6] LYU X C, CHEN M, HUANG Z R, et al. Potential mechanisms underlying the ameliorative effect of Lactobacillus paracasei FZU103 on the lipid metabolism in hyperlipidemic mice fed a high-fat diet[J]. Food Research International, 2021, 139:109956.
[7] SONNENBURG J L, SONNENBURG E D. Vulnerability of the industrialized microbiota[J]. Science, 2019, 366(6464): eaaw9255.
[8] LI C H, STRAŽAR M, MOHAMED A M T, et al. Gut microbiome and metabolome profiling in Framingham heart study reveals cholesterol-metabolizing bacteria[J]. Cell, 2024, 187(8):1834-1852.e19.
[9] 库尔旦·胡达依别尔根, 刘学莲, 卡吾萨尔·恰依马尔旦, 等. 分离、鉴定和筛选具有益生特性和降胆固醇能力的发酵马乳源益生菌[J]. 食品与发酵工业, 2025, 51(11):171-178.KUERDAN H D Y B G, LIU X L, KAWUSAER Q Y M E D, et al. Isolation, identification, and screening of probiotic strains with cholesterol-lowering potential from fermented mare’s milk[J]. Food and Fermentation Industries, 2025, 51(11):171-178.
[10] 肖春进, 岳秀英, 吴晓岚, 等. 羊源卷曲乳杆菌DY38的体外益生特性及抗氧化活性研究[J]. 动物营养学报, 2025, 37(2):1340-1353.XIAO C J, YUE X Y, WU X L, et al. In vitro probiotic properties and antioxidant activity of Lactobacillus crispatus DY38 from goats[J]. Chinese Journal of Animal Nutrition, 2025, 37(2):1340-1353.
[11] 陈大卫, 程月, 任晨瑜, 等. 乳杆菌耐消化应激能力及消化应激对其肠道黏附能力的影响[J]. 食品科学, 2022, 43(14):143-150.CHEN D W, CHENG Y, REN C Y, et al. Capability of Lactobacillus to tolerate digestive stress and effect of digestive stress on its intestinal adhesion capacity[J]. Food Science, 2022, 43(14):143-150.
[12] 韩雪, 李明清, 任昕宇, 等. 正常糖耐量个体粪菌液对db/db小鼠粪便短链脂肪酸的影响[J]. 中国微生态学杂志, 2022, 34(10):1117-1121; 1128.HAN X, LI M Q, REN X Y, et al. Effects of fecal microbiota from individuals with normal glucose tolerance on short-chain fatty acids in db/db mice[J]. Chinese Journal of Microecology, 2022, 34(10):1117-1121; 1128.
[13] 申屠佳倩,郑成栋,王晶宇,等.具有潜在免疫保护作用的戊糖片球菌CCFM1443及其益生特性评价[J]. 食品与发酵工业, 2025, DOI: 10.13995/j.cnki.11-1802/ts.043043.SHENTU J Q, ZHENG C D, WANG J Y, et,al. Evaluation of Pentosaccharomyces cerevisiae CCFM1443 with potential immunoprotective effects and its probiotic properties[J]. Food and Fermentation Industry, 2025, DOI: 10.13995/j.cnki.11-1802/ts.043043.
[14] ZHENG Y X, ZHAO J R, NIE X Y, et al. Mutual adhesion of Lactobacillus spp. to intestinal cells: A review of perspectives on surface layer proteins and cell surface receptors[J]. International Journal of Biological Macromolecules, 2024, 282(Pt 4):137031.
[15] 宋莺丽, 李安章, 徐帅帅, 等. 鲈鱼肠道来源降胆固醇乳酸菌分离筛选及其益生功能评价[J]. 现代食品科技, 2022, 38(8):44-52.SONG Y L, LI A Z, XU S S, et al. Isolation, screening, and probiotic function evaluation of lactic acid bacteria with cholesterol-lowering effects from the intestinal tract of seabass[J]. Modern Food Science and Technology, 2022, 38(8):44-52.
[16] 徐晶晶, 于俊娟, 严浩东, 等. 母婴来源植物乳杆菌的体外益生特性及安全性评价[J]. 食品与发酵工业, 2025, 51(6):144-151.XU J J, YU J J, YAN H D, et al. Evaluation of in vitro probiotic characteristics and safety of Lactobacillus plantarum isolated from breast milk and infant feces[J]. Food and Fermentation Industries, 2025, 51(6):144-151.
[17] WANG G, JIAO T, XU Y, et al. Bifidobacterium adolescentis and Lactobacillus rhamnosus alleviate non-alcoholic fatty liver disease induced by a high-fat, high-cholesterol diet through modulation of different gut microbiota-dependent pathways[J]. Food &Function, 2020, 11(7):6115-6127.
[18] WANG M, ZHANG B J, HU J L, et al. Intervention of five strains of Lactobacillus on obesity in mice induced by high-fat diet[J]. Journal of Functional Foods, 2020, 72:104078.
[19] ZIAEI R, GHAVAMI A, KHALESI S, et al. The effect of probiotic fermented milk products on blood lipid concentrations: A systematic review and meta-analysis of randomized controlled trials[J]. Nutrition, Metabolism and Cardiovascular Diseases, 2021, 31(4):997-1015.
[20] HUANG Z R, CHEN M, GUO W L, et al. Monascus purpureus-fermented common buckwheat protects against dyslipidemia and non-alcoholic fatty liver disease through the regulation of liver metabolome and intestinal microbiome[J]. Food Research International, 2020, 136:109511.
[21] LIU Y, JIN Y, LI J, et al. Small bowel transit and altered gut microbiota in patients with liver cirrhosis[J]. Frontiers in Physiology, 2018, 9:470.
[22] STOJANOV S, BERLEC A,  TRUKELJ B. The influence of probiotics on the firmicutes/bacteroidetes ratio in the treatment of obesity and inflammatory bowel disease[J]. Microorganisms, 2020, 8(11): 1715.
TRUKELJ B. The influence of probiotics on the firmicutes/bacteroidetes ratio in the treatment of obesity and inflammatory bowel disease[J]. Microorganisms, 2020, 8(11): 1715.
[23] CHAI Y Y, LUO J Y, BAO Y H. Effects of Polygonatum sibiricum saponin on hyperglycemia, gut microbiota composition and metabolic profiles in type 2 diabetes mice[J]. Biomedicine &Pharmacotherapy, 2021, 143:112155.
[24] LI S, ZHAI J Y, CHU W W, et al. Alleviation of Limosilactobacillus reuteri in polycystic ovary syndrome protects against circadian dysrhythmia-induced dyslipidemia via capric acid and GALR1 signaling[J]. npj Biofilms and Microbiomes, 2023, 9:47.
[25] SHANG L Y, ZHANG S, ZHANG M, et al. Natto alleviates hyperlipidemia in high-fat diet-fed mice by modulating the composition and metabolic function of gut microbiota[J]. Journal of Functional Foods, 2024, 112:105968.
[26] 王敏, 王子依, 蒋泽祯, 等. 脂肪酸摄入与肥胖的相关性研究进展[J]. 中国食品学报, 2025, 25(7):392-404.WANG M, WANG Z Y, JIANG Z Z, et al. Research progress on the correlation between fatty acid intake and obesity[J]. Journal of Chinese Institute of Food Science and Technology, 2025, 25(7):392-404.
[27] KIM K N, YAO Y, JU S Y. Short chain fatty acids and fecal microbiota abundance in humans with obesity: A systematic review and meta-analysis[J]. Nutrients, 2019, 11(10): 2512.
[28] AGOLINO G, PINO A, VACCALLUZZO A, et al. Bile salt hydrolase: The complexity behind its mechanism in relation to lowering-cholesterol lactobacilli probiotics[J]. Journal of Functional Foods, 2024, 120:106357.
[29] YAN S M, TIAN Z W, LI M, et al. Effects of probiotic supplementation on the regulation of blood lipid levels in overweight or obese subjects: A meta-analysis[J]. Food &Function, 2019, 10(3):1747-1759.