γ-氨基丁酸(γ-aminobutyric acid,GABA)是一种四碳非蛋白氨基酸,作为人体中枢神经系统内重要的抑制性神经递质。大量研究表明GABA具有多重生理功能,包括情绪调节、降血压、抗糖病、抗炎性、抗癌等作用[1],在医药和功能性食品领域备受关注。
目前制备GABA主要以化学合成、生物催化、微生物发酵等方式进行。化学合成法生产率高,但其产物杂质较多,所使用的原料或试剂具有毒性,因此所合成出的GABA不适合应用于食品、医药等行业。生物催化法合成效率、纯度高,但催化剂成本高且易失活,底物适用范围窄,大规模生产时受到限制。微生物发酵法则是利用微生物细胞内源性的谷氨酸脱羧酶(glutamic acid decarboxylase,GAD),催化L-谷氨酸脱羧,生成GABA和CO2,制备过程成本低、工艺简单,更易于规模化生产。酵母、乳酸菌、真菌等许多微生物都具有合成GABA的能力,主要通过GAD途径催化生成[2]。乳酸菌是公认安全(Generally Recognized as Safe,GRAS)的食品微生物,在发酵过程中能够产生GABA,从而被广泛应用于发酵食品、保健品和药物开发中。AHN等[3]从泡菜出筛选出产GABA的肠膜明串珠菌作为泡菜发酵剂;刘碧琦等[4]开发出GABA含量为2.01 mg/g的功能性再制奶酪,且展现出了良好的降血压潜力。TAMÉS等[5]筛选出兼具高效GABA转化能力、高冻干存活率及良好的胃肠道耐受性的青春双歧杆菌。
亚硝酸盐是一类含有亚硝酸根阴离子![]() 的化合物,通常以盐的形式存在,其摄入人体后在胃酸环境下可与蛋白质反应生成N-亚硝胺,具有较强的基因毒性,长期过量摄入可导致胃癌、肝癌、食肠癌等疾病的发生[6-7]。目前降解亚硝酸盐的方法主要分为3种:物理降解法、化学降解法、生物降解法。其中微生物降解法因高效、安全而备受关注。已有研究表明,乳酸菌接种发酵可以有效降低发酵蔬菜中的亚硝酸盐含量,因此学者们分别以发酵蔬菜、发酵乳制品等作为来源筛出可降解亚硝酸盐的菌株[8]。熊玉帛等[9]从芥菜分离出2株乳酸菌株,在培养24 h后亚硝酸盐降解率均大于90%。赵海霞等[10]从自制浆水中分离出35株乳酸菌,其中5株亚硝酸盐降解率超过90%,最高可达93.81%。肖秋颖等[11]从川西发酵牦牛乳中筛选出3株亚硝酸盐降解率大于95%的菌株。酱菜、发酵蔬菜等腌制食品是我国传统食品,风味独特深受消费者喜爱,在生产制作过程中易产生亚硝酸盐存在健康隐患。近年来,随着消费者对食品安全与营养功能的重视和大健康产业快速发展,市场对低亚硝酸盐、具备功能性的发酵食品需求持续增长,推动着传统腌制品产业加速向健康化、功能化方向转型升级。
的化合物,通常以盐的形式存在,其摄入人体后在胃酸环境下可与蛋白质反应生成N-亚硝胺,具有较强的基因毒性,长期过量摄入可导致胃癌、肝癌、食肠癌等疾病的发生[6-7]。目前降解亚硝酸盐的方法主要分为3种:物理降解法、化学降解法、生物降解法。其中微生物降解法因高效、安全而备受关注。已有研究表明,乳酸菌接种发酵可以有效降低发酵蔬菜中的亚硝酸盐含量,因此学者们分别以发酵蔬菜、发酵乳制品等作为来源筛出可降解亚硝酸盐的菌株[8]。熊玉帛等[9]从芥菜分离出2株乳酸菌株,在培养24 h后亚硝酸盐降解率均大于90%。赵海霞等[10]从自制浆水中分离出35株乳酸菌,其中5株亚硝酸盐降解率超过90%,最高可达93.81%。肖秋颖等[11]从川西发酵牦牛乳中筛选出3株亚硝酸盐降解率大于95%的菌株。酱菜、发酵蔬菜等腌制食品是我国传统食品,风味独特深受消费者喜爱,在生产制作过程中易产生亚硝酸盐存在健康隐患。近年来,随着消费者对食品安全与营养功能的重视和大健康产业快速发展,市场对低亚硝酸盐、具备功能性的发酵食品需求持续增长,推动着传统腌制品产业加速向健康化、功能化方向转型升级。
因此,分离筛选出产GABA且具有降解亚硝酸盐能力的乳酸菌菌株,在新型功能性发酵蔬菜、酱菜的开发过程中具有至关重要的作用,不仅能够提升产品的营养价值和健康功能,还能增强其市场竞争力,满足消费者对健康食品日益增长的需求。目前,已有研究主要集中于单一功能菌株的筛选与应用,分别对产GABA能力或亚硝酸盐降解能力开展研究,而对兼具这2种功能的乳酸菌研究较少。本研究从自然发酵的发酵蔬菜、奶制品中分离筛选同时具备高产GABA及高效降解亚硝酸盐的优势菌株,通过形态学及16S rDNA 分子生物学鉴定,研究其生长能力、产酸能力、降解亚硝酸盐能力等发酵特性,并针对耐酸能力、耐胆盐能力、耐胃肠液能力等进行耐受性评价及安全性评价,以获得高产GABA且具有高效降解亚硝酸盐能力的优良乳酸菌菌株,以期为开发富含GABA的健康发酵蔬菜、酱菜产品提供一定的理论参考。
1 材料与方法
1.1 材料与试剂
菌株来源:a)传统发酵酸菜:木瓜泡菜、酸芥菜、酸豇豆、酸笋,市售;b)发酵奶酪:内蒙古奶酪、云南奶酪,市售;c)其他:海南鱼茶、山东虾酱、崇左酸粥,市售。
MRS肉汤培养基、MRS琼脂培养基,广东环凯微生物科技有限公司;哥伦比亚血平板,青岛海博生物技术有限公司;GABA(色谱纯)、胃蛋白酶、胰蛋白酶,北京索莱宝科技有限公司;硼酸、四硼酸钠,天津博迪化工股份有限公司;重蒸酚,生工生物工程(上海)股份有限公司;无水乙醇、碳酸钙,成都市科隆化学品有限公司;革兰氏染色液,比常德比克曼生物科技有限公司;碳酸钙、次氯酸钠,成都金山化学试剂有限公司;亚硝酸钠,天津奥普升化工有限公司;对氨基苯磺酸、盐酸萘乙二胺,天津大茂化学试剂厂;牛胆盐,上海源叶生物科技有限公司;亚硝酸盐试剂盒,南京建成生物工程研究所。
1.2 仪器与设备
Epoch全波长扫描酶标仪,美国Biotek公司;雅马拓SQ510C立式压力蒸汽灭菌锅,重庆雅马拓科技有限公司;PHS-3C数字pH计,雷磁公司;D-37520高速冷冻离心机,德国赛默飞世尔有限公司;MJ-160生化恒温培养箱,上海博迅实业有限公司;SW-CJ-2FD净化工作台,上海博迅实业有限公司医疗设备厂。
1.3 实验方法
1.3.1 乳酸菌分离与纯化
将木瓜泡菜、酸芥菜、酸豇豆、酸笋、奶酪等样品用生理盐水按梯度稀释,取100 μL稀释液涂布于含2%(质量分数)的碳酸钙MRS琼脂培养基平板上,于37 ℃恒温倒置培养48 h。根据菌落的钙圈、菌落大小、形状、颜色等挑选出不同的单菌落,用平板进行划线,纯化至单菌落。对纯化后的菌株进行革兰氏染色镜检、过氧化氢酶实验,选取革兰氏阳性及过氧化氢酶阳性菌保存于30%(体积分数)的甘油管中,-80 ℃冻存。
1.3.2 降解亚硝酸盐菌株的初筛
参考赵强等[12]所述方法,对降解亚硝酸盐的菌株进行初步筛选。将纯化后的菌株接种至MRS肉汤培养基中活化,并以体积分数为2%的添加量将活化后的菌液接种于含有150 mg /L NaNO2的10 mL MRS肉汤中,37 ℃下静置培养48 h。后向培养基中加入2 mL 对氨基苯磺酸溶液,混匀后静置3 min,再加入1 mL 盐酸萘乙二胺溶液,混匀后静置15 min,观察各菌株培养基的颜色,与添加150 mg /L NaNO2的MRS肉汤培养基以及不添加 NaNO2 的MRS肉汤培养基进行颜色对比,筛选降解亚硝酸盐的菌株。
1.3.3 产GABA菌株的筛选
参考熊蝶等[13]方法,将纯化后的菌株接种至MRS肉汤培养基中活化,按体积分数为4%的接种量将活化好的菌种接种于100 mL 胰蛋白胨酵母膏葡萄糖(tryptone-yeast extract-glucose,TYG)肉汤培养基中,37 ℃ 150 r/min培养72 h。取菌液12 000 r/min 离心10 min,测定上清液GABA含量。
TYG肉汤培养基(g/L):胰蛋白胨10、酵母浸膏5、葡萄糖20、丁二酸钠5、L-谷氨酸10,加热溶解,冷却至室温,调节pH值至6.5,115 ℃灭菌25 min。
GABA测定方法:参考刘璐等[14]方法,采用Berthelot比色法测定。发酵液离心(10 000×g、15 min)取上清液200 μL,加入6%(体积分数)重蒸酚溶液1.0 mL、硼酸盐缓冲溶液(pH 9.5)0.5 mL,混匀,再加入5.2%(体积分数)次氯酸钠溶液1 mL,静置5 min,沸水浴加热10 min后,冰浴10 min,再加入60%(体积分数)乙醇溶液2 mL,混匀,于645 nm波长处测定吸光度值,试剂空白调零。
1.3.4 菌株鉴定
将纯化的菌株委托生工生物工程(上海)股份有限公司进行16S rDNA测序鉴定。用试剂盒提取细菌基因组DNA,用27F(AGAGTTTGATCMTGGCTCAG)和1492R(GGTTACCTTGTTACGACTT)进行16S rDNA序列扩增。经1.5%(质量分数)的琼脂糖凝胶电泳检后,将测序序列提交至NCBI数据库,进行BLAS同源性对比鉴定。
1.3.5 菌株生长曲线
参考张戴等[15]的方法,将活化后的菌液以体积分数为2%的接种量接种于MRS液体培养基中,37 ℃培养24 h。每隔2 h取样测定600 nm处吸光度值,绘制菌株的生长曲线。
1.3.6 菌株产酸曲线
参考胡此海等[16]的方法,将活化后的菌液以体积分数为2%的接种量接种于MRS液体培养基中,37 ℃培养24 h。每隔2 h取样测定总酸含量,绘制菌株的产酸曲线。
1.3.7 菌株亚硝酸盐降解能力
参考黎蓓蓓等[17]的测定方法,将活化后的菌液以体积分数为2%的接种量接种于含200 mg/L亚硝酸盐的MRS肉汤培养基中,37 ℃下静置培养24 h。采用亚硝酸盐试剂盒测定12、24 h 时MRS肉汤培养基中亚硝酸盐含量,根据公式(1)计算亚硝酸盐降解率:
亚硝酸盐降解率![]()
(1)
式中:C0为未接种培养基中NaNO2质量,mg;C1为发酵菌液中NaNO2质量,mg。
1.3.8 菌株耐酸性
参考姚有莉[18]方法,将菌液在600 nm处的吸光度值调整至(1.0±0.1),按体积分数为2%的接种量分别接种于pH值为2.0、3.0、4.0、5.0的MRS 液体培养基中,37 ℃培养24 h后测定菌液在600 nm处的吸光度值,以pH 6.5 MRS液体培养基在600 nm处的吸光度值为对照,根据公式(2)计算存活率:
存活率![]()
(2)
式中:样品组OD600nm值为不同pH的MRS液体培养基OD600nm值,对照组OD600nm值为pH 6.5的MRS 液体培养基OD600nm值。
1.3.9 菌株耐胆盐性
参考汤凯等[19]方法,将菌液在600 nm处的吸光度值调整至(1.0±0.1),按体积分数为2%的接种量接种于含质量分数为0.1%、0.2%、0.3%牛胆盐的MRS液体培养基中,37 ℃恒温培养24 h,测定24 h的OD600nm值,以不加牛胆盐的MRS液体培养基为对照,根据公式(3)计算菌株对胆盐的存活率:
存活率![]()
(3)
式中:样品组OD600nm值为含胆盐组MRS液体培养基OD600nm值,对照组OD600nm值为不含胆盐组MRS液体培养基OD600nm值。
1.3.10 菌株人工胃肠液耐受性
参考孙晓琛等[20]方法。取1 mL菌悬液加到9 mL 模拟胃液中,充分混合后37 ℃ 150 r/min消化3 h,取消化0、3 h 菌液进行平板计数,以消化0 h的活菌数为对照,计算存活率。从模拟胃液取1 mL加入9 mL模拟肠液,37 ℃下培养3 h,取消化0、3 h菌液进行平板计数,以消化0 h的活菌数为对照,按照公式(4)计算菌株对模拟胃肠液的耐受性:
存活率![]()
(4)
式中:N0h为接种第0 h的活菌数,lg CFU/mL;N3h为接种第3 h的活菌数,lg CFU/mL。
1.3.11 菌株安全性
参考武芷伊等[21]的方法,将纯化后的菌株活化,接种于哥伦比亚血平板上,37 ℃培养48 h后,观察溶血现象并拍照记录。菌落周围出现绿色溶血圈为α-溶血;菌落周围出现透明溶血圈为β-溶血;无溶血圈为γ-溶血。
1.4 数据处理
所有测定数据为3次以上重复实验的“平均值±标准差”;使用SPSS 26.0、GraphPad Prism9.5.0软件进行统计分析、绘图,利用邓肯多重比较法(Duncan)对数据间进行差异显著性分析,P<0.05表示差异显著。
2 结果与分析
2.1 乳酸菌筛选
2.1.1 乳酸菌分离与纯化
将从发酵蔬菜、乳制品等样品中分离筛选出的菌株在MRS琼脂培养基平皿中划线分离纯化,部分菌落形态与镜检结果见图1,共筛选获得74株疑似乳酸菌。这些菌株菌落呈乳白色,表面光滑湿润,在菌落周围形成明显的透明钙圈。显微镜下观察菌体形态多为杆状、球状或卵圆形,排列方式包括单个、成对或链状排列。经革兰氏染色结果均为阳性,过氧化氢酶试验均为阴性,均符合乳酸菌的典型生理生化特征。
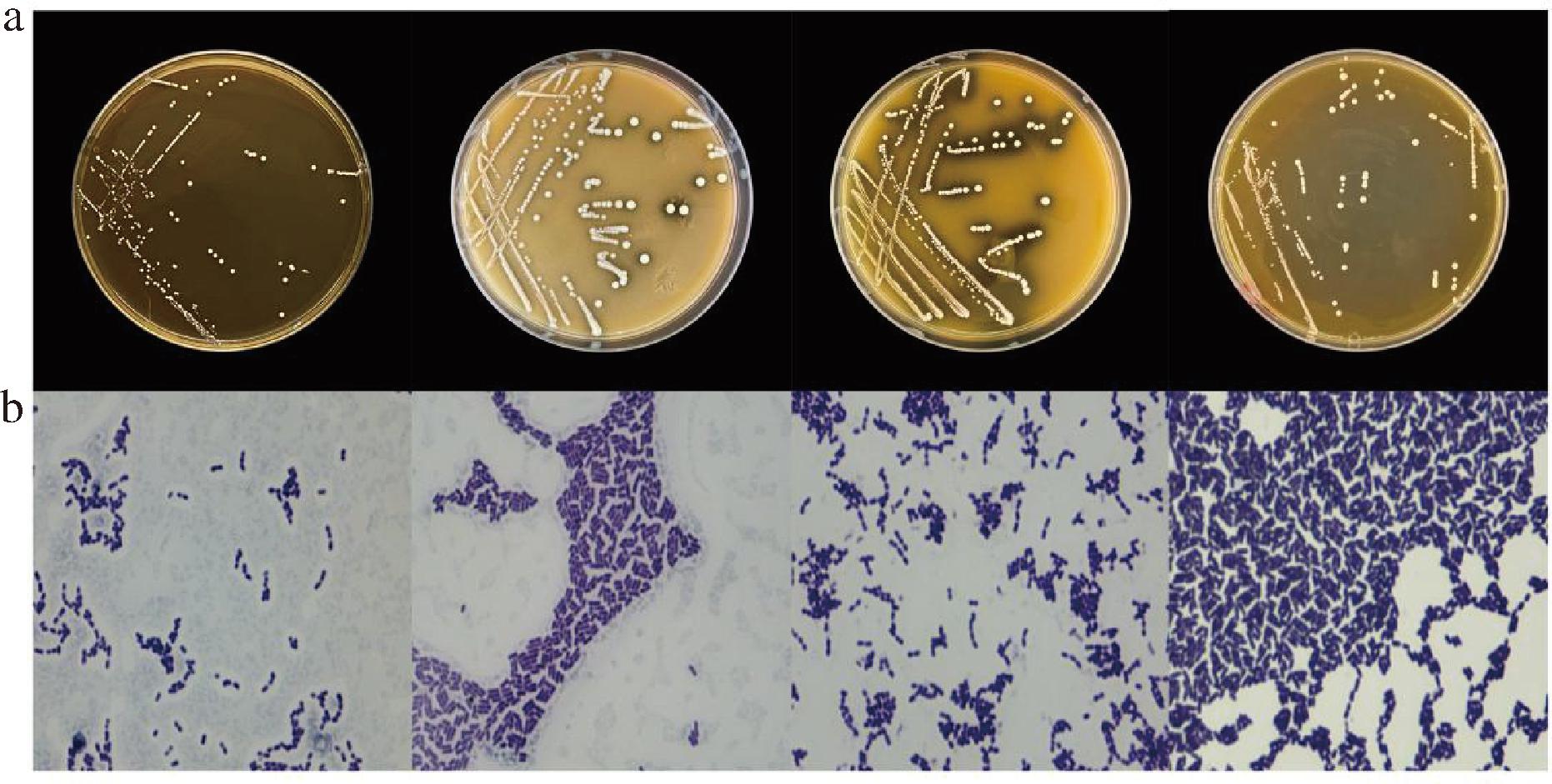
a-分离培养形态;b-革兰氏染色
图1 部分菌株菌落形态
Fig.1 Colony morphology of some strain
2.1.2 降解亚硝酸盐乳酸菌的初筛
通过比色法反应后的溶液颜色变化初步判断乳酸菌降解亚硝酸盐的能力。若颜色与对照管接近或更深,其亚硝酸盐残留量越高,说明菌株降解能力较低或毫无降解能力;颜色越浅残留量越低,说明降解亚硝酸能力越高[22-23]。对74株菌进行了亚硝酸盐降解能力筛选,发现所有菌株均具有一定的亚硝酸盐降解能力,图2为部分乳酸菌的亚硝酸盐反应图。由图2可知,乳酸菌试管颜色均浅于对照管,各管颜色不一,说明均能够降解亚硝酸盐,且不同菌株降解能力不同。

图2 降解亚硝酸盐筛选
Fig.2 Degradation of nitrite screening
注:A0为空白(无亚硝酸钠MRS肉汤培养基),A1为阴性对照
(含亚硝酸钠的MRS肉汤培养基),A2~A20为样品组(不同菌株)。
2.1.3 产GABA乳酸菌的筛选
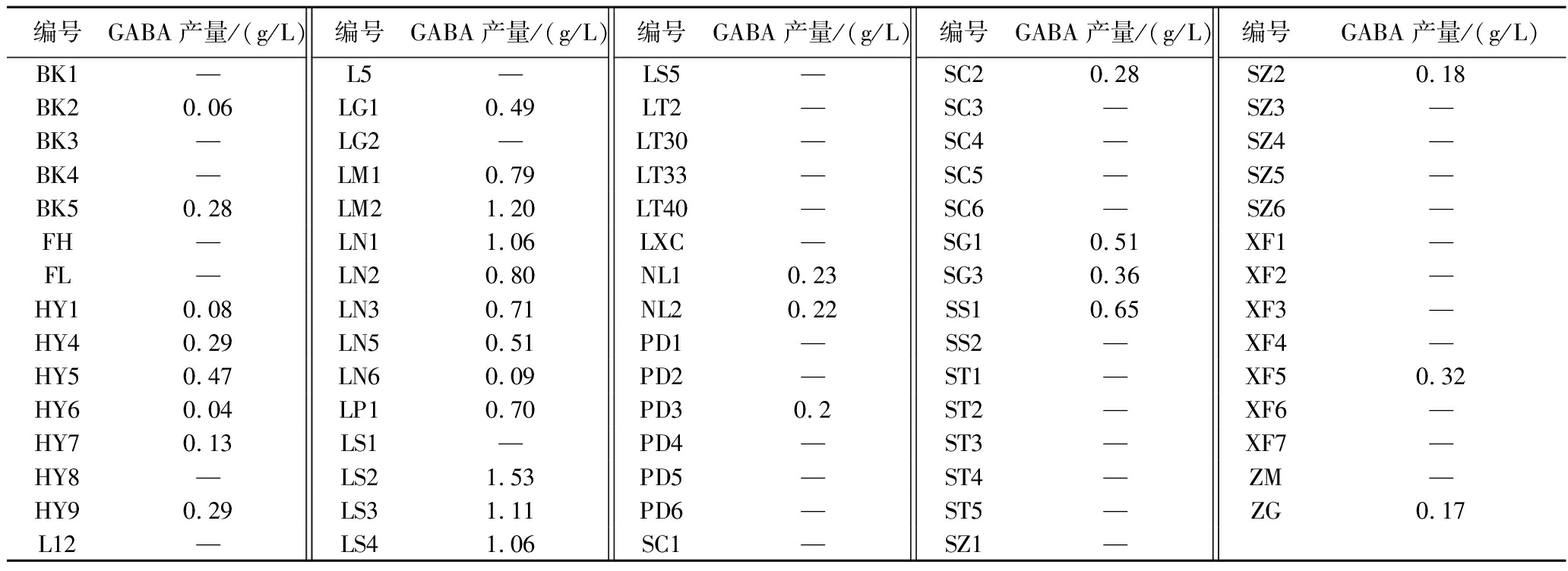
从样品中共筛选出74株乳酸菌,Berthelot比色法测定GABA产量如表1所示。结果表明,部分菌株具有较高的GABA产出能力。其中,5株菌(LM2、LS2、LS3、LN1、LS4)GABA产量超过1.0 g/L,LS2产量最高为1.53 g/L,LM2次之为1.20 g/L。相较之下,大多数菌株GABA产量较低或未检测出,说明不同菌株GABA生成能力存在较大差异。因此,选择GABA产量前10的菌株进行后续实验。
表1 产GABA乳酸菌筛选
Table 1 Screening of GABA producing lactic acid bacteria
编号GABA产量/(g/L)编号GABA产量/(g/L)编号GABA产量/(g/L)编号GABA产量/(g/L)编号GABA产量/(g/L)BK1—L5—LS5—SC20.28SZ20.18BK20.06LG10.49LT2—SC3—SZ3—BK3—LG2—LT30—SC4—SZ4—BK4—LM10.79LT33—SC5—SZ5—BK50.28LM21.20LT40—SC6—SZ6—FH—LN11.06LXC—SG10.51XF1—FL—LN20.80NL10.23SG30.36XF2—HY10.08LN30.71NL20.22SS10.65XF3—HY40.29LN50.51PD1—SS2—XF4—HY50.47LN60.09PD2—ST1—XF50.32HY60.04LP10.70PD30.2ST2—XF6—HY70.13LS1—PD4—ST3—XF7—HY8—LS21.53PD5—ST4—ZM—HY90.29LS31.11PD6—ST5—ZG0.17L12—LS41.06SC1—SZ1—
注:—表示未检出。
2.2 菌株鉴定
2.2.1 形态学鉴定
图3可以看出,10株菌株的菌落呈圆形或椭圆形,表面光滑湿润,边缘整齐,呈乳白色;如图4所示,经革兰氏染色,10株菌株均为革兰氏阳性菌,其中LP1为葡萄球形,其他菌株均为杆状。
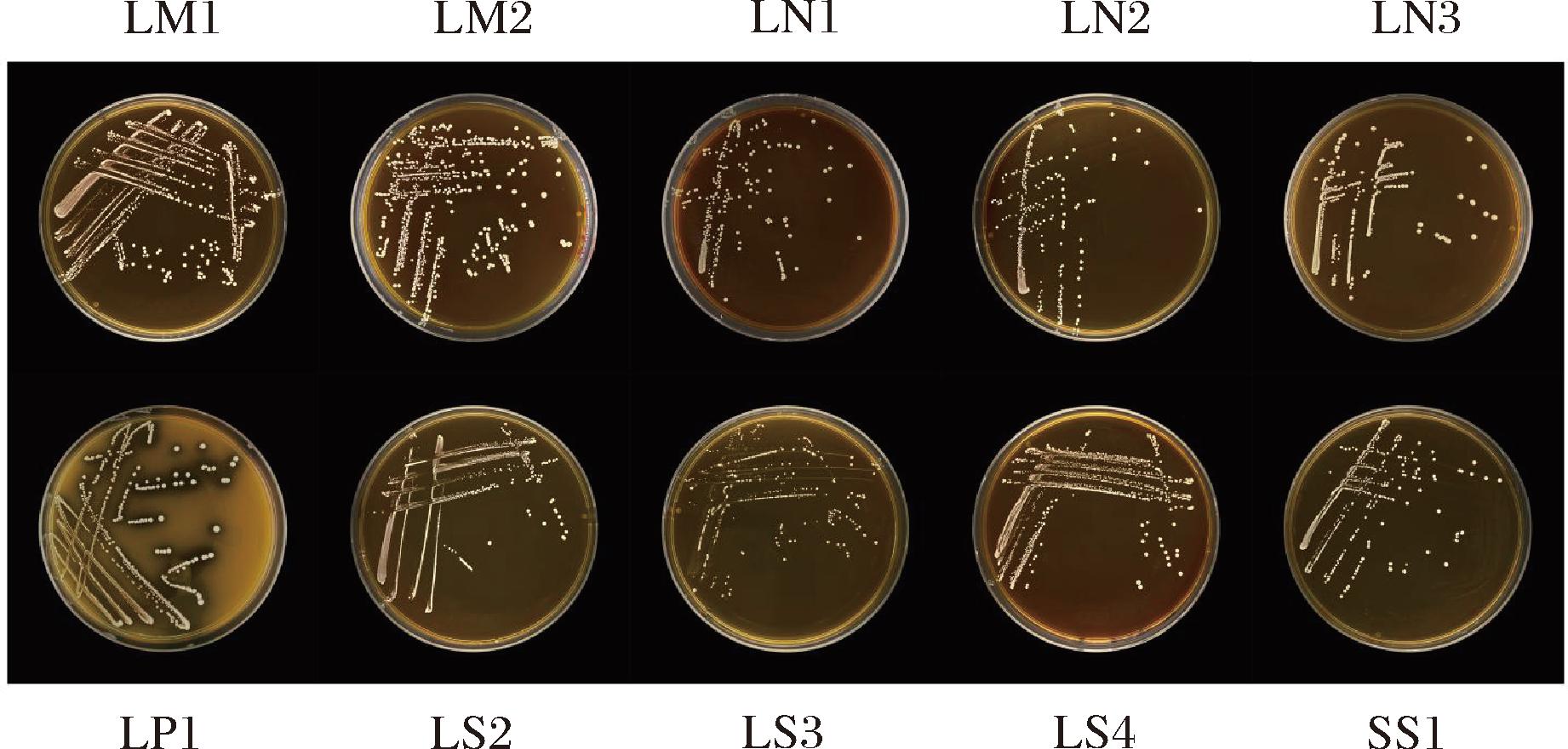
图3 10株菌株的菌落形态
Fig.3 Colony morphology of ten strains
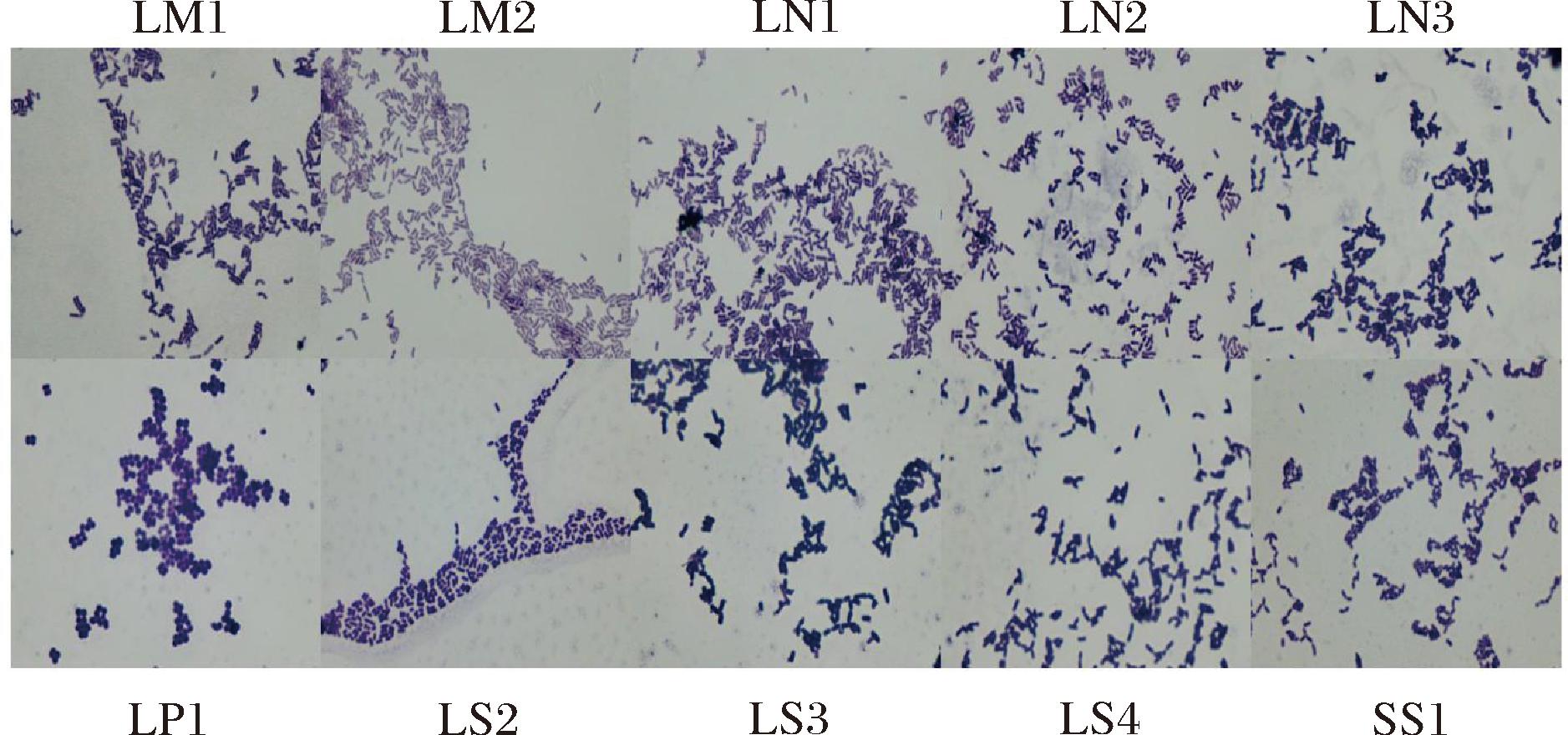
图4 10株菌株的革兰氏染色镜检图
Fig.4 Gram stain microscope image of ten strains
2.2.2 菌株16S rDNA鉴定
图5为10株乳酸菌的16S rDNA的PCR扩增产物电泳图。由图可知,10株乳酸菌的目标片段在约1 500 bp处均出现明亮单一条带,均被成功扩增。对10株菌进行16S rDNA测序鉴定。菌株LM1、LM2、LN1、LN2、LN3、LS2、LS3、LS4、SS1鉴定为植物乳植杆菌(Lactiplantibacillus plantarum),LP1鉴定为戊糖片球菌(Pediococcus pentosaceus)。
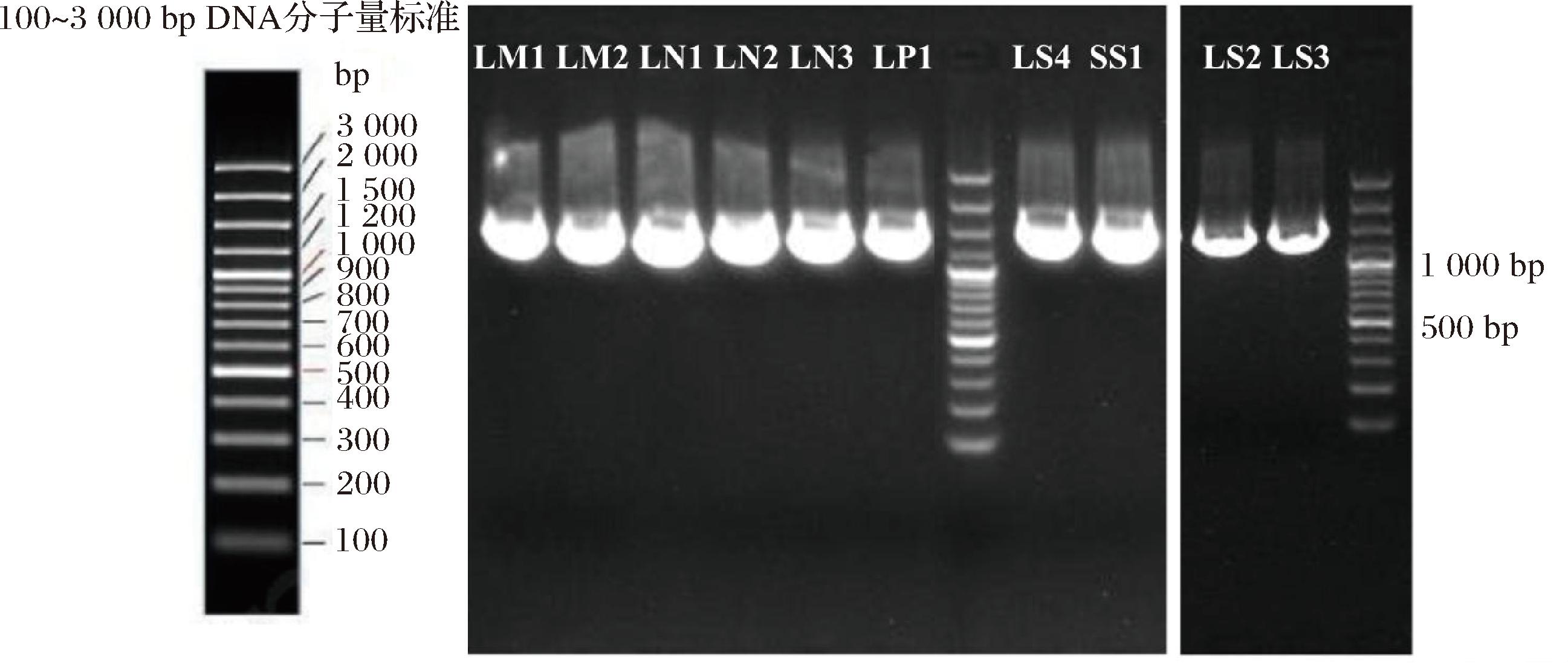
图5 16S rDNA PCR电泳图
Fig.5 16S rDNA PCR amplification map
2.3 乳酸菌生长曲线
乳酸菌生长曲线反映菌体数量随时间变化的规律,是评估菌株活力和发酵效果的重要依据。由图6-a可知,10株菌呈现典型的S型的生长曲线[24]。在培养初期(0~3 h)OD600nm值增幅较小,应是乳酸菌处于适应期,代谢活动缓慢,增殖不明显。3 h后进入生长对数期,OD600nm值快速上升,说明乳酸菌代谢活性增强,细胞分裂旺盛,菌体密度增高。18 h后,OD600nm值增长变缓并趋于稳定,表明乳酸菌进入稳定期,此时细胞增殖和死亡速率大致相等,菌液浓度达到相对稳定状态[13]。10株菌株在培养24 h后OD600nm值均达到1.6左右,整体增殖能力较强。LM2、LS2的OD600nm值在培养初期至24 h均从0.14持续上升至1.64、1.65,其中LS2增幅最大,LM2次之。
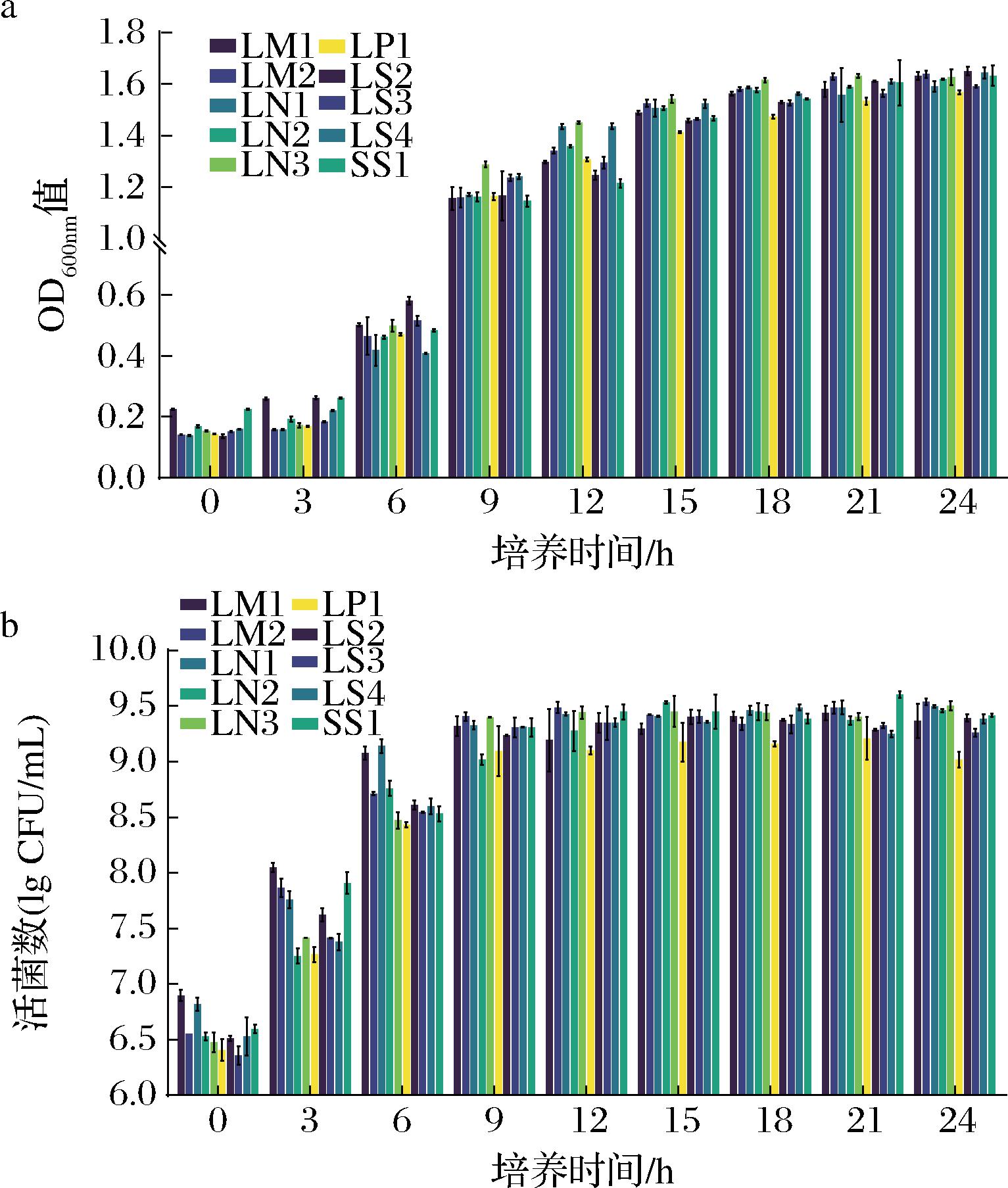
a-OD600nm值;b-活菌数
图6 10株菌株的生长曲线
Fig.6 Growth curves of ten strains
由图6-b可知,10株菌株活菌数在0~9 h时缓慢上升,9 h后进入稳定期,其中在24 h时LM2活菌数最大[(9.53±0.16)lg CFU/mL],LS2活菌数较低[(9.39±0.03)lg CFU/mL]。综上,LM2和LS2均表现出较强的增殖能力和良好的生长特性,其中LM2在活菌数方面更具优势,显示出良好生长特性与应用潜力。
2.4 乳酸菌产酸曲线
乳酸菌产酸曲线是衡量其代谢活性和发酵性能的重要指标。图7-a表示不同菌株在培养过程中产酸量的变化情况,10株菌株的产酸能力存在差异。随着培养时间的延长,各菌株产酸量均呈上升趋势。所有菌株都处于快速增长的对数期间时(3 h后),乳酸菌迅速扩增导致乳酸和其他有机酸的大量产生,进而使总酸含量快速累积。随后当菌株达到稳定生长期时(3 h后),其产酸速度趋于平缓,总酸含量上升缓慢。生长速度快、产酸能力强的乳酸菌,能有效提高发酵效率及降低pH值,从而抑制腐败菌的生长。培养初期时,10株菌总酸含量为4.4~5.3 g/L,至培养24 h时,总酸含量为17.7~21.7 g/L,其中LM2总酸产量最高,LS2排名第二。在培养15~21 h时,LM2、LS2的产酸量分别从15.05、13.89 g/L增至21.65、20.42 g/L,总酸含量分别增加6.6、5.3 g/L,与其他菌株相比,增幅明显。
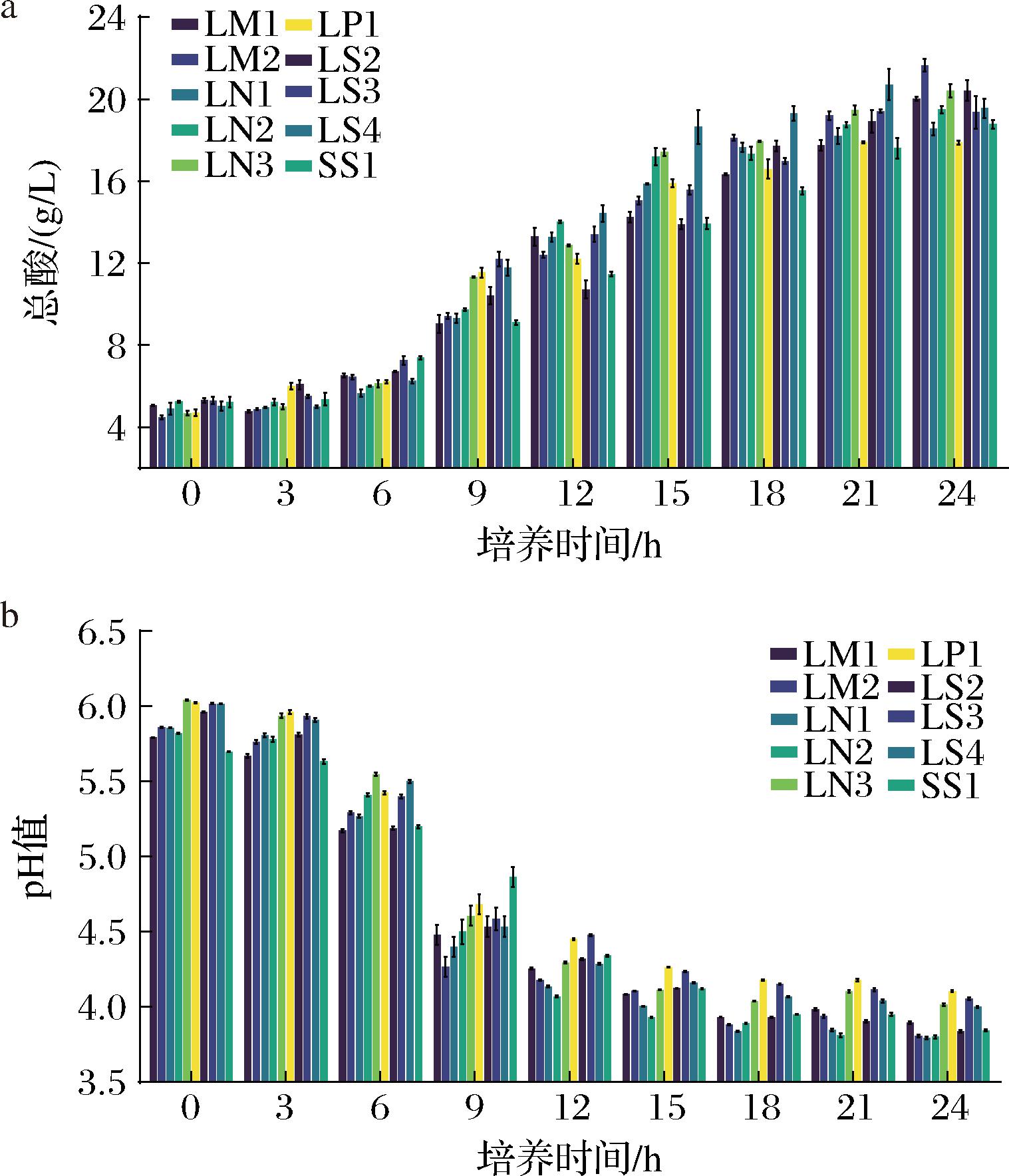
a-总酸;b-pH值
图7 10株菌株的产酸曲线
Fig.7 Acid production curves of ten strains
不同菌株在培养过程中pH值的变化情况见图7-b。10株菌株均随着培养时间延长而降低,并在18 h后趋于稳定,与总酸曲线呈明显的负相关关系,展现出典型的产酸曲线变化特征。培养初期时,10株菌pH值为5.70~6.04,培养24 h时,下降至3.79~4.11。在培养15~21 h时,LM2和LS2的总酸含量显著上升,产酸速率加快,均与其pH值下降幅度一致。表明LM2和LS2两株菌产酸能力强,代谢活性较高。
2.5 乳酸菌亚硝酸盐降解能力
在发酵蔬菜、酱菜等传统发酵食品中,乳酸菌对亚硝酸盐的降解是提升食品安全性的重要作用机制之一。乳酸菌通过产酸降pH值、分泌亚硝酸盐还原酶、抑制产亚硝酸盐微生物及构建稳定微生态系统等多重机制,有效降解发酵蔬菜、酱菜等传统发酵食品中的亚硝酸盐[25]。由图8可知,在含有200 mg/L NaNO2的培养基中培养12 h时,SS1、LM2的降解率最高,分别为95.73%、94.15%,显著高于其他8株菌株(P<0.05);LN1亚硝酸盐降解率最低,仅为37.20%;其余菌株的降解率为43%~81%。培养24 h时,10株菌的降解率均在93%之上,SS1降解率最高为99.83%;其次有7株菌(LM1、LM2、LN1、LN3、LP1、LS2、LS3)降解率为98.5%~99.1%且无显著性差异(P>0.05);LN2、LS4降解率最低,分别为97.38%、93.72%。结果说明10株菌株均有高降解亚硝酸的能力,不同菌株降解能力不同。
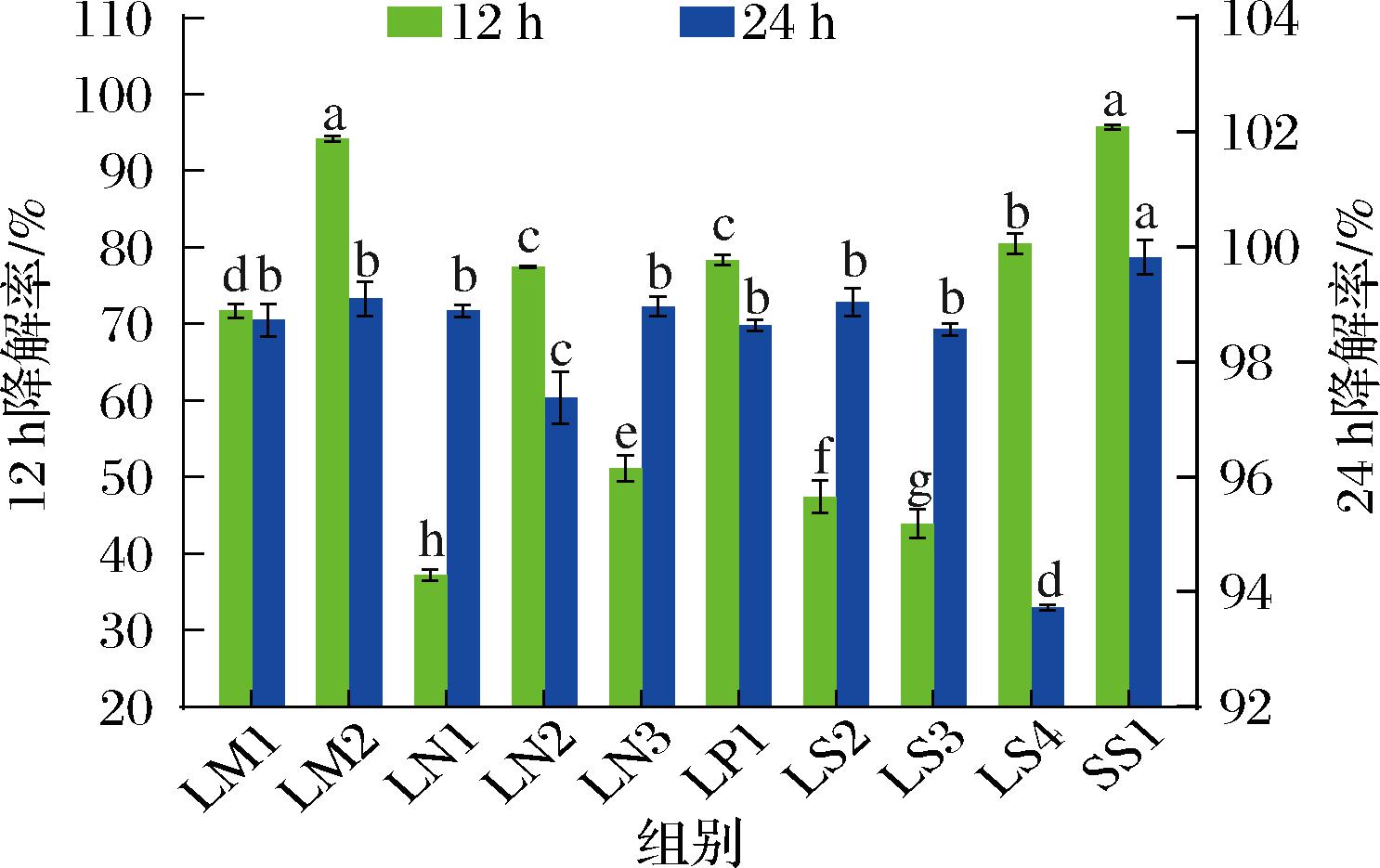
图8 10株菌株亚硝酸盐降解率
Fig.8 Nitrite degradation rate of ten strains
注:组间不同小写字母表示差异显著(P<0.05)(下同)。
2.6 菌株耐酸性
乳酸菌在酸性环境下的耐受性会影响其益生功能的功效。如表2所示,随着培养环境pH值升高,菌株存活率也随之升高,这说明酸性环境对乳酸菌的生长有很大的影响。在pH 2.0和pH 3.0的条件下,10株菌的存活率较低,生长活性受到了抑制,其存活率为4.13%~7.71%。随着pH值的升高,菌株的耐酸性也随之增强。在pH 4.0时,有7株菌株的存活率高于75%;在pH 5.0时10株菌株的存活率均高于80%。LS2在pH值为2.0~5.0时,与其他菌株相比存活率均较高,其中在pH 2.0、pH 5.0最高,分别为5.83%、99.27%;LM2在pH 5.0时为98.55%,略低于LS2。
表2 10株菌株耐酸性
Table 2 Acid resistance of ten strains
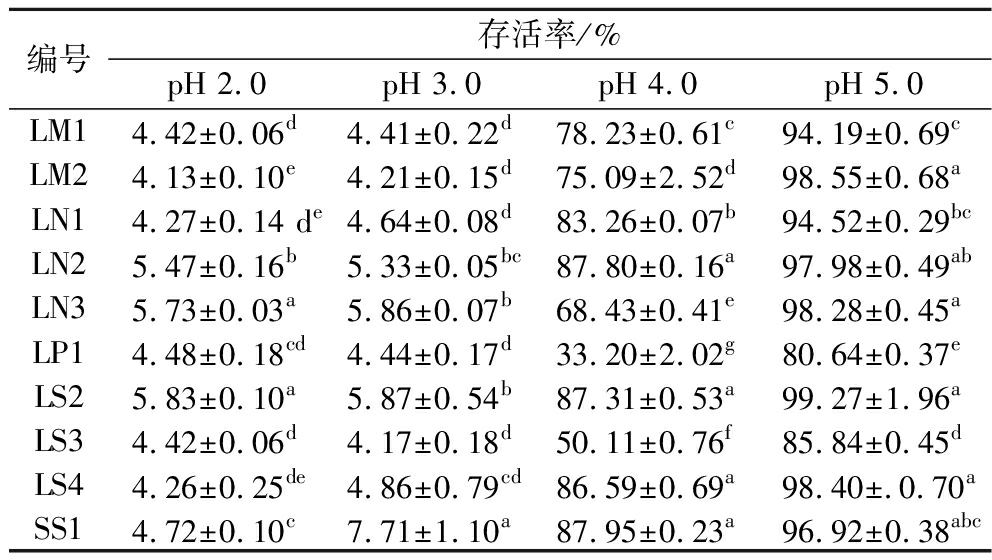
编号存活率/%pH 2.0pH 3.0pH 4.0pH 5.0LM14.42±0.06d4.41±0.22d78.23±0.61c94.19±0.69cLM24.13±0.10e4.21±0.15d75.09±2.52d98.55±0.68aLN14.27±0.14 de4.64±0.08d83.26±0.07b94.52±0.29bcLN25.47±0.16b5.33±0.05bc87.80±0.16a97.98±0.49abLN35.73±0.03a5.86±0.07b68.43±0.41e98.28±0.45aLP14.48±0.18cd4.44±0.17d33.20±2.02g80.64±0.37eLS25.83±0.10a5.87±0.54b87.31±0.53a99.27±1.96aLS34.42±0.06d4.17±0.18d50.11±0.76f85.84±0.45dLS44.26±0.25de4.86±0.79cd86.59±0.69a98.40±.0.70aSS14.72±0.10c7.71±1.10a87.95±0.23a96.92±0.38abc
注:组间不同小写字母表示差异显著(P<0.05)(下同)。
2.7 菌株胆盐耐受性
胆盐是人体胆汁的主要成分,不仅参与脂质消化,还能破坏微生物细胞膜结构,从而影响乳酸菌在人体肠道存活、定殖并发挥其益生菌作用[26]。不同菌株对胆盐的耐受能力如表3所示,发现不同菌株在不同胆盐浓度下的存活率存在显著差异(P<0.05)。在含0.1%~0.3%(质量分数)胆盐的培养基中培养24 h,LN2存活率均为最高且较为稳定,分别为88.01%、83.69%、88.27%,应是在胆盐胁迫下,菌株的细胞损伤较小,能保持稳定的存活率。LM2存活率随着胆盐添加量增加呈现先上升后下降趋势,但在添加量为0.2%、0.3%时存活率分别为82.00%、67.38%,均保持在较高水平。LS2则随着胆盐添加量增加出现下降后上升的趋势,在添加量为0.3%时存活率为67.84%。相比之下,3株菌(LM1、LP1、LS4)在添加量为0.3%时存活率较低,分别为34.50%、20.95%、32.67%,说明菌株在高胆盐的环境下细胞膜受到破坏,细胞的正常代谢活动受到影响,也抑制了菌株的生长[27]。
表3 10株菌株耐胆盐存活率 单位:%
Table 3 Bile salt tolerant survival rate of ten strains
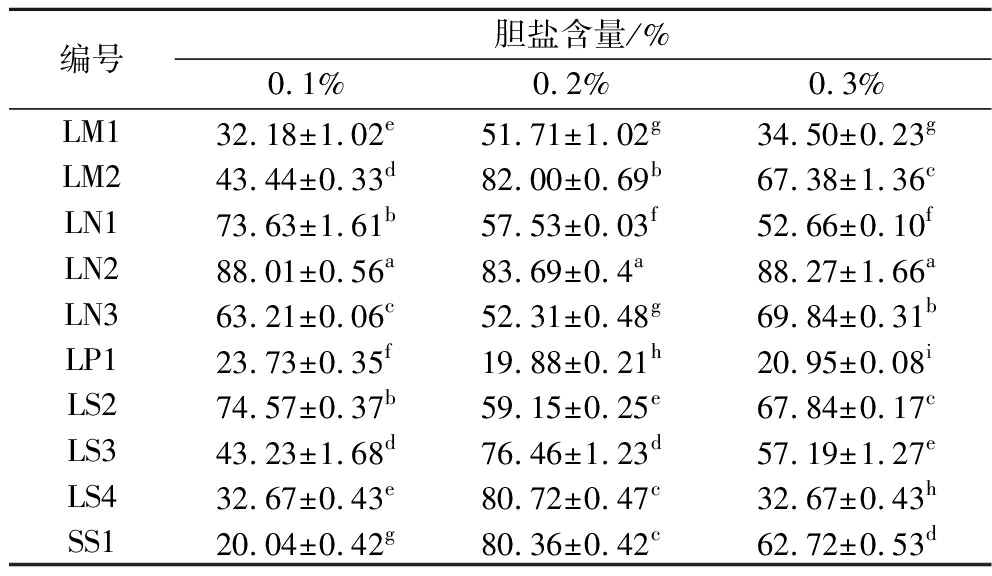
编号胆盐含量/%0.1%0.2%0.3%LM132.18±1.02e51.71±1.02g34.50±0.23gLM243.44±0.33d82.00±0.69b67.38±1.36cLN173.63±1.61b57.53±0.03f52.66±0.10fLN288.01±0.56a83.69±0.4a88.27±1.66aLN363.21±0.06c52.31±0.48g69.84±0.31bLP123.73±0.35f19.88±0.21h20.95±0.08iLS274.57±0.37b59.15±0.25e67.84±0.17cLS343.23±1.68d76.46±1.23d57.19±1.27eLS432.67±0.43e80.72±0.47c32.67±0.43hSS120.04±0.42g80.36±0.42c62.72±0.53d
2.8 菌株人工胃肠液耐受性
模拟人工胃肠液耐受性实验反映了菌株在实际人体胃肠道环境中,抵御消化液侵蚀、维持活性的潜力。乳酸菌因独特的细胞结构和生理特性使其能够有效抵御人工胃液的强酸环境及胃蛋白酶的降解作用,在胃肠道中维持较高的活菌数。活菌数与乳酸菌调节肠道菌群平衡、强化肠道屏障功能、实现免疫调节作用等益生功能密切相关,若活菌数过低,难以实现预期的益生效果。如图9所示,10株菌通过pH 3.0的模拟人工胃液处理3 h后,其中LM2耐受性最好,存活率高达99.42%;LN3、LS4次之,存活率96.78%、95.41%;LN2存活率最低为76.64%,其余6株菌存活率较高为82%~93%。经过模拟人工肠液处理3 h后,LS3、LM2存活率最高分别为94.18%、93.43%,2株菌之间无显著性差异(P>0.05);LN2存活率最低,为36.16%,说明LN2在人工肠液环境适应能力较差[28],影响了菌株存活。
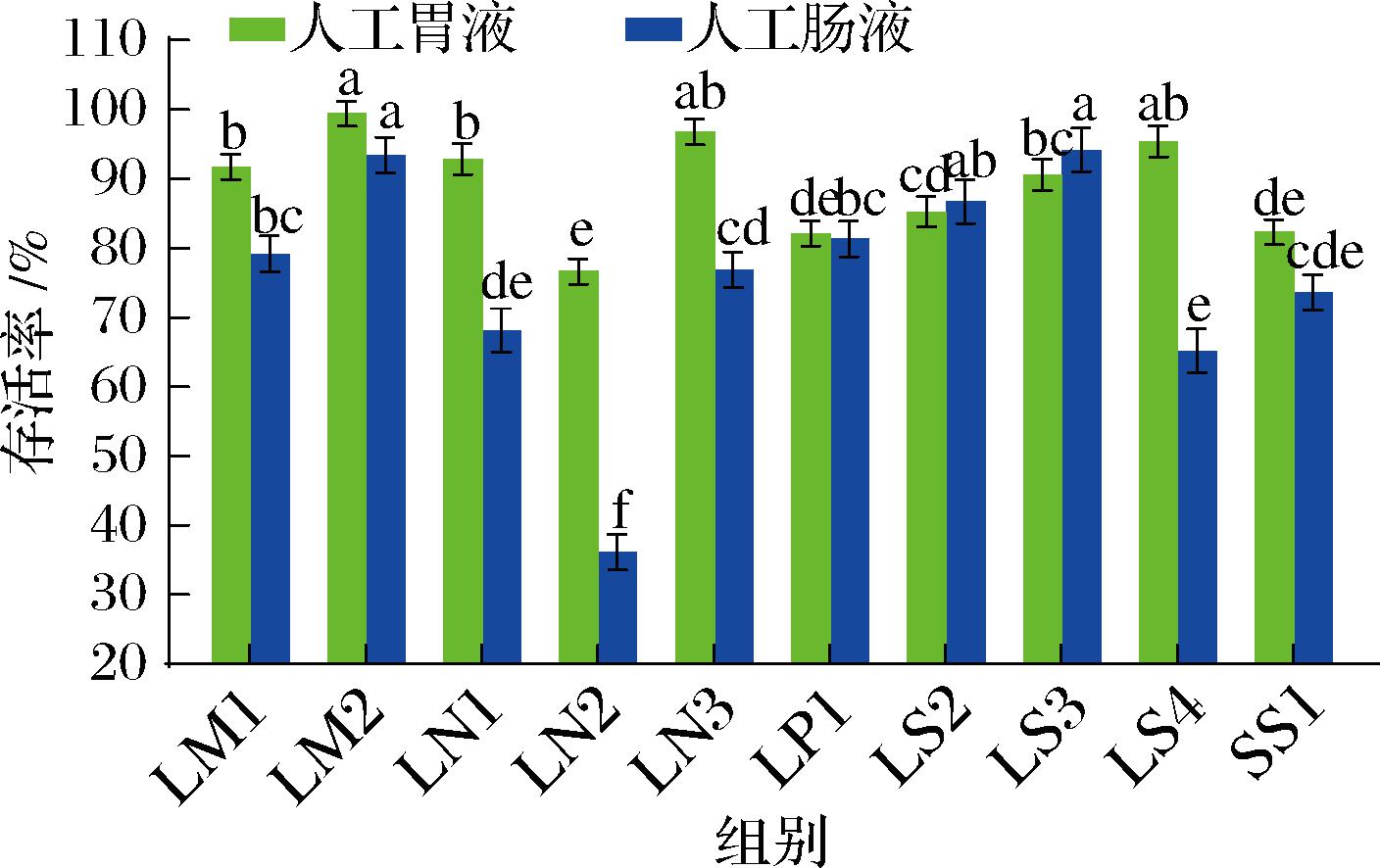
图9 10株菌株人工胃肠液耐受性
Fig.9 Tolerance of ten strains to artificial gastrointestinal fluid
2.9 菌株安全性
采用哥伦比亚血平板评估10株菌株的溶血特性。如图10所示,所有菌株培养48 h后均未出现溶血环(γ-溶血),排除了α和β溶血可能。结果表明10株菌均不产生溶血毒素,符合益生菌安全性要求,为临床应用提供了重要依据。
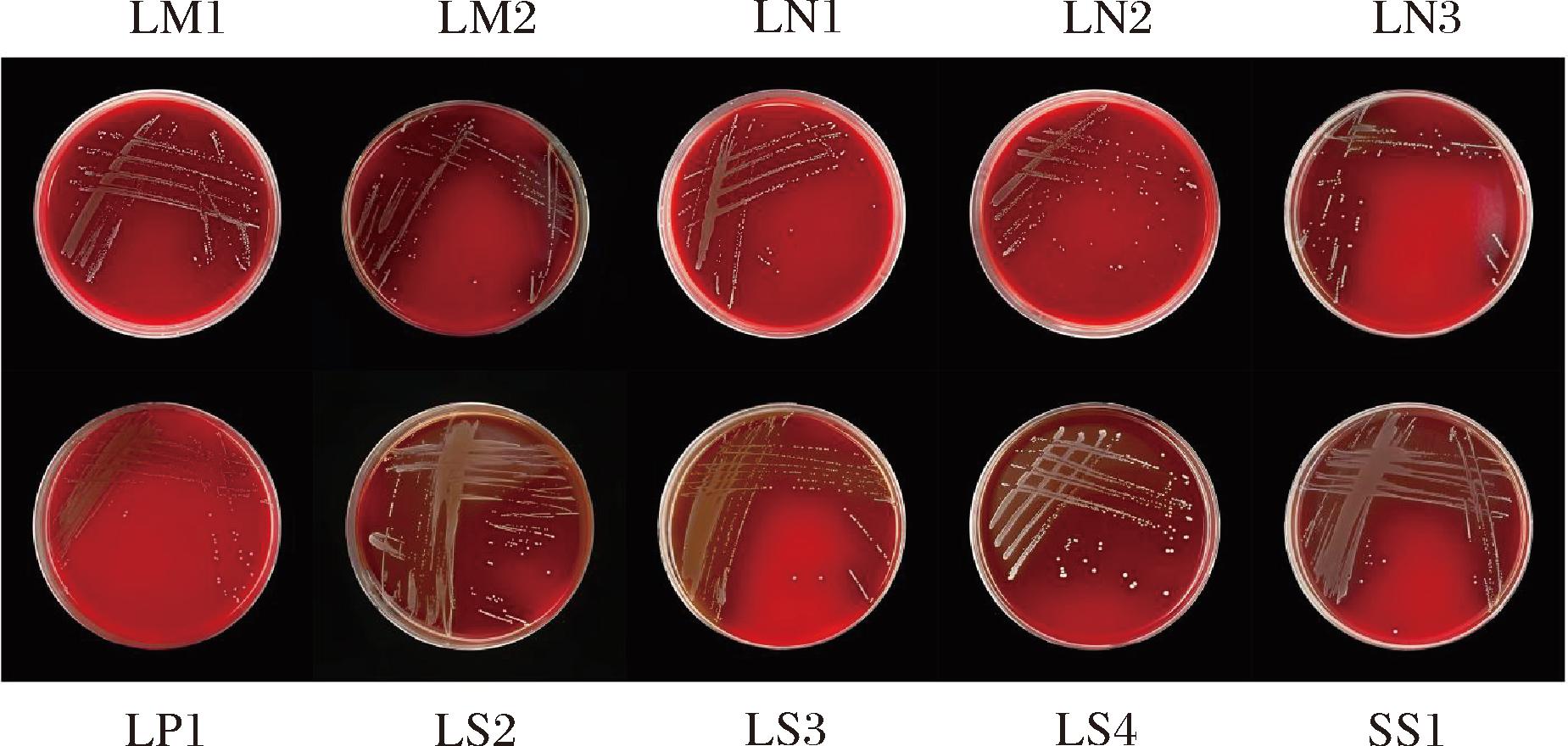
图10 10株菌株的安全性
Fig.10 Safety of ten strains
2.10 主成分分析的多变量分析
以GABA产量、亚硝酸盐降解率、耐酸性、耐胆盐性、耐人工肠胃为指标,利用主成分分析对10株乳酸菌进行综合评价。结果如图11所示,二者累计贡献率达68.46%,能有效反映数据主要特征。图中不同菌株样本在二维空间中的聚集与分离,表明其在GABA产量、亚硝酸盐降解率等指标上存在明显差异。综合评分结果显示,LS2排名第一、LM2排名第二。综合分析这2株菌株在GABA产量、亚硝酸盐降解能力等方面均表现优异,具有较高的开发潜力,适合作为功能性益生菌的候选菌株,进一步开展深入研究与应用开发。
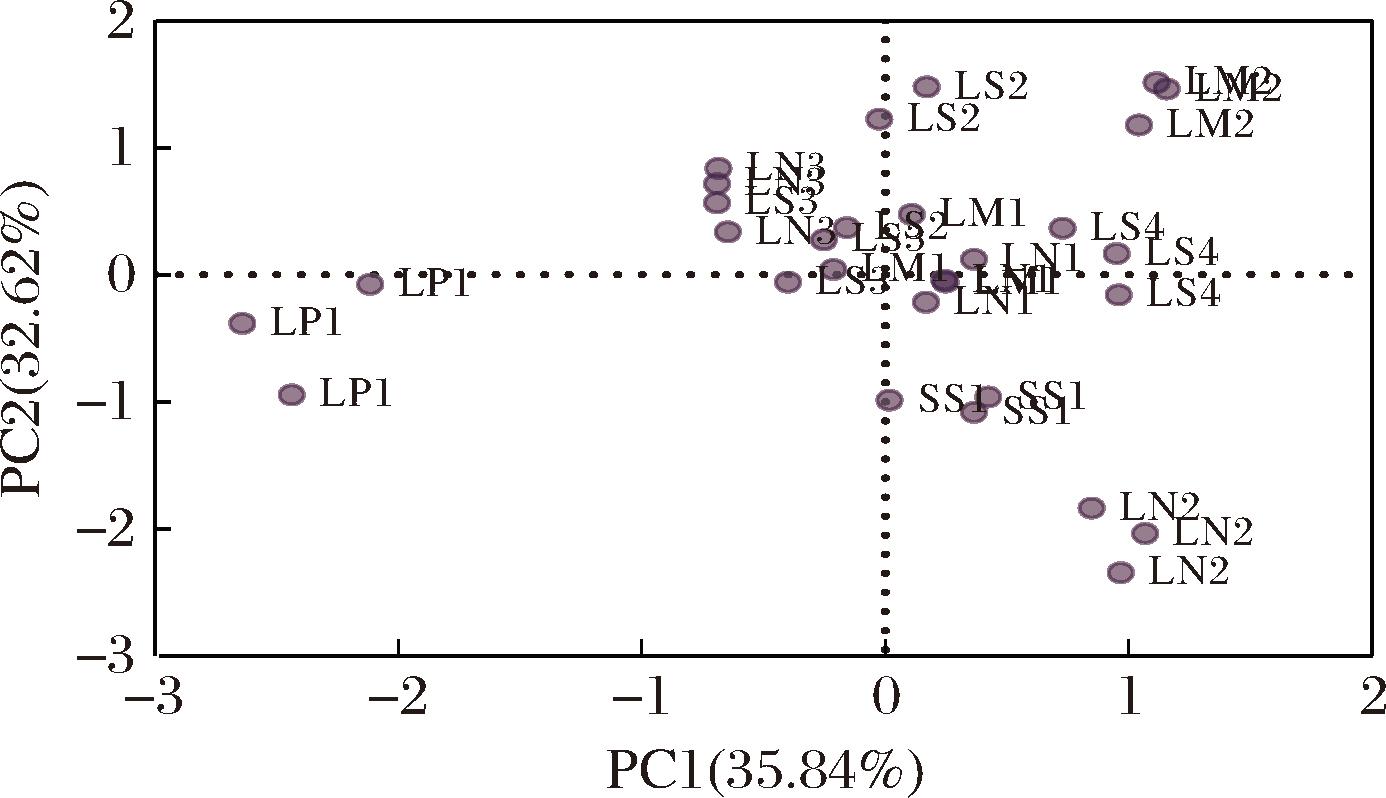
图11 10株菌株的主成分分析
Fig.11 Principal component analysis of ten strains
3 讨论与结论
本研究从自然发酵的发酵蔬菜、乳制品中分离菌株经革兰氏染色镜检、过氧化氢酶实验后,获得74株乳酸菌,从中筛选出10株产GABA、能够降解亚硝酸盐的菌株。经16S rDNA鉴定分别为L.plantarum(9株)、P.pentosaceus(1株)。发现10株菌培养24 h后亚硝酸盐降解率均在93%之上,其中SS1降解速率最快(12 h为95.70%,24 h为99.83%),LM2次之(12 h为94.15%,24 h为99.10%),LS2稍弱(12 h为47.40%,24 h为99.05%)。在GABA产量方面却是LS2产量最高(1.53 g/L),LM2第二(1.20 g/L)。陈颖等[29]从酸菜中筛出6株乳酸菌,其中布氏乳杆菌(Lactobacillus buchneri)C1菌株的发酵液GABA含量最高,为1.45 g/L。彭梦玲等[30]从自然发酵的毛竹笋中筛选的24株乳酸菌,在发酵24 h时亚硝酸盐降解率均达到80%以上,其中有11株降解率达到90%以上。有研究表明从我国新疆传统库米斯中分离获得的发酵乳杆菌RC4在含150 mg/L亚硝酸盐的MRS肉汤中培养6、10、14 h时,其亚硝酸盐降解率分别为43.8%、59.5%、82.0%,该研究还进一步探讨了其亚硝酸盐降解机制[31]。FAN等[32]通过过表达NirB基因,将Lactobacillus fermentum-NirB菌株的亚硝酸盐降解率从83.0%提高至91.7%。本研究从自然发酵的蔬菜与乳制品中分离乳酸菌株,不仅具备高降解亚硝酸盐的能力,还具有GABA生成能力,体现出菌株良好的应用潜力。
10株乳酸菌在生长能力和产酸能力方面表现各异,整体增殖能力较强。LS2在pH 2.0、pH 5.0的耐酸性最高,分别为5.83%、99.27%;LN2耐胆盐存活率最高且较为稳定,在含0.1%~0.3%胆盐的培养基中存活率分别为88.01%、83.69%、88.27%;LM2的人工胃液耐受性最好,存活率最高为99.42%;LS3、LM2人工肠液耐受性最好,存活率分别为94.18%、93.43%。经主成分分析,LS2、LM2排名前二,在GABA产量、亚硝酸盐降解能力、耐受性等方面均表现优异,具有较高的开发潜力,为开发功能性发酵蔬菜、酱菜产品提供了重要的菌株资源。后续研究可进一步探究菌株之间的协同发酵效应,优化培养发酵工艺参数,提高GABA的产量,为功能性菌剂工业化生产与应用提供理论依据与数据支撑。
[1] BARAKAT H, ALJUTAILY T.Role of γ-aminobutyric acid (GABA) as an inhibitory neurotransmitter in diabetes management:Mechanisms and therapeutic implications[J].Biomolecules, 2025, 15(3):399.
[2] 范婷婷, 王淇, 王慕瑶, 等.西藏来源的植物内生酵母Wickerhamomyces rabaulensis生产γ-氨基丁酸[J].微生物学报, 2023, 63(7):2609-2619.FAN T T, WANG Q, WANG M Y, et al.Production of γ-aminobutyric acid by the endophytic yeast Wickerhamomyces rabaulensis isolated from Tibetan plant[J].Acta Microbiologica Sinica, 2023, 63(7):2609-2619.
[3] AHN J, PARK J Y.Potential of γ-aminobutyric acid-producing Leuconostoc mesenteroides strains isolated from kimchi as a starter for high-γ-aminobutyric acid kimchi fermentation[J].Preventive Nutrition and Food Science, 2023, 28(4):492-501.
[4] 刘碧琦, 王佳悦, 解庆刚, 等.富含γ-氨基丁酸的乳粉制再制奶酪工艺优化及其降血压活性分析[J].食品工业科技, 2025,46(15):276-287.LIU B Q, WANG J Y, XIE Q G, et al.Optimization of the process for processed cheese made from milk powder rich in γ-aminobutyric acid and analysis of its antihypertensive activity[J].Science and Technology of Food Industry, 2025,46(15):276-287.
[5] TAMÉS H, SABATER C, MARGOLLES A, et al.Production of GABA in milk fermented by Bifidobacterium adolescentis strains selected on the bases of their technological and gastrointestinal performance[J].Food Research International, 2023, 171:113009.
[6] SHAKIL M H, TRISHA A T, RAHMAN M, et al.Nitrites in cured meats, health risk issues, alternatives to nitrites:A review[J].Foods, 2022, 11(21):3355.
[7] SROUR B, CHAZELAS E, FEZEU L K, et al.Nitrites, nitrates, and cardiovascular outcomes:Are we living “La vie en rose” with pink processed meats?[J].Journal of the American Heart Association, 2022, 11(24):e027627.
[8] 刘笑笑, 金永梅, 吴迪, 等.传统发酵樱菜中降解亚硝酸盐肠膜明串珠菌的分离鉴定及特性分析[J].中国酿造, 2020, 39(6):58-62.LIU X X, JIN Y M, WU D, et al.Isolation, identification and characteristic of Leuconostoc mesenteroides with nitrite degradation capacity from traditional fermented Lepidium sativum[J].China Brewing, 2020, 39(6):58-62.
[9] 熊玉帛, 赵野, 曾瑶英, 等.华容芥菜降亚硝酸盐乳酸菌的筛选鉴定及发酵特性研究[J].中国酿造, 2024, 43(8):122-127.XIONG Y B, ZHAO Y, ZENG Y Y, et al.Screening,identification and fermentation characteristics of nitrite degradation lactic acid bacteria from Huarong mustard[J].China Brewing, 2024, 43(8):122-127.
[10] 赵海霞, 吴丹, 王晓蕾, 等.降解亚硝酸盐乳酸菌的筛选及其在菜用枸杞浆水发酵中的应用[J].中国酿造, 2022, 41(11):113-119.ZHAO H X, WU D, WANG X L, et al.Screening of high nitrite-degrading lactic acid bacteria strains and their application in Jiangshui with Lycium barbarum fermentation[J].China Brewing, 2022, 41(11):113-119.
[11] 肖秋颖, 陈炼红, 王琳琳, 等.川西高原发酵牦牛乳中降解亚硝酸盐乳酸菌的筛选与耐受性研究[J].食品工业科技, 2020, 41(9):119-123;130.XIAO Q Y, CHEN L H, WANG L L, et al.Screening and tolerance of degrading nitrite-lactant bacteria in fermented yak milk of western Sichuan Plateau[J].Science and Technology of Food Industry, 2020, 41(9):119-123;130.
[12] 赵强, 谷云静, 程伟烨, 等.一株降解亚硝酸盐的乳酸乳球菌对辣白菜风味品质的影响[J].中国调味品, 2024, 49(12):42-52.ZHAO Q, GU Y J, CHENG W Y, et al.Effect of a nitrite-degrading Lactococcus lactis strain on flavor and quality of kimchi[J].China Condiment, 2024, 49(12):42-52.
[13] 熊蝶, 袁岚玉, 李媛媛, 等.陕西泡菜中降解亚硝酸盐乳酸菌的筛选及其发酵特性与耐受性研究[J].食品与发酵工业, 2021, 47(6):139-144.XIONG D, YUAN L Y, LI Y Y, et al.Screening, fermentation characteristics and tolerance of nitrite-degrading lactic acid bacteria in Shaanxi Paocai[J].Food and Fermentation Industries, 2021, 47(6):139-144.
[14] 刘璐, 吴江丽, 杨金桃, 等.发酵鱼酱酸产GABA乳酸菌的分离筛选及发酵特性[J].食品科学, 2021, 42(18):73-79.LIU L, WU J L, YANG J T, et al.Isolation and fermentation characteristics of γ-aminobutyric acid-producing lactic acid bacteria from Yujiangsuan, a traditional Miao ethnic fermented condiment[J].Food Science, 2021, 42(18):73-79.
[15] 张戴, 朱力, 赵玲艳, 等.乳酸菌的筛选、鉴定及多菌系复合发酵藠头[J].中国酿造, 2025, 44(4):71-79.ZHANG D, ZHU L, ZHAO L Y, et al.Screening and identification of lactic acid bacteria and Allium chinense fermentation by multi-bacterial system[J].China Brewing, 2025, 44(4):71-79.
[16] 胡此海, 杨絮, 郭全友, 等. 萝卜泡菜母水中乳酸菌分离鉴定与发酵特性比较[J]. 食品与发酵工业, 2023, 49(23): 111-119.HU C H, YANG X, GUO Q Y, et al. Isolation, identification, and fermentation characteristics of lactic acid bacteria from the radish pickles brines[J]. Journal of Chinese Institute of Food Science and Technology, 2023, 49(23): 111-119.
[17] 黎蓓蓓, 冯书珍, 李德军, 等.果菜类蔬菜混合发酵菌种筛选及其发酵特性研究[J].食品与发酵工业, 2025, 51(1):158-166.LI B B, FENG S Z, LI D J, et al..Screening of mixed fermentation strains of fruits and vegetables and research on their fermentation characteristics[J].Food and Fermentation Industries, 2025, 51(1):158-166.
[18] 姚有莉, 张朋, 王永奔, 等.降解霉菌毒素乳酸菌的筛选及鉴定[J].动物营养学报, 2024(4):2674-2689.YAO Y L, ZHANG P, WANG Y B, et al.Screening and identification of mycotoxin-degrading lactic acid bacteria[J].Chinese Journal of Animal Nutrition, 2024(4):2674-2689.
[19] 汤凯, 武运, 王雪, 等.伊犁地区奶疙瘩中乳酸菌的筛选及其特性研究[J].食品工业科技, 2025, 46(3):188-195.TANG K, WU Y, WANG X, et al.Screening and characteristics of lactic acid bacteria from cheese in Yili area[J].Science and Technology of Food Industry, 2025, 46(3):188-195.
[20] 孙晓琛, 张晓千, 李玲玉, 等.降血脂功能乳酸菌的体外筛选、驯化及鉴定[J].食品工业科技, 2024, 45(24):125-132.SUN X C, ZHANG X Q, LI L Y, et al. In vitro screening, domestication and identification of lipid-lowering functional lactic acid bacteria[J].Science and Technology of Food Industry, 2024, 45(24):125-132.
[21] 武芷伊, 魏玥, 李瑜, 等. 云南香格里拉地区牦牛乳中乳酸菌的分离及耐盐菌株筛选[J]. 食品与发酵工业, 2025, 51(20):291-298.WU Z Y, WEI Y, LI Y, et al. Isolation and screening of salt-tolerant strains of lactic acid bacteria from yak milk in Shangri-La, Yunnan Province[J]. Food and Fermentation Industries, 2025, 51(20):291-298.
[22] 郭志华, 张兴桃, 段腾飞, 等.泡菜中降解亚硝酸盐乳酸菌的筛选及生物学特性研究[J].食品与发酵工业, 2019, 45(17):66-72.GUO Z H, ZHANG X T, DUAN T F, et al.Screening and biological characterization of nitrite degrading lactic acid bacteria in kimchi[J].Food and Fermentation Industries, 2019, 45(17):66-72.
[23] 李卉, 李莉.食品中亚硝酸盐检测方法的研究进展[J].食品工业科技, 2022, 43(23):429-435.LI H, LI L.Research progress on the determination of nitrite in food[J].Science and Technology of Food Industry, 2022, 43(23):429-435.
[24] 徐云凤, 张欣, 褚泽军, 等.一株具有高效抑菌活性乳酸菌的分离鉴定及生长特性研究[J].食品与机械, 2021, 37(3):12-14, 21.XU Y F, ZHANG X, CHU Z J, et al.Isolation,identification and growth characteristics of a strain of lactic acid bacteria with efficient antimicrobial activity[J].Food and Machinery, 2021, 37(3):12-14, 21.
[25] 龚福明, 何彩梅, 吴桂容, 等.乳酸菌降解发酵蔬菜中亚硝酸盐的研究现状[J].中国调味品, 2022, 47(10):201-205.GONG F M, HE C M, WU G R, et al.Research status of nitrite degradation in fermented vegetables by lactic acid bacteria[J].China Condiment, 2022, 47(10):201-205.
[26] 洪青平, 邸子清, 孙大庆, 等. 耐胆汁酸戊糖片球菌32M07筛选、基因组测序及其胆汁酸耐受机制的解析[J]. 食品工业科技, 2025, 46(17):213-223.HONG Q P, DI Z Q, SUN D Q, et al. Screening, genome sequencing and tolerance mechanism analysis of bile acid-resistant Pediococcus pentosaceus 32M07[J]. Science and Technology of Food Industry, 2025, 46(17):213-223.
[27] 朱宗涛, 屈婉, 刘松玲, 等.高产γ-氨基丁酸的双歧杆菌的筛选及对抑郁细胞模型的改善作用[J].食品工业科技, 2020, 41(5):130-135.ZHU Z T, QU W, LIU S L, et al.Screening of bifidobacterium strains with high yield of γ-aminobutyric acid and its improvement in depressive cell[J].Science and Technology of Food Industry, 2020, 41(5):130-135.
[28] 陈春霏. 基于比较基因组的乳杆菌耐胆盐功能基因挖掘[D].无锡:江南大学, 2023.CHEN C F.Identification of bile salt-tolerant genes in Lactobacillus using comparative genomics[D].Wuxi:Jiangnan University, 2023.
[29] 陈颖, 杨炫康, 王陈晨, 等. 高产γ-氨基丁酸乳酸菌的筛选及益生特性研究[J]. 食品与发酵工业, 2025, 51(17):40-46.CHEN Y, YANG X K, WANG C C, et al. Research on screening and probiotic characteristics of lactic acid bacteria with high yield of γ-aminobutyric acid[J]. Food and Fermentation Industries, 2025, 51(17):40-46.
[30] 彭梦灵, 朱倩, 杨松, 等. 降解亚硝酸盐乳酸菌的筛选及其生物特性研究[J]. 中国食品学报, 2025, 25(5):134-145.PENG M L, ZHU Q, YANG S, et al. Screening and biological characteristics of nitrite-degrading lactic acid bacteria[J]. Journal of Chinese Institute of Food Science and Technology, 2025, 25(5):134-145.
[31] ZENG X Q, PAN Q, GUO Y X, et al.Potential mechanism of nitrite degradation by Lactobacillus fermentum RC4 based on proteomic analysis[J].Journal of Proteomics, 2019, 194:70-78.
[32] FAN Q, XIA C R, ZENG X Q, et al.Effect and potential mechanism of nitrite reductase B on nitrite degradation by Limosilactobacillus fermentum RC4[J].Current Research in Food Science, 2024, 8:100749.