细菌性阴道病(bacterial vaginosis,BV)是育龄女性中最常报告的微生物综合征,其特征在于阴道菌群从以乳酸杆菌为主转变为乳酸杆菌数量急剧减少,兼性厌氧菌和严格厌氧菌大量存在的状态[1]。流行病学研究结果显示,BV与一系列健康问题有关,包括早产、性传播感染(sexually transmitted infections,STIs)、人类免疫缺陷病毒的感染与传播以及其他慢性健康问题。BV的主要症状是出现灰白色稀薄均匀的分泌物,并伴有难闻气味或“鱼腥味”, 以及阴道区域有灼烧感和不适感,影响被感染女性的生活质量[2-3]。
阴道加德纳菌是细菌性阴道感染的主要病原体,通过产生唾液酸酶、脯氨酸酶和腐胺,在降解黏蛋白等黏膜保护因子方面发挥作用,并可能导致阴道上皮细胞脱落,降低阴道上皮屏障防御功能[4]。还可通过黏附素类似物紧密黏附于人体组织,并分泌阴道溶素等细胞溶素毒素,破坏上皮细胞和红细胞以获取营养,同时激活局部炎症反应,产生多种细胞因子,如IL-1α、IL-1β和TNF-α等。此外,该菌能形成生物膜,为其他致病菌定植创造条件,共同破坏阴道微生态平衡,引发细菌性阴道病[2,5-6]。
抗生素治疗(口服甲硝唑)是临床研究中用于治疗BV的标准疗法[7]。然而,抗生素治疗常常面临高失败率和高复发率的问题。这可能是由于其消除了阴道中的共生生物,从而增加病原体侵染的优势[8]。益生菌是一类活的微生物,当以足够数量摄入时,能够通过恢复微生物和宿主免疫稳态而赋予宿主健康益处。乳酸杆菌和双歧杆菌是最常用于治疗阴道健康的益生菌种类[9]。为促进阴道健康而研究的口服和阴道用益生菌包括嗜酸乳杆菌(Lactobacillus acidophilus)、鼠李糖乳酪杆菌(Lacticaseibacillus rhamnosus)、罗伊氏粘液乳杆菌(Limosilactobacillus reuteri)、植物乳植杆菌(Lactiplantibacillus plantarum)、格氏乳杆菌(L.gasseri)和卷曲乳杆菌(L.crispatus)[10]。它们通常通过分泌代谢物抑制病原菌黏附、生长、增殖以及菌丝向生物膜形成等机制,保护宿主免受病原菌感染[11]。HOUTTU等[12]的研究发现,口服益生菌可以降低阴道菌群中潜在致病菌的丰度,尤其是Sneathia、普氏菌等的丰度。LI等[3]的研究发现卷曲乳杆菌、鼠李糖乳酪杆菌、唾液联合乳杆菌和植物乳植杆菌制备成的联合菌群和健康小鼠阴道菌群移植可以改善BV的临床症状并恢复健康的阴道微生物群。
研究发现,乳杆菌后生元(postbiotics)也具有益生作用。YIN等[13]的研究发现,热灭活约氏乳杆菌作为后生元能激活肠道先天免疫,通过肠-肝轴途径,在小鼠模型中改善酒精相关肝病(alcohol-associated liver disease,ALD)。国际益生菌与益生元科学协会将后生元定义为“一种无生命微生物和/或其成分的制剂,能给宿主带来健康益处”。有效的后生元必须包含失活的微生物细胞或细胞成分,可有可无代谢物[14]。SHEN等[15]的临床研究发现,益生菌制备的后生元凝胶可改善BV的临床症状。然而,目前关于乳杆菌后生元在缓解阴道感染方面的研究较少,仍需进一步探索。因此,开发具有调节阴道上皮屏障作用的菌株及其后生元对于预防阴道感染具有重要意义。
本研究通过建立脂多糖(lipopolysaccharide,LPS)诱导的阴道上皮细胞模型探究在体外条件下德氏乳杆菌CCFM1337菌体裂解物对阴道上皮屏障的改善作用。随后通过建立阴道加德纳菌诱导的细菌性阴道炎模型评估德氏乳杆菌CCFM1337活菌及其热灭活菌体外用干预能否有效改善小鼠阴道上皮屏障完整性,从而缓解BV,希望为阴道健康的破坏提供解决方案,也为阴道感染患者的治疗提供辅助支持,促进益生菌功能产品的开发与应用。
1 材料与方法
1.1 材料与试剂
1.1.1 供试菌株、细胞
德氏乳杆菌CCFM1337和卷曲乳杆菌FHNXY73M2来自江南大学食品微生物菌种保藏中心(Culture Collection of Food Microbiology,CCFM)。德氏乳杆菌DM8909分离自定君生阴道用乳杆菌活菌胶囊,作为阳性对照。阴道加德纳菌(ATCC 14018),购买于广东省微生物研究所菌种保藏中心。人阴道上皮细胞VK2/E6E7由江苏省无锡市人民医院妇产科惠赠。
1.1.2 菌株、细胞制备
乳杆菌及阴道加德纳菌菌悬液的制备参考LI等[3]描述的方法。乳杆菌接种至MRS液体培养基中培养至对数生长期,收集菌体沉淀并使用PBS清洗3次后调节浓度为1×109 CFU/mL。死菌菌悬液浓度与制备方法与活菌相同,采用105 ℃、10 min 高压蒸汽灭活,通过平板涂布检查灭活效果。将收集的菌体沉淀使用MRS液体培养基调节浓度为1×109 CFU/mL,高压均质机中均质(800~1 200 MPa)10次后,用0.22 μm滤膜过滤,即获得乳杆菌菌体裂解液。阴道加德纳菌在脑心浸出液培养基中培养至对数生长期,收集菌体沉淀并用无菌PBS调整浓度至1×1010 CFU/mL,后续用于动物实验造模。冻存的VK2/E6E7细胞在37 ℃水浴锅中快速融化,低速离心之后弃去细胞冻存液,用细胞完全培养基重悬并接种于细胞培养皿中,于5%(体积分数)CO2,37 ℃培养箱中培养。当细胞贴壁融合率达到85%~90%之后,进行传代及后续的实验操作。
1.1.3 试剂
胎牛血清、DMEM 培养基、胰酶,美国Gibco公司;青霉素、链霉素,上海博光生物公司;Trizol,上海赛默飞世尔科技公司;LPS(L4391),美国Sigma公司;反转录试剂盒、qPCR 荧光定量试剂盒,南京诺唯赞生物科技股份有限公司;实时荧光定量 PCR引物,生工生物工程(上海)股份有限公司;小鼠ZO-1、OCLN、CLDN1、sECAD、sIgA、IgG 和HBD-2试剂盒,南京森贝伽生物科技有限公司。
1.2 仪器与设备
SW-CJ-1 CV微生物操作超净工作台、BSC-1004IIA2 生物安全柜,安泰空气技术有限公司;MLS-3750高温高压灭菌锅,日本 SANYO 公司;高速冷冻离心机,德国 Eppendorf;Multiscan Go全波长酶标仪,美国Thermo 公司;高通量组织研磨机,宁波新芝生物科技股份有限公司;切片电子扫描仪,匈牙利3DHISTECH 公司;PCR仪、实时荧光定量PCR仪,美国Bio-Rad公司。
1.3 实验方法
1.3.1 VK2/E6E7细胞屏障相关基因表达的测定
按照每孔2×105个细胞的密度将细胞接种在12孔细胞培养板中,培养24 h后加入含LPS(25 μg/mL)的1 mL无血清细胞培养基刺激细胞24 h,之后用预热至37 ℃的PBS清洗细胞3次,然后加入含有5%(体积分数)的不同乳杆菌的菌体裂解液(干预组)或5% (体积分数)MRS的细胞完全培养基(对照组)与细胞共孵育24 h,干预24 h之后弃去培养上清液,收集细胞,加入Trizol 反复吹打裂解细胞以提取总RNA,之后按照试剂盒说明书进行逆转录,并以逆转录之后的cDNA为模板进行荧光实时定量评估VK2/E6E7细胞中基因的表达情况[16]。最后采用2-ΔΔCt法处理数据,计算细胞基因的相对表达量。荧光定量基因扩增引物序列如表1所示。
表1 细胞实验荧光定量基因扩增引物序列
Table 1 Primers’ sequences used in cell experiments
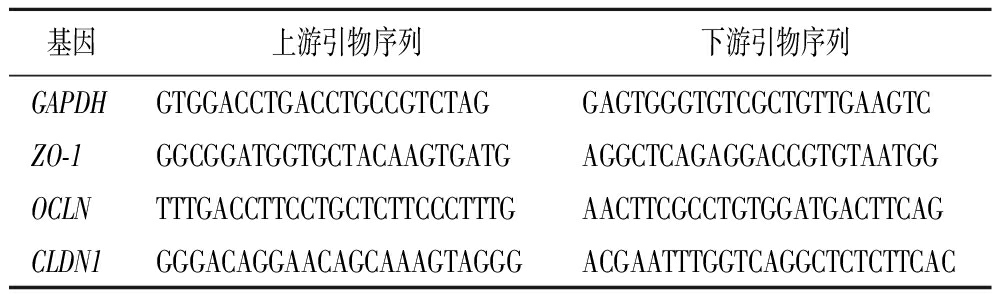
基因上游引物序列下游引物序列GAPDHGTGGACCTGACCTGCCGTCTAGGAGTGGGTGTCGCTGTTGAAGTCZO-1GGCGGATGGTGCTACAAGTGATGAGGCTCAGAGGACCGTGTAATGGOCLNTTTGACCTTCCTGCTCTTCCCTTTGAACTTCGCCTGTGGATGACTTCAGCLDN1GGGACAGGAACAGCAAAGTAGGGACGAATTTGGTCAGGCTCTCTTCAC
1.3.2 动物实验
SPF级BALB/c小鼠,雌性,7周龄,体重18~20 g,购于北京维通利华实验动物技术有限公司(生产许可证号SCXK(京)2012-0001)。小鼠放置于20~22 ℃,湿度(50±10)%,光照/黑暗周期为12 h的交替循环环境中。7 d适应期后,40只小鼠随机分为空白对照组、模型组、甲硝唑干预组、DM8909活菌组(DM8909-L)、DM8909灭活菌体组(DM8909-D)、CCFM1337活菌组(CCFM1337-L)、CCFM1337灭活菌体组(CCFM1337-D)、FHNXY73M2活菌组(FHNXY73M2-L)。参考ZHANG等[17]的方法,除空白对照组外,其余小鼠均连续3 d(第1~3天)颈部皮下注射100 μL戊酸雌二醇溶液(5 mg/mL芝麻油)诱导发情。随后连续5 d(第4~8天),用枪头吸取20 μL浓度为1010 CFU/mL的阴道加德纳菌悬液,缓缓注入小鼠阴道内,并将小鼠倒立,停留1~2 min,以防止菌液流出。在第9~19天,实验组分别用枪头吸收相应菌悬液20 μL缓缓注入小鼠阴道内,将小鼠倒立,停留1~2 min,放入笼中。甲硝唑干预方式为将1.62 mg/20 g小鼠体重的甲硝唑溶解于PBS中用枪头吸取20 μL缓缓注入小鼠阴道内。对照组和模型组注射等体积PBS。实验结束后(第20天),处死实验小鼠并剥离阴道组织用于病理学分析,以及各项指标的检测等。实验流程如图1所示。

图1 动物实验流程图
Fig.1 Flow chart of animal experiments
该研究遵循的程序符合江苏省寄生虫病研究所实验动物护理和使用委员会所制订的伦理学标准,并得到批准(IACUC-JIPD-2023111)。所有实验均按照江苏省寄生虫病研究所实验动物护理和使用指南进行。
1.3.3 阴道组织中蛋白表达水平测定
取20 mg小鼠阴道组织,加入180 μL预冷的PBS溶液对阴道组织进行匀浆处理。在4 ℃下,以3 000 r/min对样品离心15 min,取阴道组织上清液按试剂盒说明书进行小鼠ZO-1、OCLN、Claudin-1、sECAD、sIgA、IgG、HBD-2 浓度测定。
1.3.4 阴道组织病理学观察
剥离小鼠阴道组织,取2~3 mm的片段完全浸泡在质量浓度为40 g/L的中性多聚甲醛固定液中进行保存与固定。之后参照KWAK等[18]的方法,经脱水、包埋和切片后,用苏木精和伊红(hematoxylin eosin stain,HE)染色。切片标本使用切片电子扫描仪,放大20倍进行观察。
1.4 数据统计与分析
数据分析和绘图采用SPSS 23.0 和GraphPad Prism 9.0软件进行。单因素方差分析用于分析组间差异,数据以“平均数±标准差”表示。P<0.05认为有统计学意义。
2 结果与讨论
2.1 德氏乳杆菌CCFM1337对VK2/E6E7细胞屏障相关基因表达的影响
宫颈阴道上皮机械屏障主要由上皮细胞与相邻细胞间的紧密连接构成,而紧密连接由一系列跨膜蛋白组成,如封闭蛋白、紧密蛋白和细胞连接黏附分子,这些蛋白质通过ZO(zonula occludens)蛋白与细胞骨架相连,是维持机械屏障的结构基础,并调控着水和溶质等小分子物质的跨上皮转运,是决定屏障完整性、通透性的关键因素[19]。DELGADO-DIAZ等[20]在人群实验中发现乳酸可以增强阴道上皮细胞培养的屏障完整性并增加细胞间连接分子的表达,从而促进上皮屏障蛋白含量的增加。首先在细胞水平上测定德氏乳杆菌CCFM1337对阴道上皮屏障的影响,选取ZO-1、OCLN、CLDN1 mRNA作为紧密连接蛋白的代表性指标。如图2所示, LPS的处理使ZO-1、OCLN、CLDN1 mRNA的表达显著下降。德氏乳杆菌CCFM1337处理使ZO-1、OCLN和CLDN1 mRNA 的表达显著提升,与模型组相比,分别提高了212.02%(P<0.000 1)、176.17%(P<0.000 1)和223.60%(P<0.000 1),效果优于DM8909处理组。卷曲乳杆菌FHNXY73M2处理组在ZO-1、OCLN、CLDN1 mRNA 的表达上无调节效果,在后续的动物实验中作为阴性对照。
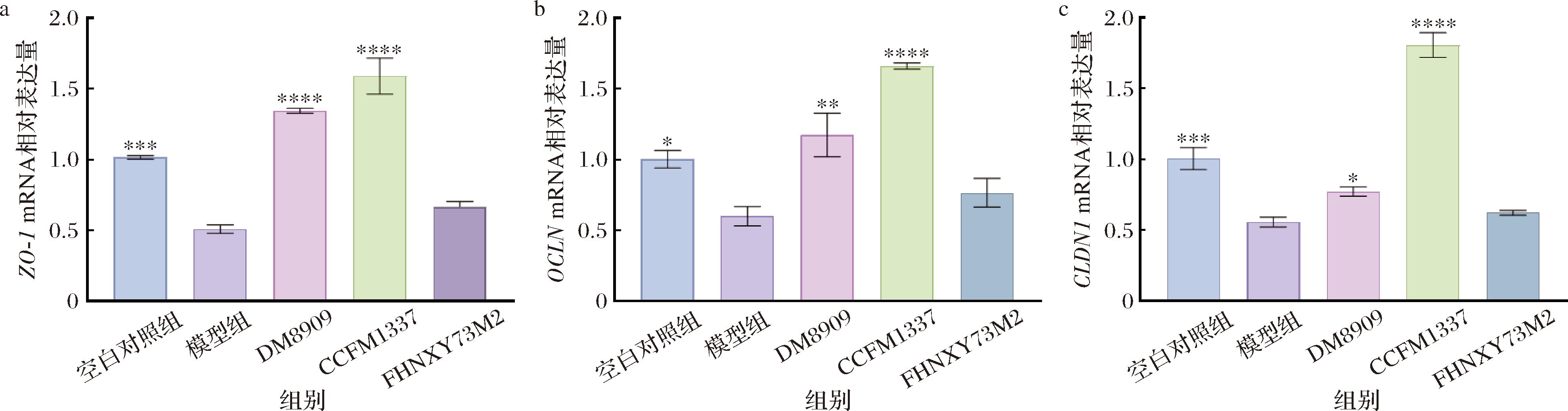
a-ZO-1 mRNA相对表达量;b-OCLN mRNA相对表达量;c-CLDN1 mRNA相对表达量
图2 乳杆菌对VK2/E6E7细胞紧密连接蛋白基因表达的影响
Fig.2 Effect of Lactobacillus on tight junction protein gene expression in VK2/E6E7 cells
注:与模型组相比,*,P<0.05,**,P<0.01,***,P<0.001,****,P<0.000 1(下同)。
2.2 小鼠阴道组织病理学分析
通过HE染色探究阴道加德纳菌造模之后,乳杆菌和甲硝唑干预对小鼠阴道组织的影响。由图3可知,空白对照组小鼠阴道黏膜结构完整,表层有一定量的角化层,模型组小鼠阴道黏膜表面角化层消失,鳞状上皮细胞有增生,黏膜内有大量炎症细胞浸润;经德氏乳杆菌DM8909活菌组和死菌组、德氏乳杆菌CCFM1337活菌组和死菌组干预后,上皮层逐渐修复,炎症浸润显著减少,黏膜表面出现一定量的角化层。卷曲乳杆菌FHNXY73M2对阴道受损屏障恢复能力较弱,较模型组相比,炎症细胞不同程度地浸润于黏膜上皮层中,黏膜固有层结构较为松散且伴有炎症细胞浸润。说明德氏乳杆菌CCFM1337可以有效促进小鼠阴道黏膜的恢复,减轻小鼠阴道组织的炎症症状,改善小鼠受损阴道结构。
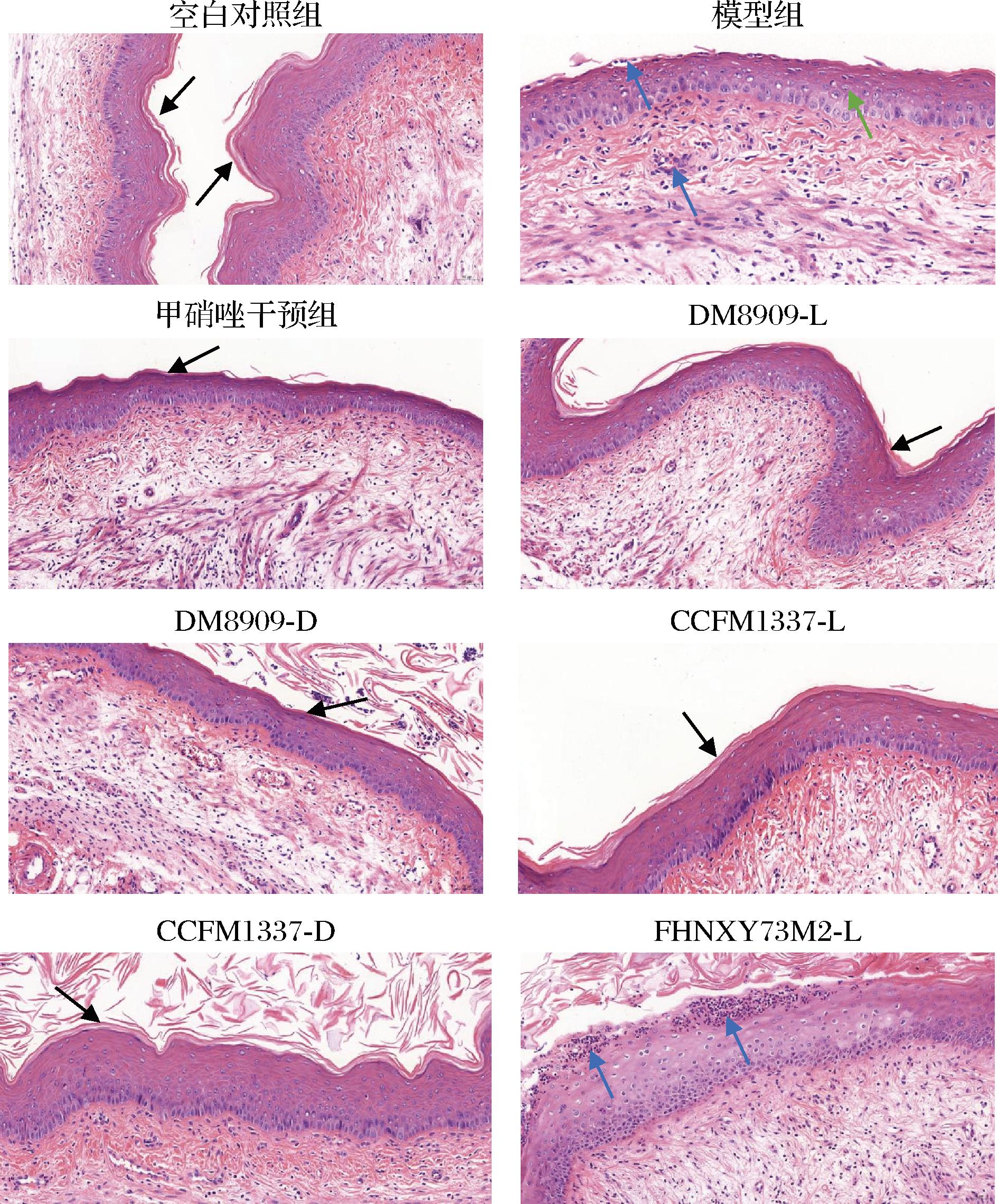
图3 乳杆菌对小鼠阴道组织的病理学影响
Fig.3 Pathological effects of Lactobacillus on vaginal tissue in mice
注:黑色箭头,阴道上皮角化层;蓝色箭头,炎性细胞浸润;绿色箭头:鳞状上皮细胞增生。
2.3 德氏乳杆菌CCFM1337对小鼠阴道上皮机械屏障的影响
E-钙粘蛋白主要在上皮细胞膜上表达,是一种跨膜、依赖钙的细胞黏附蛋白,可调节细胞间黏附并维持上皮组织的结构和功能完整性。E-钙粘蛋白表达降低会破坏细胞间接触,从而使细胞发生迁移,是屏障破坏的标志物[21-22]。如图4所示,与空白对照组相比,阴道加德纳菌干预的造模组可溶性E-钙粘蛋白(soluble epithelial cadherin,sECAD)的含量显著上升(P<0.001),为102.4 pg/mL,说明阴道加德纳菌对阴道上皮屏障造成了损伤。甲硝唑的干预并没有显著下降sECAD的分泌。不同乳杆菌处理干预后sECAD的水平均呈现了一定程度的下降。与模型组相比,德氏乳杆菌DM8909活菌和死菌菌体干预使sECAD的水平分别降低了22.93%(P<0.001)和16.57%(P<0.05),德氏乳杆菌CCFM1337活菌和死菌菌体干预使sECAD的水平分别降低了18.53%(P<0.01)和14.43%(P<0.05),乳杆菌灭活菌体对sECAD的水平也具有显著的调节作用,但是效果不如活菌处理。推测活菌可在阴道黏膜定植,定植使活菌能与宿主细胞建立更紧密、持久的联系,并持续分泌多种活性物质,提供更强效、更动态的屏障保护。研究表明,源自鼠李糖乳酪杆菌GG的分泌蛋白Msp1/p75和Msp1/p40可增强上皮屏障功能[23]。双歧杆菌属释放的的胞外多糖,可以通过尚未明确的信号传导机制减轻炎症,从而促进屏障功能[24]。乳杆菌灭活菌体仅能在阴道短暂存留,对sECAD水平的调节可能依赖于其菌体结构成分被宿主模式识别受体识别后,启动的免疫调节作用。WANG等[25]的研究发现,副干酪乳酪杆菌D3-5的胞壁成分脂磷壁酸(lipoteichoic acid,LTA),可通过调节TLR-2/p38 MAPK/NF-kB途径,促进杯状细胞表达Muc2,从而修复肠道屏障和缓解炎症。
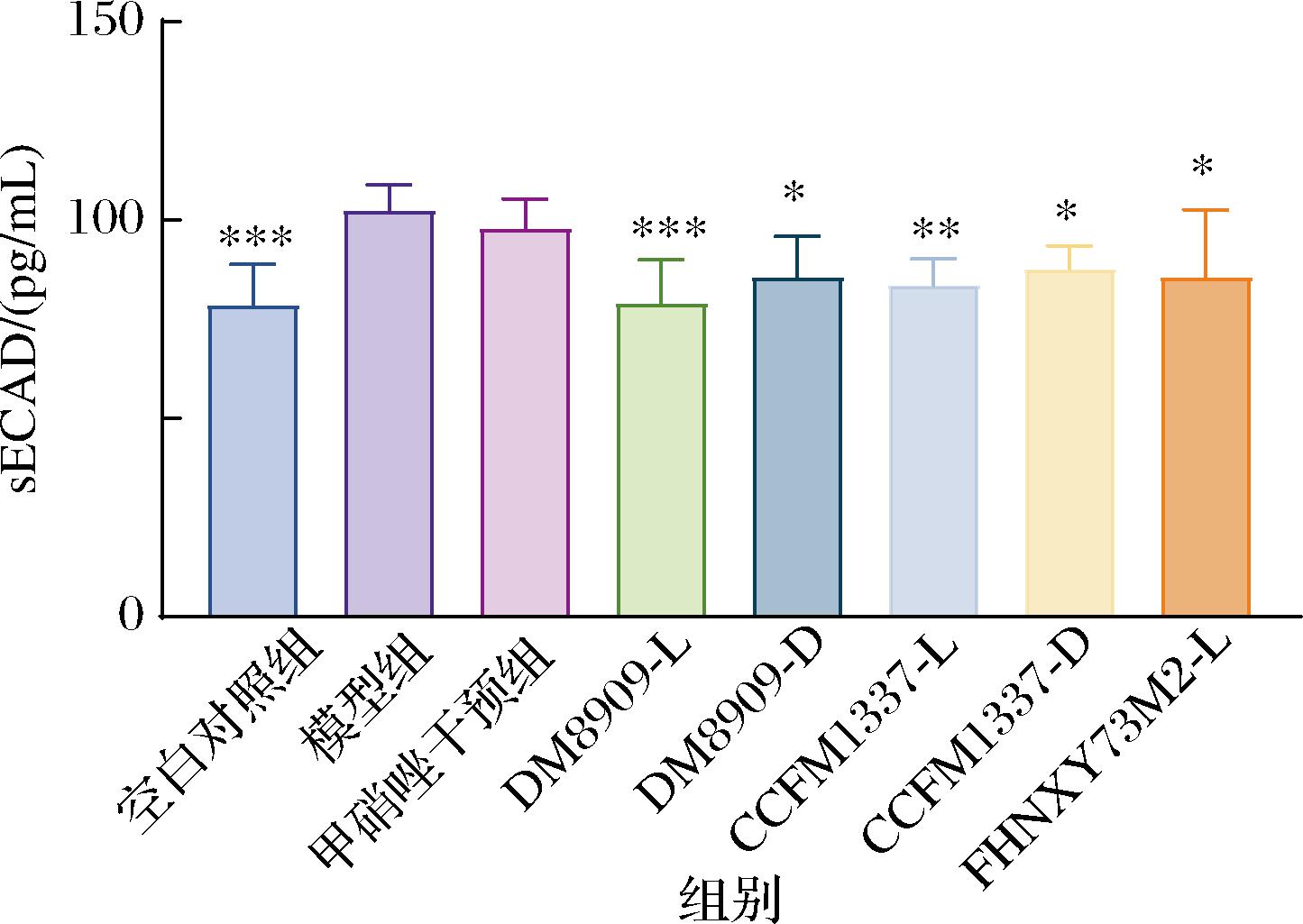
图4 乳杆菌对小鼠阴道sECAD水平的影响
Fig.4 Effect of Lactobacillus on vaginal sECAD level in mice
紧密连接(tight junctions,TJs)蛋白是上皮细胞和内皮细胞最顶端的复合物,主要由闭合蛋白、咬合蛋白、周质蛋白家族(ZO蛋白)和连接黏附分子组成,在维持正常上皮细胞间黏附以及加强细胞间机械连接方面发挥着重要作用。当紧密连接蛋白减少时,屏障功能丧失[26-27]。图5展示了阴道组织中ZO-1、CLDN1和OCLN蛋白的表达情况。结果表明,与空白对照组相比,模型组小鼠紧密连接蛋白的表达明显降低。CCFM1337-L和CCFM1337-D组ZO-1、CLDN1和OCLN蛋白的表达得到了显著的提高,且总体提升水平优于甲硝唑、DM8909-L、DM8909-D和FHNXY73M2-L干预组。这与ANTON等[28]的研究具有一致性,研究表明乳杆菌能够提高紧密连接的表达,具有增强上皮屏障的能力。甲硝唑组对ZO-1、CLDN1和OCLN蛋白的表达也有一定的提升作用,推测可能由于其对致病菌的抑制作用,从而导致损伤上皮屏障的有害因子减少,机体进行了部分恢复。

a-ZO-1蛋白水平;b-OCLN蛋白水平;c-CLDN1蛋白水平
图5 乳杆菌对小鼠阴道上皮屏障中紧密连接蛋白表达的影响
Fig.5 Effect of Lactobacillus on the expression of tight junction protein in the vaginal epithelial barrier of mice
黏蛋白(mucoprotein,MUC)是黏液的主要结构蛋白,为一些细菌提供附着位点和营养来源。黏液和MUC在保护黏膜表面、防止上皮接触以及通过捕获清除入侵者方面发挥着作用。当机体处于平衡的状态下,MUC的分泌处于正常水平,当有致病菌进行侵袭时,MUC的分泌显著增加[29]。临床研究表明, BV女性体内的 MUC1、MUC4、MUC5AC、MUC5B和MUC7水平显著更高[30-31]。由图6可知,模型组小鼠阴道组织MUC1、MUC5B和MUC16水平有所增高,且与空白对照组存在显著性差异(P<0.000 1)。与模型组相比,DM8909、CCFM1337活菌和灭活菌体均对于MUC的表达具有较好的调控作用,使黏膜向着平稳的趋势发展。甲硝唑干预使MUC1、MUC5B 和 MUC16的表达有所下降,但效果不及乳杆菌的使用。FHNXY73M2-L同样能够抑制阴道加德纳菌造成的黏蛋白的急速上升,但是效果不及其他乳杆菌干预组,可能反映菌株特异性定植效率或代谢产物差异。
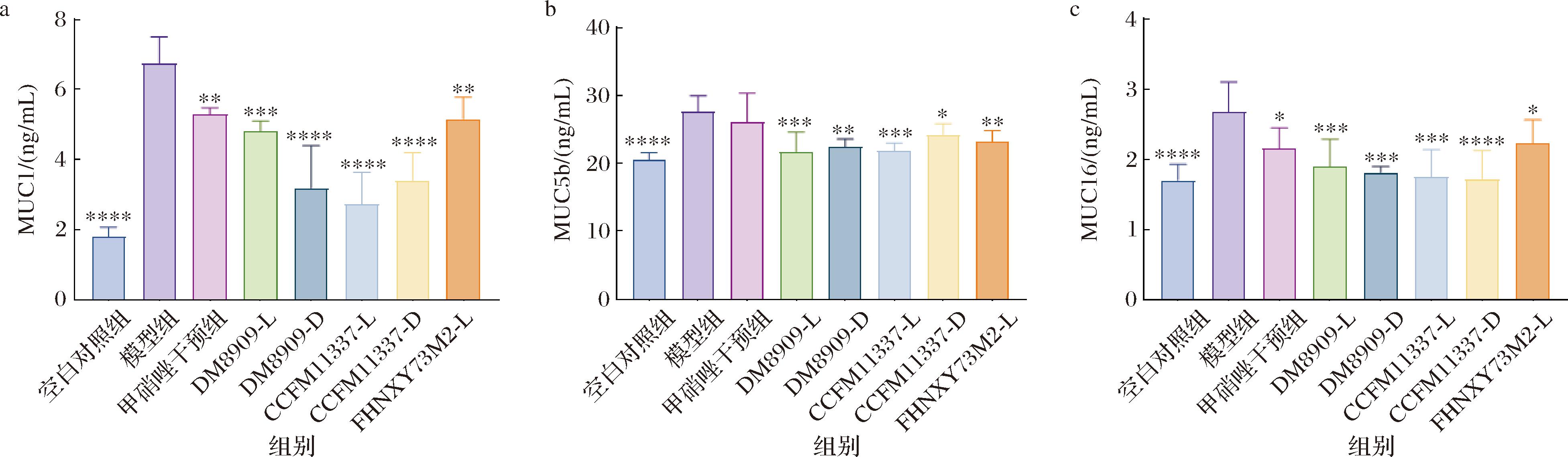
a-MUC1蛋白水平;b-MUC5B蛋白水平;c-MUC16蛋白水平
图6 乳杆菌对小鼠阴道上皮屏障中黏蛋白表达的影响
Fig.6 Effect of Lactobacillus on the expression of mucin in the vaginal epithelial barrier of mice
2.4 德氏乳杆菌CCFM1337对小鼠阴道上皮免疫屏障的影响
阴道感染会导致女性生殖系统黏膜菌群失调和免疫系统状态异常。致病微生物产生的酶对免疫球蛋白的结构具有特异性,会导致其降解[32]。IgG是宫颈和阴道分泌物中主要的免疫球蛋白,与病原体表面结合的IgG可以将原本易于扩散的病原体固定在黏蛋白基质上,阻止它们与靶细胞接触,并通过自然的黏液清除机制促进其清除,发挥关键的抗感染作用[33]。IgG的含量如图7-a 所示,模型组IgG受到了大量的消耗,甲硝唑干预组IgG的分泌没有显著提升。不同乳杆菌活菌和灭活菌体干预后,IgG含量均得到了显著提升,德氏乳杆菌CCFM1337活菌和死菌菌体处理使IgG含量分别提升至8.810 μg/mL(P<0.01)和8.367 μg/mL(P<0.05)。在黏膜免疫的背景下,IgA作为抗体,特别是分泌型IgA(sIgA),是黏膜上皮细胞为对抗HIV-1感染和其他病原体威胁所组织的首要防线机制[34-35]。sIgA通过与黏膜表面的微生物结合并中和病毒来发挥抗感染作用[36]。阴道加德纳菌的感染使sIgA的水平显著下降(图7-b)。甲硝唑干预虽能一定程度提高sIgA的水平,但是效果并不显著。FHNXY73M2-L处理组的效果与甲硝唑组类似。CCFM1337活菌和灭活菌体处理分别提升小鼠阴道组织中sIgA的含量至697.50 μg/mL(P<0.01)和634.30 μg/mL(P<0.01),且效果优于DM8909活菌(649.60 μg/mL)和灭活菌体(604.00 μg/mL)处理组。
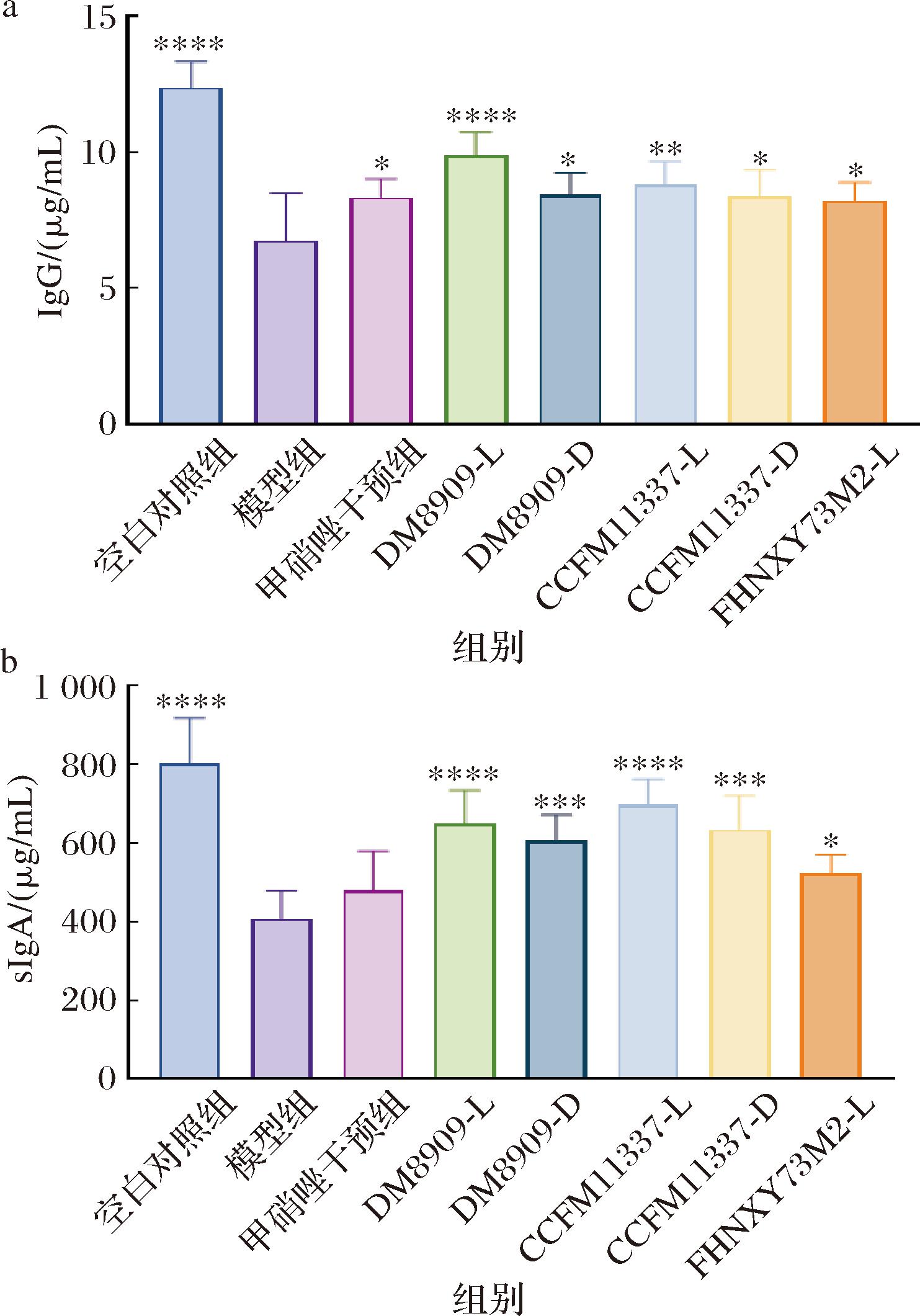
a-IgG水平;b-sIgA水平
图7 乳杆菌对小鼠阴道免疫球蛋白含量的影响
Fig.7 Effect of Lactobacillus on the content of vaginal immunoglobulin in mice
研究报道,细菌性阴道炎与育龄妇女阴道抗菌肽HBDs1-3水平降低有关[37],HBD-2 对革兰氏阴性和阳性细菌都有效[38]。选取HBD-2作为研究对象,检测其在小鼠阴道组织中的含量(图8)。与模型组较低的HBD-2 含量(6.98 ng/L)无显著性差异的主要是甲硝唑干预组与FHNXY73M2,说明甲硝唑并不能促进机体抗菌肽的分泌,抗生素的使用不能预防复发性阴道炎的发作。同时乳杆菌具有菌株差异,FHNXY73M2对于抗菌肽的释放也是无明显的作用。与之相反,德氏乳杆菌CCFM1337活菌与灭活菌体能够显著促进HBD-2的分泌,相比于模型组提高了41.12%(P<0.001)、43.55%(P<0.001),促进效果优于DM8909-L干预组的33.95%(P<0.01)。
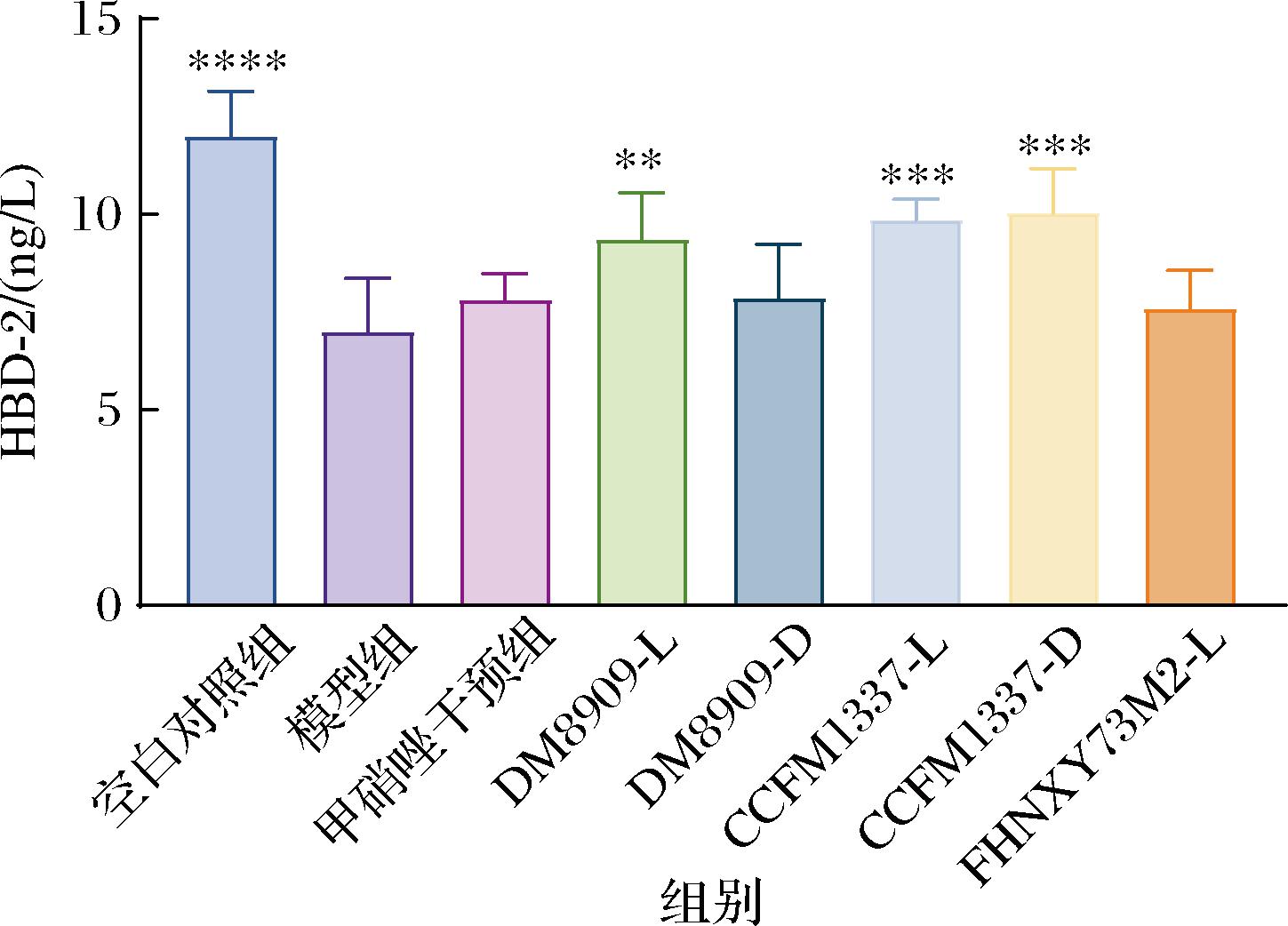
图8 乳杆菌对小鼠阴道抗菌肽的影响
Fig.8 Effect of Lactobacillus on vaginal antimicrobial peptides in mice
3 结论
本文主要探究了德氏乳杆菌CCFM1337在细胞水平上改善上皮屏障的效果以及其活菌和灭活菌体外用干预对于改善小鼠阴道上皮屏障,缓解阴道加德纳菌诱导的细菌性阴道炎的效果。结果表明,德氏乳杆菌CCFM1337能够显著提高阴道上皮细胞屏障相关基因ZO-1、OCLN和CLDN1的表达。德氏乳杆菌CCFM1337活菌和灭活菌体外用能够通过调节sECAD、OCLN、CLDN1和ZO-1 等阴道上皮紧密连接蛋白的水平,恢复阴道上皮机械屏障的完整性,并有效提高免疫屏障相关指标IgG、sIgA和抗菌肽HBD-2的分泌,最终有效缓解了由阴道加德纳菌侵袭导致的小鼠阴道组织炎症状况,为乳杆菌及其后生元在阴道健康中的应用提供了数据支持。然而,乳杆菌具体的起效机制和后生元活性成分还需进一步研究。
[1] ONDERDONK A B, DELANEY M L, FICHOROVA R N.The human microbiome during bacterial vaginosis[J].Clinical Microbiology Reviews, 2016, 29(2):223-238.
[2] JOSEPH R J, SER H L, KUAI Y H, et al.Finding a balance in the vaginal microbiome:How do we treat and prevent the occurrence of bacterial vaginosis?[J].Antibiotics, 2021, 10(6):719.
[3] LI Y X, ZHU W, JIANG Y, et al.Synthetic bacterial consortia transplantation for the treatment of Gardnerella vaginalis-induced bacterial vaginosis in mice[J].Microbiome, 2023, 11:54.
[4] FREITAS A C, HILL J E.Bifidobacteria isolated from vaginal and gut microbiomes are indistinguishable by comparative genomics[J].PLoS One, 2018, 13(4):e0196290.
[5] GELBER S E, AGUILAR J L, LEWIS K L T, et al.Functional and phylogenetic characterization of Vaginolysin, the human-specific cytolysin from Gardnerella vaginalis[J].Journal of Bacteriology, 2008, 190(11):3896-3903.
[6] CAUCI S, CULHANE J F, DI SANTOLO M, et al.Among pregnant women with bacterial vaginosis, the hydrolytic enzymes sialidase and prolidase are positively associated with interleukin-1β[J].American Journal of Obstetrics and Gynecology, 2008, 198(1):132.e1-132.e7.
[7] CHIENG W K, ABDUL JALAL M I, BEDI J S, et al.Probiotics, a promising therapy to reduce the recurrence of bacterial vaginosis in women? a systematic review and meta-analysis of randomized controlled trials[J].Frontiers in Nutrition, 2022, 9:938838.
[8] SCOTT E, DE PAEPE K, VAN DE WIELE T.Postbiotics and their health modulatory biomolecules[J].Biomolecules, 2022, 12(11):1640.
[9] CHEE W J Y, CHEW S Y, THAN L T L.Vaginal microbiota and the potential of Lactobacillus derivatives in maintaining vaginal health[J].Microbial Cell Factories, 2020, 19:203.
[10] ANAHTAR M N, GOOTENBERG D B, MITCHELL C M, et al.Cervicovaginal microbiota and reproductive health:The virtue of simplicity[J].Cell Host &Microbe, 2018, 23(2):159-168.
[11] BOAHEN A, THAN L T L, LOKE Y L, et al.The antibiofilm role of biotics family in vaginal fungal infections[J].Frontiers in Microbiology, 2022, 13:787119.
[12] HOUTTU N, MOKKALA K, SALEEM W T, et al.Potential pathobionts in vaginal microbiota are affected by fish oil and/or probiotics intervention in overweight and obese pregnant women[J].Biomedicine &Pharmacotherapy, 2022, 149:112841.
[13] YIN R P, WANG T, SUN J Z, et al.Postbiotics from Lactobacillus Johnsonii activates gut innate immunity to mitigate alcohol-associated liver disease[J].Advanced Science, 2025, 12(2):2405781.
[14] SALMINEN S, COLLADO M C, ENDO A, et al. The International Scientific Association of Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of postbiotics[J]. Nature Reviews Gastroenterology &Hepatology, 2021, 18(9):649-667.
[15] SHEN X, XU L, ZHANG Z Q, et al.Postbiotic gel relieves clinical symptoms of bacterial vaginitis by regulating the vaginal microbiota[J].Frontiers in Cellular and Infection Microbiology, 2023, 13:1114364.
[16] HUANG X Y, LIN R M, MAO B Y, et al.Lactobacillus crispatus CCFM1339 inhibits vaginal epithelial barrier injury induced by Gardnerella vaginalis in mice[J].Biomolecules, 2024, 14(2):240.
[17] ZHANG Q X, CHENG Q H, CUI S M, et al.Inhibitory effect of Lactobacillus gasseri CCFM1201 on Gardnerella vaginalis in mice with bacterial vaginosis[J].Archives of Microbiology, 2022, 204(6):315.
[18] KWAK J, PANDEY S, CHO J, et al.Development of the standard mouse model for human bacterial vaginosis induced by Gardnerella vaginalis[J].Frontiers in Veterinary Science, 2023, 10:1226859.
[19] DUSIO G F, CARDANI D, ZANOBBIO L, et al.Stimulation of TLRs by LMW-HA induces self-defense mechanisms in vaginal epithelium[J].Immunology and Cell Biology, 2011, 89(5):630-639.
[20] DELGADO-DIAZ D J, JESAVELUK B, HAYWARD J A, et al.Lactic acid from vaginal microbiota enhances cervicovaginal epithelial barrier integrity by promoting tight junction protein expression[J].Microbiome, 2022, 10:141.
[21] ARMSTRONG E, HEMMERLING A, MILLER S, et al.Sustained effect of LACTIN-V (Lactobacillus crispatus CTV-05) on genital immunology following standard bacterial vaginosis treatment:Results from a randomised, placebo-controlled trial[J].The Lancet Microbe, 2022, 3(6):e435-e442.
[22] PEREZ-MORENO M, JAMORA C, FUCHS E.Sticky business orchestrating cellular signals at adherens junctions[J].Cell, 2003, 112(4):535-548.
[23] YAN F, LIU L P, DEMPSEY P J, et al.A Lactobacillus rhamnosus GG-derived soluble protein, p40, stimulates ligand release from intestinal epithelial cells to transactivate epidermal growth factor receptor[J].Journal of Biological Chemistry, 2013, 288(42):30742-30751.
[24] SCHIAVI E, GLEINSER M, MOLLOY E, et al.The surface-associated exopolysaccharide of Bifidobacterium longum 35624 plays an essential role in dampening host proinflammatory responses and repressing local TH17 responses[J].Applied and Environmental Microbiology, 2016, 82(24):7185-7196.
[25] WANG S H, AHMADI S, NAGPAL R, et al.Lipoteichoic acid from the cell wall of a heat killed Lactobacillus paracasei D3-5 ameliorates aging-related leaky gut, inflammation and improves physical and cognitive functions:From C.elegans to mice[J].GeroScience, 2020, 42(1):333-352.
[26] CHASIOTIS H, KOLOSOV D, BUI P, et al.Tight junctions, tight junction proteins and paracellular permeability across the gill epithelium of fishes:A review[J].Respiratory Physiology &Neurobiology, 2012, 184(3):269-281.
[27] LI D D, ZHANG T, YANG H, et al.Effect of vitamin D on the proliferation and barrier of atrophic vaginal epithelial cells[J].Molecules, 2023, 28(18):6605.
[28] ANTON L, SIERRA L J, DEVINE A, et al.Common cervicovaginal microbial supernatants alter cervical epithelial function:Mechanisms by which Lactobacillus crispatus contributes to cervical health[J].Frontiers in Microbiology, 2018, 9:2181.
[29] DONG M T, DONG Y L, BAI J Y, et al.Interactions between microbiota and cervical epithelial, immune, and mucus barrier[J].Frontiers in Cellular and Infection Microbiology, 2023, 13:1124591.
[30] BORGDORFF H, GAUTAM R, ARMSTRONG S D, et al.Cervicovaginal microbiome dysbiosis is associated with proteome changes related to alterations of the cervicovaginal mucosal barrier[J].Mucosal Immunology, 2016, 9(3):621-633.
[31] MONCLA B J, CHAPPELL C A, DEBO B M, et al.The effects of hormones and vaginal microflora on the glycome of the female genital tract:Cervical-vaginal fluid[J].PLoS One, 2016, 11(7):e0158687.
[32] KALIA N, SINGH J, KAUR M.Immunopathology of recurrent vulvovaginal infections:New aspects and research directions[J].Frontiers in Immunology, 2019, 10:2034.
[33] SCHROEDER H A, NUNN K L, SCHAEFER A, et al.Herpes simplex virus-binding IgG traps HSV in human cervicovaginal mucus across the menstrual cycle and diverse vaginal microbial composition[J].Mucosal Immunology, 2018, 11(5):1477-1486.
[34] SHEN H, GOLDBERG E, SALTZMAN W M.Gene expression and mucosal immune responses after vaginal DNA immunization in mice using a controlled delivery matrix[J].Journal of Controlled Release, 2003, 86(2-3):339-348.
[35] AKAGI T, KAWAMURA M, UENO M, et al.Mucosal immunization with inactivated HIV-1-capturing nanospheres induces a significant HIV-1-specific vaginal antibody response in mice[J].Journal of Medical Virology, 2003, 69(2):163-172.
[36] ZHENG J J, SONG J H, YU C X, et al.Difference in vaginal microecology, local immunity and HPV infection among childbearing-age women with different degrees of cervical lesions in Inner Mongolia[J].BMC Women’s Health, 2019, 19:109.
[37] NODA-NICOLAU N M, DE CASTRO SILVA M, BENTO G F C, et al.Cervicovaginal levels of human beta defensins during bacterial vaginosis[J].PLoS One, 2021, 16(12):e0260753.
[38] PIVARCSI A, NAGY I, KORECK A, et al.Microbial compounds induce the expression of pro-inflammatory cytokines, chemokines and human β-defensin-2 in vaginal epithelial cells[J].Microbes and Infection, 2005, 7(9-10):1117-1127.