由于天然肠衣供应不足,人造肠衣广泛应用于香肠加工。人造肠衣分为可食用肠衣和不可食用肠衣,而胶原蛋白肠衣作为可食用肠衣受到了广泛的关注。近年来,胶原蛋白肠衣在香肠工业的应用具有不可替代的作用[1]。胶原蛋白肠衣是以胶原蛋白为原料制备的一类肠衣,胶原蛋白作为动物组织中一类重要的蛋白质,其中Ⅰ型胶原蛋白含量最为丰富。胶原蛋白由3条相同或略有不同的多肽链组成,形成卷曲的三螺旋结构,具有良好的生物相容性和成膜性能[2]。在动物组织中,胶原蛋白常以胶原纤维的形式存在,是丝状准结晶聚集体[3]。胶原纤维因其具有优异的生物相容性、生物可降解性、低免疫原性、促进细胞行为的生物学活性及良好的机械性能而被广泛应用于食品、生物与医药及医学方面[4-5]。目前,胶原纤维膜在食品工业的研究包括上述的人造肠衣外,还广泛应用于新型包装材料,延长食品的保质期、检测食品新鲜度[6]。TANG等[7]在胶原纤维膜中添加苹果多酚制备出一款可降解活性包装膜,减少了青椒在贮存过程中维生素C含量的减少。LI等[8]以鱼鳞明胶制备出一款环保型复合保鲜膜,并延长草莓的保存期7 d。因此预计胶原纤维膜未来5年将在可持续包装市场占据重要地位。
在胶原纤维膜制备过程中,主要包括对原料进行预处理、酸溶胀、均质、湿挤压或干挤压法挤压成型、氨水中和及烘干成型。相关研究发现,酸的种类及pH对胶原纤维制备胶原纤维膜的结构及交联程度会产生一定的影响。徐金龙[3]使用盐酸溶胀黄牛皮,发现在pH=3时溶胀率(swelling rate,SR)最大,此时制备的胶原纤维膜具有最佳机械性能。ANDONEGI等[9]发现柠檬酸的加入不影响胶原纤维的三螺旋结构,且添加柠檬酸后能增强其交联,使薄膜机械性能增强。DE GUZZI PLEPIS等[10]使用乙酸处理牛浆膜和牛肌腱制备牙周引导组织再生的重构胶原膜。ZHANG等[11]研究发现随着盐酸浓度的增加,胶原纤维的三螺旋结构、二级结构和共价交联逐渐受到破坏。
近年来,随着可食用膜的深入研究,其原料来源丰富,主要包括植物基原料和动物基原料,动物基原料有鱼皮、黄牛皮、鸡皮等,而对于牦牛皮制备可食用膜的研究却鲜有报道。牦牛长期生活在高寒、缺氧、强紫外线的青藏高原地区,牦牛皮营养价值颇为丰富,其皮中的蛋白含量高于黄牛皮[12]、安格斯牛皮和西门塔尔牛皮[13],牦牛皮具有较高的热稳定性,且牦牛皮中水分含量(water content,WC)、脂肪含量低于安格斯牛皮[13],其胶原纤维具有更致密的结构[14],牦牛皮中亚氨基酸(羟脯氨酸、脯氨酸)含量远高于黄牛皮,脯氨酸与羟脯氨酸形成的吡咯环可产生空间位阻,限制多肽链构象,从而增强三螺旋结构稳定性,部分通过羟脯氨酸羟基的氢键来维持结构稳定,此外,牦牛皮中疏水氨基酸的含量较高,具有更高的热稳定性[15]。牦牛皮经酶水解后具有降血糖[16]、抗氧化活性[17]等功能,更适用于食品原料。牦牛皮资源相对稀缺,在高原地区常将牦牛皮视为牦牛产业的主要副产物之一。目前对于牦牛皮的研究主要集中在胶原蛋白提取工艺及性能[12]、牦牛胶原蛋白肽的功能活性[16],在食品行业并未得到深入的研究及开发,将牦牛皮用于制备胶原纤维膜,促进青海地区的经济发展,将资源优势转化为经济优势。因此,本文以牦牛皮为原料,经预处理后,采用盐酸、乙酸进行溶胀,制备胶原纤维膜,以胶原纤维膜理化特性为指标,并进一步研究其相关机理,为后续提高牦牛皮胶原纤维膜的机械性能奠定一定理论基础。
1 材料与方法
1.1 材料与试剂
牦牛皮,采自当地农户;甘油、氨水、冰醋酸,天津市富宇精细化工有限公司;浓盐酸、氯化钠,天津市河东区红岩试剂厂;羧甲基纤维素钠(carboxymethyl cellulose sodium,CMC-Na),天津市致远化学试剂有限公司;无水碳酸钠、氢氧化钠均为分析纯,国药集团化学试剂有限公司。
1.2 仪器与设备
电动绞肉机,添美家Tenfly公司;高速剪切机,上海哲函仪器有限公司;JHY-1000M电子拉力试验机,厦门亿恩达仪器设备有限公司;DL321025B数显外径千分尺,宁波得力工具有限公司;UV-2000紫外可见分光光度计、JSM 7900F傅里叶变换红外光谱(Fourier infrared spectroscopy,FTIR)仪,日本岛津;JSM 7900F扫描电子显微镜(scanning electron microscopy,SEM),日本电子株式会社;STA449 F3-STA449 F3同步热分析仪,德国耐驰仪器制造有限公司。
1.3 实验方法
1.3.1 牦牛皮预处理
牦牛皮皮毛层采用酸酶法将大部分的毛进行脱去,基于SUURS等[18]的研究,并进行适当调整。去脂肪时使用质量分数为5%的碳酸钠溶液代替0.1 mol/L NaOH,其余步骤一致。
1.3.2 胶原团的制备
取适量牛皮,将牦牛皮和碎冰以质量比1∶2加入高速剪切机中打碎,分别在质量分数为0.96%的盐酸和0.7 mol/L乙酸中4 ℃溶胀24 h,样品与溶液料液比为1∶2(g∶mL),放入绞肉机中进行打碎成胶原团,取适量胶原团加入质量分数为1%的CMC-Na,CMC-Na的质量是基于胶原团质量的1/4,混揉均匀。并放入真空干燥箱中脱气处理,干燥温度20 ℃,干燥时间60 min。取出,备用。
1.3.3 胶原纤维膜的制备
取5 g胶原团,使用0.5 mm凹槽的不锈钢辊进行擀压,将膜放入质量分数为5%的氨水溶液中浸泡10 min进行固化,去离子水清洗,放入质量分数为3%的甘油溶液浸泡30 min。室温晾干24 h,接着放入25 ℃、相对湿度为(58±3)%的干燥器中平衡48 h。
1.3.4 胶原纤维膜厚度的测定
使用测厚仪进行测定,每张膜测定5次,取平均值即为膜厚。
1.3.5 胶原纤维膜干、湿态拉伸强度(tensile strength,TS)和断裂延伸率(elongation at break,EAB)测定
参考徐菲菲等[19]的研究,并进行调整;将胶原蛋白肠衣膜剪成10 mm×50 mm的长方形,采用拉力试验机测定样品在干、湿态下(将裁好的膜放入25 ℃的水中浸泡1 min取出)的TS、EAB,重复3~5次,取平均值。测试参数:自动判断裂(到达力)30%,自动判断裂(灵敏度)30%,运行速度100 mm/min。TS和EAB的计算分别如公式(1)和公式(2)所示:
(1)
(2)
式中:TS为拉伸强度,MPa;F为最大力,N;S为膜的横截面积,mm2;EAB为断裂延伸率,%;d为最大变形,mm;d0为膜原长,mm。
1.3.6 胶原纤维膜透光率的测定
使用紫外分光光度计测膜在600 nm波长下的吸光度值来评价膜的透光性能。具体方法参考TANG等[7]方法。
1.3.7 胶原纤维膜WC和SR的测定
参考TANG等[7]的方法,测定胶原纤维膜的WC及SR。
1.3.8 胶原纤维膜热收缩率(hot shrinkage rate,HSR)和热溶胀率(thermal swelling rate,TSR)的测定
参考CHEN等[20]的研究并进行适当调整;将胶原蛋白外壳样品切成30 mm×10 mm的条带。在沸水中蒸煮1 min后,分别测量胶原纤维膜的长度和宽度。然后根据蒸煮前后长度(machine direction,MD)和宽度(transverse direction,TD)的变化,HSR和TSR的计算分别如公式(3)和公式(4)所示:
(3)
(4)
1.3.9 FTIR分析
将胶原纤维膜剪碎成粉末,以质量比1∶100的样品∶KBr进行压片,使用FTIR仪在400~4 000 cm-1的范围内进行,扫描32次,分辨率为1 cm-1。对数据使用Omnic软件计算蛋白质二级结构的含量。
1.3.10 X射线衍射(X-diffraction,XRD)分析
使用XRD仪测定样品的结晶度。每个样品在5°~50°范围内扫描,步宽为0.02°,扫描速率为0.02°/0.1 s。
1.3.11 SEM分析
将样品置于液氮中进行淬断,在10 kV电压下分别以3 000×和5 000×的放大倍数观察胶原纤维膜的截面特征。
1.3.12 热重分析(thermogravimetric analysis,TGA)
使用TGA探索胶原纤维膜在25~600 ℃的热降解行为。称取5 mg薄膜样品,在N2环境下以10 ℃/min的加热速率从25 ℃加热至600 ℃。
1.4 数据处理
对实验数据进行统计学分析,所有数据均进行3次重复实验,实验结果以“平均值±标准差”的形式表示。采用IBM SPSS Statistics 26软件进行分析。
2 结果与分析
2.1 胶原纤维膜厚度、机械性能分析
2种胶原纤维膜的厚度见表1,盐酸组和乙酸组胶原纤维膜的厚度分别为0.059、0.072 mm,盐酸组制备的胶原纤维膜的厚度小于乙酸组。商业胶原肠衣的厚度约为0.050 mm,盐酸组胶原纤维膜厚度更为接近。
表1 胶原纤维膜的理化指标
Table 1 Physical and chemical properties of collagen fiber film

样品厚度/mm机械性能干湿TS/MPaEAB/%TS/MPaEAB/%透光度/%含水量/%乙酸0.072±0.005b54.16±7.32a23.14±2.64a8.13±0.79a21.19±1.99a8.88±0.001a15.60±2.04a盐酸0.059±0.007a69.70±4.53b24.74±2.19a10.73±0.77b26.42±2.13b5.58±0.008b12.43±1.09b
注:不同小写字母表示差异显著(P<0.05)(下同)。
TS表示膜抵抗破坏拉伸的能力,EAB反映了膜的柔韧性[21],是评价胶原纤维膜保证香肠品质的2个重要参数。结果见表1,盐酸组湿态下的TS和EAB均显著高于乙酸组(P<0.05),总的来说,盐酸组胶原纤维膜机械性优于乙酸组,这可能是盐酸组对牦牛皮胶原纤维的充分溶胀,小分子物质和胶原纤维之间充分接触,在膜中形成了更为紧密的共存互穿的网络[22]。ZHU等[23]利用黄牛皮制备胶原纤维膜,并加入矿化CMC-Na增强其湿拉伸性能,经处理后的湿TS达到了2.5 MPa;HOU等[2]以转谷氨酰胺酶交联罗非鱼胶原蛋白制备可食用膜,经交联后,其干TS达到了3.07 MPa;PARK等[24]以甘油作为增塑剂制备明胶基可食性膜,可食性膜的干TS为17.3 MPa;GIOSAFATTO等[25]使用转谷氨酰胺酶(transglutaminase,TG)交联柑橘果胶和菜豆蛋白制备可食性膜,其干TS为36.71 MPa,EAB为2.4%。与其他来源动、植物胶原纤维膜相比,牦牛皮胶原纤维膜在干态及湿态下均表现出更优的机械性能。
2.2 胶原纤维膜WC和透光分析
薄膜的含水量与其防水能力有关,对食品贮存期内稳定性起着关键作用[26]。盐酸组WC显著少于乙酸组,为12.43%,这可能是因为盐酸诱导的致密化疏水重构[3],显著降低了胶原纤维表面的亲水性,而乙酸作为弱酸,仅溶胀表面,故亲水基团(—OH、—COOH)仍占主导。TANG等[27]研究发现以黄牛皮为原料制备胶原纤维膜的含水量为12.73%,略高于牦牛皮制备胶原纤维膜。
透光度值越高,表明膜的透明度越低;而肠衣产品的透明度是影响消费者购买意愿的重要因素。与乙酸组相比,盐酸处理显著降低了胶原纤维膜的透光度值,提升了其透明度与表观品质。
2.3 胶原纤维膜溶胀性质分析
HSR反映了膜在热水中因热变性而沿纤维取向发生收缩的程度,与胶原蛋白肠衣的应用密切相关[28]。2种胶原纤维膜的HSR如表2所示,盐酸组TD显著低于乙酸组(P<0.05),MD无显著变化(P>0.05),盐酸组整体表现为较低的HSR,这可能是由于盐酸组胶原纤维膜分子间的交联和缠结更加紧密、有序,形成了致密的结构,因此形成致密的膜。CHEN等[20]以黄牛皮为原料制备胶原纤维膜,发现在干燥温度为55 ℃,胶原纤维膜的MD和TD分别为37.5%和20.0%,提高干燥温度能增强膜的交联强度,降低胶原纤维膜的HSR,提高其热稳定性。
表2 两种胶原纤维膜SR、HSR和TSR 单位:%
Table 2 SR, HSR, and TSR for two collagen fiber films
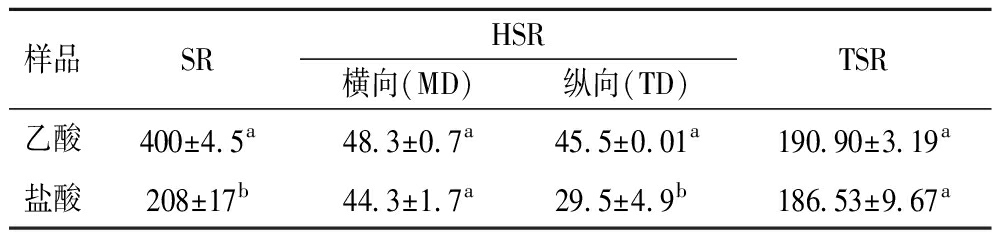
样品SRHSR横向(MD)纵向(TD)TSR乙酸400±4.5a48.3±0.7a45.5±0.01a190.90±3.19a盐酸208±17b44.3±1.7a29.5±4.9b186.53±9.67a
SR和TSR反映胶原纤维膜在室温和沸水中吸水膨胀情况,与胶原纤维膜的耐水性相关。盐酸组胶原纤维膜的SR和TSR值均小于乙酸组,说明盐酸组纤维膜耐水性增强,这可能是因为牦牛皮经盐酸溶胀后所形成的纤维束小,促进其分子间和分子内交联,纤维结构紧密,使其耐水性增强,黄牛皮制备胶原纤维膜SR和TSR分别为175%和205%[20],因此,牦牛皮制备胶原纤维膜具有较高的热耐水性。
2.4 SEM分析
为了解不同溶胀酸对胶原纤维膜结构的影响,对胶原纤维膜及酸溶胀后的牦牛皮浆的微观结构进行了评价(图1)。结果表明,盐酸组胶原纤维膜截面均匀致密,这可能是因为盐酸作为小分子酸,盐酸溶胀后牦牛皮胶原纤维更加松散,而乙酸溶胀后呈现片状(图1-c),盐酸充分溶胀,而乙酸仅对于其表面进行了溶胀,后续添加CMC-Na能够充分进入到胶原纤维束之间,CMC-Na中的羧基与胶原纤维末端肽链中氨基的分子间缠结,形成更为致密的交联结构,使结构更致密[28],而乙酸组胶原纤维膜截面观察到了不均匀、破裂和孔的出现。通常,膜的机械性能取决于聚合物基体中分子间和分子内相互作用的分布和密度[29]。可食用膜的紧密和致密结构可能是其较高TS的原因[26],这与上文中提到的盐酸溶胀纤维膜机械性能强度较大一致。

a-胶原纤维膜(3 000×);b-胶原纤维膜(5 000×);c-冻干牛皮浆
图1 酸溶胀胶原纤维膜及牦牛皮浆的SEM图像
Fig.1 SEM images of collagen fiber film and yak hide pulp
2.5 FTIR分析
为评估薄膜中各成分之间相互作用,不同酸溶胀胶原纤维膜的FTIR如图2所示。2种酸溶胀的纤维膜均表现出胶原蛋白的特征峰;对应O—H和N—H伸缩振动和分子间以及分子内氢键的酰胺A带,交联程度越大,会使羟基发生明显的伸缩振动,向更高的波长发生移动[9,30]。盐酸组和乙酸组出峰位置分别为3 432.1、3 434.7 cm-1,与乙酸组相比,盐酸组吸收峰向低波数移动,说明了N—H基团参与形成了更强或更多的氢键;对应N—H伸缩振动的酰胺B带出现在2 923 cm-1处;酰胺I带(1 600~1 700-1)区域能够较为灵敏的反应蛋白的二级结构,属于酰胺或多肽中C![]() O基团的伸缩振动,与乙酸组相比,盐酸组胶原纤维膜出现了轻微红移,且峰宽有所增加,可能是由于盐酸组形成更多的氢键,导致伸缩振动频率降低[31];纤维膜的稳定性与蛋白质的二级结构有关,而蛋白质的二级结构表现为分子间和分子内的作用力,如二硫键、氢键等[32],蛋白质二级结构含量如表3所示,与乙酸组相比,盐酸组β折叠含量高,而α螺旋含量低。相关研究表明,β折叠是胶原分子间通过氢键相互作用、自组装形成纤维网络的标志性有序构象[33],胶原蛋白的有序结构含量的增加是蛋白稳定的基础[34],α螺旋是胶原三螺旋结构核心构象,乙酸组α螺旋含量占比略高于盐酸组,说明乙酸作为弱酸,对胶原纤维结构溶胀更温和,使其胶原分子天然构象保留更完整。2种酸溶胀处理无规卷曲含量无显著差异,说明2种酸对胶原无序区域的破坏程度相近。酰胺Ⅱ与N—H平面弯曲和C—N伸展振动有关,位置在1 540 cm-1处;酰胺Ⅲ出现在约1 240 cm-1处,由酰胺键的C—N伸缩振动和N—H弯曲振动以及来自甘氨酸主链和脯氨酸侧链基团的CH2振动引起的。不同酸处理后胶原纤维膜并未出现显著的官能团变化,但能观察到盐酸组的特征吸收峰强度有所增加,这可能与盐酸组存在强作用力相关[22]。
O基团的伸缩振动,与乙酸组相比,盐酸组胶原纤维膜出现了轻微红移,且峰宽有所增加,可能是由于盐酸组形成更多的氢键,导致伸缩振动频率降低[31];纤维膜的稳定性与蛋白质的二级结构有关,而蛋白质的二级结构表现为分子间和分子内的作用力,如二硫键、氢键等[32],蛋白质二级结构含量如表3所示,与乙酸组相比,盐酸组β折叠含量高,而α螺旋含量低。相关研究表明,β折叠是胶原分子间通过氢键相互作用、自组装形成纤维网络的标志性有序构象[33],胶原蛋白的有序结构含量的增加是蛋白稳定的基础[34],α螺旋是胶原三螺旋结构核心构象,乙酸组α螺旋含量占比略高于盐酸组,说明乙酸作为弱酸,对胶原纤维结构溶胀更温和,使其胶原分子天然构象保留更完整。2种酸溶胀处理无规卷曲含量无显著差异,说明2种酸对胶原无序区域的破坏程度相近。酰胺Ⅱ与N—H平面弯曲和C—N伸展振动有关,位置在1 540 cm-1处;酰胺Ⅲ出现在约1 240 cm-1处,由酰胺键的C—N伸缩振动和N—H弯曲振动以及来自甘氨酸主链和脯氨酸侧链基团的CH2振动引起的。不同酸处理后胶原纤维膜并未出现显著的官能团变化,但能观察到盐酸组的特征吸收峰强度有所增加,这可能与盐酸组存在强作用力相关[22]。
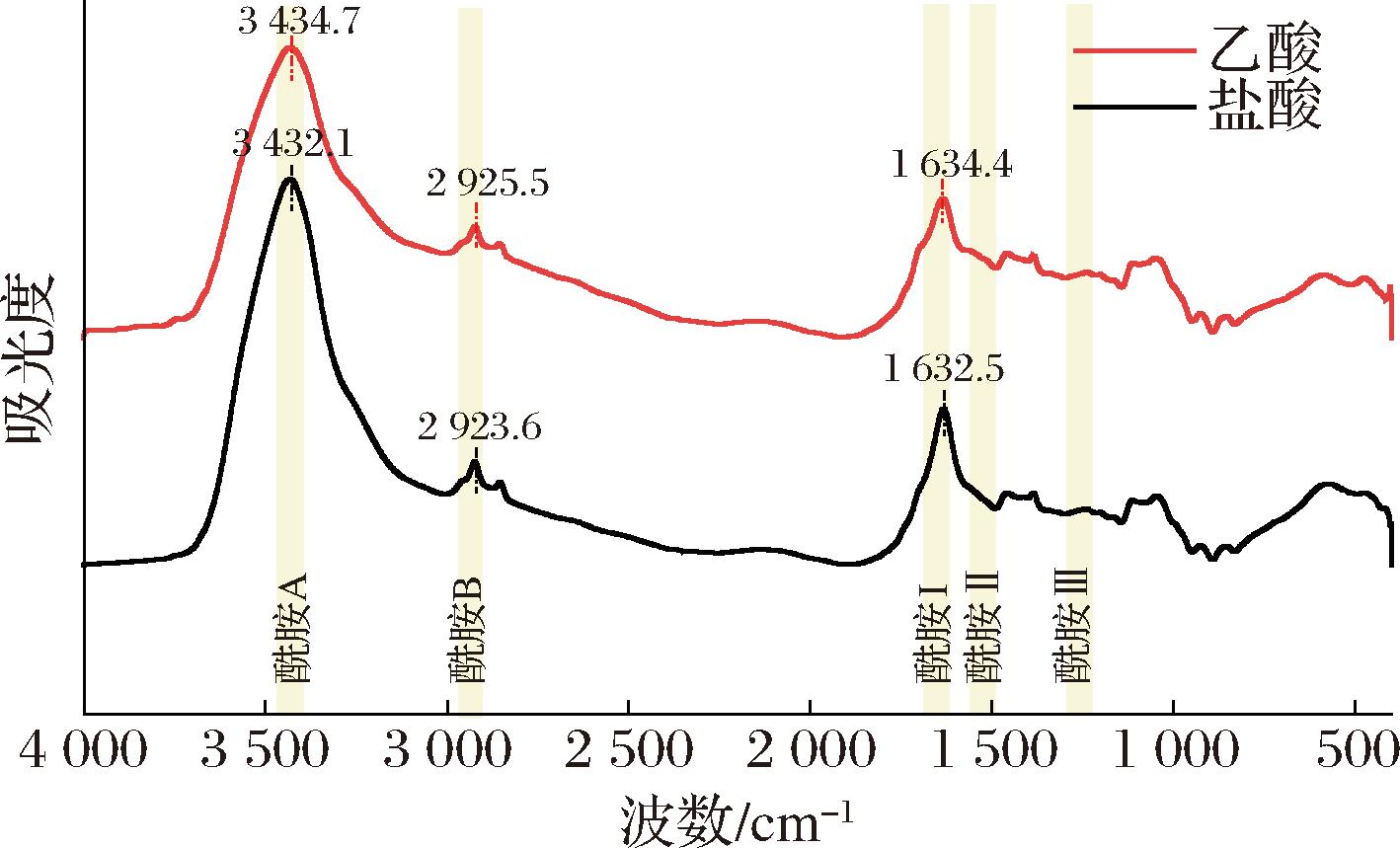
图2 两种胶原纤维膜FTIR图像
Fig.2 FTIR images of two collagen fiber films
表3 通过FTIR获得的样品的二级结构含量 单位:%
Table 3 Secondary structure contents of samples obtained by FTIR

样品β折叠(1 630~1 640-1)无规则卷曲(1 640~1 650-1)α螺旋(1 650~1 660-1)β转角(1 660~1 680-1)盐酸组41.2418.8526.7813.12乙酸组39.2118.7928.3113.69
2.6 XRD分析
使用XRD分析胶原纤维膜的结构、分子链之间的距离和蛋白质的三螺旋结构的含量,如图3所示,2张胶原纤维膜图谱均在7.62°(2θ)附近显示出1个尖峰,在22.2°(2θ)附近显示出1个宽峰。第1个尖峰与三螺旋结构的直径有关,强度与蛋白质三螺旋含量有关,第2个宽的无定形峰与胶原蛋白三螺旋链沿着氨基酸残基之间的距离相关[28],由图3可知,盐酸组相对于乙酸组具有更高的三螺旋含量。
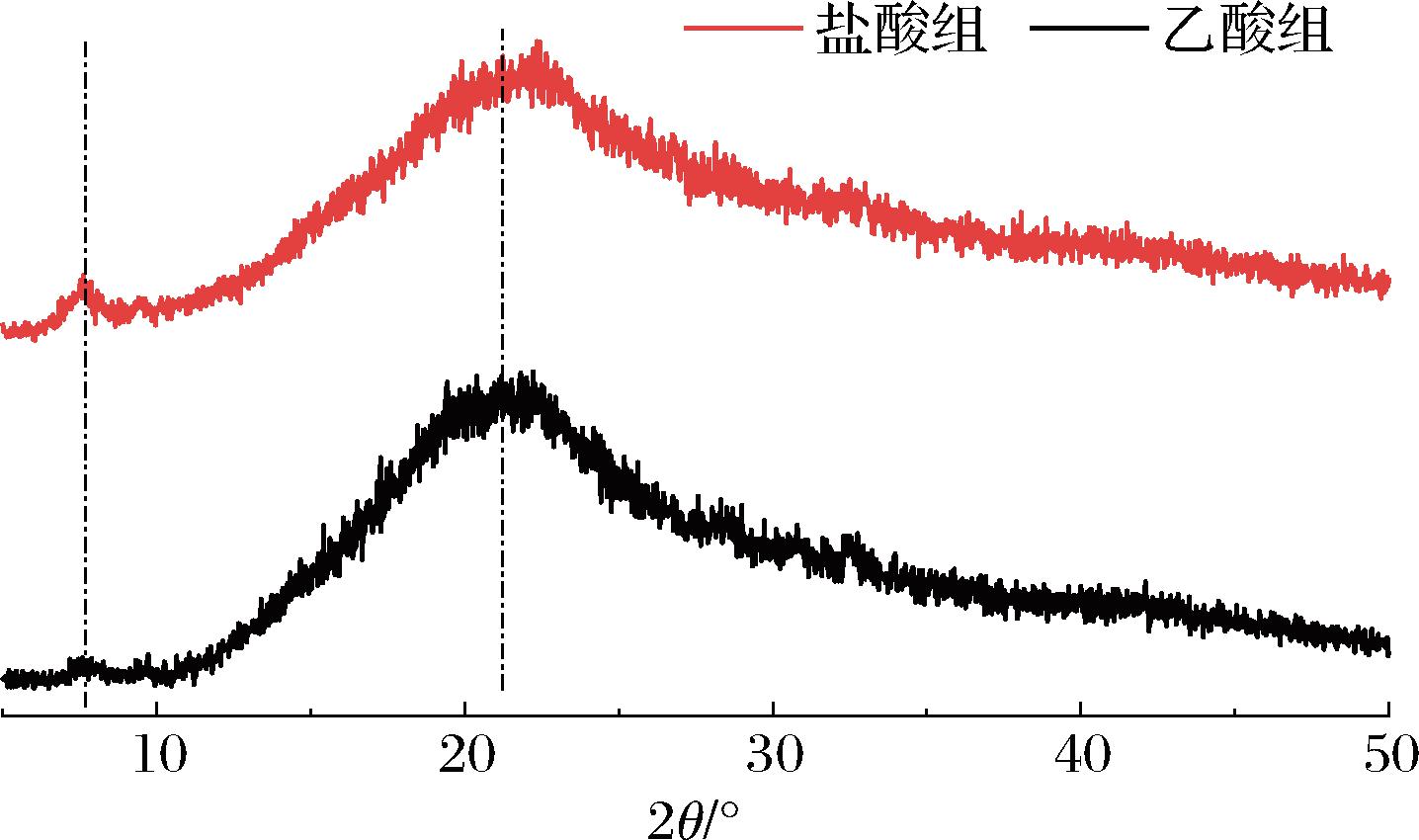
图3 两种胶原纤维膜XRD图像
Fig.3 XRD images of two collagen fiber films
2.7 TGA
通过TGA评价纤维膜的热稳定性,以确定薄膜的热降解速率,图4中分别是2种不同酸处理下胶原纤维膜的TGA和DGA曲线,有3个主要质量损失阶段,降解温度(Td)、质量损失(wi)和纤维膜的残留物列于表4中。在低于150 ℃的温度下,盐酸组和乙酸组样品质量损失分别为4.15%和4.88%,在这个温度下主要损失的是纤维膜中的自由水和其他挥发性物质的蒸发[30];此外,第2阶段发生在240~250 ℃,归因于甘油的蒸发[9]和CMC-Na主链糖苷键断裂,处于300 ℃以上的第3阶段与低分子质量蛋白质和生物聚合物的降解行为有关,特别是混合物或交联组分,与黄牛皮胶原纤维膜观察一致[20]。由图4可知,盐酸组主DTG峰温大于乙酸组,表明盐酸组热稳定性大于乙酸组。与乙酸组相比,盐酸组胶原纤维膜在3次主要损失阶段均表现出较高的降解温度和较低的质量损失,这可能是由于盐酸组中存在的高疏水性和较少的游离和结合水[32],且盐酸组纤维膜的残留物含量高于乙酸组,表明通过盐酸溶胀能够提高胶原纤维膜的热稳定性,这可能是因为盐酸处理后使得分子间和分子内的氢键增强,胶原纤维膜交联密度增大,胶原纤维膜抗拉伸、抗断裂能力增强,且盐酸处理组中纤维排列规整、有序,降低了分子间的间隙,CMC-Na分子能充分进入到胶原纤维束间,相互作用力增强,使纤维膜形成致密结构,热稳定性增强,此外,纤维的定向排列使受力均匀,机械性能增大[35],这与前文FTIR及SEM所观察到的结果一致。
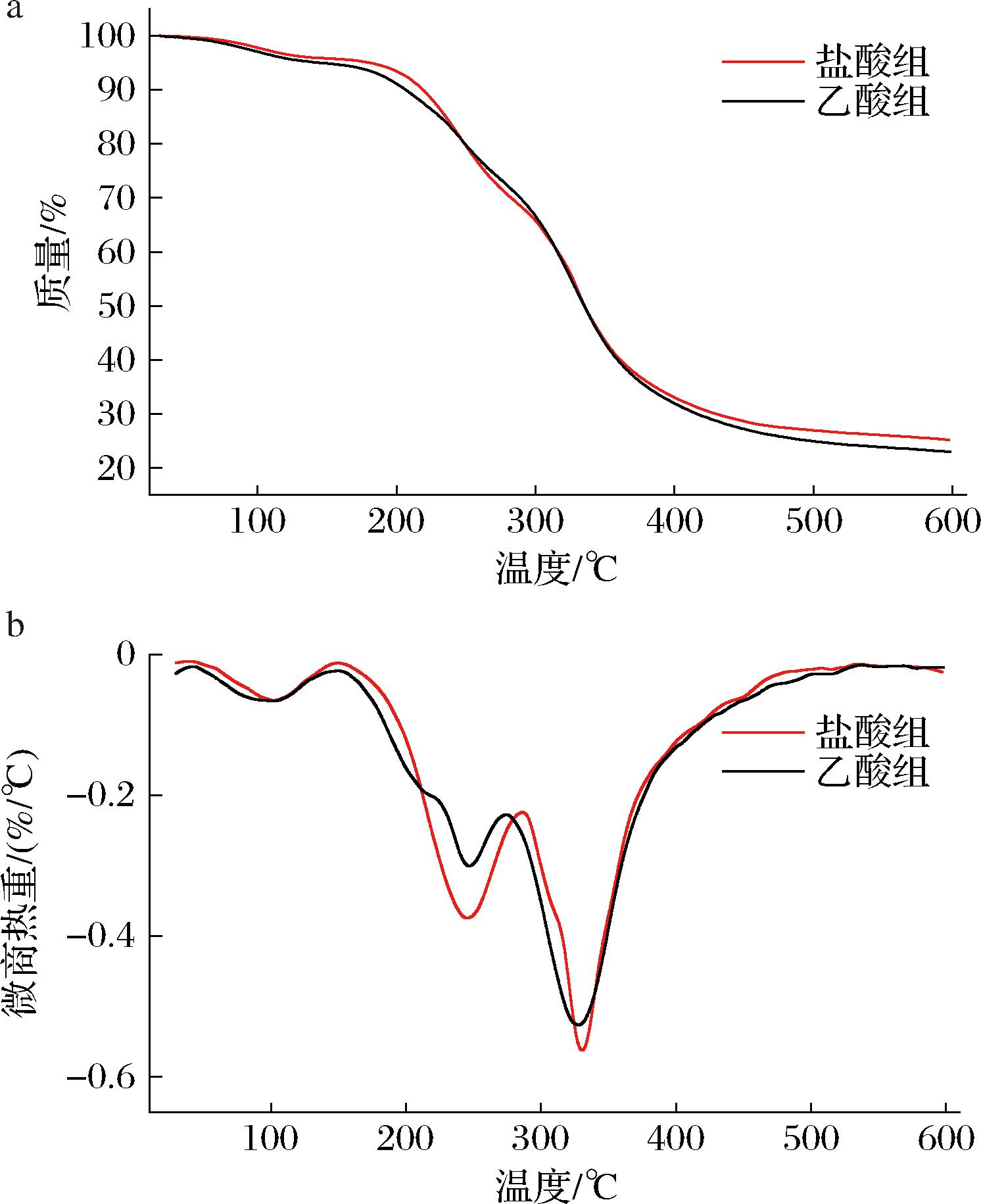
a-TGA曲线;b-DTG曲线
图4 两种胶原纤维膜的TGA和DTG曲线
Fig.4 TGA and DTG curves of two collagen fiber films
表4 两种胶原纤维膜的热降解温度(Td)和质量损失(wi)
Table 4 Thermal degradation temperature and weight loss of two collagen fiber films
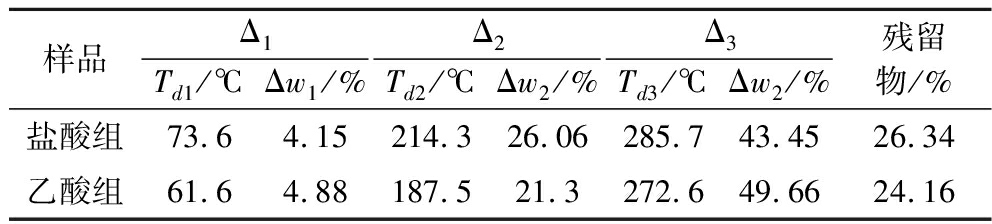
样品Δ1Δ2Δ3Td1/℃Δw1/%Td2/℃Δw2/%Td3/℃Δw2/%残留物/%盐酸组73.64.15214.326.06285.743.4526.34乙酸组61.64.88187.521.3272.649.6624.16
3 结论
牦牛皮作为高寒地区特色畜牧资源,其胶原蛋白的高值化利用对促进区域经济发展具有重要意义。本文以牦牛皮为原料,研究盐酸和乙酸作为溶胀酸对牦牛皮胶原纤维膜的影响。结果表明,盐酸作为溶胀酸制备的胶原纤维膜表现出较优的理化特性,并通过SEM、FTIR、XRD及TGA数据表明,盐酸处理组呈现有序的平行排列,且处理后分子间和分子内的氢键等化学键增多、相互作用力增强,表明盐酸能促进交联,形成更加致密的网状结构,牦牛皮胶原纤维经盐酸处理后,其微观结构的调控显著增强了胶原纤维膜的综合性能。以上研究揭示了牦牛皮胶原纤维膜在食品可食用膜领域的应用潜力,为牦牛皮制备胶原纤维膜的高值化利用提供了理论依据。
[1] 田其英, 翟玮玮, 王强.肠衣在香肠中的应用研究进展[J].食品研究与开发, 2022, 43(2):220-224.TIAN Q Y, ZHAI W W, WANG Q.Research progress on the application of casing in sausage[J].Food Research and Development, 2022, 43(2):220-224.
[2] HOU B Y, WANG B J, WENG Y M.Transglutaminase cross-linked and lysozyme-incorporated antimicrobial tilapia collagen edible films:Development and characterization[J].Foods, 2023, 12(7):1475.
[3] 徐金龙. 胶原纤维可食用膜的机械性能改善策略及相关机制[D].无锡:江南大学, 2021.XU J L.Improving strategies and related mechanisms for mechanical properties of collagen fiber edible film[D].Wuxi:Jiangnan University, 2021.
[4] LIU Z Q, TUO F Y, SONG L, et al.Action of trypsin on structural changes of collagen fibres from sea cucumber (Stichopus japonicus)[J].Food Chemistry, 2018, 256:113-118.
[5] MA C Y, WANG H T, CHI Y J, et al.Preparation of oriented collagen fiber scaffolds and its application in bone tissue engineering[J].Applied Materials Today, 2021, 22:100902.
[6] RAN R M, XIONG Y M, ZHENG T T, et al.Active and intelligent collagen films containing laccase-catalyzed mulberry extract and Pickering emulsion for fish preservation and freshness indicator[J].Food Hydrocolloids, 2024, 147:109326.
[7] TANG P P, LI X, LI H Y, et al.Development of active film based on collagen and hydroxypropyl methylcellulose incorporating apple polyphenol for food packaging[J].International Journal of Biological Macromolecules, 2024, 273:132960.
[8] LI Y S, YANG J X, SUN L P, et al.Crosslinked fish scale gelatin/alginate dialdehyde functional films incorporated with carbon dots derived from pomelo peel waste for active food packaging[J].International Journal of Biological Macromolecules, 2023, 253(P6):127290.
[9] ANDONEGI M, DE LA CABA K, GUERRERO P.Effect of citric acid on collagen sheets processed by compression[J].Food Hydrocolloids, 2020, 100:105427.
[10] DE GUZZI PLEPIS A M, GOISSIS G, DAS-GUPTA D K.Dielectric and pyroelectric characterization of anionic and native collagen[J].Polymer Engineering &Science, 1996, 36(24):2932-2938.
[11] ZHANG Y H, MA L, CAI L Y, et al.Effects of acid concentration and the UHP pretreatment on the gelatinisation of collagen and the properties of extracted gelatins[J].International Journal of Food Science &Technology, 2016, 51(5):1228-1235.
[12] 吴茜, 刘芳芳, 苗宇, 等.牦牛皮在食品领域的利用现状及应用前景分析[J].食品与发酵工业, 2020, 46(13):305-309.WU Q, LIU F F, MIAO Y, et al.Analysis of utilization status and application prospect of yak skin in food field[J].Food and Fermentation Industries, 2020, 46(13):305-309.
[13] 李天婵, 张松山, 张志胜, 等.3种牛皮加热过程中食用品质变化规律及其胶原蛋白结构差异性[J].肉类研究, 2020, 34(12):18-23.LI T C, ZHANG S S, ZHANG Z S, et al.Changes in eating quality and differences in collagen structure of cattle and yak hide during heating[J].Meat Research, 2020, 34(12):18-23.
[14] XU M Q, WEI L X, XIAO Y C, et al.Molecular structural properties of extracted gelatin from yak skin as analysed based on molecular weight[J].International Journal of Food Properties, 2017, 20(sup1):S543-S555.
[15] 王杉杉, 罗学刚, 苏峰丙, 等.牦牛皮胶原蛋白的提取及性能分析[J].精细化工, 2018, 35(5):830-837.WANG S S, LUO X G, SU F B, et al.Extraction and characterization of collagen from the skin of yak[J].Fine Chemicals, 2018, 35(5):830-837.
[16] 李金, 黄彪, 刘惠考, 等.牦牛胶原蛋白肽降血糖效果研究[J].食品工业科技, 2022, 43(15):338-343.LI J, HUANG B, LIU H K, et al.Study of yak collagen peptides on reducing blood sugar[J].Science and Technology of Food Industry, 2022, 43(15):338-343.
[17] ZHANG F, LIU H T, PANG X Y, et al.Fabrication and characterization of the bio-based nanofiber solid facial mask with moisturizing and antioxidant efficacy[J].Collagen and Leather, 2025, 7:25.
[18] SUURS P, VAN DEN BRAND H, TEN HAVE R T, et al.Evaluation of cattle skin collagen for producing co-extrusion sausage casing[J].Food Hydrocolloids, 2023, 140:108595.
[19] 徐菲菲, 许健, 刘飞, 等.戊二醛添加顺序对胶原蛋白肠衣膜品质的影响[J].食品与生物技术学报, 2022, 41(12):30-39.XU F F, XU J, LIU F, et al.Effect of glutaraldehyde addition sequence on quality of collagen casing films[J].Journal of Food Science and Biotechnology, 2022, 41(12):30-39.
[20] CHEN C, LIU F, YU Z, et al.Improvement in physicochemical properties of collagen casings by glutaraldehyde cross-linking and drying temperature regulating[J].Food Chemistry, 2020, 318:126404.
[21] YAN Z H, DOU R R, WEI F, et al.Effects of eugenol on physicochemical properties of sturgeon skin collagen-chitosan composite membrane[J].Journal of Food Science, 2024, 89(7):4032-4046.
[22] XU J L, LIU F, YU Z, et al.Influence of softwood cellulose fiber and chitosan on the film-forming properties of collagen fiber[J].Food Bioscience, 2021, 42:101056.
[23] ZHU K D, YU Z, LI J, et al.Sodium carboxymethyl cellulose as a stabilizer for fabricating mineralized collagen films with improved wet mechanical properties[J].Food Hydrocolloids, 2024, 150:109676.
[24] PARK J W, SCOTT WHITESIDE W, CHO S Y.Mechanical and water vapor barrier properties of extruded and heat-pressed gelatin films[J].LWT-Food Science and Technology, 2008, 41(4):692-700.
[25] GIOSAFATTO C V L, DI PIERRO P, GUNNING P, et al.Characterization of Citrus pectin edible films containing transglutaminase-modified phaseolin[J].Carbohydrate Polymers, 2014, 106:200-208.
[26] ZAREIE Z, TABATABAEI YAZDI F T, ALI MORTAZAVI S A.Development and characterization of antioxidant and antimicrobial edible films based on chitosan and gamma-aminobutyric acid-rich fermented soy protein[J].Carbohydrate Polymers, 2020, 244:116491.
[27] TANG P P, ZHENG T T, YANG C K, et al.Enhanced physicochemical and functional properties of collagen films cross-linked with laccase oxidized phenolic acids for active edible food packaging[J].Food Chemistry, 2022, 393:133353.
[28] WU J M, LIU F, YU Z, et al.Facile preparation of collagen fiber-glycerol-carboxymethyl cellulose composite film by immersing method[J].Carbohydrate Polymers, 2020, 229:115429.
[29] 胡婧瑶, 李丹, 王明月, 等.无机纳米粒子增强大豆蛋白膜功能特性的比较[J].现代食品科技, 2023, 39(10):244-252.HU J Y, LI D, WANG M Y, et al.Comparison of the functional properties of soy protein isolate films enhanced by inorganic nanoparticles[J].Modern Food Science and Technology, 2023, 39(10):244-252.
[30] 张义. 不同交联剂对胶原蛋白可食膜性能的影响[D].天津:天津科技大学, 2016.ZHANG Y.Influence of different crosslinking agents on properties of edible collagen film[D], Tianjin:Tianjin University of Science and Technology, 2016.
[31] 胡可欣. 漆酶/没食子酸协同催化交联胶原制备可食用膜的研究[D].成都:四川大学, 2021.HU K X.Study on preparation of edible membrane by crosslinking collagen catalyzed by laccase/gallic acid[D], Chengdu:Sichuan University, 2021.
[32] WU X M, LIU A J, WANG W H, et al.Improved mechanical properties and thermal-stability of collagen fiber based film by crosslinking with casein, keratin or SPI:Effect of crosslinking process and concentrations of proteins[J].International Journal of Biological Macromolecules, 2018, 109:1319-1328.
[33] MISRA N N, KAUR S, TIWARI B K, et al. Atmospheric pressure cold plasma (ACP) treatment of wheat flour[J]. Food Hydrocolloids, 2015, 44: 115-121.
[34] WU X M, LIU Y W, LIU A J, et al.Improved thermal-stability and mechanical properties of type I collagen by crosslinking with casein, keratin and soy protein isolate using transglutaminase[J].International Journal of Biological Macromolecules, 2017, 98:292-301.
[35] WANG W H, ZHANG X L, LI C, et al.Using carboxylated cellulose nanofibers to enhance mechanical and barrier properties of collagen fiber film by electrostatic interaction[J].Journal of the Science of Food and Agriculture, 2018, 98(8):3089-3097.