花鲈(Lateolabrax maculatus),隶属鲈形目、鮨科、花鲈属[1],作为我国重要海水养殖鱼种,2023年产量达24.69万t,位居全国前三[2]。其鱼肉富含高生物价蛋白,必需氨基酸含量占比高达42.3%,其中赖氨酸与亮氨酸含量尤为突出。同时,长链多不饱和脂肪酸二十碳五烯酸和二十二碳六烯酸含量之和超过总脂肪酸的10%,亚油酸比例高达27%,显著优于多数常见食用鱼种[3]。此外,花鲈天然富集多种维生素及硒等必需微量营养素,结合传统中医药学理论所阐释的“补肝肾、益脾胃”食补功效,使其成为开发高营养鱼糜制品的理想原料。
鱼糜制品是以鱼肉为原料,经漂洗、脱水、斩拌及热诱导凝胶化等工艺加工而成的蛋白凝胶网络体系[4],其品质核心源于肌原纤维蛋白通过分子间交联形成的三维网络结构[5]。随着消费者对高蛋白低脂健康食品需求的增长,我国鱼糜产业已形成规模化发展格局,成为水产加工领域的重要支柱[2]。在传统鱼糜生产中,漂洗作为关键工序可有效去除水溶性蛋白、色素及脂质,显著改善鱼糜凝胶性能,但不可避免地造成鱼肉中多不饱和脂肪酸的同步流失,从而降低鱼糜的营养价值。针对这一痛点,外源添加物的引入已成为品质改良的重要研究方向。现有研究表明,植物性成分的添加可通过物理填充、化学交联等机制改善鱼糜凝胶特性。DEBUSCA等[6]证实膳食纤维能改善鱼糜凝胶质地,同时与鱼糜凝胶基质中的蛋白质进行化学键合来稳定水。GUO等[7]发现酚类物质能诱导肌原纤维蛋白通过巯基或氨基去折叠并促进交联,从而提高凝胶性能。HUANG等[8]指出木薯淀粉通过增强凝胶系统中的氢键和疏水相互作用,改善鱼糜的凝胶强度。
钦州海红米,又称“药稻”,是钦州地区的一种特色功能稻米,其糙米皮层富含花青素、花色苷等抗氧化活性物质,研究显示,花色苷可有效提高超氧化物歧化酶与谷胱甘肽过氧化物酶等抗氧化酶的活性,进而延缓细胞氧化应激损伤[9]。钟凯翠等[10]基于海红米花色苷开发复合饮料,证实了其在动物模型研究中可显著改善模型小鼠的高血糖状态、缓解胰岛素抵抗并减轻相关组织病理损伤,充分展现出海红米的潜在食疗价值。此外,海红米以淀粉为主要成分,蛋白质含量可达11%,且富含多种微量元素[11-12]。这些特性预示其在鱼糜体系中兼具质构改良与营养强化的应用潜力。然而,目前关于海红米全粉(sea red rice powder,SRRP)对鱼糜体系的影响尚未见系统报道,其与鱼糜蛋白的相互作用机制,以及对凝胶网络结构、水分分布、抗氧化活性等的调控作用仍有待深入探索。
基于此,本研究以花鲈鱼糜为载体,系统探究海红米添加量(0%~10%,质量分数,下同)对鱼糜白度值、凝胶强度、持水性、蒸煮损失率、流变特性等理化指标的影响,通过红外光谱揭示其对肌原纤维蛋白二级结构的调控机制。同时,结合体外抗氧化实验综合评价海红米对鱼糜抗氧化能力的影响。研究结果不仅能拓展功能性稻米资源高值化利用的新途径,也将为开发兼具质构改良与营养强化的新型鱼糜制品提供理论依据。
1 材料与方法
1.1 材料与试剂
海红米、花鲈,钦州市购;DPPH溶液、ABTS,Phygene生物科技有限公司;水杨酸、氯化钠等试剂,上海麦克林生化科技股份有限公司。
1.2 仪器与设备
SMF2004研磨机,苏泊尔股份有限公司;CT3质构仪,美国Brookfield公司;BTP-3ES00X冷冻干燥机,美国Virtis公司;PD500高速匀浆分散机,上海戈普仪器有限公司;TGL-16M高速台式冷冻离心机,湖南湘仪实验室仪器开发有限公司;LMR-30低场核磁共振分析仪,北京拉莫尔科技发展有限公司;CM-2600D色差仪,日本柯尼卡美能达控股公司;DHR-2流变仪,美国TA公司;Nicolet iS5傅里叶变换红外光谱仪、Evolution 201紫外分光光度计、Apreo 2 SEM场发射扫描电镜,美国赛默飞世尔科技公司。
1.3 实验方法
1.3.1 海红米粉的制备
将海红米粉碎后过120目筛(孔径0.125 mm),得到SRRP。
1.3.2 花鲈海红米复合凝胶的制备
参照曾泽政等[13]的方法,略作改动。将新鲜花鲈宰杀取肉,吸去表面水分,切成小块后放入斩拌机斩拌2 min,加入鱼肉质量1.5%的NaCl,同时加入鱼肉质量5%的去离子冰水,进行第2次斩拌,时间为2 min,取6组100 g鱼肉分别加入鱼肉质量0%(对照)、2%、4%、6%、8%、10%的SRRP,再次斩拌2 min,全程温度控制在10 ℃以下。将斩拌完成的鱼糜溶胶注入直径30 mm的塑料肠衣中,密封两端,采用两段式加热工艺(45 ℃加热30 min,90 ℃加热30 min)进行熟制。将熟制后的鱼糜复合凝胶置于冰水中冷却15 min,随后剥离肠衣于4 ℃冰箱冷藏,供后续指标检测。具体见图1。

图1 技术路线图
Fig.1 Technical route diagram
1.3.3 白度值(W)测定
使用校准后的色差仪测定鱼糜凝胶样品的L*、a*和b*值。凝胶白度W值的计算如公式(1)所示:
(1)
式中:L*,鱼糜的亮度值;a*,鱼糜的红/绿度值;b*,鱼糜的黄/蓝度值。
1.3.4 质构参数测定
将鱼糜凝胶制成直径30 mm、高25 mm的圆柱形样品,于室温条件下静置平衡30 min,使用CT3型质构仪测定样品凝胶强度。采用TA/5柱形探头,测试条件设定为:质地多面剖析模式、测试速度1 mm/s、压缩比50%、触发力10 g。选取硬度、弹性、内聚性、胶着性和咀嚼性为全质构(texture profile analysis,TPA)参数。
1.3.5 凝胶强度测定
参照朱士臣等[14]的方法,略作改动。将鱼糜凝胶制成直径30 mm、高25 mm的圆柱形样品,于室温条件下静置平衡30 min,使用CT3型质构仪测定样品凝胶强度。采用TA/18球形探头,测试条件设定为:压缩模式、测试速度1 mm/s、下压距离15 mm、触发力10 g。将曲线上获得的第一个峰值定义为破断强度,其对应距离定义为破断距离。凝胶强度为破断强度(g)与破断距离(mm)的乘积。
1.3.6 感官评价
鱼糜凝胶的感官评价由8名食品专业学生组成的评价小组完成。
小组成员(年龄20~25岁,男女各4人)均熟悉鱼糜制品特性。依据表1所列标准,对样品的色泽、气味、口感及组织状态进行评分。
表1 鱼糜感官评价标准
Table 1 Sensory evaluation criteria for surimi

项目评分标准等级呈现诱人、自然的红褐色或乳白色,色泽高度均匀,富有光泽,无粉状聚集色斑优(18~20分)色泽(20分)呈现红褐色或乳白色,色泽较均匀,有一定光泽,无明显色斑或颜色分层良(14~17分)颜色暗淡(偏灰、偏褐),均匀性一般,光泽度差,或有轻微色斑/颜色不均现象中(7~13分)颜色异常(如发黑、发绿),或极其暗淡无光,或存在明显色斑、颜色分层差(0~6分)具有浓郁的花鲈鲜香味和清晰的海红米谷物香味,二者融合协调,气味愉悦,无粉味优(18~20分)气味(20分)具有较明显的花鲈鲜香和海红米谷物香,气味较协调,无异味,粉味极微弱或不明显良(14~17分)鱼腥味或海红米味其一占主导,或两者皆不明显,气味平淡,或能感觉到轻微粉味中(7~13分)鱼腥味过重,或海红米味令人不悦(如陈味、哈喇味),或有明显异味(酸败、氨味等),或有明显粉味差(0~6分)质地极佳:弹性足、脆性好、韧性适中,硬度适宜,口感细腻润滑,无粉质感、无砂砾感、无粘牙感优(25~30分)口感(30分)质地良好:弹性、脆性、韧性较好,硬度稍偏硬或稍软;粉质感极微弱或不明显,基本无粘牙感良(18~24分)质地一般:弹性、脆性较弱,偏硬或偏软;能感觉到轻微粉质感、略有砂砾感、或轻微粘牙中(10~17分)质地差:缺乏弹性脆性,过硬、过软、过粘或松散;有明显粉质感、砂砾感、糊或严重粘牙差(0~9分)凝胶结构致密、均匀、强韧;切面极其光滑细腻;粉末完全分散,无任何粉体聚集、色斑;无明显可见气泡优(25~30分)组织状态(30分)凝胶结构较致密均匀;切面较光滑;粉末分散均匀,偶见极细微色点,无聚集;有少量细小气泡良(18~24分)凝胶结构不够致密,略有粗糙感;切面可见轻微不平整;可见少量细微色点;有可见气泡中(10~17分)凝胶结构松散、粗糙、多气孔或易碎;切面粗糙;有明显色斑或粉体聚集现象;产品分层、未形成有效凝胶差(0~9分)
1.3.7 持水性测定
将约2 g形状大小相近的完整鱼糜凝胶样品用3层滤纸包裹后置于25 mL离心管中。以6 000 r/min离心15 min,结束后小心移除包裹的滤纸并再次称重。鱼糜凝胶持水性的计算如公式(2)所示:
持水性![]()
(2)
式中:W1,鱼糜凝胶取样质量,g;W2,离心后鱼糜凝胶质量,g。
1.3.8 蒸煮损失率测定
制备直径3 cm、高度0.5 cm(质量约5 g)的鱼糜凝胶圆柱体样品,记录其初始质量。将该样品装入蒸煮袋,抽真空密封,置于沸水中蒸煮10 min后取出。用滤纸吸除样品表面水分,随后称量其质量。鱼糜凝胶蒸煮损失率的计算如公式(3)所示:
蒸煮损失率![]()
(3)
式中:M1,鱼糜凝胶取样量,g;M2,蒸煮后鱼糜凝胶质量,g。
1.3.9 水分分布测定
取约10 g鱼糜凝胶样品平衡至32 ℃后,置入低场核磁共振(low field nuclear magnetic resonance,LF-NMR)检测瓶内。采用CPMG(carr-purcell-meiboom-gill)序列测量其横向弛豫时间(T2)。参数设置为:SFI=7 MHz、P1=14.3 μs、SW=200.00 kHz、NS=8、P2=25.8 μs、TW=6 000 ms、TE=0.20 ms、NECH=20 000。
1.3.10 动态流变学特性测定
取样2 g鱼糜溶胶样品置于流变仪载物台,安装PP25探头并调整板间距至1 mm,进行温度扫描。参数设定为:温度范围25~90 ℃、升温速率5 ℃/min、剪切应变1%、角频率10 rad/s。测定样品的储能模量(G′)和损耗模量(G″)。
1.3.11 蛋白质的二级结构测定
使用傅里叶变换红外光谱(Fourier transform infrared spectroscopy, FTIR)对鱼糜凝胶的蛋白质二级结构进行分析。将真空冷冻干燥磨碎后的鱼糜凝胶粉末与溴化钾以1∶100比例混匀,充分研磨均匀后置于压片机下压成透明薄片。在400~4 000 cm-1波数内进行32次扫描,分辨率为8 cm-1。
1.3.12 微观结构测定
将鱼糜凝胶制成5 mm×5 mm×5 mm的正方体小块,用质量分数为2.5%的戊二醛溶液在4 ℃下浸泡固定过夜,用磷酸缓液冲洗3次,每次10 min。之后依次使用体积分数为50%、70%、80%、95%的乙醇溶液及无水乙醇各洗脱20 min。处理后的样品进行真空冷冻干燥。干燥后的样品用导电胶带固定在扫描电镜样品台上,喷金后,置于扫描电镜下,在5 kV电压下分别放大80倍和500倍观察样品微观结构。
1.3.13 抗氧化活性测定[15]
取2 g鱼糜样品置于烧杯中,加入10 mL去离子水均质,37 ℃下浸提1 h后6 000 r/min离心10 min取上清液记为S1,在残渣中加入10 mL的95%(体积分数)乙醇均质,37 ℃下浸提1 h,6 000 r/min离心10 min取上清液记为S2,合并S1和S2并用去离子水定容至50 mL,得到样品稀释液。
1.3.13.1 DPPH自由基清除率
取2 mL稀释液于试管中加入1 mL浓度为0.2 mmol/L的DPPH乙醇溶液混匀,避光反应30 min后,DPPH自由基清除率的计算如公式(4)所示:
DPPH自由基清除率![]()
(4)
式中:A0,使用蒸馏水代替样品稀释液的吸光度;A1,样品与DPPH反应后的吸光度;A2,以无水乙醇代替DPPH的吸光度。
1.3.13.2 羟自由基清除率
依次将1 mL样品稀释液、1 mL 6 mmol/L FeSO4和1 mL 6 mmol/L H2O2溶液加入试管中,充分混匀后静置10 min,加入1 mL 6 mmol/L水杨酸溶液,在室温下静置反应30 min,于510 nm处测定吸光值。羟自由基清除率的计算如公式(5)所示:
羟自由基清除率![]()
(5)
式中:A0,使用去离子水代替样品稀释液的吸光度;A1,样品与H2O2反应后的吸光度;A2,以去离子水代替H2O2的吸光度。
1.3.13.3 ABTS阳离子自由基清除率
将浓度为7 mmol/L的ABTS溶液与2.4 mmol/L的过硫酸钾溶液按1∶1体积比充分混合。混合液于室温下避光静置反应12 h,得到储备液,用磷酸盐缓冲液(pH=7.4)将其释至在734 nm处吸光值为0.75±0.02,得到ABTS测试液,取0.1 mL稀释液于试管中加入2 mL 的ABTS测试液混匀,避光反应10 min,于波长734 nm处测定吸光度,ABTS阳离子自由基清除率的计算如公式(6)所示:
ABTS阳离子自由基清除率![]()
(6)
式中:A0,使用去离子水代替样品稀释液的吸光度;A1,样品与ABTS溶液反应后的吸光度;A2,以磷酸盐缓冲液代替ABTS后的吸光度。
1.4 数据统计与分析
实验独立重复3次,数据结果以“平均值±标准差”表示。实验数据分析采用SPSS 27软件,图表制作采用Origin 2021软件,相关性分析使用Matlab软件。同一指标数据若标注不同字母,即表示组间差异达到统计学显著性水平(P<0.05)。
2 结果与分析
2.1 W值分析
白度是评价鱼糜制品品质的关键视觉指标,其优劣直接关系到产品的可接受度。如表2所示,随着SRRP添加量的增加(0%~10%),鱼糜L*值逐渐变暗,同时a*值和b*显著上升(P<0.05),导致W值持续降低。RAWDKUEN等[16]的研究表明,添加剂的颜色和数量是决定鱼糜制品白度的关键影响因素。由于海红米中富含花青素,其固有的高a*、b*值属性在均匀分散至鱼糜凝胶后,显著影响了鱼糜的颜色,形成剂量依赖性的色泽加深效应,当添加量达10%时,W值(58.56)较对照组(76.69)下降23.6%,直观表现为鱼糜由乳白色渐变为浅褐色(图2)。
表2 SRRP对鱼糜白度值的影响
Table 2 The effect of SRRP on whiteness value of surimi
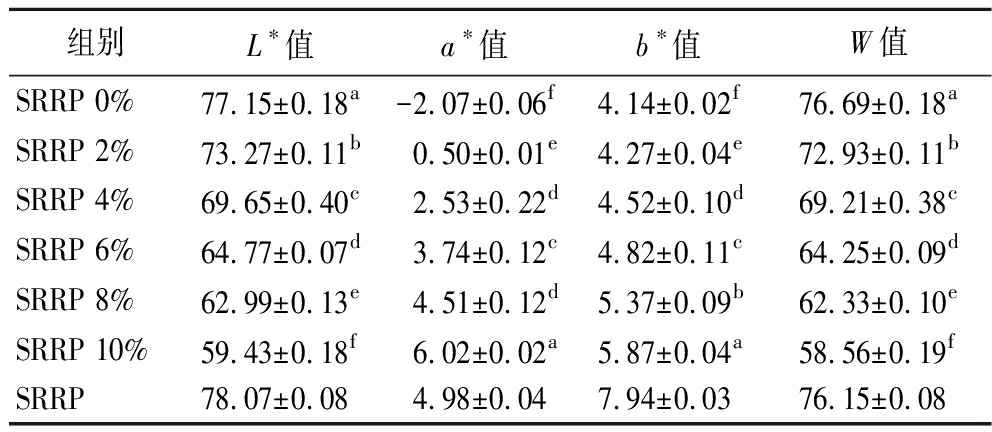
组别L∗值a∗值b∗值W值SRRP 0%77.15±0.18a-2.07±0.06f4.14±0.02f76.69±0.18aSRRP 2%73.27±0.11b0.50±0.01e4.27±0.04e72.93±0.11bSRRP 4%69.65±0.40c2.53±0.22d4.52±0.10d69.21±0.38cSRRP 6%64.77±0.07d3.74±0.12c4.82±0.11c64.25±0.09dSRRP 8%62.99±0.13e4.51±0.12d5.37±0.09b62.33±0.10eSRRP 10%59.43±0.18f6.02±0.02a5.87±0.04a58.56±0.19fSRRP78.07±0.084.98±0.047.94±0.0376.15±0.08
注:同列数据肩标相同字母表示差异不显著(P>0.05),不同字母表示差异显著(P<0.05)(下同)。

图2 不同SRRP添加量鱼糜图片
Fig.2 Images of surimi with different SRRP addition levels
2.2 质构参数分析
TPA分析通过特定探头对样品进行穿刺挤压,以模拟人口腔对食物的加工行为,来定量表征鱼糜凝胶的感官品质。其中硬度是探头进行第一压缩周期的峰值力;弹性表现为第一次压缩变形后的回弹程度;内聚性为抗二次变形能力,在一定程度上能够反映鱼糜凝胶结构的致密程度;咀嚼性为口腔破碎凝胶所需能量[17]。如表3所示,海红米全粉添加量对鱼糜的各项质构特性产生了显著影响(P<0.05),随着添加量的增加(0%~10%),鱼糜的硬度从2 317.67 g升至3 580.33 g,咀嚼性由173.03 mJ增至251.97 mJ,分别提升了54.5%和45.6%,但内聚性无显著性变化(P<0.05),而弹性在6%添加量时达峰值,6%~10%间维持稳定。
表3 SRRP对鱼糜TPA参数的影响
Table 3 The effect of SRRP on the TPA parameters of surimi
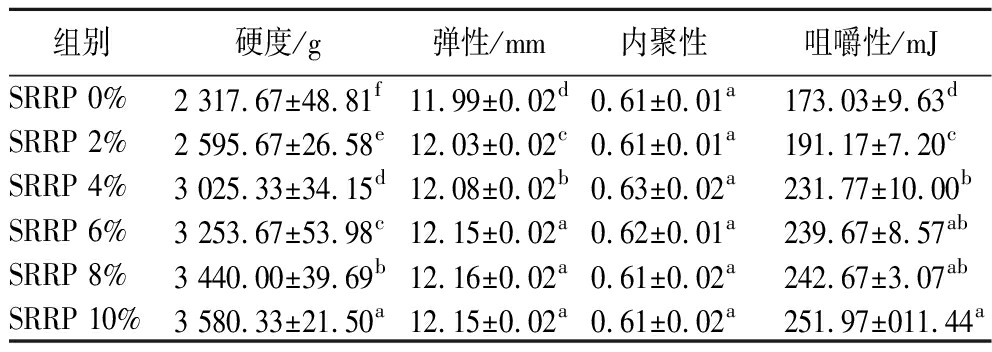
组别硬度/g弹性/mm内聚性咀嚼性/mJSRRP 0%2 317.67±48.81f11.99±0.02d0.61±0.01a173.03±9.63dSRRP 2%2 595.67±26.58e12.03±0.02c0.61±0.01a191.17±7.20cSRRP 4%3 025.33±34.15d12.08±0.02b0.63±0.02a231.77±10.00bSRRP 6%3 253.67±53.98c12.15±0.02a0.62±0.01a239.67±8.57abSRRP 8%3 440.00±39.69b12.16±0.02a0.61±0.02a242.67±3.07abSRRP 10%3 580.33±21.50a12.15±0.02a0.61±0.02a251.97±011.44a
凝胶强度表示鱼糜凝胶基质抵抗破裂的综合能力,其值为破断强度(g)与破断距离(mm)的乘积,直接反映凝胶交联网络的稳定性[18]。如图3所示,在添加量为0%~10%时,破断强度和破断距离与SRRP添加量呈显著正相关(P<0.05),当添加量达到10%时,凝胶强度相比对照组提升了79.6%,这与MI等[19]的研究结果类似,主要是由于海红米的高淀粉含量,在加热过程中与蛋白质竞争性结合水分吸水膨胀,迫使鱼糜蛋白质紧密交联,形成强度更高的凝胶网络结构,从而带来质构特性的提升[15]。
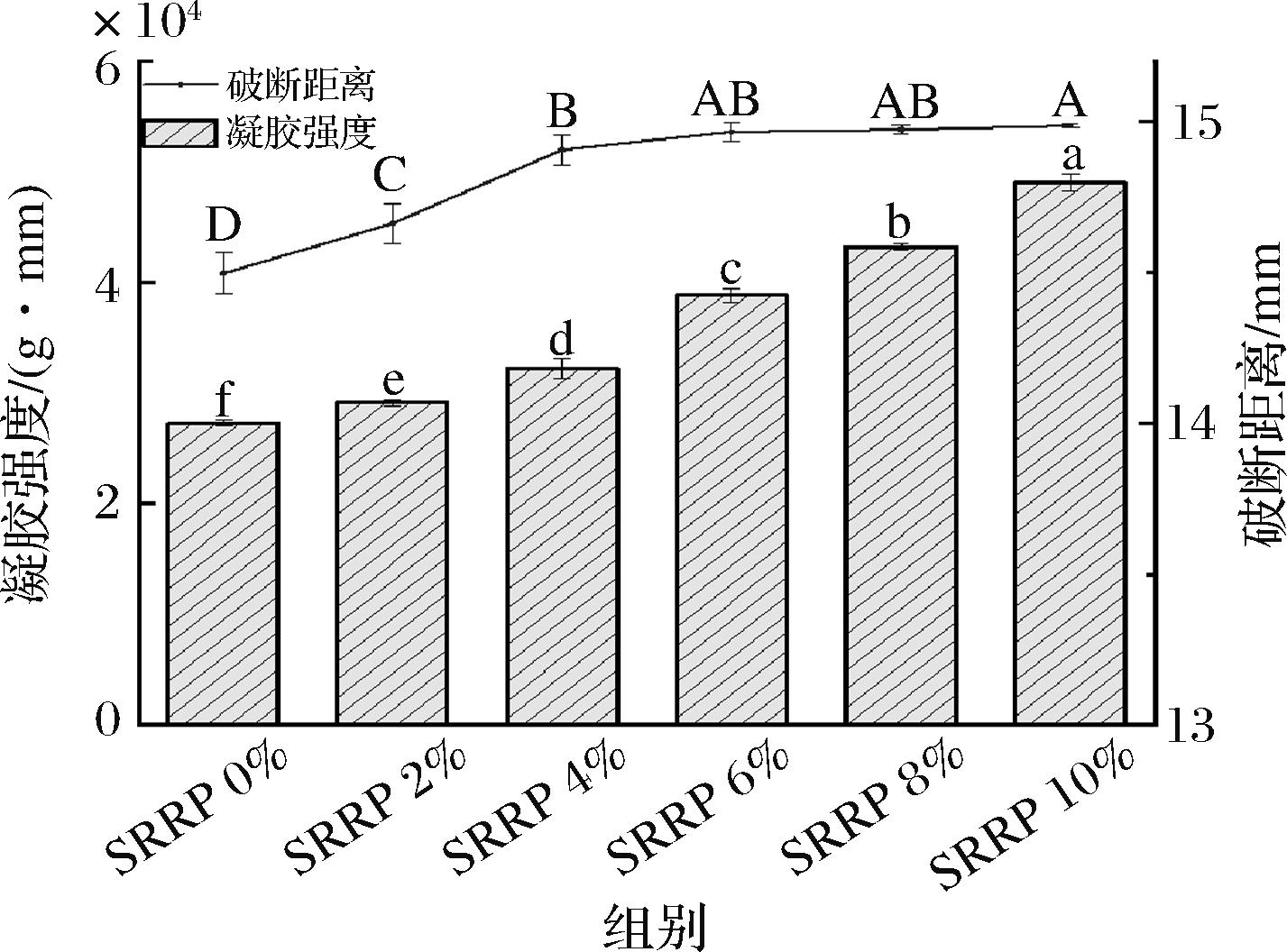
图3 SRRP对鱼糜凝胶强度及破断距离的影响
Fig.3 The effect of SRRP on the gel strength and rupture distance of surimi
注:图中相同字母表示差异不显著(P>0.05),不同字母表示差异显著(P<0.05)(下同)。
2.3 感官评价分析
感官评分是评价鱼糜制品品质的重要方法,直接反映消费者对产品的喜好程度。如表4所示,随着SRRP添加量的增加,色泽评分呈显著下降趋势(P<0.05),感官评价人员表示亮度逐渐变暗是导致其评分降低的关键因素,这与2.1节W值分析中观察到的中L*值的逐渐降低结果一致。在气味方面,评分呈现出先升高后降低的趋势,SRRP的添加赋予了鱼糜一定的去腥效果,同时带来一些海红米特有的谷物香气,在添加量8%达到最高分(15.88分),相比对照组提升122.72%,但10%的SRRP添加量带来了微弱的粉味,导致评分降低。口感方面,0%~6%的添加量范围内口感逐渐改善,在6%达到最高分(26.75分),而8%~10%的添加量反而使鱼糜口感过硬,导致评分降低,这与2.2节质构分析中所得结果一致。组织状态方面,各添加组评分则均低于对照组,但组间差异不显著(P<0.05),推测与SRRP中淀粉在加热过程中吸水膨胀使鱼糜切面不平滑有关。综上,在感官总分方面,6%的SRRP添加量时花鲈鱼糜总分达到80.75分,较对照组提升8分。结果表明,SRRP的适量添加能改善花鲈鱼糜的感官品质,提高消费者接受度。
表4 SRRP对鱼糜感官评分的影响
Table 4 The effect of SRRP on the sensory score of surimi
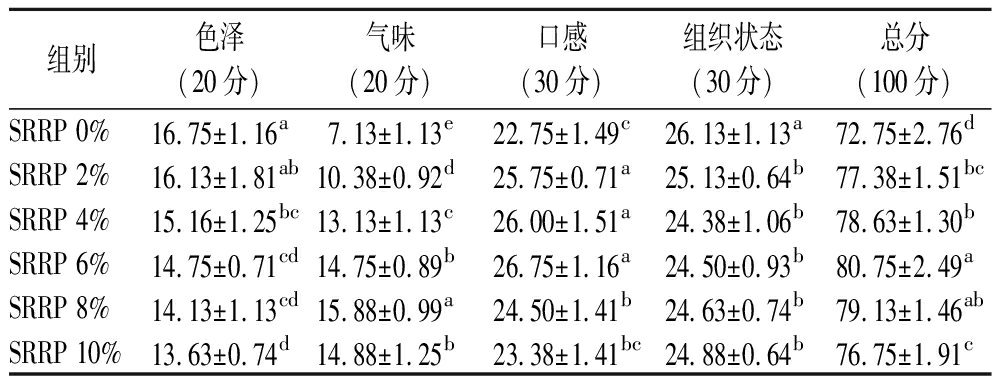
组别色泽(20分)气味(20分)口感(30分)组织状态(30分)总分(100分)SRRP 0%16.75±1.16a7.13±1.13e22.75±1.49c26.13±1.13a72.75±2.76dSRRP 2%16.13±1.81ab10.38±0.92d25.75±0.71a25.13±0.64b77.38±1.51bcSRRP 4%15.16±1.25bc13.13±1.13c26.00±1.51a24.38±1.06b78.63±1.30bSRRP 6%14.75±0.71cd14.75±0.89b26.75±1.16a24.50±0.93b80.75±2.49aSRRP 8%14.13±1.13cd15.88±0.99a24.50±1.41b24.63±0.74b79.13±1.46abSRRP 10%13.63±0.74d14.88±1.25b23.38±1.41bc24.88±0.64b76.75±1.91c
2.4 持水性分析
作为衡量鱼糜品质的核心指标,持水性本质上反映了凝胶网络通过物理截留与化学作用对水分的束缚能力[20]。如图4所示,随着SRRP的添加,鱼糜持水性呈现出显著提升趋势,添加2%时持水性提升最大,此后增速放缓。当添加量达到10%时,从对照组的87.49%提升到了95.17%。这主要归因于海红米中的淀粉等成分与鱼糜蛋白的协同作用—形成淀粉-蛋白复合凝胶网络结构,增大界面面积并形成更多水分截留位点,有效提升水分束缚能力[21]。
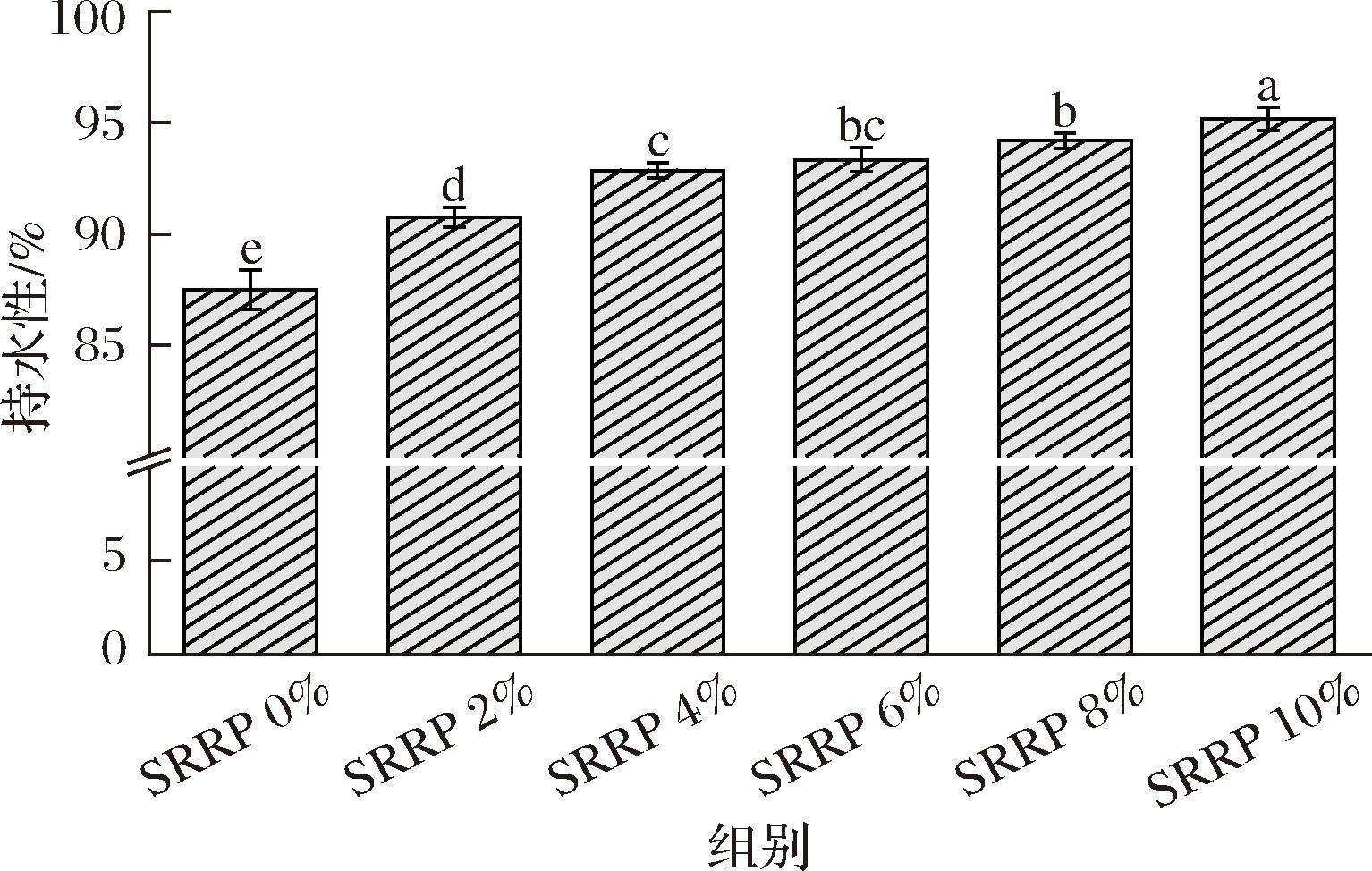
图4 SRRP对鱼糜持水性的影响
Fig.4 The effect of SRRP on the water holding capacity of surimi
2.5 蒸煮损失率分析
蒸煮损失率表示鱼糜内含物质在蒸煮过程中损失的质量占比,直接反映凝胶网络结构对汁液的固定能力,一般持水性越高,蒸煮损失率越低[22]。由图5中可以看出,随着SRRP添加量的增加,蒸煮损失率呈现出先降低后稳定的变化规律,在添加量为0%~6%时显著降低(P<0.05),6%~10%时趋于平稳,8%添加量时降至最低,为3.34%,相对对照组降低了31.11%,表明海红米粉的添加能显著改善花鲈鱼糜的蒸煮损失,但可能存在阈值效应。结合持水性的结果来看,海红米对花鲈鱼糜中水分固定起到显著效果,归因于海红米中高支链淀粉含量,其高度分支的分子结构吸水膨胀后形成连续胶体相,通过分子间相互作用与鱼糜肌原纤维蛋白形成复合凝胶网络,从而增强水分束缚能力。类似地,HUANG等[8]的研究指出热处理时淀粉颗粒吸水膨胀挤压凝胶基质以增强鱼糜保水性,尤以高支链淀粉为甚,若其结构受损则支链淀粉裂解并暴露更多羟基,进一步强化水分束缚能力。
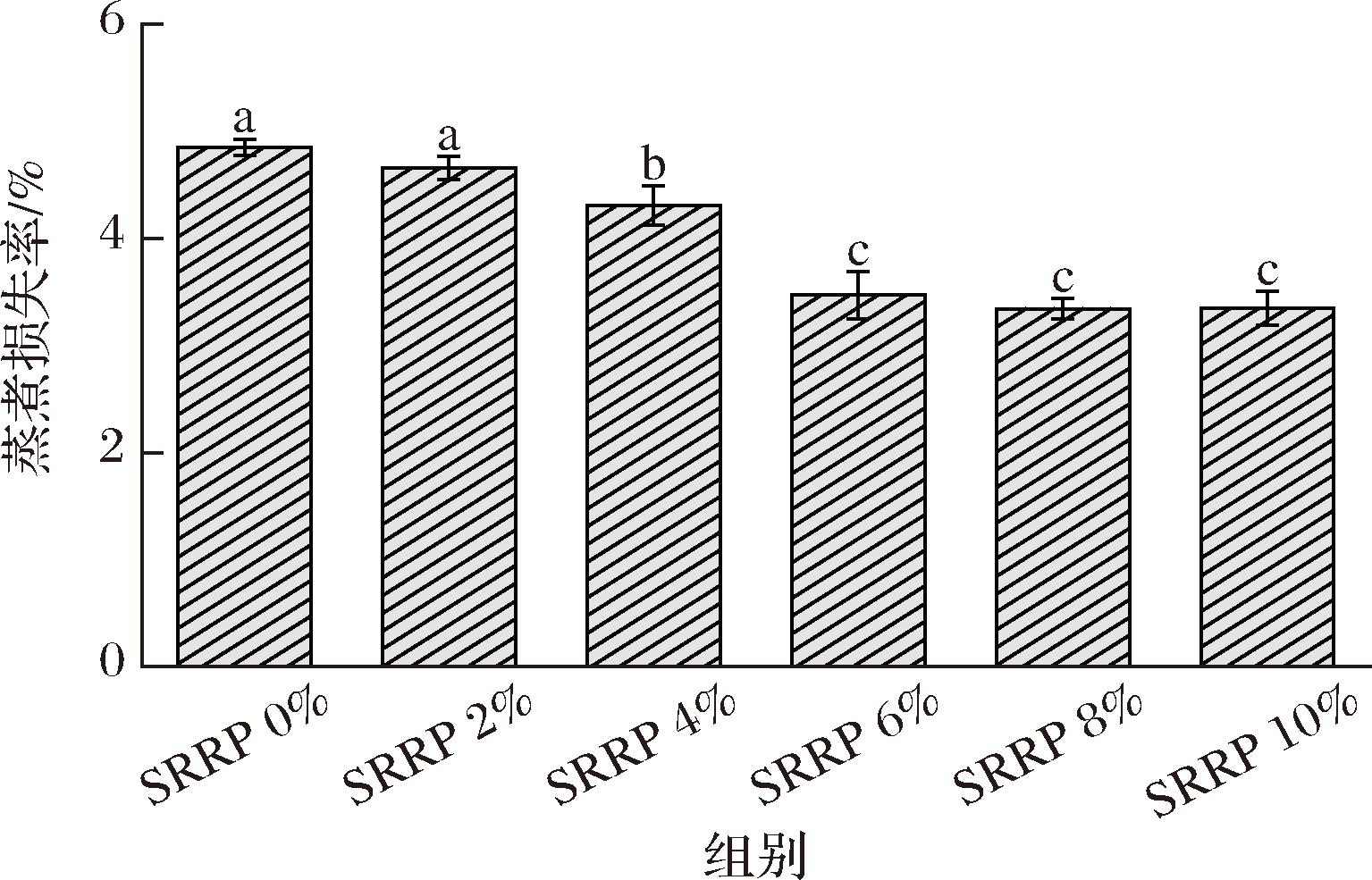
图5 SRRP对鱼糜蒸煮损失率的影响
Fig.5 The effect of SRRP on the cooking loss rate of surimi
2.6 水分分布分析
基于LF-NMR技术,通过CPMG脉冲序列解析鱼糜凝胶内部水分动态特性,其反演拟合生成的横向弛豫时间(T2)分布图谱可定量表征鱼糜内部水分存在状态及受限程度[23]。T2值越小,表明氢质子所处微环境的束缚作用越强,对应水分稳定性越高。将数据归一后制图,如图6所示,各组鱼糜凝胶T2图谱均呈现出3个特征峰,分别代表3种不同水分状态。具体表示为,T21(0~10 ms):结合水,迁移能力极低;T22(10~150 ms):不易流动水,截留于鱼糜复合凝胶网络结构中的水分,受三维网络空间位阻制约,是鱼糜凝胶中最主要的水分;T23(150~1 000 ms):自由水,不受鱼糜凝胶网络结构限制,流动性强[24]。
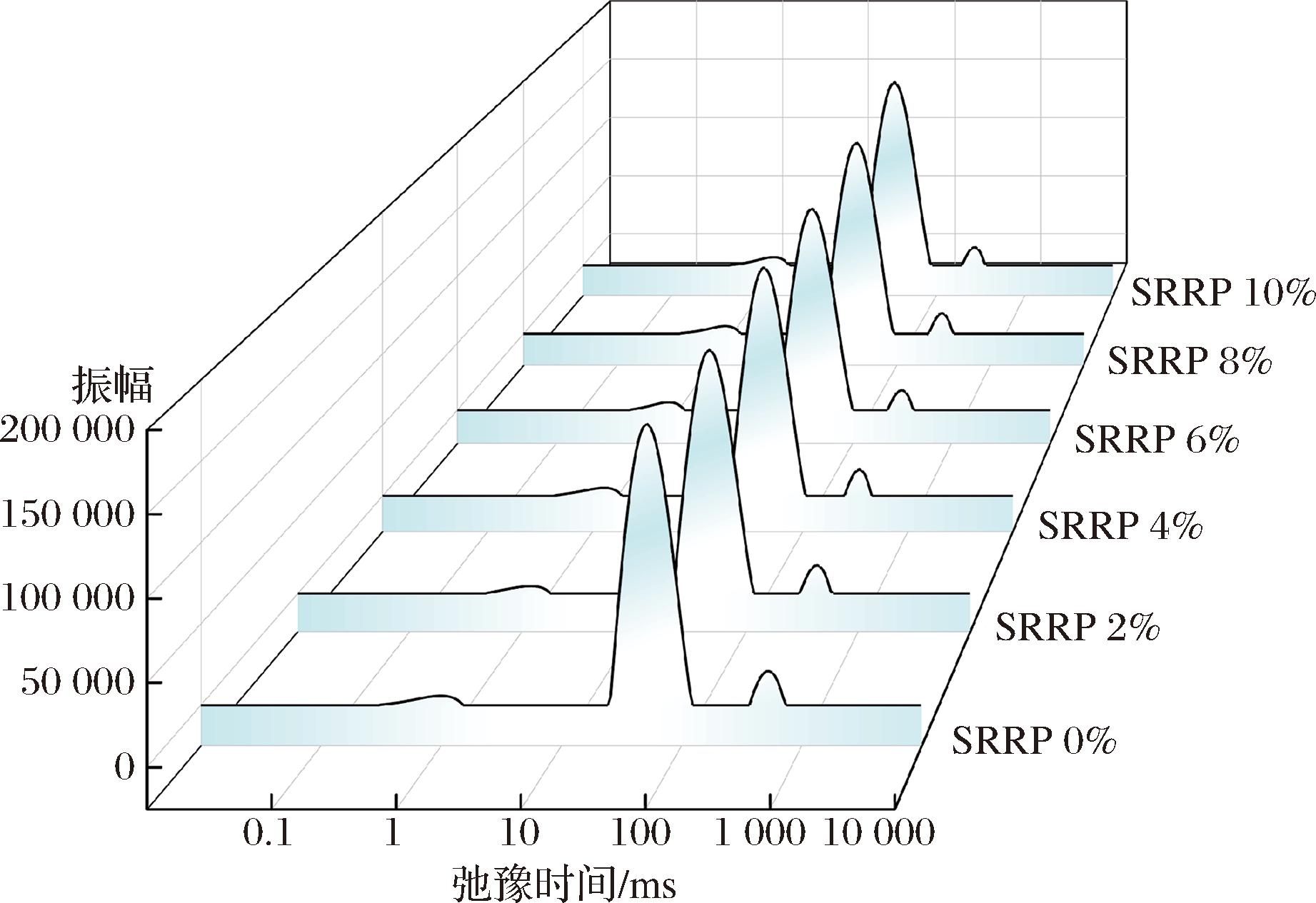
图6 SRRP对鱼糜T2弛豫时间的影响
Fig.6 The effect of SRRP on T2 relaxation time of surimi
不同SRRP添加量的鱼糜凝胶相应峰的峰值对应的T2弛豫时间不同,通过对比其T2弛豫时间可以比较SRRP对不同状态水分的影响。如表5所示,T22、T23随着SRRP添加量的增加(0%~10%)显著缩短(P<0.05),分别由对照组的53.17、556.21 ms降至33.87、265.43 ms,表明SRRP的添加显著增强了鱼糜凝胶对不易流动水及自由水的束缚能力,这主要归因于SRRP添加后形成的淀粉-蛋白质复合凝胶网络。该网络的形成涉及淀粉分子链上的大量亲水性羟基与肌原纤维蛋白侧链上的极性基团之间形成的密集氢键网络,提供了更多与水分子的结合位点[8],将自由水及不易流动水有效捕获并固定,从而限制了其运动。而T21略有延长的原因,可能与复合网络形成后局部微环境的极性或氢键模式发生细微调整有关,使得结合水的运动自由度略有增加,但其核心结合状态并未被破坏。
表5 SRRP对鱼糜3个峰的峰值对应的T2弛豫时间的影响
Table 5 Effects of SRRP on T2 relaxation time corresponding to three peaks of surimi
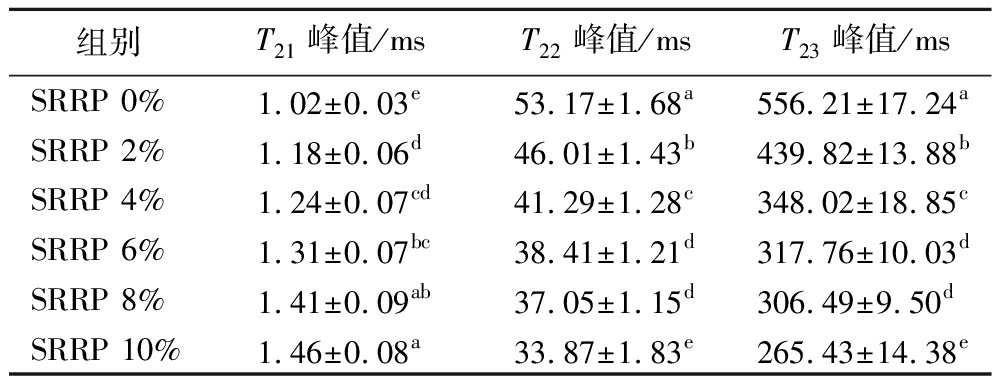
组别T21峰值/msT22峰值/msT23峰值/msSRRP 0%1.02±0.03e53.17±1.68a556.21±17.24aSRRP 2%1.18±0.06d46.01±1.43b439.82±13.88bSRRP 4%1.24±0.07cd41.29±1.28c348.02±18.85cSRRP 6%1.31±0.07bc38.41±1.21d317.76±10.03dSRRP 8%1.41±0.09ab37.05±1.15d306.49±9.50dSRRP 10%1.46±0.08a33.87±1.83e265.43±14.38e
谱峰所对应的各离散点的纵坐标求和值为相应状态水分的信号强度,与总信号强度之比为该状态水在总水分中的占比。如图7所示,随着SRRP添加量增加,自由水占比从5.23%显著降至3.46%,而不易流动水占比在总体上呈现出上升趋势,这一现象表明SRRP中的淀粉在加热过程中吸水膨胀,构建淀粉-蛋白复合凝胶网络,有效地将自由水捕获并固定,使其转变为受三维网络结构制约的不易流动水。不易流动水因受网络束缚难以在离心或蒸煮过程中流失,直接体现为凝胶体系持水能力的增强及蒸煮损失的减少,这与2.4节、2.5节中结果对应。
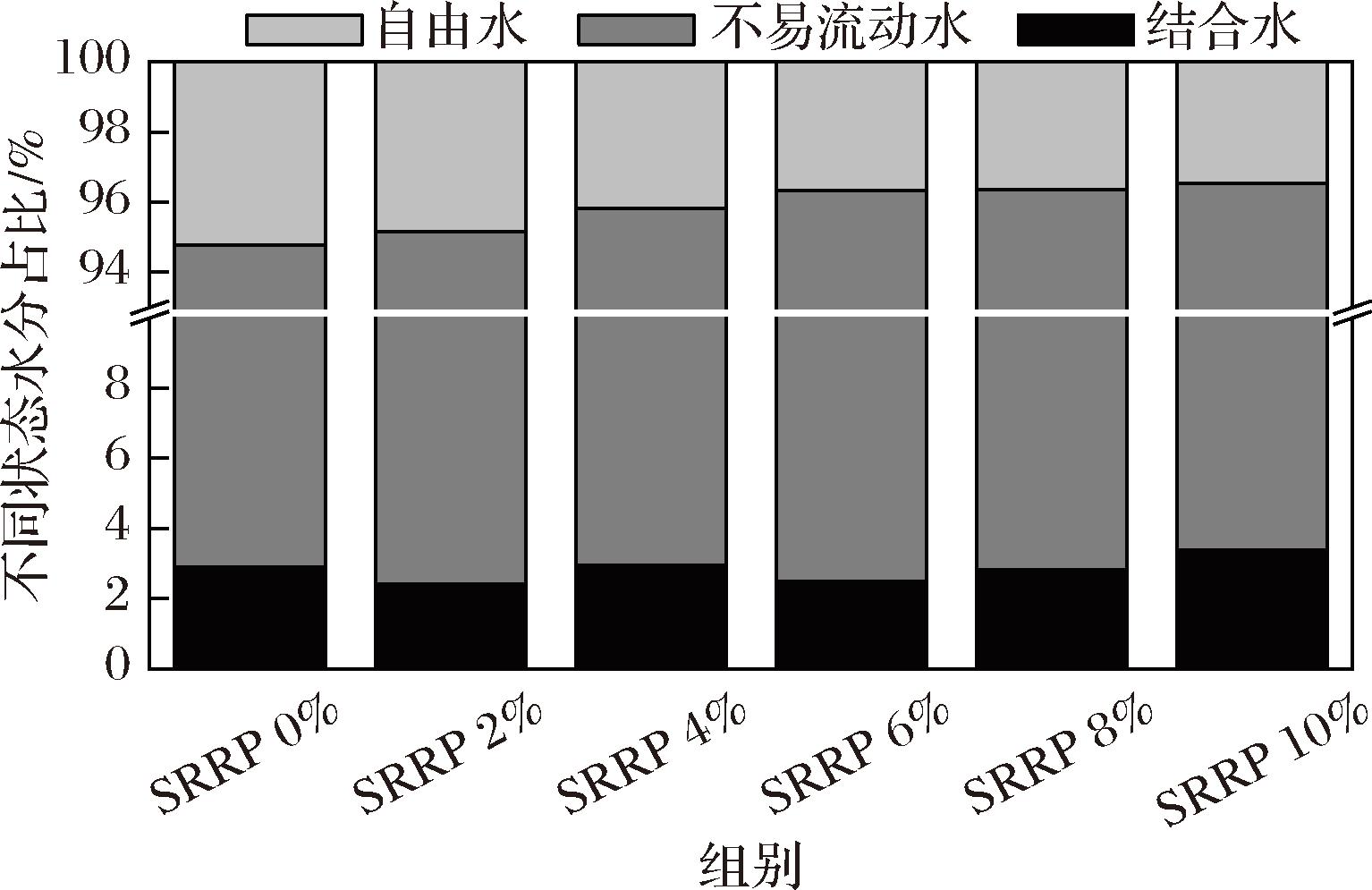
图7 SRRP对鱼糜水分分布的影响
Fig.7 The effect of SRRP on the water distribution of surimi
2.7 动态流变学特性分析
鱼糜在热诱导凝胶化过程中的黏弹性演变可通过动态流变学参数G′和G″来表征。其中,G′主要反映样品的弹性响应特性,G″则主要反映样品的黏性响应特性。在凝胶形成过程中,G′值的显著升高标志着凝胶网络结构的形成和强化。G′值越高,表明样品中肌原纤维蛋白分子间的交联作用越强,形成的三维网络结构越稳固[25]。
如图8展示了在20~90 ℃加热过程中,各添加量组鱼糜G′和G″的变化趋势。在整个加热过程,各组G′和G″变化趋势大致相同,但G′值始终高于G″值,揭示了鱼糜凝胶形成过程中弹性的主导地位。凝胶化过程可分为3个阶段:在初始升温阶段(20~50 ℃),G′和G″值均缓慢上升,在50 ℃左右达到峰值,此阶段肌原纤维蛋白受热展开重组,形成初级凝胶网络,但结构脆弱[26];进入网络解离阶段(50~55 ℃),G′和G″值从峰值迅速下降,在55 ℃左右达到最低,这归因于肌球蛋白结构域解离,导致分子流动性增强,凝胶网络暂时劣化崩解[27-28];当温度升至网络重构与强化阶段(55~90 ℃)时,G′和G″值开始急速上升,随后趋于平缓,表明随温度的进一步升高,肌原纤维蛋白与SRRP协同交联,形成稳固的弹性网络,实现半溶胶向弹性凝胶的转变[29]。在凝胶化过程中,各添加组的G′和G″值均高于对照组,且随SRRP添加量(0%~10%)的增加呈上升趋势,10% SRRP组G′和G″值达到最高值,表明SRRP的添加影响了鱼糜凝胶的形成过程。这与SRRP富含支链淀粉密切相关,其在加热过程中填充于鱼糜蛋白中,高温阶段糊化与肌原纤维蛋白共同形成SRRP-蛋白凝胶网络,使鱼糜刚性增强,宏观表现为硬度与凝胶强度提升,这与2.2节质构结果吻合。
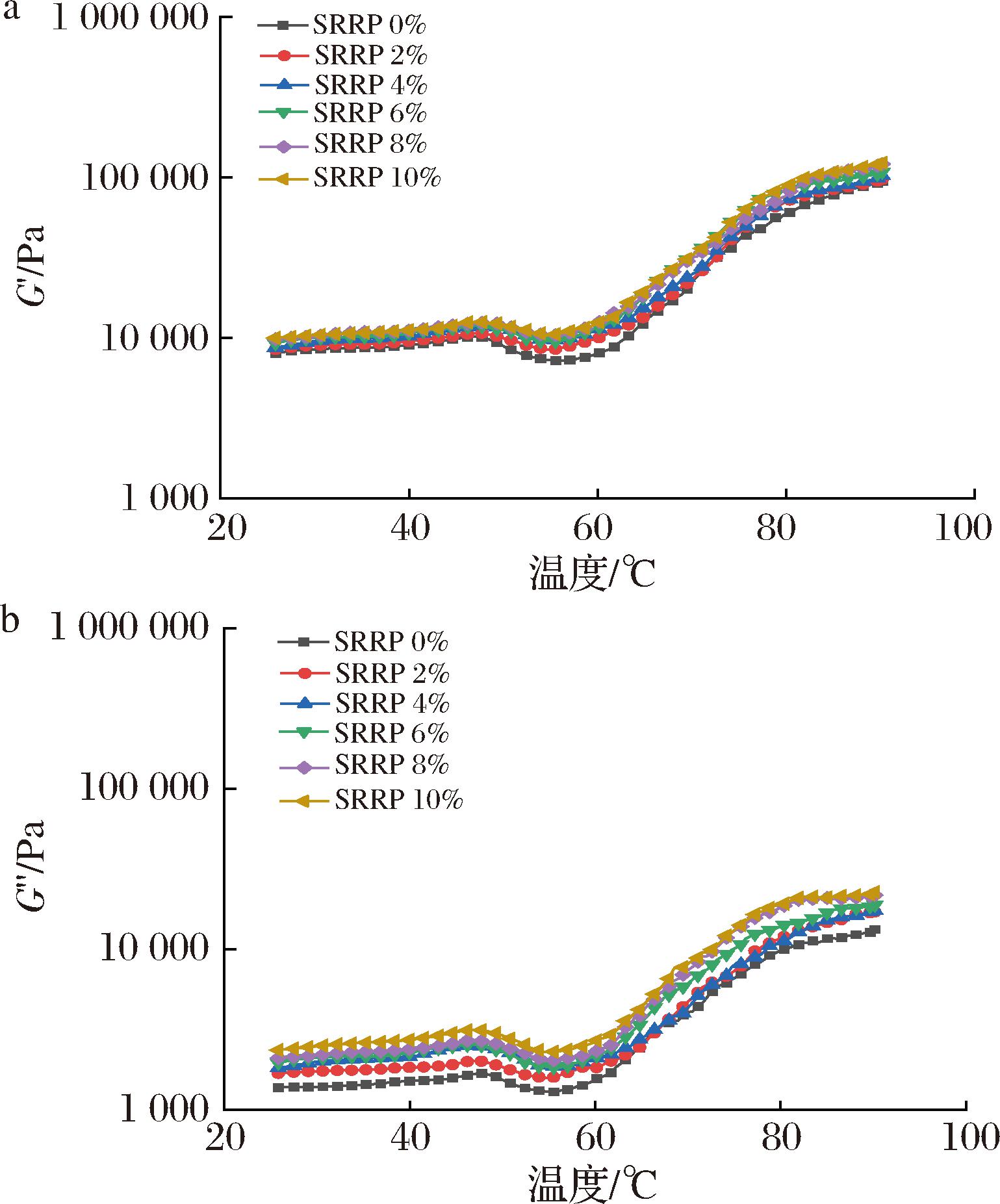
a-G′;b-G″
图8 SRRP对鱼糜储能模量G′与损耗模量G″的影响
Fig.8 The effect of SRRP on G′ and G″ of surimi
2.8 蛋白质的二级结构分析
为探究SRRP对花鲈鱼糜蛋白质二级结构的影响,采用FTIR对不同SRRP添加量样品进行结构表征(图9),重点解析酰胺Ⅰ带(1 600~1 700 cm-1)的振动特征,该区间内不同波数区间与特定二级结构存在典型对应关系[30]:β-折叠(1 600~1 640 cm-1)、无规则卷曲(1 640~1 650 cm-1)、α-螺旋(1 650~1 660 cm-1)和β-转角(1 660~1 700 cm-1),通过计算对应区间特征吸收峰面积与酰胺Ⅰ带总面积之比,可以定量获得4种二级结构的相对含量(图10)。
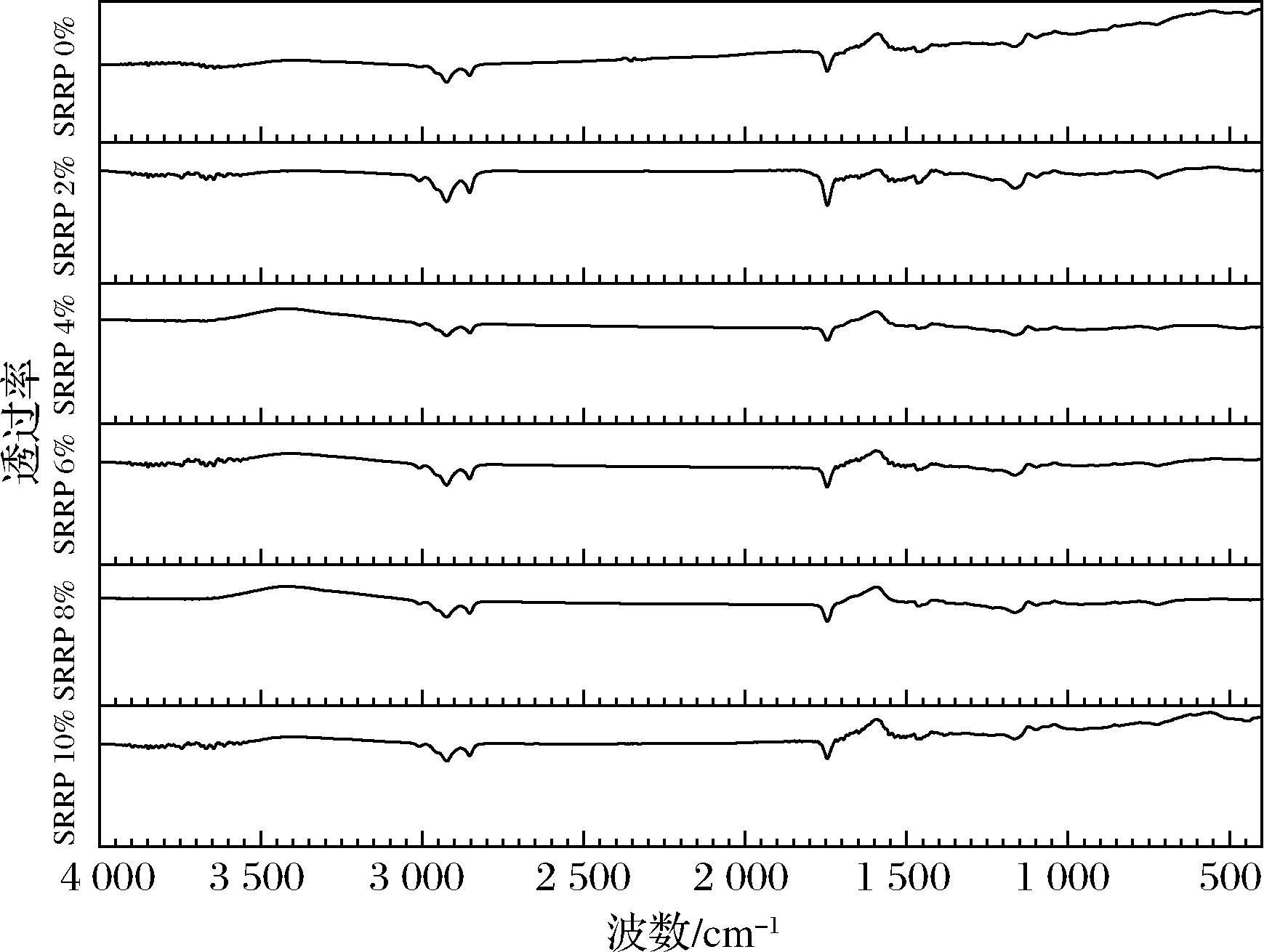
图9 SRRP对鱼糜FTIR谱图的影响
Fig.9 The effect of SRRP on the FTIR spectra of surimi
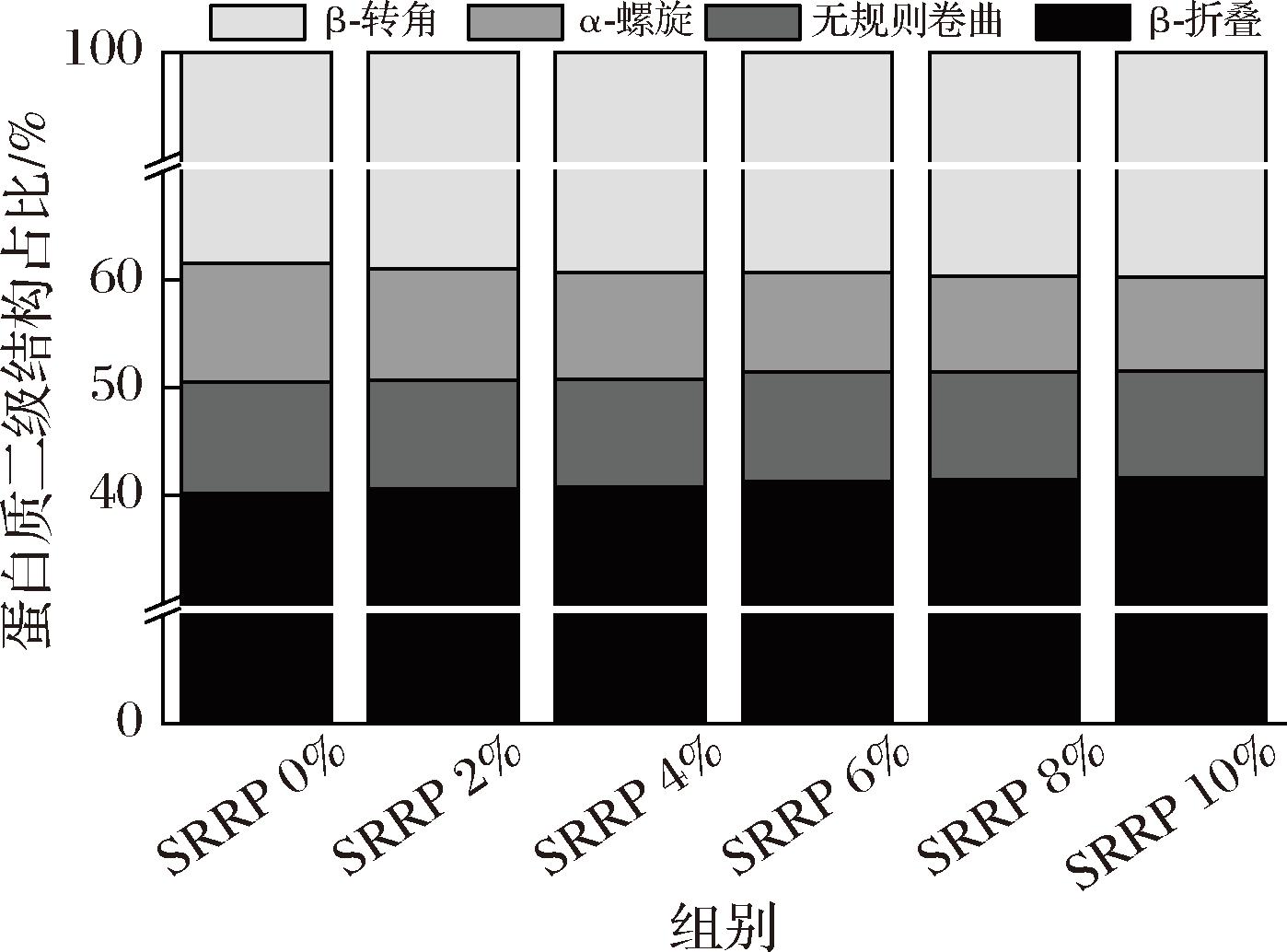
图10 SRRP对鱼糜蛋白质二级结构含量的影响
Fig.10 The effect of SRRP on the protein secondary structure content of surimi
由图10可知,随着SRRP添加量的增加,花鲈鱼糜蛋白质二级结构组成呈现规律性改变,其中β-折叠和β-转角含量均呈现出持续上升趋势,分别从40.20%、38.49%上升到41.63%、39.77%。与之相反,α-螺旋含量则呈梯度下降趋势,从10.98%降至8.72%,各添加组无规则卷曲含量均低于对照组,整体呈下降趋势。这表明SRRP的添加使鱼糜蛋白质中α-螺旋和无规则卷曲向β-折叠和β-转角转化,这种转变可能归因于SRRP表面的亲水性羟基与蛋白质侧链极性基团形成氢键网络,增强β-折叠链间氢键稳定性,同时其空间位阻效应限制肽链自由度,诱导局部β-转角形成,共同驱动蛋白质二级结构有序化重排[30]。β-折叠是刚性的二级结构单元,它们之间通过大量氢键形成稳定的片层结构。其含量的增加意味着分子间交联点的数量和稳定性增加,这直接导致了凝胶网络的刚性增强。正如ZHOU等[31]所述,β-折叠具有更大的分子界面面积及促进分子间交联的能力,有利于形成更致密、更坚固的凝胶网络。这也与流变特性提升密切相关。在凝胶化过程中,更高的β-折叠含量为构建具有更高弹性和刚性的凝胶网络提供了分子层面的保障,最终宏观表现为10% SRRP组获得了最高的G′值及最佳的质构特性。
2.9 微观结构分析
通过扫描电子显微镜观察不同SRRP添加量的花鲈鱼糜凝胶微观结构,如图11所示,随着SRRP添加量的增多,鱼糜凝胶在80倍与500倍放大倍数下的微观结构均呈现孔隙增大的趋势,该现象与SRRP的粒径紧密相关。已有同类型研究观察到类似结果,如汪婕[32]在糙米对草鱼糜凝胶性能的影响研究中观察到,80目糙米粉的适度颗粒膨胀可有效支撑蛋白网络,而160目糙米粉由于粒径较小,填充效率不足,凝胶网络结构较对照组更为稀疏松散。类似地,丁昊[33]在藜麦全粉对虾糜凝胶特性影响的研究中也发现,60~90目藜麦全粉使虾糜微观结构变得致密有序且平滑,而100目细粉因多酚释放过量,阻碍了蛋白质的交联甚至破坏了肌原纤维蛋白的结构,从而使蛋白结构分布不均匀,空隙增大。此外,宋雅婕等[34]研究发现,糊化温度也与凝胶网络结构紧密与否关系密切。其报道,当糊化温度为60 ℃时,凝胶网络结构最为均一致密,而温度进一步增加时,结构则变得疏松。至于本研究中孔隙增大而凝胶性能却持续增强的现象,可以解释为SRRP富含支链淀粉,其高水合特性在加热过程中与花鲈肌原纤维蛋白竞争性结合水分,淀粉颗粒吸水膨胀并挤压蛋白网络,虽促使凝胶孔隙结构扩张,但肌原纤维蛋白因局部脱水而产生的浓缩效应提升了蛋白交联密度,形成刚性骨架,同时SRRP与浓缩蛋白网络进一步构建双相互穿凝胶结构,增强基质整体强度,从而有效抵消了孔隙增多带来的负面影响。

图11 SRRP对鱼糜微观结构的影响
Fig.11 The effect of SRRP on the microstructure of surimi
2.10 抗氧化活性分析
贮藏期间鱼糜制品的品质衰减主要源于蛋白质氧化与脂质过氧化反应[35]。其中,构成凝胶基质的肌原纤维蛋白发生氧化变性会直接导致凝胶三维网络结构破坏,而脂质过氧化不仅产生异味,还会进一步破坏蛋白质结构[36]。因此,有效抑制氧化反应,是维持鱼糜品质的关键。海红米富含花青素等酚类物质,能有效阻断自由基链式反应,有望在鱼糜体系中发挥清除自由基的作用,在延长货架期的同时赋予鱼糜制品抗氧化的功能特性。本研究通过测定添加SRRP的鱼糜凝胶的DPPH自由基清除率、ABTS阳离子自由基清除率及羟自由基清除率,评估SRRP的添加对鱼糜抗氧化能力的影响。
如图12为不同添加量SRRP对鱼糜抗氧化活性的影响,DPPH自由基清除率、ABTS阳离子自由基清除率及羟自由基清除率均随SRRP添加量的增加(0%~10%)呈显著上升趋势(P<0.05),其中DPPH自由基清除率从48.40%提升到73.27%,ABTS阳离子自由基清除率从52.73%提升到76.16%,羟自由基清除率从61.08%提升到69.73%。上述结果表明,SRRP的添加能有效提升鱼糜的自由基清除能力,且呈现出剂量依赖性。WEI等[37]研究指出,向金丝鳍肌原纤维蛋白中添加多酚可显著增强其抗氧化性能,其机制可能在于多酚与蛋白质的相互作用将强抗氧化基团引入蛋白质分子表面,从而提升其抗氧化能力。
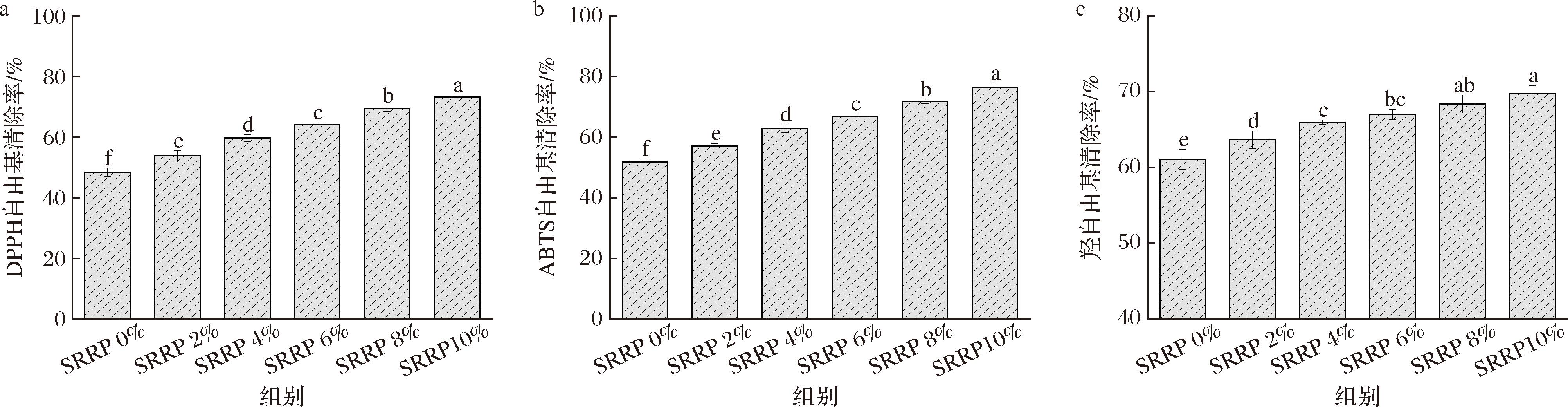
a-DPPH自由基清除率;b-ABTS阳离子自由基清除率;c-羟自由基清除率
图12 SRRP对鱼糜抗氧化活性的影响
Fig.12 The effect of SRRP on the antioxidant activity of surimi
2.11 相关性分析
为系统探究添加不同水平SRRP对体系综合特性的影响,选取12项关键指标进行相关性分析,结果以热图可视化呈现(图13)。统计分析表明,指标间普遍存在高度显著的关联性,共39对指标呈极显著相关(P<0.01),7对指标呈显著相关(P<0.05),表明指标间存在广泛的协同或拮抗效应。但内聚性与所分析的其余11项指标均未表现出显著或极显著的相关性,这表明在本研究中内聚性的变化模式相对独立于其他指标的变化。其次为无规则卷曲,该指标除与持水性和β-转角存在一定程度的显著关联外,与其余9项指标的相关性均不显著,这可能是由于在本研究的实验背景下,无规则卷曲的构象变化主要与持水行为和特定的转角结构有关,而与其他整体特性及结构单元关联较弱。
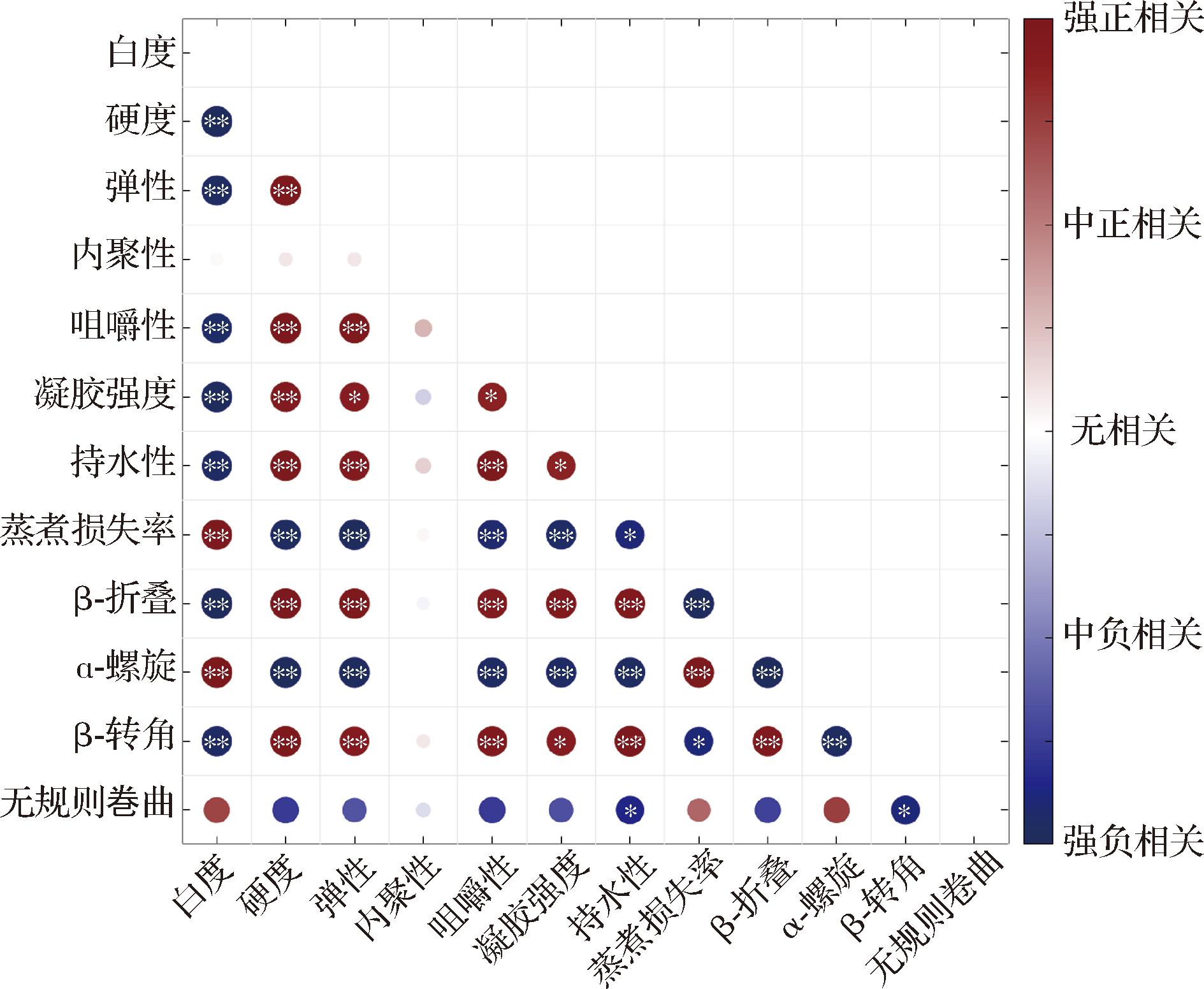
图13 鱼糜凝胶各指标间的相关性
Fig.13 Correlation among various parameters of surimi gel
注:*表示显著相关(P<0.05),**表示极显著相关(P<0.01),圆圈大小和颜色表示相关强度和方向。
3 结论与讨论
本实验通过在花鲈鱼糜中加入鱼肉质量0%~10%的SRRP,探究SRRP对花鲈鱼糜理化性质及抗氧化活性的影响。结果表明,SRRP的添加对花鲈鱼糜的凝胶特性产生了积极影响。随着SRRP添加量的增加,鱼糜凝胶形成过程中G′和G″逐渐升高,鱼糜蛋白质中α-螺旋和无规则卷曲向β-折叠和β-转角转化,形成强度更高的凝胶网络。表现为鱼糜凝胶的硬度、弹性、内聚性、咀嚼性以及凝胶强度均得到显著提升。同时,SRRP使鱼糜凝胶自由水和结合水的T2弛豫时间显著缩短,自由水被捕获并固定为不易流动水,显著提高了鱼糜持水性并降低蒸煮损失率。此外,SRRP添加显著提升了鱼糜的抗氧化能力,但会降低鱼糜的白度。这些发现为海红米资源在鱼糜制品中的高值化利用提供了新思路,也为开发兼具质构改良与营养强化功能的新型鱼糜制品提供了理论依据和技术支撑。但需要指出的是,这种不同于传统白色鱼糜的新颜色产品能否被消费者广泛接受以及鱼糜体系中的体外抗氧化活性提升在人体内是否能发挥相应的生理功能,仍有待后续深入研究。
[1] 温海深, 张美昭, 李吉方, 等. 我国花鲈养殖产业现状与种子工程研究进展[J]. 渔业信息与战略, 2016, 31(2):105-111.WEN H S, ZHANG M Z, LI J F, et al. Research progress of aquaculture industry and its seed engineering in spotted sea bass(Lateolabrax maculatus) of China[J]. Fishery Information &Strategy, 2016, 31(2):105-111.
[2] 农业农村部渔业渔政管理局. 中国渔业统计年鉴-2024[M]. 北京: 中国农业出版社, 2024. Ministry of Agriculture and Rural Affairs of the People’s Republic of China. China Fishery Statistical Yearbook[M]. Beijing: China Agriculture Press, 2024.
[3] HOU S Y, ZHANG B, WANG P F, et al. The nutritional characteristic of spotted seabass (Lateolabrax maculatus) flesh[J]. Israeli Journal of Aquaculture-Bamidgeh, 2023, 75(2): 1-12.
[4] BUDA U, PRIYADARSHINI M B, MAJUMDAR R K, et al. Quality characteristics of fortified silver carp surimi with soluble dietary fiber: Effect of apple pectin and konjac glucomannan[J]. International Journal of Biological Macromolecules, 2021, 175:123-130.
[5] LI M G, YANG J, BAO H L, et al. The effect of heating method on the gel structures and properties of surimi prepared from Bombay duck (Harpadon nehereus)[J]. Frontiers in Nutrition, 2022, 9:1060188.
[6] DEBUSCA A, TAHERGORABI R, BEAMER S K, et al. Physicochemical properties of surimi gels fortified with dietary fiber[J]. Food Chemistry, 2014, 148:70-76.
[7] GUO A Q, JIANG J, TRUE A D, et al. Myofibrillar protein cross-linking and gelling behavior modified by structurally relevant phenolic compounds[J]. Journal of Agricultural and Food Chemistry, 2021, 69(4):1308-1317.
[8] HUANG X B, LIU Q G, WANG P K, et al. Tapioca starch improves the quality of virgatus Nemipterus surimi gel by enhancing molecular interaction in the gel system[J]. Foods, 2024, 13(1):169.
[9] 朱晓晗, 铁芳芳, 欧阳健, 等. 桑葚花色苷对PC12细胞氧化损伤的保护作用[J]. 食品与发酵工业, 2024, 50(8):105-113.ZHU X H, TIE F F, OUYANG J, et al. Protective effects of mulberry anthocyanin on oxidative stress in PC12 cells[J]. Food and Fermentation Industries, 2024, 50(8):105-113.
[10] 钟凯翠, 邹雯清, 陈忠琴, 等. 海红米花色苷-牡蛎肽新型复合饮料制备工艺及降血糖作用研究[J]. 食品与发酵工业, 2025, 51(7):194-203.ZHONG K C, ZOU W Q, CHEN Z Q, et al. Study on the preparation technology and hypoglycemic effect of a new composite beverage based on sea red rice anthocyanins and oyster peptides[J]. Food and Fermentation Industries, 2025, 51(7):194-203.
[11] 时萍, 卢进娟, 李洁思, 等. 不同超声处理对海红米淀粉-月桂酸复合物理化性质的影响[J]. 食品工业科技, 2026, 47(1):159-167.SHI P, LU J J, LI J S, et al. Influence of different ultrasonic treatments on physicochemical properties of sea red rice starch-lauric acid complex[J]. Science and Technology of Food Industry, 2026, 47(1):159-167.
[12] 国家食品质量监督检验中心. 海红米检验报告(2019总字第190461号分字第01号)[R]. 北京: 国家食品质量监督检验中心, 2019.National Food Quality Supervision And Inspection Center. Inspection Report of Sea Red Rice (2019 General No. 190461, Sub No. 01)[R]. Beijing: National Food Quality Supervision and Inspection Center, 2019.
[13] 曾泽政, 朱礼锋, 曹扬洪, 等. 金花茶多糖对巴沙鱼糜理化性质及凝胶特性的影响[J]. 食品工业科技, 2025, 46(17):191-202.ZENG Z Z, ZHU L F, CAO Y H, et al. Effect of Camellia nitidissima Chi polysaccharide on the physicochemical properties and gel properties of surimi gel in Pangasius bocourti[J]. Science and Technology of Food Industry, 2025, 46(17):191-202.
[14] 朱士臣, 徐思瑶, 周绪霞, 等. 超声微波协同改性肌原纤维蛋白Pickering乳液对鱼糜凝胶特性的影响[J]. 食品与发酵工业, 2026, 52(2):28-34.ZHU S C, XU S Y, ZHOU X X, et al. Effect of ultrasound-microwave modified myofibrillar protein-based Pickering emulsion on gel properties of surimi[J]. Food and Fermentation Industries, 2026, 52(2):28-34.
[15] 汲晨洋. 条斑紫菜多糖流变特性研究及其对鲢鱼鱼糜凝胶特性的影响[D]. 湛江: 广东海洋大学, 2022.JI C Y. Rheological properties of Porphyra yezoensis polysaccharide and its effect on gel properties of silver carp surimi[D]. Zhanjiang: Guangdong Ocean University, 2022.
[16] RAWDKUEN S, BENJAKUL S, VISESSANGUAN W, et al. Effect of chicken plasma protein and some protein additives on proteolysis and gel-forming ability of sardine (Sardinella gibbosa) surimi[J]. Journal of Food Processing and Preservation, 2007, 31(4):492-516.
[17] QIAO L K, LI Y P, CHI Y Z, et al. Rheological properties, gelling behavior and texture characteristics of polysaccharide from Enteromorpha prolifera[J]. Carbohydrate Polymers, 2016, 136:1307-1314.
[18] MI H B, LI Y, WANG C, et al. The interaction of starch-gums and their effect on gel properties and protein conformation of silver carp surimi[J]. Food Hydrocolloids, 2021, 112:106290.
[19] MI H B, WANG C, SU Q, et al. The effect of modified starches on the gel properties and protein conformation of Nemipterus virgatus surimi[J]. Journal of Texture Studies, 2019, 50(6):571-581.
[20] CAO Y, ZHAO L Y, HUANG Q L, et al. Water migration, ice crystal formation, and freeze-thaw stability of silver carp surimi as affected by inulin under different additive amounts and polymerization degrees[J]. Food Hydrocolloids, 2022, 124:107267.
[21] 陈宇翔, 王萍, 王颖, 等. 大豆分离蛋白-大米粉复合凝胶特性及形成机理研究[J]. 食品与发酵工业, 2024, 50(22):98-105.CHEN Y X, WANG P, WANG Y, et al. Research on gelation characteristics and formation mechanism of soy protein isolate-rice flour composite gel[J]. Food and Fermentation Industries, 2024, 50(22):98-105.
[22] ALAKHRASH F, ANYANWU U, TAHERGORABI R. Physicochemical properties of Alaska pollock (Theragra chalcograma) surimi gels with oat bran[J]. LWT-Food Science and Technology, 2016, 66:41-47.
[23] 程小璇, 张楠, 唐月, 等. 添加不同粒径及比例的纤维素对鱼糜制品凝胶特性的影响[J]. 食品与发酵工业, 2024, 50(12):63-73.CHENG X X, ZHANG N, TANG Y, et al. Effect of cellulose with different particle sizes and addition ratios on gel properties of surimi products[J]. Food and Fermentation Industries, 2024, 50(12):63-73.
[24] ZHUANG X B, HAN M Y, BAI Y, et al. Insight into the mechanism of myofibrillar protein gel improved by insoluble dietary fiber[J]. Food Hydrocolloids, 2018, 74:219-226.
[25] ZHOU X X, LIN H H, ZHU S C, et al. Textural, rheological and chemical properties of surimi nutritionally-enhanced with lecithin[J]. LWT, 2020, 122:108984.
[26] XIONG Z Y, SHI T, JIN W G, et al. Gel performance of surimi induced by various thermal technologies: A review[J]. Critical Reviews in Food Science and Nutrition, 2024, 64(10):3075-3090.
[27] SUN F Y, HUANG Q L, HU T, et al. Effects and mechanism of modified starches on the gel properties of myofibrillar protein from grass carp[J]. International Journal of Biological Macromolecules, 2014, 64:17-24.
[28] FAN M C, HUANG Q L, ZHONG S Y, et al. Gel properties of myofibrillar protein as affected by gelatinization and retrogradation behaviors of modified starches with different crosslinking and acetylation degrees[J]. Food Hydrocolloids, 2019, 96:604-616.
[29] LIU R, ZHAO S M, XIONG S B, et al. Role of secondary structures in the gelation of porcine myosin at different pH values[J]. Meat Science, 2008, 80(3):632-639.
[30] BUAMARD N, BENJAKUL S. Improvement of gel properties of sardine (Sardinella albella) surimi using coconut husk extracts[J]. Food Hydrocolloids, 2015, 51:146-155.
[31] ZHOU X X, JIANG S, ZHAO D D, et al. Changes in physicochemical properties and protein structure of surimi enhanced with Camellia tea oil[J]. LWT, 2017, 84:562-571.
[32] 汪婕. 糙米对草鱼糜凝胶性能的影响及应用研究[D]. 雅安: 四川农业大学, 2024.WANG J. Effect of brown rice on the gel properties of Grass Carp surimi and its application[D]. Ya’an: Sichuan Agricultural University, 2024.
[33] 丁昊. 藜麦全粉对虾糜凝胶特性的影响及应用研究[D]. 天津: 天津科技大学, 2023.DING H. Study on the effect of whole quinoa flour on the gel characteristics of shrimp mince and its application[D]. Tianjin: Tianjin University of Science and Technology, 2023.
[34] 宋雅婕, 刘雨潇, 冯紫蓝, 等. 玉米淀粉预糊化温度对罗非鱼肌原纤维蛋白乳液凝胶特性与3D打印性能的影响[J/OL]. 食品工业科技, 2025. DOI: 10.13386/j.issn1002-0306.2025030146.
SONG Y J, LIU Y X, FENG Z L, et al. Effect of corn starch pregelatinization temperature on gel properties and 3D printing performance of tilapia myofibrillar protein lotion[J/OL]. Science and Technology of Food Industry, 2025. DOI: 10.13386/j.issn1002-0306.2025030146.
[35] LIN J, HONG H, ZHANG L T, et al. Antioxidant and cryoprotective effects of hydrolysate from gill protein of bighead carp (Hypophthalmichthys nobilis) in preventing denaturation of frozen surimi[J]. Food Chemistry, 2019, 298:124868.
[36] HEMATYAR N, RUSTAD T, SAMPELS S, et al. Relationship between lipid and protein oxidation in fish[J]. Aquaculture Research, 2019, 50(5):1393-1403.
[37] WEI X L, ZHOU C X, LUO D H, et al. Insighting the effect of ultrasound-assisted polyphenol non-covalent binding on the functional properties of myofibrillar proteins from golden threadfin (Nemipterus virgatus)[J]. Ultrasonics Sonochemistry, 2024, 109:106988.