吡咯喹啉醌(pyrroloquinoline quinone,PQQ)自1964年被发现以来[1],因其多元的生物学活性引起了广泛关注。作为一种氧化还原酶的辅基,PQQ在人体复杂的生理调控网络和疾病发生发展中扮演着关键角色。研究发现,PQQ不仅能保护并增强现有线粒体的功能,还能促进新线粒体的产生[2];作为一种强大的抗氧化剂,它能够有效清除体内有害自由基,其还原性是维生素C的5 000倍[3-4]。由于其在细胞能量代谢和抗氧化防御中的关键作用,PQQ表现出许多独特的生理功能。它在改善认知和记忆能力[5-6]、神经保护[7]、延缓衰老[8]方面表现出一定的作用;同时在维护生殖健康[9-10],强化心血管和肝脏功能[11],以及提供骨关节保护方面也发挥重要作用[12]。此外,PQQ在农业和畜牧养殖领域也展现出重要的应用潜力[13]。PQQ在生物医药、功能食品、化妆品以及现代农业等领域具有广泛的应用前景。
由于PQQ在细胞能量代谢和抗氧化中的关键作用,市场需求逐年增长,开发高效生产方法成为当前研究重点。目前,PQQ的制备方法有化学合成法和微生物发酵法。其中微生物发酵法因其安全性、环境友好和可持续性成为产业化发展的主要方向[14]。研究显示甲基杆菌属(Methylobacterium sp.)和生丝微菌属(Hyphomicrobium sp.)等甲基营养菌具有较高合成PQQ的能力[15-18]。然而,由于缺乏对PQQ生物合成途径调控机制的深入了解,尽管在诱变育种、发酵工艺优化及定向改造方面已开展诸多研究,但目前大多数菌株产量仍未能满足日益增长的工业需求。如ZHAO等[19]通过多种诱变将Methylobacterium sp. NI91突变株的PQQ产量提升至19.3 mg/L,传统的随机诱变方法存在筛选难度大、效率低等问题。WEI等[20]通过响应面和人工神经网络遗传算法等系统优化培养基,使Methylobacterium sp. zju323的PQQ产量达到232 mg/L,较未优化培养基提高了约47.6%。尽管该研究取得了一定进展,但其提升幅度仍相对有限,且主要集中于培养基组分的精细调控,对于菌株自身的代谢瓶颈突破仍需更深层次的干预。叶润乐等[21]通过基因工程改造Gluconobacter oxydans,结合培养条件优化,实现了51.32 mg/L的PQQ产量。然而,工程菌株的产量与工业应用需求仍有较大差距,且对宿主菌株的适用性及遗传稳定性仍需深入研究。因此,筛选具有高产高效潜力的底盘菌株仍是当前PQQ生物制造领域亟待解决的关键问题。
本研究采用高通量初筛、光谱法快速检测与HPLC精准验证结合的筛选方法,从环境污水中分离出一株PQQ高产菌株,对其进行菌株鉴定和发酵工艺优化,并结合常压室温等离子体(atmospheric and room temperature plasma,ARTP)诱变技术和精细化的动态甲醇流加补料发酵工艺,进一步提高PQQ产量。本研究获得的菌株具有一定的工业化应用潜力,为PQQ的工业化生产提供了新的菌株资源。
1 材料与方法
1.1 材料与试剂
样品采自于福建省福清市化工厂附近的排污口。
PQQ标准品(99.6%),北京曼哈格生物科技有限公司;细菌基因组DNA提取试剂盒,天根生化科技有限公司;其他试剂均采购于西陇科学股份有限公司。
1.2 仪器与设备
GR85DA高压灭菌锅,致微(厦门)仪器有限公司;Multiskan Sky酶标仪,赛默飞世尔科技(中国)有限公司;Agilent-1260 HPLC,安捷伦科技(中国)有限公司;ARTP-C型ARTP诱变仪,无锡源清天木生物科技有限公司;SBA-40D生物传感分析仪,山东省科学院生物研究所。
1.3 培养基
基础培养基(g/L):硫酸铵3.0、磷酸氢二钠3.0、硫酸镁1.5、磷酸二氢钾1.5,再添加10.0 mL/L微量元素溶液。其中微量元素溶液(g/L):FeSO4·7H2O 5.0、ZnSO4·7H2O 10.0、MnSO4·4H2O 5.0、CoCl2·6H2O 0.05、(NH4)6Mo7O24·4H2O 0.05、CaCl2·2H2O 0.05。固体培养基在基础培养基中添加2.0%(质量分数)琼脂,固体培养基和液体培养基均在121 ℃灭菌后补充20 mL/L甲醇。
1.4 实验方法
1.4.1 PQQ产生菌的分离和鉴定
将样品制备成适当浓度梯度的稀释液,涂布于固体培养基平板上,30 ℃培养5~8 d。从平板上挑选不同形态的单菌落,接种至含有4 mL液体培养基的48孔深孔板中进行高通量筛选,30 ℃、180 r/min培养5 d。离心获得发酵液上清液,采用光谱法测定PQQ含量。对初筛中PQQ产量较高的菌株,用HPLC进行复筛检测。利用HPLC-MS对甲基营养菌发酵液中的PQQ进行初步鉴定。将菌株在固体培养基平板上划线分离,30 ℃培养5~8 d,观察菌体的形态特征。取单个菌落接种至液体培养基中培养,30 ℃培养至菌体OD600达到0.5~1,取3 mL发酵液10 000 r/min离心10 min。采用细菌基因组DNA提取试剂盒提取DNA。利用细菌通用引物27F(5′-AGAGTTTGATCMTGGCTCAG-3′)和1492R(5′-GGTTACCTTGTTACGACTT-3′),进行PCR扩增16S rDNA序列。扩增产物委托上海生工生物工程股份有限公司测序,所得序列在NCBI数据库中进行BLAST比对,MEGA7.0软件构建系统发育树。
1.4.2 摇瓶发酵工艺优化
分别考察培养温度(22~38 ℃)、pH(5.0~8.0)、转速(160~240 r/min)对PQQ产量的影响,确定最佳条件后,进行碳源筛选(10.0 g/L葡萄糖、果糖、蔗糖及20 mL/L甲醇、甘油和乙醇),结果确定甲醇为最适碳源,进一步优化其浓度(体积分数1.0%~4.0%)。在此基础上筛选氮源(3.0 g/L玉米浆粉、蛋白胨、酵母浸膏、尿素、硫酸铵和氯化铵),确定硫酸铵为最适氮源,考察了不同硫酸铵质量浓度(1.0~4.0 g/L)对PQQ产量的影响。在优化碳氮源基础上,考察磷酸氢二钠(2.0~4.0 g/L)、磷酸二氢钾(1.0~3.0 g/L)及硫酸镁(1.0~3.0 g/L)对菌株生长及PQQ产量的影响。
以上实验均在装液量100 mL的500 mL三角瓶中培养5 d,培养结束后,发酵液经10 000 r/min离心10 min,测定上清液中的PQQ含量。
1.4.3 ARTP诱变选育高产PQQ突变株
将成熟斜面培养物用无菌生理盐水洗脱,使用无菌脱脂棉过滤。在滤液中加入玻璃珠,涡旋振荡5 min,将菌体悬浮液进行梯度稀释,将菌体浓度调整至106~107 CFU /mL。诱变条件设定如下[22]:氦气流量10 L/min,功率100 W,等离子体发射源与样品距离2 mm,样品体积为10 μL。分别照射10~60 s。诱变处理后的样品转移至装有1 mL生理盐水的离心管,置于振荡器上涡旋振荡。对菌悬液进行梯度稀释,取100 μL稀释液均匀涂布于固体培养基平板,30 ℃培养8~12 d,进行菌落计数并按公式(1)计算致死率。将诱变获得的单菌落接种至48孔深孔板中,每孔加入4 mL液体培养基,于30 ℃、250 r/min培养5 d。采用光谱法对各培养孔中的PQQ浓度进行初步测定。对初筛中PQQ产量较高的菌株,采用HPLC法进行复筛,确认PQQ高产突变株。
致死率![]()
(1)
式中:U,平板上生长的对照菌落总数,CFU;T,经诱变后平板上生长的存活菌落总数,CFU。
1.4.4 20 L发酵罐甲醇流加补料发酵生产PQQ
将成熟斜面培养物经15 mL无菌生理盐水洗脱并制成均匀菌悬液,将1 mL菌悬液接种至装有100 mL经1.4.2节优化后的液体培养基中。采用优化后的温度、pH、转速培养40~48 h,种子液OD600值达1.0左右。PQQ的发酵实验在20 L发酵罐中进行,装有12 L优化后的液体培养基。将制备好的种子液以5%的接种量接入发酵罐。培养温度30 ℃,通气速率为12 L/min,搅拌转速为600 r/min[23]。通过自动流加氨水控制发酵液pH 7.0。甲醇的补料采用周期性反馈控制策略,即接种后每8 h取样,通过测定发酵液中甲醇含量,调整100%纯甲醇补料速率,以维持发酵液中甲醇含量不超过0.5 mL/L。发酵48 h后开始补料(优化后的基础培养基),补料速率约为1 L/d。整个发酵周期为10 d。
1.4.5 检测与分析方法
1.4.5.1 发酵液OD值测定
取PQQ发酵液适量,加水稀释使吸光度介于0.2~0.8,使用分光光度计在600 nm波长下测定其吸光度。OD值通过吸光度乘以稀释倍数计算。
1.4.5.2 光谱法检测PQQ含量[24]
将PQQ标准品溶解于纯水,制备质量浓度梯度为2.02、4.59、9.17、13.76、18.35、27.52 mg/L的系列标准溶液。利用酶标仪检测上述PQQ标准溶液在330 nm处的吸光值,以建立标准曲线;检测发酵液时,发酵液经10 000 r/min离心10 min后,取上清液,在相同条件下测定其330 nm处的吸光度值。
1.4.5.3 HPLC法检测PQQ含量
HPLC法的条件为:采用Eclipse XDB-C8色谱柱(4.6 mm×150 mm,5 μm),检测波长254 nm,柱温30 ℃;流动相由0.1%甲酸水溶液(A相)和乙腈(B相)组成,梯度洗脱程序为:0~3 min,A相97%,B相3%;3~5 min,A相由97%线性降至60%,B相由3%线性升至40%;5~8 min,A相60%,B相40%。流速设定为0.7 mL/min,进样量10 μL。检测发酵液时,发酵上清液需经0.22 μm微孔滤膜过滤后进样。通过检测不同浓度的PQQ标准溶液建立HPLC标准曲线,将其结果与光谱法进行对比验证。
1.4.5.4 质谱分析方法
采用电喷雾负离子模式进行数据采集,主要参数包括鞘气温度350 ℃、鞘气流速11.0 L/min、喷嘴电压500 V、毛细管电压3 500 V、雾化气压力0.24 MPa、干燥气温度320 ℃、干燥气流速8.0 L/min、毛细管出口电压105 V、Skimmer电压65 V、八级杆电压750 V,质荷比扫描范围为m/z 100~800。
1.4.5.5 甲醇检测方法
采用生物传感器分析仪进行测定,样品经适当稀释后手动进样,与甲醇标准品浓度比较,来确定培养基中的甲醇含量。
2 结果与分析
2.1 光谱法和HPLC法测定PQQ含量的比较
光谱法基于 PQQ 特征吸收峰进行定量,具有操作简便、分析快速的特点,适合对大批量样品进行快速筛查。PQQ在紫外-可见光区域有2个主要吸收峰,分别位于250 、 330 nm 左右。考虑到发酵液中含有大量蛋白质、核酸等在 250 nm 处有强吸收干扰的物质,而 330 nm 处干扰较少[25],因此选择在330 nm波长下进行光谱法检测,并与HPLC法进行验证。结果表明,2种方法均建立了良好的线性标准曲线。如图1所示,光谱法检测0~30 mg/L PQQ的标准曲线为y=0.035 24x+0.016 5,HPLC法的标准曲线为y=41.029 9x+28.491 5,且决定系数R2均大于0.99,表明线性关系良好。光谱法与HPLC法测定结果高度吻合,表明基于330 nm波长的光谱法准确可靠,可作为 PQQ 的快速定量检测手段用于大规模初筛。
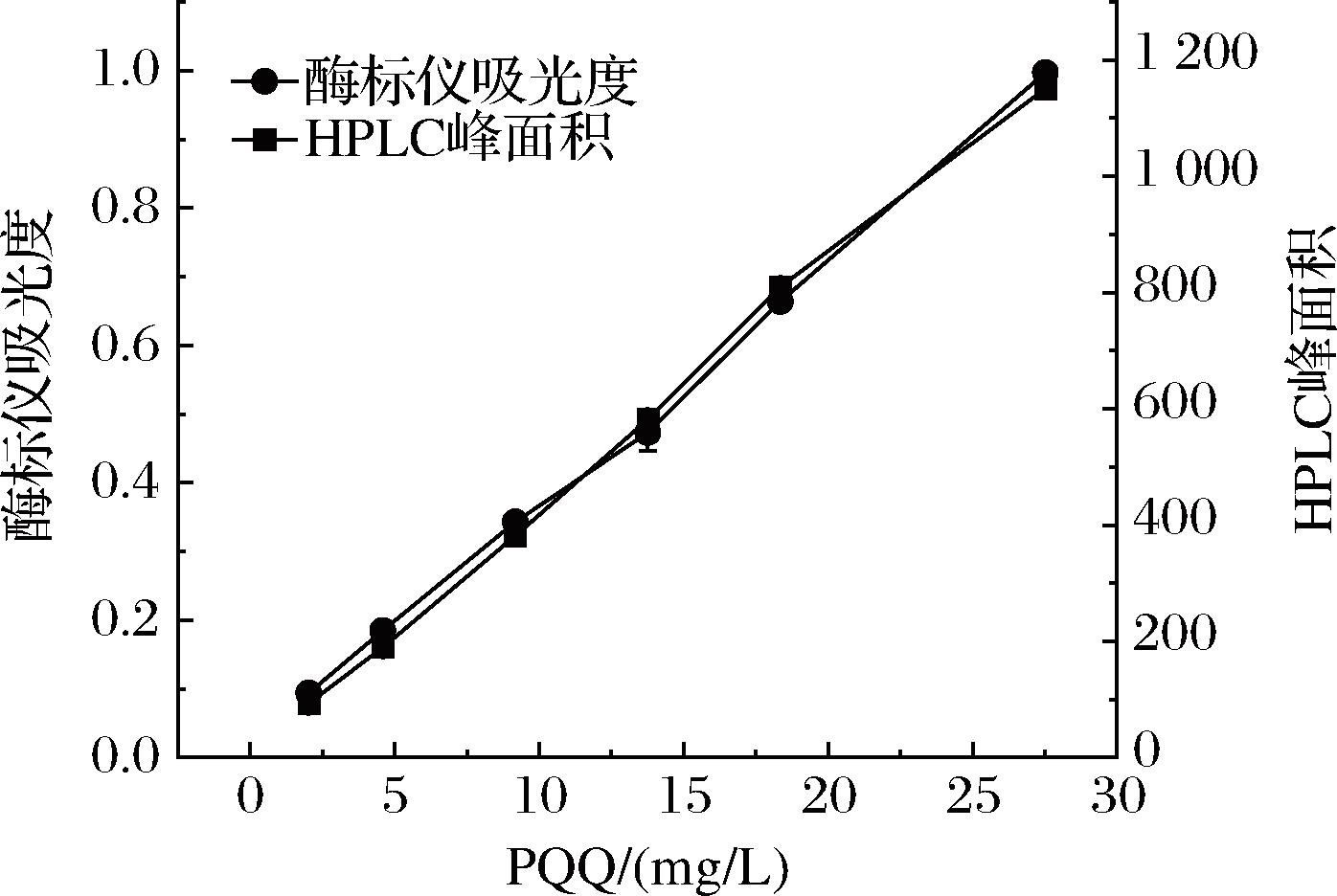
图1 光谱法与HPLC检测PQQ的结果对比
Fig.1 Comparison of PQQ concentration detected by spectrophotometry and HPLC
2.2 PQQ产生菌的分离和鉴定
将50份采集样品进行梯度稀释后涂布于筛选平板上,得到600多株甲基营养菌。挑选不同形态单菌落,接种至含有4 mL液体培养基的48孔板中进行发酵。发酵5 d后对发酵液进行离心,上清液经过光谱法初筛,53株菌的发酵液在330 nm具有一定的吸光值,表明这些菌株可能具有合成PQQ能力。通过HPLC复筛筛选出PQQ产量最高的菌株FQ00818,其产量达(25.6±1.2) mg/L。HPLC图谱(图2-a)在4.26 min处显示出PQQ特征峰。HPLC-MS分析(图2-b)证实主要代谢产物为PQQ。
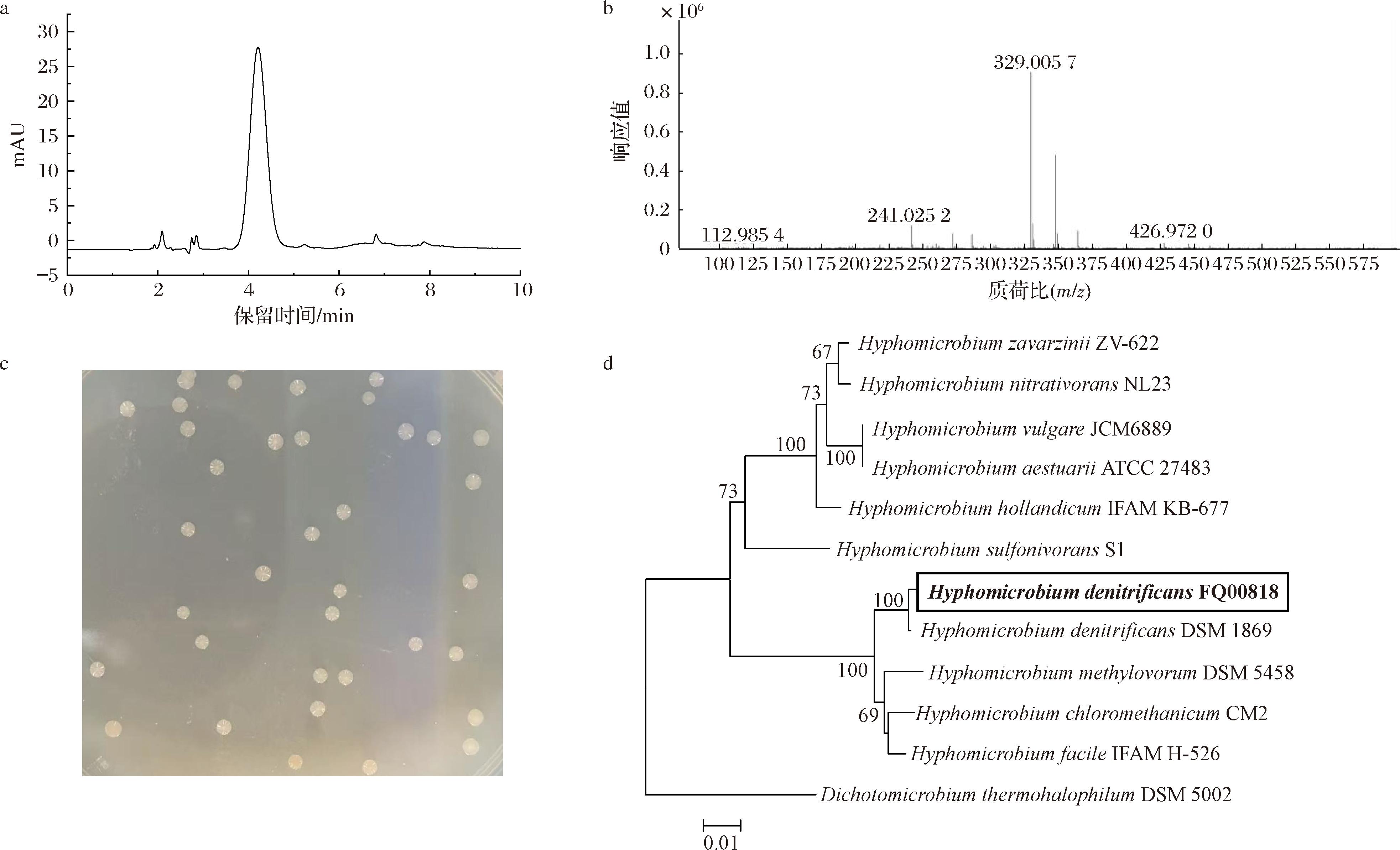
a-FQ00818菌株发酵产物的HPLC图;b-FQ00818菌株发酵产物质谱图;c-FQ00818菌落形态;d-FQ00818菌株系统进化分析图
图2 脱氮生丝微菌FQ00818的分离与鉴定
Fig.2 Isolation and identification of Hyphomicrobium denitrificans FQ00818
甲基营养菌FQ00818是一种革兰氏阴性梭形杆菌,菌落形态为乳白色、质地黏稠、边缘整齐,直径约为1~2 mm(图2-c)。对菌株的16S rDNA序列进行PCR扩增,利用BLASTN对序列进行比对分析。比对结果显示,FQ00818菌株的16S rDNA序列与Hyphomicrobium denitrificans ATCC51888菌株的同源性最高,达到99.8%(图2-d)。根据16S rDNA序列采用邻接法进行系统发育分析,综合菌落形态及细胞形态特征,将该菌株初步鉴定为H.denitrificans。
2.3 PQQ产生菌FQ00818摇瓶发酵条件的优化
分别考察了温度、pH和转速对PQQ产量的影响。如图3-a所示,PQQ产量在30 ℃时达到最高(25.2±1.6) mg/L。较高温度可能抑制PQQ合成关键酶活性,较低温度可能影响细胞膜的流动性。pH值是影响PQQ合成的重要因素,当培养体系pH值低于7.0时,PQQ产量急剧下降至(14.4±2.0) mg/L(图3-b),因为酸性环境对PQQ合成有抑制作用,PQQ分子在低pH环境也不稳定。pH 7.0时PQQ产量最高,可能与甲醇脱氢酶的最适pH特性密切相关[26],该酶在pH 7.0具有最大催化活性,促进PQQ的合成。转速实验如图3-c所示,当转速为200 r/min时PQQ产量达到最高(27.8±2.4) mg/L。表明适度的搅拌有助于优化培养体系中的氧气传质效率和营养物质分布,促进PQQ的生物合成。
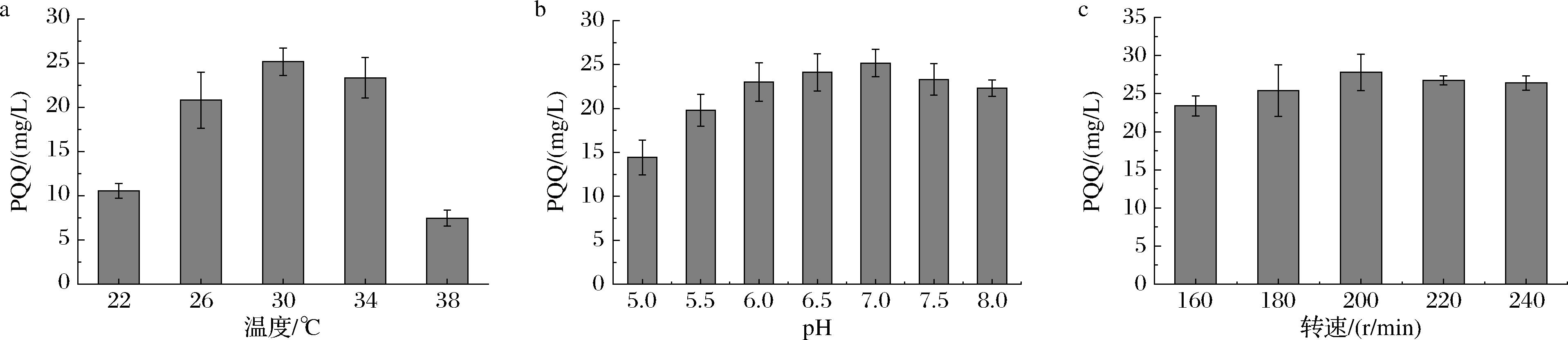
a-温度;b-pH;c-转速
图3 不同温度、pH、转速对PQQ产量的影响
Fig.3 Effects of temperature, pH, and agitation speed on PQQ production
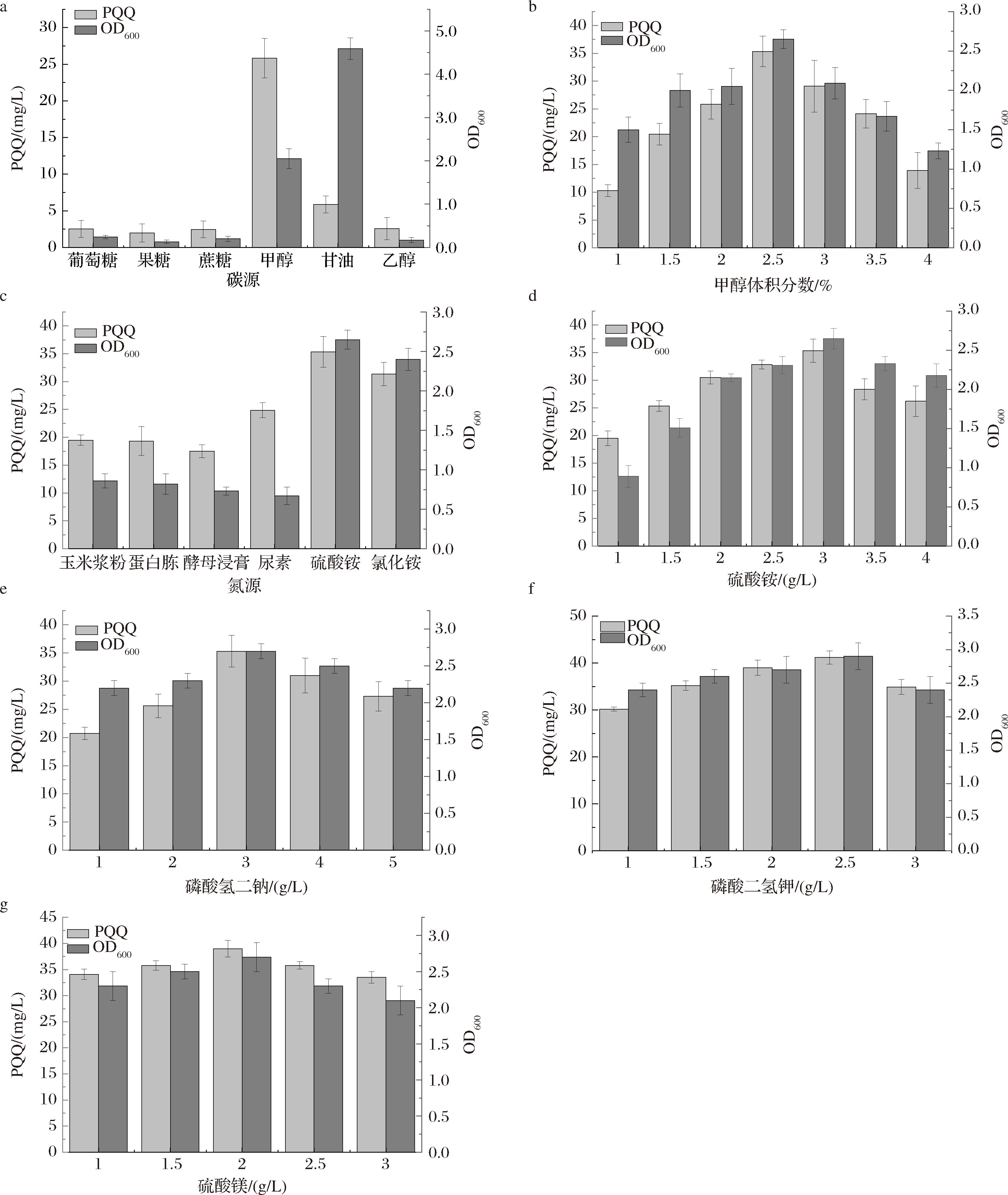
a-不同碳源;b-甲醇含量;c-不同氮源;d-硫酸铵含量;e-磷酸氢二钠含量;f-磷酸二氢钾含量;g-硫酸镁含量
图4 FQ00818菌株发酵工艺优化及其对菌株生长和PQQ产量的影响
Fig.4 Fermentation process optimization of FQ00818 strain and its effects on cell growth and PQQ production
探讨不同碳源对FQ00818生长及PQQ合成的影响。如图4-a所示,甘油有利于菌体生长,培养120 h达到OD600=4.6±0.3,甲醇次之(OD600=2.1±0.2),其他碳源均不利于菌体生长(OD600<1.0)。甲醇作为碳源时PQQ产量达到(25.8±2.7) mg/L,高于其他碳源条件下的产量(<10 mg/L)。葡萄糖等碳源可能通过碳分解代谢物抑制效应[27],阻遏了甲醇代谢相关基因的表达;甲醇作为PQQ依赖性甲醇脱氢酶的专一性底物,可促进PQQ的生物合成[28]。研究不同甲醇浓度的影响(图4-b),在体积分数为2.5%的甲醇浓度下,菌体生长(OD600=2.7±0.1)和PQQ产量[(35.3±2.8) mg/L]均达到最高。甲醇浓度过高,细胞毒性开始显现,导致细胞损伤。分析不同氮源对菌体生长和PQQ产量的影响(图4-c)。当添加硫酸铵3.0 g/L时,PQQ产量达到最高(图4-d)。有机氮源虽然富含生长因子,但其杂质成分可能干扰PQQ合成途径的精确调控。磷酸氢二钠(3.0 g/L)和磷酸二氢钾(2.5 g/L)作为磷源,既满足PQQ合成需求又维持培养液的pH,硫酸镁(2.0 g/L)作为PQQ与甲醇脱氢酶的配位金属离子,优化3个成分初始浓度使PQQ产量提升至(41.2±1.4) mg/L。
通过上述实验确定了FQ00818菌株发酵工艺参数:体积分数2.5%甲醇、3.0 g/L硫酸铵、3.0 g/L磷酸氢二钠、2.5 g/L磷酸二氢钾、2.0 g/L硫酸镁,以及30 ℃、pH 7.0、200 r/min的培养条件。后续的研究将在此基础上进行。
2.4 ARTP诱变选育高产PQQ突变株
本研究采用ARTP对野生型FQ00818菌株进行诱变,按1.4.3节中公式(1)计算诱变致死率,结果如图5-a所示。当处理时间超过50 s时,菌落致死率达99.9%,大多数细胞已失去增殖能力。根据文献致死率在90%为高效突变窗口[22],因此本研究采用30 s为最佳处理时间(致死率89.8%)。通过高通量筛选,选取单个菌落接种至48孔板进行高通量筛选,发酵结束后采用光谱法进行批量检测,对PQQ产量较高的菌株进行复筛,用HPLC法进行产量确认,最终获得一株高产突变株FQ00818-31(图5-b)。与野生型菌株相比,FQ00818-31生物量(OD600=3.1)提高了6.9%,PQQ产量达到(51.2±1.4) mg/L,较诱变前菌株[(41.2±1.4) mg/L]提升了24.3%。
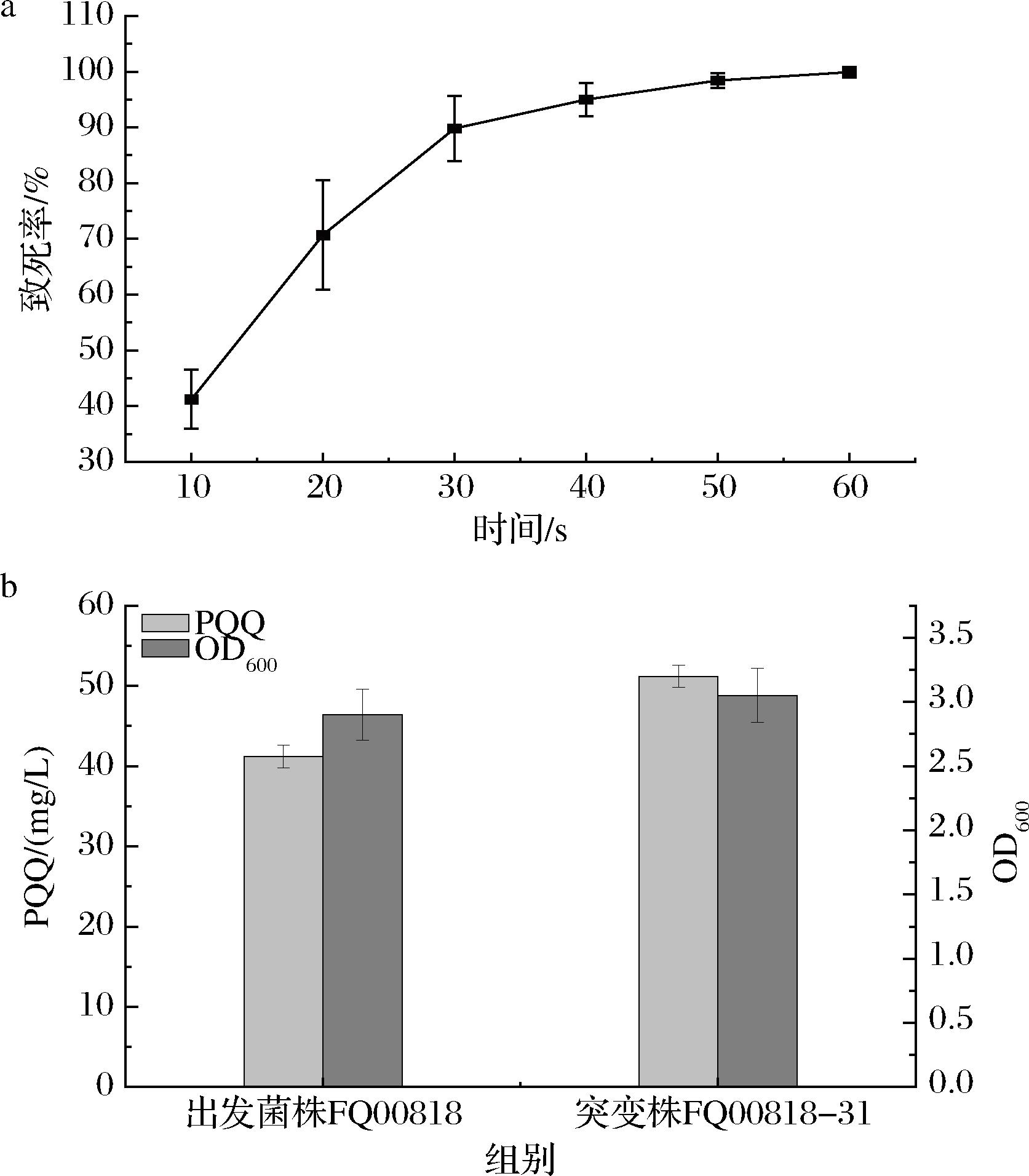
a-ARTP对菌株诱变致死曲线;b-出发菌株和突变株的生长能力和PQQ产量比较
图5 诱变选育高产PQQ菌株FQ00818-31
Fig.5 Mutagenesis breeding of high PQQ-producing strain FQ00818-31
2.5 甲醇流加补料发酵高效合成PQQ
本研究2.3节的甲醇浓度实验表明,甲醇作为唯一碳源具有一定的生物毒性,过高浓度将损害细胞生长。同时补料发酵已被证明是提高PQQ含量的有效策略[23,27-29]。因此,本研究在20 L发酵罐中,参考上述培养工艺研究和已报道的文献,以甲醇为底物,发酵过程中控制甲醇含量不超过0.5 mL/L,开展了突变株FQ00818-31的甲醇流加补料发酵工艺研究,结果如图6所示。发酵初期(0~72 h),菌体主要处于适应和生物量积累阶段,OD600稳步上升(0.3→9.5),相应的每8 h甲醇消耗量也呈增加趋势(2→60 mL/8 h),表明菌体正积极利用甲醇进行细胞增殖。在此期间PQQ的产量极少。随后进入快速生长期(72~152 h),OD600显著增长,每8 h的甲醇消耗量稳定维持在约50 mL,以支持菌体的旺盛生长。PQQ开始逐步累积,但增长速率相对平缓(10→245 mg/L)。在发酵后期(152~232 h),每8 h的甲醇消耗量急剧下降(从约60 mL骤降至约10 mL),而PQQ产量却呈现爆发式增长(245→772 mg/L)。这现象表明,菌体代谢模式在此阶段可能发生了重新定向:在甲醇低浓度稳定供应下,菌体将代谢重心从快速生物量增长转向了PQQ的高效合成,实现了生长与PQQ生产的部分解耦。在此期间,OD600增长速率放缓但仍保持在较高水平,表明了菌体进入了非快速增长但高产PQQ的生理状态。发酵至208~232 h,甲醇消耗量有所回升,OD600趋于平缓,而PQQ产量仍持续攀升并在224 h达到最高值772 mg/L。结果表明通过精准控制甲醇流加速率,诱导菌体代谢重定向,是实现PQQ高产的关键策略。
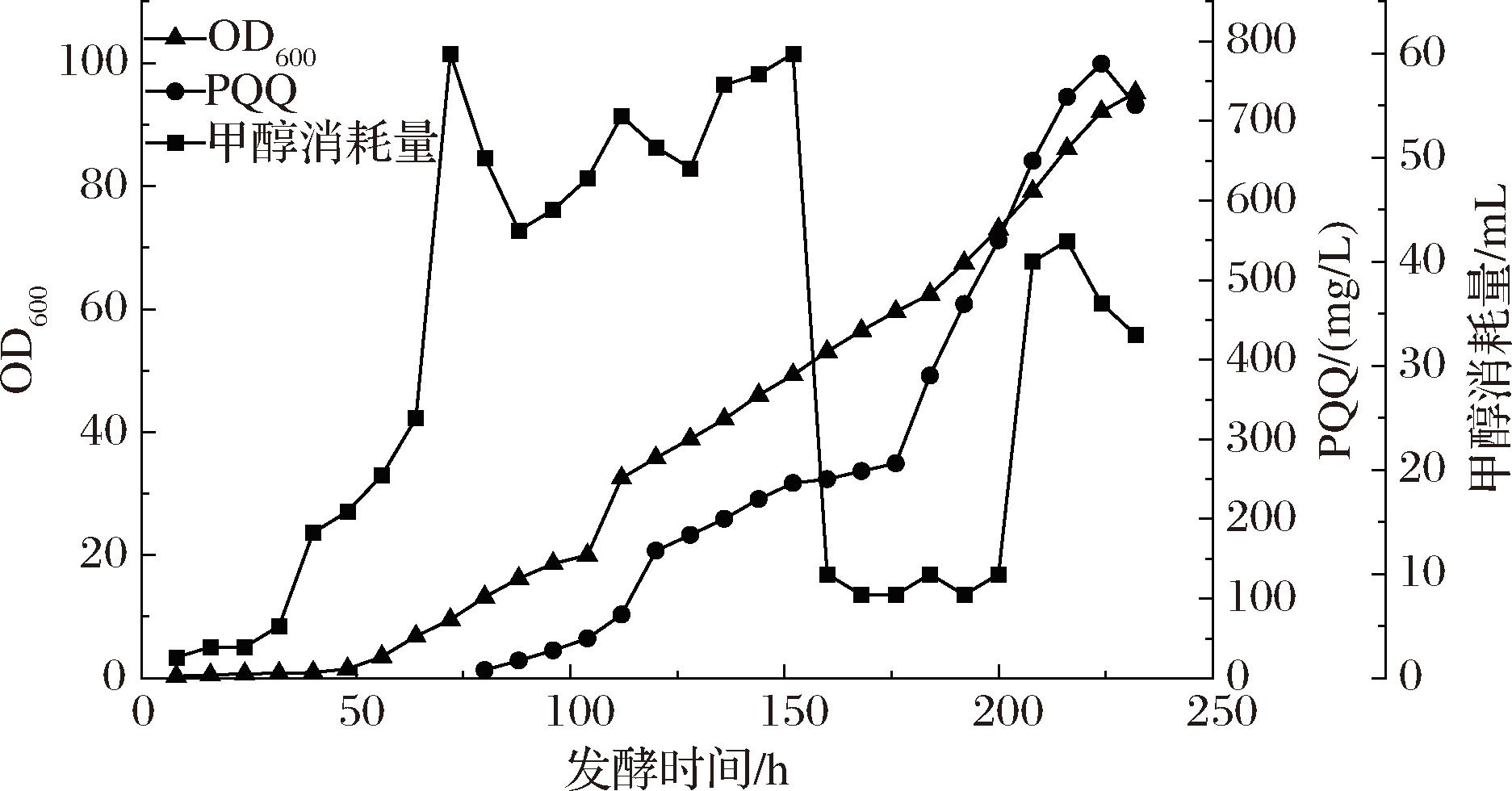
图6 菌株FQ00818-31在20 L发酵罐甲醇流加补料发酵过程中生物量、PQQ产量及甲醇消耗的变化曲线
Fig.6 Biomass, PQQ production, and methanol consumption during methanol-fed-batch fermentation of strain FQ00818-31 in a 20 L bioreactor
3 结论与讨论
本研究从环境污水样本中成功分离并鉴定出一株具有PQQ生产能力的菌株脱氮生丝微菌FQ00818。其初始PQQ产量为(25.6±1.2) mg/L,与朱道洋等[25]报道的甲基营养菌如Methylopila sp.起始产量20.6 mg/L相比,该菌株已展现出一定的生产潜力。通过单因素优化摇瓶发酵工艺,FQ00818菌株的PQQ产量提升至(41.2±1.4) mg/L,较优化前工艺提高61%。与张静等[28]报道的通过多因素正交实验Hyphomicrobium sp.产量提升94%相比仍有差距,表明后续需通过系统的发酵工艺设计和过程优化来充分挖掘菌株遗传潜力持续提升产量。本研究采用ARTP诱变技术获得高产突变株FQ00818-31,其摇瓶培养条件下PQQ产量达到(51.2±1.4) mg/L,较原始菌株提升24%。这一提升幅度与SUN等[30]通过化学诱变获得的突变株NJTU3-43的产量提升23.1%相近。尽管该提升幅度低于柯崇榕[31]通过多代诱变实现1倍左右的增长,但这充分表明通过后续多轮诱变策略,该菌株在PQQ生产方面仍具备巨大的遗传潜力待进一步挖掘,有望实现产量的大幅提升。在20 L 发酵罐中实施动态甲醇流加补料策略后,菌株FQ00818-31的PQQ产量最终达到772 mg/L。这一产量水平高于目前文献中多数报道,如WEI等[20]通过发酵工艺优化使Methylobacterium sp.zju323的PQQ产量达到232 mg/L。SUN等[30]在5.0 L生物反应器分批补料发酵突变株NJTU3-43的PQQ产量为208.4 mg/L。尽管低于郑玲辉等[17]多种方式诱变Hyphomicrobium sp.在80 T发酵罐中获得的1.78 g/L和REN等[18]通过多代诱变及适应性进化Hyphomicrobium sp.FJNU-A26获得的1.52 g/L,但本研究通过快速高通量筛选、发酵工艺优化、ARTP诱变及精准补料的系统策略,在较短周期内实现了高产量,充分展现了该菌株在大规模生产中的巨大潜力及工业应用价值。
尽管本研究在PQQ高产菌株的筛选和发酵工艺优化方面取得了一定进展,但对菌体在生长过程中代谢模式由侧重生物量积累转向高效产物合成的深层调控机制及其如何维持其高产效率,仍有待更深入研究,以期实现产量的持续突破。为进一步挖掘该菌株的PQQ合成潜力,未来的研究工作应着重于深入代谢机制解析,结合基因组学、转录组学和代谢组学等多组学技术,系统解析菌体在生长后期或特定高产阶段,代谢流如何高效地从生物量积累向PQQ合成重定向的深层分子机制,分析甄别影响PQQ合成关键全局调控基因,为菌株的理性设计和代谢工程改造提供理论依据,以期进一步提升PQQ的累积量和生产效率。此外,基于对代谢机制的深入理解,还需优化补料策略与发酵控制,开发更精细化的动态甲醇补料控制策略,实现甲醇供给与菌体代谢状态的精准匹配,最大化PQQ合成效率并延长高产周期。
[1] HAUGE J G.Glucose dehydrogenase of bacterium anitratum:An enzyme with a novel prosthetic group[J].Journal of Biological Chemistry, 1964, 239(11):3630-3639.
[2] HARRIS C B, CHOWANADISAI W, MISHCHUK D O, et al.Dietary pyrroloquinoline quinone (PQQ) alters indicators of inflammation and mitochondrial-related metabolism in human subjects[J].The Journal of Nutritional Biochemistry, 2013, 24(12):2076-2084.
[3] KILLGORE J, SMIDT C, DUICH L, et al.Nutritional importance of pyrroloquinoline quinone[J].Science, 1989, 245(4920):850-852.
[4] MUKAI K, OUCHI A, NAGAOKA S I, et al.Pyrroloquinoline quinone (PQQ) is reduced to pyrroloquinoline quinol (PQQH2) by vitamin C, and PQQH2 produced is recycled to PQQ by air oxidation in buffer solution at pH 7.4[J].Bioscience, Biotechnology, and Biochemistry, 2016, 80(1):178-187.
[5] ZHANG Q, DING M, CAO Z, et al.Pyrroloquinoline quinone protects rat brain cortex against acute glutamate-induced neurotoxicity[J].Neurochemical Research, 2013, 38(8):1661-1671.
[6] SHIOJIMA Y, TAKAHASHI M, TAKAHASHI R, et al.Effect of dietary pyrroloquinoline quinone disodium salt on cognitive function in healthy volunteers:A randomized, double-blind, placebo-controlled, parallel-group study[J].Journal of the American Nutrition Association, 2022, 41(8):796-809.
[7] LIU S Q, LI H H, OUYANG J P, et al.Enhanced rat sciatic nerve regeneration through silicon tubes filled with pyrroloquinoline quinone[J].Microsurgery, 2005, 25(4):329-337.
[8] EBELING M C, POLANCO J R, QU J, et al.Improving retinal mitochondrial function as a treatment for age-related macular degeneration[J].Redox Biology, 2020, 34:101552.
[9] DAI X L, YI X J, WANG Y F, et al.PQQ dietary supplementation prevents alkylating agent-induced ovarian dysfunction in mice[J].Frontiers in Endocrinology, 2022, 13:781404.
[10] PENG Y, XU D, DING Y D, et al.Supplementation of PQQ from pregnancy prevents MK-801-induced schizophrenia-like behaviors in mice[J].Psychopharmacology, 2022, 239(7):2263-2275.
[11] JONSCHER K R, CHOWANADISAI W, RUCKER R B.Pyrroloquinoline-quinone is more than an antioxidant:A vitamin-like accessory factor important in health and disease prevention[J].Biomolecules, 2021, 11(10):1441.
[12] WU X, LI J, ZHANG H W, et al.Pyrroloquinoline quinone prevents testosterone deficiency-induced osteoporosis by stimulating osteoblastic bone formation and inhibiting osteoclastic bone resorption[J].American Journal of Translational Research, 2017, 9(3):1230-1242.
[13] 何秀兰, 彭宇翔, 陶禹, 等.醋酸钙不动杆菌合成吡咯喹啉醌发酵条件优化及干旱胁迫下对辣椒生长的影响[J].微生物学报, 2025, 65(1):182-195.HE X L, PENG Y X, TAO Y, et al.Acinetobacter calcoaceticus CDWB36:Optimization of fermentation conditions for pyrroloquinoline quinone production and effect on growth of pepper under drought stress[J].Acta Microbiologica Sinica, 2025, 65(1):182-195.
[14] GAO H, WANG Y S, YANG J H, et al.Microbial synthesis of pyrroloquinoline quinone[J].World Journal of Microbiology and Biotechnology, 2024, 40:31.
[15] SI Z J, MACHAKU D, WEI P L, et al.Enhanced fed-batch production of pyrroloquinoline quinone in Methylobacillus sp.CCTCC M2016079 with a two-stage pH control strategy[J].Applied Microbiology and Biotechnology, 2017, 101(12):4915-4922.
[16] XIONG X H, ZHAO Y, GE X, et al.Production and radioprotective effects of pyrroloquinoline quinone[J].International Journal of Molecular Sciences, 2011, 12(12):8913-8923.
[17] 郑玲辉,杜敏娜,朱小容,等.一种生丝微菌和吡咯喹啉醌的制备方法:中国, CN106282044B[P].2019-10-29.ZHENG L H, DU M N, ZHU X R, et al.Hyphomicrobium sp.and preparation method for pyrroloquinoline quinone:China, CN106282044B[P].2019-10-29.
[18] REN Y, YANG X W, DING L T, et al.Adaptive evolutionary strategy coupled with an optimized biosynthesis process for the efficient production of pyrroloquinoline quinone from methanol[J].Biotechnology for Biofuels and Bioproducts, 2023, 16:11.
[19] ZHAO C L, WAN Y P, CAO X J, et al.Mechanism of PQQ and CoQ10 overproduction in Methylobacterium as revealed by comparative genomic analysis between mutant and wild-type strains[J].World Journal of Microbiology and Biotechnology, 2021, 37(6):1-10.
[20] WEI P L, SI Z J, LU Y, et al.Medium optimization for pyrroloquinoline quinone (PQQ) production by Methylobacillus sp.zju323 using response surface methodology and artificial neural network-genetic algorithm[J].Preparative Biochemistry &Biotechnology, 2017, 47(7):709-719.
[21] 叶润乐, 李沣, 丁凡, 等. 基于重组氧化葡萄糖酸杆菌生物合成吡咯喹啉醌[J]. 生物工程学报, 2020, 36(6):1138-1149.YE R L, LI F, DING F, et al. Synthesis of pyrroloquinoline quinone by recombinant Gluconobacter oxydans[J]. Chinese Journal of Biotechnology, 2020, 36(6):1138-1149.
[22] 李文鑫, 曾伟主, 周景文.高产辅酶Q10类球红细菌的选育及发酵优化[J].食品与发酵工业, 2022, 48(23):34-41;56.LI W X, ZENG W Z, ZHOU J W.Breeding and fermentation optimization of Rhodobacter sphaeroides with high yield of coenzyme Q10[J].Food and Fermentation Industries, 2022, 48(23):34-41;56.
[23] 赵子刚, 金明义, 刘露, 等.吡咯喹啉醌连续发酵工艺初探[J].食品与发酵工业, 2024, 50(5):29-34.ZHAO Z G, JIN M Y, LIU L, et al.Preliminary study on continuous fermentation process of pyrroloquinoline quinone[J].Food and Fermentation Industries, 2024, 50(5):29-34.
[24] 杨延新, 熊向华, 游松, 等.3种检测吡咯喹啉醌的方法比较[J].生物技术通讯, 2011, 22(4):544-547.YANG Y X, XIONG X H, YOU S, et al.Comparing three kinds of pyrroloquinoline quinone detection methods[J].Letters in Biotechnology, 2011, 22(4):544-547.
[25] 朱道洋, 魏春雨, 余晓斌.吡咯喹啉醌产生菌的筛选和菌种鉴定[J].食品与发酵工业, 2021, 47(10):159-163.ZHU D Y, WEI C Y, YU X B.Screening and identification of pyrroloquinoline quinone producing strains[J].Food and Fermentation Industries, 2021, 47(10):159-163.
[26] KALIMUTHU P, DAUMANN L J, POL A, et al.Electrocatalysis of a europium-dependent bacterial methanol dehydrogenase with its physiological electron-acceptor cytochrome cGJ[J].Chemistry-A European Journal, 2019, 25(37):8760-8768.
[27] DUSNY C, SCHMID A.The MOX promoter in Hansenula polymorpha is ultrasensitive to glucose-mediated carbon catabolite repression[J].FEMS Yeast Research, 2016, 16(6):fow067.
[28] 张静, 刘孟粟, 秦志杰, 等.吡咯喹啉醌高产菌株选育及发酵优化[J].食品与发酵工业, 2022, 48(16):56-64.ZHANG J, LIU M S, QIN Z J, et al.Breeding and fermentation optimization of high titer pyrroloquinoline quinone strain[J].Food and Fermentation Industries, 2022, 48(16):56-64.
[29] SI Z J, ZHU J Z, WANG W G, et al.Novel and efficient screening of PQQ high-yielding strains and subsequent cultivation optimization[J].Applied Microbiology and Biotechnology, 2016, 100(24):10321-10330.
[30] SUN J X, YUE H T, MA W X, et al.Breeding and genomic analysis of the high PQQ-producing strain Hyphomicrobium denitrificans NJTU3-43[J].Chemical Engineering Journal, 2025, 511:162001.
[31] 柯崇榕.适应性驯化选育高产吡咯喹啉醌的生丝微菌突变株[J].生物工程学报, 2020, 36(1):152-161.KE C R.Breeding of Hyphomicrobium denitrificans for high production of pyrroloquinoline quinone by adaptive directed domestication[J].Chinese Journal of Biotechnology, 2020, 36(1):152-161.