糖尿病是全球最为普遍的代谢紊乱疾病之一,其主要特征为血糖的异常升高[1]。在糖尿病的形成中,α-葡萄糖苷酶是一种存在于肠细胞刷状缘表面膜上的水解酶,能够通过水解低聚糖非还原端葡萄糖基残基与葡萄糖基氧之间的α-1,4糖苷键来促进游离葡萄糖分子的释放,从而导致血糖升高[2-3]。因此,抑制α-葡萄糖苷酶活性是降低餐后血糖水平、缓解和干预治疗2型糖尿病的有效策略之一[4]。近年来,食源性α-葡萄糖苷酶抑制肽因其低免疫原性、干预治疗糖尿病效果明显、较传统α-葡萄糖苷酶抑制剂副作用低等优点备受研究学者关注[5-6]。值得注意的是,肉类蛋白及其衍生肽已被报道为天然血糖调节剂的潜在来源。例如,来自猪肉中的肽GF,MW,MF,PF,PW具有维持血糖稳态和抗糖尿病的功能特性[7]。伊比利亚干腌火腿[8]、大河乌猪火腿[6]和皖浙花猪火腿[1]腌制和后熟过程中产生的小肽AEEEYPDL、GGLGP、LGVGG、GPMGPSGPR、LGFGGPSGPNAGR、APAPAPAPAPAPPK和IEEALGDK具有较强的α-葡萄糖苷酶抑制活性,是潜在的血糖调节肽。这说明火腿蛋白肽也是血糖调节剂的潜在来源。然而,有关火腿源α-葡萄糖苷酶抑制肽的研究仍然较少。因此,进一步从其他干腌火腿中提取和分离降血糖肽,研究其结构特征和相关的降血糖机制是有必要的[9]。
近年来,随着肉类市场需求的不断增大,杂交育种成为一种提高本地猪生长速率、瘦肉率和经济价值的有效方法。同时,杂交猪也渐渐成为生产火腿的原料,其火腿中潜在的营养品质有待探究[4]。约长大乌杂交猪是一种以约克夏猪、长白猪与云南大河乌猪杂交而来的新品种杂交猪种[10]。先前的研究揭示了约长大乌杂交猪火腿的风味物质和理化指标,其蛋白质含量为(32.6±3.5) mg/100 g,明显高于大河乌猪火腿[(29±2.3) mg/100 g],主要的风味物质以短链脂肪酸、醇类和醛类等代谢物为主[11]。这说明杂交育种可能有助于提高本地猪火腿蛋白质含量等营养品质。此外,探究火腿中的生物活性肽,也是解析和证明火腿潜在营养价值和优良品质的重要手段之一[1]。HU等[9]报道,干腌火腿是天然生物活性肽的丰富来源,火腿中生物活性肽是其营养和潜在健康益处的体现。WANG等[4]基于肽组学、分子构型关系和分子模拟技术快速挖掘洋三元杂交猪火腿的生物活性肽,研究发现提取肽YDEAGPSIVH不仅有助于延长火腿贮藏期,还可能具有潜在的血糖调节功能。黄晶晶等[1]基于肽组学、计算机分析和量子力学探究了皖浙花猪干腌火腿源血糖调节肽的作用机制,为证明皖浙花猪的营养价值提供了理论支撑。此外,源于大河乌猪火腿的提取肽具有较强的α-葡萄糖苷酶抑制活性,这表明以其杂交猪为原料生产的约长大乌杂交猪干腌火腿也可能是α-葡萄糖苷酶抑制肽的潜在来源[6]。因此,解析约长大乌杂交猪干腌火腿肽的α-葡萄糖苷酶抑制活性不仅能够丰富火腿中α-葡萄糖苷酶抑制肽的研究,还有助于表征其潜在的生物学价值。然而,约长大乌杂交猪干腌火腿中肽的α-葡萄糖苷酶抑制活性及其作用机理尚未进行研究。
随着科学技术的高速发展,基于计算机分析、分子对接和分子构效关系的生物信息分析方法因为快速、高效、低成本等优点,而被广泛用于筛选并预测生物活性肽的潜在作用机制[5-6]。同时,网络药理学也被作为一种有效工具,主要用于预测功能活性物质对相关疾病治疗的潜在机制[12]。基于此,本研究对约长大乌杂交猪干腌火腿中的多肽进行超滤和鉴定,基于计算机工具预测和分子对接技术筛选新型的α-葡萄糖苷酶抑制肽,并进行肽的活性验证和体外消化测定,最后通过网络药理学方法进一步探究新型肽防治糖尿病的潜在作用靶点和潜在的途径,以期为解析杂交猪干腌火腿的潜在营养价值和进一步的精深加工利用提供新思路。
1 材料与方法
1.1 材料与试剂
约长大乌杂交猪火腿,云南东恒集团火腿有限公司;对硝基苯基-β-D-吡喃葡萄糖苷(p-nitrophenyl β-D-glucopyranoside,PNPG),上海宝曼生物科技有限公司;甲酸、乙腈、甲醇,德国默克股份两和公司;α-葡萄糖苷酶(700 000 U/mL),上海源叶生物科技有限公司;火腿肽FLGFPTTKF和IIPADLEAK(纯度>95%),生工生物工程(上海)股份有限公司;超滤膜,上海摩速科学器材有限公司;本实验所用其他实验材料和试剂均为国产分析纯。
1.2 仪器与设备
Millipore UFSC40001型超滤装置,上海羽令过滤器材有限公司;L6 J-12冷冻干燥机,郑州南北仪器设备有限公司;Nano-HPLC液相色谱仪,上海赛梵科分离技术有限公司;Easy-nLC 1000液相色谱仪、Q Exactive四极杆质谱仪、Thermo MultiskaTM FC酶标仪,赛默飞世尔科技公司。
1.3 实验方法
1.3.1 肽的提取及超滤分离
参照WANG等[4]的方法制备火腿肽。取适量火腿的肱二头肌部分,剔除脂肪,加入液氮冷冻、细磨。向25 g细磨后的火腿中添加100 mL 0.01 mol/L的盐酸,充分搅拌10 min,使用高速分散器进行匀浆剪切;离心后,向上清液中添加3倍体积的甲醇,经20 h的静置冷藏和离心,除去蛋白质沉淀,得到火腿粗肽提取液。用分子质量为3 kDa的超滤膜分离出F1(MW<3 kDa)和F2(MW>3 kDa)2个组分的超滤肽,真空冷冻干燥,保存于-80 ℃冰箱中备用。
1.3.2 α-葡萄糖苷酶抑制活性测定
分别向96孔板中加入体积为100 μL的样品肽溶液和50 μL的α-葡萄糖苷酶溶液(700 U/mL),在37 ℃恒温培养箱中孵育20 min后,加入50 μL 10 mmol/L PNPG溶液;紧接着,将混合反应液再次移入37 ℃恒温培养箱中孵育0.5 h,最后加入50 μL 0.67 mol/L的Na2CO3溶液终止反应。以0.02 mol/L的磷酸盐缓冲液(pH 6.8)作为对照组。使用酶标仪在吸收波长为405 nm处测定反应液的OD值,计算样品肽的α-葡萄糖苷酶抑制率。通过拟合α-葡萄糖苷酶抑制率与肽浓度的线性回归方程,计算各样品肽抑制α-葡萄糖苷酶的IC50值。α-葡萄糖苷酶抑制率的计算如公式(1)所示[6]:
α-葡萄糖苷酶抑制率![]()
(1)
式中:Ac为对照组的OD值;Ab为空白组的OD值;As为样品组的OD值;An为样品空白对照的OD值。
1.3.3 火腿肽的鉴定
委托上海中科新生命生物科技有限公司使用液相色谱质谱联用仪对F1组分的火腿超滤肽进行鉴定。使用Proteome Discoverer 1.4软件和数据库(Uniprot-Sus-scrofa-122175-20220218)进行鉴定肽的查库鉴定和比对分析[6]。
1.3.4 生物信息学分析
基于ToxinPred在线工具(https://webs.iiitd.edu.in/raghava/toxinpred/multi_submit.php)评估鉴定肽的安全性;通过PepDraw(https://pepdraw.com/)评估鉴定肽的净电荷和等电点。采用PEPTIDE 2.0在线工具(https://www.peptide2.com/)评估鉴定肽的疏水性氨基酸占比。使用Expasy系统(https://web.expasy.org/protparam/)评估鉴定肽的不稳定指数,不稳定指数>40的肽为不稳定性肽。通过BIOPEP和EROP-Moscow等生物活性肽数据库检索筛选肽的新颖性。通过ADMET lab 2.0在线系统(https://admetmesh.scbdd.com/service/evaluation/cal)评估新型α-葡萄糖苷酶抑制肽的药物代谢动力学(absorption distribution metabolism excretion toxicity, ADMET)。DFBF系统(http://cqudfbp.net/enzymes/hydrolysis_tools/dataInput.jsp)用于预测α-葡萄糖苷酶抑制肽的计算机模拟消化的酶解片段及其片段的生物活性。
1.3.5 分子对接
参照XIE等[13]的方法,使用Discovery Studio 2019软件进行多肽与α-葡萄糖苷酶的分子对接。使用Chem3D 20.0绘制小分子肽的3D结构并进行能量优化,定义小分子肽为配体。从PDB数据库(http://www.rcsb.org)下载α-葡萄糖苷酶受体(PDB ID:3 WY1)的3D结构,去除蛋白周围水分子和多余配体,将该蛋白定义为受体。根据CDOCKER评分确定最佳对接构象。对接得分由结合能(-CDOCKER_energy,-CE)和亲和力(-CDOCKER_interaction_energy,-CIE)表示,用于评估配体-受体相互作用的强度。紧接着,利用Discovery Studio 2019软件receptorligand Interactions模块中的Ligand Interactions(Interaction options),分析肽段与α-葡萄糖苷酶的关键作用位点和相互作用方式(包含:氢键、疏水相互作用及静电相互作用)[12]。
1.3.6 体外消化稳定性
参照LI等[14]的方法稍作修改,评估体外模拟胃肠消化对新型肽生物活性的影响。用浓度为0.01 mol/L HCl溶液配制2份pH值为2,质量浓度为2 mg/mL的肽溶液,向混合溶液中加入1%(质量分数,以底物质量计)的胃蛋白酶,37 ℃条件下恒温振荡反应3 h得到2份胃消化液。取其中一份胃消化液于90 ℃水浴锅中恒温水浴10 min灭酶处理,冷藏备用。用0.01 mol/L的NaOH溶液调节另一份胃消化液的pH值至8,加入1%(质量分数,以底物质量计)的胰蛋白酶和糜蛋白酶,37 ℃条件下恒温振荡反应3 h,于90 ℃条件下恒温水浴灭酶,得到肠消化液。通过测定2种不同消化阶段条件下样品的α-葡萄糖苷酶抑制活性来评价肽的胃肠消化稳定性。
1.3.7 网络药理学分析
1.3.7.1 肽对糖尿病潜在作用靶点预测
参考李佳芸等[15]的方法稍作修改,基于Swiss Target Prediction平台(http://www.swisstargetprediction.ch/)预测肽FLGFPTTKF在体内的潜在作用靶点。同时,采用Genecards在线平台(https://www.genecards.org/)获取2型糖尿病相关的基因靶点,所设关键词为“diabetes”。最后,通过相同靶点比对,去重取并集,绘制药物和疾病基因靶点韦恩图(http://bioinformatics.psb.ugent.be/webtools/Venn/),获取到肽FLGFPTTKF治疗糖尿病的潜在作用靶点。
1.3.7.2 蛋白质-蛋白质相互作用(protein-protein interaction, PPI)网络构建
将肽FLGFPTTKF的潜在作用靶点置入STRING平台(https://cn.string-db.org/)进行蛋白质-蛋白质相互作用分析(PPI网络);参数设置为“Homo sapiens”、置信度>0.4,其余参数选择默认参数[13]。利用Cytoscape 3.9.0软件中的CytoNCA插件对PPI网络进行拓扑属性分析,计算网络拓扑参数,度值大小用来评估节点在网络中的重要性[12]。
1.3.7.3 GO分析及KEGG通路富集分析
参照XIE等[13]的方法,基于GO功能富集和KEGG代谢通路富集分析,研究了肽FLGFPTTKF干预治疗糖尿病的潜在作用靶点和涉及到的相关路径。将FLGFPTTKF的潜在作用靶点导入到DAVID(https://david.nci fcrf.gov/home.jsp)平台中,设定限定物种为“Homo sapiens”,P<0.05。在微生信平台(http://www.bioinformatics.com.cn/)上,对富集到的结果进行GO富集结果和KEGG通路富集分析的可视化[12]。
1.4 数据统计分析
所有实验皆重复3次,结果以“平均值±标准差”表示。采用IBM SPSS 25.0软件分析实验数据,基于单因素方差分析进行Duncan检验,P<0.05表示数据具有显著性差异;采用Origin 2021b进行图表绘制。
2 结果与分析
2.1 火腿超滤肽的α-葡萄糖苷酶抑制活性
抑制α-葡萄糖苷酶活性能够减缓碳水化合物的消化,从而降低血液中葡萄糖水平,有助于缓解糖尿病及相关并发症[16]。使用分子质量为3 kDa的超滤膜进行分离,并测定了不同组分火腿超滤肽的α-葡萄糖苷酶抑制活性。由图1可知,不同超滤组分火腿肽的α-葡萄糖苷酶抑制活性随其样品质量浓度的增加而提高,且F1(<3 kDa)组分的生物活性明显强于F2(>3 kDa)组分。赵才冬等[17]研究了甲鱼蛋蛋白水解物的α-葡萄糖苷酶抑制活性,12 mg/mL超滤肽(MW<2.5 kDa)及其胃消化产物的活性都低于60%,低于本研究结果中的FI组分(68.96%)。前人研究发现,MW<3 kDa的洋三元杂交猪火腿肽具有比其他超滤组分更强的抗氧化活性和α-葡萄糖苷酶抑制活性[4],与本研究结果类似。此外,分子质量是蛋白质水解物生物活性的决定因素之一,分子质量较低的短肽不仅稳定性和溶解性好,还有助于与溶液中的底物结合反应[4,18],这可能是F1组分活性更强的原因。总之,F1组分的火腿超滤肽具有较强的α-葡萄糖苷酶抑制活性,可对其进行鉴定分析,以确定肽的氨基酸序列组成。
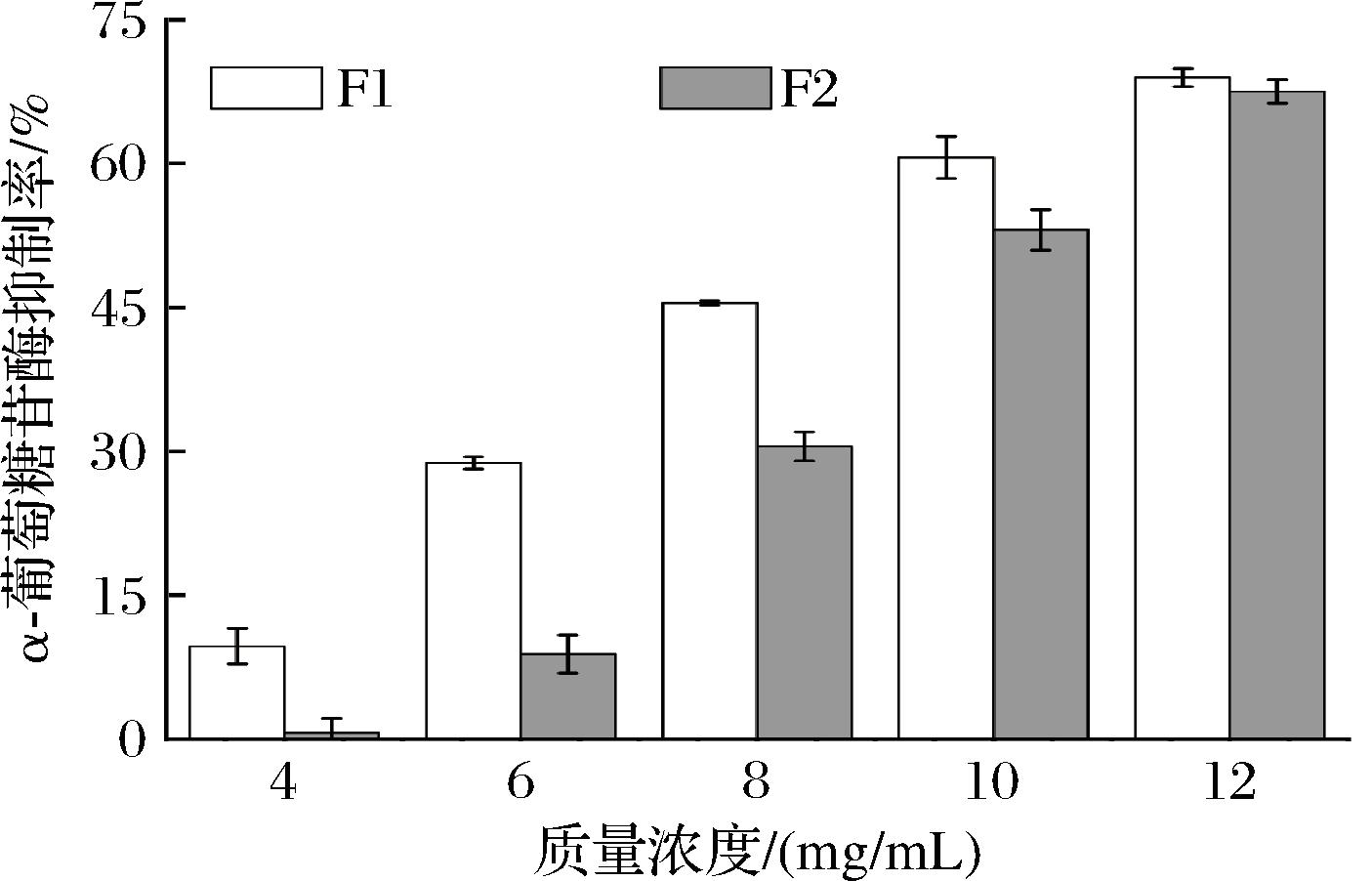
图1 火腿不同超滤组分肽的α-葡萄糖苷酶抑制活性
Fig.1 α-glucosidase inhibitory activity of different ultrafiltration fractions of ham peptides
2.2 火腿肽的质谱鉴定及新型活性肽的筛选
2.2.1 质谱鉴定
通过液相色谱质谱联用技术鉴定火腿F1组分的肽谱,共鉴定137条肽序列,鉴定肽的总离子流色谱图见图2-a。由图2-b可知,鉴定肽主要来源于肌球蛋白(57条)、肌红蛋白(10条)和肌钙蛋白(9条)。这些肽序列主要由9~20个氨基酸组成,数量高达117条(图2-c);其分子质量主要分布1 000~2 000 Da,占比达到60%(图2-d)。前人研究报道,生物活性肽是由2~20个氨基酸组成的寡肽[19],大多数具有血糖调节活性的肽分子质量低于2 000 Da[18]。本研究中,大部分鉴定肽的分子质量和链长分布结果与这一条件符合。这表明可以从鉴定肽中进一步筛选潜在的生物活性肽。
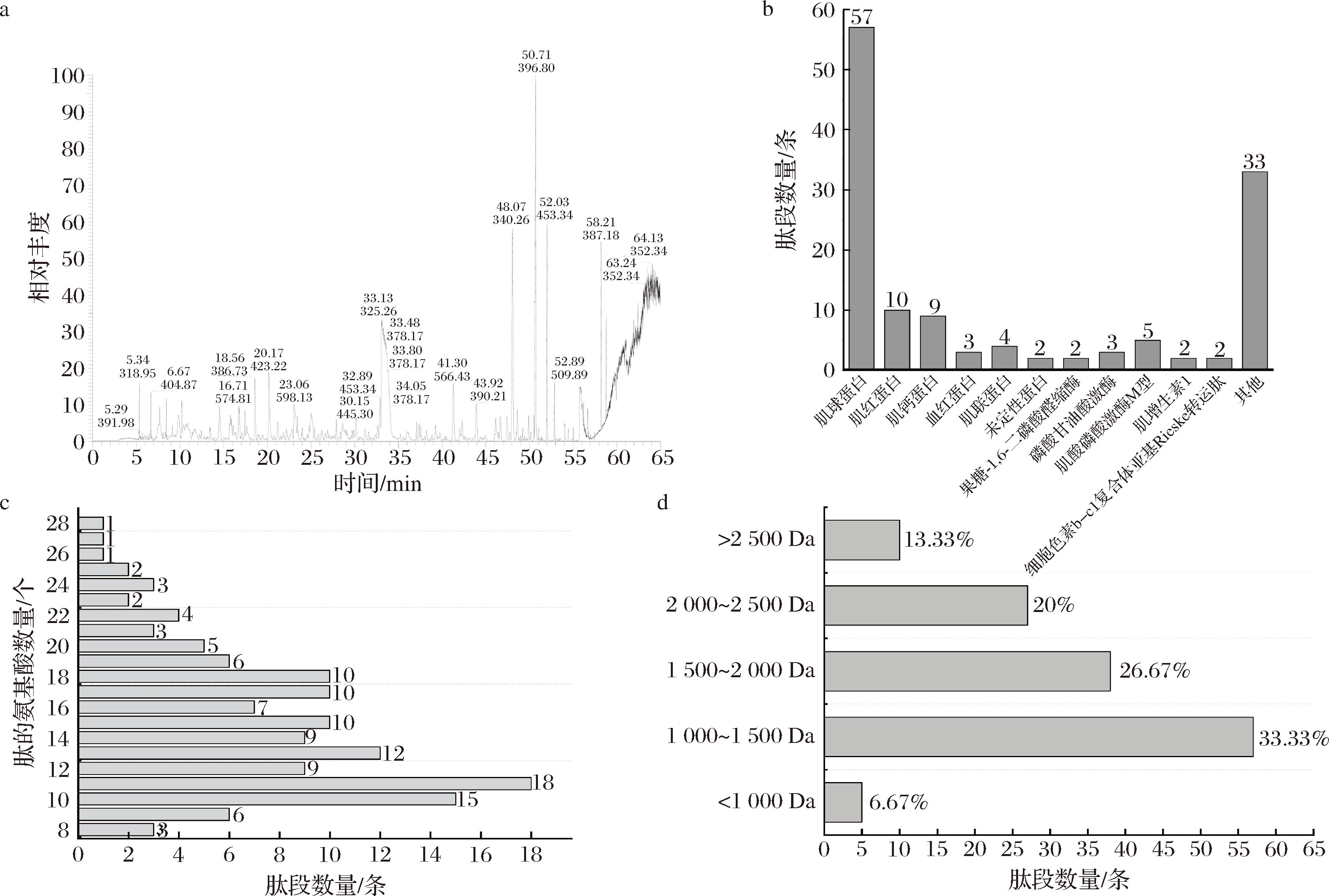
a-总离子色谱;b-肽的主要蛋白来源;c-肽的链长分布;d-肽的分子质量分布
图2 火腿肽的鉴定和分析
Fig.2 Identification and analysis of ham peptides
2.2.2 新型α-葡萄糖苷酶抑制肽的筛选
综合生物活性肽的结构组成、生物信息学分析和理化特性进一步筛选新型的α-葡萄糖苷酶抑制肽。据报道,具有较强α-葡萄糖苷酶抑制活性的生物活性肽,氨基酸残基数量小于10,分子质量低于1 000 Da[6,20]。在本研究中,仅有4条肽满足这一条件(表1)。此外,肽的疏水性、稳定性和安全性等会直接影响肽的结构、功能和吸收利用。肽不稳定性指数小于40时被认为是稳定的,而高于40则稳定性较差[21]。较强的疏水活性不仅有助于提高肽的α-葡萄糖苷酶抑制活性,还有助于促进肽在细胞膜等磷脂结构中的溶解度,促进其吸收利用[19,22]。如表1所示,筛选到的4条肽段皆无毒性,DHLEPEEK不稳定性指数为95.30,稳定性较差。YKELGFQG和DHLEPEEK的疏水性氨基酸占比较低,仅为25%。综合肽的不稳定性指数和疏水特性,本实验进一步挑选出无毒、疏水性较高和稳定性好的FLGFPTTK和IIPADLEAK这2条潜在的α-葡萄糖苷酶抑制肽,2条肽的二级质谱图如图3所示。经BIOPEP和EROP-Moscow等生物活性肽数据库检索,2条肽均为新型肽,未被研究报道。
表1 多肽的理化性质预测
Table 1 Predicted physicochemical properties of peptides
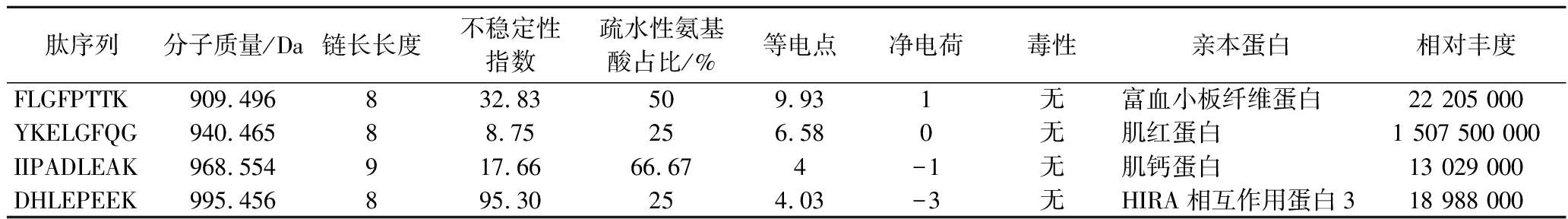
肽序列分子质量/Da链长长度不稳定性指数疏水性氨基酸占比/%等电点净电荷毒性亲本蛋白相对丰度FLGFPTTK909.496832.83509.931无富血小板纤维蛋白22 205 000YKELGFQG940.46588.75256.580无肌红蛋白1 507 500 000IIPADLEAK968.554917.6666.674-1无肌钙蛋白13 029 000DHLEPEEK995.456895.30254.03-3无HIRA相互作用蛋白318 988 000
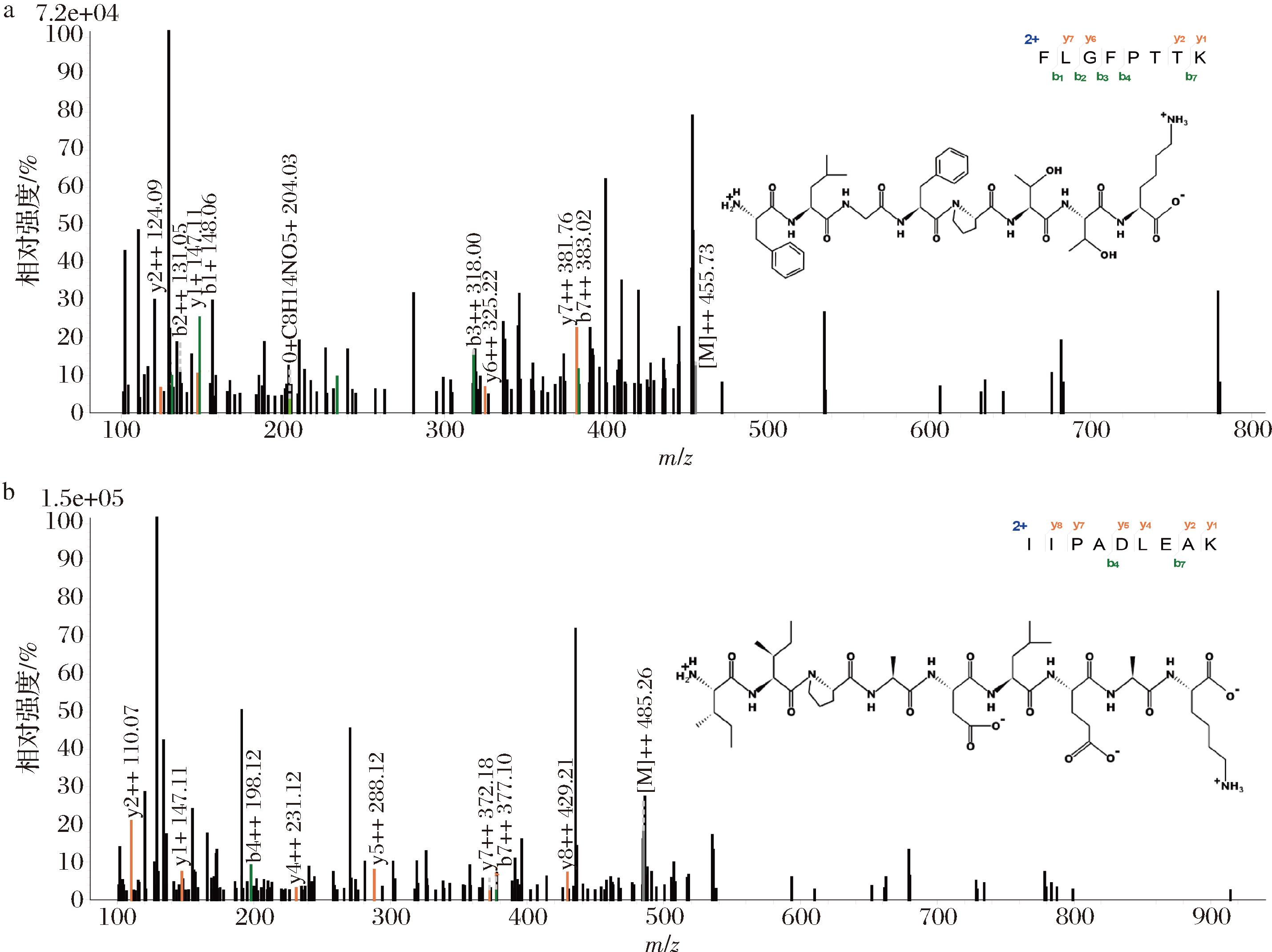
a-FLGFPTTK;b-IIPADLEAK
图3 新型肽FLGFPTTK和IIPADLEAK的二级质谱图
Fig.3 Secondary mass spectra of the novel peptides FLGFPTTK and IIPADLEAK
2.2.3 药代动力学分析
由表2可知,2条肽都具有较好的人体肠道吸收特性(HIA+)和Caco-2渗透性,未显示出P-糖蛋白抑制活性,这说明2条肽吸收性较好,不会影响其他物质的转运吸收[13]。同时,2条肽均未表现出细胞色素P450/2D6抑制性、PPB低于90%、不容易跨过血脑屏障(BBB-),这说明这些肽均不会影响药物结合的效率,不会干扰到其他物质的代谢[12]。总之,FLGFPTTK和IIPADLEAK都具有良好的吸收和代谢特性,可进一步研究利用。
表2 新型肽的ADMET分析
Table 2 ADMET analysis of novel peptides

肽段肠道吸收(human intestinal absorption,HIA)Caco-2渗透性P-糖蛋白抑制性细胞色素P450/2D6抑制性血脑屏障穿透性(blood brain barrier,BBB)血浆蛋白结合率(plasma protein binding,PPB)/%FLGFPTTKHIA+-7.02无无BBB-24.53IIPADLEAKHIA+-7.543无无BBB-15.22
注:注:HIA+表示具有较好的人体肠道吸收特性;BBB-表示不容易跨过血脑屏障。
2.2.4 分子对接模拟解析肽的潜在作用机理
基于分子对接技术预测和阐明了肽与α-葡萄糖苷酶之间的潜在结合机制,结果如图4和表3所示。由图4-a和图4-b可知,FLGFPTTKF和IIPADLEAK都能很好地嵌入到α-葡萄糖苷酶的活性空腔内。FLGFPTTKF与α-葡萄糖苷酶之间的结合能(-CE)和亲和力(-CIE)分别为133.234和122.487 kcal/mol;IIPADLEAK与α-葡萄糖苷酶之间的结合能和亲和力分别为164.231和132.902 kcal/mol(表3)。-CIE代表配体和受体之间的最小结合能,-CE不仅包括结合能,还包括配体的应变能。ZHANG等[23]表明,高且正的-CIE或-CE通常与相互作用过程中的高能量释放有关,这意味着配体与受体之间的结合是自发产生的。马寅龙等[24]研究表明,受体与配体间的结合能和亲和力越高,其复合物之间结合得越容易和越紧密。在本研究中,FLGFPTTKF和IIPADLEAK的结合能和亲和力都为正,且IIPADLEAK的值更大(表3)。这说明,2条肽都可能具有潜在的α-葡萄糖苷酶抑制活性,且IIPADLEAK与α-葡萄糖苷酶形成的复合物更佳稳定。
表3 新型肽与α-葡萄糖苷酶分子的相互作用模式
Table 3 Interaction patterns of novel peptides with α-glucosidase molecule
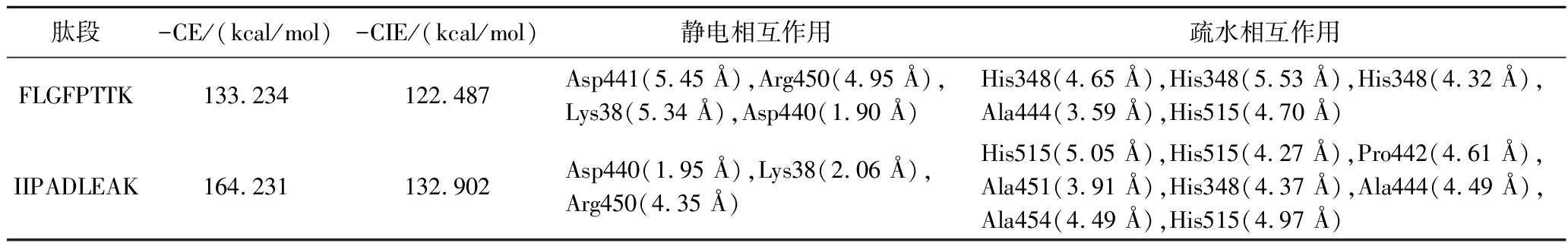
肽段-CE/(kcal/mol)-CIE/(kcal/mol)静电相互作用疏水相互作用FLGFPTTK133.234122.487Asp441(5.45 Å),Arg450(4.95 Å),Lys38(5.34 Å),Asp440(1.90 Å)His348(4.65 Å),His348(5.53 Å),His348(4.32 Å),Ala444(3.59 Å),His515(4.70 Å)IIPADLEAK164.231132.902Asp440(1.95 Å),Lys38(2.06 Å),Arg450(4.35 Å)His515(5.05 Å),His515(4.27 Å),Pro442(4.61 Å),Ala451(3.91 Å),His348(4.37 Å),Ala444(4.49 Å),Ala454(4.49 Å),His515(4.97 Å)
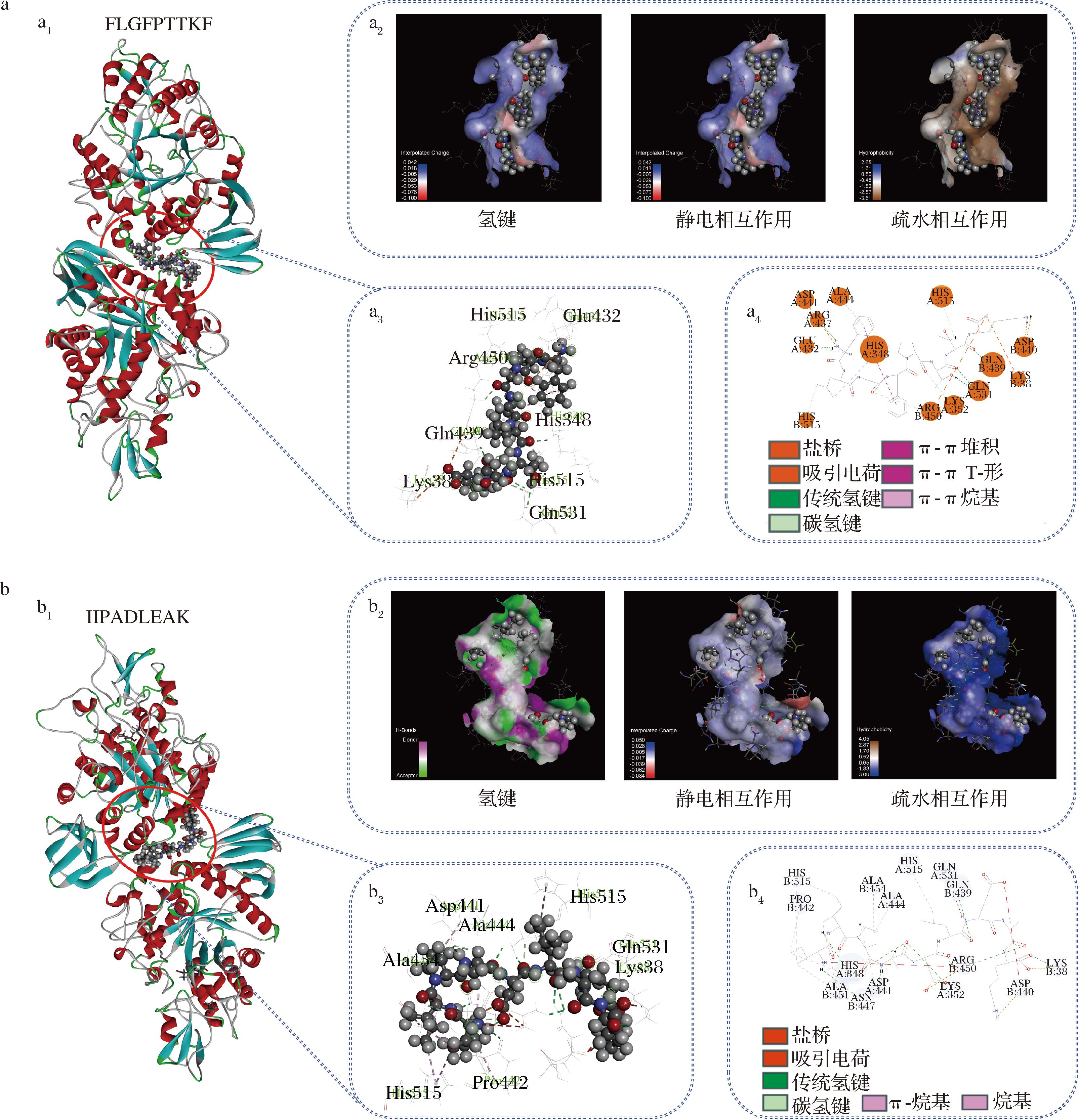
a1、b1-复合物最佳对接构象3D视图;a2、b2-复合物的氢键、静电力和疏水相互作用分布图;a3、b3-对接的局部放大图;a4、b4-复合物的相互作用2D图。
a- FLGFPTTKF;b- IIPADLEAK
图4 新型肽FLGFPTTKF和IIPADLEAK与α-葡萄糖苷酶分子的对接构象图
Fig.4 Docking conformations of the novel peptides FLGFPTTKF and IIPADLEAK interacting with the α-glucosidase molecule
图4显示了新型肽与α-葡萄糖苷酶结合的作用模式。由图4-a中的a2和图4-b中的b2可知,氢键(常规氢键、碳氢键和π-载体氢键)、静电相互作用(盐桥和电荷吸引)和疏水相互作用(π-π堆积、π-π T-形、π-烷基和烷基)是肽与α-葡萄糖苷酶之间主要的相互作用力。图4-a中的a3、a4和表3显示,FLGFPTTK与α-葡萄糖苷酶的支链残基His515(2.62 Å)、Gln531(2.47 Å)、Gln531(2.71 Å)、Gln439(2.45 Å)、Lys352(2.74 Å)、Arg450(2.92 Å)、Glu432(1.75 Å)、Glu432(2.75 Å)、Arg437(2.31 Å)、Asp440(1.90 Å)之间形成10个氢键,与支链残基Asp441(5.45 Å)、Arg450(4.95 Å)、Lys38(5.34 Å)、Asp440(1.90 Å)之间形成4个静电相互作用,与支链残基His348(4.65 Å)、His348(5.53 Å)、His348(4.32 Å)、Ala444(3.59 Å)、His515(4.70 Å)形成5个疏水相互作用。由图4-b中的b3、b4和表3可知,IIPADLEAK与α-葡萄糖苷酶的支链残基Asn447(2.53 Å)、Ala451(2.23 Å)、Ala451(2.95 Å)、His348(3.03 Å)、His348(2.34 Å)、Asp441(2.90 Å)、Asp441(2.69 Å)、Asp441(2.76 Å)、Lys352(2.24 Å)、Lys352(2.54 Å)、Arg450(2.53 Å)、Gln439(2.65 Å)、Lys38(1.92 Å)、LysS38(2.06 Å)、Asp440(1.95 Å)之间形成15个氢键,与支链残基Asp440(1.95 Å)、Lys38(2.06 Å)、Arg450(4.35 Å)形成3个静电相互作用,与残基His515(5.05 Å)、His515(4.27 Å)、Pro442(4.61 Å)、Ala451(3.91 Å)、His348(4.37 Å)、Ala444(4.49 Å)、Ala454(4.49 Å)、His515(4.97 Å)间形成8个疏水相互作用。在上述支链残基中,His515、Asp440、Asn447、Pro442、Ala451和Ala454已经被报道为肽与α-葡萄糖苷酶结合的关键活性位点[25]。同时,先前研究表明,α-葡萄糖苷酶的催化结构域主要位于残基358-720,关键的活性靶点上含有氨基酸残基R(精氨酸,Arg),W(色氨酸,Trp)和C(半胱氨酸,Cys)[26]。此外,氢键、疏水相互作用和静电相互作用是肽与α-葡萄糖苷酶结合的关键作用力[6, 27]。谢玉霞等[12]报道氢键、静电相互作用和疏水相互作用有助于驱动配体和受体形成稳定复合物,从而阻碍底物和酶的相互作用。王道滇等[6]报道氢键和疏水相互作用是肽IEEALGDK与α-葡萄糖苷酶结合的主要驱动力。这些研究报道与本研究的模拟预测结果相似。因此,FLGFPTTK和IIPADLEAK主要通过氢键、静电相互作用和疏水相互作用与α-葡萄糖苷酶的活性位点His515、Asp440、Asn447、Pro442、Ala451、Ala454、Arg437和Arg450等结合为稳定的复合物。这说明2条肽都可能具备良好的α-葡萄糖苷酶抑制活性。
2.3 新型肽的α-葡萄糖苷酶抑制活性验证
通过化学合成和α-葡萄糖苷酶抑制实验进一步验证了新型肽的生物活性。图5-a~图5-b显示了合成肽FLGFPTTK和IIPADLEAK的液相色谱纯度图以及质谱鉴定图。
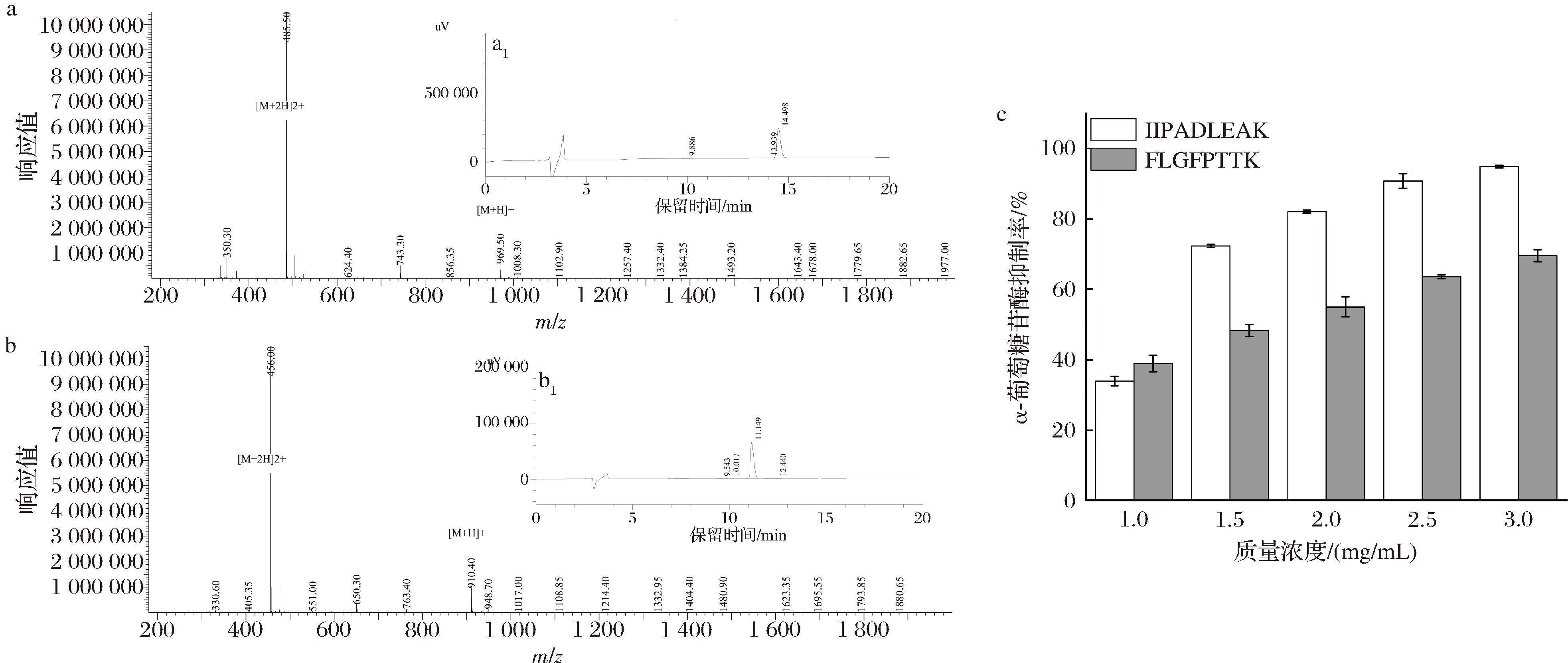
a-IIPADLEAK的质谱图(a1-IIPADLEAK的液相图);b-FLGFPTTK的质谱图(b1-FLGFPTTK的液相图);c-新型肽的α-葡萄糖苷酶抑制活性
图5 合成肽的液相图、质谱图和α-葡萄糖苷酶抑制活性
Fig.5 Liquid chromatograms, mass spectra and α-glucosidase inhibitory activity of synthetic peptides
由图5-c可知,FLGFPTTK和IIPADLEAK的α-葡萄糖苷酶抑制活性随其质量浓度的增加而增强,IC50值分别1.67和1.12 mg/mL。本研究中,2条新型α-葡萄糖苷酶抑制肽的活性明显强于伊比利亚干腌火腿降糖肽LGVGG(IC50=2.55 mg/mL)、GGLGP(IC50=3.48 mg/mL)、AEEEYPDL(IC50=5.38 mg/mL)[8]和洋三元杂交猪火腿肽YDEAGPSIVH(IC50=2.31 mg/mL)和FAGDDAPRAVF(IC50=3.48 mg/mL)[4]。此外,肽的氨基酸组成在很大程度上影响了其生物活性。L(亮氨酸,Leu)、I(异亮氨酸,Ile)、A(丙氨酸,Ala)、M(蛋氨酸,Met)、K(赖氨酸,Lys)、F(苯丙氨酸,Phe)和P(脯氨酸,Pro)等是构成α-葡萄糖苷酶抑制肽的关键氨基酸残基[5-6,18]。肽的α-葡萄糖苷酶抑制活性强度与疏水性呈正相关,活性较强的α-葡萄糖苷酶抑制肽具备更高的疏水性[25]。在本研究中,上述关键氨基酸残基在FLGFPTTK序列中的占比为62.5%,低于IIPADLEAK(88.89%);FLGFPTTK的疏水性氨基酸占比为50%,低于IIPADLEAK(66.67%)。这可能是IIPADLEAK α-葡萄糖苷酶抑制活性高于FLGFPTTK的原因。
2.4 新型α-葡萄糖苷酶抑制肽的胃肠消化稳定性
生物活性肽在被吸收利用之前可能会收到胃、肠道消化酶的影响,从而降低其生物活性[9]。本实验通过计算机模拟消化和体外模拟消化评估了2条肽的稳定性。首先,经DFBF系统进行计算机模拟消化后,FLGFPTTK被分解为4个片段(F、L、GF、和PTTK),IIPADLEAK被分解为3个片段(IIPAD、L和EAK)。经活性预测,2条肽酶解片段中的F、PTTK和IIPAD无生物活性,L和EAK表现为抗氧化活性,GF显示具有降血压和降血糖等多功能活性。这说明胃肠消化可能有助于释放2条肽的抗氧化活性,但2条肽的α-葡萄糖苷酶抑制活性可能会降低,且胃肠消化可能对肽IIPADLEAK的影响更大。
进一步探究了2条肽在体外模拟胃肠消化条件下的α-葡萄糖苷酶抑制活性(图6)。FLGFPTTK的胃肠耐受性优于IIPADLEAK,这说明胃肠道消化酶对FLGFPTTK的影响较小,这与计算机模拟消化结果相似。胃肠消化对IIPADLEAK影响较大,消化后IIPADLEAK的α-葡萄糖苷酶抑制率降低至34.25%(P<0.05)。此外,值得注意的是,胃消化阶段,FLGFPTTK的活性略有降低,但其活性能保持在50%以上;再经肠消化后,FLGFPTTK的α-葡萄糖苷酶抑制活性显著增加至65.33%。朱巧楠等[28]研究油茶饼粕抗氧化肽TSCSSPSYPFQ的胃肠消化稳定性结果与FLGFPTTK消化前后活性的变化相似,他们认为出现这种现象的原因可能是胃消化将肽序列分解为多个片段,导致活性下降;再经胰消化酶作用后,短肽内部的活性残基进一步暴露,肽的构象、电荷和疏水性发生改变,有助于肽序列中活性位点与底物间的反应[29]。总之,上述结果表明,IIPADLEAK和FLGFPTTK都是潜在的α-葡萄糖苷酶抑制肽,且FLGFPTTK的胃肠消化稳定性更佳。
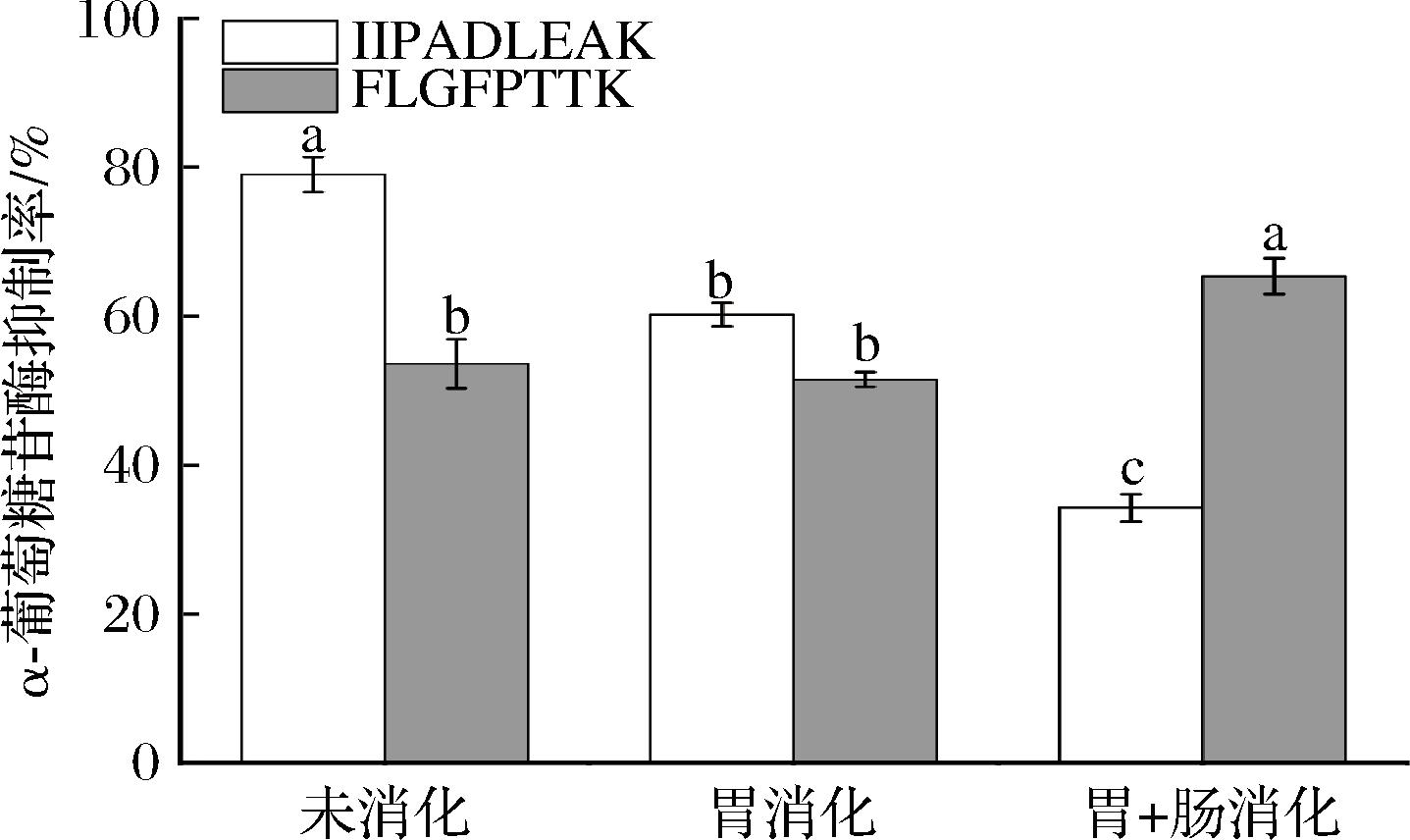
图6 新型肽在模拟胃肠消化条件下的α-葡萄糖苷酶抑制活性
Fig.6 α-glucosidase inhibitory activity of novel peptides under simulated gastrointestinal digestion conditions
注:图中不同小写字母代表同一肽段不同条件下活性差异显著(P<0.05)。
2.5 网络药理学分析预测肽的血糖调节机制
2.5.1 FLGFPTTK的抗糖尿病作用靶点预测和PPI网络构建
为了探索新型肽辅助治疗糖尿病的潜在作用靶点,选择了胃肠消化后,活性保持较高的FLGFPTTK进行网络药理学分析。如图7-a所示,将FLGFPTTK经Swiss Target Prediction网站预测到的潜在作用靶点与Genecards数据库中治疗2型糖尿病的相关基因靶点进行交叉比对,得到86个共同靶点。这些靶点可能是FLGFPTTK改善治疗2型糖尿病的潜在靶点。为进一步探究FLGFPTTK治疗2型糖尿病的机制,本实验将获得的靶点数据库上传到STRING数据库,构建出PPI网络[12]。由图7-b所见,在PPI网络中呈现出78个节点和373条边,网络的平均度值为9.56。以度值大小进行排序,最终筛选出20个重要的核心作用靶点基因(表4)。节点和度值越大,表示相关蛋白在网络中的相互作用越强[30]。由此,根据图7-b中的节点大小和表4的度值大小,推测SRC、STAT3、SIRT1、MMP9、PTGS2、REN和ACE等关键靶基因可能在FLGFPTTK干预治疗糖尿病过程中发挥关键的作用,这与前人的研究结果相似[12-13]。在这些靶点中,磷酸化的STAT3可调节促炎因子的表达水平,促进白细胞分化抗原36(cluster of differentiation 36,CD36)的表达和运输,进而改善糖尿病小鼠的炎症、动脉粥样硬化和糖代谢功能[12,31]。MMP9基因的主要功能是编码基质金属蛋白酶,与多种糖尿病的发生有关[15]。胰岛β细胞会因为MMP9的缺失和失活而发生细胞凋亡或丧失发挥相关功能调节的作用[32-33]。ACE是编码血管紧张素转化蛋白酶的基因,是引发糖尿病患者高血压的关键因子,在肾素-血管紧张素系统和激肽释放酶-激肽系统中都起着重要作用[13]。
表4 FLGFPTTK的前20个核心作用靶点拓扑参数
Tab 4 Degree of the top 20 core action targets of FLGFPTTK
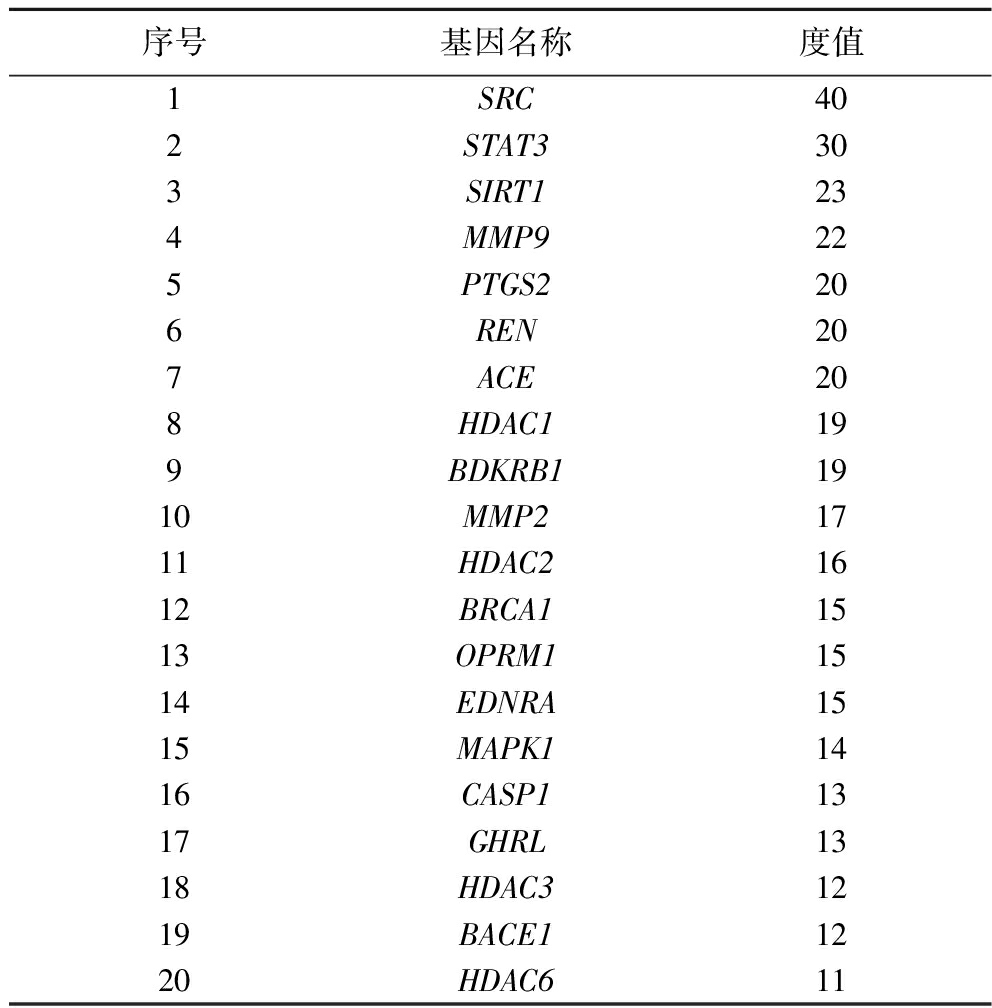
序号基因名称度值1SRC402STAT3303SIRT1234MMP9225PTGS2206REN207ACE208HDAC1199BDKRB11910MMP21711HDAC21612BRCA11513OPRM11514EDNRA1515MAPK11416CASP11317GHRL1318HDAC31219BACE11220HDAC611
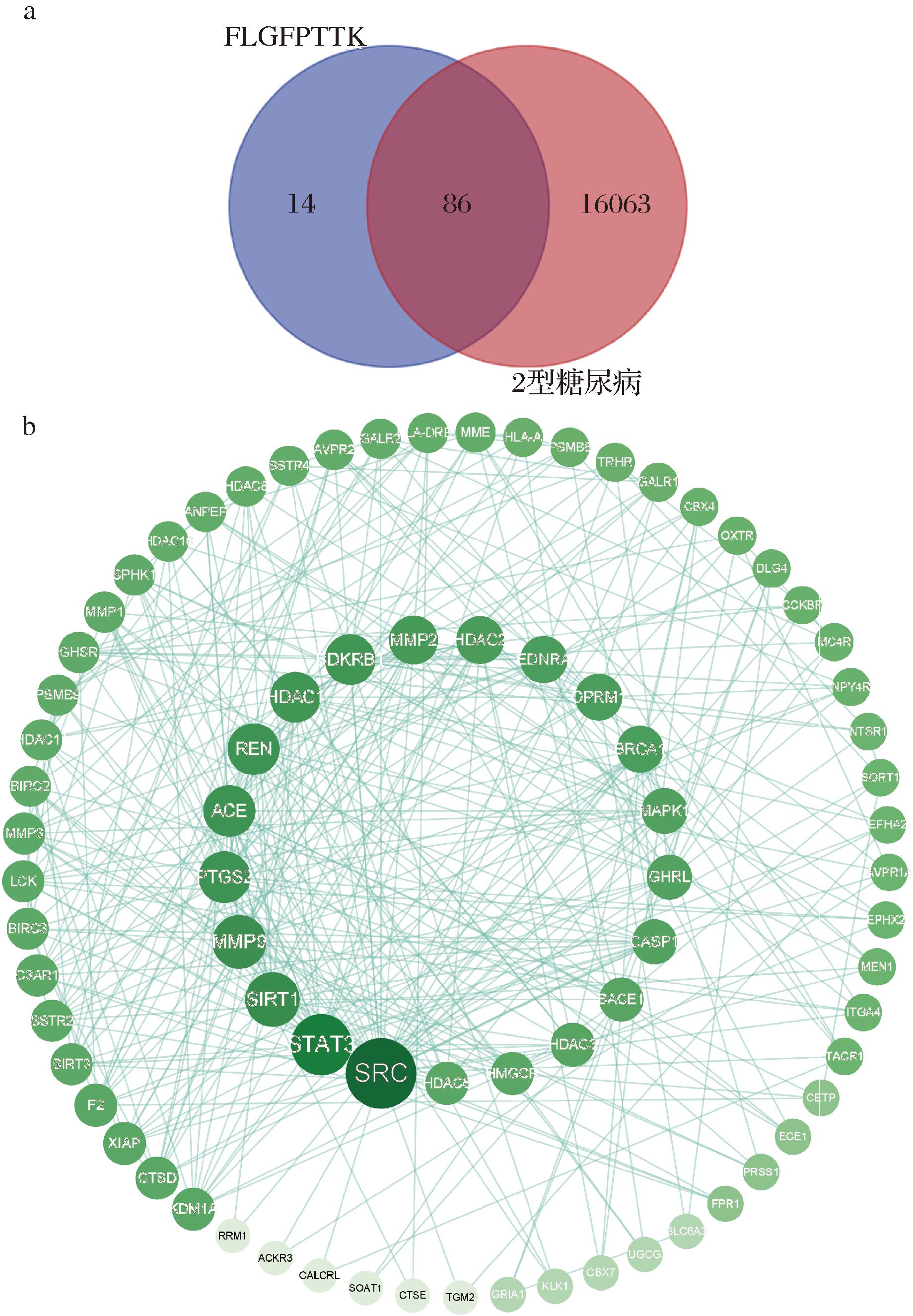
a-韦恩图;b-PPI网络图
图7 FLGFPTTK与糖尿病交集靶点的韦恩图和核心靶点的PPI网络图
Fig.7 Wayne diagram of FLGFPTTK with diabetic intersection targets and PPI network diagram of core targets
2.5.2 GO富集分析和KEGG通路富集分析
为进一步探究FLGFPTTK治疗糖尿病的具体作用途径,对86个共同作用靶点进行了GO功能分析和KEGG富集分析。图8-a、图8-b和图8-c分别为GO富集分析中的生物过程、细胞组分与分子功能。根据P值从小到大进行排列,生物过程中的靶点主要涉及到细胞质钙离子浓度的正向调节、神经肽信号途径、蛋白酶解反应和磷脂酶C激活G蛋白偶联受体信号等生物过程。细胞组分中的靶点主要涉及到质膜、组蛋白去乙酰化酶复合物、细胞表面和膜筏等细胞组分。分子功能中的靶点主要涉及蛋白赖氨酸去乙酰化酶活性、内肽酶活性、组蛋白去乙酰化酶活性和组蛋白H4K12去乙酰化酶活性和水解机制等分子功能。
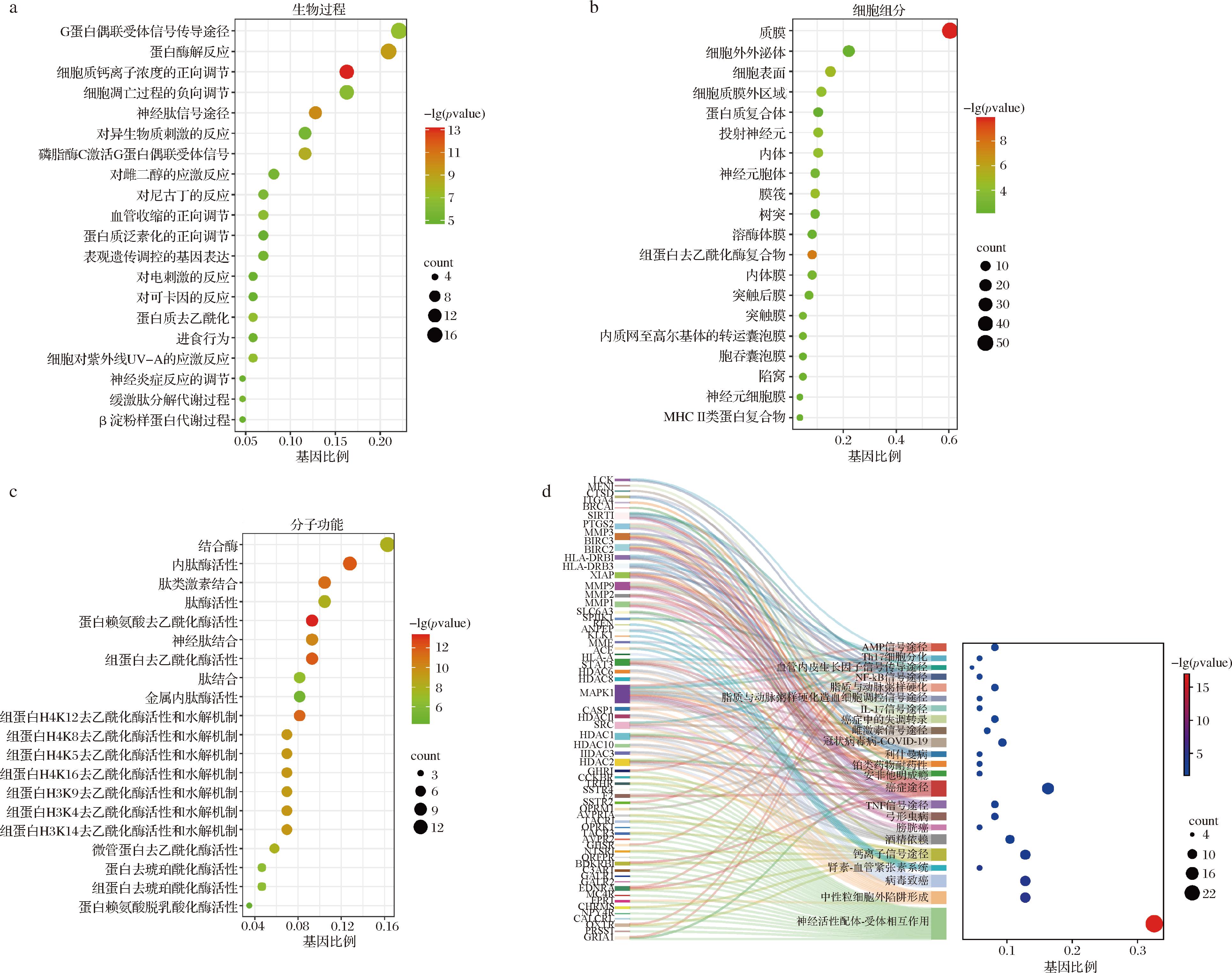
a-GO-生物过程;b-GO-细胞组分;c-GO-分子功能;d-KEGG通路富集分析
图8 FLGFPTTK与糖尿病交集靶点的富集分析
Fig.8 Enrichment analysis of FLGFPTTK with diabetic intersection targets
此外,通过KEGG数据库富集到35条代谢通路。图8-d显示了富集基因数排名前23的信号通路,结果表明FLGFPTTK干预治疗糖尿病的作用通路主要涉及到:神经活性配体-受体相互作用、癌症途径、中性粒细胞外陷阱形成、病毒致癌、脂质与动脉粥样硬化、钙离子信号途径、酒精依赖、膀胱癌、弓形虫病、TNF信号途径和cAMP信号途径等多条通路。与相关通路相关性较高的基因主要涉及MAKP1、MMP9、STAT3、SRC、HDAC1、HDAC2、PTGS2、BIRC3、BIRC2和MMP1等靶点基因,这些基因对于调控葡萄糖代谢以及相关通路蛋白的表达至关重要[30, 34]。总之,网络药理学结果表明,FLGFPTTK可能通过与各种靶点基因的相互作用和对多种途径进行调节,从而发挥潜在的糖尿病治疗效果。
3 结论
本研究综合肽组学,分子对接和网络药理学等方法探究了约长大乌杂交猪火腿中的α-葡萄糖苷酶抑制肽。从F1组分中鉴定到137条链长主要介于9~20,分子质量主要分布在1 000~2 000 Da的火腿肽。基于肽的结构特性和计算机在线分析,筛选到FLGFPTTKF和IIPADLEAK这2条潜在的新型α-葡萄糖苷酶抑制肽。分子对接显示,2条肽可以通过氢键、疏水相互作用和静电相互作用与α-葡萄糖苷酶的活性位点(His515、Asp440、Asn447、Pro442、Ala451、Ala454、Arg437和Arg450)结合,从而发挥酶的抑制作用。体外实验证明FLGFPTTKF(IC50=1.67 mg/mL)和IIPADLEAK(IC50=1.12 mg/mL)是2条活性较强的新型α-葡萄糖苷酶抑制肽。模拟胃肠消化显著降低了IIPADLEAK的生物活性,促使FLGFPTTK的α-葡萄糖苷酶抑制活性提升至65.33%(P<0.05)。网络药理学分析表明,FLGFPTTK可能通过与SRC、STAT3、SIRT1、MMP9、PTGS2、REN和ACE等关键靶基因的相互作用和对神经活性配体-受体相互作用、癌症途径、中性粒细胞外陷阱形成、病毒致癌、脂质与动脉粥样硬化、钙离子信号途径、酒精依赖、膀胱癌、弓形虫病、TNF信号途径和cAMP信号途径等多种途径的调节,从而干预治疗糖尿病。本研究为解析杂交猪火腿的潜在营养功能及其精深加工提供了参考依据。未来,需要通过细胞实验和动物实验等进一步验证新型肽FLGFPTTK的安全性以及干预治疗糖尿病的活性机制。
[1] 黄晶晶, 周迎芹, 罗章, 等.皖浙花猪干腌火腿源血糖调节肽的分离纯化、鉴定及量子化学表征[J].食品科学, 2024, 45(3):25-33.HUANG J J, ZHOU Y Q, LUO Z, et al.Isolation, purification, identification and quantum chemical characterization of blood glucose-regulating peptides derived from dry-cured ham of wanzhe spotted pigs[J].Food Science, 2024, 45(3):25-33.
[2] 陶强, 李姣, 曹皖雪, 等.肽Tyr-Pro-Ile-Trp(YPIW)对α-葡萄糖苷酶的抑制机理及其稳定性[J].食品科学, 2025, 46(7):43-50.TAO Q, LI J, CAO W X, et al.Mechanism for the inhibition of α-glucosidase by peptide Tyr-pro-ile-trp(YPIW) and its stability[J].Food Science, 2025, 46(7):43-50.
[3] LIU W W, LI H Y, WEN Y Y, et al.Molecular mechanism for the α-glucosidase inhibitory effect of wheat germ peptides[J].Journal of Agricultural and Food Chemistry, 2021, 69(50):15231-15239.
[4] WANG D D, WEI G Q, YANG Y Y, et al.Identification and molecular mechanism of novel bifunctional peptides from Duroc×(Landrace×Yorkshire) pig dry-cured ham:A peptidomics and in silico analysis[J].Food Research International, 2024, 180:114066.
[5] 李志明, 张舒, 孟维洪, 等.食源性α-葡萄糖苷酶抑制肽:构效关系、安全性及生物利用度研究进展[J].食品科学, 2023,44(15):298-309.LI Z M, ZHANG S, MENG W H, et al.Food-derived α-glucosidase inhibitory peptides:Research progress on structure-activity relationship, safety and bioavailability[J].Food Science, 2023, 44(15):298-309
[6] 王道滇, 魏光强, 陶继芳, 等.大河乌猪火腿中新型α-葡萄糖苷酶抑制肽的分离、鉴定及活性研究[J].食品科学技术学报, 2024, 42(1):114-125.WANG D D, WEI G Q, TAO J F, et al.Study on isolation, identification and activity of novel α-glucosidase inhibitory peptide derived from Dahe black pig ham[J].Journal of Food Science and Technology, 2024, 42(1):114-125.
[7] K![]() SKA P, STADNIK J, BAK O, et al.Meat proteins as dipeptidyl peptidase IV inhibitors and glucose uptake stimulating peptides for the management of a type 2 diabetes mellitus in silico study[J].Nutrients, 2019, 11(10):2537.
SKA P, STADNIK J, BAK O, et al.Meat proteins as dipeptidyl peptidase IV inhibitors and glucose uptake stimulating peptides for the management of a type 2 diabetes mellitus in silico study[J].Nutrients, 2019, 11(10):2537.
[8] MORA L, GONZ LEZ-ROGEL D, HERES A, et al.Iberian dry-cured ham as a potential source of α-glucosidase-inhibitory peptides[J].Journal of Functional Foods, 2020, 67:103840.
LEZ-ROGEL D, HERES A, et al.Iberian dry-cured ham as a potential source of α-glucosidase-inhibitory peptides[J].Journal of Functional Foods, 2020, 67:103840.
[9] HU Y Y, XIAO S, ZHOU G C, et al.Bioactive peptides in dry-cured ham:A comprehensive review of preparation methods, metabolic stability, safety, health benefits, and regulatory frameworks[J].Food Research International, 2024,186:114367.
[10] WEI G Q, LI X, WANG D D, et al.Discovery of specific antioxidant peptide from Chinese Dahe black pig and hybrid pig dry-cured hams based on peptidomics strategy[J].Food Research International, 2023, 166:112610.
[11] WEI G Q, LI X, WANG D D, et al.Insights into free fatty acid profiles and oxidation on the development of characteristic volatile compounds in dry-cured ham from Dahe black and hybrid pigs[J].LWT, 2023, 184:115063.
[12] 谢玉霞, 葛武鹏, 李国薇, 等.驼乳乳铁蛋白DPP-IV抑制肽的筛选验证及其防治糖尿病潜在作用机制探究[J].食品工业科技, 2023, 44(6):384-395.XIE Y X, GE W P, LI G W, et al.In silico analysis of novel DPP-IV inhibitory peptides released from camel milk lactoferrin and the possible pathways involved in diabetes protection[J].Science and Technology of Food Industry, 2023, 44(6):384-395.
[13] XIE Y X, WANG J, WANG S S, et al.Preparation, characterization, and mechanism of DPP-IV inhibitory peptides derived from Bactrian camel milk[J].International Journal of Biological Macromolecules, 2024, 277:134232.
[14] LI J F, HU H H, CHEN F, et al.Characterization, mechanisms, structure-activity relationships, and antihypertensive effects of ACE inhibitory peptides:Rapid screening from sufu hydrolysate[J].Food &Function, 2024, 15(18):9224-9234.
[15] 李佳芸, 王欣之, 韦源青, 等.基于网络药理学与分子对接研究马氏珍珠贝降糖活性肽[J].食品与发酵工业, 2022,48(15):176-184.LI J Y, WANG X Z, WEI Y Q, et al.Screening of potential anti-diabetic peptides from Pinctada martensii flesh based on network pharmacology and molecular docking techniques[J].Food and Fermentation Industries, 2022, 48(15):176-184.
[16] 李焯颖,刘精杏,廖丹葵,等.火麻仁α-葡萄糖苷酶抑制肽的快速筛选、鉴定及抑制机理研究[J].食品与发酵工业, 2025,51(22):264-271.LI Z Y, LIU J X, LIAO D K, et al.Rapid screening, identification and inhibition mechanism of α-glucosidase inhibitory peptide from hemp seed [J].Food and Fermentation Industries, 2025,51(22):264-271.
[17] 赵才冬, 漆姚姚, 雷楚文, 等.甲鱼蛋蛋白水解物的体外消化及对抗氧化和α-葡萄糖苷酶抑制活性的影响[J].中国食品学报, 2022, 22(10):126-133.ZHAO C D, QI Y Y, LEI C W, et al.The digestion characteristic of protein hydrolysate of soft-shelled turtle egg and its effects on antioxidative and α-glucosidase inhibitory activities[J].Journal of Chinese Institute of Food Science and Technology, 2022, 22(10):126-133.
[18] ZHAO Q, WEI G Q, LI K L, et al.Identification and molecular docking of novel α-glucosidase inhibitory peptides from hydrolysates of Binglangjiang buffalo casein[J].LWT, 2022, 156:113062.
[19] MANZOOR M, SINGH J, GANI A.Exploration of bioactive peptides from various origin as promising nutraceutical treasures:in vitro, in silico and in vivo studies[J].Food Chemistry, 2022, 373:131395.
[20] WEI G Q, ZHAO Q, WANG D D, et al.Novel ACE inhibitory, antioxidant and α-glucosidase inhibitory peptides identified from fermented rubing cheese through peptidomic and molecular docking[J].LWT, 2022, 159:113196.
[21] 窦宝杰, 翁南海, 卢静, 等.泥鳅抗氧化活性肽的制备、鉴定及其生物活性[J].中国食品学报, 2024, 24(5):223-232.DOU B J, WENG N H, LU J, et al.Preparation, identification and activity of antioxidant active peptides from Misgurnus anguillicaudatus[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(5):223-232.
[22] 杨泽瑶, 许静, 王江雪, 等.牛骨源血管紧张素转换酶抑制肽的鉴定与表征[J].食品与发酵工业, 2025,51(13):234-242.YANG Z Y, XU J, WANG J X, et al.Identification and characterization of angiotensin-converting enzyme inhibitory peptide from bovine bone[J].Food and Fermentation Industries, 2025,51(13):234-242.
[23] ZHANG J, WU Y L, TANG H G, et al.Identification, characterization, and insights into the mechanism of novel dipeptidyl peptidase-IV inhibitory peptides from yak hemoglobin by in silico exploration, molecular docking, and in vitro assessment[J].International Journal of Biological Macromolecules, 2024, 259:129191.
[24] 马寅龙, 郭锐斌, 于雁松, 等.基于分子模拟技术筛选牛乳清蛋白源抗氧化肽[J].中国食品学报, 2024, 24(2):11-31.MA Y L, GUO R B, YU Y S, et al.Screening antioxidant peptides from bovine whey protein based on molecular simulation technology[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(2):11-31.
[25] WANG X, DENG Y J, XIE P J, et al.Novel bioactive peptides from Ginkgo biloba seed protein and evaluation of their α-glucosidase inhibition activity[J].Food Chemistry, 2023, 404:134481.
[26] FU Y X, LIU Z Y, WANG H, et al.Comparison of the generation of α-glucosidase inhibitory peptides derived from prolamins of raw and cooked foxtail millet:in vitro activity, de novo sequencing, and in silico docking[J].Food Chemistry, 2023, 411:135378.
[27] MU X X, WANG R C, CHENG C L, et al.Preparation, structural properties, and in vitro and in vivo activities of peptides against dipeptidyl peptidase IV (DPP-IV) and α-glucosidase:A general review[J].Critical Reviews in Food Science and Nutrition, 2024, 64(27):9844-9858.
[28] 朱巧楠, 王鹏, 杨选, 等.油茶饼粕抗氧化肽的鉴定及其稳定性[J].中国食品学报, 2024, 24(7):332-341.ZHU Q N, WANG P, YANG X, et al.Identification and stability of antioxidant peptides from Camellia seed cake[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(7):332-341.
[29] YANG X Y, WANG D, DAI Y Y, et al.Identification and molecular binding mechanism of novel α-glucosidase inhibitory peptides from hot-pressed peanut meal protein hydrolysates[J].Foods, 2023, 12(3):663.
[30] 李玲玉, 朱文卿, 朱姗姗, 等.基于网络药理学分析咖啡酰奎宁酸类化合物治疗Ⅱ型糖尿病的作用机制[J].食品工业科技, 2021, 42(14):16-24.LI L Y, ZHU W Q, ZHU S S, et al.Mechanism of caffeoylquinic acids in the treatment of type Ⅱ diabetes based on network pharmacology[J].Science and Technology of Food Industry, 2021, 42(14):16-24.
[31] JIANG X X, BIAN W K, ZHU Y R, et al.Targeting the KCa3.1 channel suppresses diabetes-associated atherosclerosis via the STAT3/CD36 axis[J].Diabetes Research and Clinical Practice, 2022, 185:109776.
[32] 潘若瑶, 任国艳, 马富利.基于网络药理学及分子对接揭示芦荟大黄素的降糖机制[J].食品与发酵工业, 2024, 50(14):69-77.PAN R Y, REN G Y, MA F L.Network pharmacology and molecular docking reveal hypoglycemic mechanism of Aloe-emodin[J].Food and Fermentation Industries, 2024, 50(14):69-77.
[33] NAGY V, BOZDAGI O, MATYNIA A, et al.Matrix metalloproteinase-9 is required for hippocampal late-phase long-term potentiation and memory[J].The Journal of Neuroscience, 2006, 26(7):1923-1934.
[34] JAHANDIDEH F, WU J P.A review on mechanisms of action of bioactive peptides against glucose intolerance and insulin resistance[J].Food Science and Human Wellness, 2022, 11(6):1441-1454.