白酒,作为中国传统文化的瑰宝,承载着数千年的历史底蕴与独特技艺,在全球酒类市场中独树一帜。其独特的酿造工艺,融合了自然微生物的神奇作用与酿酒师的精湛技艺,孕育出了丰富多样的产品风格,一直以来都是酿酒领域研究的核心与热点[1]。在白酒酿造工艺中,酒曲承担着糖化、发酵与生香的关键作用,素有“曲为酒之骨”之说。在生产时,酒醅降温后加入大曲并混合,入池发酵,白酒风味物质的生成主要依靠酒曲的糖化发酵及产物转化作用。大曲从成型、培菌到贮存,最终用于酿酒,曲醅内部的功能微生物经生长、繁殖和代谢活动,相互依存竞争,逐渐形成稳定多菌种、多酶系群落,多风味前体物质为酿酒奠定了基础[2]。
目前研究显示,小麦作为核心制曲原料,为酿酒微生物的生长和酶的产生提供丰富的营养与适宜的环境,淀粉含量、蛋白质含量等理化指标对大曲品质起着关键性作用。同时,开放环境使微生物来源多样,诸多因素共同构成制曲过程中的微生物群落,原粮作为大曲微生物群的重要来源,对大曲品质和酿酒过程中微生物群落结构产生显著影响[3]。DU等[4]对大曲中微生物的来源进行深入研究,发现大曲菌群的组成和特性与制曲原料的选择密切相关。ZHANG等[5]的研究表明,小麦源微生物在高温大曲的初步发酵阶段对菌群的构建和早期代谢物的形成起到了重要作用。然而,对于不同特质小麦的理化品质、微生物群落结构的系统比较研究相对较少。
因此,本研究对不同特质的常用7种制曲小麦进行理化指标测定,通过高通量测序技术研究小麦来源微生物群落,并通过相关性分析、聚类分析和微生物群落多样性分析,比较筛选优质制曲小麦品种,并探究不同品种小麦微生物组成及制曲小麦潜在核心功能微生物。
1 材料与方法
1.1 材料与试剂
选取7种不同品种特征小麦(西农977、泛麦8号、富麦666、徐麦39、宁中麦、存麦8号、存麦633),取样后于-80 ℃保存。
DNeasy PowerSoil Pro试剂盒,德国QIAGEN公司;AMPure XP 核酸纯化试剂盒,美国Beckman Coulter公司;MiSeq试剂盒,美国Illumina公司。
1.2 仪器与设备
JYD×100×40小麦硬度指数测定仪,浙江伯利恒仪器设备有限公司;绿洲牌谷物水分分析仪,上海青浦绿洲检测仪器有限公司;GHCS-1000AP谷物电子容重器、微电脑自动数粒仪,浙江托普云农科技股份有限公司;傅立叶变换近红外光谱仪,德国Bruker公司;HCD-800多参数品控指标测定仪,南京至匠汇创仪器有限公司;QubitTM 4荧光计,美国Thermo Fisher公司;Qsep1生物片段分析仪,中国台湾光鼎生物科技股份有限公司;MiSeq测序仪,美国Illumina公司。
1.3 实验方法
1.3.1 理化指标测定
硬度指数:参考GB/T 21304—2007《小麦硬度测定 硬度指数法》,使用小麦硬度指数测定仪进行测定,每次重复25 g完整籽粒;水分含量:参考GB/T 5497—1985《粮食、油料检验 水分测定法》,使用谷物水分分析仪进行测定;容重:参考GB/T 5498—2013《粮油检验 容重测定》,使用谷物电子容重器进行测定;千粒重:使用自动数粒仪进行测定;粗蛋白:使用傅立叶变换近红外光谱仪进行测定;总淀粉含量:参考GB 5009.9—2023《食品安全国家标准 食品中淀粉的测定》通过品控指标测定仪进行测定;直链淀粉含量:参考GB/T 15683—2025《粮油检验 大米直链淀粉含量的测定》通过品控指标测定仪进行测定;支链淀粉含量:利用差值法(即测量总淀粉和直链淀粉后通过差值法得出支链淀粉的含量)得出。
1.3.2 高通量测序
小麦经PBS洗脱处理后得到菌体沉淀,按照说明书使用DNeasy PowerSoil Pro试剂盒提取样品的总基因组DNA,并贮存在-20 ℃以供进一步分析。分别使用QubitTM 4荧光计和Qsep1生物片段分析仪检测提取的DNA的浓度和完整性。DNA检测合格后使用引物F(5′-GTGARTCATCGARTCTTTG-3′)和R(5′-TCCTCCGCTTATTGATATGC-3′)扩增真菌ITS2区域。使用引物338F(5′-ACTCCTACGGGAGGCAGCAG-3′)和806R(5′-GGACTACHVGGGTWTCTAAT-3′)扩增V3~V4高变区的细菌16rRNA基因。在进行 Illumina MiSeq 测序(2×300 bp)之前,使用 AMPPure XP核酸纯化试剂盒和MiSeq试剂盒V3(600个循环)对PCR产物进行纯化并调整到合适浓度以构建文库。
1.3.3 生信分析
采用Illumina平台对DNA片段进行测序,使用Fastp进行质量修剪,然后使用QIIME2(2021.2.0)修剪引物。使用DADA2流程进行进一步处理。分别使用 SILVA v138和UNITE 数据库对小麦源细菌和真菌扩增子序列变体进行分类学分类。
1.4 数据处理
理化检测结果通过SPSS 27.0软件进行检验分析,以评估样品间差异的显著性(P<0.05)。数据可视化主要利用Origin 2021、R studio 4.4.1完成,以增强数据展示的清晰度和直观性。
2 结果与分析
2.1 不同特质小麦理化品质分析
2.1.1 不同特质小麦籽粒品质特性分析
由表1可知,所检测7种小麦的水分均在12.5%以下,符合贮藏标准。硬度指数方面,存麦8号、存麦633硬度指数大于60%,为硬质小麦,泛麦8号和富麦666硬度指数处于45~60%,为混合小麦,其余小麦硬度指数均低于45%,为软质小麦。过硬小麦使曲块紧实,水分难蒸发;过软小麦则曲块易散碎,水分易蒸发。刘宇等[6]研究浓香型白酒酿造时发现,软质麦大曲的感官质量与理化指标有助于提升白酒优质品率,硬质麦大曲香气浓郁舒适、糖化能力佳,且软质麦占比40~50%时,浓香型大曲优质曲率更高,这进一步印证了软硬质小麦搭配制曲的合理性。小麦的容重与籽粒饱满程度、胚乳含量相关,容重高的小麦籽粒饱满,胚乳含量高,利于提高出酒率。其中,泛麦8号的容重显著高于其他小麦品种,具有一定优势。千粒重和粗蛋白含量与微生物生长代谢紧密相关。7种小麦中,宁中麦的千粒重最大为54.69 g,存麦633的粗蛋白含量最高为13.28%。这主要归因于小麦中的氨基酸含量以及饱满籽粒的稳定结构。蛋白质分解为氨基酸,为微生物提供氮源,促进大曲酶活性,提高出酒率,但过高易致杂菌滋生,影响酒质风味。而千粒重高的小麦籽粒饱满、营养丰富、发酵环境稳定,更适宜制曲微生物生长[7]。总体而言,不同品种小麦的理化特性差异显著,凸显其在小麦生产中的独特价值。
表1 不同特质小麦籽粒品质特性分析
Table 1 Analysis of quality characteristics of wheat kernels with different traits
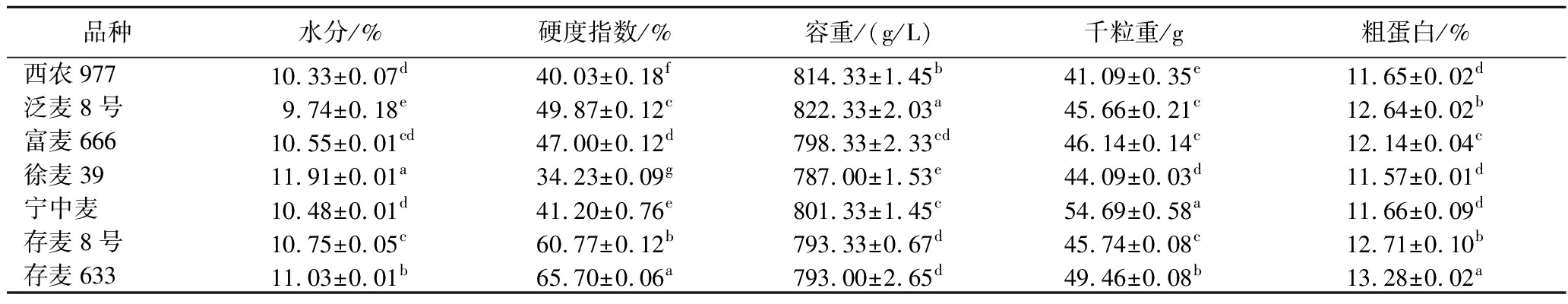
品种水分/%硬度指数/%容重/(g/L)千粒重/g粗蛋白/%西农97710.33±0.07d40.03±0.18f814.33±1.45b41.09±0.35e11.65±0.02d泛麦8号9.74±0.18e49.87±0.12c822.33±2.03a45.66±0.21c12.64±0.02b富麦66610.55±0.01cd47.00±0.12d798.33±2.33cd46.14±0.14c12.14±0.04c徐麦3911.91±0.01a34.23±0.09g787.00±1.53e44.09±0.03d11.57±0.01d宁中麦10.48±0.01d41.20±0.76e801.33±1.45c54.69±0.58a11.66±0.09d存麦8号10.75±0.05c60.77±0.12b793.33±0.67d45.74±0.08c12.71±0.10b存麦63311.03±0.01b65.70±0.06a793.00±2.65d49.46±0.08b13.28±0.02a
注:不同小写字母表示差异显著(P<0.05)(下同)。
2.1.2 不同特质小麦淀粉及淀粉组分含量分析
淀粉是小麦籽粒的主要组分,其含量对酿酒与食品制造至关重要。由表2可知,7种小麦品种总淀粉含量均较高,且支链淀粉占比具优势,除富麦666和宁中麦外,其余品种支链淀粉平均占比超70%,直链淀粉含量占比均在35%以下。高支链淀粉原料酿出的白酒口感绵柔、甜味柔和;高直链淀粉原料因结构紧密,蒸煮糊化时间长,酒体粮食香气浓郁,但支链淀粉易蒸煮糊化,直链淀粉易老化,故酿酒原料多选用高支链淀粉的品种[8]。
表2 不同特质小麦淀粉组分含量分析 单位:%
Table 2 Analysis of starch component content in wheat with different traits
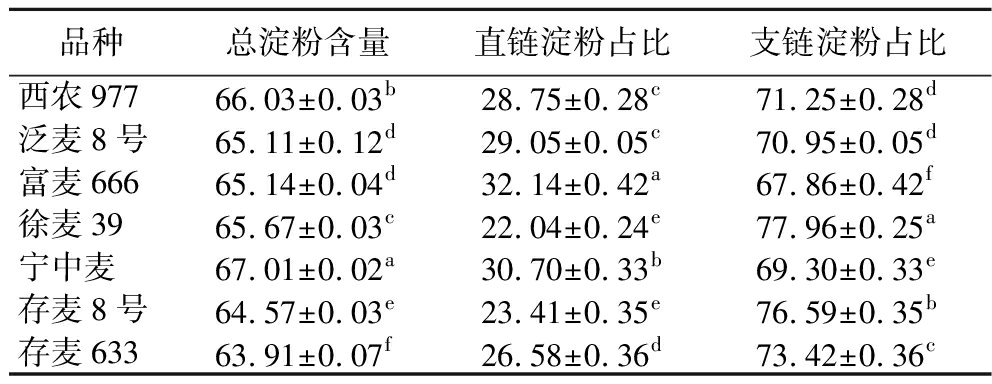
品种总淀粉含量直链淀粉占比支链淀粉占比西农97766.03±0.03b28.75±0.28c71.25±0.28d泛麦8号65.11±0.12d29.05±0.05c70.95±0.05d富麦66665.14±0.04d32.14±0.42a67.86±0.42f徐麦3965.67±0.03c22.04±0.24e77.96±0.25a宁中麦67.01±0.02a30.70±0.33b69.30±0.33e存麦8号64.57±0.03e23.41±0.35e76.59±0.35b存麦63363.91±0.07f26.58±0.36d73.42±0.36c
2.1.3 不同特质小麦籽粒品质相关性及聚类分析
对7种不同特质小麦的籽粒品质进行相关性分析,分析结果见图1,水分和容重之间呈现极显著负相关(P<0.01),主要是因为小麦籽粒的密度变化主要受其水分含量的影响。当水分含量较高时,小麦籽粒吸收水分导致体积膨胀,进而使籽粒间的空隙增大,从而引起籽粒密度的降低。相反,随着水分的逐渐减少,籽粒因失水而体积收缩,间隙也随之减少,这促使籽粒密度相应增加。粗蛋白和硬度指数之间呈现极显著正相关(P<0.01)。这可能是由于蛋白质含量会直接影响胚乳细胞的物理结构,同时,蛋白质合成过程中产生的氨基酸和多肽可能通过渗透调节作用影响胚乳细胞的水分分布,间接改变细胞膨胀度和结构紧实度[9]。整体而言,水分、硬度、直链以及支链淀粉含量,可作为小麦品控的关键指标。制曲本质是物理破碎、物质分解及微生物转化的过程,这些指标精准对应各环节关键控制点,能通过检测预判制曲品质(如酶活高低、风味物质多寡、转化效率),也可指导工艺调整(如粉碎度、润水量、发酵参数),因此需作为制曲小麦品质检测的核心依据。
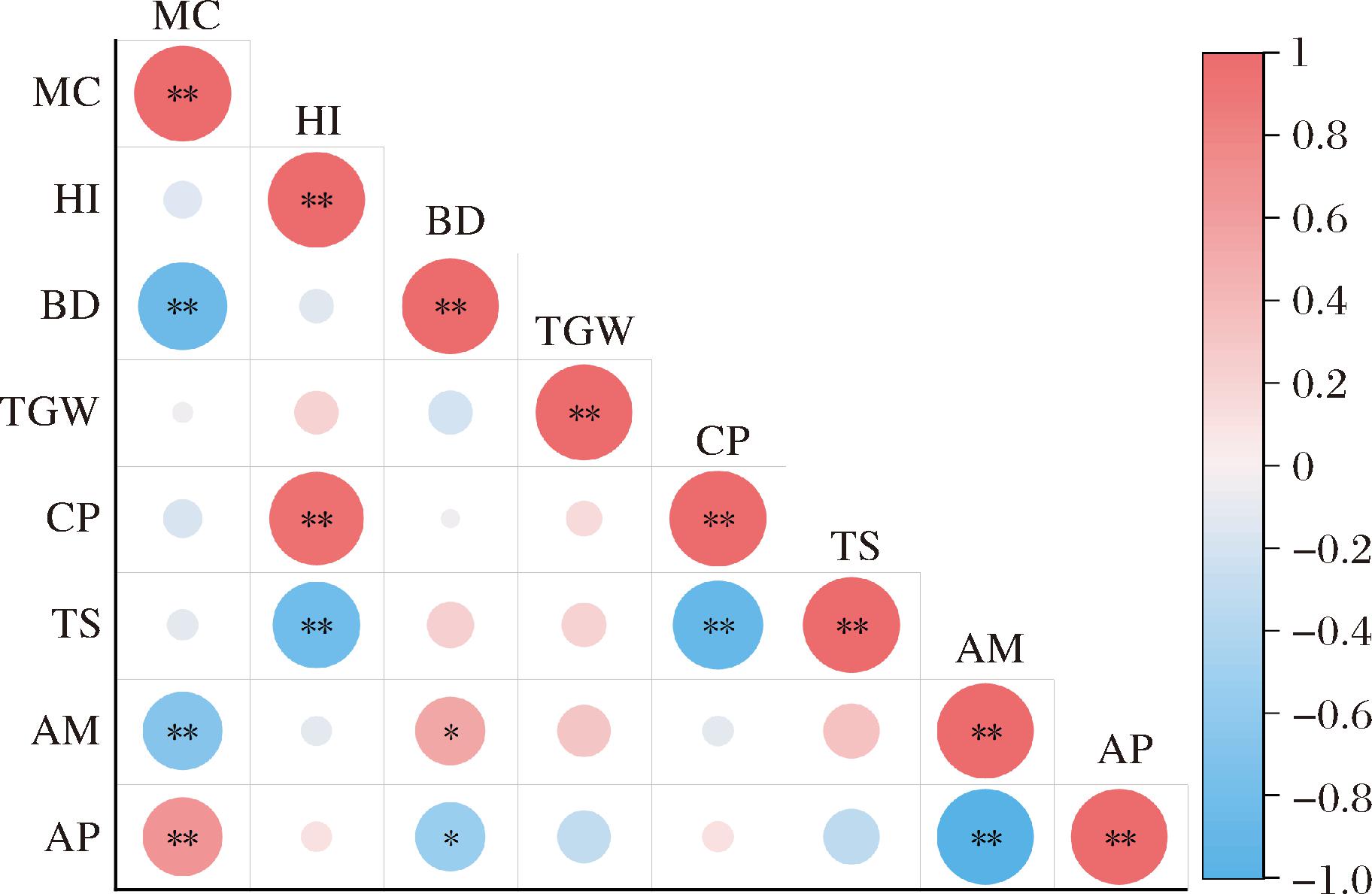
图1 不同特质小麦籽粒品质相关性分析
Fig.1 Correlation analysis of grain quality for wheat with different traits
注:MC:水分(moisture content);HI:硬度指数(hardness index);BD:容重(bulk density);TGW:千粒重(thousand-grain weight);CP:粗蛋白(crude protein);TS:总淀粉含量(total starch);AM:直链淀粉(amylose);AP:支链淀粉(amylopectin);*表示P<0.05;**表示P<0.01(下同)。
通过聚类分析更加清晰地表明不同品种小麦间的相似度和相关性,结果见图2。在欧氏距离20处,聚类分析将所有品种小麦分成3个类群,类群Ⅰ包括存麦8号和存麦633,其籽粒硬度、粗蛋白含量均高于其他类群;类群Ⅱ包括富麦666、宁中麦、西农977和泛麦8号,其容重、总淀粉含量相对较高;类群Ⅲ为徐麦39,其淀粉中支链淀粉占比、水分含量较高,粗蛋白、硬度、容重相较其他2个类群较低。综合考量来看,泛麦8号优势明显,在硬度指数、容重、总淀粉含量等关键指标方面处于较高水平,且其余指标仍能维持在中等水准,可作为优质制曲小麦品种。西农977和徐麦39与泛麦8号存在一定差异,在硬度、容重、千粒重方面略低于泛麦8号,但总淀粉和支链淀粉含量高于泛麦8号,因此可作为制曲小麦优势备选品种。此外,存麦8号和存麦633作为纯硬质小麦,在理化指标整体也处于中等水平,因此可考虑将硬质小麦与软质小麦进行科学结合制曲,以满足不同酿造需求及风味导向。
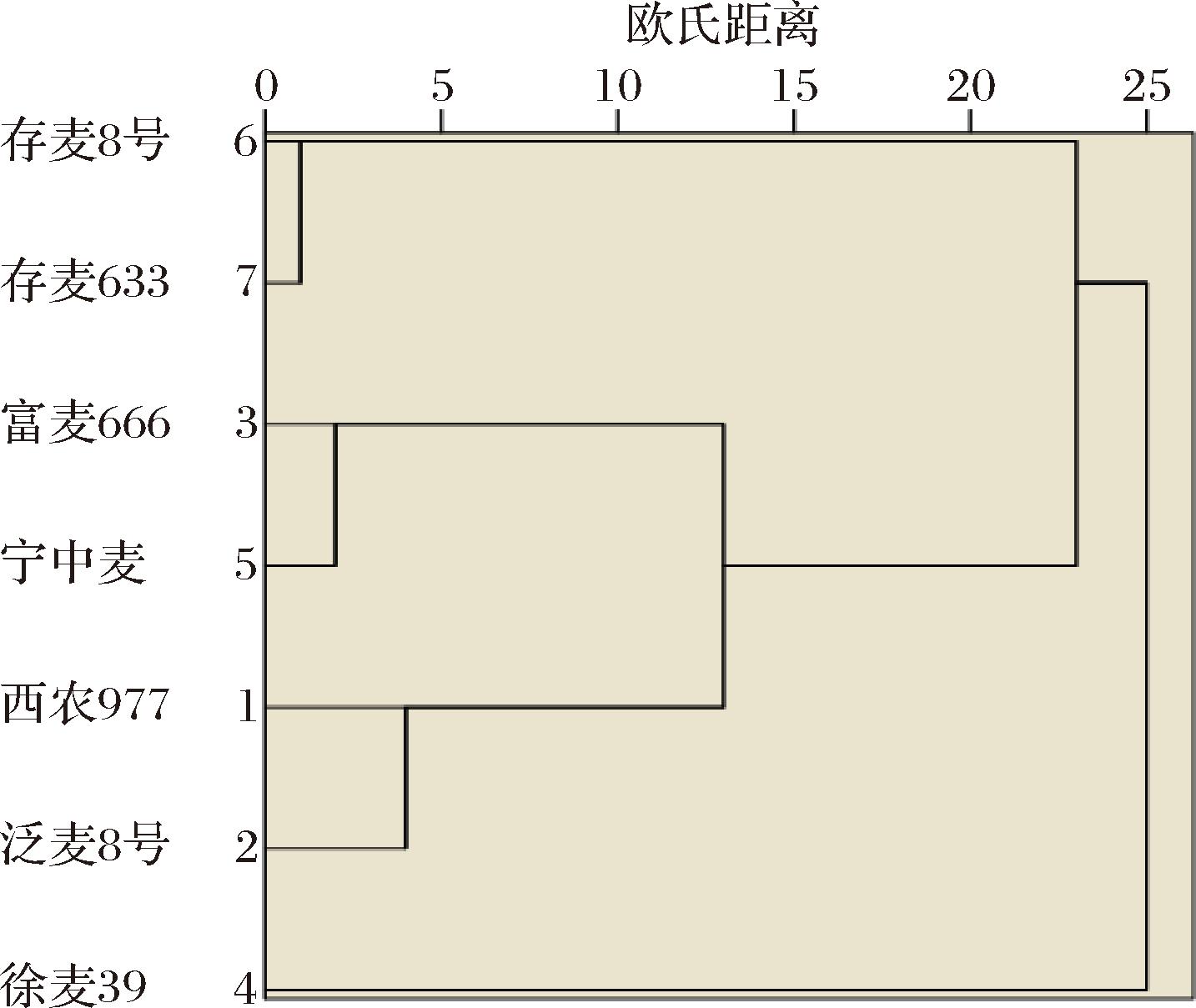
图2 不同特质小麦籽粒品质聚类分析图
Fig.2 Cluster analysis of wheat grain quality with different traits
2.2 不同特质小麦微生物群落组成差异分析
2.2.1 不同特质小麦微生物多样性分析
采用高通量测序技术,分析7种不同特质小麦的微生物组成。本研究通过Shannon指数和Simpson指数对样品小麦微生物的Alpha多样性进行表征。Alpha多样性的结果揭示了不同小麦样本之间多样性的差异。对于细菌群落而言,西农977、泛麦8号、富麦666的多样性均高于其他小麦品种,徐麦39和宁中麦的多样性较低(图3-a、3-b)。对于真菌群落,泛麦8号、存麦8号的多样性较高,其余几种小麦多样性差异不显著,徐麦39和宁中麦相对较低(图3-c、图3-d)。
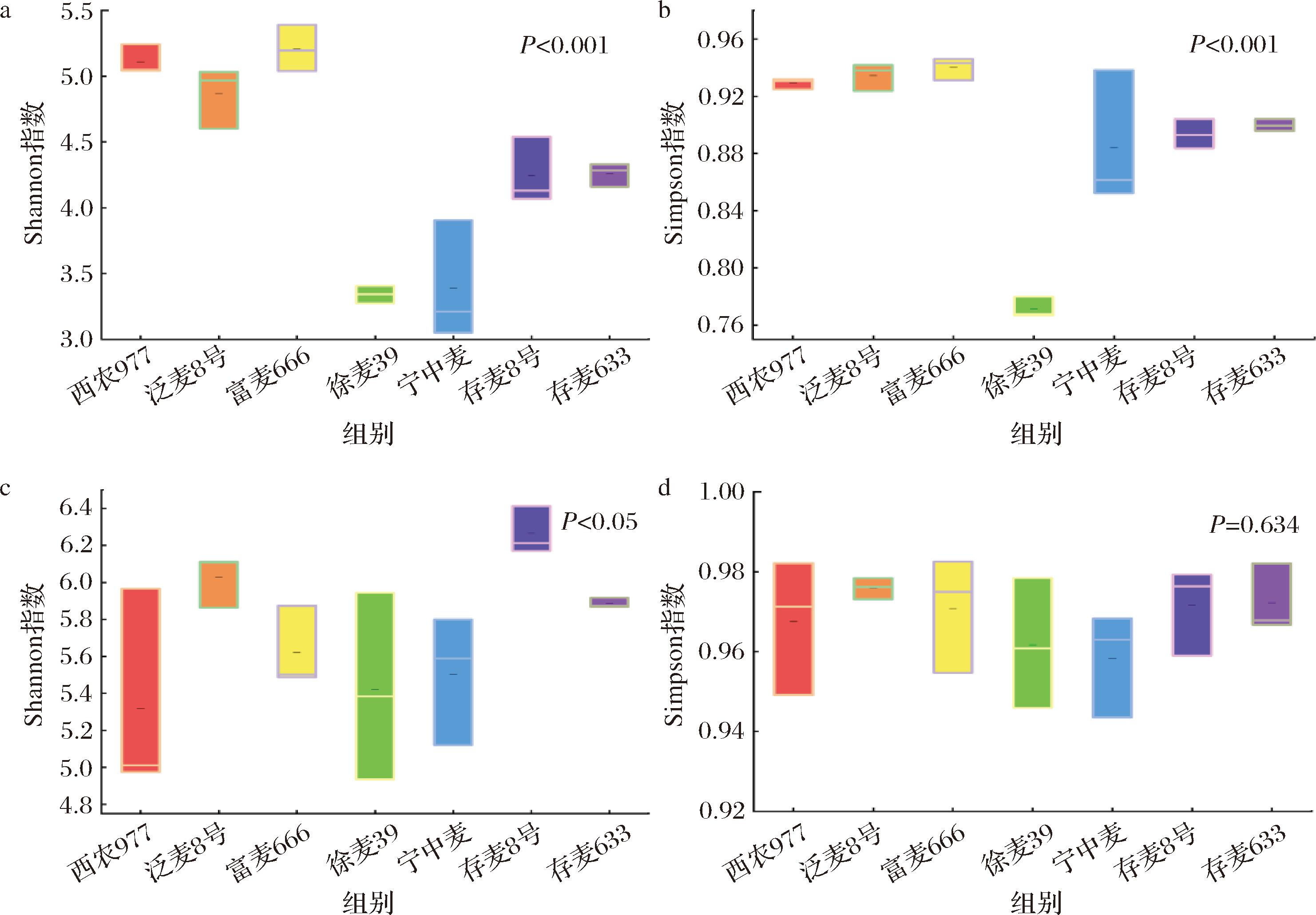
a-细菌Shannon指数;b-细菌Simpson指数;c-真菌Shannon指数;d-真菌Simpson指数
图3 不同特质小麦细菌和真菌Alpha多样性分析
Fig.3 Alpha diversity analysis of bacteria and fungi in wheat with different traits
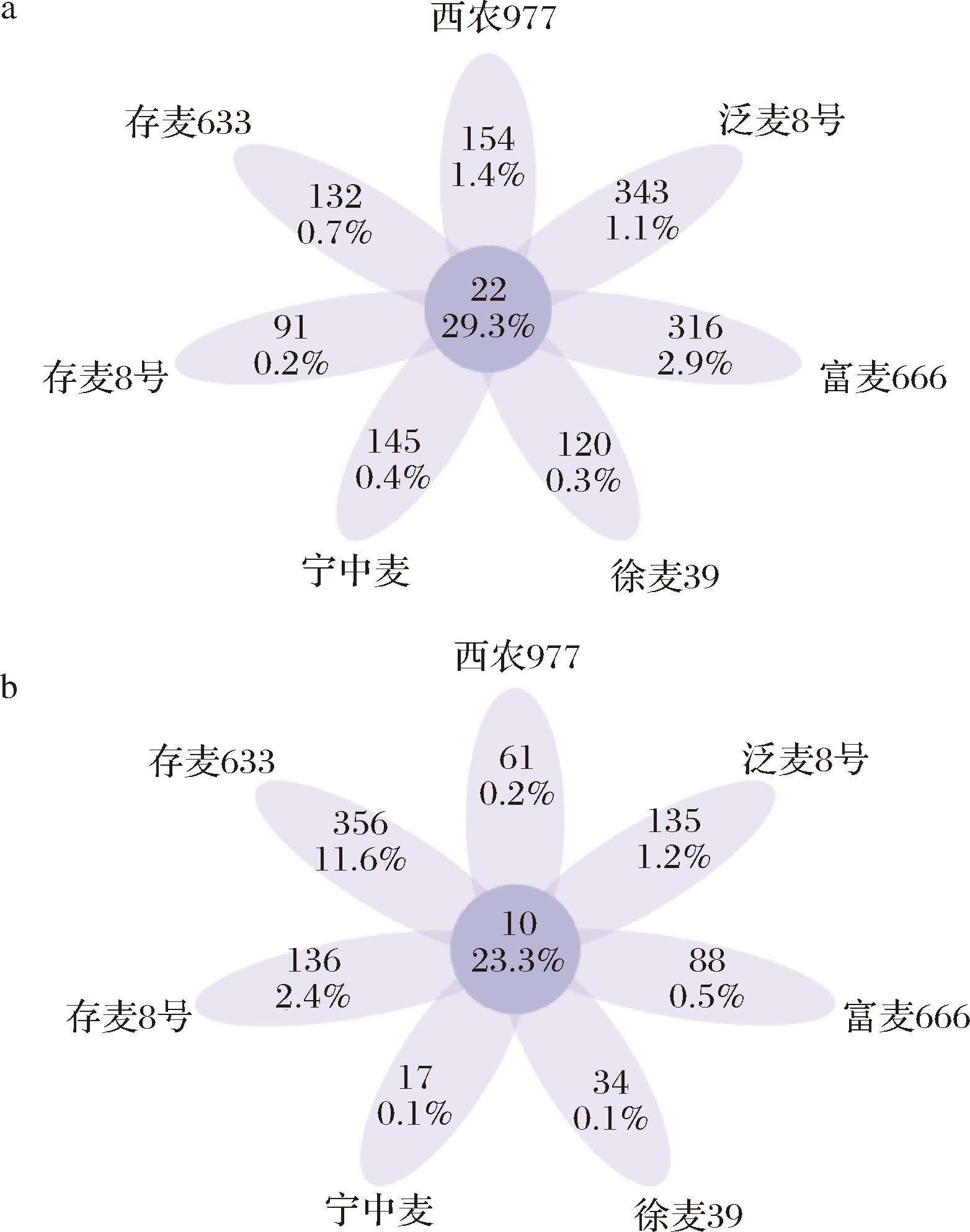
a-细菌;b-真菌
图4 不同特质小麦细菌和真菌菌群属数目的花瓣图
Fig.4 A petal diagram of the number of genus of bacteria and fungi communities in different trait wheat
基于2种小麦携带细菌和真菌菌群的组成分析结果,可进一步深入分析细菌真菌菌群的差异,结果见图4。由图4-a可知,在细菌方面,7种小麦特有的细菌属数目分别为154、343、316、120、145、91、132,共有的细菌属数目为22个;由图4-b可知,真菌方面,7种小麦特有的真菌属数目分别为61、135、88、34、17、136、356,共有的真菌属数目为10个。
Beta多样性由主坐标分析(principal co-ordinates analysis,PCoA)表征,揭示不同产地小麦样品OTU存在差异。细菌方面,PCO1解释了总变异的37.27%,PCO2解释了总变异的17.93%(图5-a),各小麦品种样本均形成较为集中的聚类,其中徐麦39与其他品种分布差距较大,表明其与其他品种的差异性。真菌方面,PCO1解释了总变异的15.11%,PCO2解释了总变异的12.29%(图5-b),各小麦品种分布较为集中,其中存麦633和宁中麦与其他品种差异较为明显,其余品种分布较为集中,表现出较高的相似性。相较于理化聚类分析结果而言,Beta多样性分析结果与其并不一致,这可能归因于环境因素以及遗传因素的影响。7种小麦并不来源于同一产地,不同生长环境可能影响微生物群落的组成。此外,小麦品种的遗传差异可能影响其对微生物的吸引力或选择性,从而导致微生物群落结构的差异。
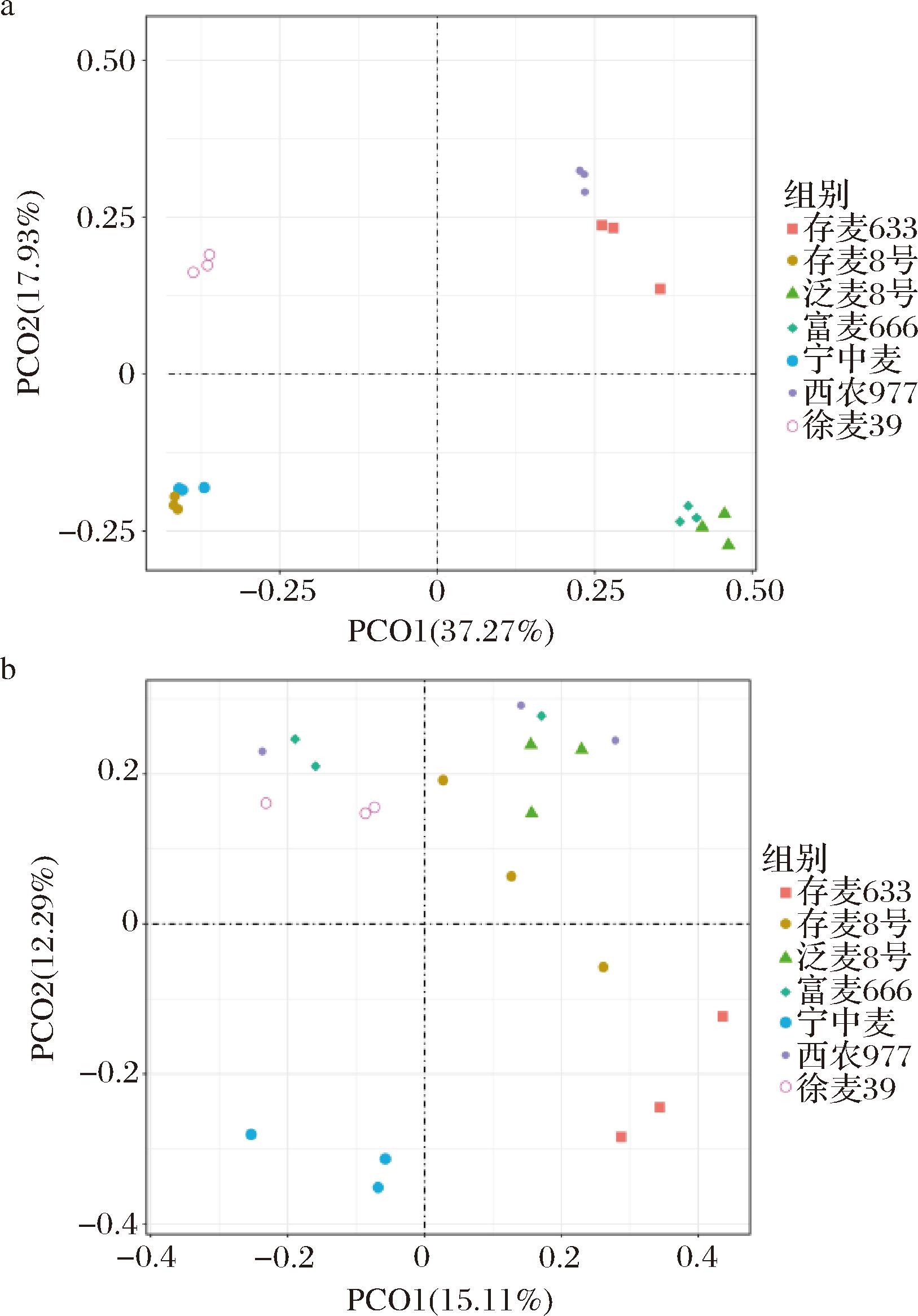
a-细菌;b-真菌
图5 不同特质小麦细菌和真菌菌群PCoA分析
Fig.5 PCoA analysis of bacterial and fungal communities in wheats with different traits
2.2.2 不同特质小麦细菌群落差异分析
7种小麦检测出的细菌门主要包括厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)、放线菌门(Actinobacteriota)、酸杆菌门(Acidobacteriota)和拟杆菌门(Bacteroidota)(图6)。厚壁菌门是7种小麦中丰度占比最高的细菌门,相对丰度均大于35%,其次为变形菌门和放线菌门,拟杆菌门在各品种小麦相对丰度占比最低,相对丰度均小于1%。厚壁菌门细菌在制曲小麦中大量繁殖,其代谢产物和生长活动可以改变小麦周围的微生态环境。例如,通过产生酸性或碱性代谢物和消耗氧气来促进微环境调节,从而产生抑制好氧竞争者并增强微生物多样性的微需氧生态位[10]。
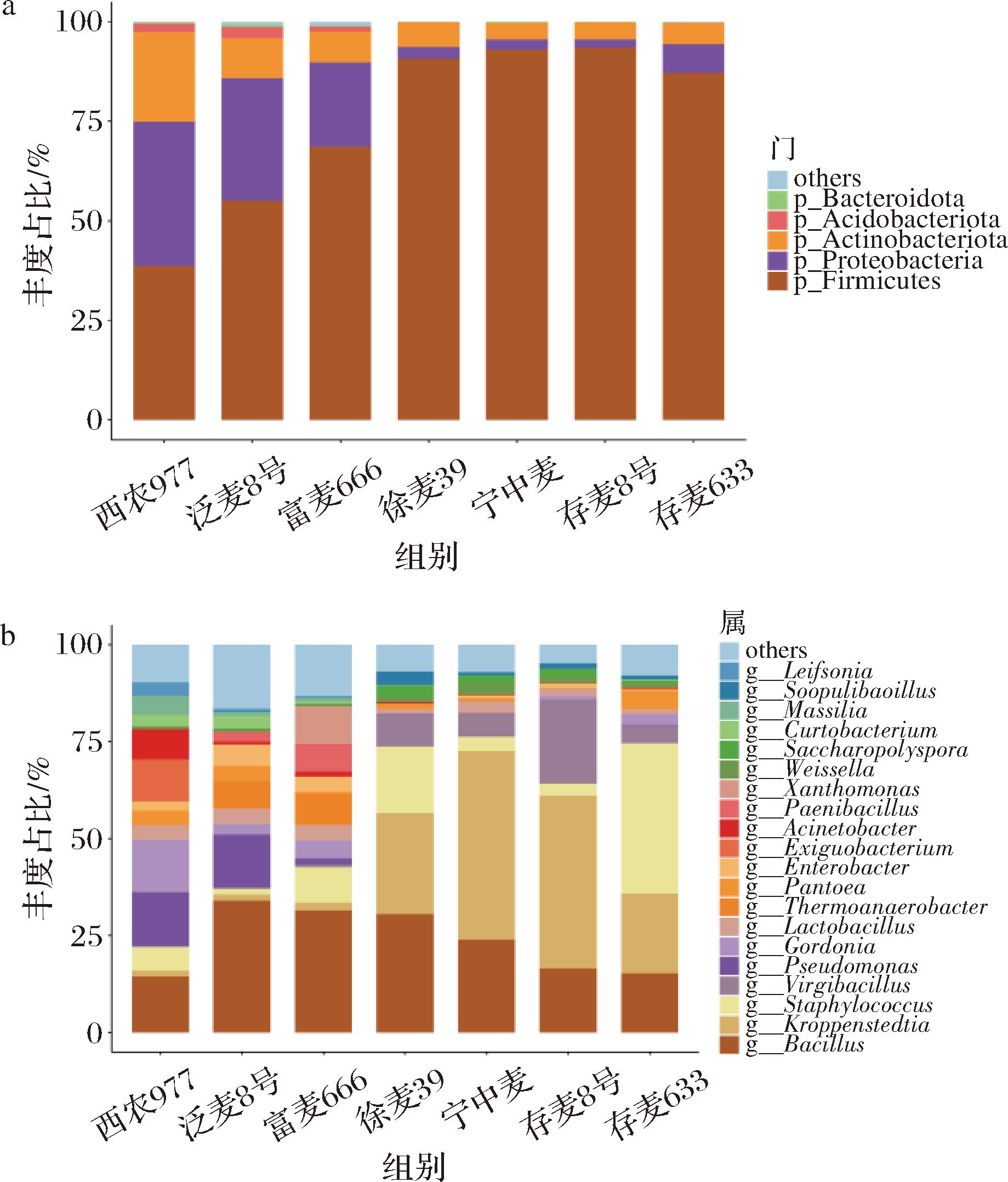
a-门;b-属
图6 不同特质小麦细菌微生物群落组成结构
Fig.6 Compositional structure of bacterial microbiota in wheat with different traits
另外,细菌属水平共检测出420个属,芽孢杆菌属(Bacillus)和克罗彭斯特菌属(Kroppenstedtia)是7种小麦中丰度占比最高的2种细菌属。芽孢杆菌属在7种小麦细菌属中均占据主要比例,在西农977(14.48%)、泛麦8号(33.97%)、富麦666(31.56%)、徐麦39(30.58%)中是相对丰度最高的细菌属。ZHENG等[11]在研究汾酒大曲的微生物群中指出,芽孢杆菌属分泌的α-淀粉酶和耐高温蛋白酶参与大曲初期的淀粉分解与氨基酸积累,为美拉德反应提供底物。克罗彭斯特菌属在宁中麦(48.55%)、存麦8号(44.56%)中是相对丰度最高的细菌属,在徐麦39(26.08%)、存麦633(20.44%)中也占有较大比例。WANG等[12]通过功能预测表明,高温大曲中编码细菌酶的高基因丰度与克罗彭斯特菌属密切相关,对大曲糖化效率提升显著。芽孢杆菌属和克罗彭斯特菌属具备形成芽孢的特性,使其拥有极强的抗逆能力,能够很好地适应制曲过程中的高温环境,有助于耐高温酶系构建,对于制曲过程具有促进作用[13]。葡萄球菌属(Staphylococcus)为存麦633(38.83%)的最优细菌属,且在徐麦39(17.05%)、富麦666(9.13%)中具有一定丰度占比。
2.2.3 不同特质小麦真菌群落差异分析
7种小麦检测出的真菌门主要包括子囊菌门(Ascomycota)、毛霉菌门(Mucoromycota)、担子菌门(Basidiomycota)、未定义门(Unidentified)、罗兹菌门(Kickxellomycota)(图7)。其中,在所有品种小麦中,子囊菌门的相对丰度占据绝对的优势,相对丰度均大于55%,这一重要的微生物类群通过分泌具有抗菌或抑菌特性的物质,有效抑制有害微生物的生长,为自身以及其他有益微生物营造出适宜的生存环境。子囊菌门拥有丰富的酶系统,能够对制曲小麦中的多种物质进行代谢转化。此外,子囊菌门衍生的前体在热加工过程中参与美拉德反应,对大曲风味物质的形成发挥着至关重要的作用[14]。其次为毛霉菌门和担子菌门,在存麦633中,担子菌门丰度占比较为突出(22.17%)。罗兹菌门仅在富麦666中被检测到,且丰度占比较低(0.01%)。
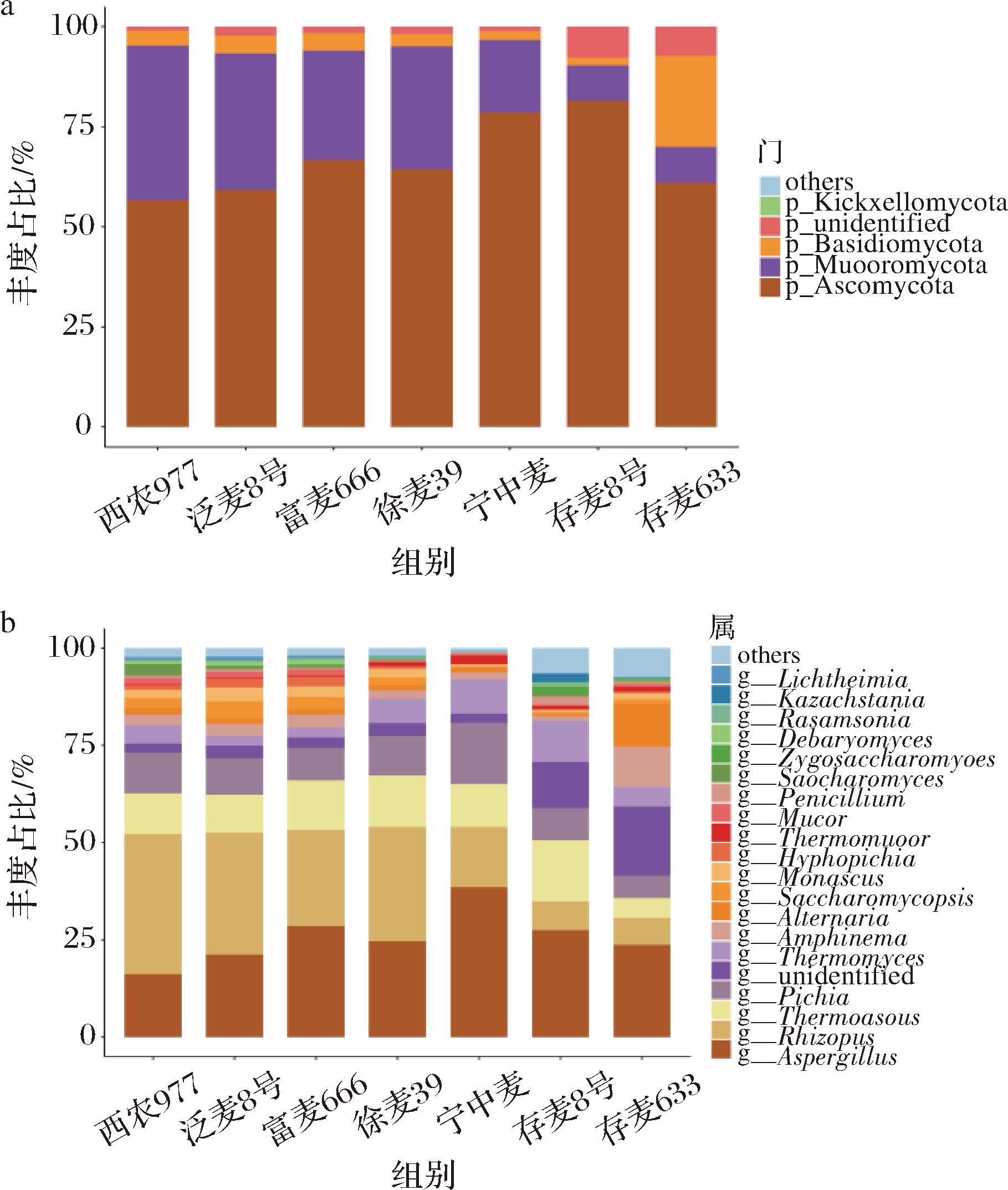
a-门;b-属
图7 不同特质小麦真菌微生物群落组成结构
Fig.7 Compositional structure of fungal microbiota in wheat with different traits
在所有样品中共检测出161个真菌属,曲霉属和根霉属在小麦真菌属中占比较为突出。其中,曲霉属(Aspergillus)在所有品种小麦中均有较高的丰度占比,是主要真菌属。在富麦666(28.57%)、宁中麦(38.51%)、存麦8号(27.54%)、存麦633(23.68%)中是相对丰度最高的真菌属,在西农977(16.24%)、泛麦8号(21.29%)、徐麦39(24.68%)中也是优势真菌属。根霉属(Rhizopus)在西农977(35.97%)、泛麦8号(31.22%)、徐麦39(29.27%)是相对丰度最高的真菌属,在富麦666(24.71%)、宁中麦(15.48%)的相对丰度也较高。曲霉属(如米曲霉)和根霉属(如米根霉)是中温大曲的核心糖化菌,其最适代谢温度(35~45 ℃)与浓香型工艺匹配,二者通过高效分泌淀粉酶驱动糖化反应,为酯类合成提供葡萄糖前体物质,且高淀粉含量同样会促进糖化进程,提高大曲糖化力[15]。WANG等[16]的研究发现,大曲的主要霉菌菌株中,曲霉属和根霉属霉菌的糖化淀粉酶的生产能力显著高于其他酶。嗜热子囊菌属(Thermoascus)和毕赤酵母菌属(Pichia)在各品种小麦中均具有一定丰度(10%左右)。嗜热子囊菌属和毕赤酵母菌属在白酒发酵过程中扮演着重要角色。在高温大曲中,嗜热子囊菌属与吡嗪类物质的形成相关,这种物质是烘烤和坚果风味的关键成分[17]。嗜热子囊菌属可显著提高甘露醇、赤藓糖醇、甲酸盐等醇酸类底物含量,为酯化反应提供充足前体物质;这些底物在其胞内或胞外酶作用下进一步生成乙酸乙酯、己酸乙酯等主体酯类,从而直接增强大曲的酯化力与风味潜力[18]。另外,容重较低通常伴随碎粉率高,曲块易板结,抑制酯化菌丝穿透,硬度的提高会促进曲块孔隙率的稳定,选择嗜热子囊菌属丰度较高,容重与硬度较高的小麦有助于提高大曲酯化力[19]。在生物增强大曲中,毕赤酵母作为监测微生物动力学的生物标志物,例如,毕赤酵母被认为是主要的风味生产者,为定义白酒香气的酯和醇做出了贡献,在低温大曲中,毕赤酵母与酵母菌一起在真菌群落中占主导地位,与酯化活性和挥发性有机化合物特征相关[20]。毕赤酵母属是高发酵力大曲的关键菌源,其代谢产物包括苯乙醇、乙偶姻等风味物质,并能耐受高温、高酸等胁迫环境,同时粗蛋白则为微生物增殖提供氮源保障,共同促进大曲发酵力的提升[21]。
2.2.4 小麦与大曲微生物关联分析
小麦是一个复杂的微生态系统,由于受多种因素影响,制曲理化性质与微生物群落组成存在一定差异。本研究中,7种小麦均检测到多菌属的高丰度存在,表明这些微生物构成小麦潜在核心功能菌群。大曲中细菌群落在很大程度上溯源至原料小麦,而真菌群落则被认为主要来源于制曲环境(空气、水、工具、场地微生物)[4]。然而,在本研究分析的小麦原料中,均检测到主要的大曲真菌属。这种不一致性提示原料小麦本身携带的真菌群落可能扮演了重要角色。小麦品种的真菌群落虽不一定构成大曲成熟期真菌群落的多数来源,但很可能在制曲初期微生物演替中起关键作用,因其处于有利的生态位,可能显著影响大曲发酵初期关键功能微生物群(如产糖化酶的霉菌)的建立速度和规模,进而间接影响最终大曲微生物区系的组成和功能[19]。例如,曲霉属是小麦的重要内生菌,根霉属可附着于籽粒表面,很可能为小麦传递到大曲的主要真菌属[22]。但是,本研究检测到的是属水平的信息,不同来源(小麦和环境)的同一真菌属,其种或菌株可能存在差异,其功能(如产酶能力、环境适应性)也可能不同。未来研究需结合分离培养等技术鉴定到种和株水平,以达到精确溯源的目的。
3 结论
本研究通过综合理化表征和微生物群落分析,系统评价7个小麦品种。聚类分析和相关性分析发现,泛麦8号、西农977和徐麦39在理化指标上优势显著,可作为优质制曲小麦品种,表明它们具有作为酿酒制曲优质原料的潜力。微生物分析显示芽孢杆菌属和克罗彭斯特菌属是优势细菌属,根霉、曲霉属、嗜热子囊菌属和毕赤酵母菌属为优势真菌属,鉴于小麦产地和特质差异,这些菌属可能为制曲小麦潜在核心功能微生物,为深入探究制曲过程中微生物作用机制奠定基础。但是,这项探索性研究在样品多样性和功能微生物验证方面存在局限性,未来的调查应纳入主要小麦产区的扩大品种选择,并结合多组学方法(宏基因组学和代谢组学),以阐明微生物相互作用网络并验证核心功能微生物群。这些进展将为小麦品种的精确选择和工业发酵过程中的微生物组工程奠定理论基础。
[1] ZUO Q C, HUANG Y G, MINGUO. Evaluation of bacterial diversity during fermentation process: A comparison between handmade and machine-made high-temperature Daqu of Maotai-flavor liquor[J]. Annals of Microbiology, 2020, 70(1):57.
[2] ALI A, WU Y F, LI W W, et al. Insight into microorganisms and flavor substances in traditional Chinese fermented food starter: Daqu[J]. Process Biochemistry, 2024, 146:433-450.
[3] HUANG X N, LI R S, XU J G, et al. Integrated multi-omics uncover viruses, active fermenting microbes and their metabolic profiles in the Daqu microbiome[J]. Food Research International, 2025, 208:116061.
[4] DU H, WANG X S, ZHANG Y H, et al. Exploring the impacts of raw materials and environments on the microbiota in Chinese Daqu starter[J]. International Journal of Food Microbiology, 2019, 297:32-40.
[5] ZHANG Y D, XU J G, DING F, et al. Multidimensional profiling indicates the shifts and functionality of wheat-origin microbiota during high-temperature Daqu incubation[J]. Food Research International, 2022, 156:111191.
[6] 刘宇, 万自然, 徐希望, 等. 小麦软硬度对兰陵浓香型大曲品质影响的研究[J]. 酿酒科技, 2023(1):104-108.LIU Y, WAN Z R, XU X W, et al. Effect of wheat hardness on the quality of Lanling Nongxiang Daqu[J]. Liquor-Making Science &Technology, 2023(1):104-108.
[7] 刘淼, 丁丽, 赵梦梦, 等. 基于主成分分析的不同小麦品种大曲发酵动态品质评价[J]. 食品与发酵工业, 2020, 46(6):19-24.LIU M, DING L, ZHAO M M, et al. Comprehensive quality evaluation of Daqu of different wheat varieties based on principal components analysis[J]. Food and Fermentation Industries, 2020, 46(6):19-24.
[8] HUANG H P, HU X J, TIAN J P, et al. Rapid and nondestructive prediction of amylose and amylopectin contents in sorghum based on hyperspectral imaging[J]. Food Chemistry, 2021, 359:129954.
[9] SHI J, ZHAO Y Q, ZHAO P, et al. Preferentially expressed endosperm genes reveal unique activities in wheat endosperm during grain filling[J]. BMC Genomics, 2024, 25(1):795.
[10] CHEN Z H, TANG S P, ZHU X, et al. Environmental stress and the deterministic assembly of bacterial communities in Daqu: The role of amino acid content fluctuations[J]. Foods, 2025, 14(5): 725.
[11] ZHENG X W, YAN Z, HAN B Z, et al. Complex microbiota of a Chinese “Fen” liquor fermentation starter (Fen-Daqu), revealed by culture-dependent and culture-independent methods[J]. Food Microbiology, 2012, 31(2):293-300.
[12] WANG Y R, CAI W C, WANG W P, et al. Analysis of microbial diversity and functional differences in different types of high-temperature Daqu[J]. Food Science &Nutrition, 2021, 9(2):1003-1016.
[13] SHI W, CHAI L J, FANG G Y, et al. Spatial heterogeneity of the microbiome and metabolome profiles of high-temperature Daqu in the same workshop[J]. Food Research International, 2022, 156:111298.
[14] HOU X G, HUI M, SUN Z K, et al. Associations between wheat varieties and the functional microbial community of Nongxiangxing Daqu from northern China[J]. LWT, 2023, 185:115119.
[15] LIU W H, LIU G Q, ZHANG R, et al. Metagenomics unveils the differences in the functions of microbial community of medium-temperature Daqu before and after maturation[J]. Chinese Journal of Biotechnology, 2024, 40(3):877-894.
[16] WANG X D, BAN S D, QIU S Y. Analysis of the mould microbiome and exogenous enzyme production in Moutai-flavor Daqu[J]. Journal of the Institute of Brewing, 2018, 124(1):91-99.
[17] DONG W W, YU X, WANG L Y, et al. Unveiling the microbiota of sauce-flavor Daqu and its relationships with flavors and color during maturation[J]. Frontiers in Microbiology, 2024, 15:1345772.
[18] ZHANG Y D, XU J G, JIANG Y L, et al. Microbial characteristics and metabolite profiles of high-temperature Daqu in different maturation stages[J]. World Journal of Microbiology and Biotechnology, 2022, 38(12):234.
[19] ZHANG Y D, SHEN Y, CHENG W, et al. Understanding the shifts of microbial community and metabolite profile from wheat to mature Daqu[J]. Frontiers in Microbiology, 2021, 12:714726.
[20] HU Y N, HUANG X N, YANG B, et al. Contrasting the microbial community and metabolic profile of three types of light-flavor Daqu[J]. Food Bioscience, 2021, 44:101395.
[21] DENG N, DU H, XU Y. Cooperative response of Pichia kudriavzevii and Saccharomyces cerevisiae to lactic acid stress in Baijiu fermentation[J]. Journal of Agricultural and Food Chemistry, 2020, 68(17):4903-4911.
[22] ZHANG Y L, XU C, XING G, et al. Evaluation of microbial communities of Chinese Feng-flavor Daqu with effects of environmental factors using traceability analysis[J]. Scientific Reports, 2023, 13:7657.