秘鲁鱿鱼(Dosidicus gigas)作为全球重要的远洋经济头足类资源,因其高蛋白、低脂肪的特性被广泛加工为冷冻制品。然而,长期冻藏过程中肌原纤维蛋白的氧化变性、冰晶损伤及脂质氧化导致的品质劣变(如质构硬化、持水力下降、异味生成)严重影响其商品价值[1]。肌原纤维蛋白作为鱿鱼肌肉的主要功能蛋白,其空间结构稳定性直接影响产品的凝胶性、乳化性及风味特性。冻藏期间,蛋白质的巯基氧化、羰基生成、疏水基团暴露及聚集沉淀不仅导致功能特性丧失,还会通过美拉德反应和脂质-蛋白互作引发挥发性异味物质(如醛、酮、硫醚类化合物)的积累[1-2]。
碱性电解水(alkaline electrolyzed water,AEW)是通过电解饱和食盐水生成的碱性溶液(pH>11.5),低氧化还原电位(oxidation-reduction potential, ORP)(ORP<-800 mV)及微量活性氯成分(HCLO/CLO-),相较于传统保鲜剂,AEW可延缓脂质氧化及蛋白羰基化,通过稳定肌原纤维蛋白二级结构(减少α-螺旋损失,促进β-折叠形成),改善产品起泡性和乳化稳定性,被证实可抑制酶活、延缓脂质氧化[3],但其单一应用对蛋白结构保护效果不足。
复合磷酸盐(compound phosphate,CPH)是水产品冻藏的主要添加剂,其通过渗透压效应减少自由水含量,抑制冰晶生长,拓展肌原纤维蛋白空间结构,延缓巯基氧化速率,促进肌动球蛋白解离,提高产品持水性和嫩度[4]。为抑制冻藏劣变,工业上常采用CPH处理,通过螯合金属离子、提高pH及离子强度维持蛋白溶解性,但过量使用可能引发安全性问题[3,5]。CPH与AEW在肉类保鲜中存在协同潜力:CPH可缓解冰晶损伤,AEW能减少蛋白氧化[5-6],但两者复配对鱿鱼蛋白特性及风味影响的研究较少。
本研究以秘鲁鱿鱼为对象,通过测定不同浸泡处理的秘鲁鱿鱼在-20 ℃冻藏0~120 d肌原纤维蛋白含量、总巯基、总羰基、表面疏水性、溶解度、浊度、起泡性及泡沫稳定性的动态变化,结合气相色谱-离子迁移谱(gas chromatography-ion mobility spectrometry,GC-IMS)解析挥发性有机物(volatile organic compounds,VOCs)指纹图谱,探究不同浸泡处理对秘鲁鱿鱼品质、肌原纤维蛋白稳定性及挥发性有机物的影响,并为后续研究秘鲁鱿鱼的持水力等提供一定依据。
1 材料与方法
1.1 材料与试剂
新鲜秘鲁鱿鱼(长约30 cm、质量约1 kg),购于中国舟山国际水产城,并在30 min内运回实验室;甲基红,天津市福晨化学试剂厂;溴甲酚绿(ACS),上海阿拉丁生化科技股份有限公司;Tris-HCl,飞净生物科技有限公司;碱性电解水,深圳市派尼克仪器设备有限公司;焦磷酸钠(sodium acid pyrophosphate,SAPP)、三聚磷酸钠(sodium tripolyphosphate,STPP)、六偏磷酸钠(sodium hexametaphosphate,SHMP)、总羰基试剂盒、总巯基试剂盒、总蛋白定量试剂盒(双缩脲法),南京建成生物工程研究所。
1.2 仪器与设备
FSH-2A可调高速均质机,金坛区指前镇旭日实验仪器厂;AJKAPPW-100电解水生成器,深圳市派尼克仪器设备有限公司;H1750R高速冷冻离心机,湖南湘仪实验室仪器开发有限公司;FlavourSpec® 1H1-008128气相色谱、MXT-5 15 m×0.53 mm×1.0 μm质谱柱、FlavourSpec® 1H1-008128离子迁移谱,德国G.A.S.公司;TU-1810紫外可见分光光度计,北京普析通用仪器有限责任公司。
1.3 实验方法
1.3.1 碱性电解水的制备
首先制备饱和食盐水,然后将其加入电解水生成器中,通直流电后电压在电极之间产生,电压和电流值分别设置为10 V和10 A。电解时,盐溶液溶于水后解离成正、负2种离子,同时产生氢离子和氢氧根离子。负电荷离子会向阳极移动,再从阳极释放电子得到盐酸(HCl)、次氯酸(HClO)、氯气(Cl2)和氧气(O2)。而带正电的离子(H+和X+)向阴极移动,获得电子后生成高pH值、低ORP的AEW和氢气(H2)[7]。
1.3.2 实验材料预处理及分组
预处理:新鲜秘鲁鱿去皮去内脏去须耳,切割成20 cm×15 cm左右的鱿鱼胴体,洗净并置于装有冰袋的泡沫箱备用。
实验分组:如表1所示,浸泡液与鱿鱼质量比例为4∶1,每组各3个平行,在4 ℃下浸泡2 h,取出后用吸水纸吸干水分后装进保鲜袋放入-20 ℃冰箱冻藏0、30、60、90、120 d并测定相关指标。
表1 实验分组
Table 1 Experimental grouping
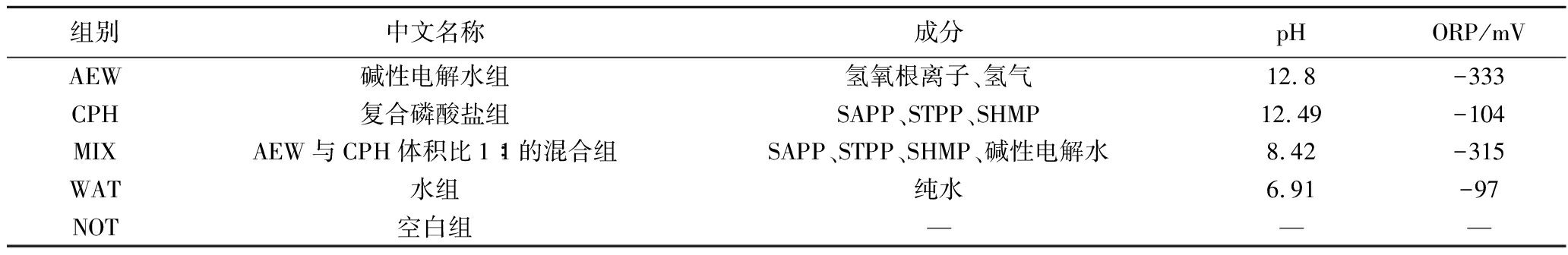
组别中文名称成分pHORP/mVAEW碱性电解水组氢氧根离子、氢气12.8-333CPH复合磷酸盐组SAPP、STPP、SHMP12.49-104MIXAEW与CPH体积比1∶1的混合组SAPP、STPP、SHMP、碱性电解水8.42-315WAT水组纯水6.91-97NOT空白组———
注:AEW:alkaline electrolyzed water、CPH:compound phosphate、MIX:mixed solution of half of alkaline electrolyzed water and compound phosphate、WAT:water、NOT:no soaking treatment;—表示无成分或无数据。
1.3.3 肌原纤维蛋白的提取与含量测定
根据姚慧等[8]和朱文慧等[9]的方法稍作修改,将鱿鱼碎肉约4.00 g(精确到0.01),加入16 mL浓度为10 mmol/L,pH值为7.2的Tris-HCl,在冰水浴条件下匀浆30 s,用4 ℃离心机4 500 r/min离心20 min,弃上清液后加入沉淀体积4倍的10 mmol/L的Tris-HCl缓冲液(含0.6 mol/L NaCl,pH 7.2)匀浆30 s,离心取上清液测定肌原纤维蛋白质含量。平行测定3次。
1.3.4 总巯基含量测定
按照总巯基试剂盒的说明书。按顺序加入样本和试剂,在波长412 nm处,测定吸光度值,平行测定3次。总巯基含量计算如公式(1)所示:
(1)
式中:Co,肌原纤维蛋白总巯基含量,μmol/mg prot;A,吸光度412 nm处的差值;ε,分子吸光系数13 600,mol·cm/L。
1.3.5 羰基含量测定
按照总羰基试剂盒的说明书。按顺序加入样本和试剂,取上清液在370 nm处,测定吸光度值,平行测定3次。总羰基含量计算如公式(2)所示:
羰基含量![]()
(2)
式中:A测定,测定管在370 nm处的吸光度;A对照,对照管在370 nm处的吸光度值;d,比色皿光径,cm;Cpr,样本蛋白浓度,mg prot/L(prot值蛋白)。
1.3.6 表面疏水性的测定
根据张斌[10]的方法稍作修改。在室温下,将5 mL肌原纤维蛋白溶液与400 μL的1 mg/mL溴酚蓝溶液涡旋10 min,8 000 r/min、4 ℃、离心10 min。取上清液稀释10倍后在595 nm处测量其吸光度,平行测定3次。肌原纤维蛋白表面疏水性用溴酚蓝结合量来表示。溴酚蓝结合量计算如公式(3)所示:
溴酚蓝结合量![]()
(3)
式中:A样品,样品的吸光度;A对照,对照管的吸光度。
1.3.7 起泡性和泡沫稳定性的测定
参照姚慧等[8]的方法并稍作修改。取30 mL浓度为20 mg/mL的肌原纤维蛋白溶液,匀浆30 s,然后快速倒入量筒内观察量筒刻度并将读数记V1;过10 min再观察量筒刻度并读数记V2。平行测定3次。肌原纤维蛋白起泡性和泡沫稳定性计算如公式(4)、公式(5)所示:
起泡性![]()
(4)
泡沫稳定性![]()
(5)
式中:V1,匀浆停止时的泡沫体积和液体体积之和;V2,匀浆10 min后泡沫体积和液体体积之和。
1.3.8 溶解度的测定
根据姚慧[8]与XUE等[11]和曾淑薇等[12]等的方法并稍作修改,将肌原纤维蛋白用0.6 mol/L NaCl溶液稀释至0.25 mg/mL,用4 ℃高速冷冻离心机离心8 000 r/min,10 min。测定蛋白溶液离心前后的质量浓度。平行测定3次。肌原纤维蛋白溶解度计算如公式(6)所示:
溶解度![]()
(6)
式中:ρ0,离心前蛋白溶液的蛋白质质量浓度,mg/mL;ρ1:离心后蛋白溶液的蛋白质质量浓度,mg/mL。
1.3.9 浊度的测定
根据姚慧等[13]的方法稍作修改,将肌原纤维蛋白用0.6 mol/L NaCl溶液稀释到1 mg/mL后,在80 ℃水浴30 min取出。平行测定3次340 nm波长处吸光度值。
1.3.10 不同浸泡处理的秘鲁鱿鱼风味分析
准备20 mL特制顶空进样瓶,将2.00 g样品于60 ℃恒温孵育平台孵育20 min后顶空进样,期间以500 r/min振荡速率维持气-液分配平衡,每个实验组设置3次平行。
气相色谱条件:分析时间:30 min;色谱柱类型:wax,30 m,ID:0.53 mm,膜厚1 μm(美国RESTEK公司);柱温60 ℃;载气/漂移气:N2;IMS温度45 ℃;进样体积500 μL;孵育时间、温度、转速:20 min、60 ℃、500 r/min;进样针温度85 ℃;流速:载气流速:0~2 min:2 mL/min,2~10 min:2~10 mL/min,随后升至100 mL/min;漂移气流速150 mL/min。
1.4 数据处理
采用仪器配套的软件LAV(Laboratory Analytical Viewer)、运用VOCal、Gallery Plot、Reporter和Dynamic PCA插件生成挥发性化合物指纹图谱定量地比较不同样品之间的挥发性有机物差异数据采用IBM SPSS Statistics 27和Origin 2022进行处理,结果用“平均值±标准差”表示。采用最小显著性差异(least significant difference,LSD)法进行统计学比较,在P<0.05水平上具有统计学意义。
2 结果与分析
2.1 不同浸泡处理对冻藏秘鲁鱿鱼肌原纤维蛋白含量的影响
由图1可知,在冻藏期间,其肌原纤维蛋白含量均不断下降。在冻藏120 d后MIX组的秘鲁鱿鱼肌原纤维蛋白含量显著大于WAT组与NOT组(P<0.05),NOT组和WAT组的下降的幅度相对最大,而经过AEW和CPH处理过的较小。WU等[14]研究发现复配SAPP和STPP能有效肌肉细胞完整性,抑制冰晶生长,在冷冻贮藏过程中,细胞内的自由水形成冰晶减少解冻损失和蛋白变性。LIN等[5]发现AEW分子较小并带有一定电位,AEW使蛋白酶失活且pH较高,在一定程度减少了蛋白质的变性。因其较强的抗氧化能力和较强的还原能力,在一定程度上可以减少蛋白质的氧化变性,这与本研究结论一致。
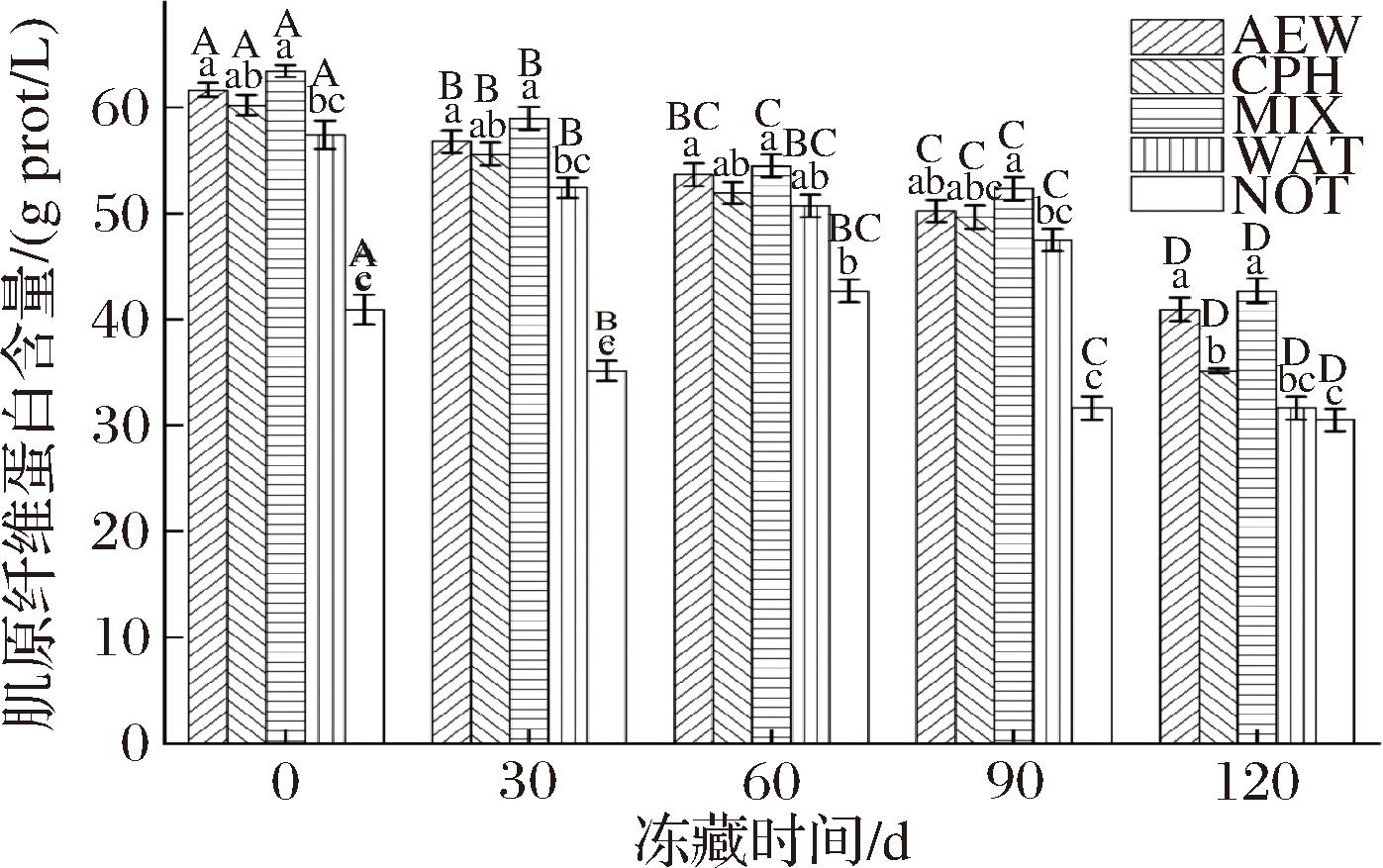
图1 不同浸泡处理对冻藏秘鲁鱿鱼肌原纤维蛋白质含量的影响
Fig.1 Effect of different immersion treatments on the protein content of myofibrillar proteins of frozen D.gigas
注:不同小写字母表示不同浸泡处理、相同贮藏时间之间差异显著;不同大写字母表示相同浸泡处理、不同贮藏时间之间差异显著。(下同)。
2.2 不同浸泡处理对冻藏秘鲁鱿鱼总巯基含量的影响
由图2可知,秘鲁鱿鱼在冻藏期间总巯基含量均显著下降,这可能是由于随着冻藏时间的延长,肌原纤维蛋白冷冻变性、机械损伤加剧而导致肌原纤维蛋白质空间结构被破坏,使内部的巯基被氧化成二硫键。冻藏120 d后,AEW组与MIX组的总巯基含量显著大于WAT组与NOT组。CHEN等[15]研究表明CPH促进了肌原纤维蛋白之间的交联,减慢巯基含量减少的速度。而AEW的负氧化还原电位可以保护蛋白质的游离巯基氧化[16]。
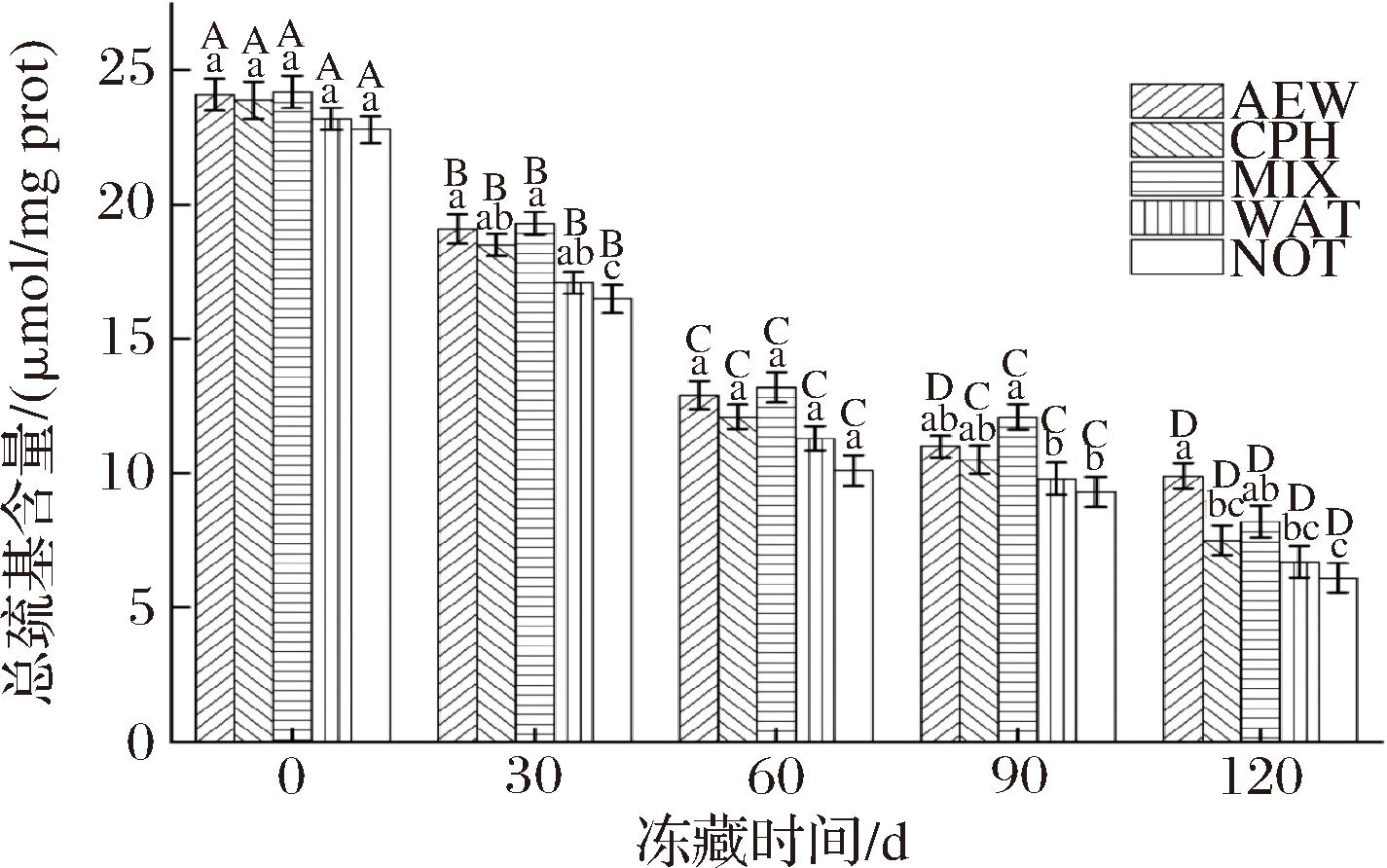
图2 不同浸泡处理对冻藏秘鲁鱿鱼肌原纤维蛋白总巯基含量的影响
Fig.2 Effect of different immersion treatments on the total sulfhydryl content of myofibrillar proteins in frozen D.gigas
2.3 不同浸泡处理对冻藏秘鲁鱿鱼总羰基含量的影响
如图3所示,在冻藏期间,不同浸泡处理的秘鲁鱿鱼肌原纤维蛋白总羰基含量呈上升趋势。冻藏前,各组总羰基含量无显著性差异(P>0.05),冻藏120 d后,总羰基含量各组均呈现上升趋势。这可能是因为在冻藏过程中活性氧自由基攻击了游离氨基或是亚氨基,生成—NH3及羰基衍生物等,接着使蛋白质肽链断裂产生了羰基基团,使得羰基含量在冻藏期间持续上升[17-18]。AEW的负氧化还原电位可以保护蛋白质的游离羰基氧化[16],这与本研究结果一致。
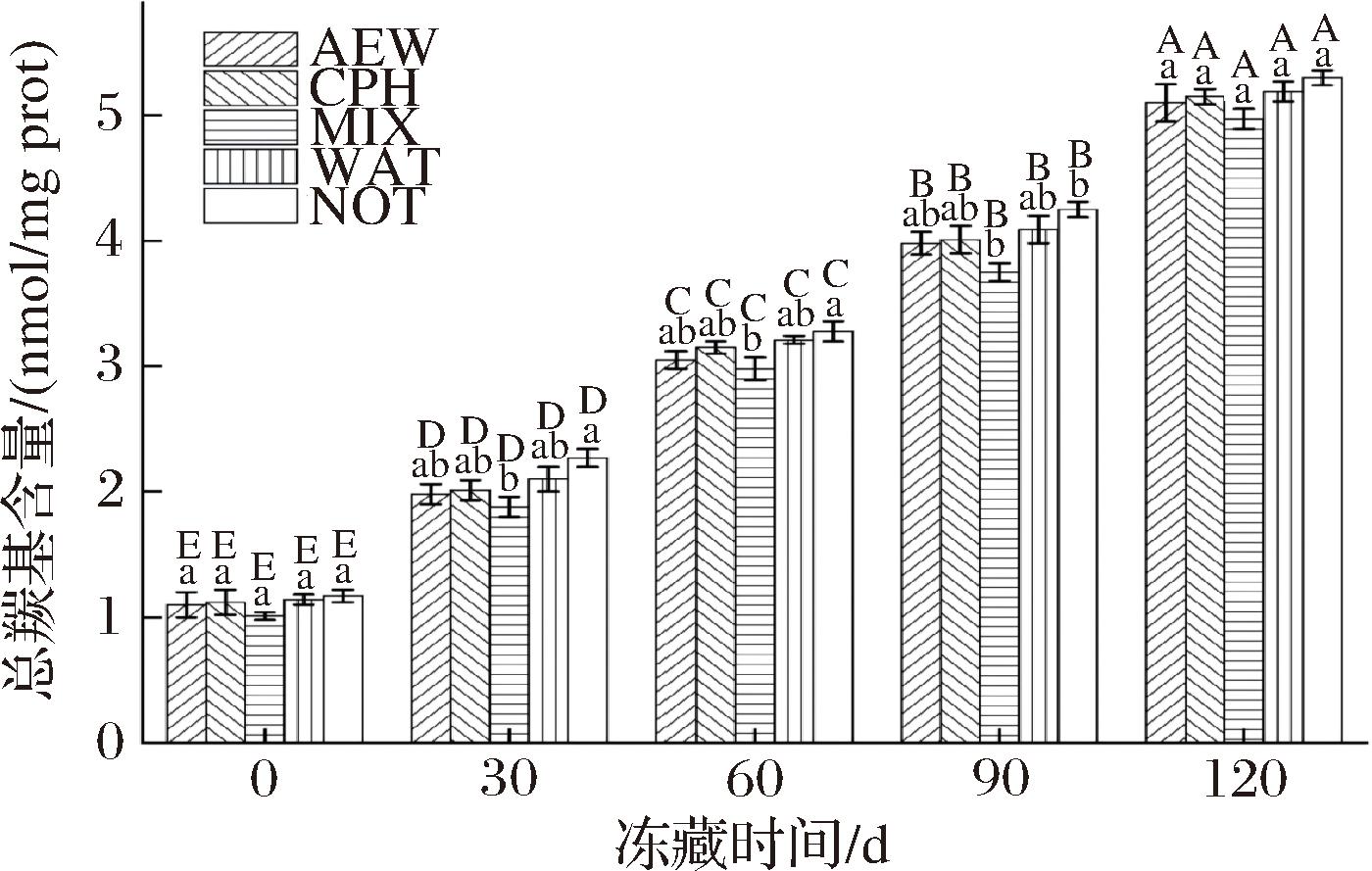
图3 不同浸泡处理对冻藏秘鲁鱿鱼肌原纤维蛋白总羰基含量的影响
Fig.3 Effects of different soaking treatments on the total carbonyl content of myofibrillar protein in frozen D.gigas
2.4 不同浸泡处理对冻藏秘鲁鱿鱼表面疏水性的影响
从图4可以看出,蛋白质的表面疏水性随着冻藏时间的延长而不断的增加。其原因可能是由于肌球蛋白末端的α-螺旋链部分解离,α-螺旋向β-转角转化,蛋白空间结构伸展,疏水性脂肪族和包埋在分子内部的巯基的暴露,使得表面疏水性含量增加[19]。在冻藏120 d后,各组表面疏水性均呈现上升趋势。经过AEW与CPH浸泡处理后秘鲁鱿鱼肌原纤维蛋白表面疏水性增幅大于WAT组与NOT组,因此推测CPH的加入会引起蛋白质分子链的伸展,使其疏水侧链暴露,进而改变肽链的螺旋结构,提高了肌原纤维蛋白表面疏水性[12,20-21]。夏立志等[20]研究表明,加入CPH后,蛋白质内部自由水增多,水分子的流动性得到提升,疏水基团周围的水的熵值增大,进一步增加肌原纤维蛋白表面的疏水性。
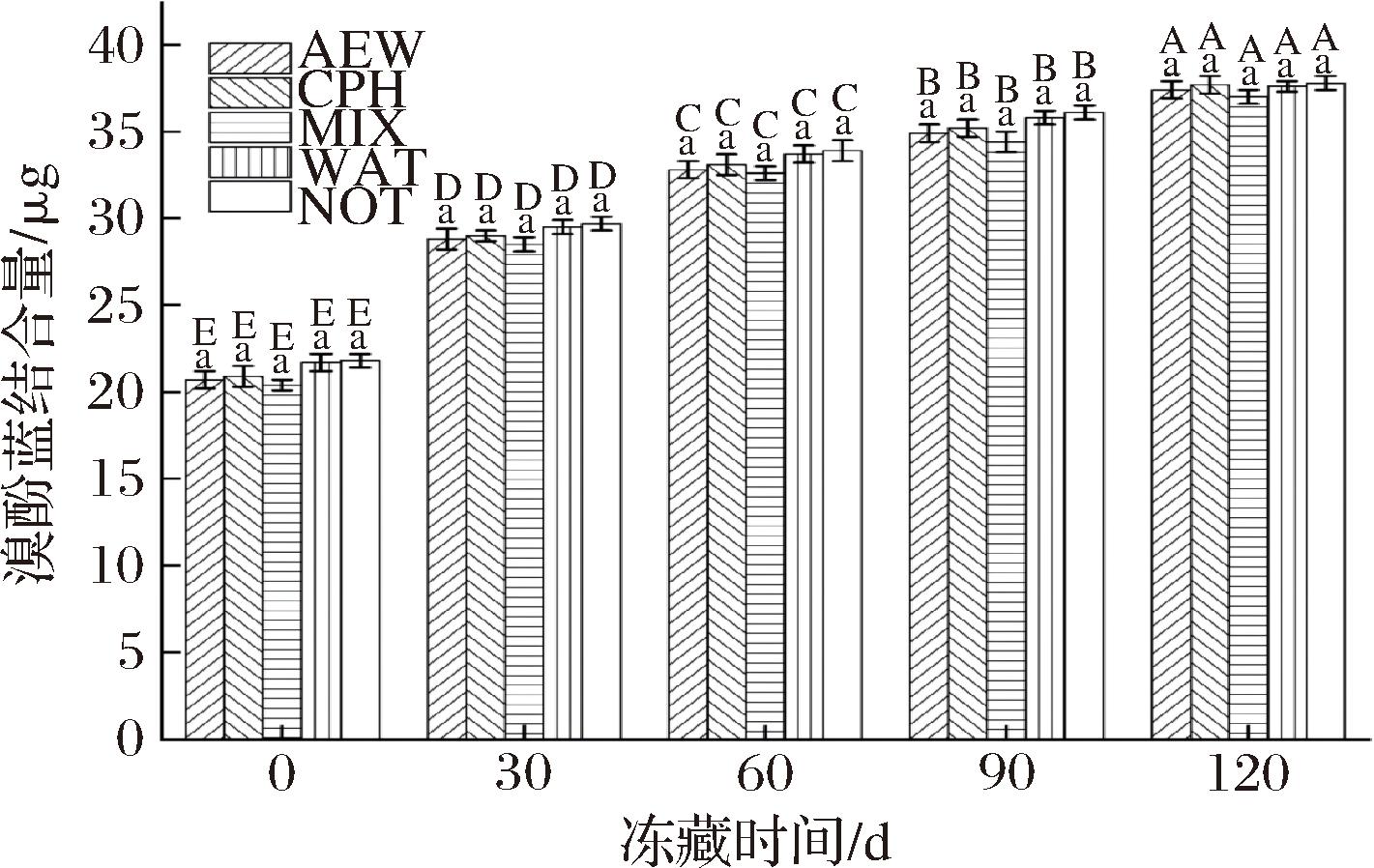
图4 不同浸泡处理对冻藏秘鲁鱿鱼肌原纤维蛋白表面疏水性的影响
Fig.4 Effect of different immersion treatments on the surface hydrophobicity of myofibrillar proteins of frozen D.gigas
2.5 不同浸泡处理对冻藏秘鲁鱿鱼起泡性和泡沫稳定性的影响
由图5可知,随着冻藏时间的延长,经过不同浸泡处理的秘鲁鱿鱼肌原纤维蛋白起泡性和泡沫稳定性呈下降趋势。分子内氨基与羧基形成氢键能力下降可能是由于蛋白含量的减少和变性程度的加剧[8],从而导致泡沫难以形成以及泡沫稳定性的降低[22]。在冻藏前,MIX组的起泡性(61.55%)显著大于NOT组(56.88%)(P<0.05),泡沫稳定性无显著性差异。在冻藏120 d后,MIX组的起泡性(28.91%)显著大于其他组(P<0.05),AEW组(96.96%)和MIX组(96.21%)的泡沫稳定性显著大于其他3组(P<0.05)。有研究显示,蛋清蛋白干燥加热磷酸化之后,起泡性明显增加[23],而AEW的负氧化还原电位有利于α-螺旋的转变,β-转变为β-折叠,可以提高起泡性、泡沫稳定性[16],说明混合使用AEW和CPH可以更大程度的提高秘鲁鱿鱼肌原纤维蛋白起泡性及泡沫稳定性。
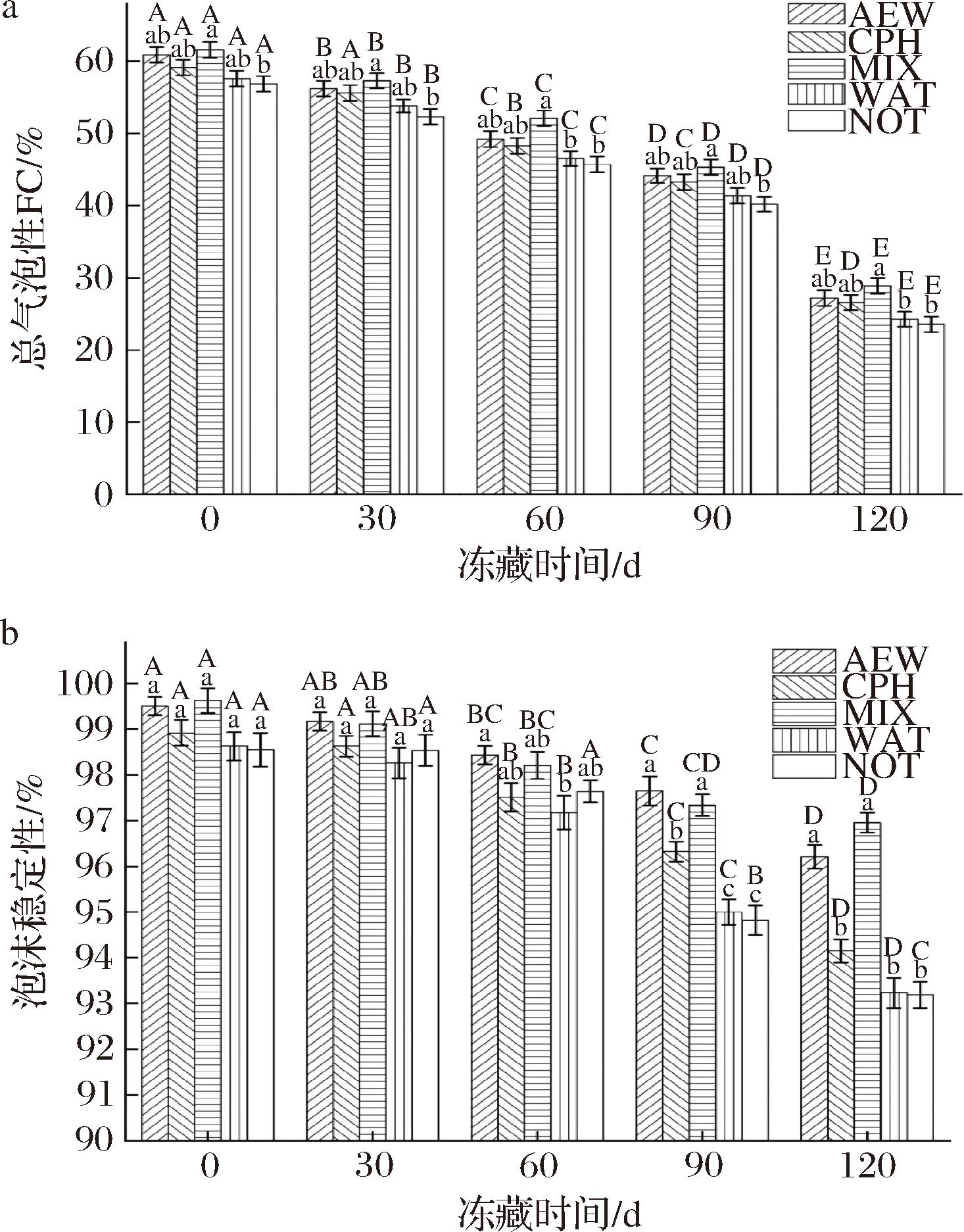
a-起泡性;b-泡沫稳定性
图5 不同浸泡处理对冻藏秘鲁鱿鱼肌原纤维蛋白起泡性及泡沫稳定性的影响
Fig.5 Effect of different immersion treatments on the foaming properties and foam stability of myofibrillar proteins in frozen D.gigas
2.6 不同浸泡处理对冻藏秘鲁鱿鱼溶解度的影响
如图6所示,随着冻藏时间的延长,秘鲁鱿鱼的肌原纤维蛋白溶解度呈下降趋势,这一现象可能与冻藏过程中肌原纤维蛋白的变性有关,此外,提取性下降也可能是二硫键等的交联聚集导致的。在冻藏前,不同浸泡处理的秘鲁鱿鱼肌原纤维蛋白溶解度没有显著性差异。在冻藏120 d后,MIX组(25.21%)的溶解度显著大于NOT组(22.33%)(P<0.05)。从热力学角度来看,蛋白质的溶解度是蛋白质-蛋白质和蛋白质-水分子相互作用达到平衡的结果[24],AEW与CPH均有较高的pH值。而MIX组在冻藏期间的秘鲁鱿鱼肌原纤维蛋白溶解度大于AEW组和CPH组,说明混合使用AEW和CPH可以更大程度地提高秘鲁鱿鱼肌原纤维蛋白溶解度,可以更好地减少秘鲁鱿鱼蛋白质品质的劣变。
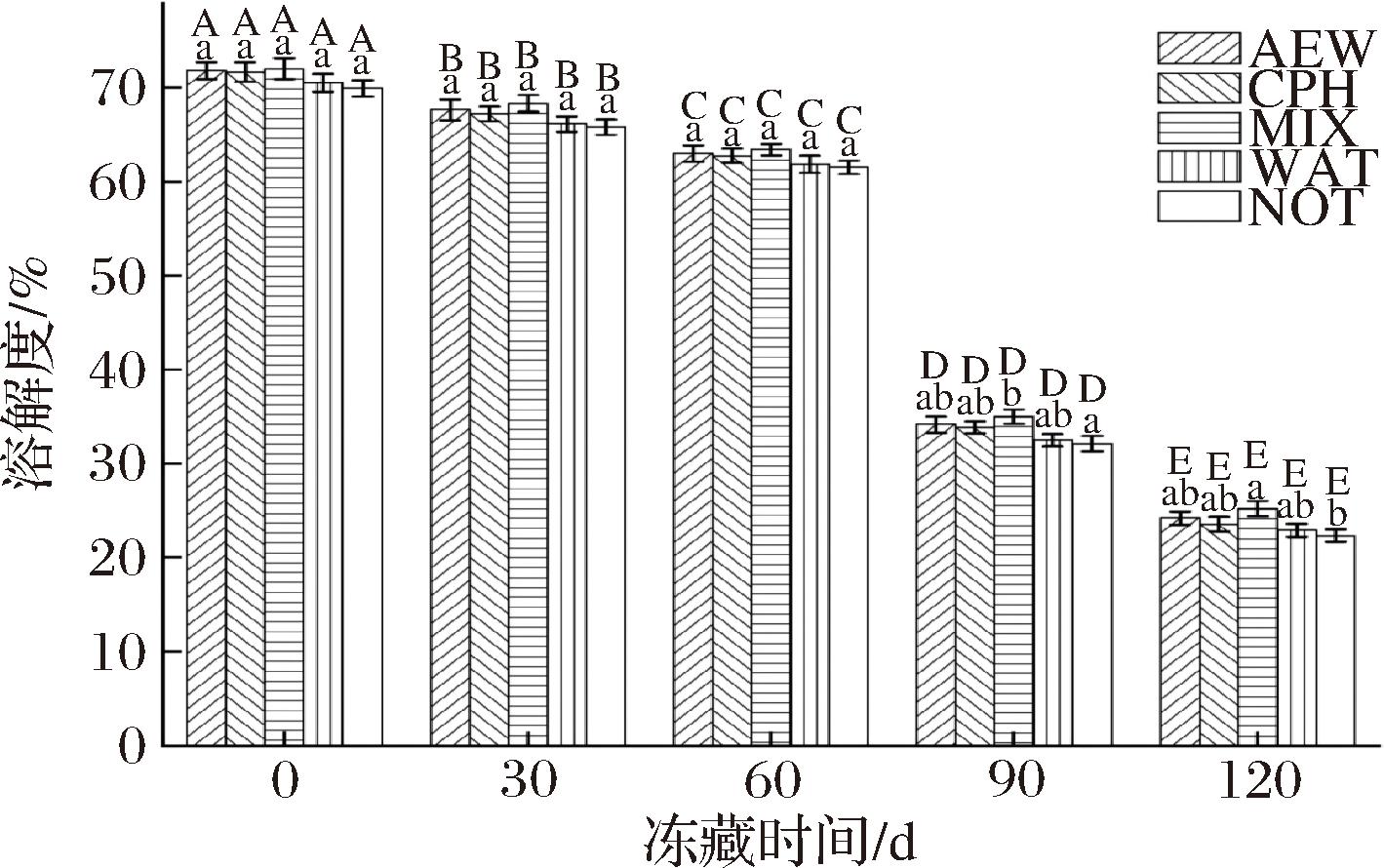
图6 不同浸泡处理对冻藏秘鲁鱿鱼肌原纤维蛋白溶解度的影响
Fig.6 Effect of different immersion treatments on the solubility of myofibrillar proteins in frozen D.gigas
2.7 不同浸泡处理对冻藏秘鲁鱿鱼浊度的影响
如图7所示,在冻藏期间,随着冻藏时间的延长,不同浸泡处理的秘鲁鱿鱼肌原纤维蛋白浊度均呈上升趋势。在冻藏120 d后,AEW组(1.08)的秘鲁鱿鱼肌原纤维蛋白浊度显著小于NOT组(1.18)(P<0.05),MIX组(1.04)的秘鲁鱿鱼肌原纤维蛋白浊度显著小于AEW组(1.08)(P<0.05)。有研究发现,CPH可通过静电斥力作用,使肌原纤维横向膨胀,离子强度增强,蛋白质的溶解度提高。这一过程导致蛋白质分子链的伸展,增强了蛋白质间的排斥力,减小了聚集作用力,从而降低了浊度[12]。而AEW的负ORP在保护蛋白质的活性基团氧化的同时,还有利于α-螺旋的转变,β-转变为β-折叠,可以有效减少鱿鱼蛋白质的浊度的上升[16],MIX组肌原纤维蛋白浊度始终小于AEW组和CPH组,说明混合使用AEW与CPH浸泡秘鲁鱿鱼,可以有效降低秘鲁鱿鱼肌原纤维蛋白的浊度水平。
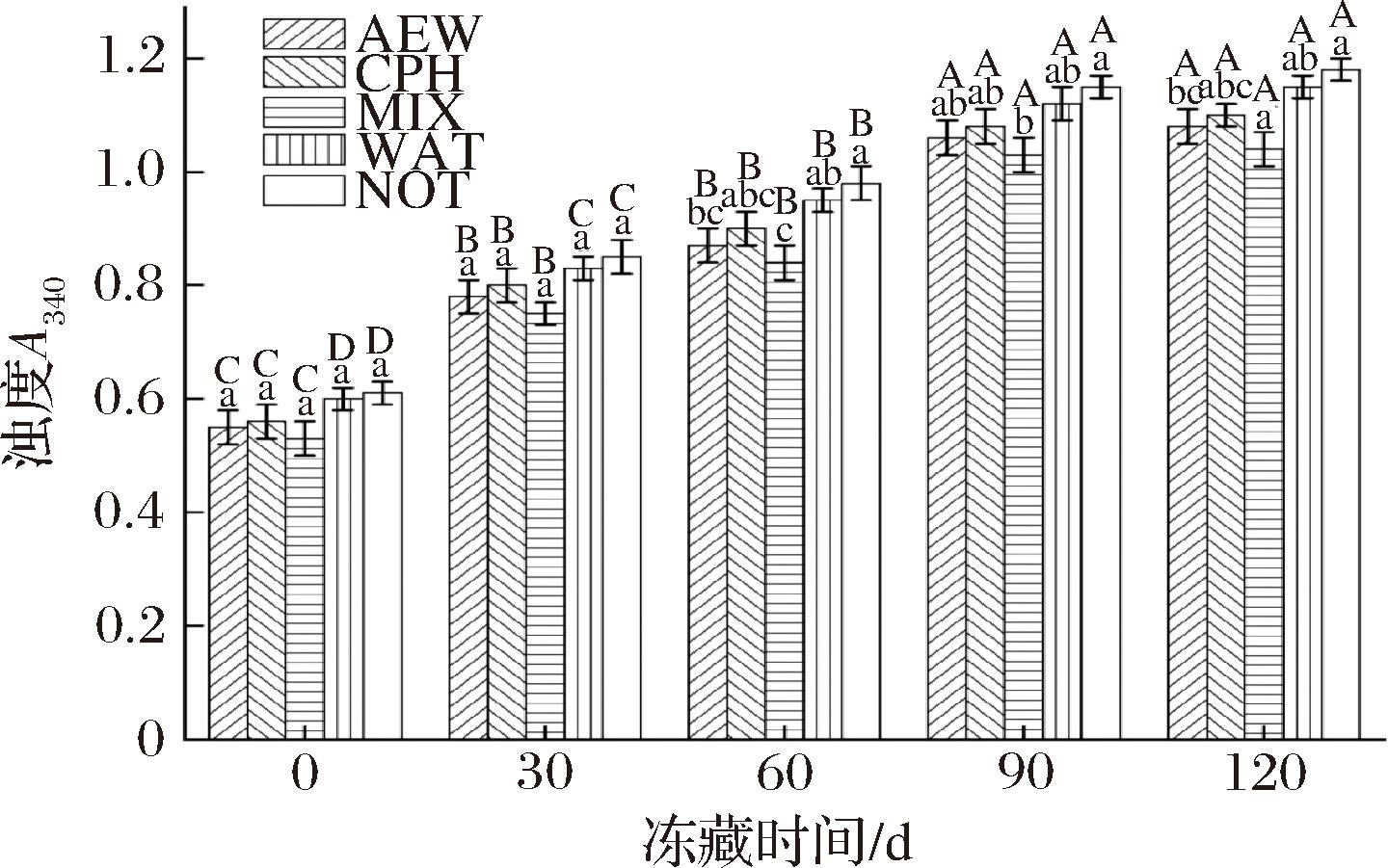
图7 不同浸泡处理对冻藏秘鲁鱿鱼肌原纤维蛋白浊度的影响
Fig.7 Effect of different immersion treatments on the turbidity of myofibrillar proteins in frozen D.gigas
2.8 GC-IMS挥发性有机物分析
图8为不同浸泡处理的秘鲁鱿鱼的GC-IMS二维谱图。RIP峰两侧的每一个点代表一种挥发性有机物[25]。由图8可得,MIX组能够有效的调控冻藏秘鲁鱿鱼的挥发性风味物质谱,抑制脂质氧化和蛋白质腐败降解产生的关键异味物质(醛、酮、酯等),同时有助于保留和形成更佳的风味特征,更能有效地维持肌肉组织相对完整的结构状态。
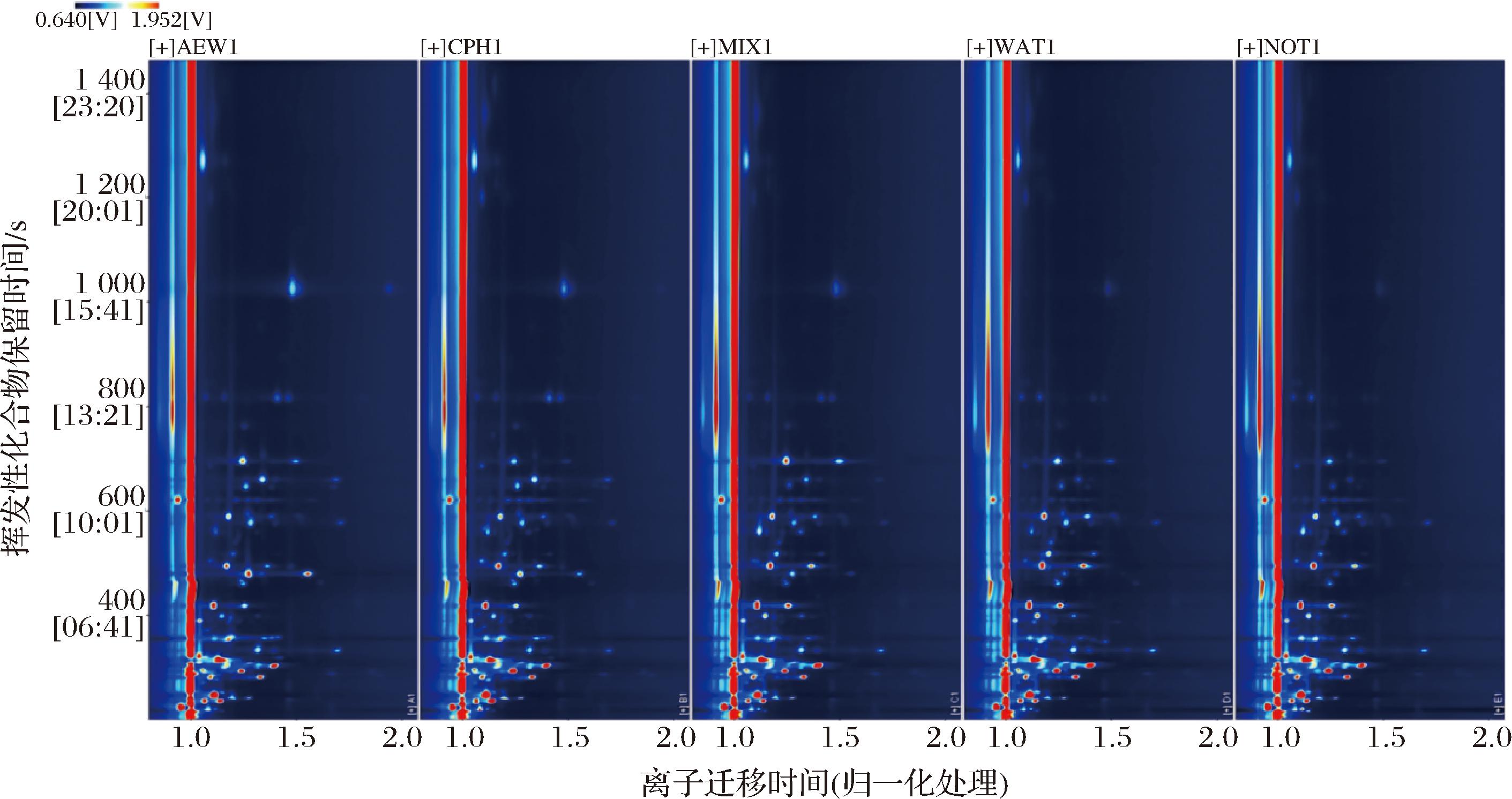
图8 不同浸泡处理的秘鲁鱿鱼的有机物二维图谱
Fig.8 Two-dimensional mapping of organic matter in D.gigas with different immersion treatments
不同浸泡处理的秘鲁鱿鱼的挥发性成分的差异如图9所示。MIX组和CPH组能有效抑制关键异味物质的生成,AEW组抑制能力较弱。WAT与NOT在醛类区域呈现深色,表明这2组脂质氧化衍生异味物质积累最显著,抑制效果最差。酯类区域丰度WAT/NOT>AEW>MIX/CPH,其含量降低进一步印证MIX和CPH处理对脂质降解途径的抑制效果较好。
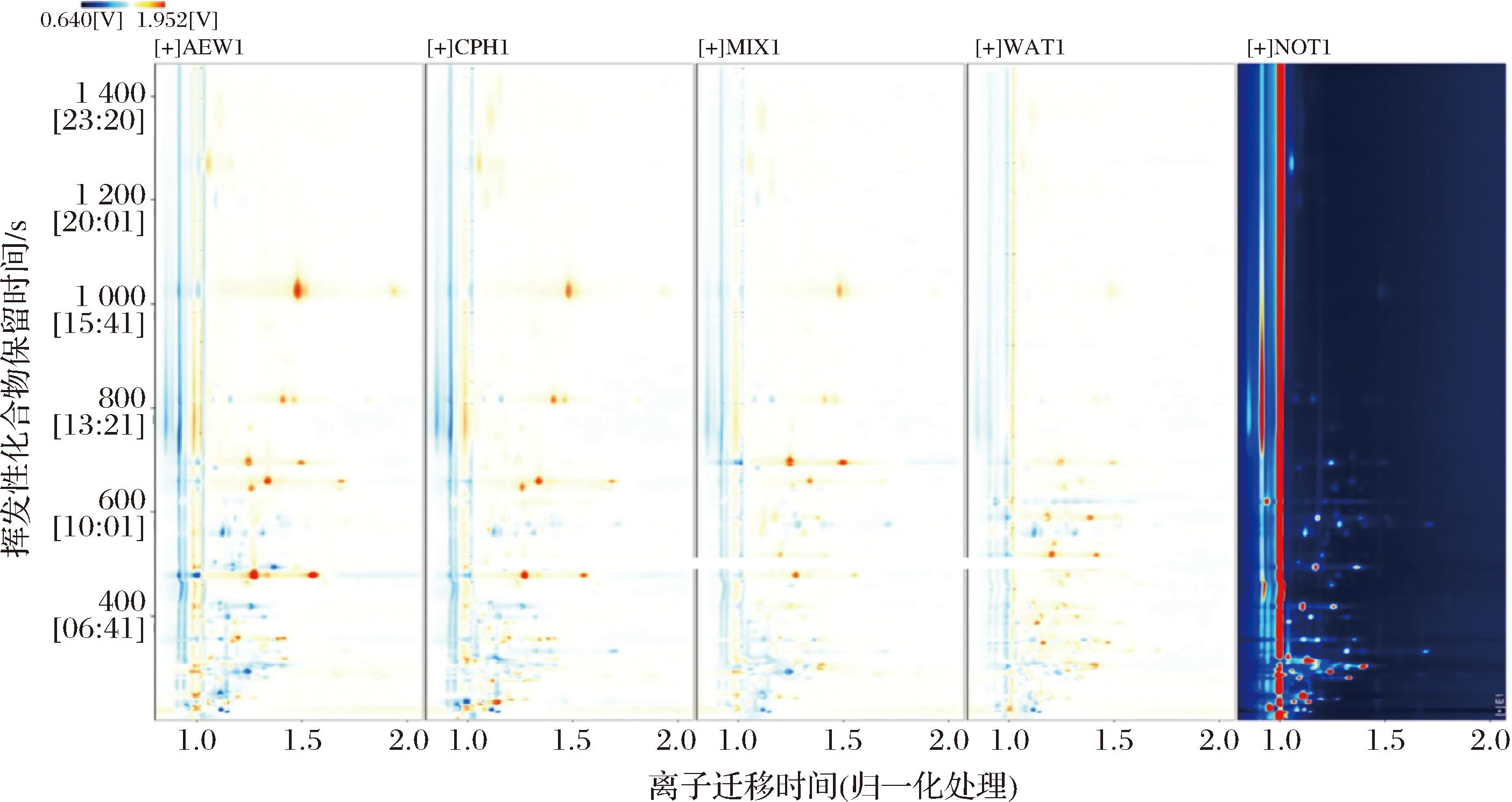
图9 不同浸泡处理的秘鲁鱿鱼的挥发性有机物差异图谱
Fig.9 Differential mapping of volatile organic compounds in D.gigas with different immersion treatments
图10为不同浸泡处理下秘鲁鱿鱼的挥发性有机物指纹图谱,不同处理组的挥发性有机物分布各有差异,既拥有独特的特征峰区域,也存在相互重叠的共同区域。AEW组以长链醛、酯类为主,CPH组醛类及其他类别协同,醇类物质可能是由脂质氧化分解产生的。MIX组中3-甲基-1-丁醇、1-丙醇、二烯丙基硫醚、乙酸异戊酯等物质的含量较高,二烯丙基硫醚属于硫醚类化合物,对整体风味的贡献较大[26],相较于前2组具有更丰富的风味。WAT组中2,3-丁二酮和3-羟基-2-丁酮可能来自鱿鱼中糖类的发酵代谢。NOT组则含丙酸丁酯、戊酸乙酯、乙醇、丙烯醛、二甲基硫醚等物质的含量较高。二甲基硫醚具有强烈的硫臭味,是海鲜类原料常见的特征性挥发性物质,而乙醇的检出可能与鱿鱼自身酶系或环境微生物的发酵活动相关[27]。MIX显著降低醛类(如丙烯醛)、酮类(2,3-丁二酮)及酯类物质的积累,富集3-甲基-1-丁醇(果香)、二烯丙基硫醚(葱蒜香)等关键风味物,维持鱿鱼特征风味;MIX通过抑制脂质氧化与蛋白腐败降解双途径减少异味前体物生成,且AEW的小分子渗透性有助于风味物质在肌肉组织内的均匀分布。

图10 不同浸泡处理的秘鲁鱿鱼的挥发性有机物指纹图谱
Fig.10 Volatile organic compounds fingerprints of D.gigas with different immersion treatments
3 结论与讨论
结果表明AEW和CPH复配的混合组浸泡液相较于AEW和CPH对水产品品质影响更佳。MIX可以减少蛋白氧化变性,减慢巯基含量的减少速度,显著提高秘鲁鱿鱼肌原纤维蛋白的起泡性和泡沫稳定性,提高其溶解度,更好的抑制蛋白质品质劣变,并且有效的降低浊度水平,说明MIX组平衡了离子强度与分子静电斥力,抑制蛋白聚集沉淀。MIX组显著抑制脂质氧化和蛋白质腐败降解产生的关键异味物质(醛、酮、酯等),表明混合溶液浸泡处理组可以更好的保留产品的整体风味,同时能有效的维持肌肉组织相对完整的结构状态。结果表明,AEW与CPH复配(体积比为1∶1)可替代传统磷酸盐单一处理,在维持冻藏鱿鱼蛋白稳定性、加工功能性和风味品质方面具有显著优势,为开发低磷、高效的水产品冻藏护色技术提供科学依据。
[1] ZHU W H, GUO H F, HAN M L, et al.Evaluating the effects of nanoparticles combined ultrasonic-microwave thawing on water holding capacity, oxidation, and protein conformation in jumbo squid (Dosidicus gigas) mantles[J].Food Chemistry, 2023, 402:134250.
[2] 朱文慧, 宦海珍, 步营, 等.低温贮藏和解冻过程对鱿鱼品质的影响研究进展[J].食品科学, 2017, 38(17):279-285.ZHU W H, HUAN H Z, BU Y, et al.Progress in the effects of low-temperature storage and thawing on squid quality[J].Food Science, 2017, 38(17):279-285.
[3] LUO Y, LV H R, LIN H M, et al.Effect of replacing phosphate with alkaline electrolyzed water (AEW) on the quality and microbial diversity of Pacific white shrimp (Litopenaeus vannamei) during frozen storage[J].LWT, 2025, 224:117812.
[4] 郭雨晨, 赵源, 李振坤, 等.海水鱼抗冻剂中复合磷酸盐的优化和应用研究[J].渔业研究, 2024, 46(5):458-467.GUO Y C, ZHAO Y, LI Z K, et al.Optimization and application of compound phosphates in seawater fish antifreeze[J].Journal of Fisheries Research, 2024, 46(5):458-467.
[5] LIN H M, HUNG Y C, DENG S G.Effect of partial replacement of polyphosphate with alkaline electrolyzed water (AEW) on the quality of catfish fillets[J].Food Control, 2020, 112:107117.
[6] ATHAYDE D R, FLORES D R M, DA SILVA J S, et al.Application of electrolyzed water for improving pork meat quality[J].Food Research International, 2017, 100:757-763.
[7] 唐奕彬, 罗燚, 房传栋, 等.碱性电解水部分替代复合磷酸盐对秘鲁鱿鱼品质的影响[J].中国食品学报, 2024, 24(11):279-288.TANG Y B, LUO Y, FANG C D, et al.Effects of alkaline electrolyzed water partial substitution of complex phosphate on the quality of Dosidious gigas[J].Journal of Chinese Institute of Food Science and Technology, 2024, 24(11):279-288.
[8] 姚慧, 祁雪儿, 齐贺, 等.卡拉胶寡糖对秘鲁鱿鱼肌原纤维蛋白功能特性的影响[J].中国食品添加剂, 2020, 31(1):68-75.YAO H, QI X E, QI H, et al.Effects of carrageenan oligosaccharide on functional properties of squid myofibrillar protein (Dosidicus gigas) during frozen storage[J].China Food Additives, 2020, 31(1):68-75.
[9] 朱文慧, 宦海珍, 步营, 等.不同解冻方式对秘鲁鱿鱼肌肉保水性和蛋白质氧化程度的影响[J].食品科学, 2017, 38(11):6-11.ZHU W H, HUAN H Z, BU Y, et al.Effect of different thawing methods on water holding capacity and protein oxidation in Dosidicus gigas[J].Food Science, 2017, 38(11):6-11.
[10] 张斌. 鸡蛋清蛋白对秘鲁鱿鱼鱼糜凝胶过程的影响及其作用机制研究[D].杭州:浙江工商大学, 2023.ZHANG B.Effect of egg white on the gel process of Peruvian squid surimi and its mechanism[D].Hangzhou:Zhejiang Gongshang University, 2023.
[11] XUE S W, XU X L, SHAN H M, et al.Effects of high-intensity ultrasound, high-pressure processing, and high-pressure homogenization on the physicochemical and functional properties of myofibrillar proteins[J].Innovative Food Science &Emerging Technologies, 2018, 45:354-360.
[12] 曾淑薇, 李吉, 熊善柏, 等.磷酸盐对草鱼肌原纤维蛋白结构的影响[J].食品科学, 2014, 35(23):48-51.ZENG S W, LI J, XIONG S B, et al.Effects of phosphates on the structure of myofibrillar proteins from grass carp muscle[J].Food Science, 2014, 35(23):48-51.
[13] 姚慧, 祁雪儿, 毛俊龙, 等.3种鱿鱼冻藏过程中肌原纤维蛋白功能特性变化[J].食品科学, 2021, 42(7):207-213.YAO H, QI X E, MAO J L, et al.Changes in functional properties of myofibrillar proteins in three species of squid during frozen storage[J].Food Science, 2021, 42(7):207-213.
[14] WU M X, XU Q, DING H, et al.Application of antifreeze substances in food cryopreservation[J].Foods, 2025, 14(12):2089.
[15] CHEN J Y, REN Y X, ZHANG K S, et al.Site-specific incorporation of sodium tripolyphosphate into myofibrillar protein from Mantis shrimp (Oratosquilla oratoria) promotes protein crosslinking and gel network formation[J].Food Chemistry, 2020, 312:126113.
[16] LI Y F, ZENG Q H, GUANG L, et al.Effects of ultrasound-assisted basic electrolyzed water (BEW) extraction on structural and functional properties of Antarctic krill (Euphausia superba) proteins[J].Ultrasonics Sonochemistry, 2021, 71:105364.
[17] 常娅妮, 马俪珍, 杨梅, 等.不同冷冻方式对调味鱼贮藏期间肌原纤维蛋白的影响[J].肉类研究, 2019, 33(10):63-68.CHANG Y N, MA L Z, YANG M, et al.Effects of different freezing methods on myofibrillar proteins from prepared fish products during storage[J].Meat Research, 2019, 33(10):63-68.
[18] 方海砚, 苑歆, 刘友明, 等.羟自由基氧化对鲢鱼肌原纤维蛋白结构的影响[J].食品工业科技, 2020, 41(4):6-12.FANG H Y, YUAN X, LIU Y M, et al.Effect of hydroxyl radical oxidation on the structure of silver carp myofibrillar protein[J].Science and Technology of Food Industry, 2020, 41(4):6-12.
[19] WU X J, LI F, WU W.Effects of oxidative modification by 13-hydroperoxyoctadecadienoic acid on the structure and functional properties of rice protein[J].Food Research International, 2020, 132:109096.
[20] 夏立志, 鲁玉凤, 李强, 等.3种磷酸盐对白鲢鱼肌原纤维蛋白磷酸化的影响[J].肉类研究, 2024, 38(1):10-18.XIA L Z, LU Y F, LI Q, et al.Effect of three phosphates on the phosphorylation of myofibrillar proteins from silver carp[J].Meat Research, 2024, 38(1):10-18.
[21] ZHAO Q L, HONG X, FAN L P, et al.Solubility and emulsifying properties of Perilla protein isolate:Improvement by phosphorylation in the presence of sodium tripolyphosphate and sodium trimetaphosphate[J].Food Chemistry, 2022, 382:132252.
[22] 严红波. 三种带鱼贮藏及加工品质变化机制研究[D].舟山:浙江海洋大学, 2022.YAN H B.Study on the physicochemical properties and its alternationmechanisms of three type of hairtail during process and storage[D].Zhoushan:Zhejiang Ocean University, 2022.
[23] 殷春雁, 赵宇婷, 刘自单, 等.磷酸盐存在时食品大分子的干燥加热磷酸化及其多功能化研究进展[J].食品研究与开发, 2020, 41(18):208-212.YIN C Y, ZHAO Y T, LIU Z D, et al.Dry-heating and phosphorylation of macromolecules of foods for the research of their functional variations:A review[J].Food Research and Development, 2020, 41(18):208-212.
[24] 尚坤. 不同磷酸盐对虾蛄肌原纤维蛋白功能特性的影响及应用[D].天津:天津商业大学, 2019.SHANG K.Effects of different phosphates on functional properties of myofibrillar protein from mantis shrimp and application[D].Tianjin:Tianjin University of Commerce, 2019.
[25] FENG Y Z, CAI Y, FU X, et al.Comparison of aroma-active compounds in broiler broth and native chicken broth by aroma extract dilution analysis (AEDA), odor activity value (OAV) and omission experiment[J].Food Chemistry, 2018, 265:274-280.
[26] 赵玲, 胡梦月, 曹荣, 等.蓝鳍金枪鱼不同部位肌肉的营养与主要风味分析[J].渔业科学进展, 2023, 44(1):219-227.ZHAO L, HU M Y, CAO R, et al.Analysis of nutrition and major flavor of different muscle parts of Thunnus thynnus[J].Progress in Fishery Sciences, 2023, 44(1):219-227.
[27] 李倩, 夏光丽, 曹荣, 等.仿刺参性腺酶解过程风味变化[J].渔业科学进展, 2022, 43(6):239-248.LI Q, XIA G L, CAO R, et al.Changes in the flavor of Apostichopus japonicus gonads during enzymatic hydrolysis[J].Progress in Fishery Sciences, 2022, 43(6):239-248.