白酒是世界六大蒸馏酒之一,拥有数千年历史[1],根据其风格的不同,可分为浓香型、酱香型、清香型和米香型四大基础香型,在此基础上又演化出兼香型、凤香型、董香型等8种小香型,其中浓香型白酒是我国最畅销的香型,常年在白酒市场占据主导地位[2]。大曲作为浓香型白酒的糖化发酵剂[3],为白酒酿造提供丰富的菌系、酶系和物系,造就其独特的风味和特征。然而,传统大曲生产主要依赖于环境微生物的富集[4],容易遭受环境因素波动的影响,极易造成大曲质量的不稳定,从而影响白酒的品质,因此如何提高大曲质量的稳定性是白酒行业面临的难题[1]。
通过接种特定内源性功能微生物对大曲进行生物强化是目前提高大曲质量和稳定性的有效途径之一[5]。例如,利用高产己酸乙酯酵母进行大曲的强化生产[6],显著提高了大曲的代谢活性和己酸乙酯的含量。接种扣囊复膜孢酵母对大曲进行强化后[7],大曲中乳球菌属(Lactococcus)和魏斯氏菌等功能乳酸菌的丰度有所升高,其酶活力全面提升。此外,有研究表明将强化大曲应用于白酒酿造,可以提高白酒的感官品质和风味物质含量[8]。
酯酶又被称为羧酸酯酶[9],能催化脂肪酸酯的合成与分解,它是催化浓香型白酒主体风味物质己酸乙酯合成的主要酶类,在白酒酿造过程中具有重要作用。实验室前期从浓香型白酒大曲中筛选出一株高产酯酶的栗酒裂殖酵母(Schizosaccharomyces pombe JM2-5),其酶活力可达15.52 U/mL。本研究使用S.pombe JM2-5进行强化大曲生产应用,并对其微生物群落结构、理化指标以及风味物质进行分析验证,以期提高浓香型白酒大曲质量和稳定性,进而提升白酒品质,同时也为白酒行业的生物强化调控发酵生产提供一定的理论基础。
1 材料与方法
1.1 材料
1.1.1 菌株与培养基
菌株S.pombe JM2-5分离自浓香型白酒大曲。
酵母浸出粉胨葡萄糖培养基(g/L):10酵母膏,20蛋白胨,20葡萄糖。
1.1.2 浓香型大曲
对照曲和强化曲均生产于安徽某浓香型白酒酒厂。大曲在曲房发酵30 d为发酵期大曲,发酵期大曲贮存于指定库房4个月为成熟大曲。为保证实验效果,选取往年大曲质量差异较小的曲房进行发酵,强化大曲和对照曲各制作一房曲。为保证取样的科学性和一致性,每次取样采用5点取样法选取15块曲块,示例见图1,将每块曲块粉碎后各取50 g混合均匀为1个样本,每种曲每个时期取3个样本作为生物学重复。
图1 取样示例图
Fig.1 The example diagram of sampling
1.2 实验方法
1.2.1 强化大曲的制备
将菌株S.pombe JM2-5用酵母浸出粉胨葡萄糖液体培养基活化,经二级扩大培养为10 L菌体浓度108 CFU/mL的菌液,将培养好的菌液倒入1 000 L贮水池后充分混匀,使得菌体浓度为106 CFU/mL,调整菌液流速和制曲原料的流加速度使得液料比为1∶3(mL∶g),菌液与制曲原料经角龙搅拌和制曲机压制后成曲,每块曲块质量约为6 kg,菌液约为1.5 kg,制作一房强化曲,随后将曲块转入曲房培养。
1.2.2 大曲DNA 提取、纯化、PCR 扩增和高通量测序
利用Power Soil® DNA试剂盒从大曲样品中(0.5 g)提取DNA[10],随后使用Nano Drop one紫外分光光度计对提取到的DNA进行纯度和浓度测定,然后将DNA样本密封保存至-80 ℃超低温冰箱,最后将其送往上海派森诺生物科技有限公司,使用Illumina MiSeq平台进行高通量测序。选取引物338F和806R对细菌的16S rRNA基因的V3~V4区进行PCR扩增;选取引物5-1737F和2-2043R扩增真菌的ITS 1区。采用QIIME 2 (2019.4)软件对其进行去除引物、质量过滤、去噪、序列拼接和去除嵌合体处理。随后使用Vsearch (v2.13.4-linux-x86-64)和cutadapt (v2.3)软件对序列进行聚类,在相似度97%以上为标准,生成代表序列和操作分类单元(operational taxonomic unit,OTU)表。最后,采用QIIME2的classifier-sklearn算法对OTU的代表性序列进行分类学比对,对于细菌选用Silva数据库进行注释,真菌选用Unite数据库对物种进行注释。
1.2.3 大曲理化指标检测
大曲的理化测定按照QB/T 4257—2011《酿酒大曲通用分析方法》进行测定[11],包括水分、可滴定酸度、液化力、糖化力、发酵力和酯化力。
1.2.4 大曲风味物质测定
采用顶空固相微萃取/气相色谱-质谱联用(headspace solid-phase micro extraction and gas chromatography mass spectrometry, HS-SPME-GC-MS)方法进行大曲风味物质的检测和定性定量分析。称取0.500 0 g大曲样品和10 mL饱和氯化钠饱和溶液均匀混合后置于20 mL顶空瓶中,再加入10 μL 2-辛醇溶液(0.002 74 g/100 mL,内标)。随后将样品顶空吸附45 min,萃取头于250 ℃进样口下解析5 min,再进行GC-MS分离鉴定。
气相色谱条件:色谱柱 HP-INNOWAX(规格为0.25 μm×60.0 m×0.25 mm),设置进样口温度为250 ℃,进样方式为不分流进样。升温程序:初始柱温40 ℃,保温4 min,随后以4 ℃/min的升温速度升至100 ℃,再以6 ℃/min的升温速度升至230 ℃,保持10 min;载气为高纯氦气,流速为1 mL/min。
质谱条件:电子电离(EI)离子源,电子能70 eV,离子源温度为230 ℃,溶剂延迟3 min;扫描模式为全扫描,质量扫描范围m/z:40~450。
1.3 数据处理
大曲理化指标、物种相对丰度、大曲风味物质含量等的测定均采用3次重复;采用生科云平台(https://www.bioincloud.tech/task-meta)和派森诺云平台(https://www.genescloud.cn/home)对微生物组成和风味物质进行相关生物分析。
2 结果与分析
2.1 大曲Alpha多样性
采用扩增子测序分析大曲的微生物群落组成,12个大曲样品经质控后分别获得746 039条16S rRNA和872 465条ITS1高质量基因序列,上述序列的覆盖率均超过99%,表明测序深度足够,满足后续实验要求。生物样本的Alpha多样性通常由Chao1和Shannon指数表征,结果见表1。在细菌微生物群落方面,发酵期和成熟期对照曲的细菌群落多样性均高于强化曲,而强化曲的细菌群落物种丰度在发酵期和成熟期均高于对照曲。真菌群落方面,发酵期对照曲真菌群落多样性和物种丰度高于强化曲,成熟后,强化曲的真菌群落和物种丰度均高于对照曲。结果表明,接种S.pombe JM2-5提高了大曲细菌群落的物种丰度,并且提高了成熟期强化曲的真菌群落物种多样性和物种丰度,生物强化对大曲的微生物群落产生了较大扰动。
表1 大曲样品的Alpha多样性分析
Table 1 Analysis of Alpha diversity of Daqu
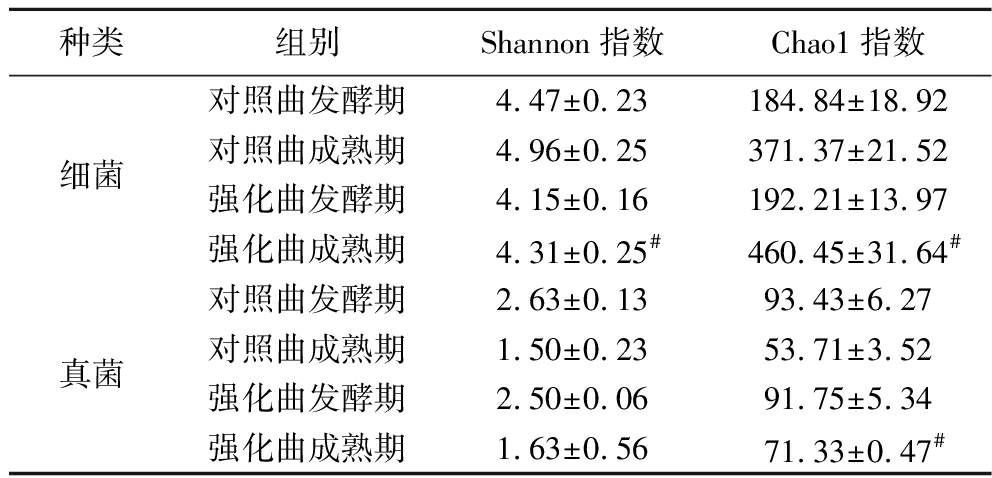
种类组别Shannon指数Chao1指数对照曲发酵期4.47±0.23184.84±18.92细菌对照曲成熟期4.96±0.25371.37±21.52强化曲发酵期4.15±0.16192.21±13.97强化曲成熟期4.31±0.25#460.45±31.64#对照曲发酵期2.63±0.1393.43±6.27真菌对照曲成熟期1.50±0.2353.71±3.52强化曲发酵期2.50±0.0691.75±5.34强化曲成熟期1.63±0.5671.33±0.47#
注:#表示强化曲与对照曲成熟期之间存在显著性差异,显著水平均为P<0.05(下同)。
2.2 大曲Beta多样性
对照曲与强化曲的主坐标分析(principal coordinate analysis, PCoA)见图2,大曲的细菌群落中,主成分得分为88%,表明此PCoA图可以解释细菌群落中62.4%的变异。对照曲与强化曲形成2个不同的组别,表明对照曲与强化曲的细菌群落差异主要是由大曲类别贡献的,即S.pombe JM2-5生物强化对大曲的细菌群落组成有较大扰动。而真菌群落则与之相反,发酵期对照曲与强化曲集中在一部分,成熟期对照曲与强化曲集中在另一部分,表明发酵时间是大曲真菌群落变异的主要贡献因素,也可能是生物强化使得发酵期强化大曲的真菌群落发生变化,而发酵时间将这种变化进一步放大,两者共同促进了大曲真菌群落的变异。
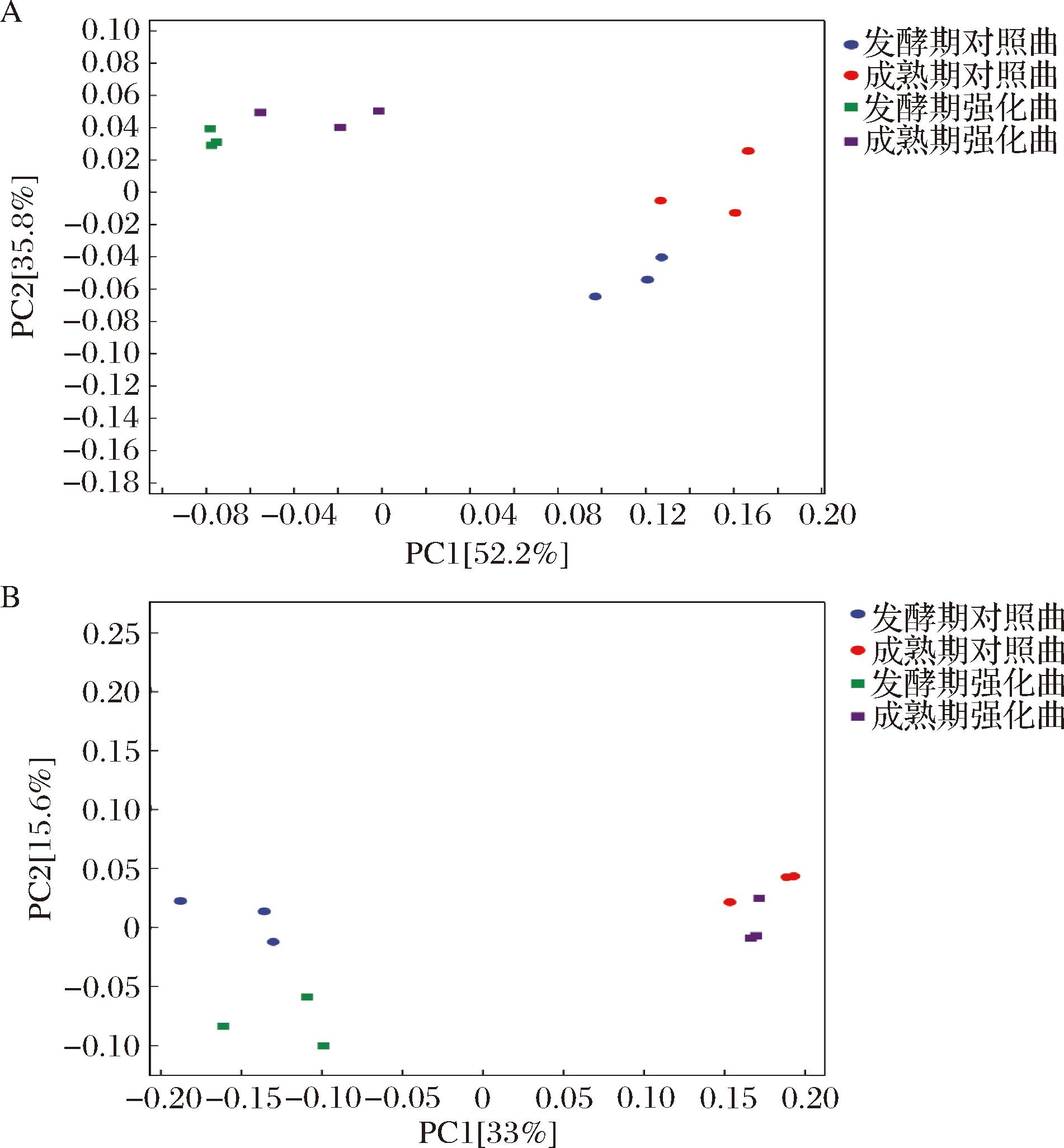
A-细菌属;B-真菌属
图2 对照曲与强化曲PCoA分析
Fig.2 PCoA analysis of control Daqu and fortified Daqu
2.3 大曲微生物组成
发酵期与成熟期的对照曲和强化曲微生物群落组成见图3,由图3-A可得,对照曲优势细菌门(某时期相对丰度>1%)为厚壁菌门(Firmicutes),变形菌门(Proteobacteria)、放线菌门(Actinobacteriota)以及梭杆菌门(Fusobacteriota),强化曲的优势菌门仅为厚壁菌门和变形菌。此前有研究表明[12],厚壁菌门和变形菌门是浓香型和酱香型白酒大曲的优势菌门。强化曲和对照曲的优势真菌门(图3-C)为子囊菌门(Ascomycota)和毛霉菌门(Mucoromycota),担子菌门(Basidiomycota)是独属于发酵期对照曲的优势真菌门,对照曲成熟后其优势菌门与对照曲一致。其中厚壁菌门和子囊菌门分别是细菌和真菌的主要菌门(相对丰度>10%)。强化曲和对照曲在成熟过程中,真菌门水平的变化是一致的,即子囊菌门的相对丰度不断提升,占据绝对优势,2种大曲在真菌门水平无显著的差异。
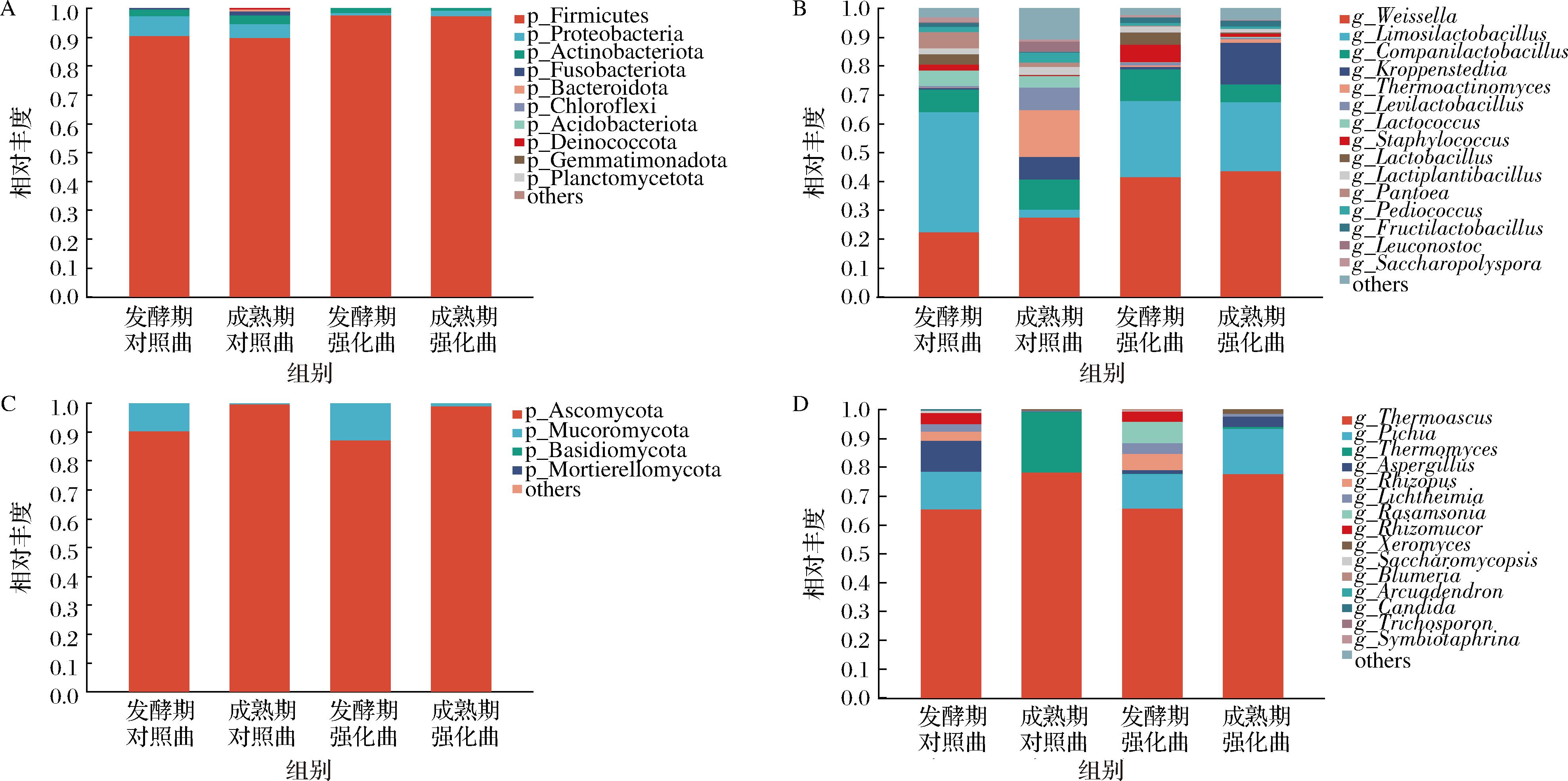
A-门水平细菌;B-属水平细菌;C-门水平真菌;D-属水平真菌
图3 大曲微生物群落组成
Fig.3 Microbial community composition in Daqu
在细菌属水平上(图3-B),粘液乳杆菌属(Limosilacto bacillus)和魏斯氏菌属(Weissella)是强化曲和对照曲共有的2个主要细菌属(某时期相对丰度大于10%),这与四川、安徽等地的浓香型白酒大曲细菌群落组成相似[13]。魏斯氏菌属是白酒中重要的乳酸菌[14],对浓香型白酒酿造过程中的风味形成和代谢调控有重要作用,其相对丰度在强化曲的全时期都显著高于对照曲(P<0.05)。此外,成熟后的对照曲和强化曲中魏斯氏菌属相对丰度都有所提升,这与大多数白酒大曲成熟后的变化一致,因此魏斯氏菌属被认为是浓香型白酒大曲的成熟标志菌属[15]。高温放线菌属(Thermoactinomyces,成熟期对照曲16.08%)和克罗彭斯特德菌属(Kroppenstedtia,成熟期强化曲14.53%)分别是对照曲和强化曲特有的主要细菌属。有研究表明,克罗彭斯特德菌属能促进丙酮酸代谢和三羧酸循环[16],因此在大曲中被认为是次级代谢产物的重要产生者,此外,克罗彭斯特德菌属可以利用多种碳源和氮源[17],合成己酸乙酯、吡嗪和乙酸等重要的风味成分。高温放线菌属能耐大曲发酵过程中的高温[18],具有开发高温淀粉酶、蛋白酶和酯化酶的潜力。乳球菌属(Lactococcus)在强化曲中的相对丰度显著下降(P<0.05),乳球菌属产生的某些细菌素可以抑制大曲微生物的生长代谢[19],其丰度在强化曲的下降可能有利于强化曲微生物群落的演替。
真菌属水平(图3-D)嗜热子囊菌属(Thermoascus)和毕赤酵母属(Pichia)是强化曲和对照曲共有的主要真菌属(某时期相对丰度大于10%),嗜热子囊菌属在白酒酿造过程中可以产生多种具有高活力及热稳定性的水解酶(α-淀粉酶,纤维素酶等),对大曲原料的降解和微生物代谢网络的构建有重要作用[20]。毕赤酵母属在所有香型的白酒中都被认为是酯类物质的重要产生者[21],有助于白酒特征风味的形成,毕赤酵母属的相对丰度在发酵期对照曲与强化曲相差不大,但在成熟期表现出差异:对照曲(发酵期12.71%,成熟期0.08%)成熟后毕赤酵母属丰度急剧下降,强化曲(发酵期10.66%,成熟期15.62)成熟后其丰度有所提升,其成熟期丰度相较于对照曲有显著提高(P<0.05)。与之类似的是曲霉属(Aspergillus),曲霉属是大曲中液化力和糖化力的重要贡献菌属[22],对照曲中曲霉属相对丰度(发酵期9.99%,成熟期0.23%)在成熟后有显著下降(P<0.05),而强化曲中曲霉属相对丰度(发酵期1.4%,成熟期3.58%)在成熟后显著升高(P<0.05)。成熟期对照曲中嗜热子囊菌属和嗜热真菌属(Thermomyces)两菌属丰度之和达到了99.12%,占绝了绝对优势,其他菌属只有1%不到的丰度,这与何猛超等[23]的研究一致。成熟期对照曲的优势真菌属(相对丰度>1%)只有嗜热子囊菌数和嗜热真菌属,而强化曲的优势真菌属有嗜热子囊菌属、毕赤酵母属、曲霉属以及耐干霉菌属(Xeromyces)4种优势真菌属。
以上结果表明,S.pombe JM2-5生物强化对大曲微生物群落的门水平没有产生明显变化,但却显著改变了大曲属水平的微生物组成:生物强化使得大曲细菌属魏斯氏菌属、克罗彭斯特德菌属和乳球菌属发生了显著改变,并且显著降低了嗜热真菌属的相对丰度,使得更多的功能真菌属(曲霉属、毕赤酵母属等)参与大曲微生物群落演替。
2.4 大曲微生物关联网络
为研究生物强化对大曲微生物互相作用关系的影响,选取对照曲、强化曲相对丰度前15的细菌属、真菌属进行微生物关联网络分析(Spearman’s rank correlations,|ρ|>0.6,P<0.05)[12],选取丰度结果前30进行展示,结果见图3。接近中心性和介数中心性是衡量微生物关联网络中的重要指标[24],接近中心性表示一个网络节点与网络中其他所有节点的最短路径长度之和的倒数,如果接近中心性值越高,表明其在微生物网络中有更高效的代谢物质交流,介数中心性计算的是网络中所有最短路径经过该节点的次数,该值越高,表明该节点在关联网络中参与的代谢交流越频繁[25]。
对照曲微生物关联网络中(图4-A),其边数为56,其中正相关边数为29,正相关占比51.79%,负相关边数为27,占比为48.21%,所有节点的平均接近中心性和平均介数中心性分别为11.17和29.91。对照曲微生物关联网络中,粘液乳杆菌属和发酵剂乳杆菌属(Levilactobacillus)的介数中心性最高,分别为80.86和79.36,同时,两者的接近中心性值分别为13.75和11.17,粘液乳杆菌属作为对照曲的主要菌属,积极地参与了大曲微生物的代谢交流。粘液乳杆菌属和发酵剂乳杆菌属的关联度分别为8和4,但大多与其他菌属呈现出显著的负相关,粘液乳杆菌属与芽孢杆菌属(Bacillus)、嗜热子囊菌属、嗜热放线菌属以及克罗彭斯特德菌属呈显著负相关,发酵剂乳杆菌属与葡萄球菌属(Staphylococcus)、泛菌属(Pantoea)以及覆膜孢酵母菌属(Saccharomycopsis)呈显著负相关,可能是由于发酵剂乳杆菌产生的抑菌细菌素会对某些微生物产生抑制作用[19]。魏斯氏菌属作为对照曲的主要菌属,并未出现在前30的关联丰度关联网络中,说明其与其他菌属的相关性和代谢交流不显著。嗜热子囊菌属的接近中心性和介数中心性分别为12.17和27.02,关联度为6,与克罗彭斯特德菌属、高温放线菌属以及芽孢杆菌属呈显著正相关,高温放线菌属与嗜热子囊菌数都可产生许多耐热水解酶,两者呈正相关,有利于大曲群落微生物对原料的利用。嗜热真菌属和毕赤酵母属在成熟前后丰度发生显著改变,因此两者在关联网络中呈现显著负相关,嗜热子囊菌属除和芽孢杆菌属呈正相关外,与假丝酵母属(Candida)和根毛霉属(Rhizomucor)等4个菌属均呈负相关。
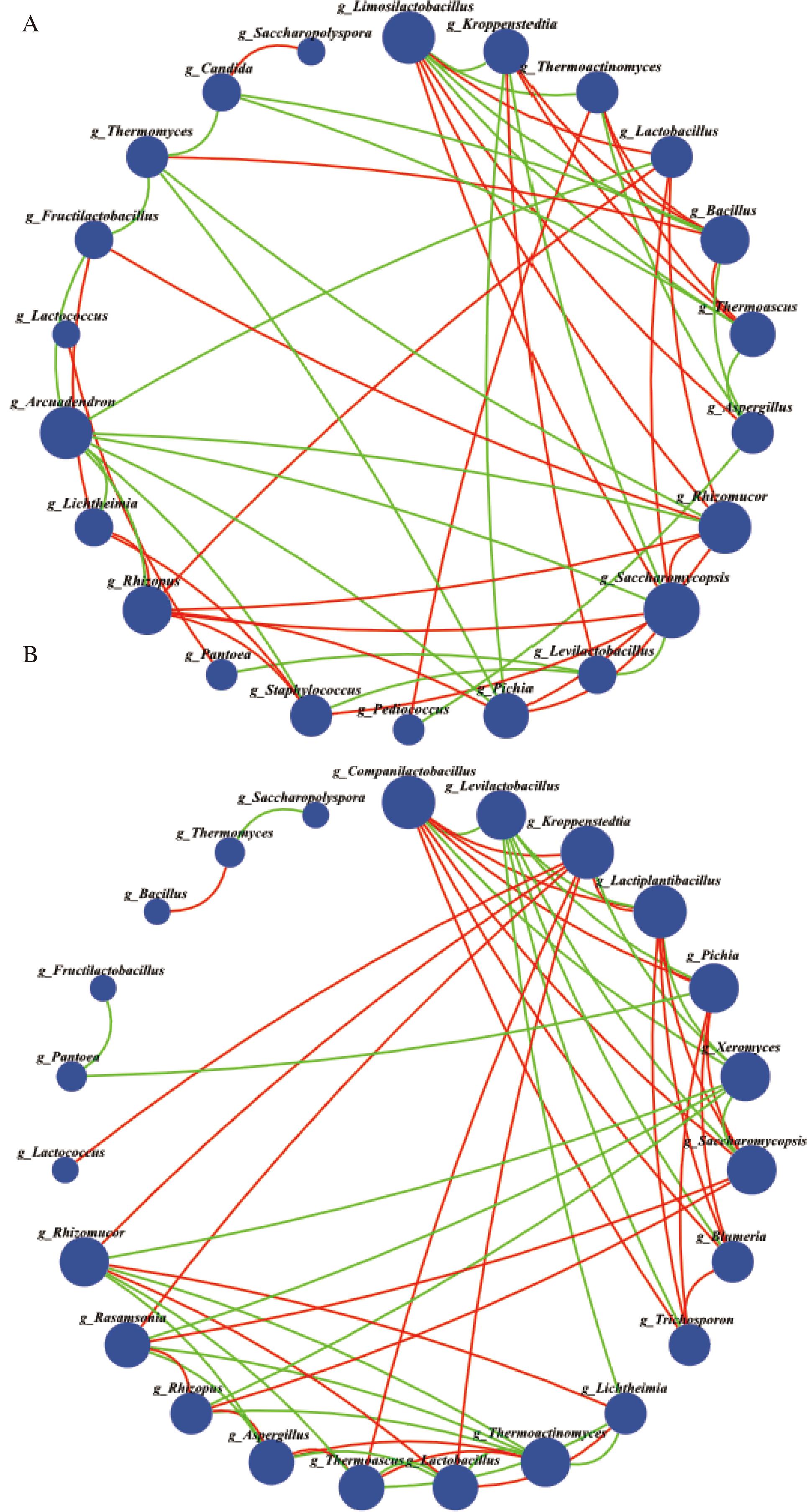
A-对照曲;B-强化曲
图4 对照曲与强化曲微生物关联网络
Fig.4 Microbial association network of control Daqu and fortified Daqu
注:红色线条表示显著正相关,绿色线条表示显著负相关,节点大小表示关联度大小。
强化曲的微生物关联网络(图4-B),其边数59,其中正相关边数为31,占比为52.54%,负相关边数为28,占比为47.46%,所有节点的平均接近中心性和平均介数中心性分别为9.88和19.30,强化曲平均介数中心性较对照曲有一定降低,表明强化曲整体的微生物互相作用较对照曲有所下降。与对照曲明显不同的是,克罗彭斯特德菌属和毕赤酵母属成为了强化曲中介数中心性最高的菌属,两者的介数中心性值分别为75.31和70.47,接近中心性值分别为13.08和12.00,均高于平均接近中心性值。克罗彭斯特德菌属关联度为8,与嗜热嗜热子囊菌属、乳酸杆菌属以及根毛霉属等7个菌属呈显著正相关,嗜热子囊菌属对大曲原料进行降解,有利于克罗彭斯特德菌属和乳酸杆菌属对大曲风味物质的合成。毕赤酵母属的关联度为7,与泛菌属和发酵剂乳杆菌属呈显著负相关,与植物乳植杆菌属(Lactiplantibacillus)、覆膜孢酵母菌属以及布氏白粉菌属(Blumeria)5个菌属呈显著正相关。在对照曲中介数中心性值最高的发酵剂乳杆菌属,在强化曲中介数中心性值为34.36,类似的,嗜热子囊菌属在强化曲的介数中心性值也有所下降,在强化曲中仅为5.47,远低于平均值19.30,可能是生物强化使得强化曲中的克罗彭斯特德菌属和毕赤酵母属对发酵剂乳杆菌属和嗜热子囊菌属的代谢交流产生了影响,进而降低其与大曲微生物的互相作用。
以上结果表明,生物强化对大曲微生物关联网络有一定改变,强化曲整体的介数中心性低于对照曲,表明强化曲整体的微生物互相作用较对照曲有所下降,但克罗彭斯特德菌属和毕赤酵母属在强化曲中介数中心性较对照曲有明显提升,且两者与多数菌属呈显著正相关,使得两者与其他微生物的互相作用加强,有利于大曲风味物质的形成。
2.5 大曲理化指标
大曲的理化指标在一定程度上可以反映大曲发酵过程中的状态和大曲质量,大曲的理化结果见表2,强化曲和对照曲的各项理化指标均符合QB/T 4259—2011《浓香大曲》要求。大曲酸度是衡量大曲质量的一个重要指标[26],酸度过高时,会抑制大曲微生物的生长代谢,进而影响大曲微生物的功能。强化曲在成熟期的酸度(0.81 mmol/10 g)显著低于对照曲(0.89 mmol/10 g)(P<0.05),可能是由于强化曲成熟期乳球菌属和伴生乳杆菌属(Companilactobacillus)相对丰度的下降,此前有研究表明这2种微生物能代谢产生、堆积大量有机酸[27]。对照曲与强化曲发酵时期的水分含量都高于成熟期,成熟后强化曲和对照曲水分含量分别下降了20.86%和17.38%。发酵力是衡量大曲质量的一个重要指标,一般采用微生物利用还原性糖发酵产生二氧化碳的多少来计算[28]。发酵期和成熟期强化曲发酵力(发酵期0.51 U,成熟期0.64 U)显著低于对照曲(发酵期0.91 U,成熟期0.98 U)(P<0.05),分别下降了43.95%和34.69%。此前有研究表明[28],高温放线菌属和嗜热真菌属能分泌多种耐高温功能酶,对大曲的发酵力有一定提升,而强化曲中2个菌属的相对丰度均有不同程度的下降,从而影响了强化曲的发酵力。
表2 大曲理化指标
Table 2 The physicochemical parameters of Daqu
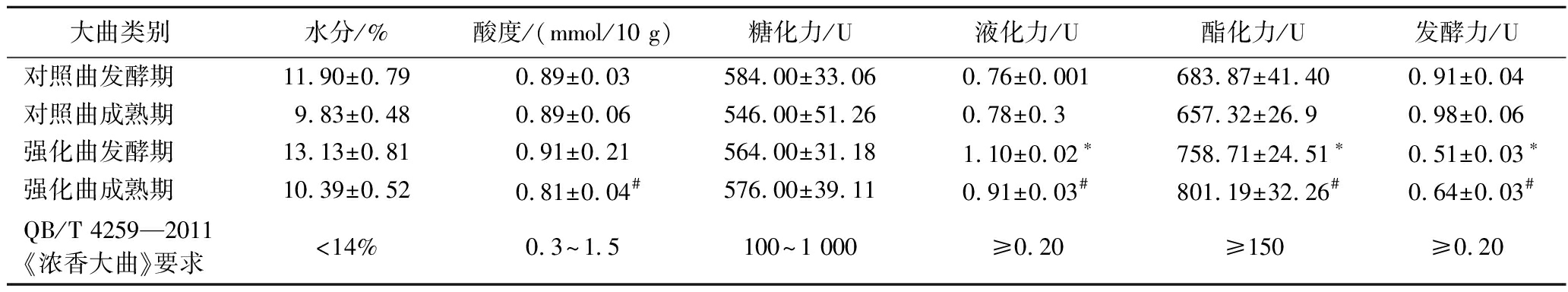
大曲类别水分/%酸度/(mmol/10 g)糖化力/U液化力/U酯化力/U发酵力/U对照曲发酵期11.90±0.790.89±0.03584.00±33.060.76±0.001683.87±41.400.91±0.04对照曲成熟期9.83±0.480.89±0.06546.00±51.260.78±0.3657.32±26.90.98±0.06强化曲发酵期13.13±0.810.91±0.21564.00±31.181.10±0.02∗758.71±24.51∗0.51±0.03∗强化曲成熟期10.39±0.520.81±0.04#576.00±39.110.91±0.03#801.19±32.26#0.64±0.03#QB/T 4259—2011《浓香大曲》要求<14%0.3~1.5100~1 000≥0.20≥150≥0.20
注:*表示强化曲与对照曲发酵期之间存在显著性差异,显著水平均为P<0.05。
强化曲的酯化力在全时期都显著高于对照曲(P<0.05),发酵期和成熟期对照曲酯化力分别为683.87 U和657.32 U,强化曲分别为758.71 U和801.19 U,分别显著提高了10.94%和21.89%。微生物来源酶催化酯化反应是浓香型白酒脂肪酸乙酯合成的主要途径[29],而关键的产酯微生物,如毕赤酵母属、葡萄球菌属和曲霉属的相对丰度在强化曲中均有显著提高(P<0.05),加之S.pombe JM2-5本身具有较强的产酯化酶能力,使得强化曲的酯化力显著高于对照曲。大曲的原料通常是优质小麦,但微生物不能直接利用小麦中的淀粉,因此需要淀粉酶和糖化酶将淀粉降解为单糖以供微生物生长代谢,液化力和糖化力就是大曲中淀粉酶和糖化酶能力强弱的体现。强化曲在糖化力方面与对照曲无显著差异。强化曲的液化力在发酵期(1.1 U)和成熟期(0.91 U)都显著高于对照曲(发酵期0.76 U,成熟期0.78 U)(P<0.05),这可能与根霉属和曲霉属在强化曲中有较高的丰度有关,根霉属和曲霉属被广泛认为是大曲中液化力和糖化力的重要来源[22],大曲糖化力和液化力表现出不同的变化,结合MetaCyc(Metabolic Pathways From all Domains of Life)数据库对大曲微生物群落的功能酶进行注释。糖化力主要涉及的关键酶主要为EC:3.2.1.3(葡萄糖淀粉酶)、EC:3.2.1.20(α-葡萄糖苷酶)以及EC:3.2.1.23(β-半乳糖苷酶)[30],液化力主要涉及的关键酶为EC:2.4.1.1(糖原磷酸化酶)、EC:3.2.1.1(α-淀粉酶)和 EC:3.2.1.2(β-淀粉酶)[31]。糖化力和液化力相关酶的相对丰度见图5,除成熟期对照曲中α-葡萄糖苷酶的相对丰度明显高于强化曲外,对照曲与强化曲中糖化力相关酶相对丰度无明显变化,因此强化曲在糖化力方面与对照曲无显著差异。而液化力相关酶中,除β-淀粉酶在发酵期的对照曲与强化曲中相对丰度相差不大外,强化曲中糖原磷酸化酶和α-淀粉酶相对丰度均明显高于对照曲。大曲中糖化力和液化力相关酶的相对丰度不同,因此对照曲与强化曲的糖化力无显著差异,而强化曲的液化力则显著高于对照曲。
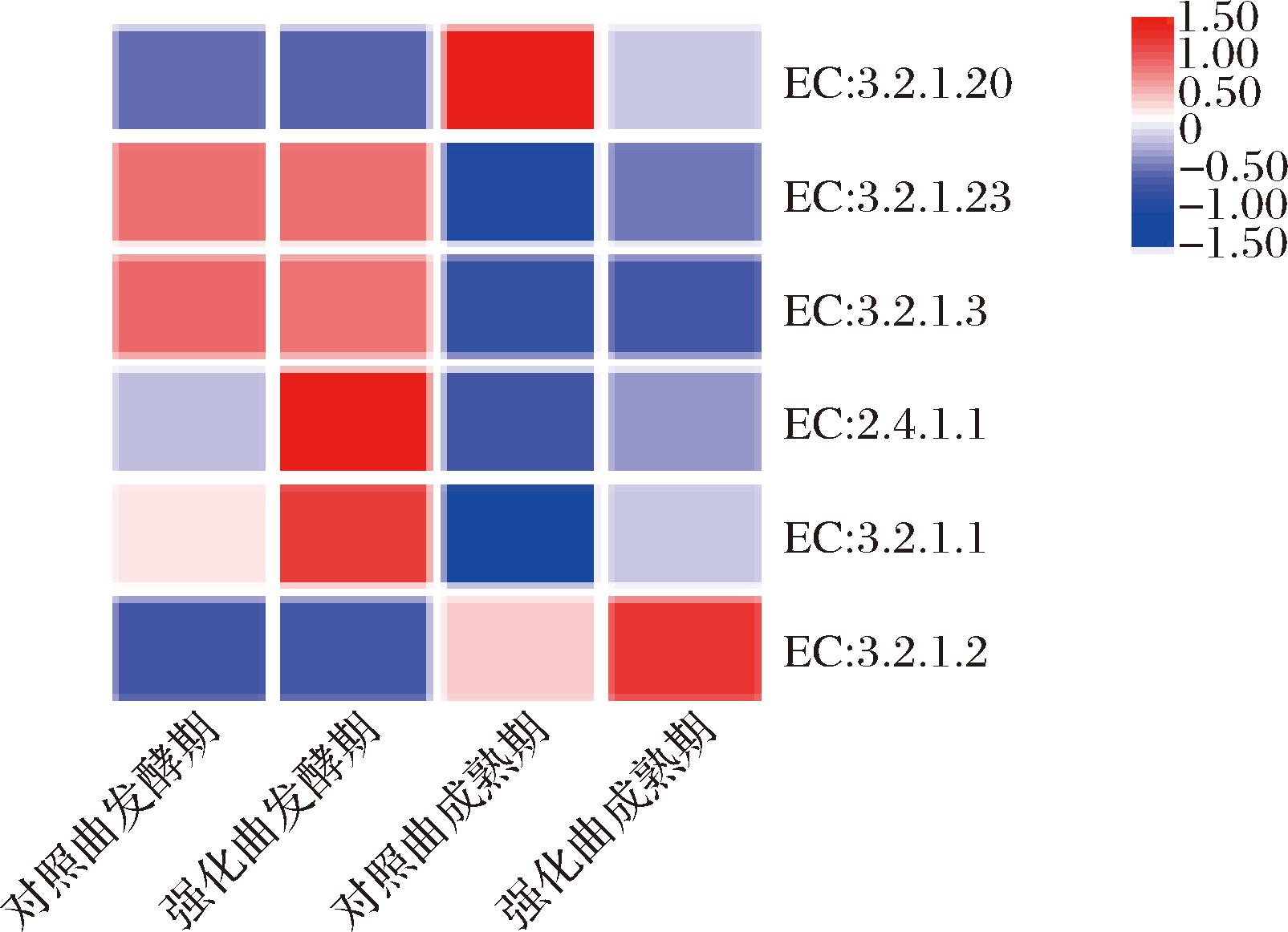
图5 糖化力和液化力相关酶相对丰度
Fig.5 Relative abundance of enzymes related to saccharifying activity and liquefying activity
强化曲和对照曲的细菌属、真菌属与大曲理化指标的冗余分析(redundancy analysis,RDA)结果见图6,经置换检验可得细菌、真菌群落与理化指标的冗余分析P值分别为0.008和0.011,均达到显著水平,表明该模型可靠[32]。大曲的发酵力和酸度与细菌属乳球菌属、高温放线菌属,真菌属嗜热真菌属呈正相关,与细菌属魏斯氏菌属和真菌属毕赤酵母属呈负相关,成熟期强化曲酸度显著低于对照曲,与其乳球菌属丰度下降相关,这与此前的报道类似[33]。强化曲中魏斯氏菌属和嗜热真菌属的相对丰度相较于对照曲分别显著上升和下降,加之成熟后强化曲水分的流失过大,影响了发酵力相关微生物的代谢,导致强化曲的发酵力显著低于对照曲。大曲酯化力和糖化力与细菌属魏斯氏菌属、粘液乳杆菌属以及嗜水果乳杆菌属(FructilactoBacillus),真菌属嗜热子囊菌属、毕赤酵母属呈正相关,与真菌属嗜热真菌属,细菌属乳球菌属和高温放线菌属呈负相关,嗜热子囊菌属可提供耐高温的纤维素酶、淀粉酶,有利于产酯微生物对大曲原料中营养物质的利用。强化曲的液化力、酯化力以及糖化力与细菌群落的相关性强于真菌群落,强化曲的酸度和发酵力对细菌群落功能的影响强于对照曲。相较于对照曲,强化曲的理化指标与大曲微生物群落相关性增强,相关的理化因子对其细菌微生物群落的组成和功能有更大的扰动作用。基于Envfit函数进行显著性检验[25],检验理化指标对微生物群落组成和功能影响是否显著,结果见表3,液化力、发酵力和酯化力与对照曲和强化曲的细菌群落的组成和功能有显著影响(r2>0.6,P<0.05),理化指标对大曲真菌群落无显著影响。
表3 强化曲理化指标差异性检验(Env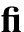 t检验)
t检验)
Table 3 EnvFit test of physicochemical indices for Daqu
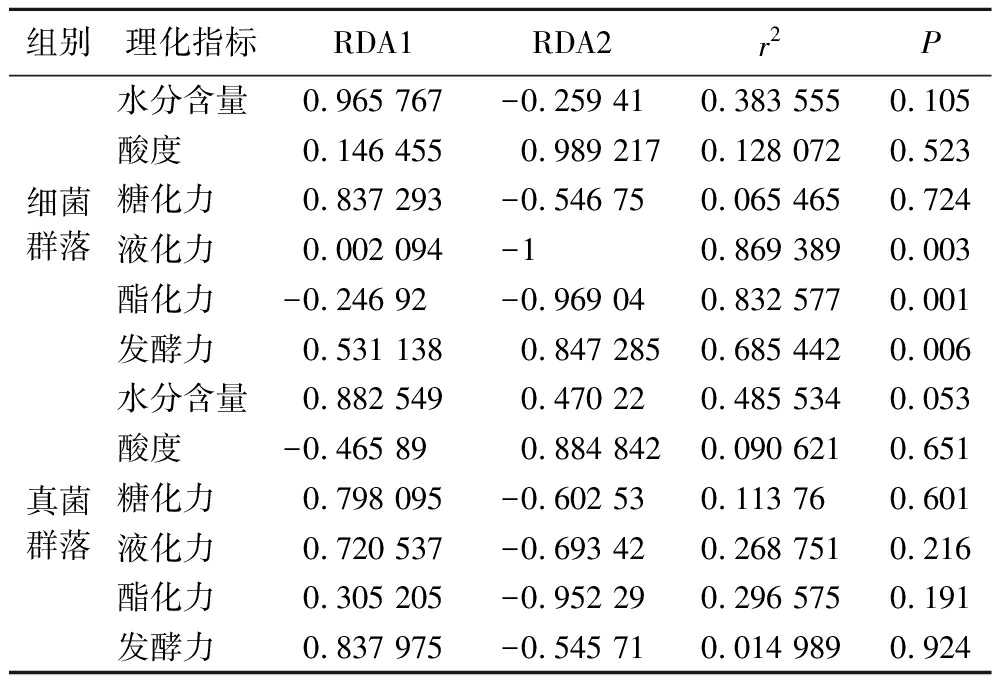
组别理化指标RDA1RDA2r2P细菌群落水分含量0.965 767-0.259 410.383 5550.105酸度0.146 4550.989 2170.128 0720.523糖化力0.837 293-0.546 750.065 4650.724液化力0.002 094-10.869 3890.003酯化力-0.246 92-0.969 040.832 5770.001发酵力0.531 1380.847 2850.685 4420.006真菌群落水分含量0.882 549 0.470 220.485 5340.053酸度-0.465 890.884 8420.090 6210.651糖化力0.798 095-0.602 530.113 760.601液化力0.720 537-0.693 420.268 7510.216酯化力0.305 205-0.952 290.296 5750.191发酵力0.837 975-0.545 710.014 9890.924
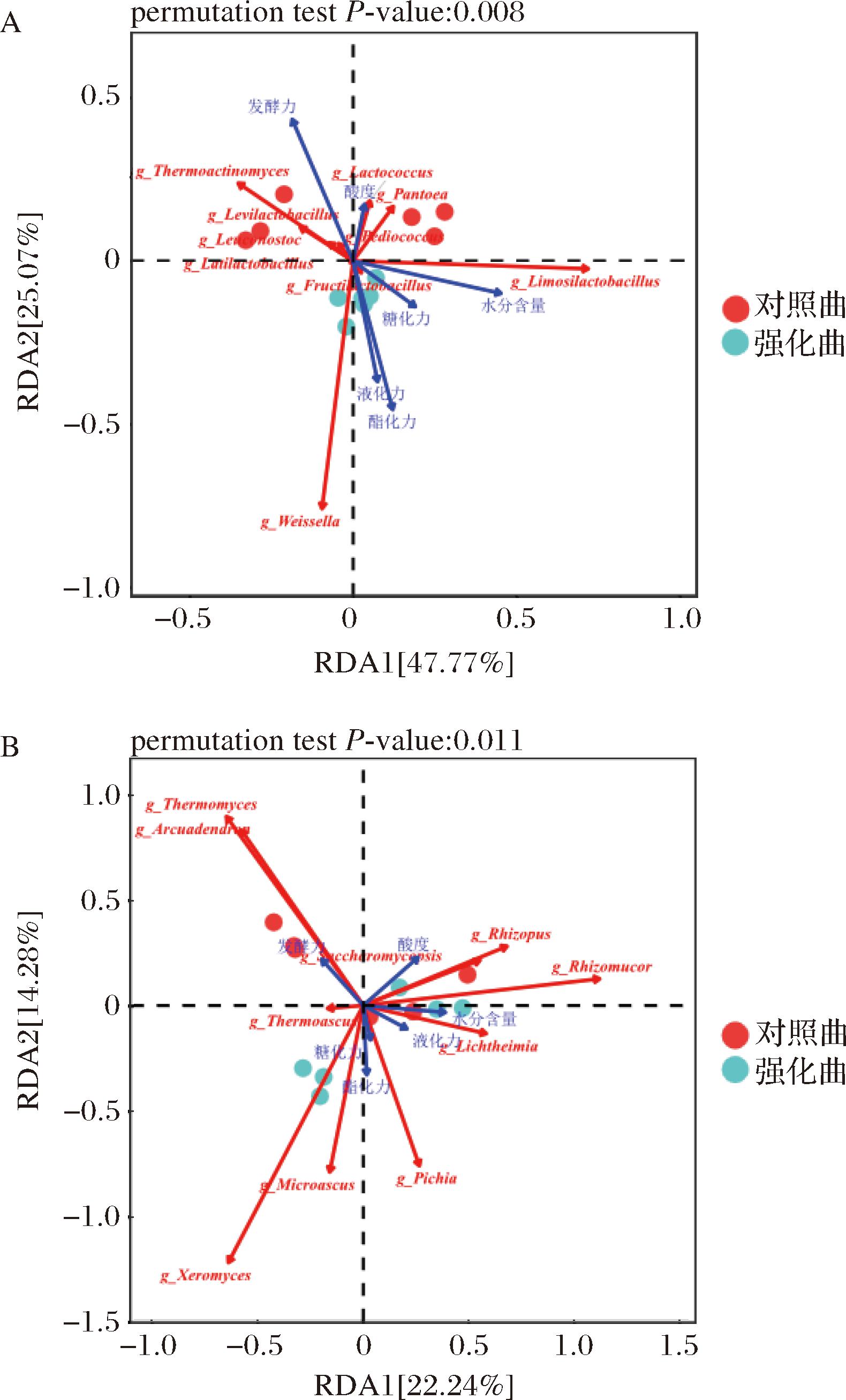
A-细菌属;B-真菌属
图6 大曲微生物群落与理化指标的冗余分析
Fig.6 The redundancy analysis of between microbial communities and physicochemical indexes
2.6 大曲风味物质
大曲风味物质是白酒酒体香气物质的重要组成部分,也是白酒风味前体物质的关键来源[34]。采用 HS-SPME-GC-MS在2种大曲中共计检测到81种风味物质(对照曲59种,强化曲67种),其中吡嗪类9种(对照曲6种,强化曲8种)、醇类19种(对照曲18种,强化曲16种)、芳香族类9种(对照曲7种,强化曲4种)、醛酮类14种(对照曲11种,强化曲12种)、酸类8种(对照曲5种,强化曲7种)、酯类21种(对照曲12种,强化曲18种)。其风味物质含量及各类物质含量见图7,对照曲发酵期和成熟期风味物质总量分别为1 719.1 μg/kg和1 806.49 μg/kg,强化曲发酵期和成熟期风味物质总量分别为2 645.57 μg/kg和2 671.74 μg/kg,强化曲风味物质总量全时期均显著高于对照曲(P<0.05),分别显著提高了53.89%和47.90%。所有大曲成熟后风味物质总量均有一定程度提升,对照曲提升了5.08%,强化曲提升了0.99%。醇类物质在强化曲和对照曲中占比最大,占比均超过40%,发酵期和成熟期强化曲中酯类物质总量(发酵期480.96 μg/kg,成熟期547.74 μg/kg)均显著高于对照曲(发酵期173.72 μg/kg,成熟期293.50 μg/kg)(P<0.05),这与强化曲中产酯微生物丰度的升高和酯化力的提升相符。强化曲除芳香族类风味物质含量低于对照曲,其他风味物质含量均高于对照曲。
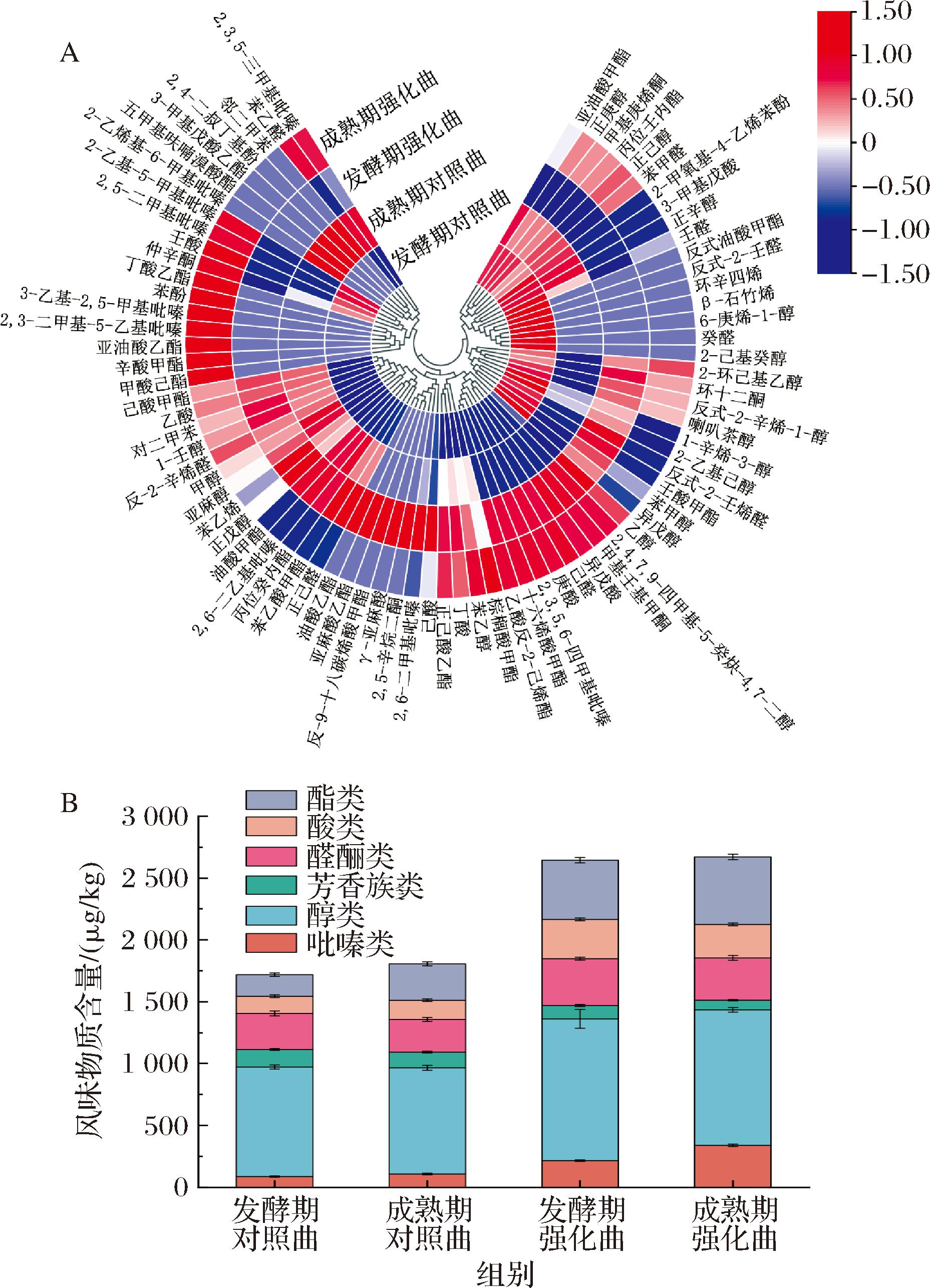
A-各风味物质含量;B-各类风味物质含量
图7 大曲风味物质总量
Fig.7 Total flavor compounds in Daqu
正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis, OPLS-DA)和200次置换验证分析结果见图8。经200次置换验证,置换验证模型中R2Y截距为0.211(图8-A),未超过0.3~0.4,且Q2Y截距为-0.620<0,表明该OPLS-DA模型可靠,不存在过度拟合[35]。由OPLS-DA结果可得(图8-B),对照曲各样本与强化曲各样本距离较远,表明两者的风味物质组成有显著不同(P<0.05)。此外,对照曲发酵期与成熟期的风味物质组成也存在明显不同,而强化曲发酵期与成熟期风味物质组成较为相似,推测可能是S.pombe JM2-5强化使得大曲风味物质组成在发酵结束时就趋于稳定,贮存没有改变其风味物质组成。
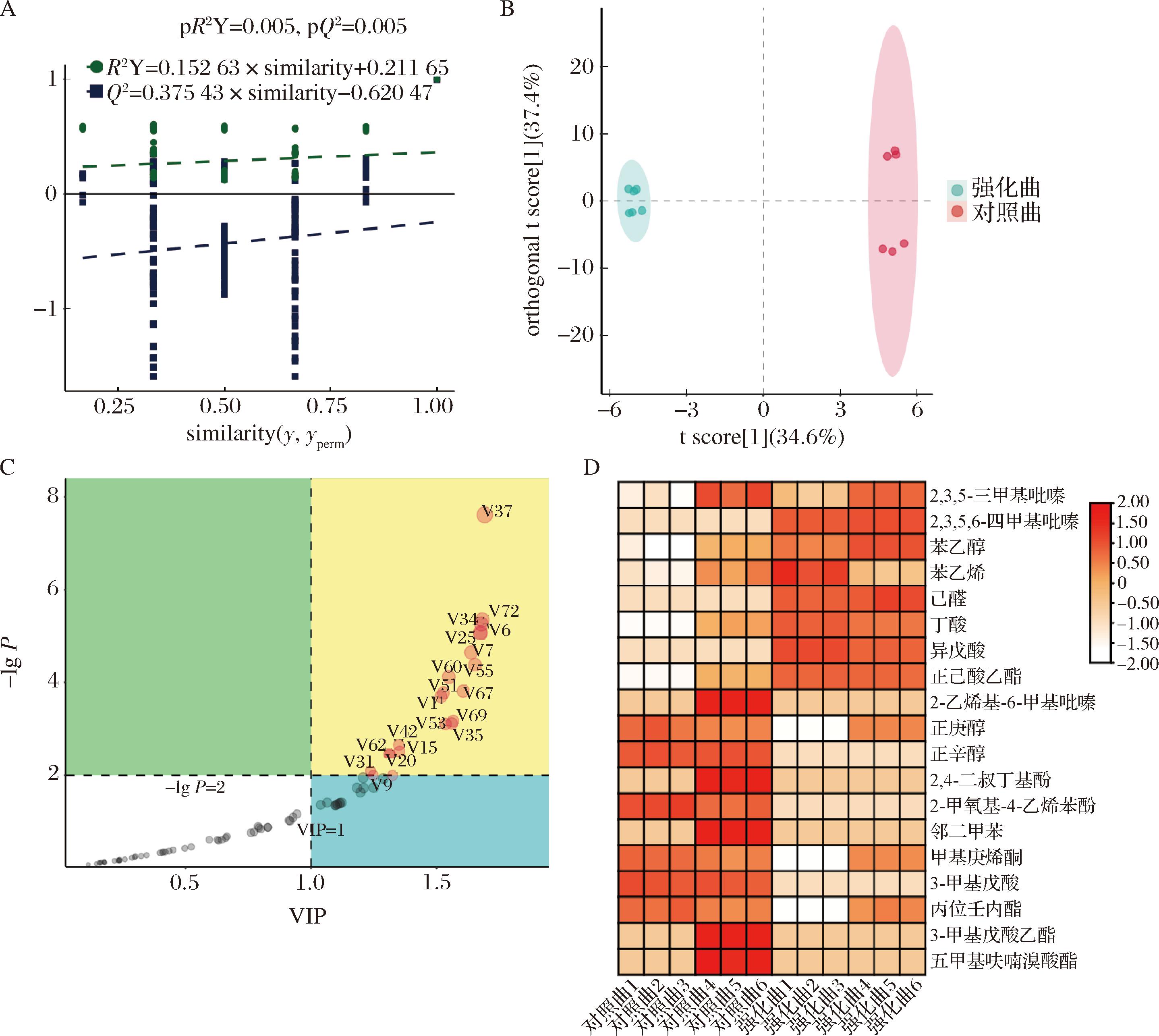
A-OPLS-DA模型;B-200次置换检验模型;C-差异风味物质筛选结果;D-差异风味物质含量热图
图8 大曲风味物质分析
Fig.8 Analysis of flavor compounds in Daqu
根据变异权重参数(variable importance in projection, VIP)值(VIP>1且P≤0.01)筛选特征差异风味物质[36],共计获得19种风味物质(图8-C),其中包括苯乙醇、己酸乙酯、四甲基吡嗪以及丁酸在内的8种风味物质含量显著提高。差异风味物质含量热图见图8-D,差异风味物质主要集中在吡嗪类、醇类和酯类物质,其中的四甲基吡嗪是白酒中重要的风味物质[37],也是白酒中的健康因子,其在对照曲中未检出,在强化曲中的含量为136.92 μg/kg,此前有报道栗酒裂殖酵母可以促进2,3-丁二醇的生成从而提高四甲基吡嗪的含量[38]。己酸乙酯是浓香型白酒的主体风味物质,是评价浓香型白酒品质的重要指标,己酸乙酯主要是由发酵过程中的己酸和乙醇在酯化酶作用下生成的,经S.pombe JM2-5强化后,己酸乙酯的含量由12.72 μg/kg提升至134.83 μg/kg。强化曲中的酯类物质种类和总含量较对照曲都有较强提升,与前文提及的大曲产酯微生物丰度提升以及酯化力的提高相符。此外,强化曲中苯乙醇的含量相较于对照曲也有显著提高,由104.63 μg/kg提升至409.57 μg/kg,苯乙醇具有玫瑰香气[39],是多种白酒的特征风味物,毕赤酵母属是白酒中苯乙醇的主要生产菌属[40]。此外,乙醇脱氢酶是苯乙醇合成的关键酶,而魏斯氏菌属、粘液乳杆菌属、根霉属被认为是大曲中乙醇脱氢酶的重要来源[41],故强化曲中的苯乙醇含量有了大幅提升。强化曲中正庚醇、正辛醇等其他高级醇含量有所下降,由271.62 μg/kg下降至179.00 μg/kg,可能是产酯酶酵母的接入使得微生物群落的代谢途径发生变化,促使高级醇向其他风味物质的转化。
3 结论
将产酯酶酵母S.pombe JM2-5应用于强化大曲生产,通过对强化曲和对照曲微生物群落组成、大曲理化指标以及风味物质的测定分析,发现菌株S.pombe JM2-5的接入提高了大曲成熟期真菌群落的物种多样性和微生物群落的物种丰度,与酯化力、液化力相关的魏斯氏菌属、毕赤酵母属、根霉属等相关微生物相对丰度均有不同程度的提升,且毕赤酵母属和克罗彭斯特德菌属的介数中心性有大幅提高,使得强化曲的酯化力和液化力有显著提高,酸度显著下降。同时,强化曲的风味物质总量有显著提升,苯乙醇、己酸乙酯及四甲基吡嗪等8种与白酒特征风味相关的风味物质含量显著升高。结果表明,菌株S.pombe JM2-5可以改善大曲微生物群落结构、酶活力以及风味物质,具有作为功能微生物进行大规模强化发酵的潜力。
[1] JIN G Y, ZHU Y, XU Y.Mystery behind Chinese liquor fermentation[J].Trends in Food Science &Technology, 2017, 63:18-28.
[2] ZHENG X W, HAN B Z.Baijiu (白酒), Chinese liquor:History, classification and manufacture[J].Journal of Ethnic Foods, 2016, 3(1):19-25.
[3] 杨阳, 魏阳, 刘晓彤, 等.基于白酒发酵过程多组学数据挖掘大曲淀粉糖化酶及其协同应用效果解析[J].生物工程学报, 2025, 41(5):2101-2118.YANG Y, WEI Y, LIU X T, et al.Mining of starch-saccharifying enzymes in Daqu from multi-omics data of the Baijiu fermentation process and analysis of their synergistic effects in application[J].Chinese Journal of Biotechnology, 2025, 41(5):2101-2118.
[4] HE G Q, HUANG J, WU C D, et al.Bioturbation effect of fortified Daqu on microbial community and flavor metabolite in Chinese strong-flavor liquor brewing microecosystem[J].Food Research International, 2020, 129:108851.
[5] OWUSU-KWARTENG J, TANO-DEBRAH K, AKABANDA F, et al.Technological properties and probiotic potential of Lactobacillus fermentum strains isolated from West African fermented millet dough[J].BMC Microbiology, 2015, 15(1):261.
[6] LI W W, FAN G S, FU Z L, et al.Effects of fortification of Daqu with various yeasts on microbial community structure and flavor metabolism[J].Food Research International, 2020, 129:108837.
[7] 孙思佳, 翟磊, 于学健, 等.扣囊复膜孢酵母CICC 33077对芝麻香白酒高温大曲微生物群落结构和功能特性的影响[J].食品与发酵工业, 2023, 49(7):99-105.SUN S J, ZHAI L, YU X J, et al.Influences of Saccharomycopsis fibuligera CICC 33077 on microbial community and functional characteristics of high temperature Daqu in sesame flavor Baijiu[J].Food and Fermentation Industries, 2023, 49(7):99-105.
[8] FAN G S, TENG C, XU D, et al.Improving ethyl acetate production in Baijiu manufacture by Wickerhamomyces anomalus and Saccharomyces cerevisiae mixed culture fermentations[J].BioMed Research International, 2019, 2019:1470543.
[9] 陈聪, 邹伟, 汤秀娟, 等.产酯酶格氏乳球菌的筛选、鉴定与基因组注释[J].食品科学, 2024, 45(8):87-95.CHEN C, ZOU W, TANG X J, et al.Screening, identification and genome annotation of esterase-producing Lactococcus garvieae[J].Food Science, 2024, 45(8):87-95.
[10] WEAR E K, WILBANKS E G, NELSON C E, et al.Primer selection impacts specific population abundances but not community dynamics in a monthly time-series 16S rRNA gene amplicon analysis of coastal marine bacterioplankton[J].Environmental Microbiology, 2018, 20(8):2709-2726.
[11] 侯强川, 王文航, 徐媛媛, 等.徐坊中高温大曲发酵过程中理化品质、风味及真菌群落结构变化规律研究[J].食品工业科技, 2024, 45(19):133-141.HOU Q C, WANG W H,XU Y Y, et al.Dynamic changes of physicochemical quality, flavor and fungal community structure during medium-high temperature daqu fermentation process in xufang region[J].Science and Technology of Food Industry, 2024, 45(19):133-141.
[12] XU B Y, XU S S, CAI J, et al.Analysis of the microbial community and the metabolic profile in medium-temperature Daqu after inoculation with Bacillus licheniformis and Bacillus velezensis[J].LWT, 2022, 160:113214.
[13] ZHU C T, CHENG Y X, SHI Q L, et al.Metagenomic analyses reveal microbial communities and functional differences between Daqu from seven provinces[J].Food Research International, 2023, 172:113076.
[14] HUANG X, LIU J, LUO H B, et al.Research progress on the diversity, physiological and functional characteristics of lactic acid bacteria in the Nongxiangxing Baijiu microbiome[J].Journal of Food Science, 2025, 90(2):e70082.
[15] 刘文虎, 刘光钱, 张芮, 等.基于宏基因组解析中温大曲成熟前后的微生物群落功能差异[J].生物工程学报, 2024, 40(3):877-894.LIU W H, LIU G Q, ZHANG R, et al.Metagenomics unveils the differences in the functions of microbial community of medium-temperature Daqu before and after maturation[J] Chinese Journal of Biotechnology, 2024,40(3):877-894.
[16] XU L,DU R B,WU Q, et al.Species-level distribution of microbiota with secondary metabolic potential in Chinese Baijiu fermentation[J].Food Bioscience, 2024,59:104231.
[17] CHEN C, YANG H Q, LIU J, et al.Systematic review of actinomycetes in the Baijiu fermentation microbiome[J].Foods,2022,11(22):3551.
[18] 田浩杰, 李豆南, 邱树毅, 等.酱香大曲中高温放线菌的筛选及基因组解析[J].食品科学, 2023, 44(18):68-76.TIAN H J, LI D N, QIU S Y, et al.Identification and genome analysis of Laceyella sacchari FBKL4.014 isolated from Moutai-flavor Daqu[J] Food Science, 2023,44(18):68-76.
[19] PORTO M C W, KUNIYOSHI T M, AZEVEDO P O S, et al.Pediococcus spp.:An important genus of lactic acid bacteria and pediocin producers[J].Biotechnology Advances, 2017, 35(3):361-374.
[20] 唐艺婧, 来欢欢, 赵微, 等.红心曲来源Thermoascus aurantiacus QH-1的生长代谢特征[J].食品工业科技, 2023, 44(22):117-124.TANG Y J, LAI H H, ZHAO W, et al.Characteristics of growth and metabolism of Thermoascus aurantiacus QH-1 derived Hongxinqu[J].Science and Technology of Food Industry, 2023, 44(22):117-124.
[21] JIANG J,LIU Y C,LI H H,et al.Modeling and regulation of higher alcohol production through the combined effects of the C/N ratio and microbial interaction[J].Journal of Agricultural and Food Chemistry,2019,67(38):10694-10701.
[22] 刘文虎, 柴丽娟, 张立强, 等.基于宏基因组学解析不同质量等级中温大曲微生物组的异质性[J].微生物学报, 2023, 63(11):4383-4398.LIU W H, CHAI L J, ZHANG L Q, et al.Metagenomics unveils the microbiome heterogeneity of medium-temperature Daqu with different quality grades[J].Acta Microbiologica Sinica, 2023, 63(11):4383-4398.
[23] 何猛超, 邬子璇, 西玉玲, 等.通过外源添加芽孢杆菌提升北方地区高温大曲的品质[J].食品工业科技, 2024, 45(1):145-154.HE M C, WU Z X, XI Y L, et al.Enhancing the quality of high-temperature Daqu in northern China by adding exogenous Bacillus spores[J].Science and Technology of Food Industry, 2024, 45(1):145-154.
[24] MARCELIN R A,RABARISON K M,RABARISON M K.Co-authorship network analysis of prevention research centers:An exploratory study[J].Public Health Reports,2019,134(3):249-254.
[25] 彭远凤, 杨阳, 赵东, 等.东方伊萨酵母对浓香型白酒酒醅微生物群落结构及挥发性风味物质合成的影响[J].食品科学, 2024, 45(16):97-104.PENG Y F, YANG Y, ZHAO D, et al.Effect of Issatchenkia orientalis on the microbial community structure and volatile flavor substance synthesis in Nongxiangxing Baijiu Jiupei(fermented grains)[J].Food Science, 2024,45(16):97-104.
[26] 徐锦, 冯文聪, 朱澳迪, 等.不同香型大曲微生态结构及其发酵特性相关性分析[J].食品科学, 2024, 45(13):104-114.XU J, FENG W C, ZHU A D.et al.Correlation analysis between microecological structure and fermentation characteristics of different aroma types of Daqu[J].Food Science, 2024,45(13):104-114.
[27] YAN Z,ZHENG X W,CHEN J Y,et al.Effect of different Bacillus strains on the profile of organic acids in a liquid culture of Daqu[J].Journal of the Institute of Brewing,2013,119(1-2):78-83.
[28] 张柱, 黄钧, 周荣清, 等.红曲霉对高温大曲的扰动及制曲工艺探究[J].食品与发酵工业, 2025, 51(2):275-284.ZHANG Z, HUANG J, ZHOU R Q, et al.Exploration of Monascus disturbance on high-temperature Daqu and their manufacturing process[J].Food and Fermentation Industries, 2025,51(2):275-284.
[29] 赵静溶, 徐友强, 朱华, 等.浓香型白酒风味乙酯微生物合成机制研究进展[J].食品与生物技术学报, 2022, 41(10):1-16.ZHAO J R, XU Y Q, ZHU H, et al.Research progress on microbial synthetic mechanism of flavor ethyl esters in strong-flavor Baijiu[J].Journal of Food Science and Biotechnology, 2022, 41(10):1-16.
[30] ZHANG Y T, DENG Y K, ZOU Y F, et al.Linking microbial functional gene abundance and Daqu extracellular enzyme activity:Implications for carbon metabolism during fermentation[J].Foods, 2022, 11(22):3623.
[31] WANG B W, WU Q, XU Y, et al.Specific volumetric weight-driven shift in microbiota compositions with saccharifying activity change in starter for Chinese Baijiu fermentation[J].Frontiers in Microbiology, 2018, 9:2349.
[32] 陈绍依, 郎莹, 邱树毅, 等.茅台镇不同区域酱香大曲微生物群落结构及生产性能对比[J].食品科学, 2023,44(14):134-143.CHEN S Y, LANG Y, QIU S Y, et al.Comparative studies on microbial community structure and production performance of jiang-flavor Daqu in different areas of Maotai Town[J].Food Science, 2023,44(14):134-143.
[33] 赵秋伟, 潘越, 王松涛, 等.浓香型白酒酿造中乳酸菌的功能及相关研究进展[J].微生物学报, 2025, 65(3):871-882.ZHAO Q W, PAN Y, WANG S T, et al.Research progress in the functions of lactic acid bacteria in the brewing of strong-flavor Baijiu[J].Acta Microbiologica Sinica, 2025,65(3):871-882.
[34] 蒋力力, 田露琴, 尚煜豪, 等.不同种类高温大曲功能特性与成分差异比较[J].食品工业科技, 2025, 46(14):362-370.JIANG L L, TIAN L Q, SHANG Y H, et al.Comparison of functional characteristics and compositional differences of different high-temperature Daqu[J].Science and Technology of Food Industry, 2025, 46(14):362-370.
[35] GAO Y Y, ZHANG G X, JIANG S Y, et al.Wekemo Bioincloud:A user-friendly platform for meta-omics data analyses[J].IMeta,2024,3(1):e175.
[36] 吴双全, 柴丽娟, 黄廷财, 等.酱香型白酒堆积酒醅中象牙色克罗彭斯特德菌的分离筛选及其代谢特性解析[J].微生物学报, 2024, 64(7):2502-2521.WU S Q, CHAI L J, HUANG T C, et al.Isolation, screening, and metabolic characterization of Kroppenstedtia eburnea from the fermented grains of Jiang-flavor Baijiu[J].Acta Microbiologica Sinica, 2024,64(7):2502-2521.
[37] 张颖, 李霄霄, 李景辉, 等.高产四甲基吡嗪芽孢杆菌的筛选及其对酱香型白酒堆积过程的影响[J].食品工业科技, 2022, 43(2):142-149.ZHANG Y, LI X X, LI J H, et al.Screening of high-yielding tetramethylpyrazine Bacillus and its effect on the accumulation process of Maotai-flavor liquor[J].Science and Technology of Food Industry, 2022, 43(2):142-149.
[38] 慕济锗. 耐酸粟酒裂殖酵母在酱香型白酒酿造中的应用 [D].天津:天津科技大学, 2023.MU J Z.Application of Acid-Resistant Schizosaccharomyces pombe in the brewing of Maotai-Flavor liquor [D].TianJin:Tianjin University of Science and Technology,2023.
[39] 张学林, 季斌, 许玲, 等.清香型大曲中产β-苯乙醇酵母的分离、鉴定及在白酒酿造中的应用[J].中国酿造, 2022, 41(1):123-127.ZHANG X L, JI B, XU L, et al.Isolation and identification of β-phenylethanol-producing yeast from light-flavor Daqu and its application in Baijiu brewing[J] China Brewing, 2022, 41(1):123-127.
[40] CHREPTOWICZ K,STERNICKA M K,KOWALSKA P D,et al.Screening of yeasts for the production of 2-phenylethanol (rose aroma) in organic waste-based media[J].Letters in Applied Microbiology,2018,66(2):153-160.
[41] LIU W H,CHAI L J,WANG H M,et al.Community-level bioaugmentation results in enzymatic activity-and aroma-enhanced Daqu through altering microbial community structure and metabolic function[J].Food Bioscience,2024,57:103630.