在葡萄酒酿造过程中,酵母菌扮演着至关重要的核心角色[1]。长期以来,利用酿酒酵母(Saccharomyces cerevisiae)进行纯种发酵已成为现代葡萄酒工业的主流模式,该工艺显著提高了发酵效率与过程可控性,保障了产品质量的稳定性。然而,其弊端也逐渐显现,尤其表现为葡萄酒风味的同质化,在一定程度上削弱了不同产区与品种所特有的风格多样性[2]。近年来,越来越多的研究关注非酿酒酵母在混合发酵中的应用潜力。本土非酿酒酵母与酿酒酵母协同发酵,可显著影响葡萄酒的最终感官特征,不仅能够增强特定香气成分,还有助于提升风味的复杂度[3]。如ZHANG等[4]采用S. cerevisiae与葡萄园有孢汉逊酵母及美极梅奇酵母进行同时和顺序发酵葡萄酒,发现混合发酵相较于单菌株发酵显著提升了葡萄酒的香气品质。许多非酿酒酵母菌株能够分泌葡萄糖苷酶,水解糖苷前体释放出挥发性化合物,包括酯类、高级醇、乙醛、有机酸、挥发性脂肪酸、羰基化合物及萜类等,从而丰富葡萄酒的香气层次[5]。因此,系统研究本土非酿酒酵母与酿酒酵母的混合发酵对葡萄酒风味品质的影响,不仅有助于挖掘和利用本土微生物资源,也为酿造具有产区特色与典型风格的高品质葡萄酒提供了可行路径。
新疆天山北麓产区位于欧亚大陆中心地带,该地区降水较少而日照充足,此类气候条件显著促进了葡萄果实风味成分的合成与积累[6]。然而,随着全球气候变暖的加剧,该产区葡萄成熟度不断提高,致使酿酒葡萄中的糖分积累显著增加,最终导致葡萄酒酒精含量升高[7]。过高的酒精浓度不仅可能掩盖其他精细风味的表达,破坏酒体的平衡性与复杂性,还会引发消费者对健康风险的关注[8]。因此,葡萄酒产业对能够在保持产品品质的前提下有效降低酒精含量的技术需求日益迫切[9]。非酿酒酵母因其在发酵过程中能够降低乙醇产量的特性而受到广泛关注[10]。相较于传统的酿酒酵母纯种发酵,某些非酿酒酵母不仅能够代谢产生更少的乙醇,还可合成更多样化的挥发性香气化合物及有益的多酚类物质,从而在实现降醇的同时提升葡萄酒的香气复杂性与营养品质[11]。其中,葡萄汁有孢汉逊酵母(Hanseniaspora uvarum)作为葡萄果皮上早期出现且丰度较高的本土非酿酒酵母,因其独特的代谢特性成为研究热点。该菌种与酿酒酵母的共培养或混合发酵体系,已被证实能够有效降低发酵液的酸度和最终乙醇体积分数,并显著提高酯类、高级醇、萜烯醇等关键香气物质的产量[12-13]。尽管混合发酵策略在降醇和增香方面展现出良好前景,然而针对新疆天山北麓这一独特风土条件下本土H. uvarum菌株在‘马瑟兰(Marselan)’葡萄酒酿造中的应用效果,目前尚未有系统研究,其潜能尚待深入挖掘。
基于此,本文以新疆天山北麓产区‘马瑟兰’葡萄为原料,研究本土分离的H. uvarum菌株与S. cerevisiae单独接种、同时接种和顺序接种发酵对葡萄酒基本理化指标、乙醇产量和挥发性风味物质的影响,并进行感官品评,以期为本土H. uvarum改善‘马瑟兰’干红葡萄酒风味品质提供理论依据。
1 材料与方法
1.1 材料与试剂
葡萄原料:‘马瑟兰’于2024年9月29日采收自新疆天山北麓产区新疆农垦科学院葡萄种植基地,还原糖含量258 g/L,可滴定酸(以酒石酸计)含量5.5 g/L。
商业酿酒酵母(S.cerevisiae,FX10),购自法国LAFFORT公司。
葡萄汁有孢汉逊酵母(H.uvarum,NK2),由新疆农垦科学院农产品加工重点实验室从天山北麓产区分离并保藏,并经26S rDNA(D1/D2)鉴定(同源性达到99%)。
YPD培养基,青岛高科园海博生物技术有限公司;2-辛醇(色谱纯),美国Sigma公司;其他试剂为国产分析纯。
1.2 仪器与设备
SPX-150B 生化培养箱,上海琅玕实验设备有限公司;PEGASUS HRT 4D plus全二维气相色谱-高分辨飞行时间质谱联用仪,美国LECO公司;LT-CPS50D立式压力蒸汽灭菌器,上海立德泰勀科学仪器有限公司;SW-CJ-1C 超净工作台;上海川昱实验仪器有限公司。
1.3 实验方法
1.3.1 酵母活化培养
将商业酿酒酵母干粉于37 ℃温水中活化15 min,将保藏菌株解冻后于YPD固体平板上涂布,26 ℃下静置培养24 h后重复活化一次,取形态良好的单菌落于YPD液体培养基中,于28 ℃、120 r/min条件下扩增培养至对数生长期,将培养液在5 000 r/min离心5 min后收集酵母细胞,并经无菌水洗涤后对酵母进行计数,将菌悬液浓度调整为1×108 CFU/mL(显微镜观察)用于后续发酵。
1.3.2 实验处理
纯种发酵:只接种单一的S.cerevisiae(Sc组)和H.uvarum(Hu组)。
混菌发酵:参照尤雅等[14]的方法设置同时接种与顺序接种处理。H.uvarum与S.cerevisiae按1∶1的比例同时接种进混菌发酵(Sc+Hu组);H.uvarum与S.cerevisiae以10∶1进行顺序接种发酵(Hu-Sc组)。其中S.cerevisiae接种量为1×106 CFU/mL;H.uvarum接种量为1×107 CFU/mL;同时接种指同时加入S.cerevisiae与H.uvarum进行酒精发酵;顺序接种指先加入H.uvarum,48 h后加入S.cerevisiae进行酒精发酵。
1.3.3 葡萄酒酿造工艺
酿造工艺如下:
马瑟兰葡萄→穗选与粒选→除梗破碎→入罐(添加果胶酶、SO2)→冷浸渍(8 ℃/24 h)→接种酵母→酒精发酵(25 ℃)→发酵结束→皮渣分离、调硫→苹果酸-乳酸发酵→稳定澄清→装瓶
各发酵处理均采用20 L发酵罐进行小规模酿造,每罐葡萄醪液入罐量为16 L,且每个处理组设置3个生物学重复。
1.3.4 酵母菌数量测定
发酵过程中每隔48 h取样,使用WL营养琼脂(Wallerstein laboratory nutrient agar,WL)培养基进行平板菌落计数。依据菌落形态学特征区分2种目标酵母菌株,分别统计其菌落形成单位(CFU)数量。每个稀释梯度设置3个平行重复。
1.3.5 发酵动力学监测
发酵过程每隔48 h取样测定葡萄酒中还原糖含量和酒精度变化。
1.3.6 发酵主产物分析
参照GB/T 15038—2006《葡萄酒、果酒通用分析方法》测定残糖、乙醇、总酸和挥发酸含量;甘油含量采用Elabscience甘油试剂盒测定。并参考文献[15]计算乙醇产量和乙醇产率,分别如公式(1)和(2)所示:
乙醇产量/(g/L)=乙醇体积分数(%)×10×乙醇密度(kg/L)
(1)
乙醇产率![]()
(2)
1.3.7 香气物质的测定
采用全二维气相-高通量高分辨质谱联用仪(comprehensive two-dimensional gas chromatography-time-of-flight mass spectrometer,GC×GC-TOF-MS)对葡萄酒样品中的挥发性香气成分进行分析。
准确量取5 mL酒样,添加20 μL内标物溶液(2-辛醇,5 mg/L)于20 mL顶空瓶中。采用50/30 um CARPDMS/DVB萃取头于50 ℃吸附30 min,然后在250 ℃进样口解吸3 min,并启动色谱-质谱系统采集数据。气相色谱升温程序为:初始温度40 ℃保持3 min,以10 ℃/min升至230 ℃,保持6 min。载气为氦气,流速1.0 mL/min。质谱采用电子电离源(EI),电子能量70 eV,接口温度250 ℃,离子源温度200 ℃。质谱数据经NIST 14和Wiley谱库检索,并结合C6~C26正构烷烃系列标准品在相同条件下的数值计算保留指数(retention index, RI)。化合物鉴定需满足匹配度大于700,且RI值与数据库标准值的差异在±50范围内。挥发性化合物定量分析采用内标法,依据结构相似性和相对分子质量相近原则,按公式(3)计算其浓度:
(3)
式中:Cm,某一挥发性化合物的质量浓度,μg/L;Am,某一香气物质的峰面积;Cn,内标物的质量浓度,μg/L;An,内标物的峰面积。
1.3.8 感官分析
感官评价参照GB/T 15038—2006《葡萄酒、果酒通用分析方法(含第1号修改单)》并借鉴周得刚等[16]的方法进行。品评小组由11名经专业训练的成员(6名男性,5名女性)组成,在空气流通、无干扰气味的标准品酒室内独立完成品评。所有样品均经随机编码,并以随机顺序呈递进行盲品。感官评价涵盖外观(色泽、澄清度)、香气(花香、果香、植物与矿物气味、动物性气味)和口感(酸度、收敛性、余味、平衡感)3个维度共计10项属性;其中收敛性指葡萄酒中多酚类物质引起的口腔干涩与紧缩感;余味指酒液吞咽后风味在口腔中的持久性;平衡感指酒体中酸度、甜度、单宁与酒精之间的协调程度。各项指标采用0~9分标度评分(1分:极低;5分:中等;9分:极高)。每个样品在每一感官属性上的最终得分为全部11位品评员所给分数的平均值。
1.4 数据处理分析
通过Excel进行数据统计,利用SPSS 26.0对数据进行单因素方差分析(ANOVA),并采用Duncan’s多重比较检验,差异显著性水平为P<0.05;应用R语言和Simca 14.1软件绘图。
2 结果与分析
2.1 酵母菌生长变化分析
各菌株在WL培养基上的菌落形态如图1所示,S.cerevisiae的菌落为奶油色(浅黄色),光滑油状,边缘整齐,不透明的球形突起菌株;H.uvarum为深绿色油状菌株,有球形凸起,表面光滑不透明,呈扁平状。因此,可根据S.cerevisiae和H.uvarum的菌落形态特征差异区分酵母种类,并进行菌落计数来监测不同菌株数量的变化。
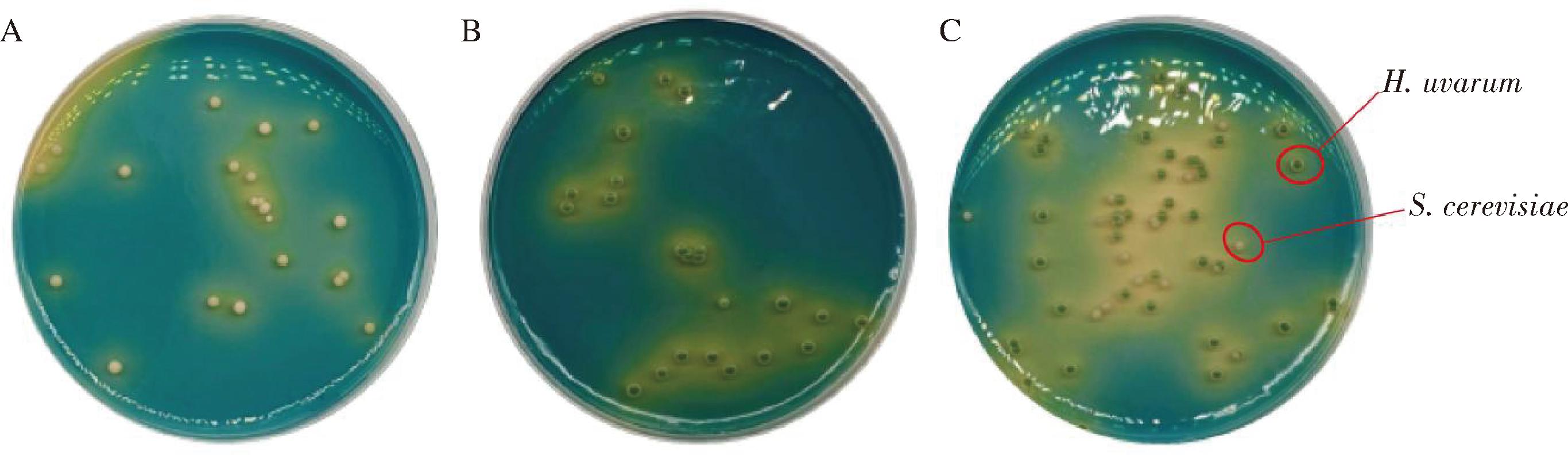
A-S.cerevisiae;B-H.uvarum;C-S.cerevisiae和H.uvarum在WL培养基上的形态
图1 WL平板鉴定S.cerevisiae和H.uvarum结果
Fig.1 Differentiation of S.cerevisiae and H.uvarum on WL nutrient agar
不同接种方式下酵母细胞的生长动态如图2所示。在单独接种发酵中(图2-A),S.cerevisiae的生物量在发酵过程中呈现先升高后降低的趋势,在第6天达到峰值(2.0×108 CFU/mL),至第16天仍维持在较高水平(4.0×107 CFU/mL);而H.uvarum的细胞数量于第4天达到最高值(1.4×108 CFU/mL),随后逐渐下降。在同时接种发酵模式下(图2-B),S.cerevisiae的细胞数量在第8天达到最大数量(1.6×108 CFU/mL),H.uvarum则于第2天即达到细胞数量峰值(6.3×107 CFU/mL),表明其较纯种发酵更快达到最大生物量,但随后其细胞密度随酒精发酵进程迅速降低。在顺序接种发酵中(图2-C),S.cerevisiae于第10天达到最大细胞密度,其生长趋势与同时接种模式无明显差异;H.uvarum于第4天达到细胞数量最高值。值得注意的是,尽管顺序接种中H.uvarum的初始接种量为S.cerevisiae的10倍,但在发酵后期,H.uvarum的细胞数量显著低于S.cerevisiae。
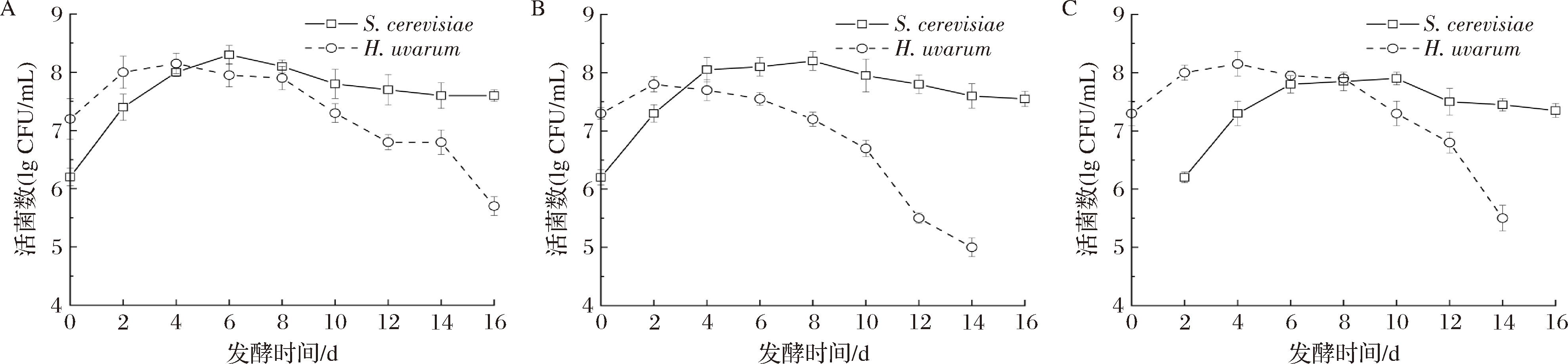
A-单独接种;B-同时接种;C-顺序接种
图2 不同接种方式下H.uvarum与S.cerevisiae活菌数量变化
Fig.2 Changes in the number of live cells of H.uvarum and S.cerevisiae under different inoculation methods
2.2 发酵动力学分析
不同接种方式发酵过程中还原糖和酒精度的变化如图3所示。Sc、Sc+Hu和Hu-Sc处理组的还原糖含量在发酵第14天均降至4 g/L以下,表明酒精发酵已基本完成;而Hu单菌发酵在发酵第16天时还原糖仍残留5.89 g/L。Sc单菌发酵组的还原糖消耗速率和酒精度积累速率最高,且完成发酵所需时间也最短。在混合发酵组中,Hu-Sc顺序接种组的酒精度增加速率显著低于同时接种组。结合图2所示的酵母菌生长动态可以发现,在接种S.cerevisiae后发酵速率显著加快,说明S.cerevisiae在发酵过程中起主导作用,而H.uvarum存在时间越长,整体发酵速率越慢,但均能正常完成酒精发酵。
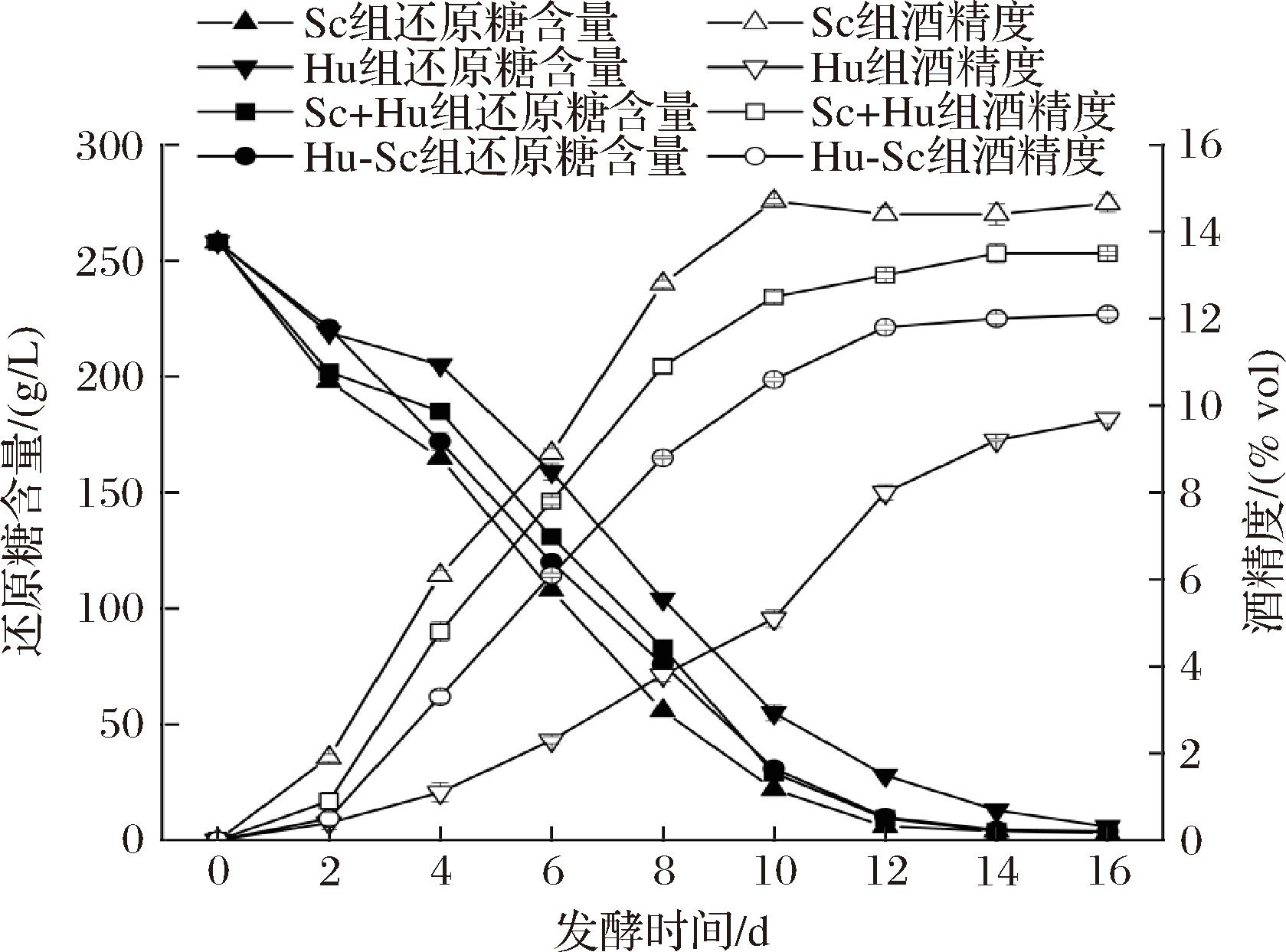
图3 不同接种方式发酵过程中的还原糖含量和酒精度变化
Fig.3 Changes in reducing sugar and ethanol content during fermentation with different inoculation methods
2.3 葡萄酒主发酵产物分析
发酵结束后,对各实验组葡萄酒的关键理化指标进行了测定,结果如表1所示。H.uvarum单菌发酵能力较弱,发酵终止时残糖量>4 g/L。这是由于非酿酒酵母因自身代谢特性限制,无法单独完成完整的酒精发酵过程,发酵液中残留较多葡萄糖,导致其乙醇产量显著低于S.cerevisiae对照组[15]。与Sc组(14.65%)相比,Sc+Hu和Hu-Sc组的乙醇体积分数分别显著降低至13.41%和12.06%(P<0.05),降幅分别为1.24%与2.59%。为客观评价H.uvarum的乙醇代谢特性,本研究引入了乙醇产量和乙醇产率2个指标[17]。结果表明,Sc组的乙醇产量和产率分别为116.91 g/L和45.87%,而Hu组仅为74.72 g/L和29.64%,二者差异显著(P<0.05),说明H.uvarum在低醇葡萄酒酿造中具备应用潜力。Sc+Hu组和Hu-Sc混合发酵组的乙醇体积分数均较Sc组下降,推测可能与H.uvarum倾向于将部分葡萄糖分流至甘油等副产物,而非完全转化为乙醇的氧化代谢特性有关[18]。而Sc+Hu和Hu-Sc组的甘油含量分别较Sc组显著提高1.05、1.35 g/L(P<0.05),进一步验证了该推测。此外,混合发酵提高了挥发酸含量,与张鸣宇等[19]研究结果一致。所有实验组的挥发酸含量为0.21~0.79 g/L,远低于GB/T 15037—2006《葡萄酒》规定的上限(1.2 g/L)。
表1 不同发酵组葡萄酒主发酵产物分析
Table 1 Analysis of main fermentation products in wines from different fermentation groups

指标Sc组Hu组Sc+Hu组Hu-Sc组残糖含量/(g/L)3.15±0.25c5.89±0.06a3.62±0.32b3.79±0.14b乙醇体积分数/%14.65±0.06a9.47±0.18d13.41±0.03b12.06±0.0.02c乙醇产量/(g/L)116.91±4.82a74.72±3.21d107.01±5.74b95.15±2.84c乙醇产率/%45.87±2.56a29.64±2.08d42.07±1.22b37.43±0.65c总酸含量/(g/L)4.53±0.09b4.22±0.02c4.47±0.02b4.69±0.01a甘油含量/(g/L)7.81±0.03c7.26±0.06d8.86±0.12b9.16±0.06a挥发酸含量/(g/L)0.21±0.02d0.79±0.01a0.32±0.03c0.56±0.01b
注:同行字母不同表示差异显著(P<0.05)。
2.4 葡萄酒挥发性香气成分分析
本研究通过GC-MS检测了不同处理组葡萄酒中的挥发性香气成分,共鉴定出59种化合物,其中酯类25种、高级醇类14种、脂肪酸类5种、苯乙基类化合物3种、羰基化合物6种、萜烯类4种和挥发性酚类2种。如电子版增强出版附表1(https://doi.org/10.13995/j.cnki.11-1802/ts.044507)和图4所示,各处理组挥发性化合物的组成与含量存在显著差异。Sc、Hu、Sc+Hu和Hu-Sc处理组分别检出55、46、57、56种挥发性香气物质,总含量分别为32 676.26、32 305.57、63 046.23、74 719.67 μg/L。
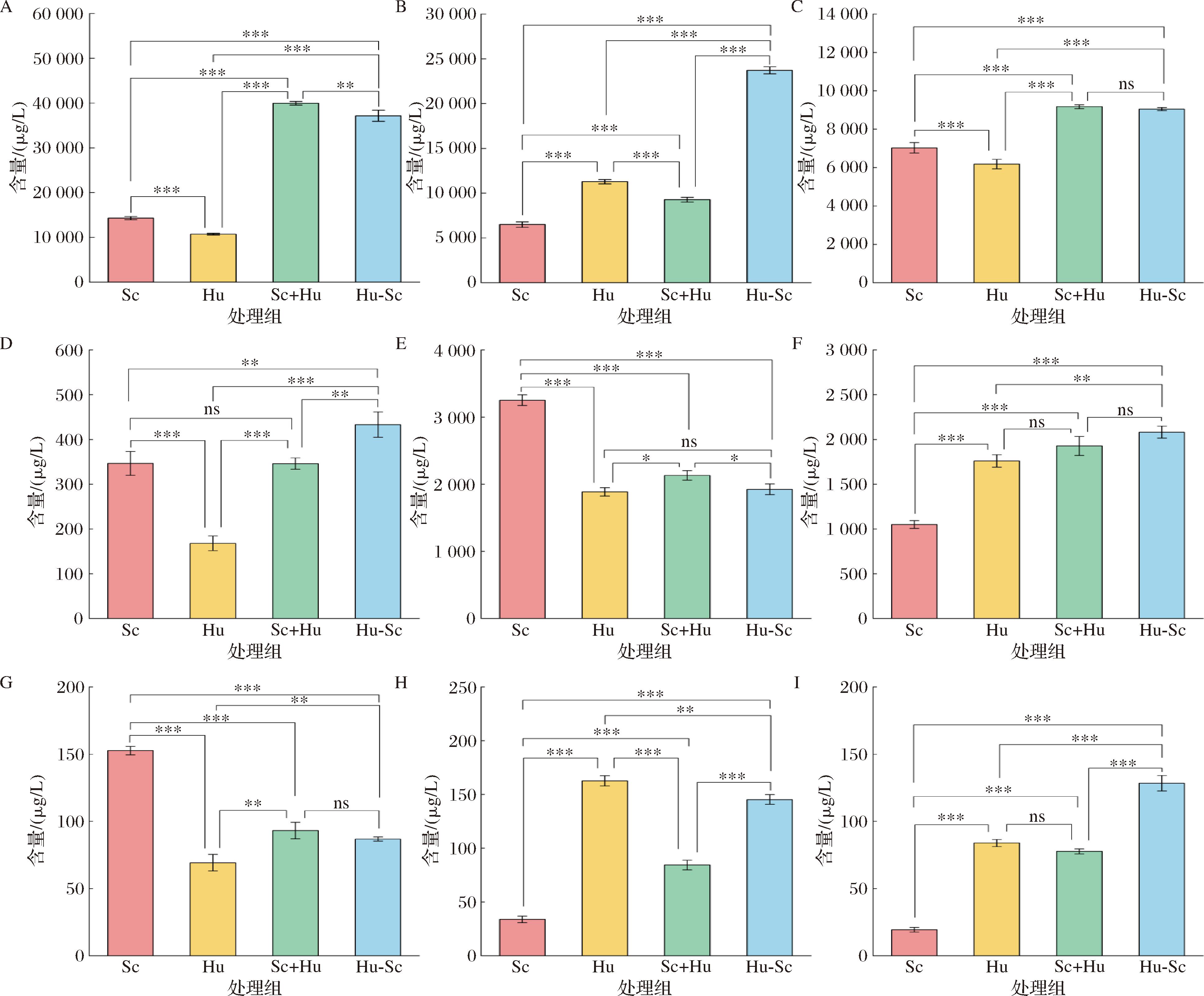
A-高级醇含量;B-乙酸酯含量;C-脂肪酸乙酯含量;D-其他酯类含量;E-脂肪酸含量;F-苯乙基类化合物含量;G-羰基化合物含量;H-挥发性酚含量;I-萜烯类含量
图4 不同处理组葡萄酒挥发性香气物质含量
Fig.4 Content of volatile aroma compounds in wines from different treatment groups
注:***表示P≤0.001,**表示0.00 1<P≤0.01,*表示0.01<P≤0.05,ns表示P>0.05。
高级醇是构成葡萄酒香气复杂度与层次感的一类重要挥发性物质,主要由支链氨基酸经由埃里希途径代谢转化生成[20]。本研究结果显示,高级醇是所有挥发性香气中浓度最高的一类(图4-A),各处理组中高级醇的总量为10 711.17~39 947.79 μg/L。结合各高级醇含量分析,异戊醇(脂肪味和化学味)、异丁醇(植物味和化学味)、1-已醇(植物味)、1-辛醇(柑橘味)、1-庚醇(甜香)是本研究中‘马瑟兰’葡萄酒的主要高级醇。其中Sc组的高级醇含量显著高于Hu组(P<0.001),而Sc+Hu与Hu-Sc混合发酵处理组的高级醇含量较单菌发酵组均显著提升。该结果推测可能与酵母间相互作用协同促进了高级醇的生物合成有关。
酯类物质是构成葡萄酒果香与花香特征的核心组分,其中以乙酸酯和脂肪酸乙酯的贡献最为突出[21]。如图4-B所示,单独发酵组中Hu组的乙酸酯含量高于Sc组,而与Sc、Hu、Sc+Hu组相比,Hu-Sc组的乙酸酯含量分别提升265.75%、110.24%、155.93%,表明顺序接种模式更利于乙酸酯的积累。脂肪酸乙酯结果显示(图4-C),Sc+Hu与Hu-Sc混合发酵处理的脂肪酸乙酯含量均显著高于Sc与Hu单独接种发酵组(P<0.001),而Sc+Hu与Hu-Sc组之间则无显著差异(P>0.05),此结果与易子程等[22]的研究一致,表明H.uvarum具有强化酯类合成(如乙酸异戊酯)的代谢特性。其他酯类物质占比为酯类化合物总量的0.20%~0.53%,与Sc单独发酵相比,仅Hu-Sc处理组的含量显著增加(P<0.01,图4-D)。
挥发性脂肪酸主要是由酵母在脂肪酸代谢过程中形成的,当其浓度超过一定值时,会使葡萄酒产生酸腐味和溶剂味[23]。实验共检测出5种脂肪酸物质,包括辛酸、异丁酸、壬酸、异戊酸和己酸,其中Sc组的脂肪酸类物质含量最高,而Hu、Sc+Hu和Hu-Sc处理组与Sc组相比,脂肪酸总量分别显著降低了42.00%、34.45%、40.85%(图4-E)。上述结果表明,H.uvarum的引入可能调控了脂肪酸代谢途径,从而有助于减少果酒中因脂肪酸过量可能产生的不良气味。
实验中还检测到3种苯乙基类化合物、6种羰基化合物和2种挥发性酚。其中苯乙基类化合物可赋予葡萄酒花香和果香,在Hu、Sc+Hu和Hu-Sc处理组中含量均显著高于Sc组(P<0.001,图4-F)。与之相反,H.uvarum的接种发酵显著降低了羰基化合物的含量(图4-G),但Sc+Hu和Hu-Sc处理组之间不存在显著差异(P>0.05)。值得注意的是,所检测到的羰基化合物、挥发性酚类物质虽然质量浓度较低,但可能会给葡萄酒带来理想的杏仁味、烧烤味和花香[23]。
萜烯类化合物是葡萄酒中品种香气(一类香气)的主要来源,主要源自葡萄果实,对葡萄酒的品种典型性具有关键的呈香贡献[24]。相较于Sc组,接种H.uvarum菌株的处理组酒样中萜烯类化合物含量均显著提高(图4-I),其中Hu-Sc处理组的的增幅最为显著,表明该本土菌株具备强化品种香气化合物合成的生物潜能。
为可视化本土H.uvarum与S.cerevisiae混合发酵对葡萄酒香气的总体影响,对所测得的挥发性香气化合物进行了聚类分析,结果如图5所示。图中颜色梯度表示物质相对含量:红色代表较高含量,蓝色代表较低含量。聚类分析表明,混菌发酵组别均聚集于同一聚类分支,与单菌发酵组之间有明显差异。尽管Sc+Hu与Hu-Sc两组在整体化合物组成上较为接近,且高含量化合物(红色区域)的分布范围无显著差异,但Hu-Sc组中深红色区域占比更大,表明其挥发性香气物质的总量显著高于Sc+Hu组。这一结果说明,Hu-Sc顺序接种策略在提升葡萄酒香气复杂性方面更具潜力。
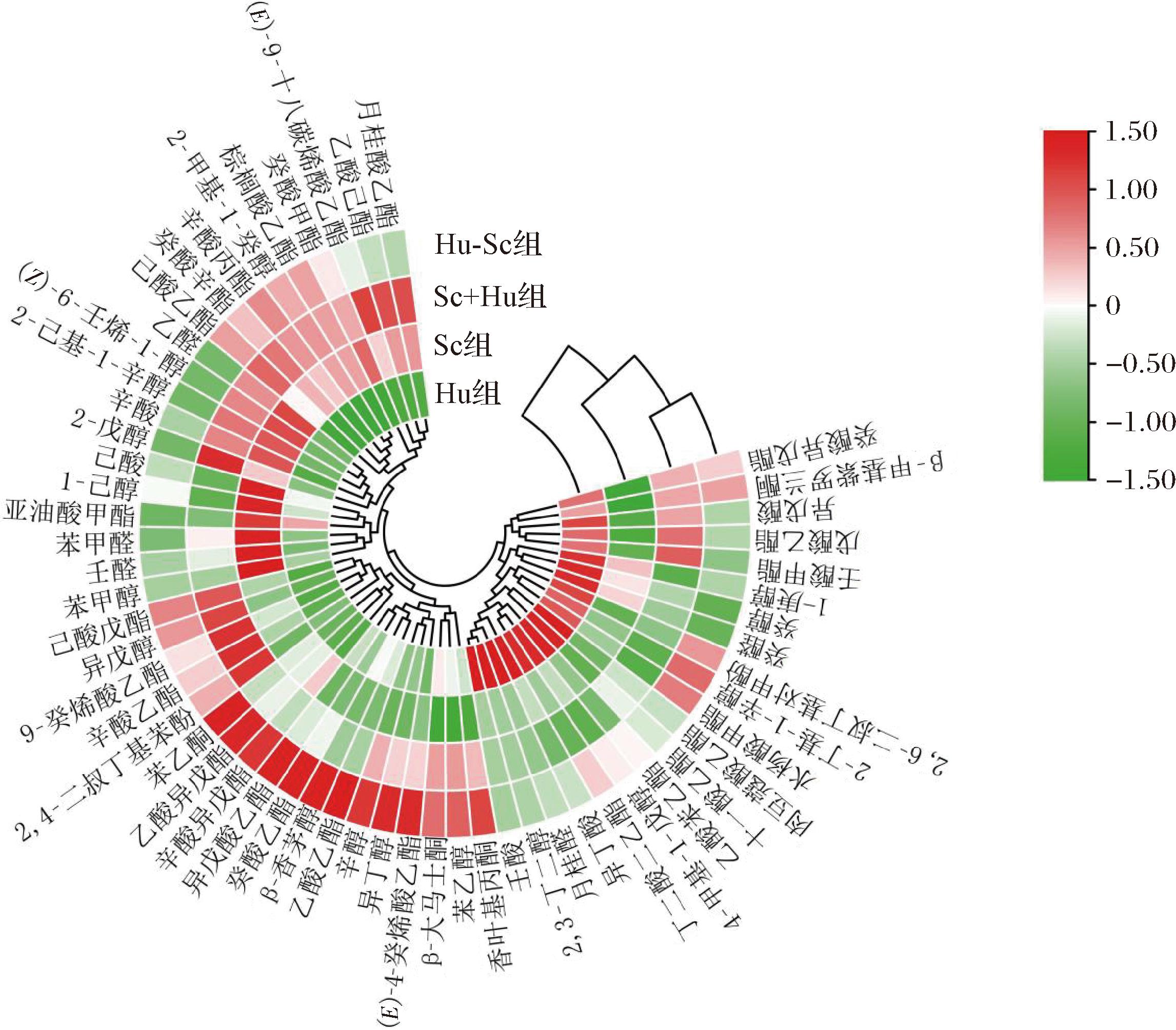
图5 不同发酵组葡萄酒挥发性香气物质热图聚类分析
Fig.5 Heat map cluster analysis of volatile aroma compounds in wines from different fermentation groups
2.5 葡萄酒差异性挥发性香气成分分析
为有效区分不同处理组葡萄酒样品的香气特征,以59种共有香气组分作为因变量,不同处理组作为自变量,进行正交偏最小二乘判别分析(orthogonal projections to latent structures-discriminant analysis,OPLS-DA)。如图6-A所示,不同处理组的样品有明显区分。模型质量评估显示,自变量拟合指数本次分析中的自变量拟合指数![]() 为0.997,因变量拟合指数
为0.997,因变量拟合指数![]() 为0.999,模型预测指数(Q2)为0.998。R2和Q2超过0.5表示模型具有良好的拟合优度和预测能力。经过200次置换检验,如图6-B所示,Q2回归线与纵轴的相交点小于0,说明模型未出现过拟合,具有较强的解释与预测效力,可用于准确鉴别不同处理葡萄酒的香气差异。通过OPLS-DA模型变量投影分析,共筛选出8种对处理组间差异贡献最大的挥发性风味物质[投影变量重要性(variable importance in the projection,VIP)值>1],包括乙酸乙酯、9-癸烯酸乙酯、癸酸乙酯、异丁醇、异戊醇、辛酸、己酸和苯乙醇(图6-C)。
为0.999,模型预测指数(Q2)为0.998。R2和Q2超过0.5表示模型具有良好的拟合优度和预测能力。经过200次置换检验,如图6-B所示,Q2回归线与纵轴的相交点小于0,说明模型未出现过拟合,具有较强的解释与预测效力,可用于准确鉴别不同处理葡萄酒的香气差异。通过OPLS-DA模型变量投影分析,共筛选出8种对处理组间差异贡献最大的挥发性风味物质[投影变量重要性(variable importance in the projection,VIP)值>1],包括乙酸乙酯、9-癸烯酸乙酯、癸酸乙酯、异丁醇、异戊醇、辛酸、己酸和苯乙醇(图6-C)。
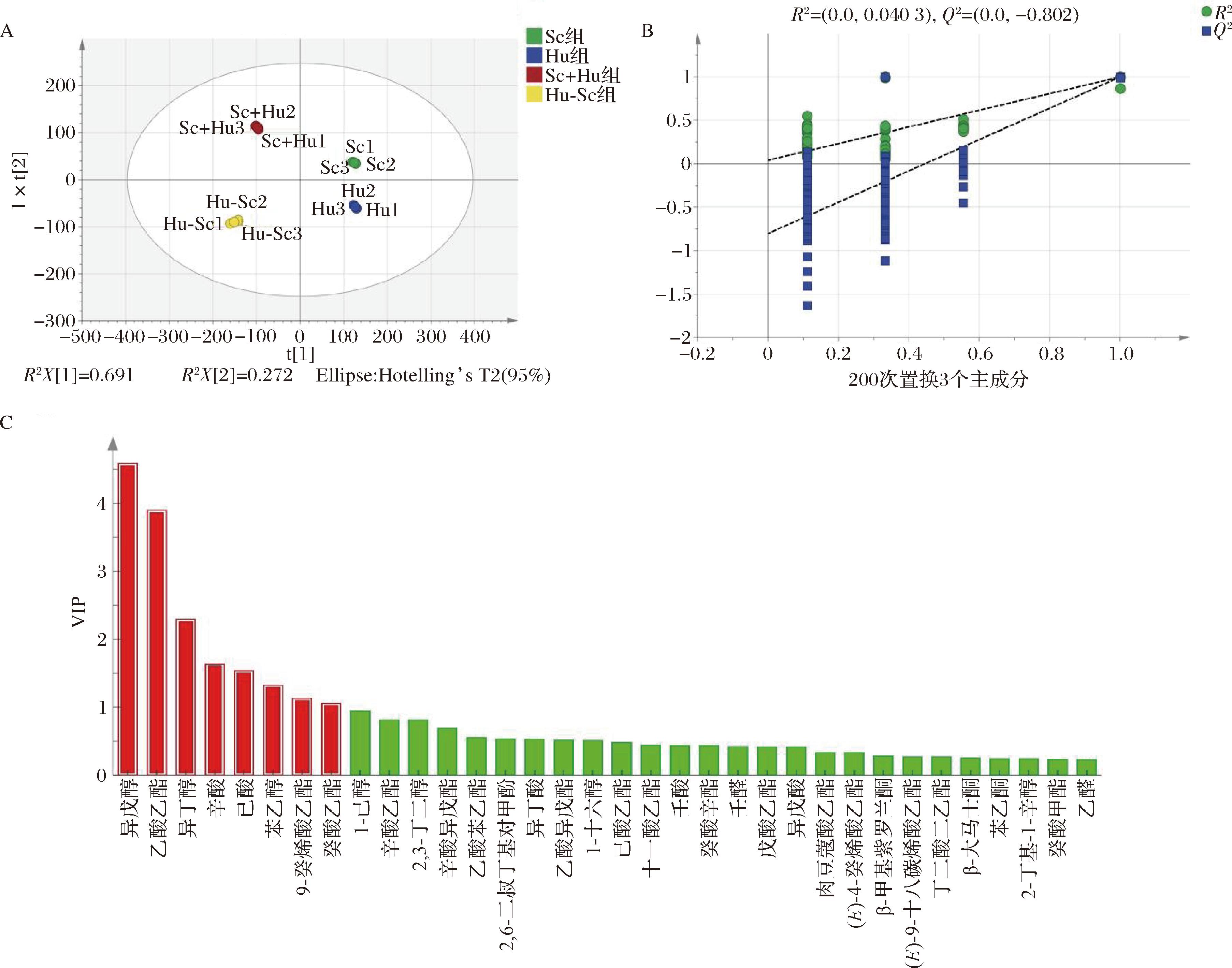
A-OPLS-DA得分图;B-模型置换检验图;C-VIP得分图
图6 不同发酵组葡萄酒发酵结束期风味物质OPLS-DA分析图
Fig.6 OPLS-DA score plot of flavor compounds in different fermentation groups at the end of wine fermentation
对OPLS-DA模型分析VIP值>1的8种差异挥发性化合物进行热图分析,结果如图7所示。与Sc组相比,Sc+Hu和Hu-Sc处理对这8种差异挥发性化合物均表现出显著影响,其中乙酸乙酯、异丁醇、异戊醇和癸酸乙酯的含量在混菌处理组中均有所提升,为葡萄酒贡献出菠萝、香蕉、坚果和水果甜香等香气特征,共同提升了葡萄酒香气的整体强度、复杂度与结构层次感。此外,辛酸和己酸在混菌处理组中的含量均低于Sc组。总体而言,Sc+Hu和Hu-Sc处理均表现出降低脂肪酸含量、同时促进乙酸酯类和高级醇类化合物生成的趋势。
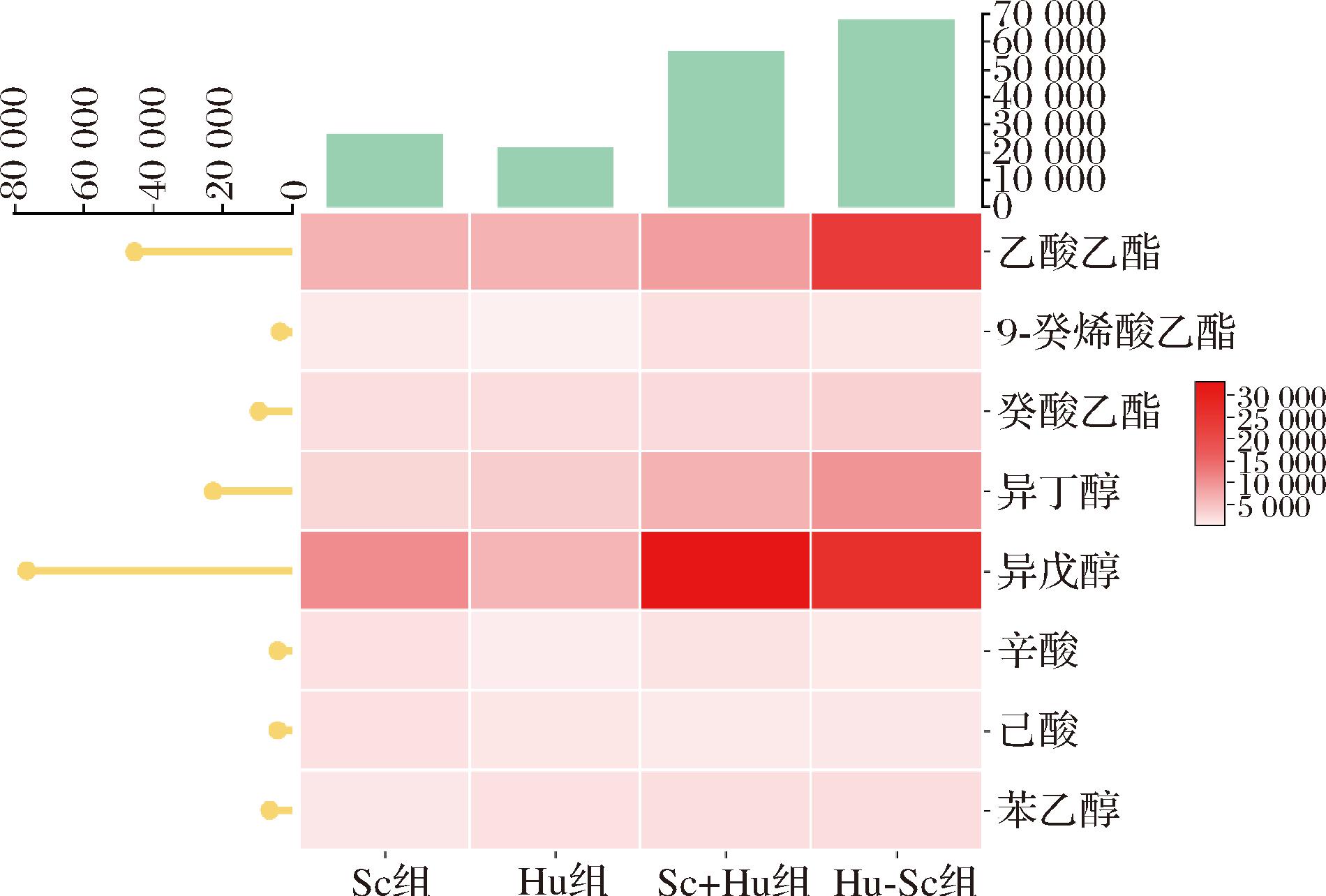
图7 不同发酵组酒样中差异挥发性香气化合物棒棒糖组合热图分析
Fig.7 Heat map analysis of lollipop combinations of differential volatile aroma compounds in wine samples from different fermentation groups
2.6 葡萄酒感官分析
为系统评估本土H.uvarum菌株混合发酵对葡萄酒感官品质的影响,对不同处理组的酒样进行了感官评价(图8)。同时对11名品评员的评分数据进行单因素方差分析(ANOVA),结果表明各品评员之间在所有感官属性上均无显著差异(P>0.05),说明评价结果具有良好的一致性。结果显示,所有酒样均呈现典型色泽且澄清透亮,各组间在色泽与澄清度方面无显著差异(P>0.05)。香气方面,所有酒样均未检出异味。与Sc单菌发酵相比,Sc+Hu和Hu-Sc混合发酵组的花香与果香强度均显著增强;其中,Hu-Sc组表现出更为浓郁的花香和果香特征,且植物与矿物类气味显著弱化(P<0.05)。值得注意的是,Hu单菌发酵时出现了相对明显的动物类气味,而其他组在此项上无显著差异。口感方面,Sc的酒样收敛性表现较差;与之相比,接种H.uvarum的处理组(Hu、Sc+Hu、Hu-Sc组)对葡萄酒的收敛性均有所改善。混合发酵组的余味长度显著长于纯种发酵组。在酸度感知上,Hu-Sc组相较于其他组别有所提升。整体平衡感评价显示,混合发酵组的评分显著高于单菌发酵组,品评人员的总体偏好排序为:Hu-Sc组>Sc+Hu组>Sc组>Hu组。上述感官分析结果证实,接种本土H.uvarum菌株,特别是采用Hu-Sc顺序接种模式,可显著提升葡萄酒的整体感官品质,其主要优势体现在香气复杂性的增强、整体协调性的改善及余味久性的提升。
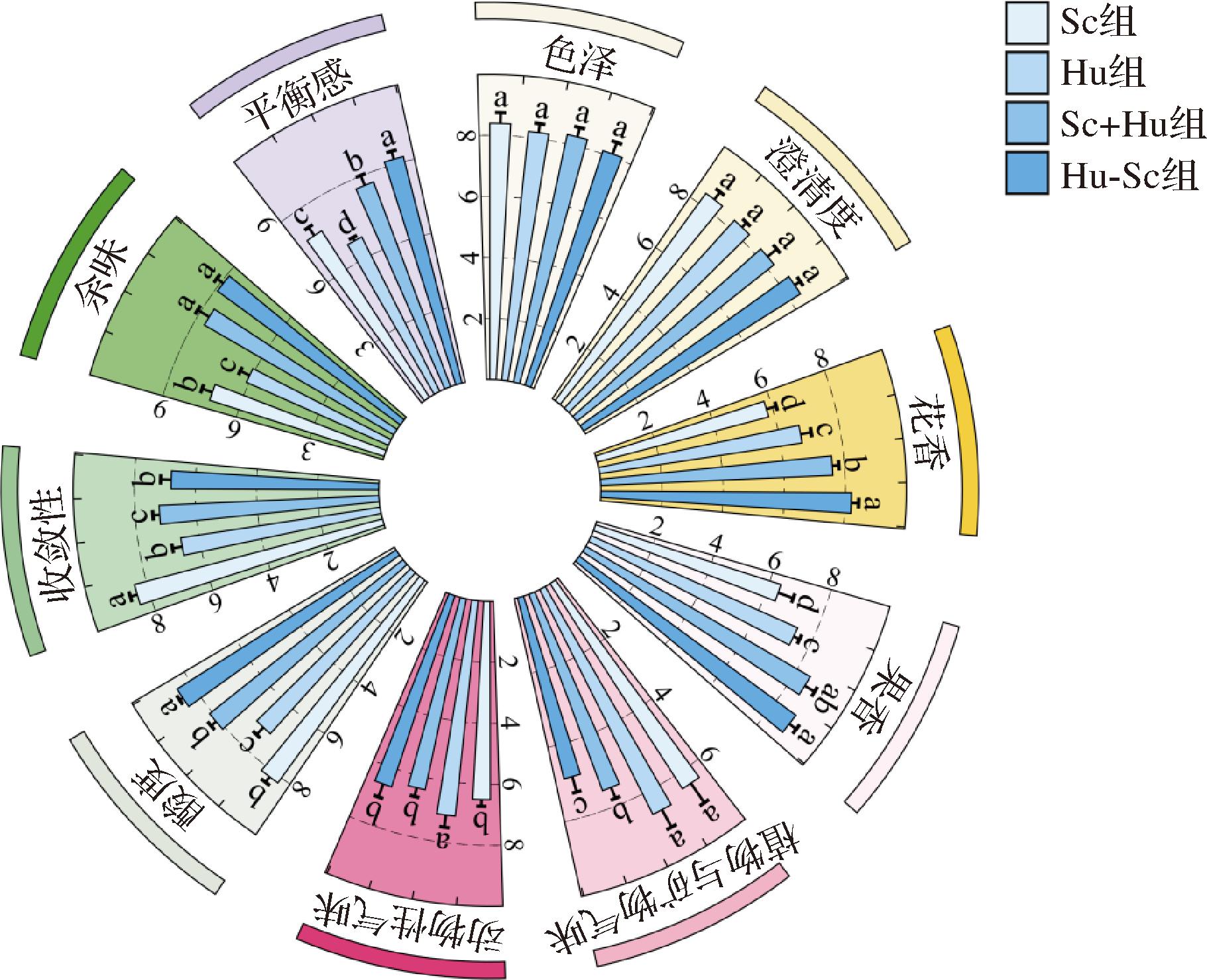
图8 不同发酵组葡萄酒感官分析
Fig.8 Sensory analysis of wines from different fermentation groups
注:同组不同字母表示样品间差异显著(P<0.05)。
3 结论
本研究系统比较了S.cerevisiae与H.uvarum在单独接种、同时接种及顺序接种3种发酵模式下对‘马瑟兰’葡萄酒发酵动力学、挥发性香气成分及感官品质的影响。结果表明,H.uvarum乙醇产量和产率低(74.72 g/L和29.64%),其在低醇葡萄酒酿造中具备应用潜力。与纯种S.cerevisiae发酵相比,同时接种和顺序接种发酵组乙醇产量和乙醇产率均显著下降,同时接种使乙醇体积分数降低约1.24%,顺序接种则可降低约2.59%,同时甘油含量显著上升。在香气方面,混合发酵,尤其是顺序接种发酵处理组显著提升了葡萄酒中挥发性化合物的总浓度,其中乙酸乙酯、异丁醇和异戊醇等关键差异性香气物质的含量显著增加;辛酸和己酸含量显著降低。感官分析结果表明,与S.cerevisiae相比,同时接种和顺序接种发酵能够表现出更浓郁的花香、果香特征,更悠长的余味及更协调的整体平衡感。综上所述,本土H.uvarum菌株协同酿酒酵母,通过酵母间互作机制,可有效降低乙醇合成并优化香气组分的生成。因此,该菌株在酿造高香气复杂度、低酒精度的葡萄酒方面展现出显著的应用潜力,也为基于多菌株混合发酵的葡萄酒品质提升策略提供了理论依据。
[1] BENITO  , CALDER
, CALDER N F, BENITO S. The influence of non-Saccharomyces species on wine fermentation quality parameters[J]. Fermentation, 2019, 5(3): 54.
N F, BENITO S. The influence of non-Saccharomyces species on wine fermentation quality parameters[J]. Fermentation, 2019, 5(3): 54.
[2] LIU D, LEGRAS J L, ZHANG P Z, et al. Diversity and dynamics of fungi during spontaneous fermentations and association with unique aroma profiles in wine[J]. International Journal of Food Microbiology, 2021, 338:108983.
[3] BINATI R L, LEMOS W J F Jr, LUZZINI G, et al. Contribution of non-Saccharomyces yeasts to wine volatile and sensory diversity: A study on Lachancea thermotolerans, Metschnikowia spp. and Starmerella bacillaris strains isolated in Italy[J]. International Journal of Food Microbiology, 2020, 318:108470.
[4] ZHANG B Q, SHEN J Y, DUAN C Q, et al. Use of indigenous Hanseniaspora vineae and Metschnikowia pulcherrima co-fermentation with Saccharomyces cerevisiae to improve the aroma diversity of vidal Blanc icewine[J]. Frontiers in Microbiology, 2018, 9:2303.
[5] CAPOZZI V, GAROFALO C, CHIRIATTI M A, et al. Microbial terroir and food innovation: The case of yeast biodiversity in wine[J]. Microbiological Research, 2015, 181:75-83.
[6] 魏巍, 卢浩成, 贾倩倩, 等. 天山北麓产区4个葡萄品种酿酒品质探究[J]. 中外葡萄与葡萄酒, 2020(2):1-8.WEI W, LU H C, JIA Q Q, et al. Study on winemaking characteristics of four grape varieties in northern foothills of Tianshan mountains[J]. Sino-Overseas Grapevine &Wine, 2020(2):1-8.
[7] MATURANO Y P, MESTRE M V, KUCHEN B, et al. Optimization of fermentation-relevant factors: A strategy to reduce ethanol in red wine by sequential culture of native yeasts[J]. International Journal of Food Microbiology, 2019, 289:40-48.
[8] VARELA C, DRY P R, KUTYNA D R, et al. Strategies for reducing alcohol concentration in wine[J]. Australian Journal of Grape and Wine Research, 2015, 21(S1):670-679.
[9] KUTYNA D R, VARELA C, HENSCHKE P A, et al. Microbiological approaches to lowering ethanol concentration in wine[J]. Trends in Food Science &Technology, 2010, 21(6):293-302.
[10] 田怀香, 熊娟涓, 于海燕, 等. 果酒中香气化合物的生物转化与调控机制研究进展[J]. 食品科学, 2022, 43(19):36-47.TIAN H X, XIONG J J, YU H Y, et al. Biotransformation and biological regulation mechanism of aroma compounds in fruit wine: A review[J]. Food Science, 2022, 43(19):36-47.
[11] WANG C H, SUN J C, LASSABLIERE B, et al. Coffee flavour modification through controlled fermentations of green coffee beans by Saccharomyces cerevisiae and Pichia kluyveri: Part I. Effects from individual yeasts[J]. Food Research International, 2020, 136:109588.
[12] 唐洁, 李婵媛, 张潆月, 等. 优选葡萄汁有孢汉逊酵母及其在野樱桃发酵饮品酿造中的应用[J]. 西华大学学报(自然科学版), 2024, 43(4):8-16.TANG J, LI C Y, ZHANG Y Y, et al. Optimization selection of Hanseniaspora uvarumand its application in fermented wild cherry beverage[J]. Journal of Xihua University (Natural Science Edition), 2024, 43(4):8-16.
[13] CONTRERAS A, HIDALGO C, HENSCHKE P A, et al. Evaluation of non-Saccharomyces yeasts for the reduction of alcohol content in wine[J]. Applied and Environmental Microbiology, 2014, 80(5):1670-1678.
[14] 尤雅, 段长青, 燕国梁. 扁平云假丝酵母与酿酒酵母混合发酵对葡萄酒乙醇含量及香气的影响[J]. 食品科学, 2018, 39(20):146-154.YOU Y, DUAN C Q, YAN G L. Effects of mixed fermentation of Candida humilis and Saccharomyces cerevisiae on ethanol content and aroma of wine[J]. Food Science, 2018, 39(20):146-154.
[15] 张博钦, 方梓庄, 成池芳, 等. 5株低产乙醇的非酿酒酵母筛选及其酿造特性[J]. 食品科学, 2021, 42(8):114-121.ZHANG B Q, FANG Z Z, CHENG C F, et al. Screening of five non-Saccharomyces strains with low ethanol yield and evaluation of their oenological properties[J]. Food Science, 2021, 42(8):114-121.
[16] 周得刚, 徐彬艳, 王青霞, 等. 戴尔有孢圆酵母与酿酒酵母细胞间接触对‘赤霞珠’葡萄酒风味品质的影响[J]. 中国农业科学, 2024, 57(16):3264-3282.ZHOU D G, XU B Y, WANG Q X, et al. Effects of cell-to-cell contact between Torulaspora delbrueckii and Saccharomyces cerevisiae on the flavor and quality of cabernet sauvignon wine[J]. Scientia Agricultura Sinica, 2024, 57(16):3264-3282.
[17] GOBBI M, DE VERO L, SOLIERI L, et al. Fermentative aptitude of non-Saccharomyces wine yeast for reduction in the ethanol content in wine[J]. European Food Research and Technology, 2014, 239(1):41-48.
[18] CONTRERAS A, HIDALGO C, SCHMIDT S, et al. The application of non-Saccharomyces yeast in fermentations with limited aeration as a strategy for the production of wine with reduced alcohol content[J]. International Journal of Food Microbiology, 2015, 205:7-15.
[19] 张鸣宇, 罗莉莎, 高特, 等. 本土美极梅奇酵母对玫瑰香葡萄酒降醇及香气的影响[J]. 中国酿造, 2023, 42(1):133-141.ZHANG M Y, LUO L S, GAO T, et al. Effects of indigenous Metschnikowia pulcherrima on alcohol reduction and aroma of Muscat wine[J]. China Brewing, 2023, 42(1):133-141.
[20] PADILLA B, GIL J V, MANZANARES P. Past and future of non-Saccharomyces yeasts: From spoilage microorganisms to biotechnological tools for improving wine aroma complexity[J]. Frontiers in Microbiology, 2016, 7:411.
[21] MARAIS J, VAN ROOYEN P C, DU PLESSIS C S. Objective quality rating of pinotage wine[J]. VITIS-Journal of Grapevine Research, 2016, 18(1): 31.
[22] 易子程, 常腾文, 司慧宁, 等. 本土非酿酒酵母对混合发酵威代尔冰酒风味及品质影响的比较分析[J]. 食品与发酵工业, 2025, 51(12):215-225.YI Z C, CHANG T W, SI H N, et al. Comparative analysis of impact of local non-Saccharomyces yeasts on flavor and quality of mixed-fermented Vidal ice wine[J]. Food and Fermentation Industries, 2025, 51(12):215-225.
[23] WANG X J, TAO Y S, WU Y, et al. Aroma compounds and characteristics of noble-rot wines of Chardonnay grapes artificially botrytized in the vineyard[J]. Food Chemistry, 2017, 226:41-50.
[24] CARPENA M, FRAGA-CORRAL M, OTERO P, et al. Secondary aroma: Influence of wine microorganisms in their aroma profile[J]. Foods, 2021, 10(1):51.