“粮为酒之肉”是白酒酿造理念的浓缩,酿酒原料高粱以其独特的理化特性与微生物代谢协同效应,不仅奠定了酒体骨架,更赋予了白酒香正甘洌的特点[1]。中国白酒为世界六大蒸馏酒之一,酿造工艺精湛,风格特征典型[2]。白酒依据不同生产工艺分为十二香型,其中以巧妙融合“前浓、中清、后酱”独特香气特征的馥郁香型白酒为白酒创新的代表。馥郁香型白酒采用大小曲并用的多轮次续糟发酵工艺,以翻醅期(9~10月)-常态发酵期(第2~5轮次,11月~次年5月)-压醅期(5~6月)为单次生产年,单轮发酵期内通过小曲将以高粱为主的多粮原料培菌糖化,糖化完成按相应比例配取酒打凉后的酒醅,混合大曲后入泥窖发酵[3]。其中,培菌糖化作为馥郁香型白酒酿造的关键环节,是微生物增殖、酶系形成及风味前体物质积累的关键阶段,直接影响着后续发酵效率和最终酒体的风味轮廓[4]。近年来,随着消费者对白酒风味多样性的需求提升,传统培菌糖化工艺的优化成为馥郁香型白酒技术革新的焦点。
馥郁香型白酒传统培菌糖化工艺选取粳高粱为原料,通过多次清蒸使高粱糊化,再配以润拌均匀的糯米、大米和玉米粉混合清蒸,摊凉后入箱糖化[3]。其中高粱种类、小曲菌种、入箱温度、糖化时长等均直接影响着原料糖化效果,进而影响最终酒体风味,如冯亮等[5]从糖化原料中定向分离筛选出高产蜜香物质的功能菌株米根霉BC70107,经过扩培制曲发现糖化力达到419 mg/(g·h),投入生产后显著提升了糖化料中苯乙酸乙酯和β-苯乙醇等蜜香风味物质含量。刘茂柯等[6]通过对比4种酿酒高粱生产发现高粱中单宁含量显著影响浓香型白酒中醛类和异丁醇的含量(P<0.05),而支链淀粉含量显著影响仲丁醇的含量(P<0.05)。而田殿梅等[7]通过追踪3种不同粳糯高粱糟醅发酵过程发现,不同高粱糟醅发酵过程理化及最终基酒风味均存在差异,其中糯高粱酒糟发酵生产的基酒浓香纯正、醇甜、干净,口感较粳高粱更优。然而,尽管目前有关高粱影响白酒风味的研究众多,对于馥郁香型白酒的研究仍大多聚焦于单一发酵轮次糖化原料的理化指标差异变化或感官差异变化,对不同糖化原料参与的整个酿造过程的跟踪研究少之又少,尤其是缺乏糖化原料在入池发酵至出池摘酒的多轮次周期性研究。
本研究旨在对比馥郁香型白酒各发酵轮次下不同高粱及糖化时长导致的酒醅发酵差异,对发酵过程酒醅升温进行监控,并分析在酒醅理化、基酒风味成分等方面的差异情况,采用重复测量方差分析、主成分分析(principal component analysis,PCA)、相关性Mantel检验等科学分析方法,探究培菌糖化对多轮次发酵影响的内在机理,为馥郁香型白酒生产工艺优化提供参考依据及数据支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 材料来源
酒醅、糯高粱(川糯一号)、粳高粱(产自内蒙赤峰)、大米、糯米、玉米粉[粉碎度:能通过20目筛的筛下物为(30±2)%]、大曲、小曲、糠壳。
1.1.2 试剂
硫酸、氢氧化钠、酚酞、乙酸乙酯、己酸乙酯、乳酸乙酯、丁酸乙酯、正丙醇、正丁醇、异丁醇、异戊醇、乙醛、乙缩醛标准品(色谱纯),上海阿拉丁生化科技股份有限公司。
表1 高粱指标
Table 1 Sorghum index

品种容重/(g/L)不完善粒/(g/L)杂质/(g/L)水分/%壳料/(g/L)淀粉含量/(g/100 g)粳高粱 742±22.4±0.10.7±0.113.0±0.22.8±0.172.4±0.5川糯一号743±22.8±0.21.0±0.113.5±0.32.0±0.164.8±0.4
1.2 仪器与设备
Agilent 7890A气相色谱仪,上海安捷伦公司;FF-1801酒醅检测仪,中国食品发酵工业研究院有限公司;DME35 Ex便携式酒精测量仪,奥地利安东帕公司;DTM-411A数显温度计,衡水朝辉自控仪表有限公司。
1.3 实验方法
1.3.1 培菌糖化工艺
高粱除杂浸泡22 h后入甑清蒸,清蒸40 min后进行第1次洒冷水降温润拌,待上层15 cm高粱冷透,排尽底锅水,进行第2次清蒸,清蒸45 min后进行第2次洒冷水降温润拌,待上层15 cm高粱冷透,排尽底锅水,第3次清蒸至高粱开花达100%,单甑高粱按7∶3质量比例加入浸润2.5 h的三米[m(糯米)∶m(大米)∶m(玉米粉)=3∶2∶1],拌合均匀,清蒸30 min保证三米熟透后出甑,打凉入箱培菌糖化,11月1日~4月30日工艺标准糖化时长为44 h。
1.3.2 原料及糖化时长控制
选取同一区域2个生产情况相似班组(A班组、B班组),设置不同原料高粱配比(100%粳高粱、85%粳高粱+15%糯高粱,质量分数)×原料糖化时长(44、22 h)双因素正交试验,15%糯高粱添加比例为梯度预实验结果最佳配比。实验分组分别以A1、A2、B1、B2表示,具体分组为A1组:100%粳高粱/糖化44 h;A2组:100%粳高粱/糖化22 h;B1组:(85%粳高粱+15%糯高粱)/糖化44 h;B2组:(85%粳高粱+15%糯高粱)/糖化22 h,实验设置3个平行,单个处理组分连续3 d于3个窖池进行。实验池自2022年11月22日开始第2轮次入池,至2023年4月17日第5轮次出池结束,共4轮次酿酒生产。
1.3.3 取样
糖化料样品:糖化料使用前5 min使用五点取样法取中层糖化料共200 g,用镊子去除谷壳后作为当日糖化料样品。
酒醅样品:采集正糟第2甑、第4甑、第6甑入池酒醅(共7甑),使用五点取样取四角及中心点位共300 g酒醅混匀作为当日入池酒醅样。采集正糟第2、4、6层出池酒醅,同样取四角与中心5个点位共300 g酒醅混匀作为当日出池酒醅样。
基酒样品:正糟酒醅结束发酵后上甑蒸馏摘酒,严格依照馥郁香型白酒摘酒工艺执行,摘酒过程中保证流酒温度、流酒速度及流酒气压一致,流酒温度为25 ℃,流酒速度为1.5 L/min,流酒气压15 kPa。其中酒头摘取量为4 kg,中段酒实施量质摘酒,摘至60%vol,准确称取出酒重量作为该窖池正糟出酒产量,取对应第2、4、6层酒醅上甑蒸馏所摘中段酒各100 mL混匀作为该组基酒样品。
1.3.4 指标测定
1.3.4.1 发酵过程温度测定
发酵温度测定:测定窖池中层正糟发酵温度,测量位置同酒醅样品中心取样位一致(距窖池顶部95 cm左右,距窖池长边150 cm左右,距窖池窄边190 cm左右),3个窖池相同发酵时间测量结果取平均值。
1.3.4.2 糖化料还原糖及酒醅理化测定
糖化料、入池酒醅、出池酒醅样品分别取100 g放入检测皿,保证样品铺平无透光,使用酒醅检测仪的还原糖检测程序、酒醅检测程序检测。
1.3.4.3 基酒理化指标及色谱
参照GB 12456—2021《食品安全国家标准 食品中总酸的测定(含第1号修改单)》中总酸的测定方法检测基酒总酸含量。参照GB/T 10345—2022《白酒分析方法》指示剂法检测基酒总酯含量。参考GB 5009.266—2016《食品安全国家标准 食品中甲醇的测定》对基酒中的挥发性风味成分进行测定,采用内标法定量分析。具体分析方法:检测器温度:250 ℃,载气(高纯氮):流速1.0 mL/min,进样口温度:230 ℃,进样量:1.0 μL,分流比:50∶1,升温程序:初温35 ℃,保持5 min,以4 ℃/min升至120 ℃,再以12 ℃/min升至124 ℃,再以15 ℃/min升到200 ℃,保持20 min。
1.4 数据处理
使用R语言对数据进行分析及可视化,使用R语言car包对不同高粱及糖化时长的入出池酒醅理化增减幅度、基酒产量、基酒风味成分含量分别进行重复测量、单因素及双因素方差分析,分析不同高粱、不同糖化时长及不同发酵轮次入出池酒醅理化增减幅度、基酒产量、基酒风味成分含量的差异。使用factoextra包、reshape2包对不同发酵轮次基酒风味成分进行主成分分析,并使用linkET包对基酒风味成分与入池酒醅理化参数进行Mantel检验以及相关显著性分析。
2 结果与分析
2.1 窖池升温曲线
采用数显温度计,对不同发酵轮次酒醅发酵过程进行温度监控,记录酒醅发酵过程的升温趋势以及达到“中挺”的温度与时间,结果如图1所示,在第2轮发酵过程中,相较于A1组,B1组酒醅在第7天更快达到发酵顶温36.0 ℃,B1组顶温较B2组高出2 ℃。而A1组在第9天达到“中挺”温度,A2组升温缓慢。第3轮发酵过程中各组间升温趋势差异不大,B1糖化组第10天达到“中挺”温度,A1、A2组均在第11天达到“中挺”温度,但A2组顶温较A1组低。第4轮发酵B1组在第8天达到“中挺”温度,A1组第9天达到“中挺”温度,A2组、B2组升温缓慢。第5轮发酵B1组第11天达到“中挺”温度,A1组第12天达到“中挺”温度,A2组、B2组升温缓慢。综合4轮次酒醅发酵情况可知,原料中添加糯高粱与缩短糖化时长均会对酒醅发酵产生影响,具体表现为添加糯高粱后酒醅升温节奏加快,达到“中挺”温度的时间减短。结合前人研究,窖池内酒醅温度的变化取决于窖池发酵体系热产出[8-9]。而相较于粳高粱,糯高粱支链淀粉含量占比更高,拌合谷壳配醅入池后更易被发酵微生物利用,进而促进微生物发酵演替,因而在本研究中表现出更快的升温响应[10]。此外,在4轮次发酵期内,粳高粱糖化22 h后配醅入池发酵,均表现出升温缓慢,难以升至“中挺”顶温的趋势,添加糯高粱后升温不良趋势缓解。传统糖化工艺以粳高粱为主要糖化原料,其直链淀粉含量占比较高,不易被微生物直接利用,因而在工艺操作中需通过多次清蒸促使其糊化。除此之外,第2~4轮次低温环境带来的抑制效应也会致使根霉菌在生长前期增殖发育延缓,而44 h的糖化时长保证了原料中淀粉的水解。与之相似的是,糯高粱的添加同样在一定程度上缓解了糖化不足带来的影响[11]。
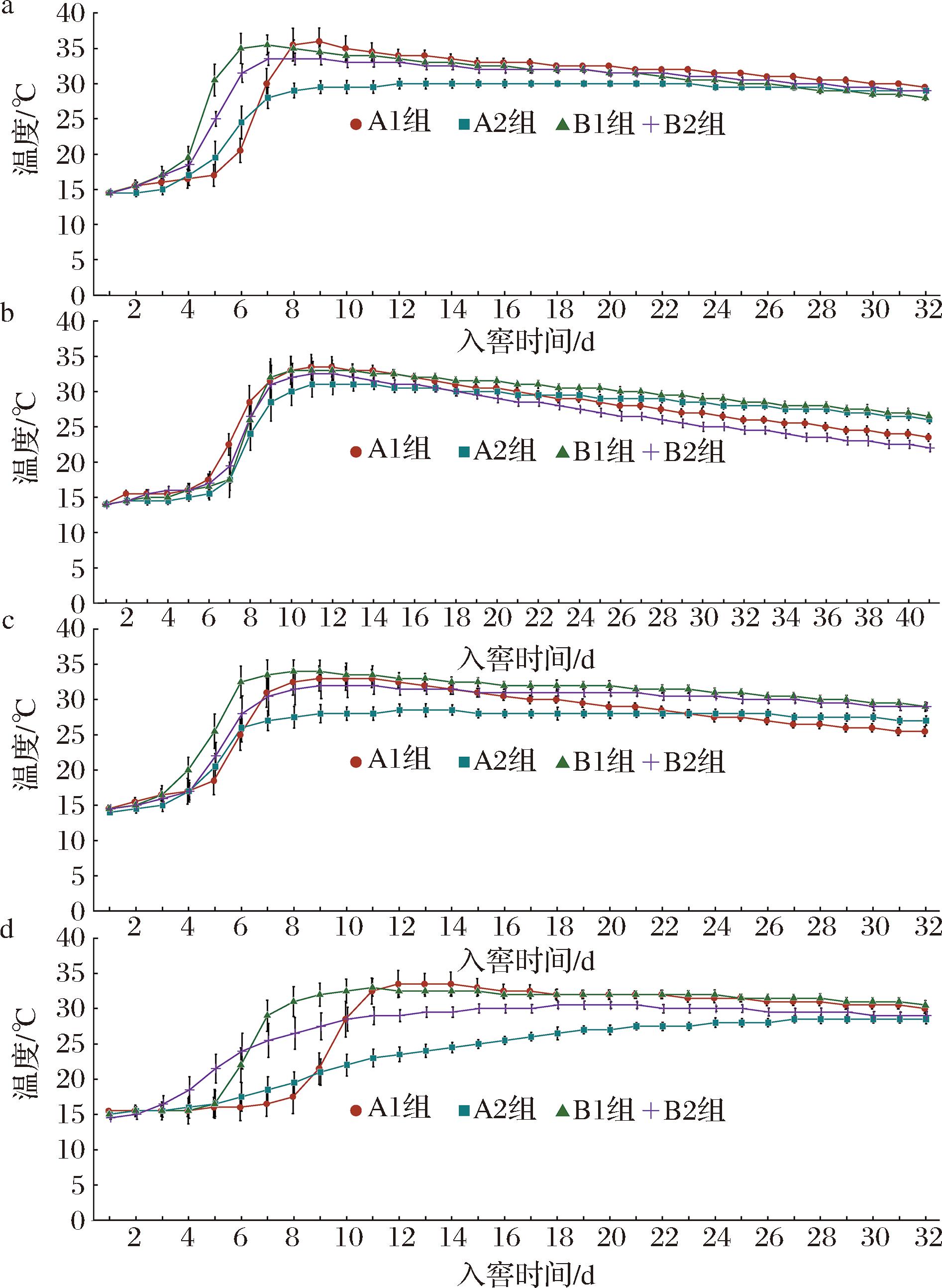
a-第2轮;b-第3轮;c-第4轮;d-第5轮
图1 发酵升温曲线
Fig.1 Temperature rise during fermentation
2.2 发酵前后酒醅理化分析
各发酵轮次酒醅发酵前后水分、酸度、淀粉含量如图2所示。在4轮次发酵中,相较于A1、A2组(平均水分增长率分别为13.4%、10.7%),B1、B2组均表现出更高的水分增长率(平均水分增长率分别为14.6%、13.5%),而A2、B2组较A1、B1组则表现出水分增长率降低的趋势。在第2轮与第4轮发酵期,A2组酒醅水分增长率显著低于A1组与B2组(P<0.05)。重复测量方差分析结果表明不同高粱配比、不同糖化时长及不同发酵轮次间酒醅水分增长率均呈现差异显著性(P值分别为0.002、0.02以及小于0.001)(表2)。其次,不同发酵轮次各组酒醅酸度增长率呈现较大差异,总体上表现为A2、B2组酸度上升幅度小于A1、B1组。重复测量方差分析结果同样表明酸度增长率受不同糖化时长与不同发酵轮次的影响显著(P值均小于0.001),而受不同高粱配比影响不显著(P=0.055)。此外,在第2轮与第5轮发酵期内,各组酒醅淀粉损耗率表现出显著性差异,具体为第2轮次A2组淀粉损耗率(平均47.7%)显著低于A1组(平均54.6%),B2组淀粉损耗率显著低于B1组(P<0.05),第5轮B1组淀粉损耗率(平均60.8%)显著高于其余组(P<0.05)。发酵期内酒醅的水分增长率与酸度增长率在一定程度上反映了窖池内发酵体系的活动强弱,而酒醅淀粉的损耗率直接反映着微生物产酒情况,更高的淀粉损耗率意味着更多的产酒[12]。本研究中粳高粱糖化22 h配醅发酵后水分增长率显著低于配糖化44 h原料的酒醅,酒醅酸度增长率与水分增长率表现出相同的变化趋势。结合酒醅发酵过程中酸度与水分含量呈正相关,而酒醅水分增长率在一定程度上又受到酒醅初始水分含量的制约,较短的糖化时长致使原料水分含量较低[13],进而导致配醅入池后发酵体系前期发酵的延缓,发酵升温曲线同样证明了这一影响途径(图1)。
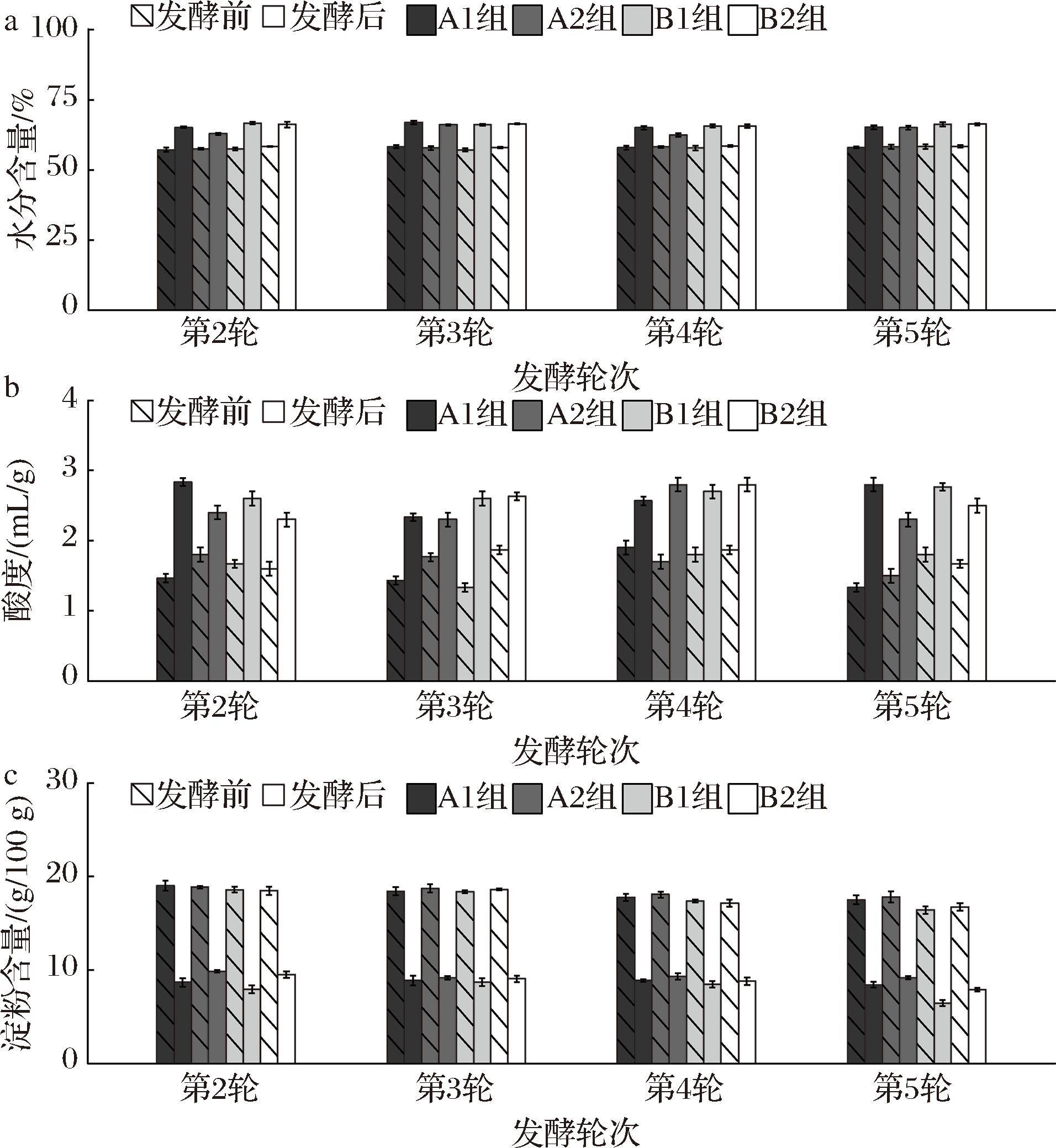
a-水分含量;b-酸度;c-淀粉含量
图2 发酵前后酒醅理化增减
Fig.2 The physicochemical changes of fermented grains before and after fermentation
表2 发酵前后酒醅理化增减率重复测量方差分析
Table 2 The repeated-measures ANOVA of physicochemical change rates before and after fermentation
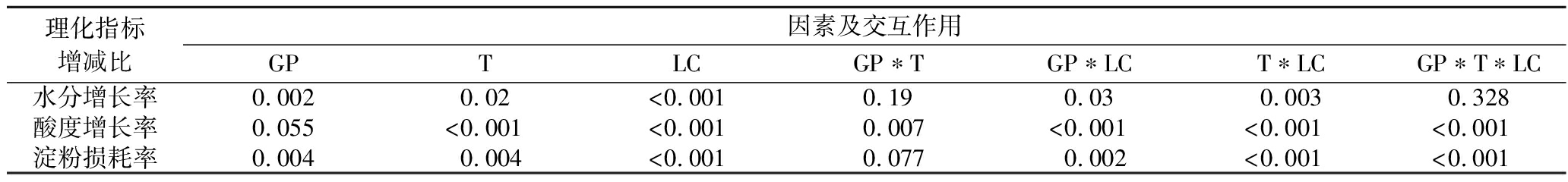
理化指标增减比因素及交互作用GPTLCGP∗TGP∗LCT∗LCGP∗T∗LC水分增长率0.0020.02<0.0010.190.030.0030.328酸度增长率0.055<0.001<0.0010.007<0.001<0.001<0.001淀粉损耗率0.0040.004<0.0010.0770.002<0.001<0.001
注:表中GP代表原料高粱配比,T代表糖化时长,LC代表发酵轮次,*代表对应因素交互作用(下同)。
此外,酒醅淀粉损耗率同样由微生物发酵的强弱所决定,较低水分含量的酒醅需更长的发酵周期完成对淀粉的转化,而糯高粱易糊化和支链淀粉更易被利用的特性使得酒醅具更高的淀粉转化率[14]。
2.3 基酒产量分析
各发酵轮次基酒产量如图3所示。不同发酵轮次基酒产量及出酒率均存在差异,其中第2~4轮基酒产量及出酒率相似,第5轮产量及出酒率均降低。与之相反的是,各发酵轮次下不同高粱及糖化时长对基酒产量表现出相同的影响趋势,均表现为B1组基酒产量及出酒率最高(总产酒6 684.27 kg,平均出酒率41.8%),其次为A1组,A2组基酒产量最低(总产酒6 405.18 kg,平均出酒率40.0%),方差分析结果表明,在4轮次发酵期内,第2~5轮不同高粱及糖化时长基酒产量均未表现出显著差异(P>0.05),4轮次基酒总产量同样未表现出显著差异。导致该现象的原因可能是酒醅发酵是一个复杂的生化过程,发酵初期糖化菌不断水解淀粉生成单糖,同时酵母菌类微生物大量增殖,随着氧气消耗酵母菌逐渐转为无氧发酵消耗单糖生成乙醇,酒醅酸度同时上升。
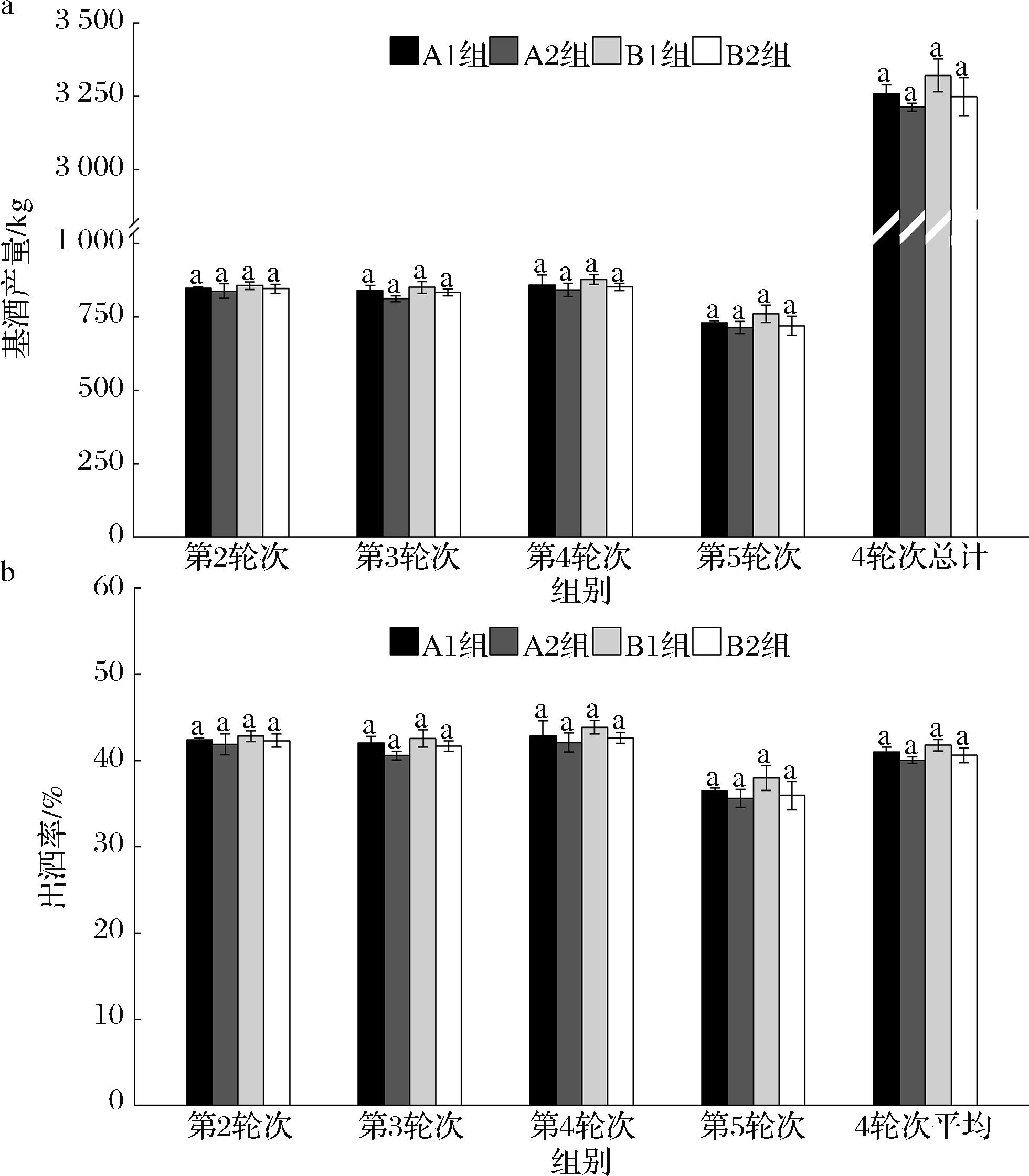
a-基酒产量;b-出酒率
图3 不同发酵轮次基酒产量
Fig.3 The distillate output of different fermentation rounds
注:不同字母代表不同处理组的差异显著性(P<0.05)(下同)。
进入中后期酵母菌类微生物活性受到抑制,转而由产酸菌与产酯菌接替发酵成为主要方式,并伴随着酸类物质与酯类物质的积累[15]。馥郁香型白酒发酵原料通过小曲添加、堆积培菌等多重糖化工艺,使粳高粱中淀粉充分水解,满足了发酵前期酵母菌类微生物发酵启动对单糖的需求,且配醅入池后糖化料中独特的糖化菌群落在发酵阶段继续糖化,同样保证了长期发酵的淀粉转化,因而在本研究中表现出不同高粱及糖化时长基酒产量的相似[16]。此外,原料中糯高粱仅占15%的比例可能也是导致产酒差异不大的原因之一。
2.4 基酒关键风味成分分析
2.4.1 不同发酵轮次基酒风味成分PCA
通过对不同发酵轮次基酒风味成分进行PCA,结果如图4示。PC1(主成分1)与PC2(主成分2)解释度分别为51.6%与23.9%,总解释度为75.5%。第2~4轮次各样本点表现出逐渐分离的趋势,第5轮次样本点与前3轮次表现出明显差异。馥郁香型白酒窖池发酵以翻醅期-第2~5轮次-压醅期为1个周期,周期内料醅配比、曲醅配比等随发酵轮次逐级降低,翻醅期最高,第2~5轮次次之,压醅期最低,酒醅淀粉含量随发酵轮次同样逐渐降低,因而在本研究中呈现出不同轮次基酒风味成分逐渐出现差异的趋势,而第5轮次为常态发酵最后轮次,酒醅淀粉含量低,且发酵时窖池环境温度相较前几轮次上升,这可能促进了发酵体系中微生物的活动代谢,进而表现出样本点的明显分离[17]。
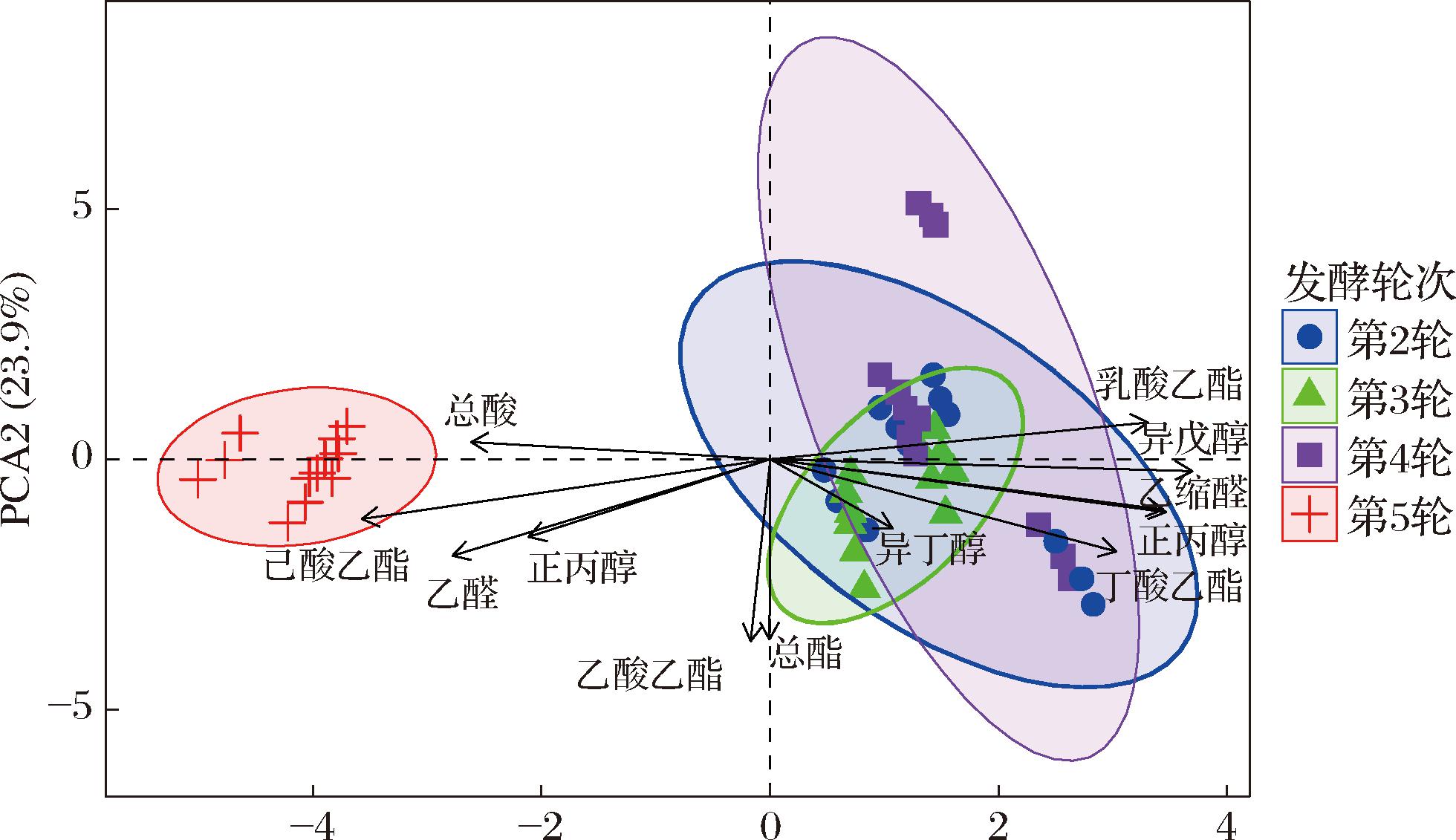
图4 基酒风味成分PCA
Fig.4 The PCA of distillate flavor ingredients
2.4.2 第2轮次不同高粱及糖化时长对基酒风味成分的影响
为进一步明确不同高粱及糖化时长对基酒风味成分的具体影响,对不同高粱及糖化时长组基酒风味成分进行双因素方差分析,并使用Mantel检验对酒醅入池理化与基酒风味成分进行相关显著性检验,结果如图5所示。不同高粱及糖化时长对基酒风味成分表现出不同的影响作用,其中总酯表现为A2组和B2组低于A1组和B1组(分别降低11.3%、18.5%),较短的糖化时长不利于酒醅中酯类物质的积累。双因素方差分析结果表明,第2轮次基酒总酸、总酯、乙酸乙酯、己酸乙酯、乳酸乙酯、乙醛、乙缩醛受不同高粱配比与糖化时长影响显著(P<0.05),醇类物质受两者影响较弱(表3)。而Mantel检验表明,在第2轮次发酵中,基酒总酸、乙酸乙酯、正丁醇、异丁醇、异戊醇、乙醛、乙缩醛与酒醅入池还原糖含量表现出极显著相关性(P<0.01),而乳酸乙酯与入池水分、酸度和淀粉含量均表现出显著相关性(P<0.01)。酒醅还原糖作为发酵微生物活动的能量来源,其初始含量不仅直接制约着酵母菌类微生物在发酵前期的增殖与发酵,同样也是发酵体系内其余微生物的直接启动能源[16,18]。不同发酵微生物通过活动代谢产生不同风味成分,微生物的活性强弱直接影响着各类风味物质的多寡,因而在研究中各风味成分表现出与酒醅还原糖的显著相关性。此外,前人研究表明,酿造原料淀粉含量高,在发酵时易导致乳酸菌利用淀粉产生大量乳酸,酒醅水分含量、酸度的高低同样直接影响着乳酸菌的活性[19],这也可能是导致基酒乳酸乙酯与酒醅淀粉等初始含量呈显著相关的原因。
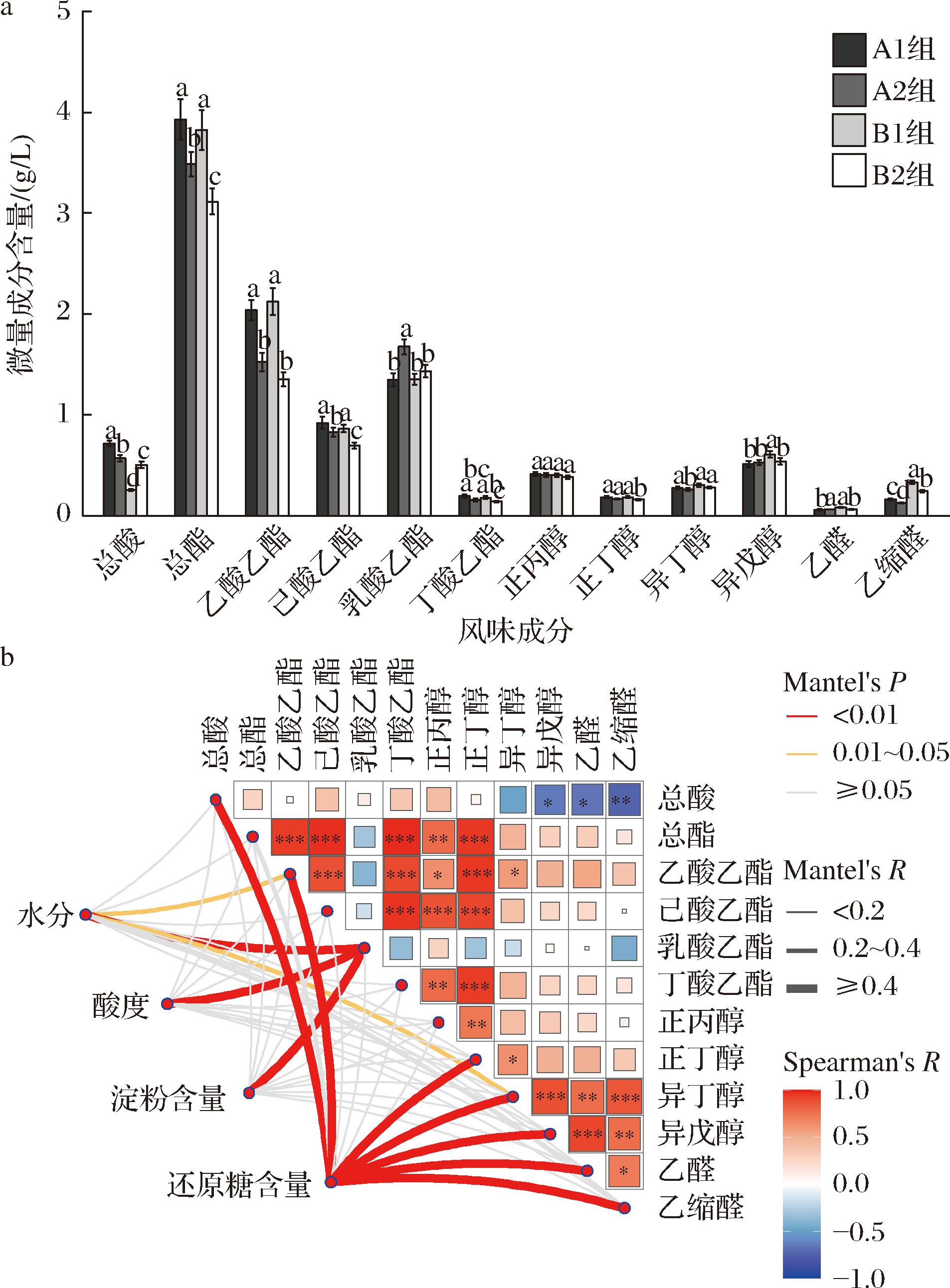
a-基酒风味成分含量;b- Mantel检验组合热图
图5 基酒风味成分与酒醅入池理化相关性分析
Fig.5 The correlation analysis of distillate flavor ingredients and initial fermented grains physicochemical matter
注:*表示P<0.05;**表示P<0.01;***表示P<0.001(下同)。
表3 不同高粱及糖化时长影响基酒风味成分的双因素方差分析
Table 3 The two-way ANOVA of different sorghum and saccharification duration affecting the distillate flavor ingredients
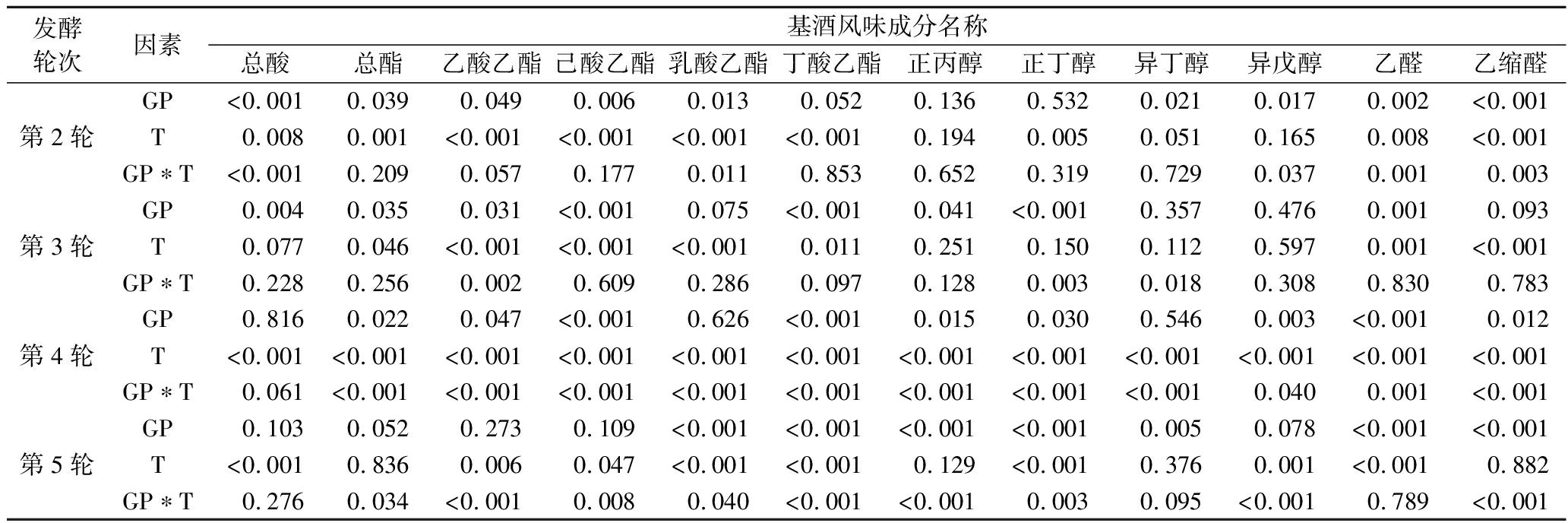
发酵轮次因素基酒风味成分名称总酸总酯乙酸乙酯己酸乙酯乳酸乙酯丁酸乙酯正丙醇正丁醇异丁醇异戊醇乙醛乙缩醛GP<0.0010.0390.0490.0060.0130.0520.1360.5320.0210.0170.002<0.001第2轮T0.0080.001<0.001<0.001<0.001<0.0010.1940.0050.0510.1650.008<0.001GP∗T<0.0010.2090.0570.1770.0110.8530.6520.3190.7290.0370.0010.003GP0.0040.0350.031<0.0010.075<0.0010.041<0.0010.3570.4760.0010.093第3轮T0.0770.046<0.001<0.001<0.0010.0110.2510.1500.1120.5970.001<0.001GP∗T0.2280.2560.0020.6090.2860.0970.1280.0030.0180.3080.8300.783GP0.8160.0220.047<0.0010.626<0.0010.0150.0300.5460.003<0.0010.012第4轮T<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001GP∗T0.061<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.0010.0400.001<0.001GP0.1030.0520.2730.109<0.001<0.001<0.001<0.0010.0050.078<0.001<0.001第5轮T<0.0010.8360.0060.047<0.001<0.0010.129<0.0010.3760.001<0.0010.882GP∗T0.2760.034<0.0010.0080.040<0.001<0.0010.0030.095<0.0010.789<0.001
2.4.3 第3轮次不同高粱及糖化时长对基酒风味成分的影响
第3轮次基酒风味成分与酒醅入池理化相关性分析如图6所示,与第2轮次不同的是,第3轮次不同高粱及糖化时长对基酒风味成分的影响减弱(表3),基酒风味成分与酒醅入池理化相关性及显著性同样呈现减少的趋势。其中,A2组和B2组基酒总酸含量高于A1组和B1组(分别提升10.1%、2.4%),而总酯含量表现为A1组最高(平均值4.21 g/L),A2组、B1组、B2组逐级降低(分别为3.79、3.77、3.64 g/L)。双因素方差分析结果表明,基酒总酸、总酯、乙酸乙酯、己酸乙酯、丁酸乙酯、正丙醇、正丁醇等风味成分受不同高粱配比影响显著(P<0.05),总酯、乙酸乙酯、己酸乙酯、乳酸乙酯、丁酸乙酯、乙醛、乙缩醛受不同糖化时长影响显著(P<0.05)。Mantel检验结果表明,己酸乙酯、乳酸乙酯、乙醛和乙缩醛与入池酸度表现出显著相关性(P<0.05),总酸、正丙醇、异丁醇和乙缩醛则与酒醅淀粉表现出显著相关性(P<0.05)。环境温度是影响窖池微生物发酵的关键因素,冷热季节酒醅中风味成分的积累表现出较大差异。结合Mantel检验结果,环境温度降低致使发酵微生物活动减弱,进而导致微生物受酒醅入池理化影响减弱,这一变化可能稀释了不同高粱及糖化时长对基酒风味成分带来的影响[20]。
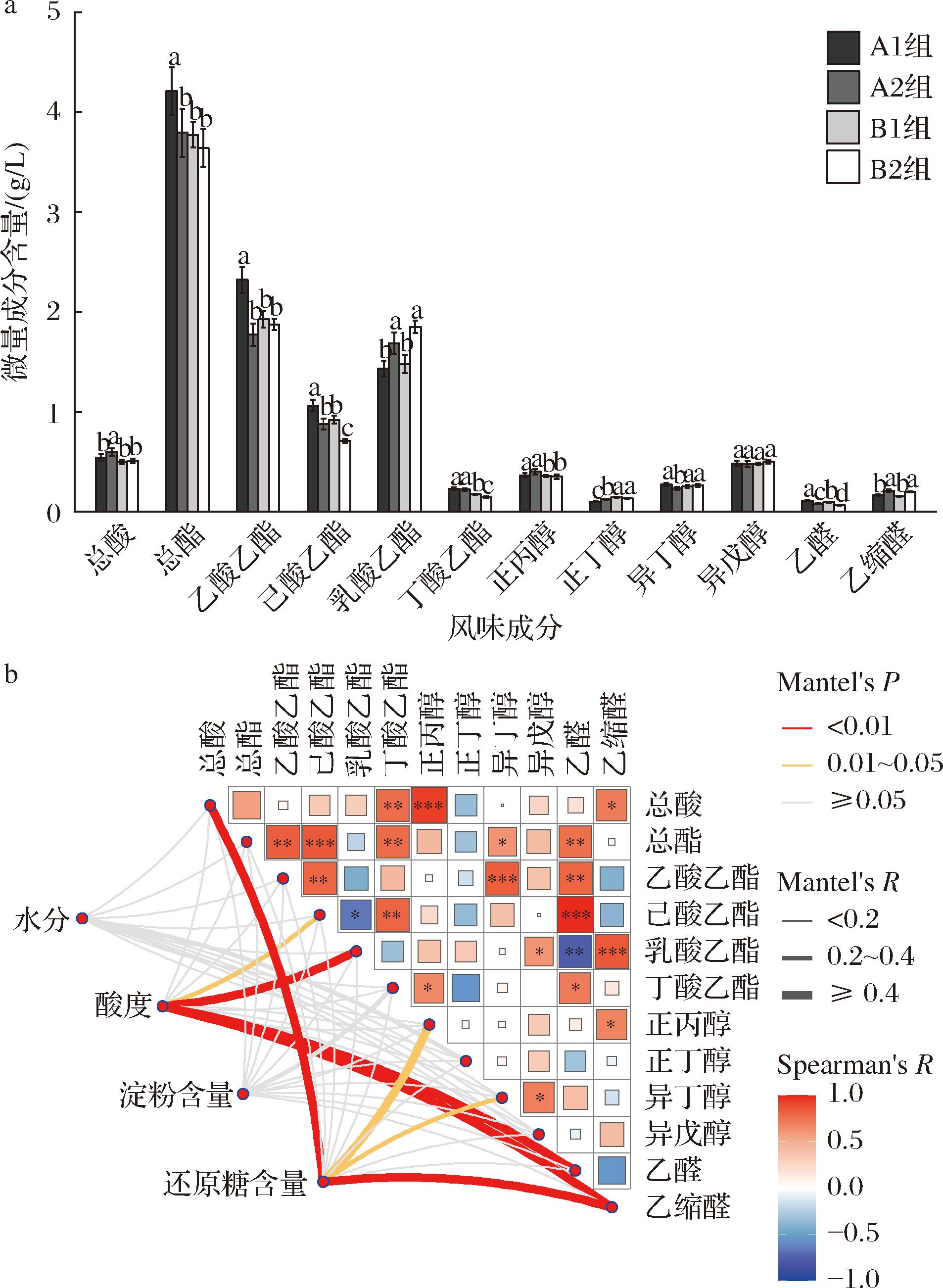
a-基酒风味成分含量;b- Mantel检验组合热图
图6 基酒风味成分与酒醅入池理化相关性分析
Fig.6 The correlation analysis of distillate flavor ingredients and initial fermented grains physicochemical matter
2.4.4 第4轮次不同高粱及糖化时长对基酒风味成分的影响
第4轮次基酒风味成分与酒醅入池理化相关性分析如图7所示,与前2轮次不同的是,发酵进入第4轮次,不同高粱及糖化时长对基酒风味成分含量的影响增强(表3),各风味成分与酒醅入池理化相关性同样增强。具体表现为A2组和B2组基酒总酸、总酯含量高于A1组和B1组(总酸提升30.7%、19.5%;总酯提升17.9%、3.4%),酯类中乙酸乙酯受不同糖化时长影响表现出显著差异(表3),A2组和B2组含量显著高于A1组和B1组(分别提升57.9%、19.2%)(P<0.001),而乳酸乙酯表现出相反的影响趋势,A2组和B2组含量显著低于A1组和B1组(分别降低34.3%、15.7%)(P<0.001),B1组基酒醇类、乙醛和乙缩醛含量均高于A1组。Mantel检验结果表明,第4轮次基酒12类风味成分与酒醅入池还原糖含量均呈现显著相关性(P<0.05),而除总酸外其余11类风味成分与酒醅入池淀粉含量同样表现出显著相关性(P<0.05),不同基酒风味成分与酒醅入池水分、酸度同样表现出显著关联。结合前人研究,酒醅淀粉含量与发酵环境温度影响着糖化菌类微生物在发酵过程的活动[21]。本研究第4轮次糖化22 h组基酒总酸、总酯含量均高于糖化44 h组,这可能是由于发酵进入第4轮次,环境温度逐渐回升,而糖化不完全组酒醅中淀粉含量更高,促进了糖化菌和产酸菌的活动,进而提升了酒醅中总酸含量,而总酯与总酸息息相关,总酸含量的上升同样促进了酯化反应的进行,进而导致总酯的积累[22]。此外,升温曲线同样表明,相较第3轮次,第4轮次酒醅升温更为迅速(图1),适宜的环境温度促进了发酵体系内微生物的增殖代谢,加速了酒醅风味成分的产生,同时也加大了微生物对初始养分含量的需求依赖,进而致使各发酵微生物与酒醅入池理化的关联增强[23]。
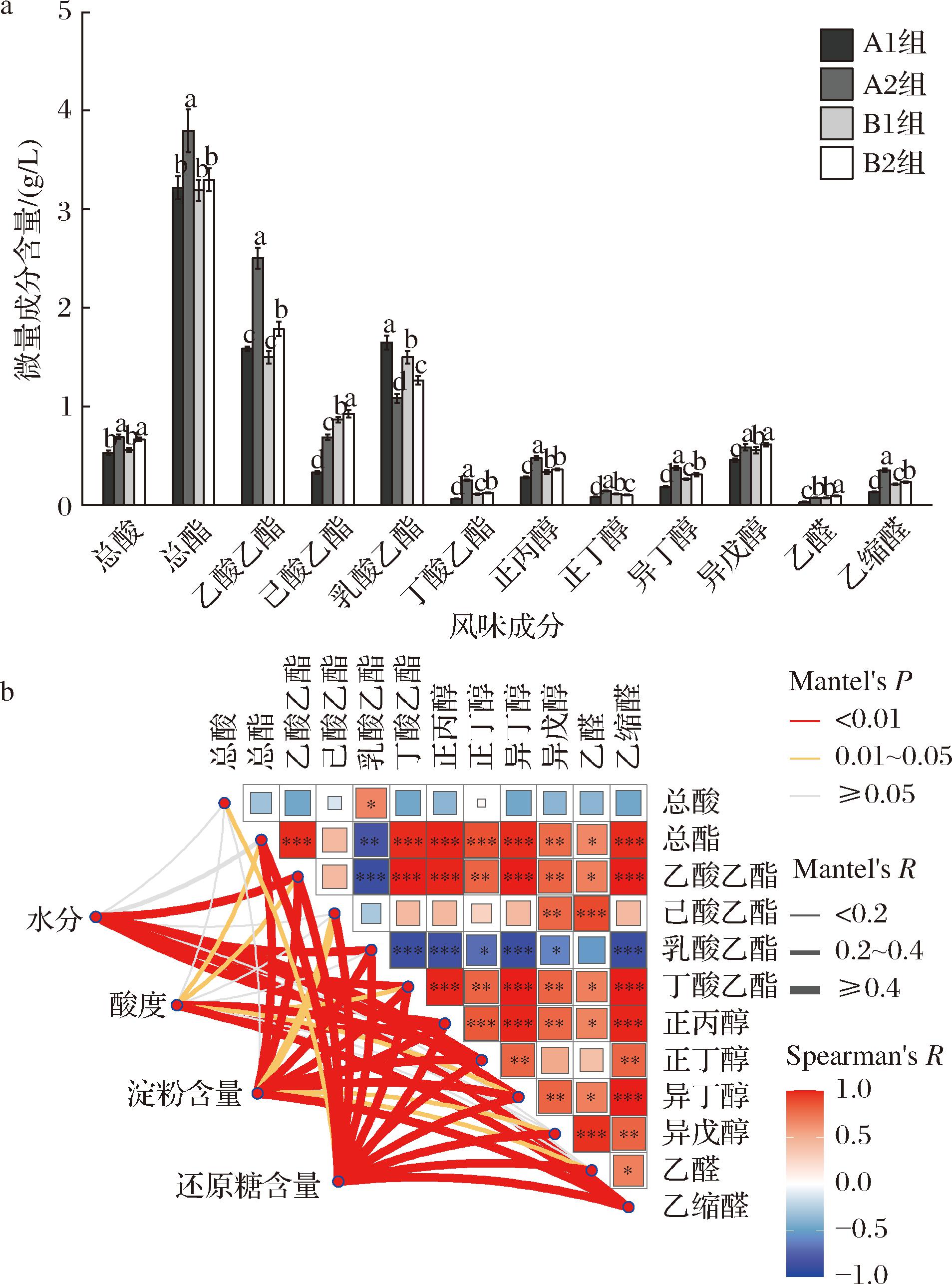
a-基酒风味成分含量;b-Mantel检验组合热图
图7 基酒风味成分与酒醅入池理化相关性分析
Fig.7 The correlation analysis of distillate flavor ingredients and initial fermented grains physicochemical matter
2.4.5 第5轮次不同高粱及糖化时长对基酒风味成分的影响
第5轮次基酒风味成分与酒醅入池理化相关性分析如图8所示,与前3个轮次不同的是,第5轮次基酒中总酸、总酯含量受不同高粱配比影响均不显著,总酸与三大酯受不同糖化时长影响显著(P<0.05)(表3)。A2组和B2组基酒总酸含量分别为0.62 g/L和0.60 g/L,较A1组和B1组分别降低18.4%和14.1%,乙酸乙酯表现出相同的变化趋势(分别降低9.8%、25.4%),而乳酸乙酯表现出相反的变化趋势(分别提升26.2%、8.3%)(图8)。Mantel检验表明,第5轮次酒醅入池淀粉和还原糖含量与不同风味成分间相关性减弱,各风味成分与入池水分间相关性消失,仅有入池酸度与己酸乙酯、乳酸乙酯、丁酸乙酯、异丁醇、乙醛和乙缩醛表现出显著相关性(P<0.05)。糯高粱中高占比的支链淀粉含量在发酵中更易被微生物利用,进而对发酵进程产生影响,但随着发酵的进行,酒醅中初始淀粉含量不断降低,这一变化可能稀释了糯高粱带来的影响[24]。此外,初始淀粉含量的降低同样会导致发酵体系整体发酵强度的降低,进而导致影响相关性减弱[25]。
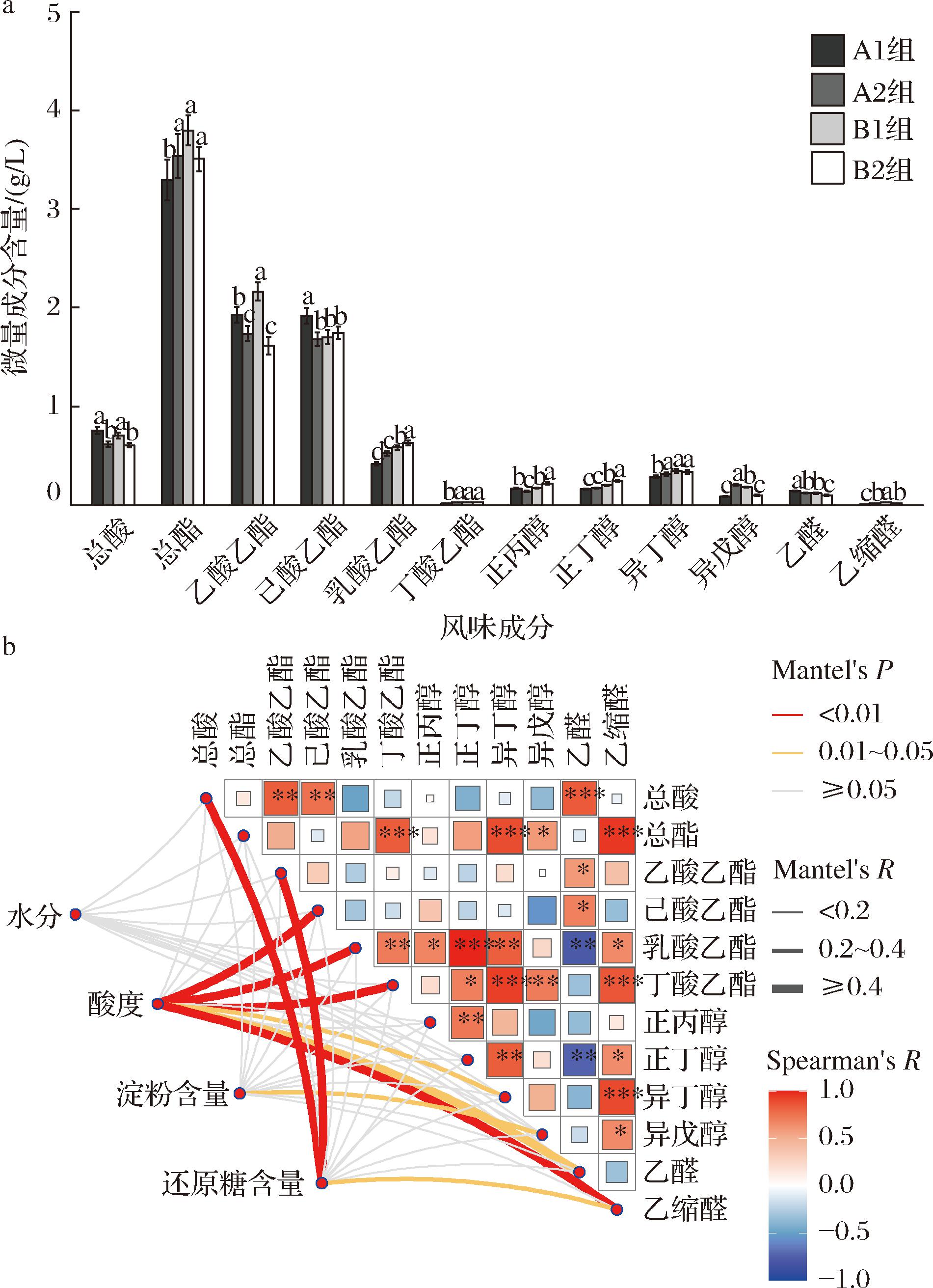
a-基酒风味成分含量;b-Mantel检验组合热图
图8 基酒风味成分与酒醅入池理化相关性分析
Fig.8 The correlation analysis of distillate flavor ingredients and initial fermented grains physicochemical matter
3 结论与讨论
在馥郁香型白酒不同发酵轮次中,改变高粱原料及糖化时长对酒醅发酵的影响存在差异,在发酵升温方面,原料添加糯高粱致使发酵节奏加快和顶温提升,而缩短糖化时长则导致升温缓慢,添加糯高粱后升温缓慢趋势缓解。在酒醅理化方面,原料添加糯高粱后酒醅水分增长与淀粉损耗均呈增加趋势,而缩短糖化时长后酒醅水分、酸度增长与淀粉损耗均减缓。在基酒产量方面,原料添加糯高粱提升了基酒产量和出酒率,但未表现出显著性,缩短糖化时长后基酒产量减少。在基酒风味成分方面,随着发酵轮次的变化,基酒风味成分间表现出差异性。在第2轮次发酵期,缩短糖化时长不利于酒醅酯类物质的积累,酒醅入池还原糖含量显著影响着酒醅总酸、除正丙醇外醇类、乙醛和乙缩醛等风味成分的形成(P<0.05)。在第3轮次发酵期,随着环境温度降低,酒醅初始理化对基酒风味成分的影响减弱,缩短糖化时长降低了基酒乙酸乙酯和己酸乙酯含量(不同高粱原料乙酸乙酯分别降低23.5%、2.7%,己酸乙酯分别降低17.2%、23.0%),提升了乳酸乙酯含量(不同高粱原料分别提升17.8%、25.0%)。在第4轮次发酵期,改变原料及糖化时长对基酒风味成分影响增大,基酒风味成分与酒醅入池理化间显著相关性增加。添加糯高粱后基酒总酸、己酸乙酯、醇类和醛类含量均上升,缩短糖化时长同样提升了基酒中总酸与总酯含量。而发酵进入第5轮次后,基酒总酸、总酯含量受高粱配比影响均不显著,缩短糖化时长显著降低了基酒中总酸和乙酸乙酯含量(P<0.05)。总而言之,原料中添加糯高粱对酒醅发酵具有积极影响,具体表现为促进发酵升温,提升酒醅产酒。而缩短糖化时长对酒醅发酵整体呈负面影响,表现为发酵升温缓慢且难以升至顶温,酒醅产酒减少等,但在第4轮次发酵中缩短糖化时长能提升总酸总酯含量,达到“降乳增己”效果。因此,对于不同发酵轮次的酒醅,应根据酒醅实际情况调整原料高粱配比和糖化时长,本研究为馥郁香型白酒多轮次发酵生产工艺优化提供了一定的参考依据。
[1] 王娜, 谌松强, 聂秋宇, 等.基于气相-离子迁移谱的酿酒高粱早期霉变判别方法研究[J].中国粮油学报, 2025, 40(2):177-185.
WANG N, CHEN S Q, NIE Q Y, et al.Early mildew discrimination method of sorghum based on gas chromatograph-ion mobility spectrometer[J].Journal of the Chinese Cereals and Oils Association, 2025, 40(2):177-185.
[2] 李亚平, 向宗府, 曹满堂, 等.白酒窖泥及其微生物与风味关联性研究进展[J].中国酿造, 2025, 44(1):6-12.LI Y P, XIANG Z F, CAO M T, et al.Research progress on pit mud and the relationship between its microorganism and Baijiu flavor[J].China Brewing, 2025, 44(1):6-12.
[3] 陈益超, 毛健, 周志磊, 等.馥郁香型白酒酿造工艺与风味研究进展[J].中国酿造, 2024, 43(7):1-6.CHEN Y C, MAO J, ZHOU Z L, et al.Research progress on brewing technology and flavor of Fuyu-flavor Baijiu[J].China Brewing, 2024, 43(7):1-6.
[4] 叶力, 谌松强, 殷红, 等.馥郁香型白酒风味与质量关系及其风味来源[J].中国酿造, 2023, 42(6):1-6.YE L, CHEN S Q, YIN H, et al.Relationship between flavor and quality of Fuyu flavor Baijiu and its flavor source[J].China Brewing, 2023, 42(6):1-6.
[5] 冯亮, 郑晓卫, 叶力, 等.高产蜜香功能菌株在馥郁香型白酒中的应用研究[J].酿酒科技, 2022(12):46-56.FENG L, ZHENG X W, YE L, et al.Application of functional strain with high yield of honey aroma substances in Fuyuxiang Baijiu[J].Liquor-Making Science &Technology, 2022(12):46-56.
[6] 刘茂柯, 田新惠, 刘成元, 等.不同品种高粱酿造浓香型白酒的香味物质组成差异及其影响因素[J].食品工业科技, 2023, 44(8):107-115.LIU M K, TIAN X H, LIU C Y, et al.Differences in the composition of flavor compounds of Nongxiangxing Baijiu brewed from different varieties of sorghum and its influencing factors[J].Science and Technology of Food Industry, 2023, 44(8):107-115.
[7] 田殿梅, 霍丹群, 张良, 等.3种不同品种高粱发酵酒糟及基酒品质的差异[J].食品与发酵工业, 2013, 39(7):74-78.TIAN D M, HUO D Q, ZHANG L, et al.Quality differences of grains and base liquor from three different species of sorghum’s fermentation[J].Food and Fermentation Industries, 2013, 39(7):74-78.
[8] 赵玉杰, 靳光远, 唐群勇, 等.基于热量平衡模型的大曲发酵升温机理研究[J].食品与发酵工业, 2024, 50(14):18-25.ZHAO Y J, JIN G Y, TANG Q Y, et al.The mechanism of heat transfer during Daqu fermentation based on heat balance modeling[J].Food and Fermentation Industries, 2024, 50(14):18-25.
[9] 杨中元, 祝辉, 王凝, 等.不同糟龄入窖糟醅酸度对浓香型白酒风味的影响[J].食品与发酵工业, 2025,51(19):41-47;48.YANG Z Y, ZHU H, WANG N, et al.Impact of different age distillery mash acidity on Nongxiang Baijiu flavor[J].Food and Fermentation Industries, 2025,51(19):41-47;48.
[10] 李媛媛, 邓杰, 郑若欣, 等.两种高粱的酿造特性对比研究[J].食品研究与开发, 2020, 41(15):40-45.LI Y Y, DENG J, ZHENG R X, et al.Comparative study on brewing characteristics of two kinds of sorghum[J].Food Research and Development, 2020, 41(15):40-45.
[11] 高银涛, 何璇, 余博文, 等.白酒固态双边发酵糖化机理及其对发酵过程的影响[J].食品与发酵工业, 2021, 47(13):92-97.GAO Y T, HE X, YU B W, et al.Saccharification mechanism of solid-state fermentation of Chinese Baijiu and its influence on fermentation process[J].Food and Fermentation Industries, 2021, 47(13):92-97.
[12] 杨明, 朱维民, 陈香梅, 等.不同生产工艺对酱香型白酒酸酯变化的影响研究[J].中国酿造, 2024, 43(12):149-154.YANG M, ZHU W M, CHEN X M, et al.Effect of different production techniques on the changes in acid and ester in sauce-flavor Baijiu[J].China Brewing, 2024, 43(12):149-154.
[13] 王乐, 魏功, 郭逸臻, 等.北方浓香型白酒发酵过程中不同空间层次糟醅理化指标及风味物质的变化[J].中国酿造, 2024, 43(3):63-71.WANG L, WEI G, GUO Y Z, et al.Changes of physicochemical indexes and flavor substances of fermented grains at different spatial levels during Northern strong-flavor Baijiu fermentation[J].China Brewing, 2024, 43(3):63-71.
[14] 蒋英丽, 沈毅, 程伟, 等.不同品种高粱应用于酱香型白酒的生产研究[J].食品与发酵工业, 2023, 49(13):93-99.JIANG Y L, SHEN Y, CHENG W, et al.Research on different varieties of sorghum used in the production of sauce-flavor Baijiu[J].Food and Fermentation Industries, 2023, 49(13):93-99.
[15] 向港兴. 浓香型白酒酿造过程中酒醅微生物群落演替及影响因素研究[D].自贡:四川轻化工大学, 2022.XIANG G X.Study on microbial community succession and influencing factors of Jiupei in brewing of Nongxiangxing Baijiu[D].Zigong:Sichuan University of Science &Engineering, 2022.
[16] 黄治国, 侯海波, 罗惠波, 等.浓香型白酒酒醅发酵过程中淀粉和还原糖的变化规律研究[J].中国酿造, 2012, 31(7):107-110.HUANG Z G, HOU H B, LUO H B, et al.Changes of starch and reducing sugars of fermented grains in fermentation of strong-flavor liquor[J].China Brewing, 2012, 31(7):107-110.
[17] 付庆凯, 陈帆, 孟廷淋, 等.酱香型白酒不同轮次发酵酒醅差异性研究[J].食品与发酵工业, 2025,51(18):322-329.FU Q K, CHEN F, MENG T L, et al.Study on differences in fermented grains across different fermentation rounds of Jiangxiangxing Baijiu[J].Food and Fermentation Industries, 2025,51(18):322-329.
[18] 王鹏, 吴群, 徐岩.中国白酒发酵过程中的核心微生物群及其与环境因子的关系[J].微生物学报, 2018, 58(1):142-153.WANG P, WU Q, XU Y.Core microbiota in Chinese liquor fermentation and associations with environmental factors[J].Acta Microbiologica Sinica, 2018, 58(1):142-153.
[19] 杨荣, 华进, 周亚宾.白酒酿造过程中乳酸乙酯产生机理及“降乳”技术研究进展[J].食品工业科技, 2024, 45(20):398-406.YANG R, HUA J, ZHOU Y B.Progress in the research of the mechanism of ethyl lactate production and “ethyl lactate reduction” techniques in the Baijiu brewing process[J].Science and Technology of Food Industry, 2024, 45(20):398-406.
[20] 李慧. 不同生产季汾香型白酒酿造微生物群落及其功能差异解析[D].太原:山西大学, 2024.LI H.Analysis of brewing microbial communities and their functional differences of Fen flavor liquor in different production seasons[D].Taiyuan:Shanxi University, 2024.
[21] YIN X, YOSHIZAKI Y, IKENAGA M, et al.Manufactural impact of the solid-state saccharification process in rice-flavor Baijiu production[J].Journal of Bioscience and Bioengineering, 2020, 129(3):315-321.
[22] 王涛, 胡先强, 游玲, 等.浓香型白酒酵母对发酵糟醅中乙醇及主要酸、酯生成的影响[J].食品与发酵工业, 2015, 41(8):18-22.WANG T, HU X Q, YOU L, et al.Contribution of yeasts isolated from Chinese strong-flavored liquor to the production of ethanol,major acid and ester in fermentative grain[J].Food and Fermentation Industries, 2015, 41(8):18-22.
[23] 黄亮. 温度对白酒固态发酵的影响研究[D].自贡:四川轻化工大学, 2022.HUANG L.Effect of temperature on solid-state fermentation of Baijiu[D].Zigong:Sichuan University of Science &Engineering, 2022.
[24] 钟敏, 张健.原料糯高粱对酱香型白酒品质影响的研究现状[J].中国酿造, 2022, 41(1):32-36.ZHONG M, ZHANG J.Research status of effect of raw glutinous sorghum on quality of sauce-flavor Baijiu[J].China Brewing, 2022, 41(1):32-36.
[25] 郭世鑫, 李细芬, 卢延想, 等.酱香型白酒轮次酒的醛类物质与对应出窖糟醅的理化指标相关性研究[J].中国酿造, 2024, 43(6):151-155.GUO S X, LI X F, LU Y X, et al.Correlation between the aldehydes of the sauce-flavor Baijiu in different rounds and the corresponding physicochemical indexes of the pit-unloading fermented grains[J].China Brewing, 2024, 43(6):151-155.