尿苷二磷酸糖基转移酶[uridine diphosphate(UDP)-glycosyltransferases,UGTs]作为糖基转移酶GT1家族的核心成员,可催化UDP-糖上的糖残基转移到特定的受体,在植物的次生代谢过程、激素调控以及逆境胁迫响应等多种途径中具有重要作用。UGTs主要以UDP-葡萄糖、UDP-半乳糖、UDP-鼠李糖、UDP-木糖等UDP-糖作为糖基供体,对类黄酮、酚酸、萜类等次生代谢物进行糖基化修饰,同时也参与生长素、脱落酸、细胞分裂素、水杨酸等植物激素的糖基化反应。UGTs可在大肠杆菌、酵母等微生物体系中实现异源表达,目前已被广泛用于甜菊糖苷、人参皂苷、积雪草苷、黄芩苷、柚皮苷、黄芪苷Ⅳ、红景天苷等糖苷类化合物的生物合成过程[1]。
红景天苷和淫羊藿次苷D2是酪醇的2种葡萄糖基化产物:红景天苷由酪醇的醇羟基糖基化形成,因抗疲劳、抗衰老和抗癌症等功效广泛应用于食品、医药和化妆品领域;淫羊藿次苷D2则由酪醇酚羟基糖基化形成,具有抑制血管紧张素转换酶和杀伤白血病癌细胞的药理活性[2-5]。相较于传统的植物提取或化学合成方法,UGTs介导的红景天苷和淫羊藿次苷D2的生物合成方法具有成本低、效率高、可持续的优点,展现出良好的应用前景[6]。然而,受底物糖基化位点多样性及酶自身结构差异的影响,不同UGTs在对酪醇进行糖基化时,通常表现出较差的区域选择性,增加了产物红景天苷与淫羊藿次苷D2分离的难度[7-8]。利用蛋白质工程实现UGTs的区域选择性改造逐渐受到关注。研究者针对红景天来源的RrUGT3,通过晶体结构解析、定点突变、分子动力学模拟、伞形采样及量子力学/分子力学计算等多手段结合,提出Ω-1环的“开放”与“关闭”构象是实现该酶对底物区域选择性的基础[9];基于定向进化发现的loop环区域对活性的影响,展开loop区的定点饱和突变,实现地衣芽孢杆菌来源的UGTBL1对天然酚类化合物的区域选择性改造[10];此外通过自由能驱动的口袋重塑以及通道工程,UGTBL1的区域选择性也得到了有效改变[11]。虽然活性中心及通道被证明是改变UGTs区域选择性的热点结构,但实现严格的区域选择性切换,仍有较大难度,需要继续深入了解区域选择性与结构关系,找到影响区域选择性的关键因素。
本研究对不同来源可催化酪醇葡萄糖基化的UGTs展开序列与结构分析,结合系统发育分析与分子动力学模拟分析,探究不同区域选择性UGTs的底物动态构象差异;进一步选择具有较好催化能力的拟南芥来源UGT85A1作为实验对象,重塑其关键催化残基周围氨基酸,破坏其严格区域选择性,进而明确底物构象在影响UGT85A1酪醇区域选择性的关键作用,为UGTs家族酶的区域选择性机制解析提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 菌体、质粒及引物
选择大肠杆菌(Escherichia coli)BL21(DE3)作为宿主菌株,pET-28a(+)作为表达质粒。菌株及质粒均由本实验室提供。
本文使用的引物如表1所示。
表1 本研究使用的引物
Table 1 Primers used in this study

突变子名称正/反向碱基序列(5′-3′)Y19SFGTGTTCCTAGCCCGGCGCAGRTGCGCCGGGCTAGGAACACAC128FFCGATGGGTTTATGTCTTTCACCRAAAGACATAAACCCATCGCTCAT148PFTCTTCTGGCCGACCAGCGGCRCCGCTGGTCGGCCAGAAGAGQ22MFTCCTTATCCGGCGATGGGTCRGTTAATATGACCCATCGCCGI25LFGCGCAGGGTCATCTGAACCCGRCATCATCGGGTTCAGATGACCN26IFGCAGGGTCATATTATTCCGATGRACACGCATCATCGGAATAATAT
注:F代表Forward(正向),R代表Reverse(反向)。
1.1.2 试剂与培养基
卡那霉素(AR),生工生物工程(上海)股份有限公司;质粒小提试剂盒,北京全式金生物技术股份有限公司;酵母粉(BR)、胰蛋白胨(BR),安琪酵母股份有限公司;琼脂粉(BR)、氯化钠(AR)、三羟甲基氨基甲烷(Tris,AR)、盐酸(AR)、异丙基-β-D-硫代半乳糖苷(isopropyl-beta-D-thiogalactopyranoside,IPTG,BR),上海阿拉丁生化科技股份有限公司;酪醇(AR)、尿苷二磷酸葡萄糖[(uridine diphosphate glucose, UDP-Glc),AR]、红景天苷(AR),上海源叶生物科技有限公司;淫羊藿次苷 D2(AR),云南西力生物技术股份有限公司。
LB培养基(g/L):胰蛋白胨10.0,酵母粉5.0,NaCl 10.0,琼脂(固体培养基)20.0,115 ℃灭菌20 min。
1.2 仪器与设备
H4-20K台式高速离心机,湖南可成仪器设备有限公司;Himac715RE冷冻离心机,日立科学仪器(北京)有限公司;Q5000紫外-可见光分光光度计,北京鼎国昌盛生物技术有限责任公司;JY92-IIDN超声波细胞粉碎机,宁波新芝生物科技股份有限公司;SPARK多功能酶标仪,帝肯(上海)贸易有限公司;1260 infinity Ⅱ高效液相色谱仪,安捷伦科技(中国)有限公司。
1.3 实验方法
1.3.1 系统发育分析
使用MAFFT软件对前期筛选所得的UGTs氨基酸序列展开多序列比对。将序列比对结果提交至IQ-TREE软件,构建UGTs的系统发育树[12]。使用iTOL网站(https://itol.embl.de)完成系统发育树的结构可视化。
1.3.2 UGTs结构及功能预测
使用AlphaFold3软件完成UGTs的三维结构预测,以及与底物酪醇的分子对接[13]。将目标UGTs的氨基酸序列与底物酪醇的SMILES号共同提交至AlphaFold3软件,批量获取对接结果文件。通过文件中的“ranking_score”分值评价结果置信度。使用PyMOL软件完成对接结果的可视化与残基距离计算。通过Discovery Studio软件进行底物与附近氨基酸的相互作用分析。
1.3.3 分子动力学模拟
使用Amber24软件对底物分子对接结果展开40 ns的分子动力学模拟[14]。分别设定蛋白和底物的力场为ff14SB和GAFF,蛋白配体溶剂盒选择TIP3P,蛋白与盒子的距离设定为12 Å。
模拟过程首先完成小分子电荷计算检测以及蛋白去氢,使用LEaP整理体系参数并生成蛋白及小分子的拓扑文件;随后对溶剂分子展开10 000步的能量优化,前5 000步采用最陡梯度法,后5 000步采用共轭梯度法;最后在150 000步内将体系升温至303 K,平衡40 ns实现体系能量收敛。
使用Amber软件包的CPPTRAJ模块计算分子动力学模拟过程中蛋白质的均方根偏差(root mean square deviation,RMSD)与均方根波动(root mean square fluctuation,RMSF)、获取轨迹动画、计算氨基酸残基与配体分子距离。
1.3.4 重组菌株的构建
拟南芥(Arabidopsis thaliana)来源的糖基转移酶基因UGT85A1(NCBI登录号:NP_173656.1)委托康为医学检验实验室(泰州)有限公司优化并合成。质粒载体为pET28a(+),载体抗性为卡那霉素抗性,选用EcoRⅠ和XhoⅠ作为单一限制性酶切位点。
向质粒干粉中加入40 μL无菌水,所得溶液离心后吸取10 μL上清液,转化至BL-21感受态细胞。挑取卡那霉素抗性平板上的菌落进行测序验证,保证UGT85A1基因成功导入E.coli BL21(DE3)细胞中构成阳性转化子,获得的重组质粒图谱如图1所示。将所得菌株与50%(质量分数)甘油按1∶1(质量比)混合冻藏至-70 ℃冰箱。
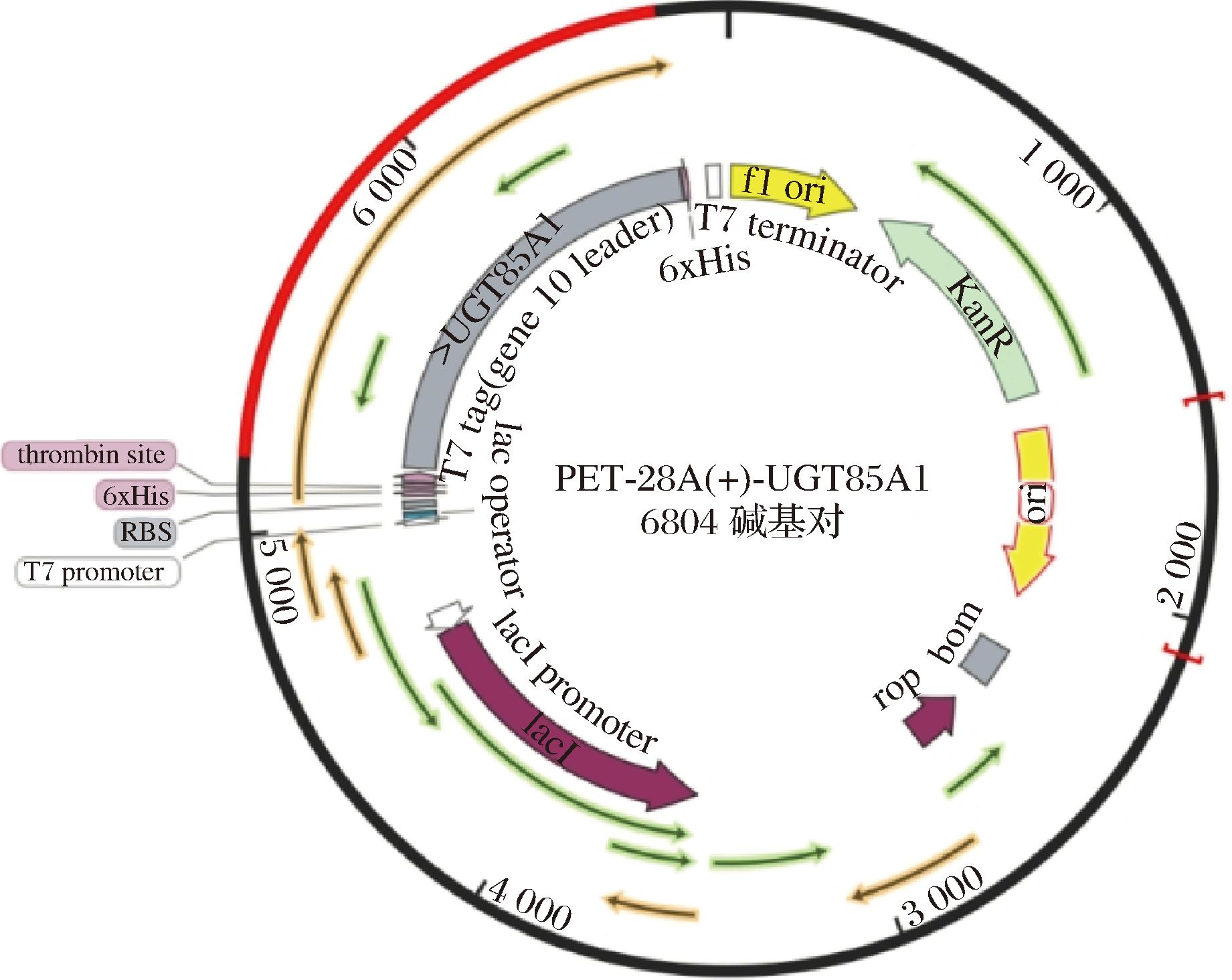
图1 pET28a(+)-UGT85A1重组质粒图谱
Fig.1 pET28a(+)-UGT85A1 recombinant plasmid map
1.3.5 基因克隆及定点突变
使用质粒小提试剂盒提取质粒pET28a(+)-UGT85A1。利用紫外-可见光分光光度计检测产物浓度后,将质粒浓度稀释到100 ng/μL。
通过全质粒PCR扩增构建突变子质粒,反应体系和扩增程序分别如表2和表3所示。
表2 PCR反应体系
Table 2 PCR reaction system

体系成分体积/μL2×Super Pfu mix10上游引物1下游引物1UGT85A1-pET28a模板1ddH2O10
表3 PCR反应程序
Table 3 PCR reaction procedure
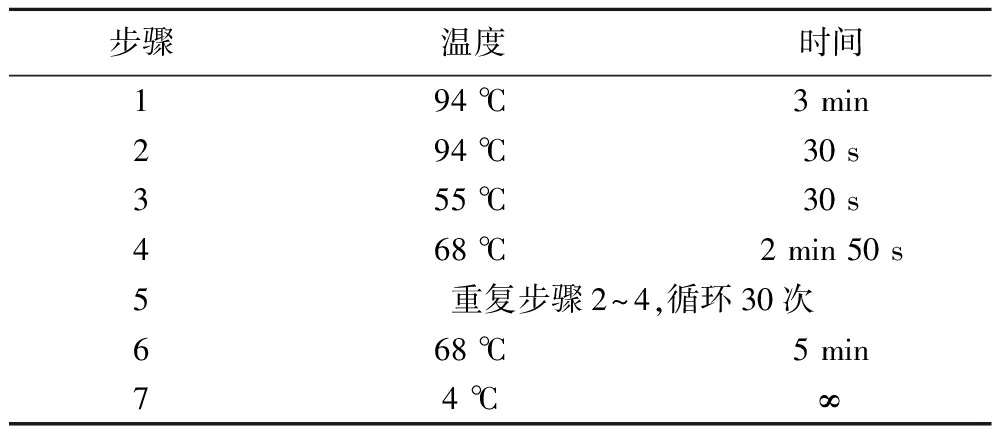
步骤温度时间194 ℃3 min294 ℃30 s355 ℃30 s468 ℃2 min 50 s5重复步骤2~4,循环30次668 ℃5 min74 ℃∞
扩增产物经DpnⅠ消化30 min后转化BL-21感受态细胞。加入1 mL新鲜LB培养基,在37 ℃,200 r/min下进行1.5 h的后培养。后培养所得菌液经12 000 r/min离心1 min,沉淀涂布LB抗性平板,37 ℃过夜培养。次日挑取单菌落于20 mL含50 μg/mL卡那霉素的LB液体培养基中,培养至菌液明显浑浊,提交测序验证后与50%甘油按1∶1冻藏至-70 ℃冰箱。
1.3.6 基因诱导表达
吸取30 μL突变子菌液接种至20 mL含50 μg/mL卡那霉素的LB液体培养基中,于37 ℃,200 r/min培养12 h作为种子液。吸取1 mL种子液接种至50 mL含50 μg/mL卡那霉素的LB液体培养基中,37 ℃,200 r/min培养至OD600nm值达到0.6~0.8,加入0.1 mmol/L IPTG,降低温度至16 ℃诱导蛋白表达24 h。发酵结束后8 000 r/min离心10 min收集菌体。
离心所得菌体用3 mL 50 mmol/L Tris-HCl(pH 8.0)重悬,超声破碎5 min(破碎2 s,停止2 s,总时间10 min)。吸取1 mL菌体破碎液,4 ℃,12 000 r/min离心5 min。丢弃不溶性颗粒,得到上清液过0.45 μm滤膜,通过SDS-PAGE分析目标蛋白表达情况。将成功表达的粗酶液稀释至蛋白浓度为3 g/L,于4 ℃冰箱保存。
1.3.7 UGTs突变子区域选择性验证
在100 μL的反应混合物中,含有50 mmol/L Tris-HCl(pH 8.0)、5 mmol/L酪醇、10 mmol/L UDP-Glc和50 μL蛋白质量浓度为3 g/L的粗酶液。反应在30 ℃下孵育2 h,加入100 μL纯乙腈终止反应。
使用高效液相色谱法(high performance liquid chromatograph, HPLC)检测反应液中底物及产物的含量。样品使用Symmetry C18色谱柱(4.6 mm×250 mm,5 μm;Waters, Ireland)进行定量。流动相为水(A)和乙腈(B)。流速设定为1 mL/min。使用紫外检测器在272 nm波长下检测底物及产物的吸光度。HPLC程序如下:30% B:0~2 min;30%~70% B:2~3 min;30% B:3~6 min;70%~30% B:6~7 min;30% B:7~12 min。
2 结果与分析
2.1 催化酪醇葡萄糖基化UGTs的区域选择性差异
通过文献调研,共统计得到13种对酪醇具有催化活性的UGTs,其名称、来源及其区域选择性等信息如表4所示。13种糖基转移酶中,除Bl-YjiC、UGTBL1来自地衣芽孢杆菌,Bs-PUGT来自枯草芽孢杆菌外,其余10种UGTs均为植物来源。
表4 不同来源可催化酪醇葡萄糖基化的UGTs
Table 4 UGTs from different sources that can catalyze the glucosylation of tyrosol
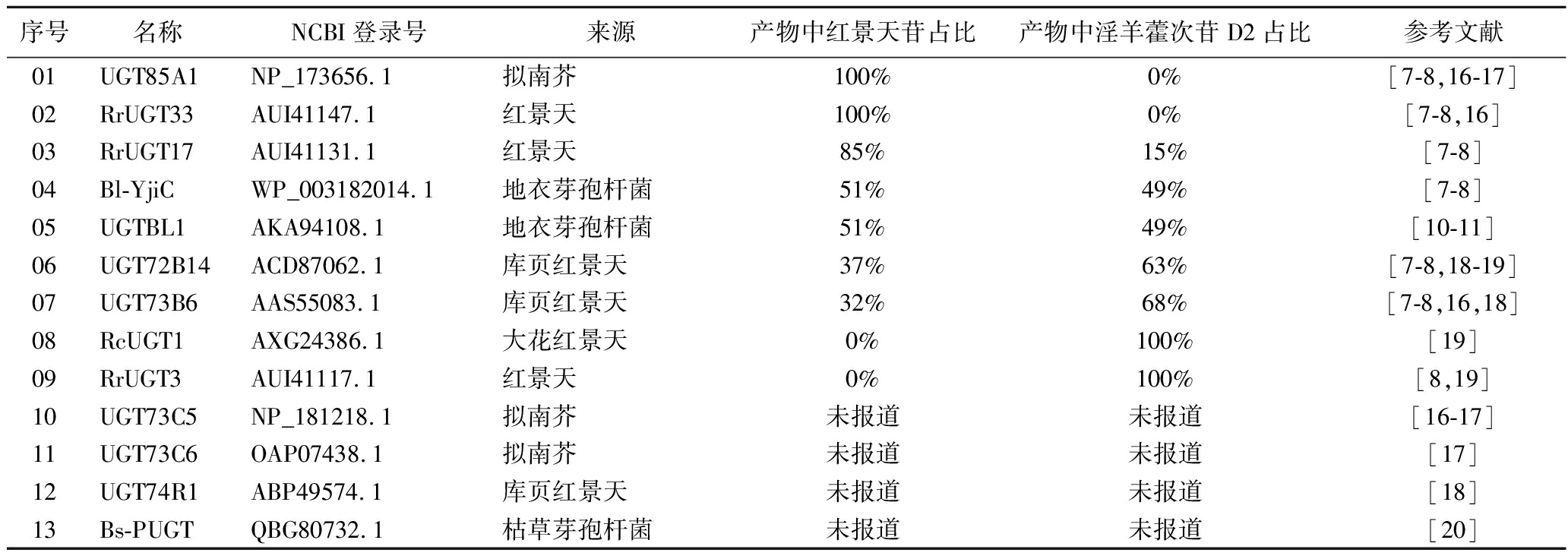
序号名称NCBI登录号来源产物中红景天苷占比产物中淫羊藿次苷D2占比参考文献01UGT85A1NP_173656.1拟南芥100%0%[7-8,16-17]02RrUGT33AUI41147.1红景天100%0%[7-8,16]03RrUGT17AUI41131.1红景天85%15%[7-8]04Bl-YjiCWP_003182014.1地衣芽孢杆菌51%49%[7-8]05UGTBL1AKA94108.1地衣芽孢杆菌51%49%[10-11]06UGT72B14ACD87062.1库页红景天37%63%[7-8,18-19]07UGT73B6AAS55083.1库页红景天32%68%[7-8,16,18]08RcUGT1AXG24386.1大花红景天0%100%[19]09RrUGT3AUI41117.1红景天0%100%[8,19]10UGT73C5NP_181218.1拟南芥未报道未报道[16-17]11UGT73C6OAP07438.1拟南芥未报道未报道[17]12UGT74R1ABP49574.1库页红景天未报道未报道[18]13Bs-PUGTQBG80732.1枯草芽孢杆菌未报道未报道[20]
酪醇在发生葡萄糖基化的过程中通常形成2种产物:当醇羟基与UDP-Glc的半缩醛羟基发生缩合反应时,其糖基化产物为红景天苷;当芳环上的酚羟基发生缩合反应时,产物为淫羊藿次苷D2(图2)。不同来源UGTs对酪醇展现出不同的区域选择性:UGT85A1和RrUGT33表现出严格的底物区域选择性,可催化酪醇专一合成红景天苷;同样地,RcUGT1和RrUGT3可催化酪醇专一合成淫羊藿次苷D2;UGT73B6、RrUGT17、UGT72B14、Bl-YjiC和UGTBL1在以酪醇为底物时,则表现出较低的底物区域选择性,其催化产物同时包含红景天苷和淫羊藿次苷D2;UGT73C5、UGT73C6、UGT74R1、Bs-PUGT对酪醇的区域选择性未在文献中报道。
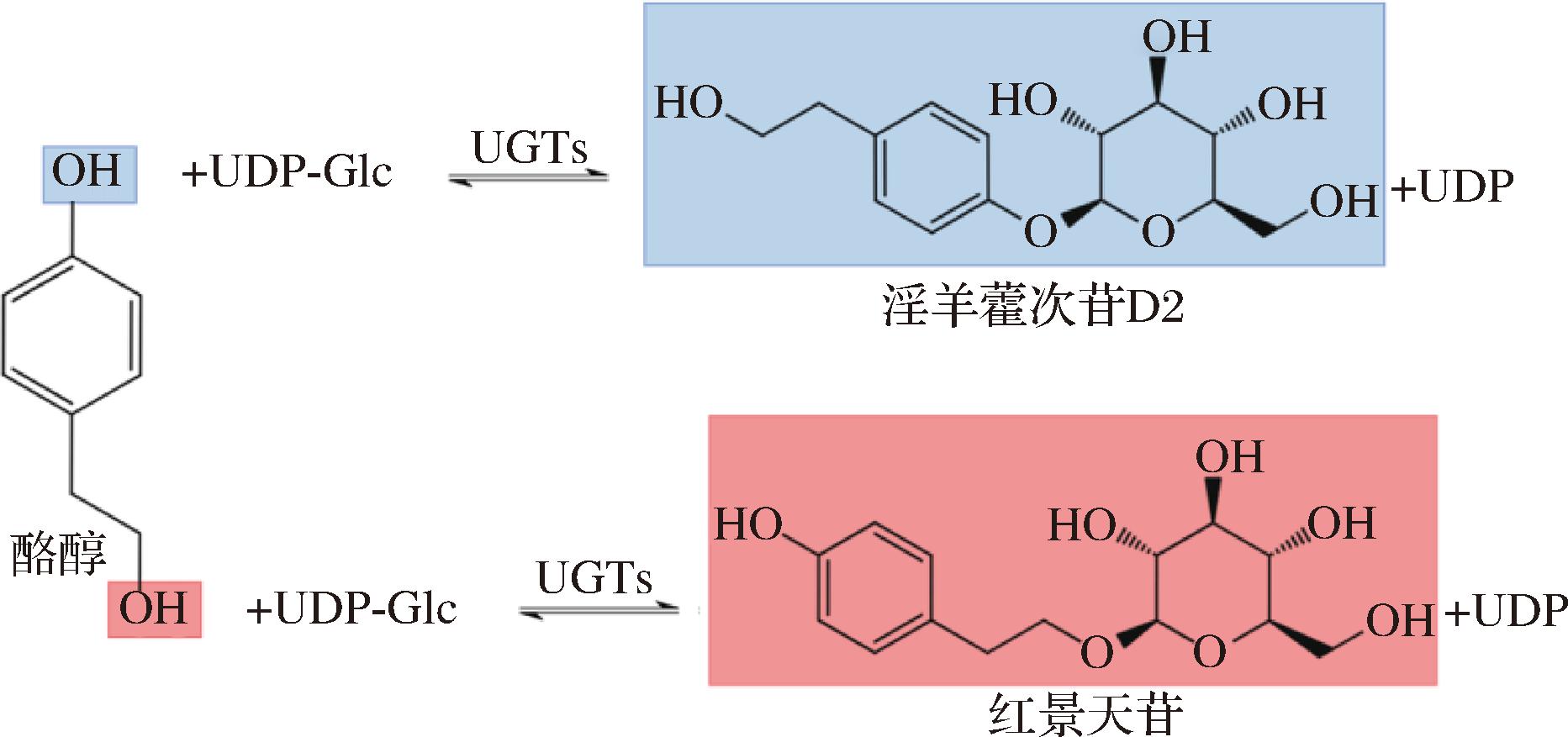
图2 酪醇的葡萄糖基化
Fig.2 Glucosylation of tyrosol
序列比对结果显示,13种UGTs关键催化残基组氨酸和天冬氨酸位点高度保守(图3-a)。在这些UGTs的催化过程中,保守的组氨酸残基负责受体底物的质子化,以便糖供体展开亲核攻击,而天冬氨酸则作为辅助残基,协助质子的转移[15]。系统发育树显示,植物来源的UGTs的形成了多个分支,且功能分化较为多样。相比之下,细菌来源的Bl-YjiC、UGTBL1和Bs-PUGT单独聚集成簇,表明它们在进化上具有相近的亲缘关系(图3-b)。
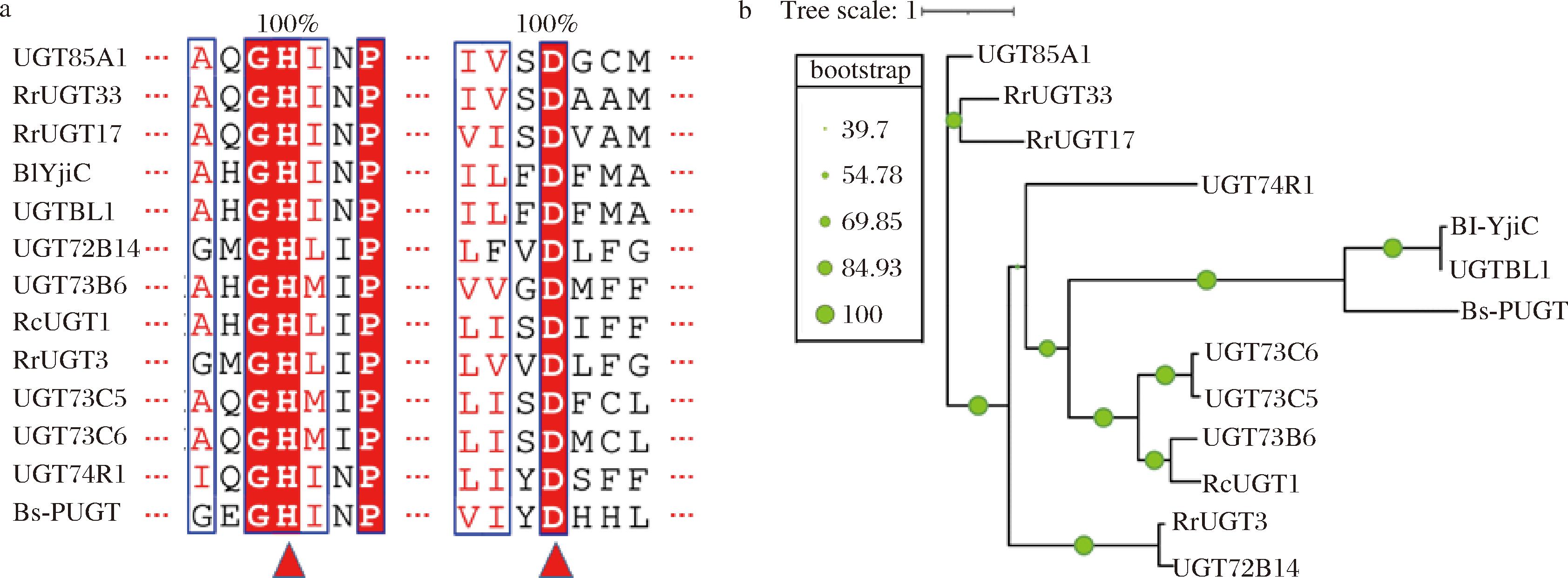
a-13种UGTs的催化残基对His-Asp;b-UGTs的系统发育树
图3 13种UGTs的序列分析及进化关系
Fig.3 Sequence analysis and evolutionary relationships of 13 UGTs
2.2 酪醇选择性不同的UGTs的结构分析
选取了8种已明确酪醇区域选择性情况的UGTs进一步展开结构-选择性分析,包括2种专一催化酪醇合成红景天苷的UGTs(UGT85A1和 RrUGT33)、2种专一催化酪醇合成淫羊藿次苷D2的UGTs(RrUGT3和RcUGT1),以及4种区域选择性较差的UGTs,其可同时催化合成红景天苷和淫羊藿次苷D2 (RrUGT17、Bl-YjiC、UGT72B14和UGT73B6)。对于具有严格区域选择性的UGTs,其底物酪醇的2个糖基化位点与催化残基组氨酸的距离更远,如具有严格酚羟基选择性的RcUGT1中,2个羟基到催化组氨酸的距离之差可达到6.1 Å,这可能导致底物构象翻转过程中,较远羟基即使翻转也难以达到催化残基的有效催化距离内而被糖基化;而区域选择性较差的UGTs中(RrUGT17、Bl-YjiC、UGT72B14和UGT73B6),所述距离之差均位于2 Å附近,底物构象翻转时酚羟基与醇羟基更易于翻转到催化残基附近而被糖基化(图4-a)。底物与UGTs氢键相互作用网络分析显示,具有严格区域选择性的UGTs与底物酪醇之间的氢键数量减少,底物与酶之间的相互作用力减弱;而区域选择性较差的UGTs与底物间的相互作用力更强(图4-b)。
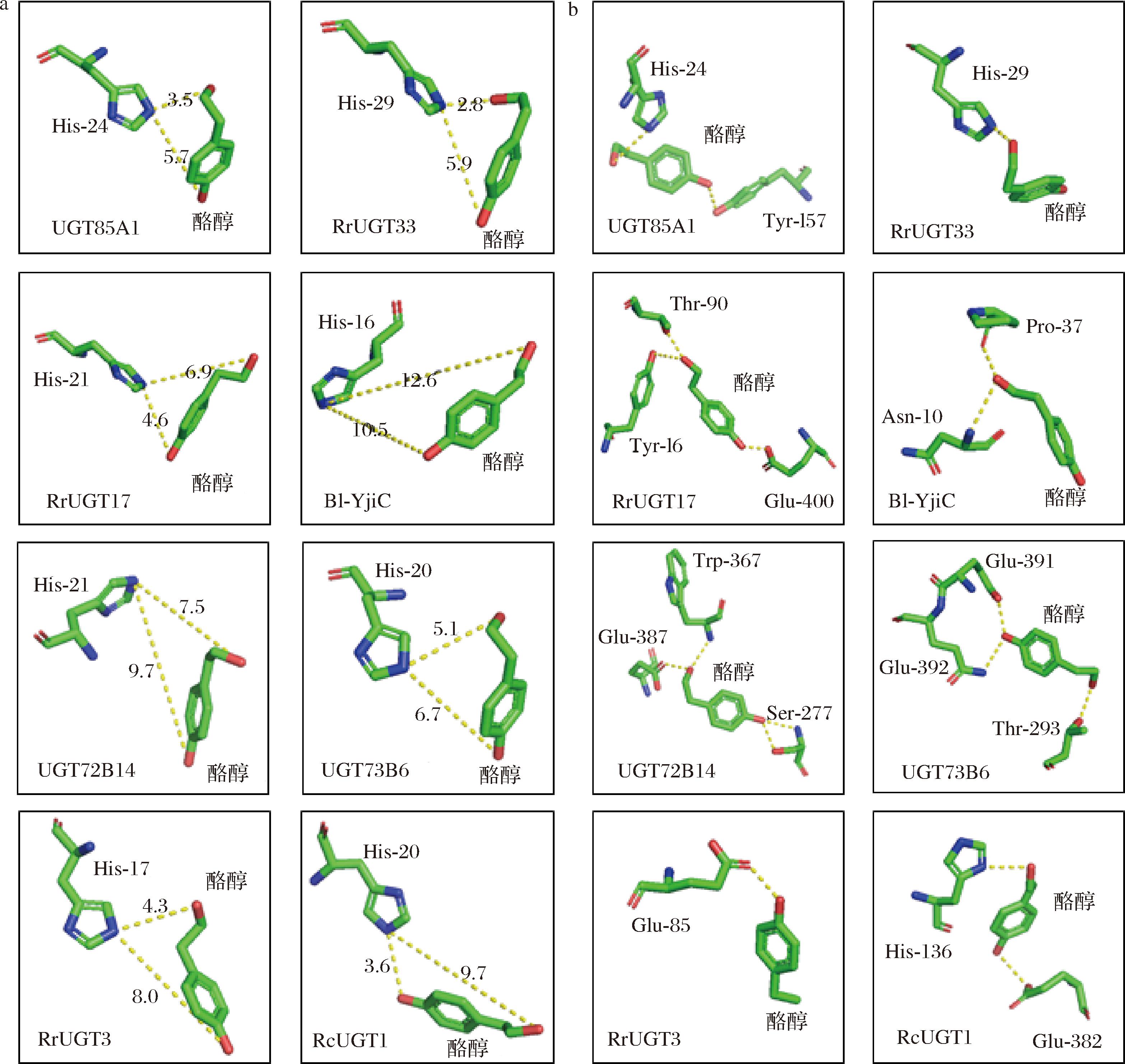
a-UGTs催化残基与酪醇酚/醇羟基的距离;b-UGTs底物酪醇与附近残基间的氢键相互作用
图4 UGTs与酪醇的对接结果
Fig.4 Docking results of UGTs with tyrosol
2.3 酪醇选择性不同的UGTs的动态构象分析
对上述8种UGTs展开40 ns的分子动力学模拟,对于每种UGTs,在模拟过程中每间隔1 ps提取1帧,计算催化残基His咪唑环上直接负责受体去质子化的N原子(NE2)与底物酪醇分子中醇羟基或酚羟基O原子(AlO/PhO)之间的距离,分别记为“DisHis_NE2-Tyrosol_AlO”和“DisHis_NE2-Tyrosol_PhO”。将两距离值作差得到Δd(Δd=DisHis_NE2-Tyrosol_AlO-DisHis_NE2-Tyrosol_PhO)。Δd的正负号直接反映了底物的优势取向:当Δd为负值时,酪醇分子醇羟基比酚羟基在空间中更靠近UGTs的催化残基,相较于酚羟基受到去质子化的机会更大,产物为红景天苷的概率更高;当Δd为正值时,酚羟基更接近UGTs的催化残基,受到去质子化的机会更大,产物为淫羊藿次苷D2的概率更高。每当Δd的正负发生变化,则记底物酪醇发生了一次构象扭转,整个动力学模拟过程中的每ns构象扭转次数被定义为扭转频率(次/ns)(图5-a)。
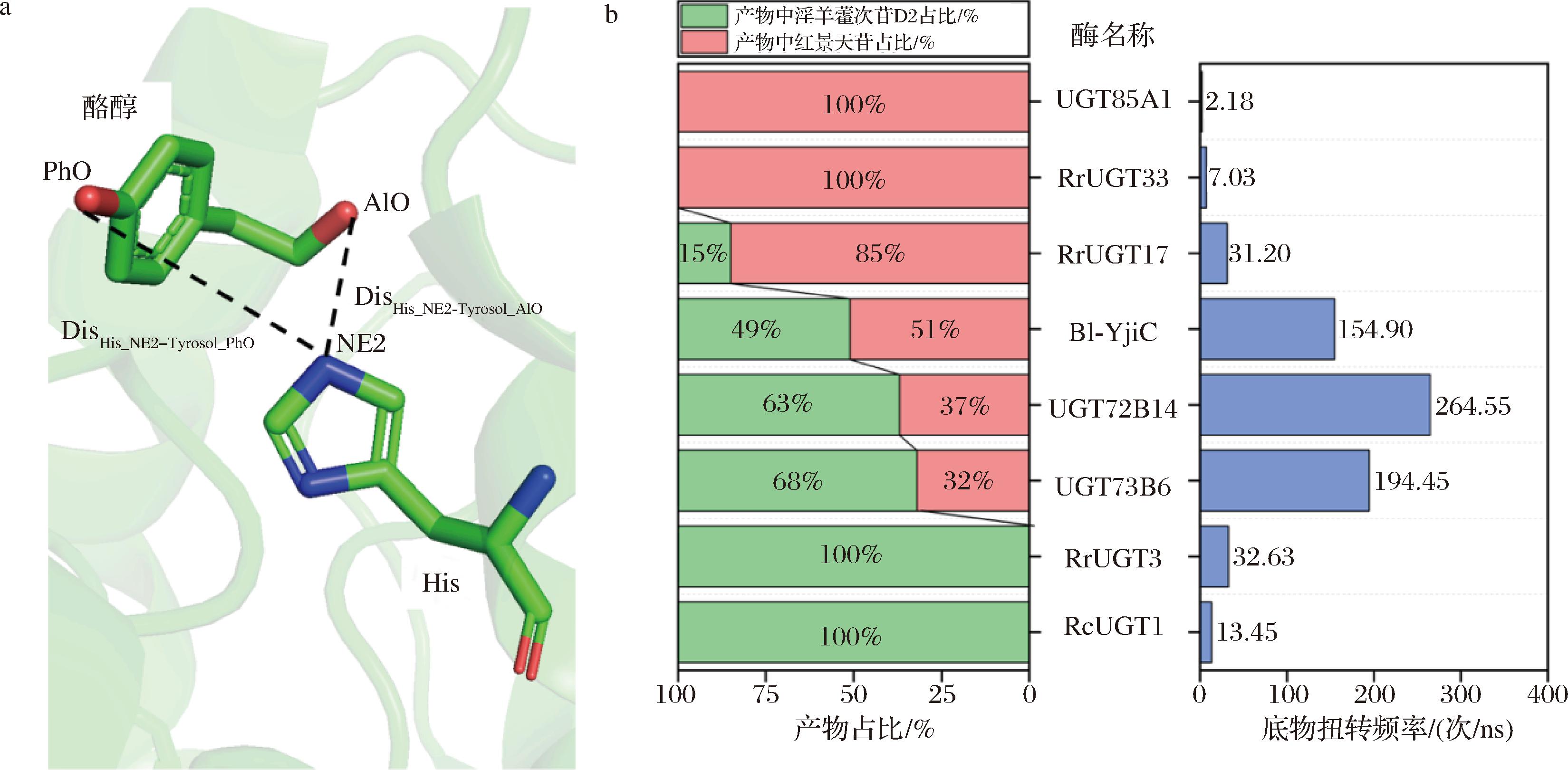
a-酪醇酚/醇羟基O原子与催化残基NE2原子的距离;b-UGTs区域选择性及分子动力学模拟过程中底物构象的扭转频率
图5 八种UGTs底物构象动态分析
Fig.5 Dynamic analysis of substrate conformations for eight UGTs
8种UGTs的区域选择性数据与分子动力学模拟结果如图5-b所示,观察到酪醇分子在活性中心的构象扭转频率与其区域选择性呈现显著的负相关性。具有严格区域选择性的UGT85A1、RrUGT33、RcUGT1和RrUGT3在40 ns的分子动力学模拟中展现出了极低的构象扭转频率(2.18、7.03、13.45、32.63 次/ns),说明其底物取向较为稳定;与之相对的,具有较差区域选择性的UGTs中,底物则呈现出显著增加的扭转频率,表明底物酪醇在40 ns的分子动力学模拟过程中发生了频繁摆动,可能使得酚羟基与醇羟基均有机会受到催化残基的去质子化,从而表现为红景天苷与淫羊藿次苷D2的混合产物。
2.4 UGT85A1区域选择性改造及其机制分析
选取具有严格醇羟基选择性且催化活性较好的UGT85A1,通过定点突变降低其区域选择性。将UGT85A1与专一合成淫羊藿次苷D2且具有高催化活性的RrUGT3展开序列和结构比对[19]。查找了位于UGT85A1活性中心的第24位组氨酸催化残基附近5 Å范围内的氨基酸,将其突变为RrUGT3中对应的氨基酸。考虑到第21位的丙氨酸位点在13种UGTs中具有较高保守性,因此保留了该位点的原始氨基酸。这一策略最终确定了Y19S、C128F、T148P、Q22M、I25L、N26I六个突变子(图6-a~图6-b)。酶活性测定结果显示,突变子Y19S、T148P、Q22M和I25L的催化产物中未检测到淫羊藿次苷D2,而C128F和N26I突变子在保留催化酪醇合成红景天苷的能力的同时,还获得了合成淫羊藿次苷D2的能力(图6-c)。
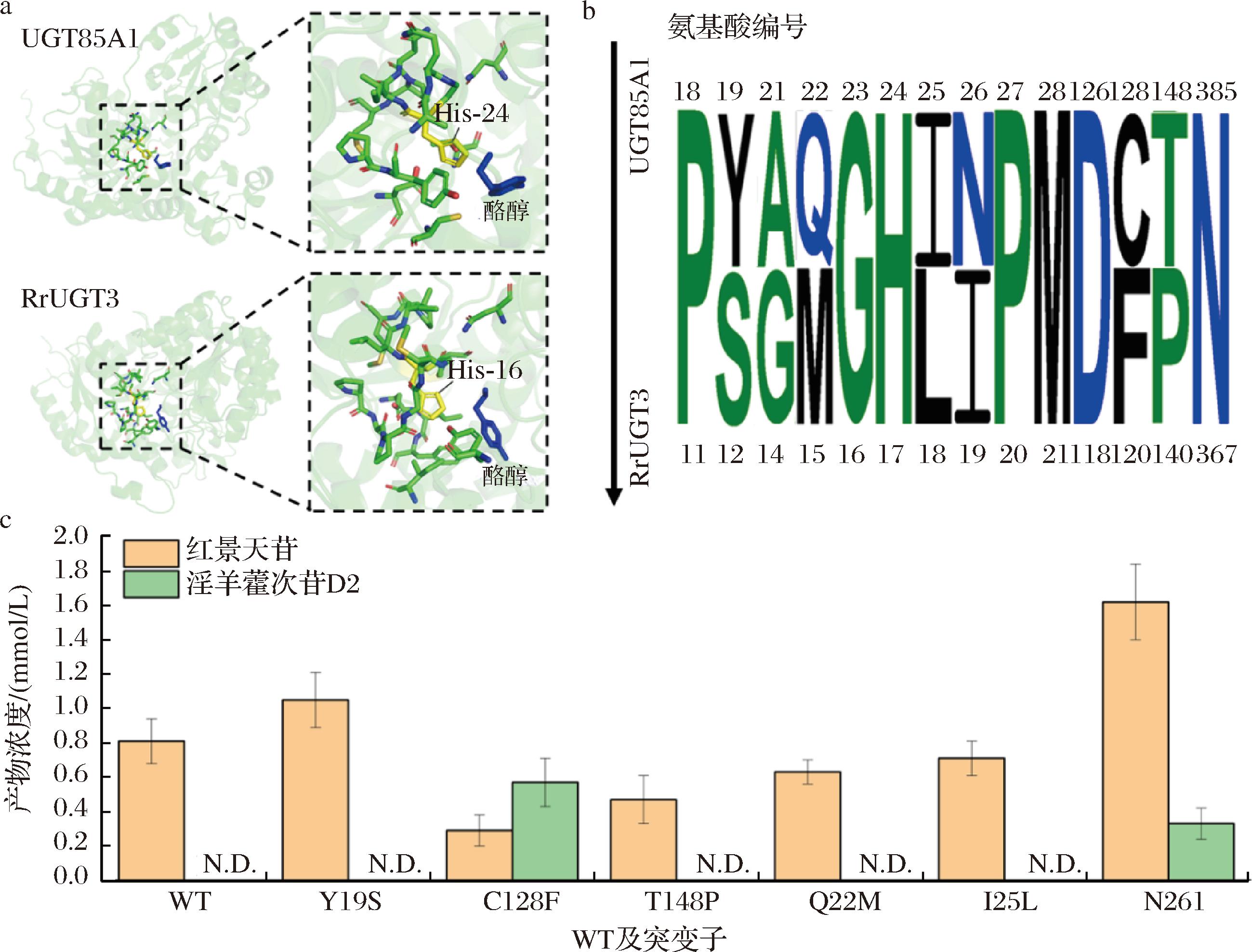
a-UGT85A1与RrUGT3催化残基附近5 Å范围内的氨基酸;b-活性中心附近的差异残基交换策略;c-WT及突变子的红景天苷及淫羊藿次苷产量
图6 UGT85A1突变子的区域选择性表征
Fig.6 Characterization of the regioselectivity of UGT85A1 mutants
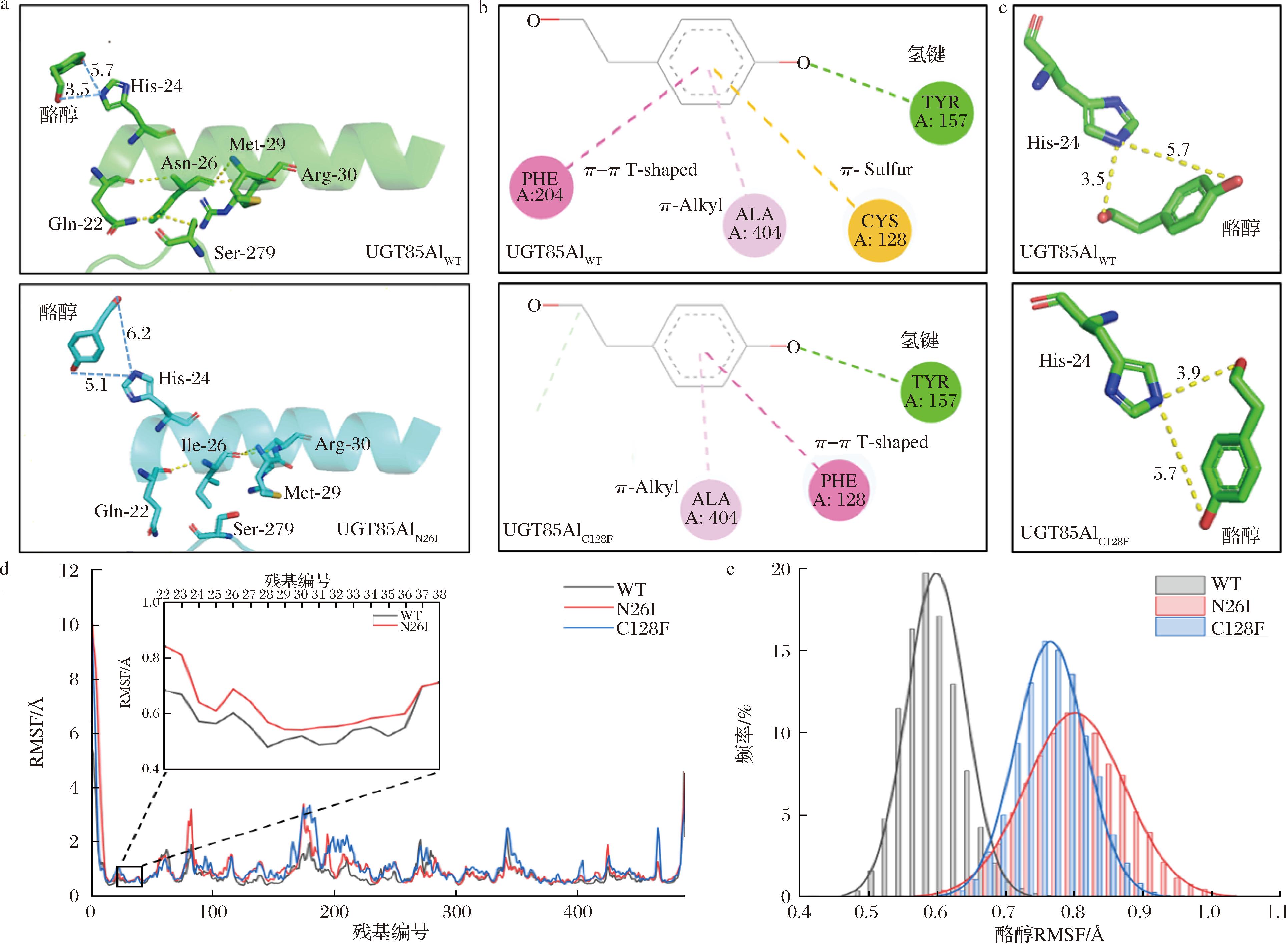
a-WT及N26I突变附近的相互作用;b-WT及C128F突变附近的相互作用;c-WT及C128F突变子催化残基His24到酪醇酚/醇羟基的距离;d-WT及2种突变子蛋白的RMSF值;e-底物酪醇的RMSD值分布
图7 N26I和C128F突变子的区域选择性机制
Fig.7 Regioselectivity mechanism of N26I and C128F mutants
对突变子展开结构-功能分析,结果显示,在原始酶UGT85A1中,第26位的天冬酰胺(N26)与催化残基H24共同位于构成底物口袋的同一α-螺旋上。N26不仅与该α-螺旋上的Gln22、Met29和Arg30形成氢键,还与相邻铰链区域279位的丝氨酸残基(Ser279)形成氢键;当N26突变为异亮氨酸(I)后,I26与铰链上S279的氢键消失(图7-a)。与此同时,在40 ns的动力学模拟过程中,该氢键形成频率从原始酶中的27.58%降至0%,这种局部相互作用的减弱降低了对I26所在α-螺旋的约束,导致其灵活性增加,RMSF升高(图7-d)。进一步分析突变子N26I中底物扭转情况,结果显示在40 ns的模拟过程中,原始酶中底物的扭转频率为2.18 次/ns,而突变后底物扭转频率提升至7.60 次/ns。突变后底物酪醇RMSD由0.60 Å提高到0.80 Å(图7-e),表明其具有更高的灵活性;同时,突变后底物中酪醇酚/醇羟基与催化残基H24距离之差为1.1 Å(图7-a),小于WT中该距离,这些都可能促使其酚羟基受到糖基化的概率提高,从而实现了淫羊藿次苷D2合成。
对于C128F突变子,突变位点引入后,底物酪醇与F204之间的π-π T-shaped作用被破坏(图7-b),同时C128F突变的分子动力学模拟结果显示,构象扭转频率由2.18 次/ns上升至76.63 次/ns,底物RMSD由0.60 Å提升至0.76 Å(图7-e),底物的自由度提高,且催化残基H24与底物的2个羟基间的距离差Δd由2.2 Å缩短至1.8 Å(图7-c),均有利于酚羟基被糖基化的概率提高,从而有效生成淫羊藿次苷D2。
N26I和C128F突变均增强了底物酪醇在催化过程中的自由度,同时根据文中所定义的扭转行为,两者底物扭转频率均显著提升;底物的这种动态行为可能使得形成淫羊藿次苷D2的酚羟基糖基化过程更易发生,从而将仅专一催化酪醇醇羟基糖基化功能转变为可同时实现2个羟基糖基化的功能。而这一特征在不同来源且区域选择性各异的UGTs动力学模拟中均存在,暗示着底物扭转对UGTs区域选择性的重要影响,同时也有望作为蛋白设计思路之一,实现对UGTs区域选择性的人工调节。
3 结论与讨论
已有研究表明,催化性His-Asp/Glu二元组是许多GT1家族成员的保守结构基序[15]。其中,位于底物口袋内的组氨酸通常作为催化残基,参与受体的去质子化,以允许糖基供体发起亲核攻击。在保守的催化机制之上,催化残基(His)与底物酪醇2个潜在糖基化位点之间的相对位置与空间取向是决定其区域选择性的关键。如对UGTBL1的研究发现蛋白中宽敞的底物结合口袋可允许酪醇以2种不同构象结合,进而为葡萄糖向底物的2个不同受体基团转移提供了结构基础[11]。这种相对位置决定了哪个羟基更易被去质子化,从而引导反应倾向生成红景天苷或淫羊藿次苷D2。
区域选择性的差异不仅取决于静态的空间距离,更与催化过程中底物的动态行为密切相关。如在使用二维红外光谱对P450cam酶识别去甲樟脑机制的研究中,通过活性位点探针CNF96检测到底物存在2种快速互变的构象状态,这种动态异质性导致了羟基化区域选择性的降低[21]。同样,在对CYP106A2酶与松香酸的研究中,使用核磁共振光谱和顺磁弛豫增强方法,发现底物在活性位点存在多个结合取向,这些取向通过动态波动快速互变,导致在多个位点发生羟基化,从而降低了区域选择性[22]。本研究通过分子动力学模拟发现,底物酪醇在活性口袋内存在显著的构象扭转。当底物扭转受到限制时,UGTs表现出高度的区域选择性;而底物扭转频率升高时,原本空间取向不利的基团能够与催化残基充分接触并发生糖基化,更易生成混合产物。而在不同来源UGTs中,底物扭转频率也呈现类似规律,具有严格区域选择性的专一生成红景天苷或淫羊藿次苷D2的UGT85A1、RrUGT33、RrUGT3和RcUGT1的底物表现出较低的构象扭转频率,而能够生成混合糖苷的UGT73B6、UGT72B14、Bl-YjiC和RrUGT17的底物构象扭转频率较高。因此,底物扭转作为影响区域选择性的关键因子,可以作为区域选择性改造中重点关注的参数,以实现更为高效的改造。
本研究通过对UGT85A1的理性设计,将其对酪醇的区域选择性从单一生成红景天苷转变为可同时合成红景天苷与淫羊藿次苷D2。突变子N26I与C128F分别通过提高底物附近α-螺旋的自由度以及降低底物与口袋残基的相互作用力,显著提高了底物酪醇的构象扭转频率,使原本处于不利位置的酚羟基获得了被催化与糖基化的机会。本文从构象动态的角度初步探究了UGT85A1区域选择性机制,为增强区域选择性提供了理论基础,同时也为UGTs类酶的底物选择性改造提供了不同角度。
[1] 于安东, 刘琳, 龙瑞才, 等. 植物UDP-糖基转移酶(UGT)的功能及应用前景[J]. 植物生理学报, 2022, 58(4):631-642.YU A D, LIU L, LONG R C, et al. Function and application prospect of plant UDP-glycosyltransferase(UGT)[J]. Plant Physiology Journal, 2022, 58(4):631-642.
[2] ZHANG X M, XIE L, LONG J Y, et al. Salidroside: A review of its recent advances in synthetic pathways and pharmacological properties[J]. Chemico-Biological Interactions, 2021, 339:109268.
[3] WANG X P, YUAN D Y, TIAN Y, et al. Multiple mechanisms of salidroside on anti-tumor effects[J]. European Review for Medical and Pharmacological Sciences, 2021, 25(17): 5349-5354.
[4] SUN S Y, TUO Q H, LI D X, et al. Antioxidant effects of salidroside in the cardiovascular system[J]. Evidence-Based Complementary and Alternative Medicine, 2020, 2020:9568647.
[5] CHEN M X, WU J F, LUO Q L, et al. The anticancer properties of herba epimedii and its main bioactive componentsicariin and icariside II[J]. Nutrients, 2016, 8(9):563.
[6] SHEN Y J, XIA Y Y, CHEN X Z. Research progress and application of enzymatic synthesis of glycosyl compounds[J]. Applied Microbiology and Biotechnology, 2023, 107(17):5317-5328.
[7] LI G S, XU Q L, HU N, et al. Highly efficient biosynthesis of salidroside by a UDP-glucosyltransferase-catalyzed cascade reaction[J]. Biotechnology Letters, 2024, 46(2):173-181.
[8] GUO F, ZHANG X W, YOU C, et al. Diversification of phenolic glucosides by two UDP-glucosyltransferases featuring complementary regioselectivity[J]. Microbial Cell Factories, 2022, 21(1):208.
[9] LI M S, YOU C, GUO F, et al. Reaction mechanism and regioselectivity of uridine diphosphate glucosyltransferase RrUGT3: A combined experimental and computational study[J]. Catalysis Science &Technology, 2024, 14(17):4882-4895.
[10] ZHANG C H, CAI Y C, ZHANG Z H, et al. Directed evolution of the UDP-glycosyltransferase UGTBL1 for highly regioselective and efficient biosynthesis of natural phenolic glycosides[J]. Journal of Agricultural and Food Chemistry, 2024, 72(3):1640-1650.
[11] ZHANG Z Y, CHEN J Y, LIANG Z Z, et al. Tailoring regioselectivity-controlled UDP-glycosyltransferase for bidirectional glycosylation of tyrosol via free energy-driven pocket reshaping and tunnel engineering[J]. Advanced Science, 2025, 12(40): e09814.
[12] MINH B Q, SCHMIDT H A, CHERNOMOR O, et al. IQ-TREE 2: New models and efficient methods for phylogenetic inference in the genomic era[J]. Molecular Biology and Evolution, 2020, 37(5):1530-1534.
[13] ABRAMSON J, ADLER J, DUNGER J, et al. Accurate structure prediction of biomolecular interactions with AlphaFold 3[J]. Nature, 2024, 630(8016):493-500.
[14] CASE D A , AKTULGA H M ,BELFON K , et al. (2025), Amber 2025, University of California, San Francisco.
[15] BRETON C, FOURNEL-GIGLEUX S, PALCIC M M. Recent structures, evolution and mechanisms of glycosyltransferases[J]. Current Opinion in Structural Biology, 2012, 22(5):540-549
[16] 魏晨昱, 黄珠莹, 沈知行, 等. 基于尿苷二磷酸葡萄糖循环再生系统高效转化酪醇合成红景天苷[J]. 生物工程学报, 2024, 40(9):3127-3141.WEI C Y, HUANG Z Y, SHEN Z X, et al. Efficient synthesis of salidroside from tyrosol based on UDPG recycling system[J]. Chinese Journal of Biotechnology, 2024, 40(9):3127-3141.
[17] CHUNG D, KIM S Y, AHN J H. Production of three phenylethanoids, tyrosol, hydroxytyrosol, and salidroside, using plant genes expressing in Escherichia coli[J]. Scientific Reports, 2017, 7:2578.
[18] 马兰青, 柳春梅, 于寒松, 等. 红景天甙生物合成途径: 酪醇合成的起始反应及其糖基化[J]. 生物工程学报, 2012, 28(3):282-294.MA L Q, LIU C M, YU H S, et al. Salidroside biosynthesis pathway: The initial reaction and glycosylation of tyrosol[J]. Chinese Journal of Biotechnology, 2012, 28(3):282-294.
[19] LIU X, LI L L, LIU J C, et al. Metabolic engineering Escherichia coli for efficient production of icariside D2[J]. Biotechnology for Biofuels, 2019, 12(1):261.
[20] LI B F, CHANG S Y, JIN D, et al. Ca2+ assisted glycosylation of phenolic compounds by phenolic-UDP-glycosyltransferase from Bacillus subtilis PI18[J]. International Journal of Biological Macromolecules, 2019, 135:373-378.
[21] RAMOS S, MAMMOSER C C, THIBODEAU K E, et al. Dynamics underlying hydroxylation selectivity of cytochrome P450cam[J]. Biophysical Journal, 2021, 120(5):912-923.
[22] WONG N R, SUNDAR R, KAZANIS S, et al. Conformational heterogeneity suggests multiple substrate binding modes in CYP106A2[J]. Journal of Inorganic Biochemistry, 2023, 241:112129.