表面活性素(surfactin)是一种由芽孢杆菌属细菌分泌的环状脂肽类生物表面活性剂[1-2],兼具优异的表面活性、生物降解性与广谱抗菌、抗病毒等活性[3-4]。其独特的分子结构由β-羟基脂肪酸与七肽头部形成亲疏水两性环状结构,使其在低浓度下即可显著降低表面张力,表面活性素在医药、农业、环境修复、食品工业及日化产品等领域展现出广阔应用前景[5-6]。然而,其在工业化生产过程中仍面临产量低、发酵成本高及规模化稳定性不足等技术瓶颈。
表面活性素的合成过程受多个信号通路和转录因子调控,其中以 ComX 和PhrC为代表的调控因子被证实在启动与增强合成表达中发挥核心作用。comX 编码一种前信号肽,通过激活ComP-ComA二组分系统启动srfA操作子表达,是群体感应调控系统的关键上游节点;PhrC属于小分子反馈肽,通过作用于Rap-Phr调控系统,解除转录抑制,进一步增强合成通路的活性[7-8]。相较于其他调控因子如degU或 spo0A,ComX与PhrC结构明确、路径清晰,且在重组表达系统中具有更好的可操作性和模块化特征,因而更适合作为外源调控元件用于合成增强。此前多项研究表明,单独或联用过表达ComX与PhrC可使表面活性素产量提升2~6倍以上,且不显著影响宿主生长状态[9]。
尽管基因改造策略在模式菌枯草芽孢杆菌(Bacillus subtilis)中已广泛应用,其在非模式芽孢杆菌中的推广仍面临诸多挑战,主要包括遗传背景差异大、外源质粒难以稳定维持、表达系统不兼容等因素[10]。相较而言,部分非模式芽孢杆菌在极端环境下表现出更强的生理稳定性与代谢适应能力,在脂肽类物质的合成能力及结构特性方面可能具有差异性优势[11]。韩国芽孢八叠球菌(Sporosarcina koreensis)为嗜碱性芽孢杆菌,有报道表明其具备初步脂肽合成能力,其在高pH环境下稳定生长,这一特性为其作为工业应用宿主提供了可行性支持[12]。此外,以Paenibacillus、Zymomonas等非模式菌为平台的工程菌种构建已显示出在特定生物合成任务中的高效能力[13]。基于上述背景,本研究聚焦S.koreensis脂肽合成路径工程化,旨在丰富合成生物学宿主资源并探索潜在的新型功能脂肽产物。
为此,本研究以实验室分离获得的S.koreensis WZ1为研究对象,首次开展其表面活性素合成能力的系统分析,并基于B.subtilis中功能明确的2个调控基因comX与phrC,分别构建重组表达菌株,进一步分析其调控效果。为增强结果对比的合理性与严谨性,选用表面活性素研究中广泛应用的模式菌株B.subtilis 1012 WT作为参照。通过比较重组前后菌株在表面活性、脂肽结构及抑菌活性等方面的差异,初步评估调控因子在非模式菌背景下的功能表现,并探讨其作为潜在脂肽生产宿主的可行性。该研究旨在为拓展表面活性素工程菌种类、丰富调控因子应用场景提供理论依据与实验基础。
1 材料与方法
1.1 材料与试剂
B.subtilis 1012 WT、PHT43质粒,德国MoBitech公司;S.koreensis WZ1,实验室分离所得;标准表面活性素,德国Sigma公司;合成基因引物sfg-f、sfg-r,生工生物工程股份有限公司;16SrDNA引物、表面活性素调控基因引物(ComX/PhrC),华大基因科技有限公司;BamHI酶、XbaI酶,碧云天生物技术有限公司;T4 DNA连接酶,普洛麦格生物产品有限公司。
LB液体/固体培养基(g/L):酵母浸粉5、胰蛋白胨10、NaCl 10,固体培养基添加琼脂15~20;2×YT(yeast extract-tryptone)培养基(g/L):胰蛋白胨16、酵母浸粉10、NaCl 5;10×Spizizen 基础盐(Spizizen salts base,S-base)培养基(g/L):K2HPO4 14、KHPO4 6、(NH4)2SO4 2、柠檬酸钠 1;高盐感受态(high-salt competence,HS)培养基(每 100 mL):蒸馏水 66.5 mL,10×S-base 10 mL,20%(质量分数)葡萄糖溶液2.5 mL,0.1%(质量分数)L-色氨酸溶液5 mL,2%(质量分数)酪蛋白溶液1 mL,10%(质量分数)酵母提取物溶液5 mL, 8%(质量分数)L-精氨酸溶液10 mL,0.4%(质量分数)L-组氨酸溶液0.4 mL;低盐转化(low-salt competence,LS)培养基(每 100 mL):蒸馏水 80 mL,10×S-base 10 mL, 20%(质量分数)葡萄糖溶液2.5 mL,0.1%(质量分数) L-色氨酸溶液0.5 mL,质量分数 2% 酪蛋白溶液0.5 mL,2%(质量分数)酵母提取物溶液5 mL,1 mol/L MgCl2 溶液0.25 mL,1 mol/L CaCl2溶液0.05 mL;50×TAE 电泳缓冲液(tris-acetate-EDTA buffer):三羟甲基氨基甲烷242 g/L、Na2EDTA·2H2O 37.2 g/L、乙酸57.1 mL/L,pH 8.3;0.1 mol/L EGTA 缓冲液(pH 7.2);0.5%(质量分数)茚三酮显色剂(将0.5 g茚三酮溶于100 mL 正丁醇中,加入 3 mL 冰乙酸混匀)。
1.2 仪器与设备
T6新世纪紫外可见分光光度计,普析通用仪器有限公司;WD-9402A基因扩增仪、DYY-6C电泳仪,北京六一仪器厂;Waters高效液相色谱仪、Gel DocTMEZ Imager凝胶成像系统,美国Waters公司;Gel DocTMEZ Imager凝胶成像系统,美国BIO-RAD公司。
1.3 实验方法
1.3.1 菌株来源与鉴定
本研究使用的WZ1菌株为实验室从环境中分离获得,经16S rDNA基因序列扩增与测序比对,使用通用引物为F:5′-AGAGTTTGATCCTGGCTCAG-3′;R:5′-GGTTACCTTGTTACGACTT-3′,对提取的基因组DNA进行PCR扩增,扩增产物经电泳验证后送测序。测序结果经BLAST比对显示,该菌株与S.koreensis同源性达99%。
培养形态观察显示,WZ1菌株在LB平板培养24 h后形成乳白色、湿润、边缘不规则的菌落;显微镜下呈短杆状革兰氏阳性细胞,形态特征与文献中S.koreensis一致[14]。
1.3.2 表面活性素的提取与纯化
依照参照文献[15-16]的方法,将1012 WT菌株和WZ1菌株分别涂布到固体LB培养基上,培养24 h,再用接种环从平板上挑取少量菌体,将其接种于液体LB培养基中,并在37 ℃、180 r/min的条件下培养60 h。培养结束后,取部分菌液进行保存,方法为:将800 μL 40%(质量分数)无菌甘油与800 μL菌液混合,装入经灭菌的2 mL离心管中,随后将其存放于-80 ℃ 冰箱中以备后用[17]。
将2种菌的发酵液进行离心处理。将培养液以10 000 r/min的转速离心25 min,除去沉淀,收集上清液。在收集的上清液中加入6 mol/L的盐酸,调节pH值至2.0左右,混匀后,将溶液放置在4 ℃冰箱中冷藏过夜。隔天在10 000 r/min的条件下离心25 min,并去除上清液收集沉淀。后用50 mL无水甲醇充分提取,获得甲醇粗提液。
随后,使用重结晶法对粗提取液进行纯化处理。首先,通过减压蒸发去除甲醇溶剂,收集沉淀,并将其溶解于蒸馏水中。溶液混匀后,使用5 mol/L NaOH溶液将pH值调节至约7.0,再使用6 mol/L盐酸溶液将pH值调整至约2.0,并在4 ℃冰箱中冷藏过夜。最后,使用10 000 r/min离心5 min收集沉淀所得灰白色沉淀即为菌株产生的脂肽类表面活性素提取物。
1.3.3 表面活性素的性质分析
a)排油圈直径法
依照参考文献[19]方法,分别取保存在-80 ℃ 冰箱中的B. subtilis 1012WT 菌株和S. koreensis WZ1 菌株的甘油保藏菌株各 1 mL,在固体LB培养基平板上于37 ℃条件下活化培养1 d。隔天用接种环按平板上1%(体积分数)的接种量将1012WT菌株接种在100 mL的液体LB培养基中,在37 ℃、180 r/min条件下培养60 h,制备1012WT菌株发酵液,以不含菌体的空白发酵液为对照,发酵液的光密度(OD600值)应控制在约2.0。
随后,称取1 g苏丹红Ⅲ,加入300 mL液体石蜡中,并使用玻璃棒充分搅拌混匀。将苏丹红Ⅲ染色液体石蜡经抽滤去杂后倒入9 cm培养皿中,均匀铺底。待其完全铺平后,分别取1 mL WZ1 菌株发酵液、1 mL 1012WT 菌株发酵液、1 mL 质量浓度 1.0 g/L 十二烷基硫酸钠溶液,以及1 mL 质量浓度0.5 g/L的标准表面活性素溶液,用移液枪缓慢滴加至培养皿中心。以1 mL甲醇作为空白对照,每组实验重复3次。
b)薄层层析(thin layer chromatography,TLC)分析
将甲醇粗提液与标准表面活性素(0.5 mg/mL)分别点样于硅胶薄层板上,展开溶剂为V(氯仿)∶V(甲醇)∶V(水)=65∶25∶4,展开后,晾干薄层板,喷洒0.5%(质量分数)茚三酮显色液后于95 ℃加热显色,为进一步验证样品中是否含有脂肽类结构特征的氨基基因,对展开后的薄层板进行原位酸水解处理,即将展开后的薄层板置于含浓盐酸的密闭容器中,在110 ℃条件下水解1 h,冷却后再次喷洒茚三酮显色液并加热,观察是否出现橙红色斑点。该操作参考赵秀香等[20]和钱常娣等[16]的TLC显色方法。
1.3.4 HPLC分析
色谱柱型号为XBridge TM C18(5 μm,4.6 mm×150 mm Column),柱温设为25 ℃,检测波长为210 nm,进样量为20 μL,流速设为0.84 mL/min。流动相A:0.1%(体积分数)三氟乙酸乙腈,流动相B:0.1%(体积分数)三氟乙酸水,采用梯度洗脱。分别对标准表面活性素溶液与脂肽类提取物进行检测。结果显示样品在13.17 min(WZ1菌株)和13.61 min(1012 WT菌株)附近出现主峰,保留时间与标准品相近,提示2种菌株的样品中可能含有与标准表面活性素色谱行为相近的脂肽类组分。
由于本实验尚未建立外标曲线,故未进行定量分析,结果为定性初步判断。
1.3.5 抑菌活性测试——牛津杯法[21]
选用金黄色葡萄球菌、铜绿假单胞菌、大肠杆菌和黑曲霉为指示菌。配制菌悬液并混合至营养琼脂中,牛津杯置于平板中间,每孔加入240 μL样品,包括WZ1菌株发酵液、标准表面活性素溶液(质量浓度20 g/L)、氯霉素溶液(质量浓度1、5、10 g/L)以及蒸馏水(空白对照)(表1)。每组实验设置3个重复样,培养24 h后测量抑菌圈直径,并计算平均值与标准差,结果绘制为带误差线的柱状图。
表1 不同浓度待测样品水溶液配制信息
Table 1 Preparation information of test sample solutions at different concentrations
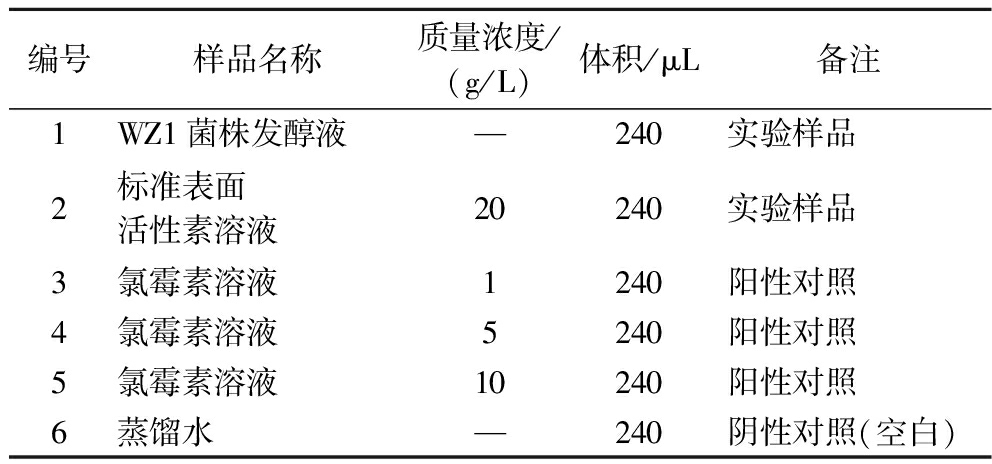
编号样品名称质量浓度/(g/L)体积/μL备注1WZ1菌株发醇液—240实验样品2标准表面活性素溶液20240实验样品3氯霉素溶液1240阳性对照4氯霉素溶液5240阳性对照5氯霉素溶液10240阳性对照6蒸馏水—240阴性对照(空白)
注:“—”表示该样品未进行质量浓度折算或不含待测物。
1.3.6 表面活性素相关基因的克隆
参照细菌基因组DNA提取试剂盒说明书,提取1012 WT菌株与WZ1菌株的基因组DNA。
使用sfg-f及sfg-r引物扩增表面活性素合成基因,所需试剂dNTP(脱氧核苷三磷酸)、Buffer缓冲液、Taq DNA聚合酶、dd H2O。引物设计sfg-f:5-ATGAAGATTTACGGAATTTA-3;sfg-r:5-TTATAAAAGCTCTTCGTACG-3。PCR体系包含dNTP、Buffer、Taq DNA聚合酶与dd H2O。同时,以同一基因组DNA为模板,使用ComX/PhrC系列引物扩增表面活性素调控基因片段,
ComX-f ACCTTGGGATCCATGCAAGACCTAATTAAC-TA
ComX-r ATTCTGTCTAGATTAATCACCCCATTGACG
PhrC-f ACTCTGGGATCCAAAGGAGGAAGGATCAA-TGAAATTGAAATCTAAGTT
PhrC-r TCG GAC TCT AGA TTA CGT CAT TCC TCT TTC
所得克隆产物命名为CX1、PC1(以1012 WT菌株为模板)和CX4、PC4(以WZ1菌株为模板)。所有PCR产物经1%(质量分数)琼脂糖凝胶电泳检测后送测序,确保序列准确性,并作为后续构建重组质粒的基础。
1.3.7 重组质粒构建[22]与转化[23-24]
将PCR扩增获得的CX4、PC4、PC1片段与PHT43质粒进行双酶切(BamHI/XbaI)处理,酶切体系为20 μL,37 ℃孵育1~2 h。回收目的片段后,采用T4 DNA连接酶在4 ℃下连接过夜,反应体系为20 μL。连接产物经热激法转化至感受态大肠杆菌DH5α(42 ℃,90 s,冰浴复温),并涂布于含氯霉素(5 μg/mL)的LB固体平板,37 ℃培养24 h筛选阳性克隆。阳性菌株经质粒提取试剂盒提取重组质粒,并通过1%(质量分数)琼脂糖凝胶电泳进行初步验证。
重组质粒经鉴定后,采用文献报道的方法制备感受态B.subtilis菌株细胞。菌液在LB培养基中37 ℃、180 r/min培养至OD600值≈0.6~0.8,采用高渗缓冲液(含0.5 mol/L蔗糖)制备感受态细胞,保持低温操作。将重组质粒导入感受态B.subtilis菌株细胞后,经42 ℃热激90 s,立即转入含氯霉素的LB液体培养基中复苏1 h,再涂布于含氯霉素(5 μg/mL)LB平板中,37 ℃培养24~48 h筛选阳性转化子。阳性克隆经液体培养、质粒提取与电泳验证确认转化成功。
后续以转化成功的重组菌株为种源进行发酵培养,收集发酵液并通过排油圈实验评估其表面活性素分泌能力。
1.3.8 重组菌产量验证
重组菌株发酵液经排油圈法评估表面活性能力,设置3组重复,对比插入调控基因前后排油圈直径的变化,以功能表征的方式间接反映表面活性素分泌水平的变化趋势。鉴于实验条件限制,未进一步开展转录水平或蛋白表达水平的验证实验。
2 结果与讨论
2.1 菌株鉴定与形态观察
通过16S rDNA序列比对分析,实验室分离获得的菌株WZ1与S.koreensis的序列同源性达99%,初步确认其为S.koreensis[25]。该菌株在LB平板上培养24 h后呈乳白色、湿润、不规则边缘菌落,显微镜下呈短杆状革兰氏阳性菌体,形态特征与文献一致。
WZ1菌株与S.koreensis的高同源性表明其归属明确,且其在形态、生长条件上具有典型的S.koreensis特征。由于该属此前极少被报道能产表面活性素,WZ1的相关研究具有一定的新颖性和应用潜力。
2.2 表面活性素提取与定性验证
经发酵、酸沉淀与甲醇提取后获得脂肽类提取物。排油圈法结果表明,WZ1菌株的平均排油圈直径为1.83 cm,略高于1012 WT菌株的1.80 cm(表2),图1展示了不同样品的排油圈图像。3次重复实验结果波动较小,表明该方法具有一定重复性。由于实验条件和样本数的限制,本研究仅进行了初步比较,差异的统计学意义仍有待在后续研究中通过更大样本量进一步验证。
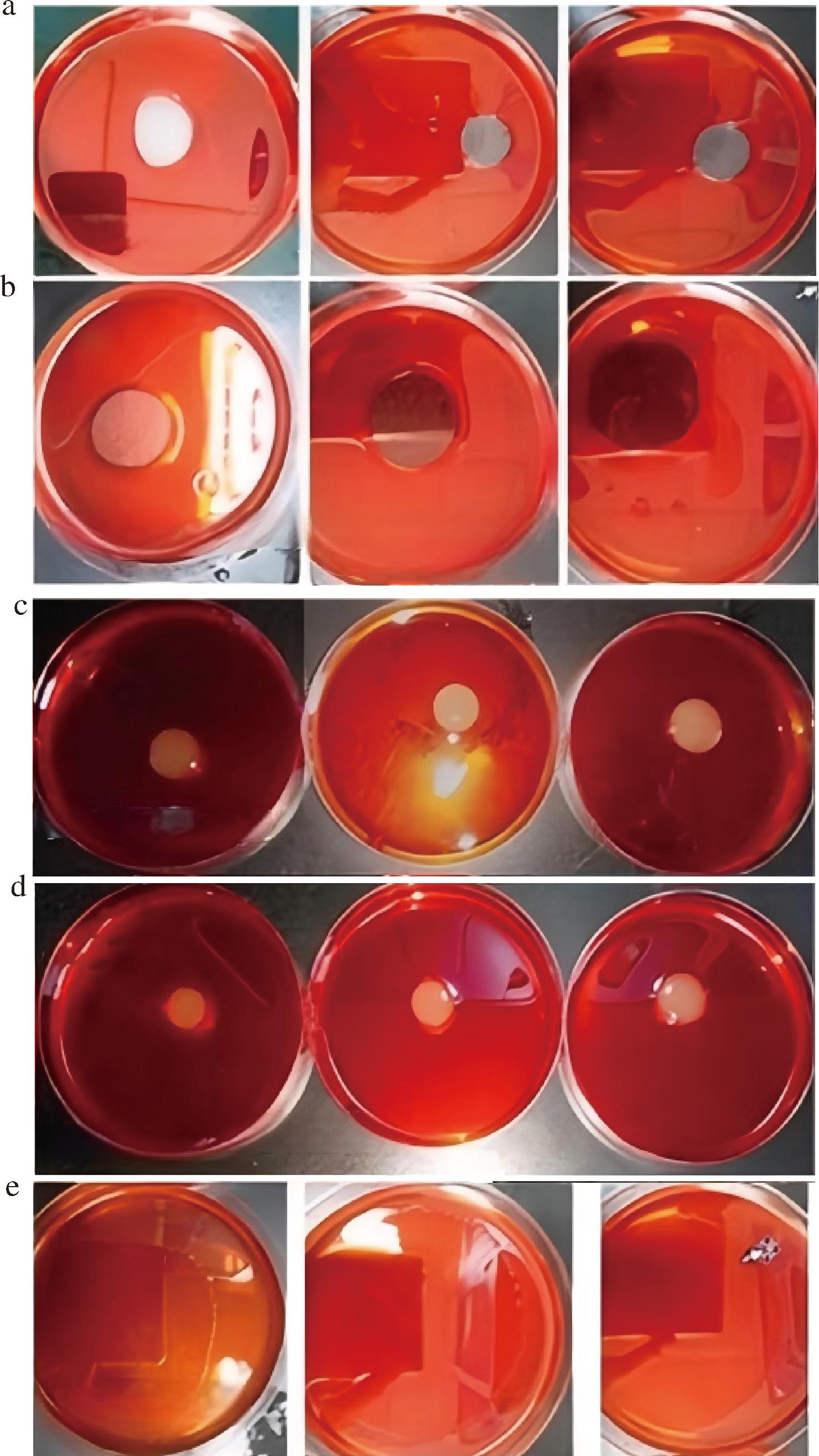
a-1.0 g/L 十二烷基硫酸钠溶液;b-0.5 g/L 标准表面活性素;c-菌株WZ1发酵液;d-菌株1 012 WT发酵液;e-甲醇(空白对照)
图1 不同样品的排油圈实验结果
Fig.1 Oil displacement assay of different samples
注:各样品均在苏丹红Ⅲ染色液体石蜡表面测试其排油能力。
表2 各物质排油圈直径记录
Table 2 Record of oil displacement ring diameters of various substances
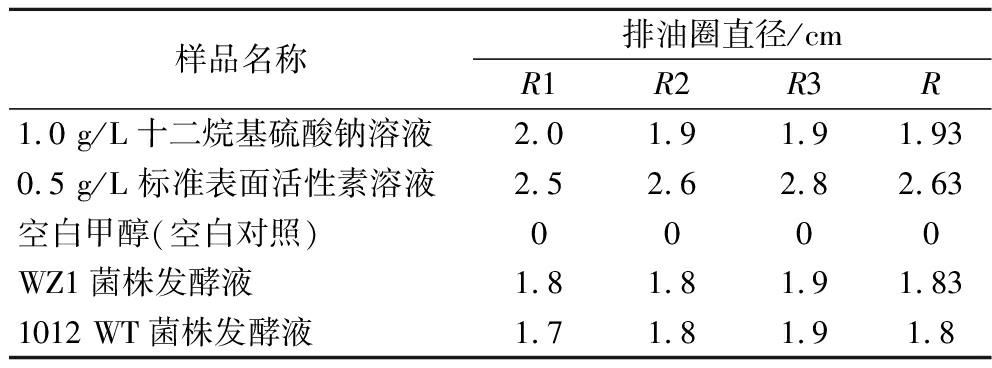
样品名称排油圈直径/cmR1R2R3R1.0 g/L十二烷基硫酸钠溶液2.01.91.91.930.5 g/L 标准表面活性素溶液2.52.62.82.63空白甲醇(空白对照)0000WZ1菌株发酵液1.81.81.91.831012 WT菌株发酵液1.71.81.91.8
TLC分析中,WZ1菌株与1012WT菌株的脂肽类提取物经茚三酮喷洒后显色,酸水解前后颜色变化显著,表明其产物含有典型脂肽类结构中的游离—NH2基团。图2展示了TLC显色结果,样品经酸水解后斑点加深,进一步支持脂肽特性。HPLC分析显示,WZ1菌株与1012WT菌株的脂肽类提取物分别在13.17、13.61 min处出现主峰,保留时间与0.5 mg/mL表面活性素标准品一致,空白甲醇组无明显响应(图3)。综上,上述多种检测手段共同验证了样品中活性成分为脂肽类表面活性素。

图a中1-表面活性素标准品,2-1012WT 菌株脂肽类提取物;
图b中1-表面活性素标准品,2-WZ1 菌株脂肽类提取物;图a及图b中左图为茚三酮直接显色结果,右图为经酸水解后显色结果。
a-1012WT菌株脂肽类提取物TLC显色;b-WZ1菌株脂肽类提取物TLC显色
图2 TLC分析图
Fig.2 TLC analysis chart
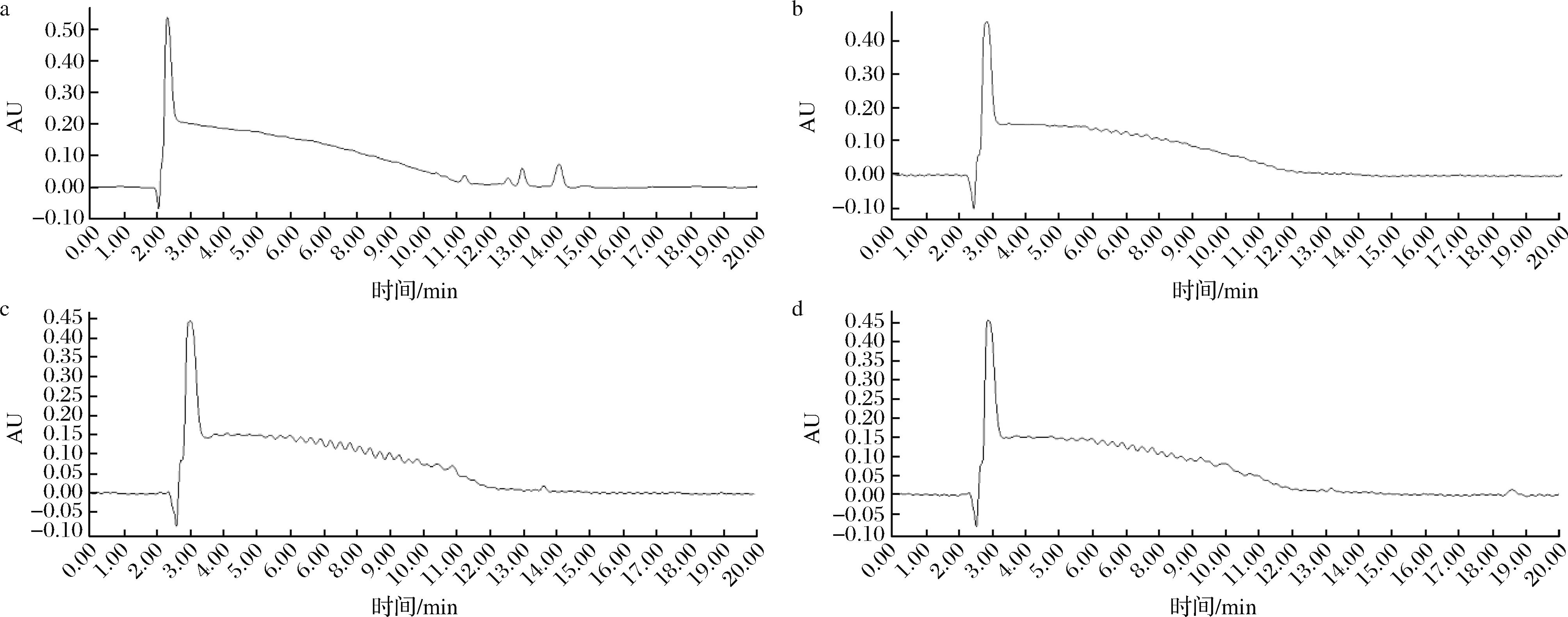
a-0.5 mg/mL标准表面活性素标品;b-甲醇(空白对照);c-1012 WT菌株脂肽类提取物;d-WZ1菌株脂肽类提取物
图3 HPLC色谱图
Fig.3 HPLC chromatogram
WZ1菌株发酵液在排油圈法中表现出更强的表面活性,可能源于其脂肽结构种类或分泌量上的优势。TLC显色与酸水解显著变化进一步支持样品中存在含游离—NH2基团的脂肽类物质。HPLC分析中,样品主峰的保留时间与表面活性素标准品相近,同时检测到次峰,提示其脂肽组分可能存在差异,后续可结合质谱技术进行进一步鉴定。
2.3 抑菌活性分析
通过牛津杯法评估表面活性素抑菌活性。结果显示,WZ1菌株发酵液及其脂肽类提取物(质量浓度 20 g/L)均对金黄色葡萄球菌、铜绿假单胞菌、大肠杆菌和黑曲霉具有不同程度抑制作用,其抑菌效果强于低剂量氯霉素对照,并在部分情况下接近高剂量对照组。图4显示了各样品对4种指示菌的抑菌圈直径(平均值±标准差),表明脂肽样品表现出较广的抑菌谱。
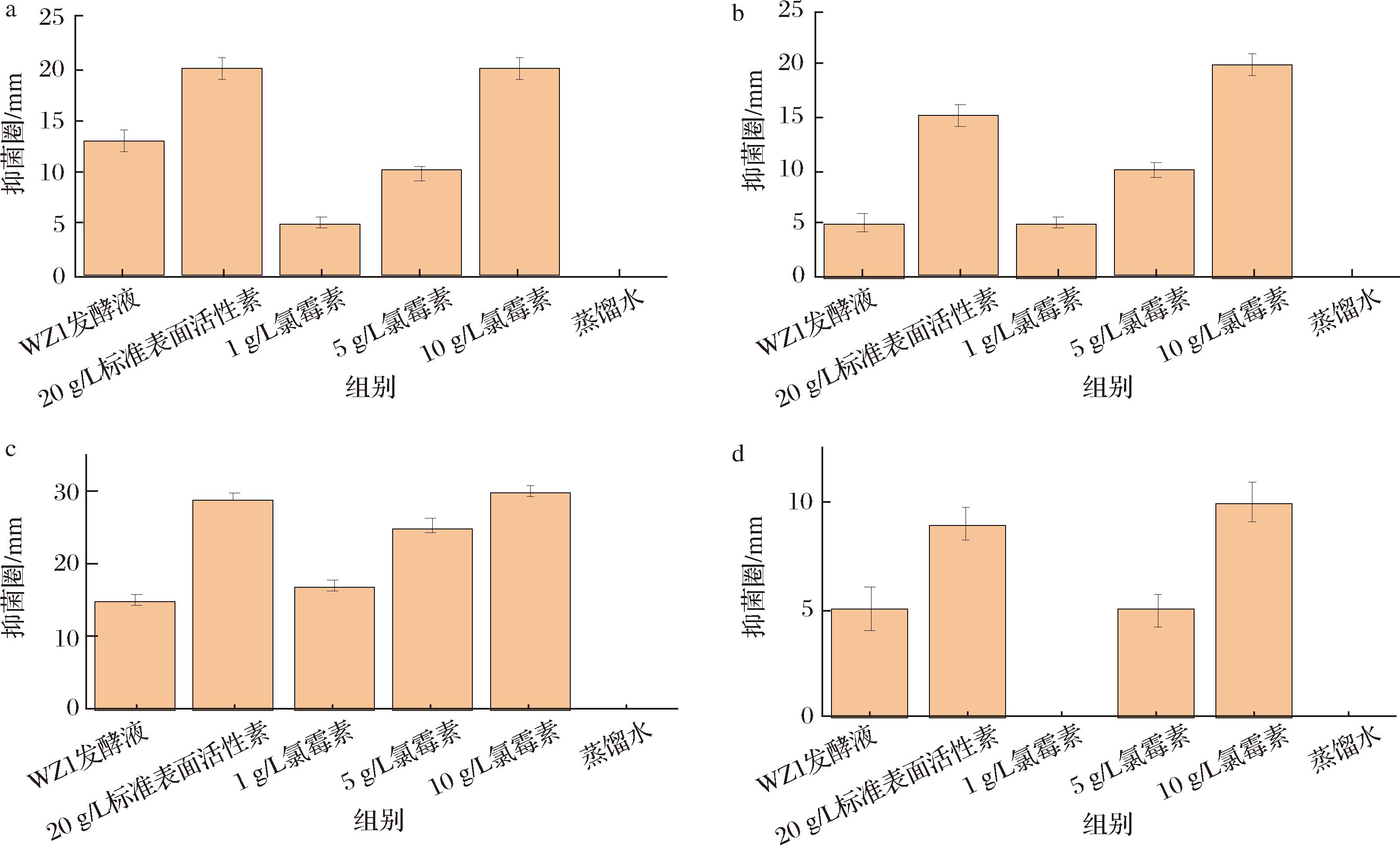
a-金黄色葡萄球菌;b-铜绿假单胞菌;c-大肠杆菌;d-黑曲霉
图4 不同样品对4种指示菌的抑菌圈直径
Fig.4 Inhibition zone diameters of different samples
注:n=3。
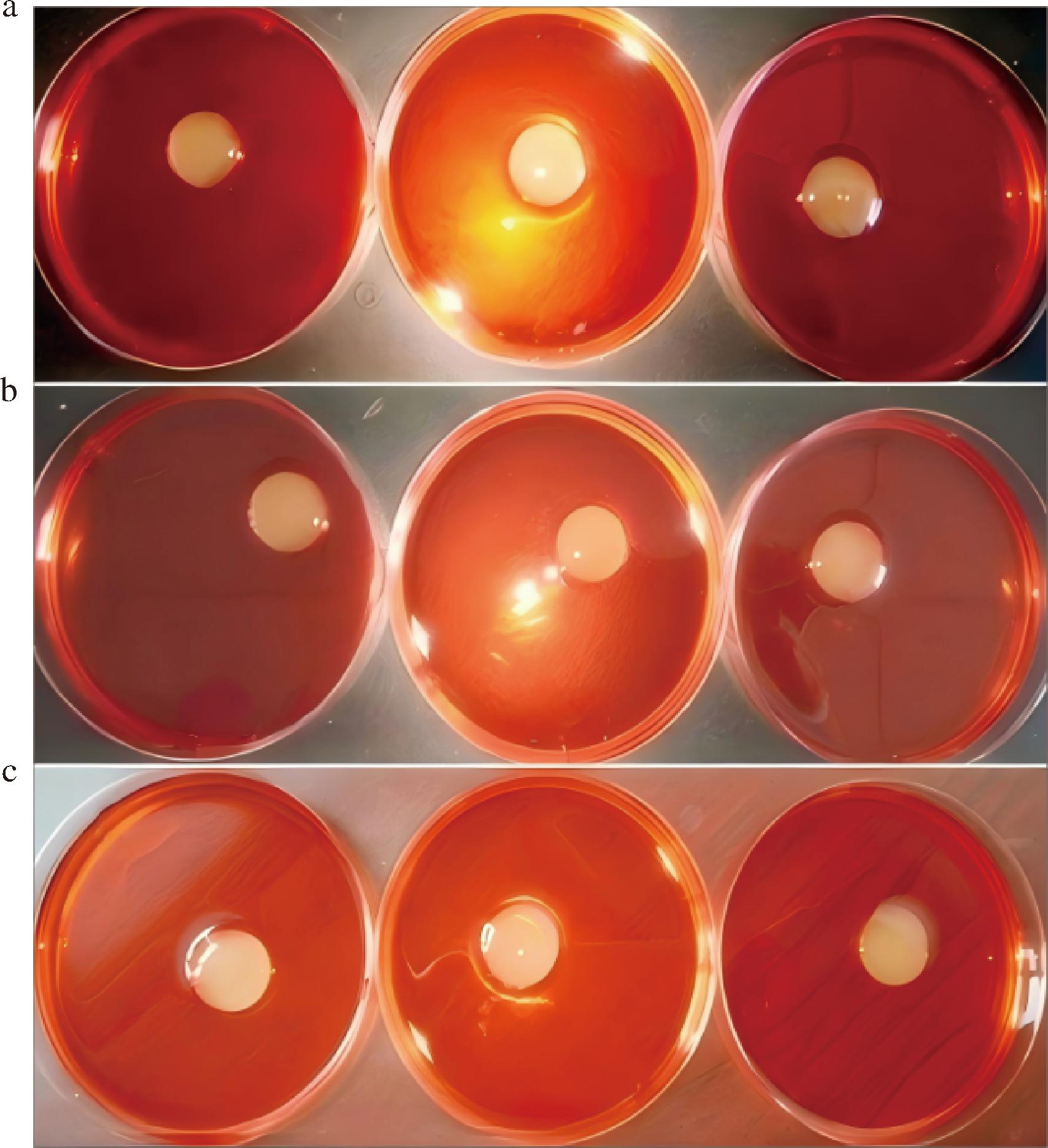
a-PC1 重组菌株(1012WT)发酵液;b-CX4 重组菌株(WZ1)发酵液;c-PC4 重组菌株(WZ1)发酵液
图5 重组菌株发酵液排油圈实验结果
Fig.5 The recombinant bacterium of oil spreading
进一步比较发现,2种菌株发酵液及其脂肽类提取物在对革兰氏阳性菌(如金黄色葡萄球菌)、革兰氏阴性菌(如大肠杆菌)及真菌(如黑曲霉)的抑制实验中均表现出一定抑菌效应,提示其抑菌活性可能与脂肽类物质的存在相关。鉴于本研究仅基于抑菌圈法进行初步功能评价,其作用机制及应用潜力仍有待在后续研究中通过更系统的实验进一步验证。
2.4 重组菌构建与表达效果验证
经表面活性素合成与调控基因克隆及重组质粒构建,将CX4、PC4、PC1导入对应芽孢杆菌中。调控基因测序结果表明:PC1与B.subtilis subsp.subtilis str.168基因组序列一致性为98%,覆盖率84%;部分克隆片段未获得有效测序结果,故未继续后续验证;CX4与PC4分别与B.subtilis TLO3基因组序列的匹配一致性为95%和96%,覆盖率分别为86%和87%。鉴于野生型菌株的排油圈实验数据已在前文2.2节展示,且实验方法与条件一致,本节重组菌功能验证采用数据对比方式进行评估,未另附图像重复展示。
将重组菌株发酵液用于排油圈实验,比较其与原始菌株的排油能力差异(图5)。如表3所示,CX4、PC4和PC1重组株的排油圈直径平均提升约0.2~0.3 cm,说明导入调控因子在一定程度上增强了表面活性素的分泌能力。排油圈扩大结果从功能层面间接验证了重组策略的可行性,为后续通过代谢工程提升目标产物产量提供实验依据。
表3 各物质排油圈直径记录
Table 3 Record of oil displacement ring diameters of various substances
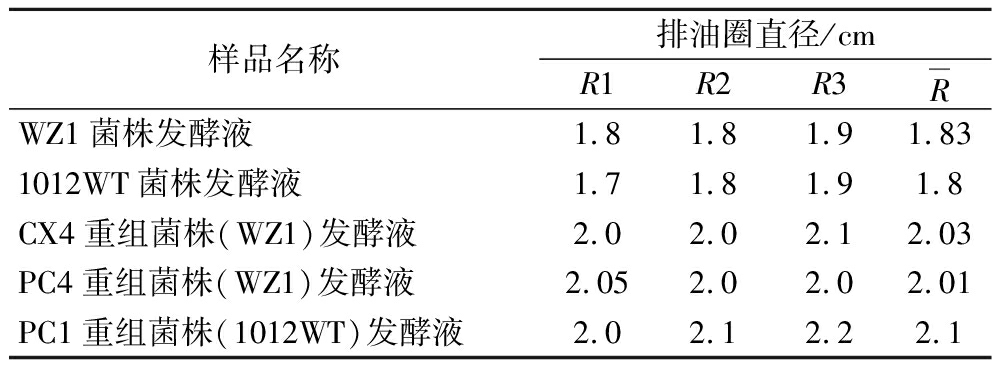
样品名称排油圈直径/cmR1R2R3RWZ1菌株发酵液1.81.81.91.831012WT菌株发酵液1.71.81.91.8CX4重组菌株(WZ1)发酵液2.02.02.12.03PC4重组菌株(WZ1)发酵液2.052.02.02.01PC1重组菌株(1012WT)发酵液2.02.12.22.1
不同调控元件在WZ1菌株与1012 WT菌株中的表现差异提示菌株背景对调控系统响应存在依赖性。考虑实验资源限制,本研究未开展转录组或蛋白水平的机制验证,相关调控通路将在后续工作中进一步解析。
3 结论
实验室分离菌株WZ1经16S rDNA测序鉴定为S.koreensis。通过发酵提取、酸沉淀与甲醇纯化获得脂肽类粗提物,经排油圈实验、TLC显色与HPLC保留时间比对,证实其具有脂肽类表面活性素合成能力。进一步采用牛津杯法评估发酵上清液与脂肽提取物的抗菌活性,结果表明其对革兰氏阳性菌、阴性菌及真菌均具抑制作用。克隆调控基因comX和phrC并导入菌株后,排油圈直径略有增加,提示其可能促进表面活性素表达。该研究为非模式芽孢杆菌在脂肽类表面活性剂合成中的应用提供了实验依据,也为后续合成生物学调控策略探索奠定了基础。相关分子机制仍有待深入研究。
[1] HE B X, SACHLA A J, RUESEWALD S B, et al.The TerC family metal chaperone MeeY enables surfactin export in Bacillus subtilis[J].Journal of Bacteriology, 2025, 207(5):e00088-e00025.
[2] NICOLAS G M.Secondary Metabolites from Bacillus spp.probiotics as potential treatments for multidrug-resistant pathogens:A comprehensive review[J].Current Research in Microbial Sciences, 2025, 8:100392.
[3] HASSANISAADI M.Surfactin as a multifaceted biometabolite for sustainable plant defense:A review[J].Journal of Plant Pathology, 2025, 107(1):149-165.
[4] CHEN X Y, LU Y J, SHAN M Y, et al.A mini-review:Mechanism of antimicrobial action and application of surfactin[J].World Journal of Microbiology and Biotechnology, 2022, 38(8):143.
[5] PARK S A, BHATIA S K, PARK H A, et al.Bacillus subtilis as a robust host for biochemical production utilizing biomass[J].Critical Reviews in Biotechnology, 2021, 41(6):827-848.
[6] 蔡巧贤, 彭倩, 李容博, 等.芽孢杆菌ZYCHH-01的鉴定与分泌产物纯化及其抑菌机理[J].集美大学学报(自然科学版), 2024, 29(4):308-320.CAI Q X, PENG Q, LI R B, et al.Identification, purification of secretory product and antibacterial mechanism of Bacillus ZYCHH-01[J].Journal of Jimei University (Natural Science), 2024, 29(4):308-320.
[7] GUO Z H, SUN J Y, MA Q Y, et al.Improving surfactin production in Bacillus subtilis 168 by metabolic engineering[J].Microorganisms, 2024, 12(5):998.
[8] ROGGIANI M, DUBNAU D.ComA, a phosphorylated response regulator protein of Bacillus subtilis, binds to the promoter region of srfA[J].Journal of Bacteriology, 1993, 175(10):3182-3187.
[9] HAO W L, YANG S H, SHENG Y O, et al.Efficient expression of recombinant proteins in Bacillus subtilis using a rewired gene circuit of quorum sensing[J].Biotechnology Progress, 2025, 41(3):e70007.
[10] YAN X Y, BAO W W, WU Y L, et al.Paradigm of engineering recalcitrant non-model microorganism with dominant metabolic pathway as a biorefinery chassis[J].Nature Communications, 2024, 15:10441.
[11] RAVAGNAN G, SCHMID J.Promising non-model microbial cell factories obtained by genome reduction[J].Frontiers in Bioengineering and Biotechnology, 2024, 12:1427248.
[12] KWON S W, KIM B Y, SONG J, et al.Sporosarcina koreensis sp.nov.and Sporosarcina soli sp.nov., isolated from soil in Korea[J].International Journal of Systematic and Evolutionary Microbiology, 2007, 57(Pt 8):1694-1698.
[13] ZHANG F, HUO K Y, SONG X Y, et al.Engineering of a genome-reduced strain Bacillus amyloliquefaciens for enhancing surfactin production[J].Microbial Cell Factories, 2020, 19(1):223.
[14] KWON S W, KIM B Y, SONG J, et al.Sporosarcina koreensis sp.nov.and Sporosarcina soli sp.nov., isolated from soil in Korea[J].International Journal of Systematic and Evolutionary Microbiology, 2007, 57(8):1694-1698.
[15] 韩旭东, 张玉苍, 李瑞松, 等.芽孢杆菌ZYCHH-01发酵条件优化及其抑菌物质的研究[J].中国酿造, 2020, 39(2):38-43.HAN X D, ZHANG Y C, LI R S, et al.Fermentation optimization and antibacterial substances of Bacillus sp.ZYCHH-01[J].China Brewing, 2020, 39(2):38-43.
[16] 钱常娣, 李宝庆, 郭庆港, 等.枯草芽孢杆菌菌株BAB-1表面活性素的分离纯化及性质分析[J].植物病理学报, 2011, 41(2):196-202.QIAN C D, LI B Q, GUO Q G, et al.Purification and characterization of surfactin produced by Bacillus subtilis strain BAB-1[J].Acta Phytopathologica Sinica, 2011, 41(2):196-202.
[17] QIAO J Q, BORRISS R, SUN K, et al.Research advances in the identification of regulatory mechanisms of surfactin production by Bacillus:A review[J].Microbial Cell Factories, 2024, 23(1):100.
[18] 陈蓉明, 林跃鑫, 黄谚谚.枯草芽孢杆菌ATCC2233产生表面活性素的研究[J].福建轻纺, 2000(12):1-4.CHEN R M, LIN Y X, HUANG Y Y.Research of surfactin produced by Bacillus subtilis ATCC2233[J].The Light &Textile Industries of Fujian, 2000(12):1-4.
[19] 毕思宁, 王彦杰, 左豫虎.生物表面活性剂排油圈检测方法的改进和应用[J].黑龙江八一农垦大学学报, 2009, 21(6):58-60.BI S N, WANG Y J, ZUO Y H.Improvement and application of oil spreading to detect biosurfactant[J].Journal of Heilongjiang Bayi Agricultural University, 2009, 21(6):58-60.
[20] 赵秀香, 赵柏霞, 马镝, 等.枯草芽孢杆菌SN-02抑菌物质的分离、纯化及结构测定[J].植物保护学报, 2008,35(4):322-326.ZHAO X X, ZHAO B X, MA D, et al.Isolation,purification and structure analysis of the antagonistic substance produced by Bacillus subtilis SN-02[J].Journal of Plant Protection, 2008,35(4):322-326.
[21] 张毅, 牛德强, 严涛, 等.凝结芽孢杆菌BC99代谢产物抑菌效果研究[J].食品研究与开发, 2022, 43(9):192-197.ZHANG Y, NIU D Q, YAN T, et al.Antibacterial effect of the metabolites of Bacillus coagulans BC99[J].Food Research and Development, 2022, 43(9):192-197.
[22] 彭冲. 表达鸭坦布苏病毒E蛋白枯草芽孢杆菌载体的构建及免疫原性分析[D].泰安:山东农业大学, 2023.PENG C.Construction and immunogenicity of Bacillus subtilis expressing DTMUV E Protein [D].Taian:Shandong Agricultural University, 2023.
[23] 孙同毅, 邵建新, 高媛媛, 等.碱性蛋白酶PB92在枯草芽孢杆菌中高效转化方法的建立及其分泌表达[J].江苏农业学报, 2009, 25(3):534-537.SUN T Y, SHAO J X, GAO Y Y, et al.Establishment of high-efficiency transformation and expression of the gene encoding alkaline protease PB92 in Bacillus subtilis DB104[J].Jiangsu Journal of Agricultural Sciences, 2009, 25(3):534-537.
[24] 王建彬. 海藻糖合酶基因(AE015451.1)在枯草芽孢杆菌中的表达[D].济南:齐鲁工业大学, 2013.WANG J B.Expression of trehalose synthase gene (AE015451.1) in B.subtilis[D].Jinan:Qilu University of Technology, 2013.
[25] 王世伟, 李萌, 孙艳梅, 等.韩国芽孢八叠球菌CGMCC No.5915应用及脂肽类表面活性素制备方法和组合物:中国, CN107828838B[P].2020-11-03.WANG S W, LI M, SUN Y M, et al.Application of Bacillus korea CGMCC No.5915 and preparation method and composition of lipopeptide surfactin:China, CN107828838B[P].2020-11-03.