根据国际有关菌种分类地位的变化情况,2022年卫健委更新发布了《可用于食品的菌种名单》及《可用于婴幼儿食品的菌种名单》,共12个菌种被更新为不同种属。其中发酵乳杆菌和罗伊氏乳杆菌分别更名为发酵粘液乳杆菌和罗伊氏粘液乳杆菌。此2种菌原来隶属于乳杆菌属,更新后分类学地位隶属于粘液乳杆菌属。粘液乳杆菌属(Limosilactobacillus)是乳杆菌属的成员,被收录于欧洲食品安全局资格认定(Qualified Presumption of Safety,QPS)名单、美国食品药品监督管理局(Food and Drug Administration,FDA)公认安全物质(generally recognized as safe,GRAS)名单[1]。其中发酵粘液乳杆菌(Limosilactobacillus fermentum)和罗伊氏粘液乳杆菌(Limosilactobacillus reuteri)是粘液乳杆菌属的重要成员[2]。粘液乳杆菌属因其具有调节肠道菌群、增强宿主免疫力、抑制病原菌、降低胆固醇水平以及缓解乳糖不耐受等优良的益生特性[3-5],作为重要的功能性菌株在食品工业中有着重要的地位[6]。作为食品用菌种(microbial food culture,MFC),主要应用于饼干、酸奶、果冻及婴幼儿食品等产品的生产[7-8]。在发酵食品、益生菌制品等领域发挥着重要的应用价值[9-10]。
MFC的安全性、稳定性及功能性直接影响食品品质和消费者的健康[11-12]。发酵粘液乳杆菌已列入欧盟QPS推荐的生物制剂列表,列入国际乳业联盟“具有在食品中安全使用记录史的微生物清单”。并通过FDA的GRAS认定,可用于婴幼儿配方粉,在欧洲和亚洲等多个国家(地区)均有销售。2010年发酵乳杆菌和罗伊氏乳杆菌列入我国《可用于食品的菌种名单》。2014年6月,原卫计委批准罗伊氏乳杆菌DSM17938作为新食品原料可用于婴幼儿食品;2016年6月,批准发酵乳杆菌CECT5716列入《可用于婴幼儿食品的菌种名单》,可用于婴幼儿食品;2010年罗伊氏乳杆菌被列入我国《可用于食品的菌种名单》。《世界胃肠病学组织全球指南(2017更新版)》建议婴儿服用罗伊氏乳杆菌DSM17938作为预防婴儿肠绞痛的措施。
随着食品发酵工业的快速发展及食品安全监管日益加强,食品行业需要MFC鉴定方法以保证生产原料的品质和真实性[13-15]。由于缺少相关检验方法,阻碍了此类新型可食用菌种的产品开发及利用,使国内企业的产品在国际上的竞争力不足,无法适应行业发展趋势。2003年制定的联合国食品与农业组织/世界卫生组织《食品益生菌评价指南》中推荐采用脉冲场凝胶电泳(plused field gel electrophoresis,PFGE)、随机扩增多态性DNA标记(random amplified polymorphic DNA,RAPD)、全基因组测序(whole genome sequencing,WGS)及特异性PCR等技术对益生菌进行鉴定[16]。现行GB 4789.34—2016《食品安全国家标准 食品微生物学检验 双歧杆菌检验》和GB 4789.35—2023《食品安全国家标准 食品微生物学检验 乳酸菌检验》中的方法主要包括乳杆菌属、双歧杆菌属和嗜热链球菌属活菌计数,适用于部分菌种鉴定,未完成包括粘液乳杆菌属菌种鉴定方法。而粘液乳杆菌属与其他乳酸菌在形态学和生理生化特性上较为相似[17],容易导致误检或漏检。为保障可食用菌种行业的健康发展,满足市场监管需求,应尽快制定粘液乳杆菌属菌种检测方法,解决我国可食用菌种鉴定方法缺失的问题,保障食品质量、维护消费者权益[18]。本文开发了一种实时荧光PCR检测方法,通过设计特异性引物和探针,优化PCR反应条件,实现对粘液乳杆菌属的高效鉴定。同时检测粘液乳杆菌属分离株的耐药基因,评估MFC的生物安全性。采用16S rRNA基因测序鉴定粘液乳杆菌属分离株,验证本文建立qPCR方法的准确性和可靠性。
1 材料与方法
1.1 材料与试剂
1.1.1 实验样品
本文用于包容性实验的粘液乳杆菌属菌种均分离于纯菌粉样品,通过16S rRNA基因测序鉴定,由本实验室验证留存。
用于交叉实验的33个阴性菌株均分离于食品样品,由本实验室验证留存。包括动物双歧杆菌乳亚种、两歧双歧杆菌、短双歧杆菌、长双歧杆菌长亚种、长双歧杆菌婴儿亚种、嗜酸乳杆菌、鼠李糖乳酪杆菌、植物乳植杆菌、干酪乳酪杆菌、副干酪乳酪杆菌、格氏乳杆菌、唾液链球菌嗜热亚种、乳酸片球菌和戊糖片球菌;芽孢杆菌包括志贺氏杆菌、普通变形杆菌、费氏柠檬酸杆菌、产气肠杆菌、阪崎肠杆菌、肠炎沙门氏菌、小肠结肠炎耶尔森、大肠埃希氏菌、恶臭假单胞菌、副溶血性弧菌、哈维弧菌、金黄色葡萄球菌、单核李斯特氏菌、枯草芽孢杆菌、解淀粉芽孢杆菌、短小芽孢杆菌、短短芽孢杆菌、地衣芽孢杆菌和巨大芽孢杆菌。
1.1.2 材料与试剂
溶菌酶溶液(Code No.RT401)、细菌基因组DNA提取试剂盒(Code No.DP302-02), 天根生化科技有限公司;Probe qPCR Mix(Code No.390A)、TB Green Premix Ex TaqⅡ(Tli Rnase H Plus)(Code No.RR820Q)、TaKaRa 16S rRNA BacteriaL Identification PCR Kit(Code No.RR176)、Agarose Regular(Code No.5260), 宝生物工程(大连)有限公司;BigDyeTM Direct 循环测序试剂盒(Code No.4458687)、Hi-DiTM Formamide (Code No.4311320), 赛默飞世尔科技公司。粘液乳杆菌属引物探针、耐药基因引物委托生工生物工程(上海)股份有限公司合成。
1.2 仪器与设备
ZXDP-A205恒温培养箱,上海智诚分析仪器制造有限公司;MX-S涡旋混匀仪,大龙兴创实验仪器(北京)股份公司;PX2242H电子天平,奥豪斯国际贸易(上海)有限公司;QuantStudio 6 和 7 Flex实时荧光定量PCR定量系统、1300 SERIES A2生物安全柜、ABI3130基因序列分析仪,赛默飞世尔科技公司;HWS-12恒温水浴锅,上海一恒科学仪器有限公司;BioPhotometer plus核酸蛋白测读仪,德国艾本德股份公司;EPS100电泳仪,上海天能科技有限公司;GDS-8000凝胶成像系统,美国UVP;S1000PCR扩增仪,美国伯乐生命医学产品公司。
1.3 实验方法
1.3.1 引物与探针
1.3.1.1 qPCR靶标序列选择与引物探针设计
基于NCBI核苷酸数据库(www.NCBI.nlm.nih.gov/nucleoties),从NCBI数据库中检索发酵粘液乳杆菌和罗伊氏粘液乳杆菌的基因序列,采用DNAStar软件分析其同源性。分别采用发酵粘液乳杆菌dnaJ基因和罗伊氏粘液乳杆菌groL基因为靶标基因序列设计特异性引物和探针。这2个基因区域的碱基序列在粘液乳杆菌属种间遗传变异较大,而在种内遗传变异较小,相对稳定,具有高度的鉴定能力。
在探针的5′端标记荧光报告基团(Reporter)6-羧基荧光素(6-FAM),在3′端标记淬灭基团(Quencher)Black Hole Quencher 1(BHQ1)。设计发酵粘液乳杆菌的上游引物序列为5′-TCCGTCCGCACCACAAC-3′,下游引物序列为5′-GACGGCATCCATGAAGTCAA-3′,探针序列为5′-6-FAM-AGGGCGCGACCTCCAGTACA-CGBHQ1-3′;罗伊氏粘液乳杆菌的上游引物序列为5′-GCCGGTGATGGTACTACAACTG-3′,下游引物序列为5′-AGCAACTTCGGTAGCCTTGTCA-3′,探针序列为5′-6-FAM-ATGAAGAACGTTACCTCTGGTGCAAACCC-ABHQ1-3′。
1.3.1.2 耐药基因引物
MFC耐药性是安全性评价中较为突出的问题。本文合成耐药基因的五类抗生素10个耐药基因的qPCR引物序列,包括四环素类、磺胺类、喹诺酮类、酰胺醇类和氨基糖苷类耐药基因,用于粘液乳杆菌属食品分离株耐药基因的筛查。表1列出了本研究中用于耐药基因筛查的引物序列信息。
表1 用于耐药基因筛查的引物序列
Table 1 Primer sequence for the screening of drug resistance genes

抗生素类别基因引物序列(5′-3′)参考文献四环素类tetAFWGCTACATCCTGCTTGCCTTC[19]RVCATAGATCGCCGTGAAGAGG磺胺类Sul1FWCGCACCGGAAACATCGCTGCAC[20]RVTGAAGTTCCGCCGCAAGGCTCGSul2FWTCCGGTGGAGGCCGGTATCTGG[20]RVCGGGAATGCCATCTGCCTTGAG喹诺酮类qnrAFWAGGATTTCTCACGCCAGGATT[21]RVCCGCTTTCAATGAAACTGCAqnrDFWAGTGAGTGTTTAGCTCAAGGAG[21]RVCAGTGCCATTCCAGCGATTqnrSFWGTATAGAGTTCCGTGCGTGTGA[21]RVGGTTCGTTCCTATCCAGCGATT酰胺醇类floRFWCGGTCGGTATTGTCTTCACG[22]RVTCACGGGCCACGCTGTATCfrFWTGTGCTACAGGCAACATTGGAT[22]RVCAAATACTTGACGGTTGGCTAGAcmlAFWGCCAGCAGTGCCGTTTAT[22]RVGGCCACCTCCCAGTAGAA氨基糖苷类Aac(6′)-1b-crFWTGCGATGCTCTATGAGTGGCTA[23]RVCTCGAATGCCTGGCGTGTTT
1.3.2 样品前处理及细菌DNA提取
分别称取菌粉样品约0.1 g于9 mL稀释液中混匀,10倍系列稀释至适宜梯度,取100 μL混合样液涂布于MRS琼脂培养基中,(36±1)℃恒温厌氧培养48 h。挑取单菌落于营养肉汤中37 ℃恒温厌氧培养24 h,所得菌液用于DNA提取。使用细菌基因组DNA提取试剂盒从纯菌粉样品中提取细菌DNA。
1.3.3 实时荧光PCR方法的建立
实时荧光PCR主混合物的组成包括12.5 μL 1×Probe qPCR Mix、0.5 μL PCR Forward Primer、0.5 μL PCR Reverse Primer、1 μL PCR Primer Probes和5 μL细菌DNA模板,加上无核酸酶水,最终体积为25 μL。
qPCR反应程序:90 ℃ 30 s,1个循环;95 ℃ 5 s, 60 ℃ 30 s, 40个循环。
1.3.4 特异性和交叉反应性分析
提取验证留存的粘液乳杆菌属菌株基因组DNA,用于交叉反应实验的33株阴性菌株基因组DNA,分别采用发酵粘液乳杆菌dnaJ基因和罗伊氏粘液乳杆groL基因的特异性引物和探针进行特异性实验,每个样本材料DNA分析重复测试3次。
1.3.5 扩增效率分析
为了计算qPCR的扩增效率(E),以连续梯度稀释发酵粘液乳杆菌和罗伊氏粘液乳杆菌的基因组DNA作为模板,制备6个系列稀释水平。每个稀释水平在重复性条件下进行2次运行。将每个稀释水平获得的平均阈值循环值(Ct值)与DNA浓度作图,使用GraphPad Prism软件进行线性回归分析。使用回归线的斜率,用公式(1)计算qPCR的扩增效率(E),以百分比表示。根据《定性实时PCR方法的单一实验室验证指南》要求,回归曲线的斜率应为-3.9~-2.9,对应的qPCR效率范围应为80%~120%。线性曲线的相关系数R2是衡量qPCR反应线性度的一个指标,每个目标的R2应该≥0.98。
(1)
1.3.6 灵敏度分析
qPCR分析方法的灵敏度由LOD95%值表示。采用MedCalc软件进行正态分布分析,获得LOD95%值和95%的置信区间。采用连续梯度稀释发酵粘液乳杆菌和罗伊氏粘液乳杆菌的基因组DNA作为模板,制备5个系列稀释水平,每个稀释水平重复测试6次,确定每个分析的最低拷贝数。
1.3.7 实际样品检测
1.3.7.1 方法验证
本文共收集6个食品样品分离株,包括2个含有发酵粘液乳杆菌的食品样品和4个含有罗伊氏粘液乳杆菌的食品样品。采用本文建立的实时荧光PCR方法对分离株进行鉴定,同时基于16S rRNA基因测序进行菌种鉴定,验证2种方法的一致性,每个样本材料DNA分析重复测试不少于3次。
1.3.7.2 分离株耐药基因筛查
通过SYBR Green qPCR测试从食品样品中分离的发酵粘液乳杆菌和罗伊氏粘液乳杆菌的耐药性。SYBR qPCR在QuantStudioTM Real-Time PCR 分析仪上进行。使用TB Green Premix Ex TaqⅡ(Tli Rnase H Plus) 进行qPCR分析。SYBR qPCR反应体系组成包括12.5 μL 2×TB Green Premix Ex TaqⅡ、1 μL PCR Forward Primer、1 μL PCR Reverse Primer和2 μL细菌DNA模板,加上平衡的无核酸酶水,最终体积为25 μL。
SYBR qPCR的反应条件为:95 ℃ 30 s,1个循环;95 ℃ 5 s,60 ℃ 34 s,40个循环;95 ℃ 15 s,60 ℃ 1 min,95 ℃ 15 s,1个循环。
2 结果与分析
2.1 引物和探针序列特异性比对
以发酵粘液乳杆菌(GenBank:CP050919.1)和罗伊氏粘液乳杆菌(GenBank:CP089962.1)的DNA基因片段为靶标基因片段,对本文设计的qPCR引物(Fw/Rev)和TaqMan探针(probe)在NCBI上进行同源性比对(图1)。进一步采用实际样品验证标准方法的特异性。

A-发酵粘液乳杆菌比对结果;B-罗伊氏粘液乳杆菌比对结果
图1 粘液乳杆菌属引物探针序列比对结果
Fig.1 Sequence alignment results of Limosilactobacillus
2.2 qPCR特异性和交叉反应性
基于TaqMan探针法qPCR检测粘液乳杆菌属的排除实验结果显示,本文设计的引物探针对发酵粘液乳杆菌和罗伊氏粘液乳杆菌的特异性为100%,对33种乳杆菌及其他菌种均无交叉反应(图2)。
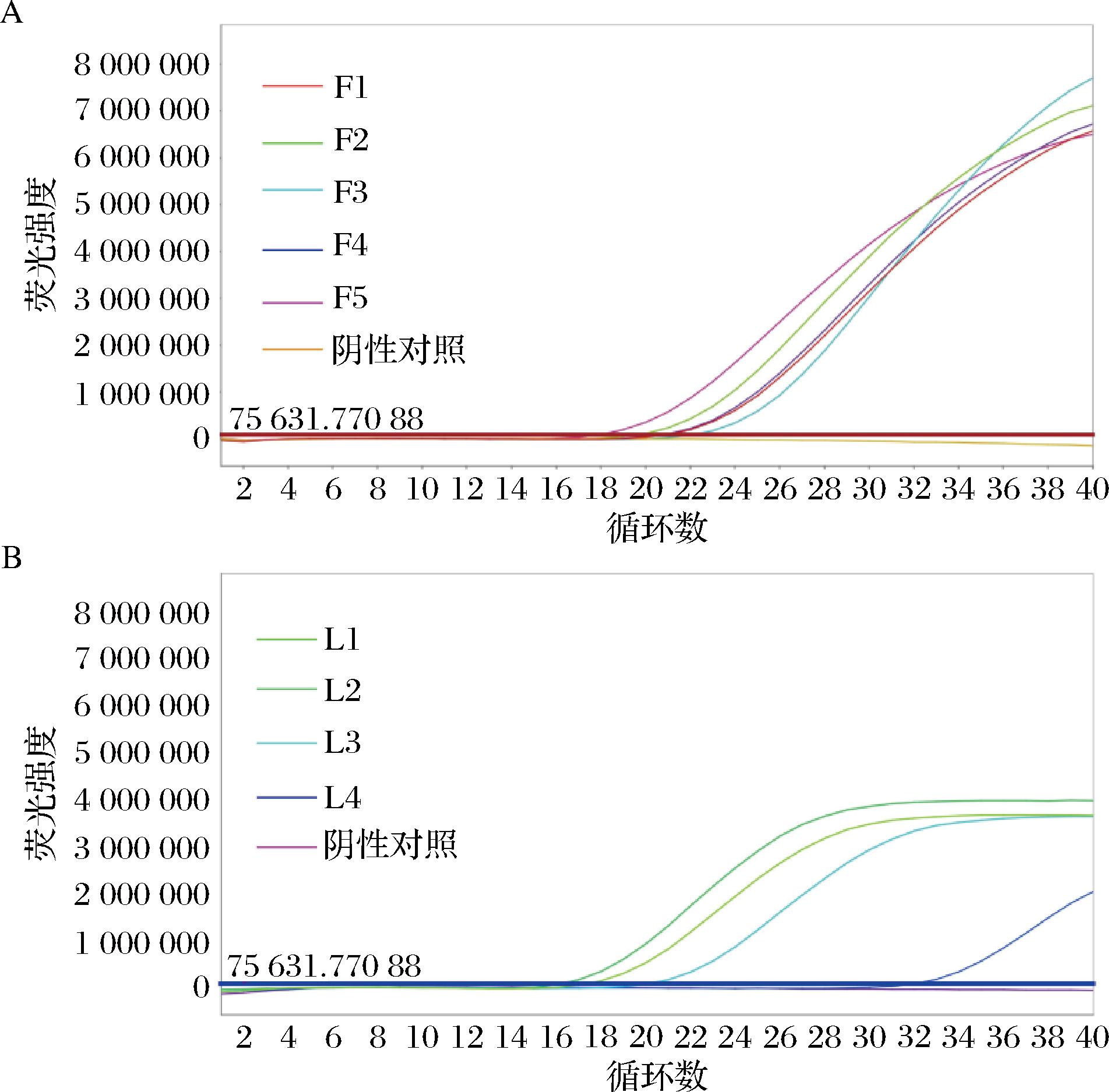
A-发酵粘液乳杆菌特异性扩增曲线;B-罗伊氏粘液乳杆菌特异性扩增曲线
图2 粘液乳杆菌属分离株特异性扩增曲线
Fig.2 Limosilactobacillus isolated strain specific amplification curve
注:F为发酵粘液乳杆菌纯菌粉样品DNA,L为罗伊氏粘液乳杆菌纯菌粉样品DNA(下同)。
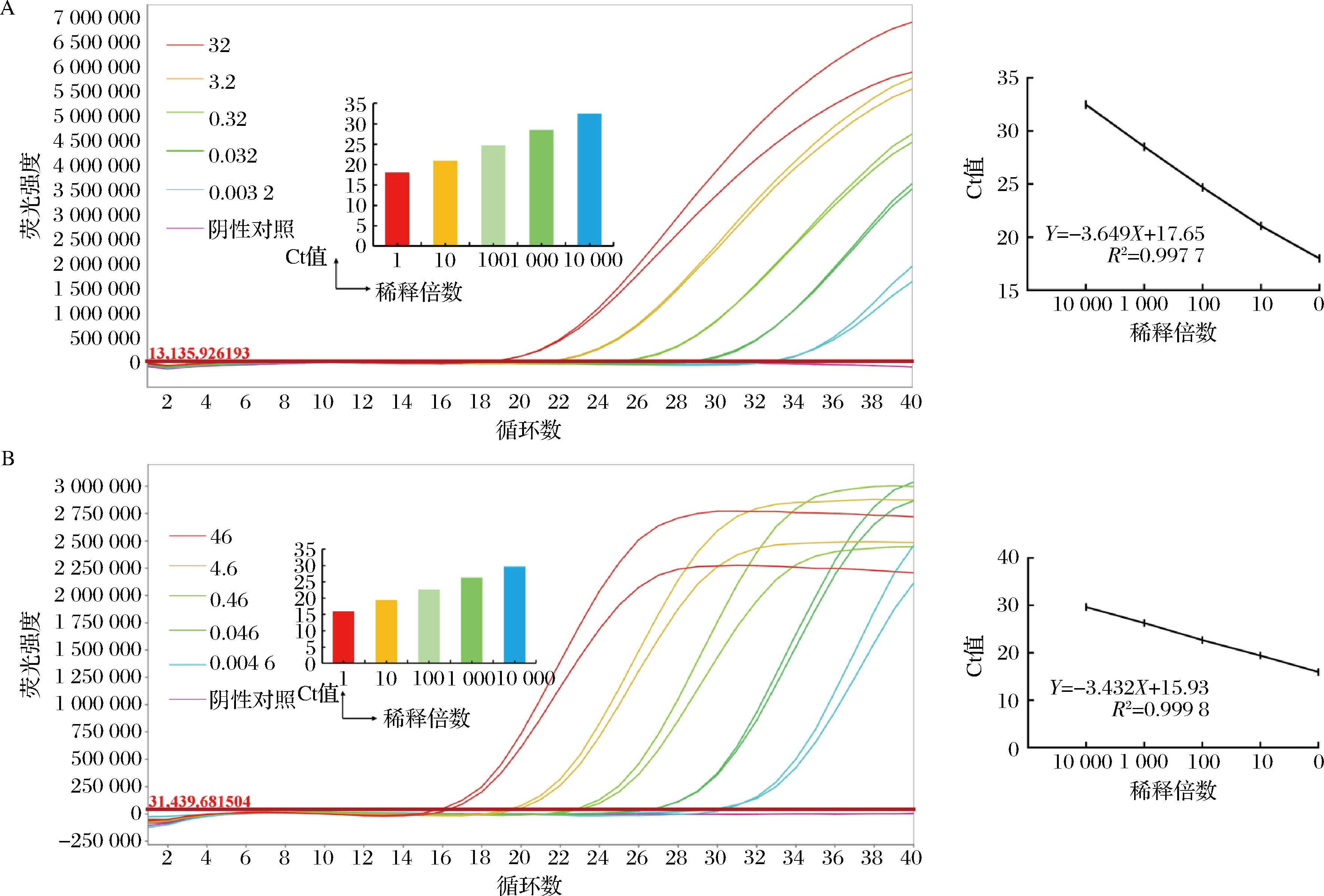
A-发酵粘液乳杆菌的扩增效率曲线(左)和线性回归曲线(右);B-罗伊氏粘液乳杆菌的扩增效率曲线(左)和线性回归曲线(右)
图3 粘液乳杆菌属分离株扩增效率分析
Fig.3 Analysis of the amplification efficiency of Limosilactobacillus isolated strain
2.3 qPCR扩增效率分析
基于发酵粘液乳杆菌(提取基因组DNA初始质量浓度3.2×104 pg/μL)和罗伊氏粘液乳杆菌(提取基因组DNA初始质量浓度4.6×104 pg/μL)的DNA作为模板,制备6个系列稀释水平,发酵粘液乳杆菌6个稀释梯度的质量浓度分别为3.2×104、3.2×103、3.2×102、3.2×10、3.2、3.2×10-1 pg/μL,罗伊氏粘液乳杆菌6个稀释梯度的质量浓度分别为4.6×104、4.6×103、4.6×102、4.6×10、4.6、4.6×10-1 pg/μL。根据Ct值与荧光强度变化绘制荧光曲线;根据Ct值与DNA浓度绘制线性回归曲线。将分析效率确定为回归线的斜率,根据公式(1),显示了Ct值与DNA浓度之间有很好的线性关系(图3)。发酵粘液乳杆菌qPCR线性回归曲线相关系数R2为0.997 7,斜率为-3.649,扩增效率E为87.9%;罗伊氏粘液乳杆菌qPCR线性回归曲线相关系数R2为0.999 8,斜率为-3.432,扩增效率E为95.6%。该结果符合《定性实时PCR方法的单一实验室验证指南》要求。
2.4 灵敏度分析
使用目标DNA作为模板,LOD95%值表示为每次检测的最高可稀释水平(通常以95%置信度为准)。发酵粘液乳杆菌5个稀释梯度的质量浓度分别为32、20.19、10.12、3.20、2.02 pg/μL;罗伊氏粘液乳杆菌5个稀释梯度的质量浓度分别为46、29.02、14.55、4.60、2.90 pg/μL。通过正态分布分析,将复孔检测概率(样本阳性个数与重复次数的比值)作为纵轴,DNA浓度作为横轴,先作散点图,再利用MedCalc软件使用Probit模型进行拟合(图4),得到发酵粘液乳杆菌的LOD95%值为1.91×102 pg/μL,95%的置信区间为3.09×104~3.67×104 pg;罗伊氏粘液乳杆菌的LOD95%值为5.33×102 pg/μL,95%的置信区间为2.64×104~4.07×104 pg。
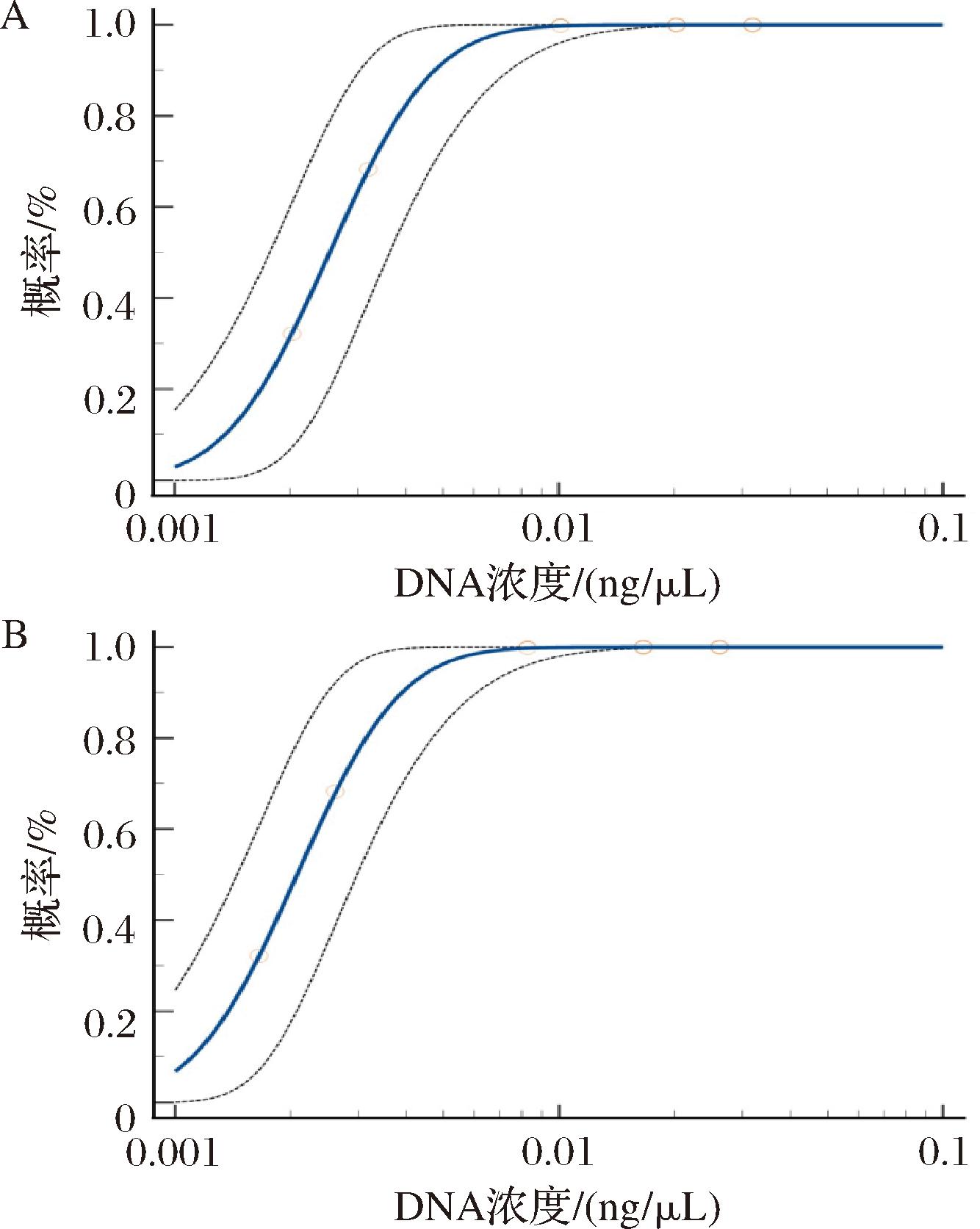
A-发酵粘液乳杆菌的LOD值;B-罗伊氏粘液乳杆菌的LOD值
图4 qPCR检验粘液乳杆菌属DNA的灵敏度
Fig.4 Gradient dilution steps for testing LimosilactobacillusDNA using for qPCR
2.5 实际样品检测
2.5.1 方法验证
基于本文建立的qPCR方法从6个食品样品分离得到2株发酵粘液乳杆菌和4株罗伊氏粘液乳杆菌(图5),通过16S rRNA基因测序进行比对验证。经NCBI blast比对,测序结果如电子版增强出版附图1(https://doi.org/10.13995/j.cnki.11-1802/ts.043796)所示。比对验证结果如表2所示,发酵粘液乳杆菌和罗伊氏粘液乳杆菌引物探针均可以检测出食品样品中粘液乳杆菌属,与16S rRNA基因测序结果一致,且与样品标签标识相符。
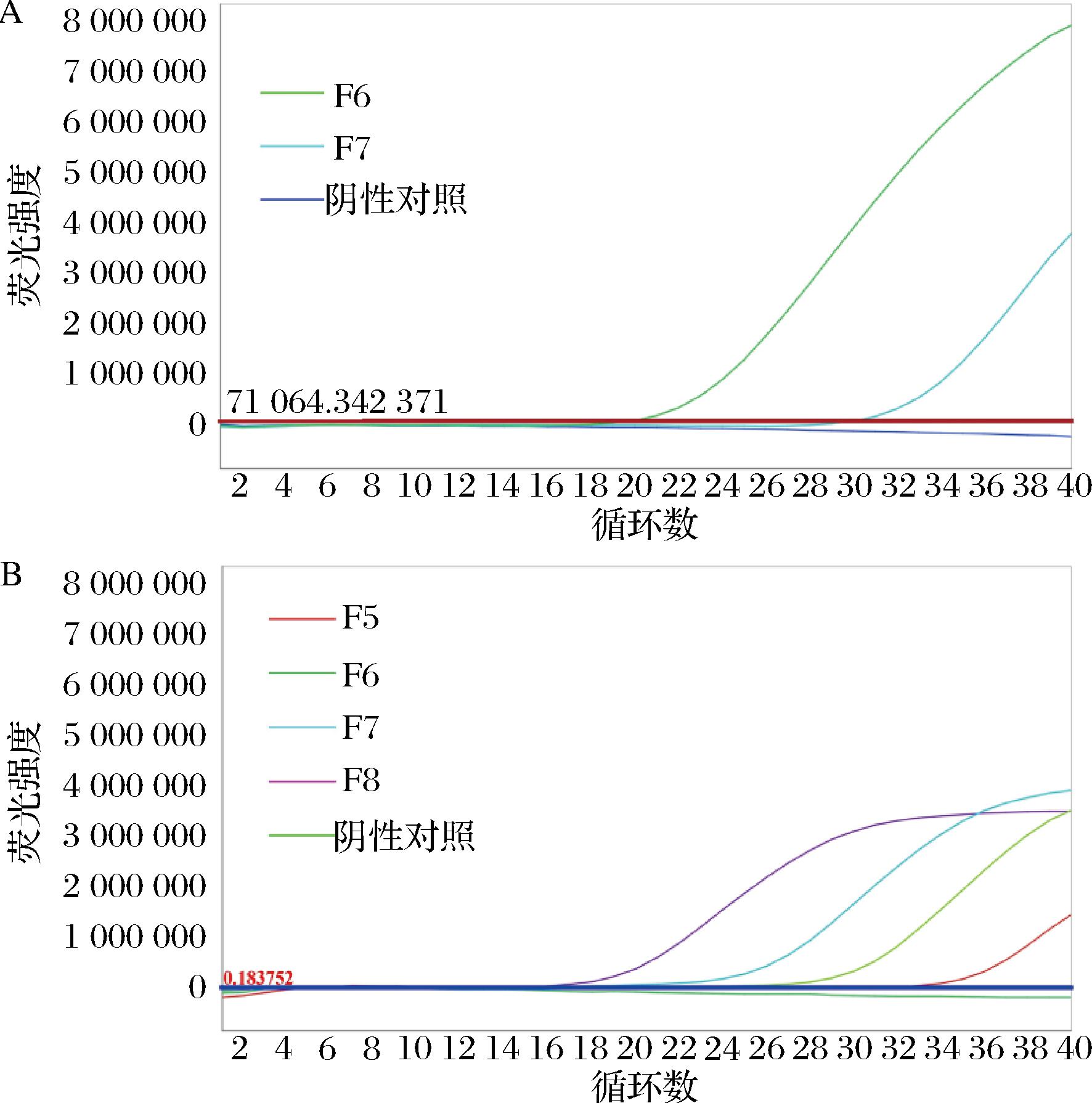
A-发酵粘液乳杆菌特异性扩增曲线;B-罗伊氏粘液乳杆菌特异性扩增曲线
图5 食品样品中粘液乳杆菌属分离株实时荧光PCR检测结果
Fig.5 Real-time fluorescent PCR results ofLimosilactobacillus isolated strains from food samples
表2 食品样品中的粘液乳杆菌属分离株测序结果
Table 2 Sequencing results of Limosilactobacillus isolated strains from food samples

样品编号16S rRNA测序比对结果NCBI比对相近菌株号16S rRNA鉴定结果实时荧光qPCR鉴定结果F6Lactobacillus fermentum strain HBUAS53211 16S ribosomal RNA gene, partial sequenceHBUAS53211发酵粘液乳杆菌发酵粘液乳杆菌F7Limosilactobacillus fermentum strain OJM 1 16S ribosomal RNA gene, partial sequenceOJM 1发酵粘液乳杆菌发酵粘液乳杆菌L5Lactobacillus reuteri strain NM12_1-47 16S ribosomal RNA gene, partial sequenceNM12_1-47罗伊氏粘液乳杆菌罗伊氏粘液乳杆菌L6Limosilactobacillus reuteri strain PB-LR09 16S ribosomal RNA gene, partial sequencePB-LR09罗伊氏粘液乳杆菌罗伊氏粘液乳杆菌L7Lactobacillus reuteri strain CICC6226 16S ribosomal RNA gene, partial sequenceCICC6226罗伊氏粘液乳杆菌罗伊氏粘液乳杆菌L8Lactobacillus reuteri strain IDCC3701 16S ribosomal RNA gene, partial sequenceIDCC3701罗伊氏粘液乳杆菌罗伊氏粘液乳杆菌
2.5.2 分离株耐药基因筛查
本文使用五类抗生素10个耐药基因引物通过SYBR Green荧光染料法分析食品中粘液乳杆菌属的耐药基因。分离株耐药基因检测结果显示,5株发酵粘液乳杆菌分离株和4株罗伊氏粘液乳杆菌分离株中四环素类tetA耐药基因检出率为100%,其他耐药基因均为阴性(图6)。
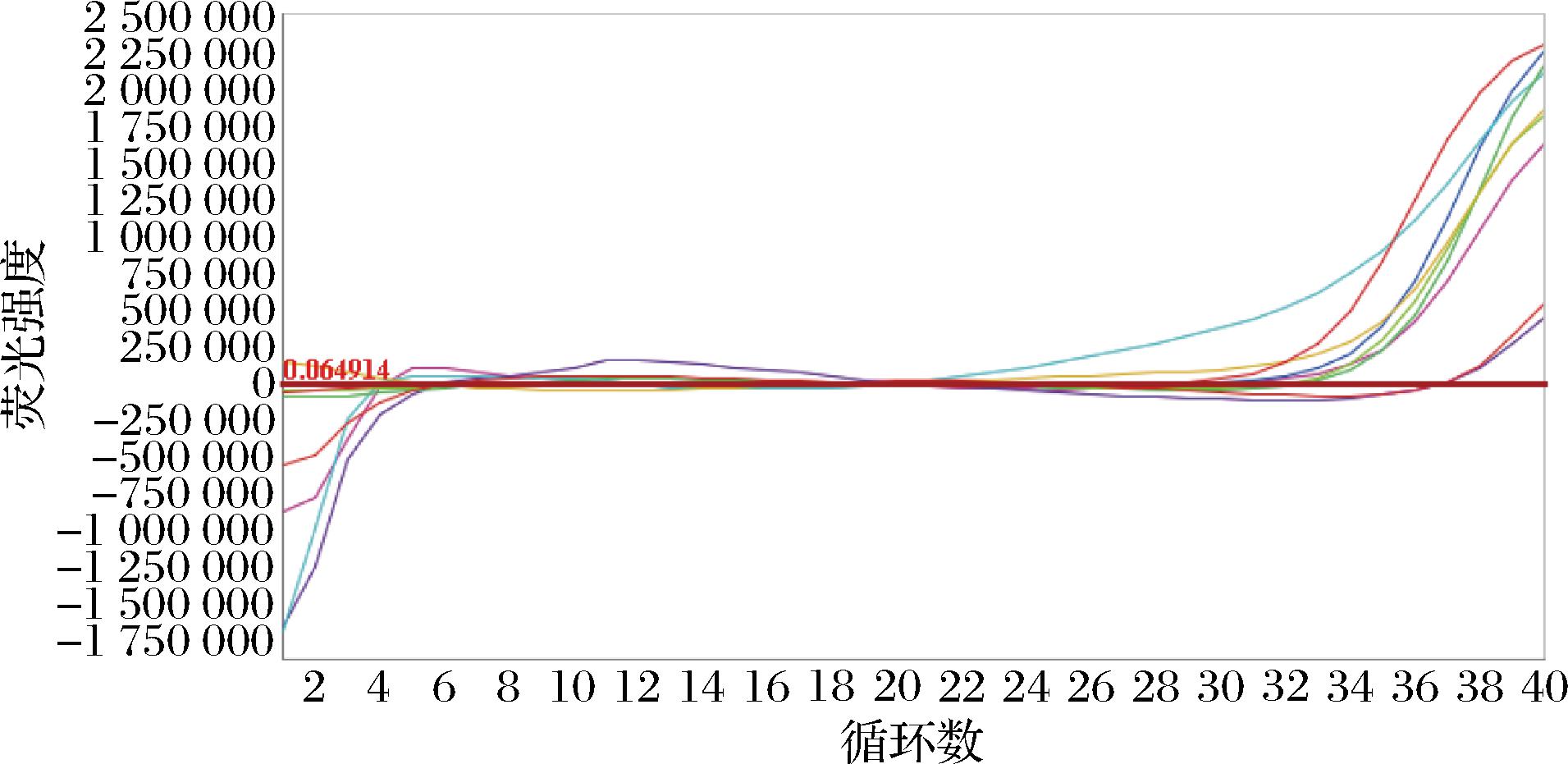
图6 粘液乳杆菌属分离株耐药基因tetA筛查结果
Fig.6 Drug resistance gene tetA text results ofLimosilactobacillus isolated strains
3 讨论
本文开发了MFC发酵粘液乳杆菌和罗伊氏粘液乳杆菌实时荧光PCR检验方法,方法的特异性好,对于近种的乳酸杆菌及其他乳酸菌没有发生交叉反应。得到发酵粘液乳杆菌的扩增效率(E)为87.9%、罗伊氏粘液乳杆菌的扩增效率(E)为95.6%,确保了食品中粘液乳杆菌属检测的准确性;在灵敏度方面,概率回归分析结果表明,发酵粘液乳杆菌的LOD95%值为1.91×102 pg/μL、罗伊氏粘液乳杆菌的LOD95%值为5.33×102 pg/μL。检测6个食品样品中分离得到的粘液乳杆菌属菌株,本文建立的基于TaqMan探针的qPCR方法均可以精准检测食品中的发酵粘液乳杆菌和罗伊氏粘液乳杆菌,与16S rRNA基因测序结果一致,验证了qPCR方法的适用性和可靠性。同时本文使用五类抗生素10个耐药基因引物,通过SYBR Green qPCR方法筛查粘液乳杆菌属分离株的耐药性,发现四环素类tetA耐药基因检出率较高,耐药基因可能通过食物链传递给人类,导致人类对四环素类产生耐药性从而影响身体健康,提示目前市场流通食品中的某些粘液乳杆菌菌株存在食品安全隐患。
综上,本文建立的实时荧光PCR方法具有操作简单、检测周期短且灵敏度高的优点,有利于促进可食用菌种行业健康发展,推动功能性食品的开发与应用,为消费者提供更安全、更健康的食品选择,加强此类新型可食用菌种的产品开发及利用,大大增强国内企业粘液乳杆菌属产品在国际上的竞争力。本研究的开发不仅可完善我国食品中粘液乳杆菌属检验方法缺失的问题、促进粘液乳杆菌属菌种制剂行业发展,还为市场管理部门提供监管依据;同时在提高粘液乳杆菌属产品的安全及质量要求方面发挥重大作用,为食品用粘液乳杆菌属的检测提供技术支持,为其他MFC的检测提供参考。
[1] RICCI A, ALLENDE A, BOLTON D, et al. Update of the list of QPS-recommended biological agents intentionally added to food or feed as notified to EFSA 5: Suitability of taxonomic units notified to EFSA until September 2016[J]. EFSA Journal, 2017, 15(3): e04663.
[2] 国家卫生健康委员会. 解读关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告(2022年第4号)[J]. 饮料工业, 2022, 25(5):3-4.National Health Commission of the People’s Republic of China.Interpretation of the announcement on updating the list of bacteria used in food and the list of bacteria used in infant food (No.4, 2022)[J]. Beverage Industry, 2022, 25(5):3-4.
[3] YAQOOB M U, EL-HACK M E A, HASSAN F, et al. The potential mechanistic insights and future implications for the effect of prebiotics on poultry performance, gut microbiome, and intestinal morphology[J]. Poultry Science, 2021, 100(7):101143.
[4] LUO Z C, CHEN A L, XIE A N, et al. Limosilactobacillus reuteri in immunomodulation: Molecular mechanisms and potential applications[J]. Frontiers in Immunology, 2023, 14:1228754.
[5] ANGAL A, SHIDTURE S, SYED J, et al. In vitro adhesion and anti-inflammatory properties of Limosilactobacillus fermentum FS-10 isolated from infant fecal sample[J]. International Microbiology, 2024, 27(1):227-238.
[6] LIN Z S, WU J M, WANG J P, et al. Dietary Lactobacillus reuteri prevent from inflammation mediated apoptosis of liver via improving intestinal microbiota and bile acid metabolism[J]. Food Chemistry, 2023, 404:134643.
[7] GU Y, QIAO R F, JIN B, et al. Effect of Limosilactobacillus fermentum 332 on physicochemical characteristics, volatile flavor components, and Quorum sensing in fermented sausage[J]. Scientific Reports, 2023, 13:3942.
[8] CONSORTIUM H T, LAVALLE L, SAUVAGEOT N, et al. Limosilactobacillus reuteri DSM 17938-containing infant formulas and the associations with gastrointestinal tolerance: A cross-sectional observational study[J]. Nutrients, 2023, 15(3):530.
[9] GIORDANO I, ABUQWIDER J, ALTAMIMI M, et al. Application of ultrasound and microencapsulation on Limosilactobacillus reuteri DSM 17938 as a metabolic attenuation strategy for tomato juice probiotication[J]. Heliyon, 2022, 8(10): e10969.
[10] LEE A H, RODRIGUEZ JIMENEZ D M, MEISEL M. Limosilactobacillus reuteri-a probiotic gut commensal with contextual impact on immunity[J]. Gut Microbes, 2025, 17:2451088.
[11] SØRENSEN H M, ROCHFORT K D, MAYE S S, et al. Bioactive ingredients from dairy-based lactic acid bacterial fermentations for functional food production and their health effects[J]. Nutrients, 2023, 15(22):4754.
[12] ARELLANO K, LIM J, BUCHELI J E V, et al. Identification of safe putative probiotics from various food products[J]. Folia Microbiologica, 2024, 69(5):1053-1068.
[13] YUN Y H, LI J B. Rapid nondestructive testing technology-based biosensors for food analysis[J]. Biosensors, 2023, 13(5):521.
[14] NAMI Y, TAVALLAEI O, KIANI A, et al. Anti-oral cancer properties of potential probiotic lactobacilli isolated from traditional milk, cheese, and yogurt[J]. Scientific Reports, 2024, 14:6398.
[15] LI F Y, LIU J H, MALDONADO-G MEZ M X, et al. Highly accurate and sensitive absolute quantification of bacterial strains in human fecal samples[J]. Microbiome, 2024, 12:168.
MEZ M X, et al. Highly accurate and sensitive absolute quantification of bacterial strains in human fecal samples[J]. Microbiome, 2024, 12:168.
[16] 吴蜀豫, 冉陆. FAO/WHO《食品益生菌评价指南》[J]. 中国食品卫生杂志, 2003, 15(4):377-379.WU S Y, RAN L. FAO/WHO guidelines for the evaluation of food probiotics[J]. Chinese Journal of Food Hygiene, 2003, 15(4):377-379.
[17] PHUJUMPA P, MUANGHAM S, JATUPONWIPHAT T, et al. Comparative genomics-based probiotic relevance of Limosilactobacillus fermentum KUB-D18[J]. Gene, 2022, 840:146747.
[18] WANG X L, YANG S J, LU J, et al. Screening and application of purine degrading Limosilactobacillus fermentum LF-1 from Huangjiu fermentation broth[J]. Journal of the Science of Food and Agriculture, 2023, 103(15):7921-7931.
[19] HUANG M H, QI F F, WANG J, et al. Changes of bacterial diversity and tetracycline resistance in sludge from AAO systems upon exposure to tetracycline pressure[J]. Journal of Hazardous Materials, 2015, 298:303-309.
[20] PEI R T, KIM S C, CARLSON K H, et al. Effect of River Landscape on the sediment concentrations of antibiotics and corresponding antibiotic resistance genes (ARG)[J]. Water Research, 2006, 40(12):2427-2435.
[21] CABELLO F C, GODFREY H P, TOMOVA A, et al. Antimicrobial use in aquaculture re-examined: Its relevance to antimicrobial resistance and to animal and human health[J]. Environmental Microbiology, 2013, 15(7):1917-1942.
[22] LI J, SHAO B, SHEN J Z, et al. Occurrence of chloramphenicol-resistance genes as environmental pollutants from swine feedlots[J]. Environmental Science &Technology, 2013, 47(6):2892-2897.
[23] PARK C H, ROBICSEK A, JACOBY G A, et al. Prevalence in the United States ofaac(6′)-Ib-crEncoding a ciprofloxacin-modifying enzyme[J]. Antimicrobial Agents and Chemotherapy, 2006, 50(11):3953-3955.