可溶性糖是茶叶品质形成的核心物质之一,为茶汤提供甜味基础,更与氨基酸、多酚类等成分协同作用,赋予茶叶栗香、糖香、花果香等独特风味[1]。然而,糖类物质的过量摄入可能引发肥胖、糖尿病、心血管损害等问题[2-4],因此精准测定茶叶中糖含量对品质调控和健康风险评估具有重要意义。
随着分析技术的发展,液相色谱法已成为糖类检测的主流手段并被纳入国家标准方法[5]。在液相色谱检测中,因糖类缺乏紫外显色基团,常依赖示差折光检测器(refractive index detector,RID)或蒸发光散射检测器(evaporative light scattering detector,ELSD)检测[6-7]。RID虽操作便捷、试剂种类少,但存在无法实现梯度洗脱、基线噪音大、可检测糖组分有限等缺陷[8];ELSD虽灵敏度较高、检测限较低,却受平衡时间长及茶叶中多酚、氨基酸等基质干扰严重的制约[9],难以满足复杂基质中糖类精准分析的需求。
为突破检测器限制,衍生化液相色谱法应运而生,主要分为柱前衍生与柱后衍生两类。柱前衍生法中,1-苯基-3-甲基-5-吡唑啉酮是常用衍生剂,可在碱性条件下与还原糖形成稳定衍生物并通过紫外检测器检测[10-11],但需手动衍生且依赖三氯甲烷萃取除杂,更关键的是无法直接检测蔗糖等非还原糖,应用范围受限[12-13]。柱后衍生法则因衍生过程自动化完成、重现性好等优势,在氨基酸、氨基甲酸酯农药等检测中已广泛应用[14-15],但在糖类检测中的研究仍较为匮乏。现有柱后衍生糖检测方法存在明显局限:文献[16]报道的1-萘硼酸柱后衍生荧光法需在pH值为11条件下进行,限制了流动相选择范围;文献[17]描述的磷酸-苯肼法虽可检测多种糖,但因使用高毒性试剂,存在操作风险。
糖分子结构中富含邻二醇基团,这一特征为衍生化检测提供了新思路。研究表明,高碘酸可特异性氧化邻二醇结构生成甲醛、甲酸等产物[18-19],而甲醛与酚试剂[3-甲基-2-苯并噻唑啉酮腙盐酸盐水合物(3-methyl-2-benzothialinone,MBTH)]在温和条件下反应可形成青蓝色化合物,该化合物在630~670 nm处具有最大吸收[20-21]。基于这一理论,本研究创新性地构建了液相色谱-柱后衍生检测体系,实现了茶叶中木糖、果糖、甘露糖、葡萄糖及蔗糖的同时测定。
本研究建立的液相色谱-柱后衍生法,突破现有柱后衍生糖检测方法的局限,采用高碘酸-MBTH衍生体系,无需苛刻pH条件,流动相选择更灵活,且避免了高毒试剂的使用,提高了方法的安全性、适用性,并降低了成本;同时,克服柱前衍生无法检测非还原糖的缺陷,实现还原糖(木糖、果糖、甘露糖、葡萄糖)与非还原糖(蔗糖)的同步分析,拓展了检测范围,可为优良品种选育、栽培措施改良、制茶工艺优化及茶叶品质提升提供新的检测技术支持。
1 材料与方法
1.1 材料与试剂
乙腈(色谱纯),成都市科隆化学品有限公司;高碘酸、酚试剂、磷酸等(分析纯)、5种可溶性糖标准品(木糖、果糖、甘露糖、葡萄糖、蔗糖),上海麦克林生化科技股份有限公司。
茶叶样品:59个不同嫩度的绿茶和红茶(鲜叶标准分别为一芽一叶为主、一芽二三叶为主、一芽三四叶为主),由宜宾职业技术学院教学茶厂提供。样品粉碎过40目筛后密封备用。
1.2 仪器与设备
LC-16液相色谱仪、SPD-16紫外-可见光检测器、316L不锈钢反应线圈(10 m×1/16英寸,内径0.3 mm),岛津仪器(苏州)有限公司;Asahipak NH2P-50 4E色谱柱(250 mm×4.6 mm,5 μm),日本昭和电工株式会社;Vector PCX柱后衍生仪,美国Pickering Laboratories公司;MC-15Pro高速离心机,宁波市鄞州群安实验仪器有限公司;101-0BS电热恒温烘箱,绍兴市尚诚仪器制造有限责任公司;KB5200B超声波清洗器,昆山禾创超声仪器有限公司;Cary 60 UV-Vis分光光度计,美国安捷伦公司。
1.3 实验方法
1.3.1 试剂配制
流动相A为乙腈(含体积分数0.5%H3PO4),流动相B为超纯水(含体积分数0.5%H3PO4),使用前均过0.45 μm滤膜,超声波脱气。
衍生剂A(2.0~5.0 g/L高碘酸溶液):称取2.0、3.0、4.0、5.0 g高碘酸,分别用1 L超声波脱气后的超纯水溶解,过0.45 μm滤膜后置于棕色试剂瓶中。高碘酸为强氧化剂,具有腐蚀性和刺激性,配制时做好安全防护。
衍生剂B(1.0~2.5 g/L MBTH溶液):称取1.0、1.5、2.0、2.5 g MBTH,分别用1 L超声波脱气后的超纯水溶解,过0.45 μm滤膜后置于棕色试剂瓶中。
1.3.2 可溶性糖标准工作溶液的配制
分别准确称取90 ℃下干燥2 h的5种糖标准品适量(精确至0.01 mg),置于50 mL容量瓶中,用水配制成木糖、果糖、甘露糖、葡萄糖和蔗糖质量浓度分别为19.494、11.082、15.868、21.300、24.552 mg/mL的糖混合标准储备液,置于4 ℃冰箱中。使用前稀释成系列糖标准工作溶液。
1.3.3 茶叶测试液制备
茶叶测试液制备参考GB 5009.8—2023《食品安全国家标准 食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖的测定》方法。准确称2.000 g茶样于50 mL离心管,加入20 mL水,涡旋混匀,超声浸提30 min后离心5 min,取上清液过0.45 μm微孔滤膜后上机检测。
1.3.4 柱后衍生系统的改造
基于液相色谱-柱后衍生法检测茶叶中可溶性糖的工作过程如图1所示。该工作系统由分离系统、反应系统和检测系统组成,其中分离系统和检测系统均由液相色谱仪组成,而反应系统由Vector PCX柱后衍生仪、电热恒温烘箱和2段10 m长的不锈钢反应线圈组成,并对Vector PCX柱后衍生仪进行改造。分析柱后的管路、衍生液A的管路连接在Vector PCX柱后衍生仪的三通上,然后连接放置于烘箱中的不锈钢反应线圈A,反应线圈A末端和衍生液B的管路通过不锈钢三通与烘箱中的反应线圈B相连,经过反应后的液体进入紫外检测器检测。
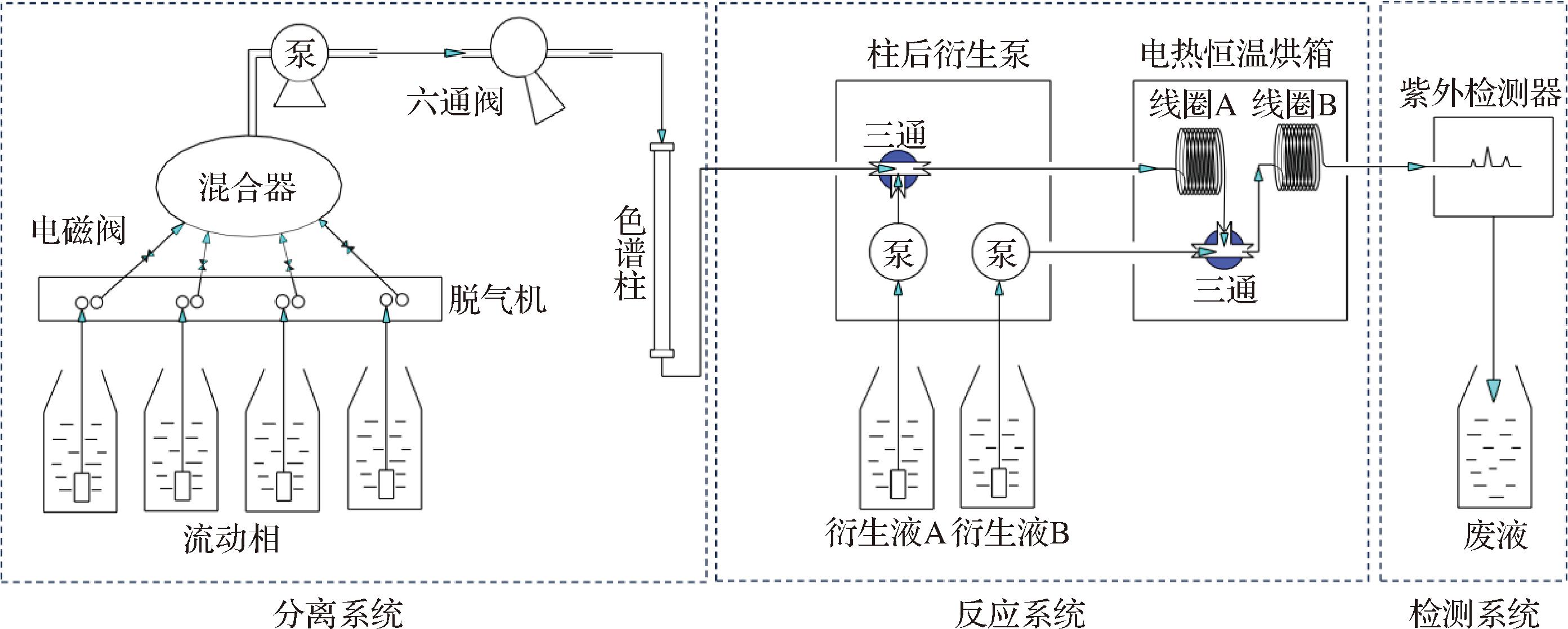
图1 液相色谱-柱后衍生法检测茶叶糖含量的工作过程示意图
Fig.1 Schematic diagram of the working process of liquid chromatography post column derivatization method for detecting sugars in tea leaves
1.3.5 色谱条件
流动相为含体积分数0.5%H3PO4的乙腈-水,采用梯度洗脱。洗脱程序:0~25 min,88% A→76% A;25~26 min,76% A→88% A;26~45 min,88% A→88% A。流速0.8 mL/min;柱温箱:40 ℃;进样量:10 μL;检测器波长:670 nm。
1.3.6 柱后衍生反应
衍生液A为2.0 g/L高碘酸溶液,流速0.2 mL/min;衍生液B为1.0 g/L MBTH溶液,流速0.2 mL/min;烘箱温度:110 ℃。
1.4 数据处理
本实验测定均重复3次,结果采用“平均值±标准差”表示;采用Origin 2021绘图;采用SPSS 19.0进行差异显著性检验。
2 结果与分析
2.1 检测波长的选择
分别取系列糖液1.0 mL于25 mL具塞试管中,以高碘酸为氧化剂,以MBHT为显色剂,按照参考文献[19]的方法进行显色反应。结果显示,5种糖均可被高碘酸氧化,氧化产物与MBHT衍生,呈现出青绿色或灰绿色。分别对各种衍生产物进行波长扫描,结果如图2所示。5种糖的衍生物在620~670 nm有强吸收,其中绝大部分衍生物最大吸收峰在670 nm附近,因此设置液相色谱仪检测器波长为670 nm。
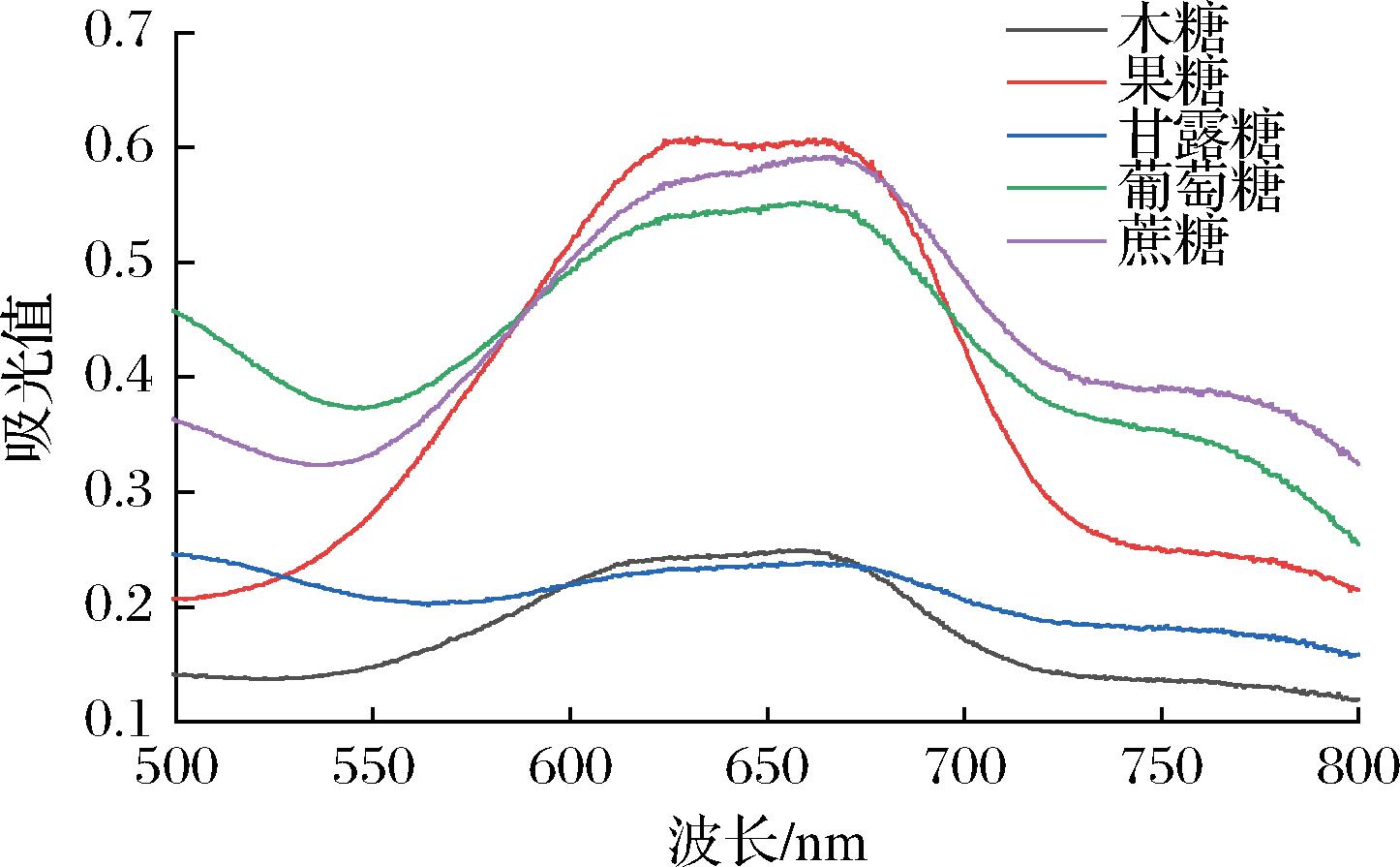
图2 五种糖组分衍生物的可见吸收光谱图
Fig.2 Visible absorption spectra of five sugar derivatives
2.2 色谱条件优化
在液相色谱分析中,常采用亲水作用色谱(hydrophilic interaction liquid chromatography,HILIC)模式分离检测糖,多使用氨基、酰胺基色谱柱,流动相以乙腈体系为主[22-23]。本实验选用了Asahipak NH2P-50 4E色谱柱(250 mm×4.6 mm,5 μm)作为分析柱,并参考GB 5009.8—2023《食品安全国家标准 食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖的测定》方法设置流动相比例,结果发现,当流动相(乙腈-水不同体积比)按不同比例等度洗脱时,果糖、甘露糖、葡萄糖分离度不佳,而较高乙腈比例模式下,蔗糖洗脱时间明显增长。进一步采用梯度模式进行洗脱,结果发现,流动相比例在25 min内从88∶12逐渐下降至76∶24时,5种糖均实现有效分离(图3)。同时调整流动相的流速,当流速为0.8 mL/min时,各种糖可在35 min内完成分离,相邻2个峰之间的分离度均大于1.5,且色谱峰型良好。柱温箱温度对糖的分离速度有一定影响,在25~40 ℃,适当提高柱温箱温度可提前出峰时间。因此,最终确定在柱温箱温度为40 ℃情况下进行梯度洗脱,流动相流速为0.8 mL/min。
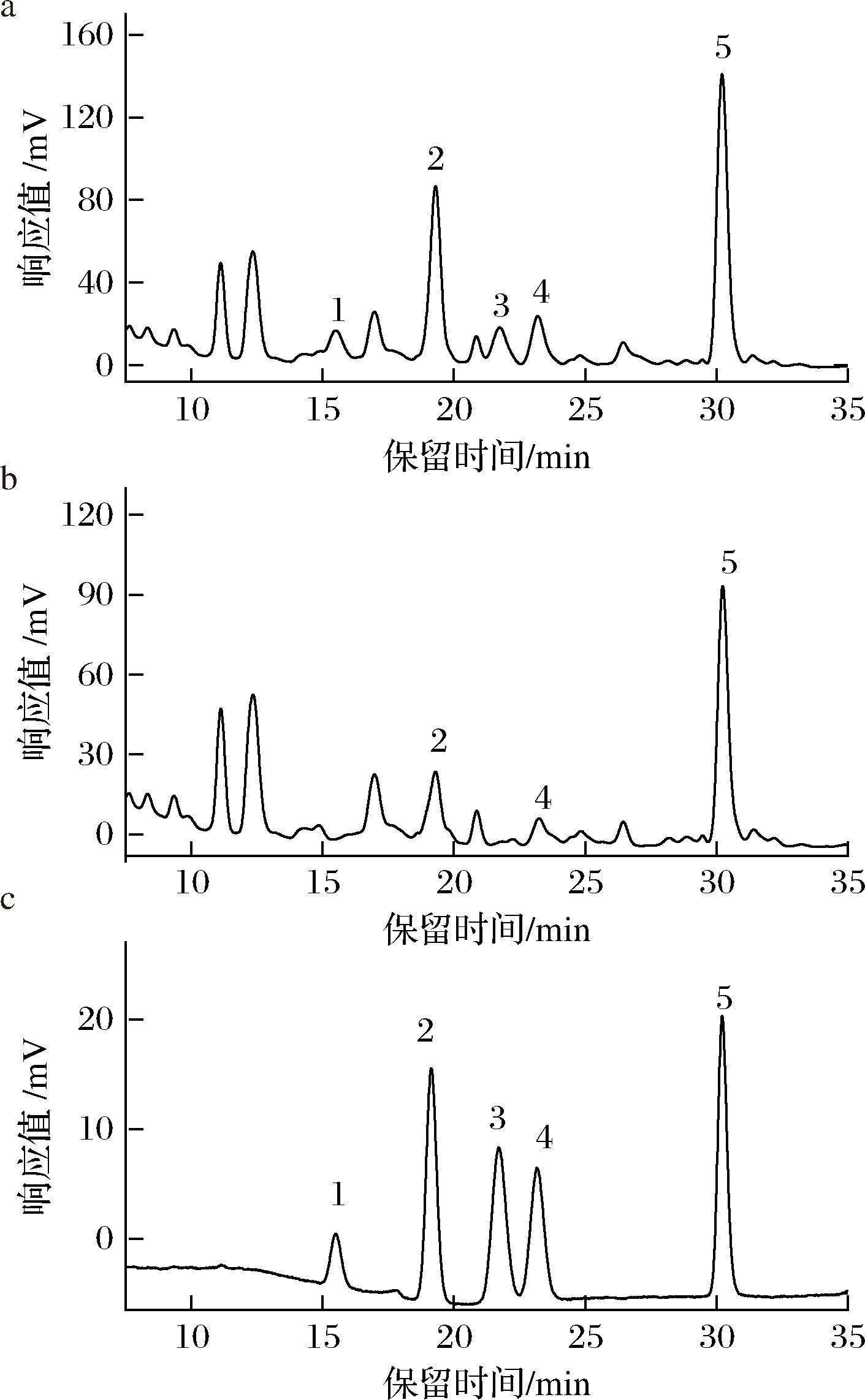
1-木糖,2-果糖,3-甘露糖,4-葡萄糖,5-蔗糖。
a-绿茶加标样;b-绿茶样品;c-糖混标
图3 梯度洗脱模式下的混标、样品及样品加标后的色谱图
Fig.3 Chromatograms of mixed standards, samples, and spiked samples under gradient elution mode
2.3 柱后衍生条件优化
高碘酸氧化糖类物质生成甲醛、MBTH与甲醛反应形成青蓝色化合物的过程,受到反应时间、反应温度以及底物质量浓度等因素的影响[19]。自动进样器注入10 μL质量浓度均为500 μg/mL的糖液混标,在固定衍生剂流速(0.2 mL/min)和固定反应线圈长度(10 m)的情况下,调整高碘酸质量浓度、MBTH质量浓度和反应温度,并探讨其对5个糖类物质峰面积的影响。结果显示,高碘酸质量浓度(2.0~5.0 g/L)和MBTH质量浓度(1.0~2.5 g/L)均对5个糖类物质的峰面积无显著影响,这是因为高碘酸和MBTH质量浓度在衍生反应中已处于过量状态。因此,在本实验中,高碘酸质量浓度设定为2.0 g/L、MBTH质量浓度设定为1.0 g/L。
进一步分析了反应温度对5个糖类物质峰面积的影响,结果如图4所示。随着反应温度的升高,5个糖类物质峰面积的影响逐渐增大,并在温度达到110 ℃时达到最大值,之后趋于下降,这可能是高温导致糖分子发生了分解所致[18,24]。因此综合考虑,设定柱后衍生温度为110 ℃。
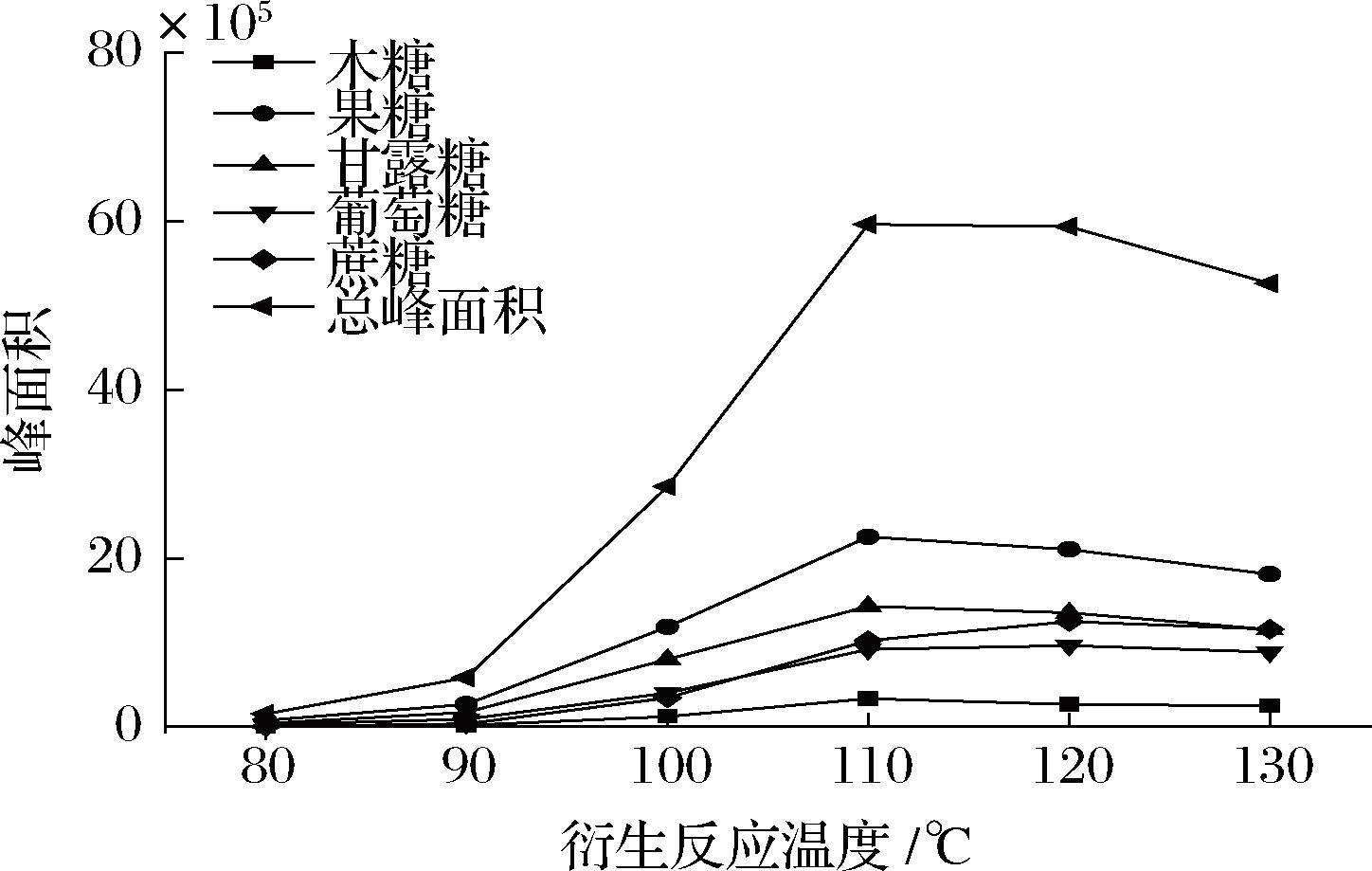
图4 衍生反应温度对色谱峰面积的影响
Fig.4 The effect of derivative reaction temperature on chromatographic peak area
2.4 线性回归方程、相关系数、线性范围、检出限
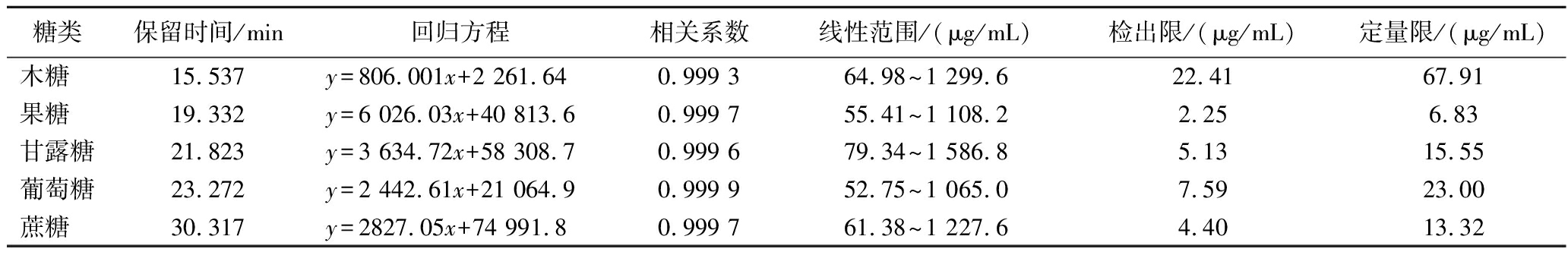
按上述色谱条件,分别对5个糖标准工作溶液进行分析测试。以各糖的衍生物峰面积为纵轴,以糖质量浓度(μg/mL)为横轴进行线性回归,其回归方程、相关系数等如表1所示,测得各糖组分的检出限为2.25~22.41 μg/mL(S/N≥3),定量限为6.83~67.91 μg/mL(S/N≥10)。
表1 回归方程、相关系数、线性范围、检出限、定量限
Table 1 Regression equations, correlation coefficients, linear range, detection limits, and quantification limits
糖类保留时间/min回归方程相关系数线性范围/(μg/mL)检出限/(μg/mL)定量限/(μg/mL)木糖 15.537y=806.001x+2 261.640.999 364.98~1 299.622.4167.91果糖 19.332y=6 026.03x+40 813.60.999 755.41~1 108.22.256.83甘露糖21.823y=3 634.72x+58 308.70.999 679.34~1 586.85.1315.55葡萄糖23.272y=2 442.61x+21 064.90.999 952.75~1 065.07.5923.00蔗糖 30.317y=2827.05x+74 991.80.999 761.38~1 227.64.4013.32
2.5 精密度与稳定性
吸取糖混合标准溶液10 μL,按优化后的程序测试6次,6次测定结果的相对标准偏差(relative standard deviation,RSD)为0.96%~3.06%,表明本方法精密度良好。
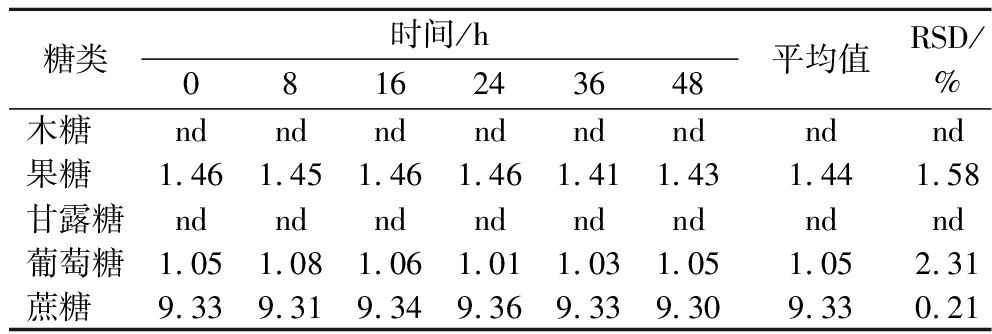
取同一份按1.3.3节方法制备的绿茶测试液,分别在48 h进行6次衍生测试,结果如表2所示。除未检出木糖和甘露糖外,其余3种糖检测结果的RSD为0.21%~2.31%,表明测试液稳定性良好。
表2 绿茶样品中糖含量不同时间段测定结果 单位:mg/g
Table 2 Determination results of sugar content in green tea at different time periods
糖类时间/h0816243648平均值RSD/%木糖 ndndndndndndndnd果糖 1.461.451.461.461.411.431.441.58甘露糖ndndndndndndndnd葡萄糖1.051.081.061.011.031.051.052.31蔗糖 9.339.319.349.369.339.309.330.21
注:“nd”表示未检出(下同)。
2.6 重复性与加标回收率
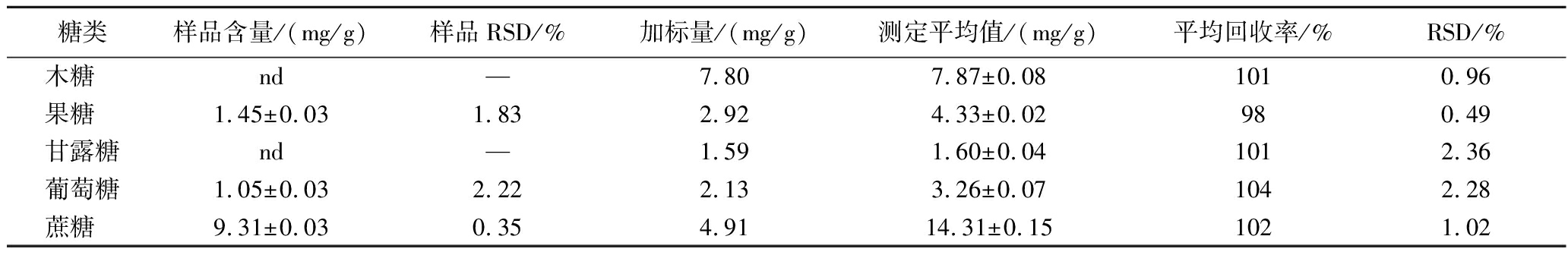
准确称取同一个绿茶样品6份,制备测试液后进行衍生测试,考察方法重复性,结果如表3所示。在样品中除未检出木糖、甘露糖外,其余糖检测的RSD为0.35%~2.22%,表明该方法重复性良好。
表3 五种糖的重复性及加标回收率测试结果(n=6)
Table 3 Repeatability and spiked recovery test results(n=6)
糖类样品含量/(mg/g)样品RSD/%加标量/(mg/g)测定平均值/(mg/g)平均回收率/%RSD/%木糖 nd—7.807.87±0.081010.96果糖 1.45±0.031.832.924.33±0.02980.49甘露糖nd—1.591.60±0.041012.36葡萄糖1.05±0.032.222.133.26±0.071042.28蔗糖 9.31±0.030.354.9114.31±0.151021.02
注:—表示无数据。
在6份同一个绿茶样品中,分别按加入适量浓度的糖标准工作溶液,并按1.3.3节方法制备测试液后进行分析,测定样品中的糖含量,计算回收率,结果如表3所示。5种糖的加标回收率为98%~104%,表明该方法准确度较高。可见,采用液相色谱-柱后衍生法同时测定5种糖含量的精密度和回收率高,具有成本低、快速、准确的特点,可用于茶叶中5种糖的快速测定。
2.7 茶叶糖含量测定
精密称取59个不同嫩度的绿茶和红茶样品2.000 g,按1.3.3节方法制备测试液,并按优化程序进行色谱和柱后衍生,将测得的峰面积带入回归方程,分别计算各种糖含量,结果如表4、表5所示。
表4 绿茶样品中的5种糖含量 单位:mg/g
Table 4 Sugar content in green tea samples
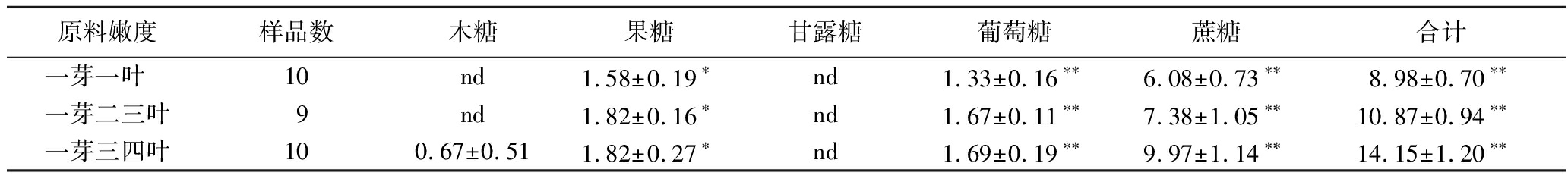
原料嫩度样品数木糖果糖甘露糖葡萄糖蔗糖合计一芽一叶 10nd1.58±0.19∗nd1.33±0.16∗∗6.08±0.73∗∗8.98±0.70∗∗一芽二三叶9nd1.82±0.16∗nd1.67±0.11∗∗7.38±1.05∗∗10.87±0.94∗∗一芽三四叶100.67±0.511.82±0.27∗nd1.69±0.19∗∗9.97±1.14∗∗14.15±1.20∗∗
注:表中同一列数据中,*表示P<0.05,**表示P<0.01(下同)。
表5 红茶样品中的5种糖含量 单位:mg/g
Table 5 Sugars content in black tea samples

原料嫩度样品数木糖果糖甘露糖葡萄糖蔗糖合计一芽一叶 90.95±0.51∗∗2.16±0.25∗∗0.027±0.0271.55±0.17∗∗0.29±0.043∗∗4.98±0.56∗∗一芽二三叶100.84±0.39∗∗3.28±0.34∗∗0.041±0.0242.78±0.20∗∗0.26±0.041∗∗7.20±0.58∗∗一芽三四叶110.25±0.20∗∗3.30±0.31∗∗0.025±0.0242.82±0.17∗∗0.11±0.076∗∗6.50±0.43∗∗
在29个绿茶样品中,均未检出甘露糖,共有13个绿茶样品中未检出木糖。从表4可知,绿茶中糖含量从高到低依次为:蔗糖[(7.83±1.93) mg/g]>果糖[(1.74±0.23) mg/g]>葡萄糖[(1.56±0.23) mg/g]>木糖[(0.23±0.43) mg/g],与李燕平[6]对20个绿茶样品中糖含量检测结果的规律一致。蔗糖含量极显著高于其他糖类含量(P<0.01),而其余3种糖含量差异不显著。绿茶中糖含量最高的是蔗糖,含量为5.21~12.84 mg/g,KAUSAR等[25]采用高效液相色谱法测定绿茶中蔗糖平均含量为(10.73±0.18) mg/g,DING等[26]采用离子色谱法测定绿茶蔗糖含量为6.16~9.94 mg/g,与本实验结果无明显差异,表明蔗糖是绿茶中普遍存在的风味成分。
进一步分析统计了不同嫩度绿茶中的糖含量,绿茶中的5种糖含量为8.19 ~16.78 mg/g,且随着绿茶原料嫩度的降低,绿茶中蔗糖、葡萄糖、果糖含量和5种糖含量总和均有所增加,这与茶叶生长过程中光合作用有关[27]。鲜叶原料成熟度高,光合作用强,转化生成的糖类物质含量高于幼嫩芽叶,因此一芽三四叶原料嫩度的绿茶中蔗糖、葡萄糖、果糖等含量均显著或极显著高于其他2种嫩度的绿茶。
在30个红茶样品中,5种糖类均检出,其总量为4.34~7.02 mg/g,但有3个样品未检出木糖,9个样品未检出甘露糖。红茶中糖含量从高到低依次为:果糖[(2.95±0.60) mg/g]>葡萄糖[(2.43±0.61) mg/g]>木糖[(0.66±0.48) mg/g]>蔗糖[(0.21±0.10) mg/g]>甘露糖[(0.031±0.025) mg/g],且果糖、葡萄糖和木糖含量极显著高于其他糖类含量(P<0.01),但三者间差异不显著。鲜叶原料嫩度对红茶中糖含量影响如表5所示,随着原料嫩度的降低,红茶中果糖、葡萄糖均有所增加,而木糖和蔗糖含量有所减少,且含量达到显著或极显著差异水平。
进一步对茶类间的5种糖含量进行了差异显著性分析。由图5可知,相同嫩度的绿茶和红茶糖含量差异极显著(P<0.01),且相同嫩度原料制作的绿茶糖含量高于红茶;各种糖含量差异达到极显著水平,尤其是蔗糖、果糖和葡萄糖,其中红茶蔗糖含量极显著低于绿茶(P<0.01),而果糖和葡萄糖含量极显著高于绿茶(P<0.01)。周金沙等[27]分析了16个茶叶鲜叶及加工的茶叶中的糖含量,发现绿茶加工前后,果糖和葡萄糖含量差异不显著,而加工后的蔗糖含量显著增加,推测其原因为加工过程中茶多糖的水解所致。但红茶中蔗糖含量远低于绿茶,相同嫩度红茶蔗糖含量仅为相同嫩度绿茶蔗糖含量的1.1%~4.8%,这可能与红茶发酵有关[26]。蔗糖是由一分子葡萄糖和一分子果糖缩合脱水而成的双糖,在酸性条件下容易发生水解作用而生成果糖和葡萄糖[19]。在红茶发酵过程中,发酵叶处于酸性环境中[1],以及在各种酶的共同作用下,蔗糖极可能分解为葡萄糖与果糖,导致红茶中的葡萄糖和果糖含量增加。与此同时,在红茶干燥提香过程中,因美拉德反应的进行,将导致糖含量下降[28]。这可能是红茶中蔗糖含量低、果糖和葡萄糖含量高的原因,其具体变化规律还有待进一步探索。
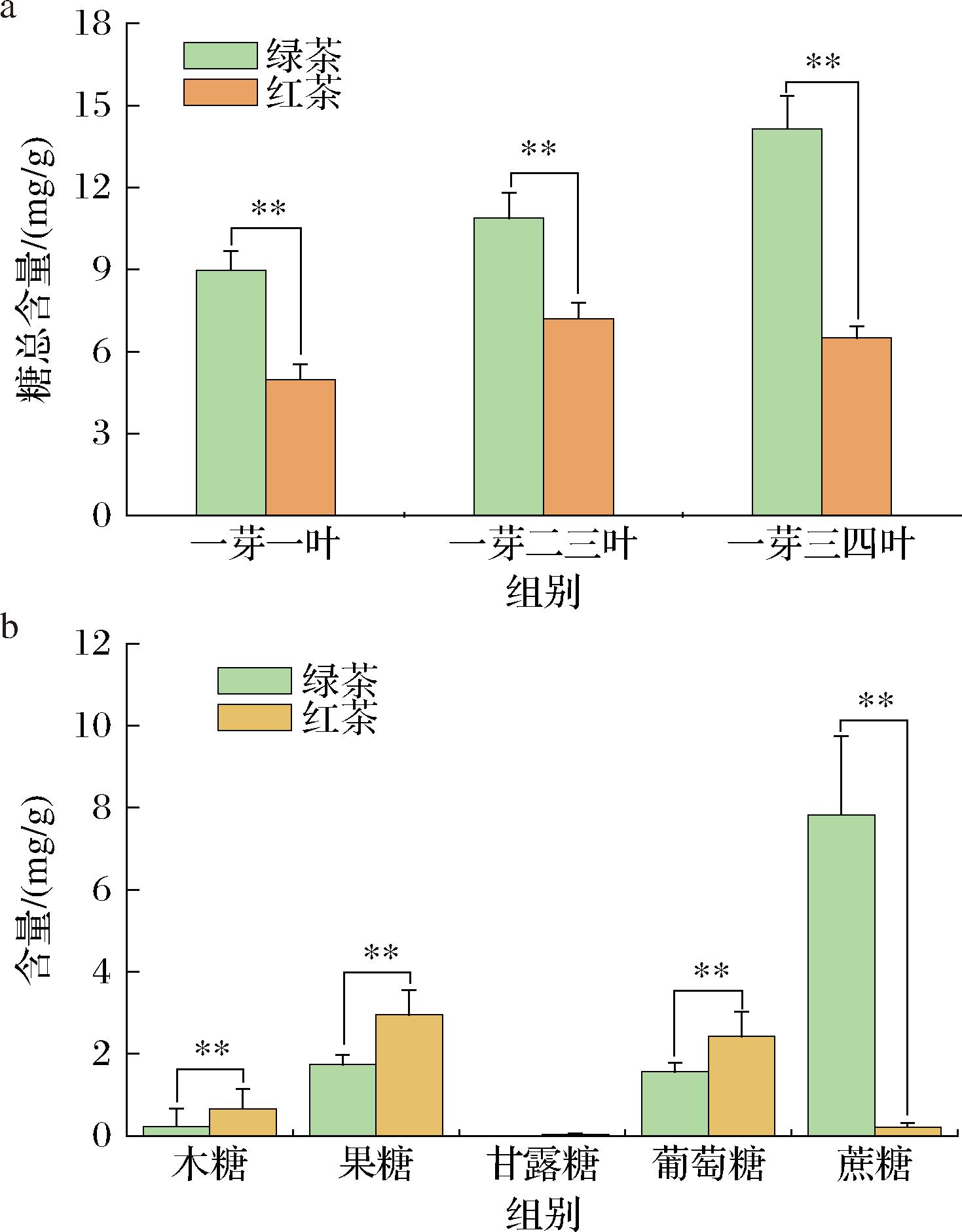
a-糖总含量;b-各糖含量
图5 绿茶和红茶中糖含量比较
Fig.5 Comparison of sugar content in black tea and green tea
注:**表示差异极显著(P≤0.01)。
3 结论与讨论
糖类是茶叶中的重要风味物质,但受检测技术手段的限制,目前对茶叶中糖类物质的研究尚不全面且存在诸多挑战。由于糖类在紫外没有吸收,因此采用液相色谱分离后的检测,往往依赖于RID或ELSD[7-9],但茶叶成分复杂,其检测受到较为严重的干扰;或依靠气质联用、液质联用等方式检测[29-30],但设备和使用试剂价格高昂。因此,开发并应用新的茶叶糖含量检测方法,将有助于制茶工艺改良、茶叶品质提升等。
糖分子化学结构中,具有大量邻二醇结构,高碘酸可将邻二醇氧化,其氧化产物有甲醛、甲酸等。生成的甲醛在高碘酸作用下与MBTH反应,生成在630~670 nm处有最大吸收的青蓝色化合物[19]。其机理如图6所示。
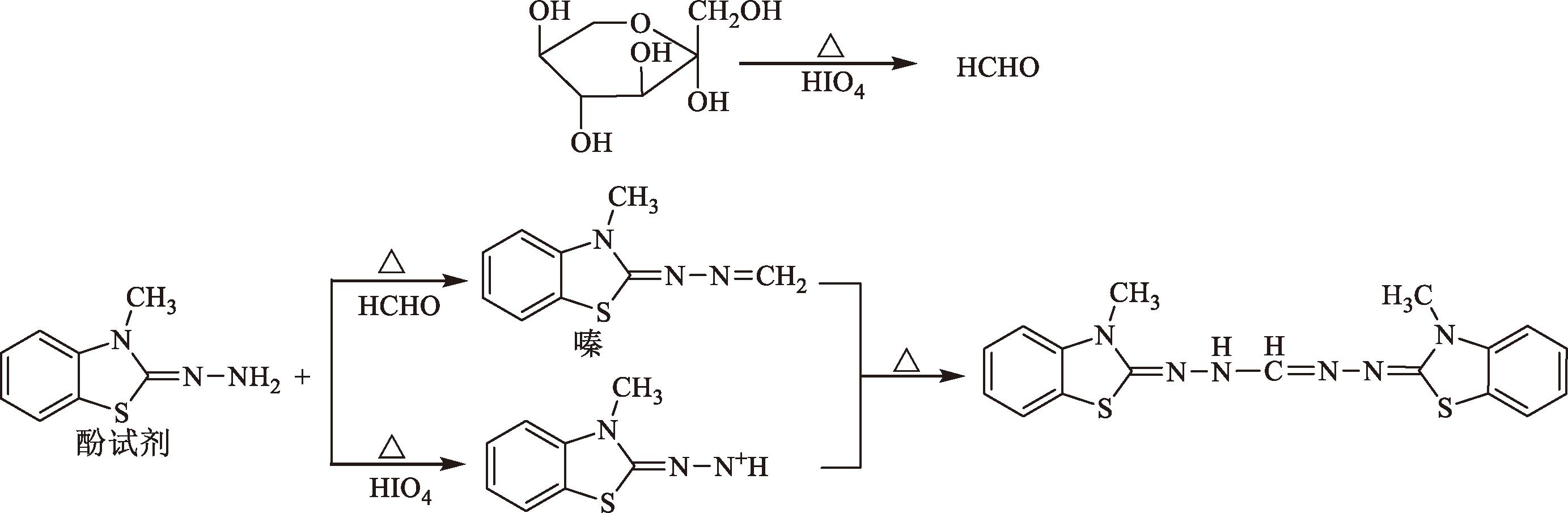
图6 糖与高碘酸、MBTH衍生反应机理
Fig.6 Derivatizational reaction mechanism of sugar with periodate and MBTH
因此,在上述理论基础下,本实验建立了液相色谱-柱后衍生法测定茶叶中糖含量的方法,采用Asahipak NH2P-50 4E色谱柱(250 mm×4.6 mm,5 μm),以含体积分数0.5%H3PO4的乙腈-水体系为流动相进行梯度洗脱,流速0.8 mL/min,柱温40 ℃,柱后于110 ℃下采用高碘酸氧化、MBTH进行衍生显色,检测波长670 nm。在此条件下,木糖、果糖、甘露糖、葡萄糖和蔗糖线性关系良好,检出限为2.25~22.41 μg/mL,定量限为6.83~67.91 μg/mL,加标回收率为98%~104%。
利用本方法对59个绿茶和红茶样品的5种糖含量进行了检测,除部分茶样未检出木糖和甘露糖外,蔗糖、果糖和葡萄糖等3种均被检出。王川丕等[30]利用超高效液相色谱-质谱联用技术检测茶叶中的单糖、寡糖,在绿茶、红茶、乌龙茶等茶类中,均未检出木糖,与本研究结果基本一致。在本研究中,相同嫩度鲜叶制作的绿茶糖含量极显著高于同等嫩度的红茶。绿茶中5种糖含量为8.19~16.78 mg/g,含量最高的是蔗糖[(7.83±1.93) mg/g],然后依次为果糖[(1.74±0.23) mg/g]、葡萄糖[(1.56±0.23) mg/g];嫩度低的绿茶糖含量极显著高于嫩度高的绿茶,这与茶树生长过程中的光合作用和绿茶加工过程中多糖的降解有关;红茶中5种糖含量为4.34~7.02 mg/g,含量最高的是果糖[(2.95±0.60) mg/g]、葡萄糖[(2.43±0.61) mg/g]和木糖[(0.66±0.48) mg/g],而蔗糖[(0.21±0.10) mg/g]含量较低,这可能受到红茶发酵中蔗糖氧化分解以及提香过程中美拉德反应的影响,对红茶加工过程中的变化规律还有待探索和研究。
综上,本研究建立了液相色谱-柱后衍生法测定茶叶中5种糖含量的方法,所用试剂均为常见试剂,具有快速简便、试剂成本低、回收率高、精密度和稳定性好等优点,可为优良品种选育、栽培措施改良、制茶工艺优化、茶叶品质提升等提供新的检测技术支持。
[1] 罗学平, 练学燕.茶叶检验技术[M].北京:北京理工大学出版社, 2025.LUO XP, LIAN XY.Tea Inspection Technology[M].Beijing:Beijing Institute of Technology Press, 2025.
[2] TRESKES R W, CLAUSEN J, MAROTT J L, et al.Use of sugar in coffee and tea and long-term risk of mortality in older adult Danish men:32 years of follow-up from a prospective cohort study[J].PLoS One, 2023, 18(10):e0292882.
[3] GYNTELBERG F, HEIN H O, SUADICANI P, et al.Sugar in coffee or tea and risk of obesity:A neglected issue[J].International Journal of Food Sciences and Nutrition, 2009, 60(sup3):56-64.
[4] SAMANT S S, WILKES K, ODEK Z, et al.Tea-induced calmness:Sugar-sweetened tea calms consumers exposed to acute stressor[J].Scientific Reports, 2016, 6:36537.
[5] 吴奇霄, 余松柏, 黄张君, 等.多元醇和糖的HPLC-RID检测方法优化及其在四种饮料酒中的应用[J].酿酒, 2022, 49(6):91-96.WU Q X, YU S B, HUANG Z J, et al.Optimization of HPLC-RID method for determination of polyols and sugars and its application to four types of alcohol beverages[J].Liquor Making, 2022, 49(6):91-96.
[6] 李燕平. 高效液相色谱-示差折光检测法测定茶叶中果糖﹑葡萄糖、蔗糖的含量[J].广东化工, 2016, 43(7):187-188.LI Y P.Determination of fructose, glucose and sucrose in tea by high performance liquid chromatography-differential refraction detector[J].Guangdong Chemical Industry, 2016, 43(7):187-188.
[7] SHANMUGAVELAN P, KIM S Y, KIM J B, et al.Evaluation of sugar content and composition in commonly consumed Korean vegetables, fruits, cereals, seed plants, and leaves by HPLC-ELSD[J].Carbohydrate Research, 2013, 380:112-117.
[8] SEQUEIRA I R, KRUGER M C, HURST R D, et al.A simple, robust, and convenient HPLC assay for urinary lactulose and mannitol in the dual sugar absorption test[J].Molecules, 2022, 27(9):2677.
[9] 黄明军, 杨新河, 覃彩芹, 等.HPLC-ELSD法测定黑茶中单糖和双糖的含量[J].食品工业, 2017, 38(1):306-310.HUANG M J, YANG X H, QIN C Q, et al.Determination of monosaccharides and disaccharides in dark tea by HPLC-ELSD[J].The Food Industry, 2017, 38(1):306-310.
[10] MIAO X L, MA H M, KE Q H, et al.The determination of monosaccharide in different years Qingzhuan dark tea polysaccharide by liquid chromatography-mass spectrometry[J].Phytochemical Analysis, 2022, 33(4):577-589.
[11] WEN M C, CUI Y Q, DONG C X, et al.Quantitative changes in monosaccharides of Keemun black tea and qualitative analysis of theaflavins-glucose adducts during processing[J].Food Research International, 2021,148:110588.
[12] ![]() CEBIN A, KOMES D, RALET M C.Development and validation of HPLC-DAD method with pre-column PMP derivatization for monomeric profile analysis of polysaccharides from agro-industrial wastes[J].Polymers, 2022, 14(3):544.
CEBIN A, KOMES D, RALET M C.Development and validation of HPLC-DAD method with pre-column PMP derivatization for monomeric profile analysis of polysaccharides from agro-industrial wastes[J].Polymers, 2022, 14(3):544.
[13] ZHANG M, AN Y, ZHANG L J.Quantitative disaccharide profiling of glycosaminoglycans from two different preparations by PMP and deuterated PMP labeling[J].Methods in Molecular Biology, 2022, 2303:111-119.
[14] 刘晓燕, 龚强, 吴延姣, 等.柱后衍生-高效液相色谱法测定动物源性食品中氨基甲酸酯类农药的残留[J].市场监管与质量技术研究, 2025(2):19-24.LIU X Y, GONG Q, WU Y J, et al.Determination of carbamate pesticide residues in food of animal origin by post-column derivatization:High performance liquid chromatography[J].Market Regulation and Quality Technology Research, 2025(2):19-24.
[15] 李巧琪, 许志彬, 黄伟乾, 等.柱后衍生阳离子交换色谱法测定酱油中38种游离氨基酸含量[J].中国调味品, 2021, 46(4):165-168, 173.LI Q Q, XU Z B, HUANG W Q, et al.Determination of 38 kinds of free amino acids in soy sauce by post-column derivatization with cation exchange chromatography[J].China Condiment, 2021, 46(4):165-168, 173.
[16] 赵鑫. 1-萘硼酸柱后衍生高效液相色谱荧光法测定单糖的研究[D].石家庄:河北师范大学, 2013.ZHAO X.Research on post column derivatization high performance liquidchromatographic method for determination of monosaccharide by 1-naphthyl boronic acid[D].Shijiazhuang:Hebei Normal University, 2013.
[17] 韩晶, 李永路.磷酸-苯肼柱后衍生法测定茶及茶饮料中的糖类[C].中国化学会第八届全国仪器分析及样品预处理学术研讨会论文集.泰州:中国化学会, 2015.HAN J, LI Y L.Determination of carbohydrates in tea and tea beverages by post-column derivatization with phosphoric acid-phenylhydrazine[C].Proceedings of the 8th National Symposium on Instrumental Analysis and Sample Pre-treatment, Chinese Chemical Society.Taizhou:Chinese Chemical Society, 2015.
[18] 蔡孟深, 李中军.糖化学:基础、反应、合成、分离及结构[M].北京:化学工业出版社, 2007.CAI M S, LI Z J.Carbohydrate Chemistry:Fundamentals, Reactions, Synthesis, Separation, and Structure[M].Beijing:Chemical Industry Press Co.Ltd., 2007.
[19] 胡静姝. 高碘酸钠氧化果糖的分析[J].广州化工, 2010, 38(7):154-156.HU J S.Analytical of the oxidation of D-fructose by sodium periodate[J].Guangzhou Chemical Industry, 2010, 38(7):154-156.
[20] 张超, 谢晓敏.浅析甲醛的危害、检测评价与治理[J].皮革制作与环保科技, 2024,5(1):148-150.ZHANG C, XIE X M.Harm, detection, evaluation and treatment of formaldehyde[J].Leather Manufacture and Environmental Technology, 2024,5(1):148-150.
[21] 蒋喆. MBTH法和HPLC法测定汽车内饰挥发甲醛含量对比[J].浙江化工, 2024, 55(7):42-49.JIANG Z.Comparison of MBTH method and HPLC method for the determination of volatile formaldehyde content in automobile interiors[J].Zhejiang Chemical Industry, 2024, 55(7):42-49.
[22] 张丹丹, 矫芮文, 米春孝, 等.用于分离单糖与寡糖的亲水色谱材料制备及应用进展[J].食品科学, 2024, 45(9):261-271.ZHANG D D, JIAO R W, MI C X, et al.Research progress in the preparation and applications of hydrophilic chromatographic materials for separation of monosaccharides and oligosaccharides[J].Food Science, 2024, 45(9):261-271.
[23] LUO X H, LIU Y, XING J L, et al.Comparison of ELSD and RID combined with HPLC for simultaneous determination of six rare sugars in food components[J].Microchemical Journal, 2024, 201:110666.
[24] 蔡磊, 吕秀阳.高温液态水中葡萄糖分解反应动力学[J].化学反应工程与工艺, 2007, 23(1):88-91.CAI L, LYU X Y.Decomposition kinetics of glucose in high temperature liquid water[J].Chemical Reaction Engineering and Technology, 2007, 23(1):88-91.
[25] KAUSAR T, AKRAM K, KWON J H.Comparative effects of irradiation, fumigation, and storage on the free amino acids and sugar contents of green, black and oolong teas[J].Radiation Physics and Chemistry, 2013, 86:96-101.
[26] DING Y S, YU H, MOU S F.Direct determination of free amino acids and sugars in green tea by anion-exchange chromatography with integrated pulsed amperometric detection[J].Chromatography A, 2002, 982(2):237-244.
[27] 周金沙, 常晓途, 汪辉, 等.茶叶中果糖、葡萄糖和蔗糖含量及蔗糖来源分析[J].茶叶通讯,2021,48(2):311-318.ZHOU J S, CHANG X T, WANG H, et al.Content of fructose, glucose and sucrose in tea and source analysis of sucrose[J].Tea Communication, 2021, 48(2):311-318.
[28] 仇方方, 陈亚忠, 余志, 等.远红外提香温度对工夫红茶品质的影响[J].福建茶叶,2015, 37(6):14-16.QIU F F, CHEN Y Z, YU Z, et al.Effect of far infrared aroma extraction temperature on the quality of Kung Fu black tea[J].Tea in Fujian, 2015, 37(6):14-16.
[29] 潘科, 方仕茂, 刘忠英, 等.基于GC-MS/MS分析加工对古茶树红茶可溶性糖含量的影响[J].福建农林大学学报(自然科学版), 2021, 50(4):490-496.PAN K, FANG S M, LIU Z Y, et al.Effects of processing on soluble sugar content of black tea from ancient tea tree based on GC-MS/MS[J].Journal of Fujian Agriculture and Forestry University (Natural Science Edition), 2021, 50(4):490-496.
[30] 王川丕, 诸力, 刘新, 等.超高效液相色谱-质谱联用技术测定茶叶中8种单、寡糖的含量[J].食品科学, 2014, 35(20):164-169.WANG C P, ZHU L, LIU X, et al.Determination of eight saccharides in teas by ultra performance liquid chromatography-tandem mass spectrometry[J].Food Science, 2014, 35(20):164-169.