洋葱(Allium cepa L.)是葱科葱属的二年生草本植物,是中国重要的外源蔬菜作物之一[1]。经过长期的栽培和改良,洋葱形成了丰富的品种资源体系,栽培品种具有红、黄、白、绿、紫等丰富的表型特征,风味差异显著。作为“蔬菜皇后”,洋葱具有卓越的营养和药用价值,富含多酚、有机硫化合物、皂苷等生物活性成分。其所含多酚是一类天然存在的化合物[2],根据结构特征,多酚可分为黄酮类、酚酸类、木脂素类、黄芪苷类等类别,其中酚酸和黄酮类化合物占比尤为突出,约占总量的90%[3]。现代药理学研究表明,洋葱多酚化合物具有抗氧化和抗炎等生理活性,在疾病预防领域展现出显著价值。
洋葱中的多酚化合物引发了国内外学者的高度关注,相关研究主要集中在成分分析,功效探索及提取工艺等方面。曹艳华等[4]以洋葱为原料,研究其提取及其体外抗氧化活性,结果显示,洋葱多酚的得率为12.77 mg/g,体外抗氧化实验表明,在质量浓度0.05~0.3 mg/mL时,洋葱多酚对DPPH自由基、羟自由基、超氧阴离子自由基具有较强的清除性,表明洋葱多酚具有良好的体外抗氧化活性。METRANI等[5]研究发现,在加利福尼亚州和德克萨斯州种植的2种红洋葱(甜意大利洋葱和金银花洋葱)中,其多酚含量存在明显差异。结果显示,金银花属的总类黄酮、总酚和总花青素含量均高于甜意大利属。另一项研究分析了捷克6个商业洋葱品种(Bingo、Dormo、Elenka、Elbrus、Spirit、和Sturon),发现这些品种的多酚含量为2.66~3.37 g/kg,其中Bingo洋葱的多酚化合物含量最高[6]。这些研究结果证实了洋葱中多酚化合物含量可能与品种、基因型之间存在相关性,但并未系统性的研究不同洋葱品种的多酚类化合物差异。因此,对不同品种洋葱多酚代谢物差异进行研究,对于全面分析此彩色洋葱品质形成机理、建立科学的品质评价体系具有重要的理论和实践意义。
近年来,广泛靶向代谢组学作为分析生物体小分子代谢物的综合性技术手段,不仅能够客观全面地反映代谢物组成与含量变化,还能有效识别未知或潜在的生物标志物。其中,基于超高效液相色谱-串联质谱联用(ultra-high performance liquid chromatography-tandem mass spectrometry,UPLC-MS/MS)技术的广靶代谢组学方法,已被证实是定量分析各类生物体内非挥发性代谢物的有效工具[7]。例如,ARKORFUL等[8]采用UPLC-MS/MS广靶代谢组学技术分析不同修剪阶段茶树枝条中促进生长发育的差异代谢物,共鉴定出80种差异代谢物。结果显示,修剪能促进枝条中吲哚-3-乙腈和甲基萘醌的合成,同时调控色氨酸代谢等通路,进而调节吲哚-3-乙腈含量,最终促进枝条生长发育。此外,另一项研究采用UPLC-MS/MS对玫瑰果的3个不同成熟阶段的多酚成分进行了广谱代谢组学分析,研究共检测到531种多酚类代谢物,包括220种酚酸、219种黄酮类、50种单宁以及42种木脂素和香豆素[9],该研究揭示了玫瑰果在不同成熟阶段非挥发性代谢物的显著变化模式。从上述研究可知,广泛靶向代谢组学技术能够为植物多酚类物质的研究提供了一种较全面、一种行之有效的技术手段。
甘肃省酒泉市是我国彩色洋葱的主要产地之一,当地彩色洋葱品种被列为国家地理标志产品[10-11]。课题组前期对酒泉3种彩色洋葱中总多酚和总黄酮含量、抗氧化活性以及挥发性代谢物进行了初步研究[12-13],然而,有关彩色洋葱品种间多酚类化合物差异未见相关研究。因此,本研究采用UPLC-MS/MS广泛靶向代谢组学结合多元统计方法,系统分析了3种彩色洋葱品种中多酚类代谢物的组成和差异,探讨其相关代谢通路,旨在为了解彩色洋葱品种间多酚谱特征及其开发利用提供理论与数据支撑。
1 材料与方法
1.1 材料与试剂
3种彩色洋葱,品种分别为:白碧龙(白色W)、红优1号(紫色P)和金稞7号(黄色Y),甘肃省酒泉市肃州区(图1);甲醇(色谱纯)、乙腈(色谱纯),德国默克公司;甲酸(色谱纯),上海阿拉丁生化科技股份有限公司;2-氯苯丙氨酸(色谱纯),北京百灵威科技有限公司。

图1 三种彩色洋葱外观数码照
Fig.1 Digital photo of three colored onions’ appearance
1.2 仪器与设备
Scientz-100F冷冻干燥机,中国宁波新芝生物科技股份有限公司;Retsch MM400研磨机,弗尔德(上海)仪器设备有限公司;MS105DM电子天平,梅特勒-托利多联合公司;IKA MS3涡旋混合器,德国IKA公司;Agilent SB-C18色谱柱,安捷伦科技有限公司。
1.3 实验方法
1.3.1 样品处理
将白色(W)、紫色(P)和黄色(Y)洋葱鳞茎洗净处理后,放入冷冻干燥机进行真空冷冻干燥;随后使用研磨机以30 Hz转速研磨1.5 min制得粉末;以2-氯苯丙氨酸为内标物,与体积分数70%甲醇水溶液混匀制成1 mg/L内标提取液,并预冷至-20 ℃备用;接着用电子天平精确称取50 mg样品粉末,并在-20 ℃条件下加入1 200 μL预冷的甲醇水内标提取液。将样品置于涡旋混合器中以每30 min涡旋1次,每次持续30 s的频率振荡处理6次;最后以12 000 r/min离心3 min,吸取上清液过0.22 μm微孔膜过滤,最终将处理后的样品装入进样瓶保存。
1.3.2 色谱和质谱条件
数据采集仪器系统包括UPLC和MS/MS。
液相条件:流动相为含体积分数0.1%甲酸的超纯水(A相)和含体积分数0.1%甲酸的乙腈(B相),洗脱梯度设定如下:0.00 min时B相比例为5%,9.00 min时线性增加至95%并保持1 min;10.00~11.10 min时B相比例降至5%,并以5%的比例平衡至14 min。此外,实验参数设置如下:流速0.35 mL/min,柱温40 ℃,进样量2 μL。
质谱条件:电喷雾离子源,参数设置如下:离子源温度为550 ℃,离子喷雾电压在正离子模式下为5 500 V,在负离子模式下为-4 500 V;离子源气体Ⅰ、气体Ⅱ和帘式气体(分别设置为50、60和25 psi。碰撞诱导电离参数设置为“高”。在多反应监测扫描模式下使用三重四极杆,碰撞气体(氮气)设置为“中”。实验通过优化解簇电压和碰撞能量确定了各多反应监测离子对的最佳操作参数,并根据不同洗脱时段的代谢物特征,采用分时段监测特定多反应监测离子对组合的动态监测策略。
1.4 数据处理
数据表示为“平均值±标准差”(n=3)。利用Analyst 1.6.3软件和MultiQuant 3.0.3软件对质谱数据进行色谱峰积分和校正,其中每个色谱峰的峰面积代表相应物质的相对含量。主成分分析(principal component analysis,PCA)和正交偏最小二乘判别分析(orthogonal partial least squares-discriminant analysis,OPLS-DA)分别利用R软件Base packpage 4.1.2和Meta boAnalystR 1.0.1构建精确的分类模型。利用变量投影重要性(variable importance in projection,VIP)筛选,筛选条件:VIP≥1、差异倍数(fold change,FC)≥2或≤0.5以及P<0.05,最后以火山图呈现。代谢物含量数据采用单位方差缩放法进行处理,并使用R软件Complex Heatmap包绘制热图。同时,K均值聚类利用R软件Base packpage 4.1.2分析探索不同洋葱品种中重要代谢物的动态变化规律。使用KEGG化合物数据库(http://www.kegg.jp/kegg/compound/)对鉴定的代谢物进行注释,随后将这些注释的代谢物映射到KEGG通路数据库中(http://www.kegg.jp/kegg/pathway.html)。
2 结果与分析
2.1 彩色洋葱质控样品分析
彩色洋葱质量控制(quality control,QC)样品在正、负离子模式下的总离子流色谱结果如图2所示,曲线重合度高,保留时间和峰强度的一致性好,说明仪器稳定性好,检测数据可靠。
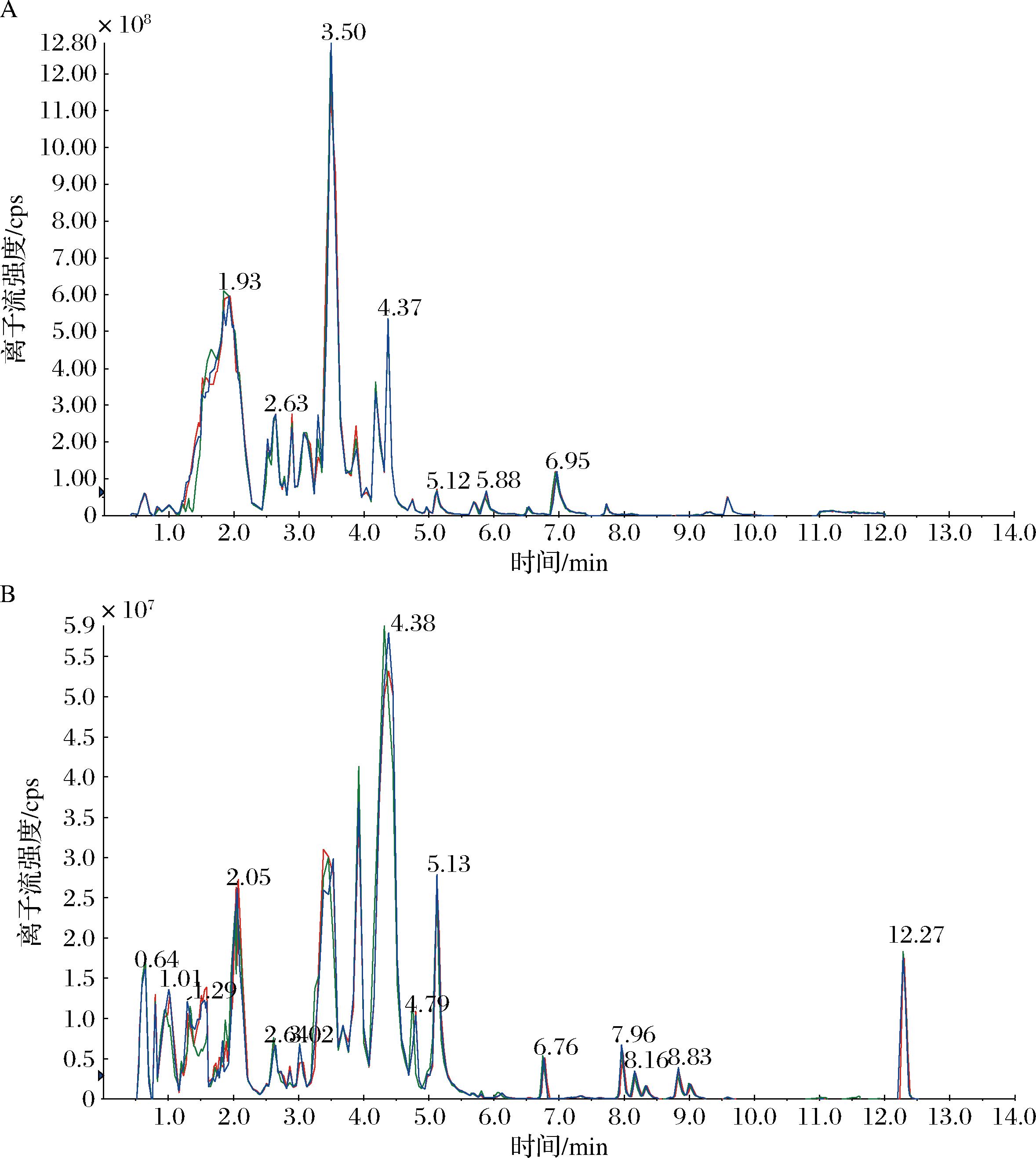
A-正离子模式下的总离子流图;B-负离子模式下的总离子流图
图2 三种彩色洋葱QC样品在正、负离子模式下的总离子流图
Fig.2 Total ion flow plots of three color onion QC samples in positiveand negativeion mode
2.2 彩色洋葱鳞茎中多酚代谢物的分类统计
为了全面了解样品中主要代谢物的分布情况,对代谢物的组成比例进行了分析,直观反映了不同类别化合物的占比信息。如图3-A所示,黄酮类代谢物占多酚代谢物总量的61.74%,在各类代谢物中占比最高;其次是酚酸类代谢物,占27.27%;木脂素和香豆素占8.9%;单宁类代谢物占1.33%;其他类占0.76%。
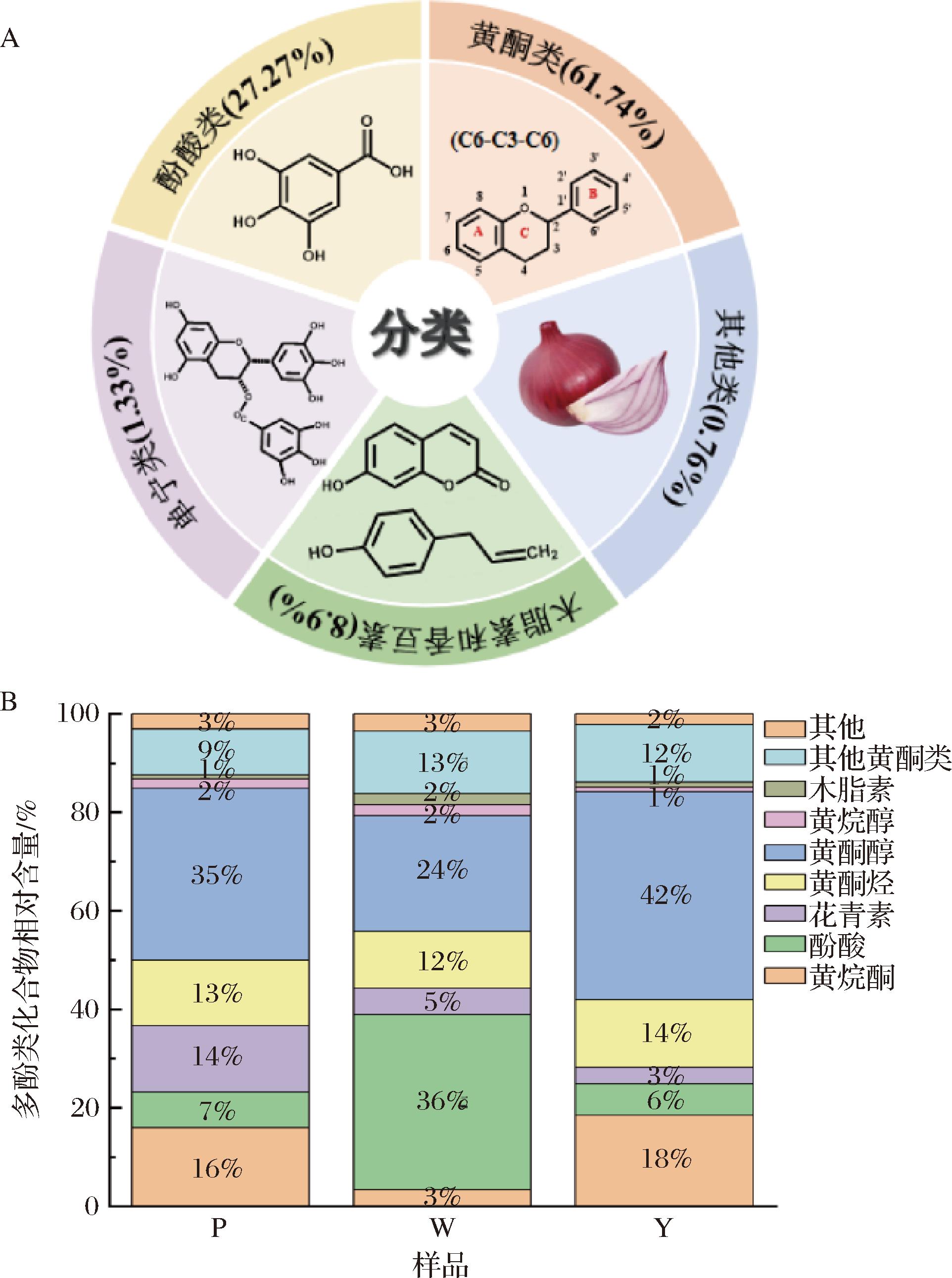
A-主要类别;B-相对含量
图3 三种彩色洋葱多酚代谢物主要类别和相对含量
Fig.3 Major classes and relative contents of three colored onion polyphenol metabolites
3个不同品种的彩色洋葱鳞茎共分离鉴定出528种多酚代谢物。热图可视化评估了不同洋葱品种之间多酚代谢物积累模式的相对差异。红色代表丰度较高,绿色代表丰度较低。对3个洋葱品种的多酚代谢物进行综合分析后发现其组成各不相同(电子版增强出版附图1,https://doi.org/10.13995/j.cnki.11-1802/ts.044102,下同),P组大部分代谢物的浓度水平高于W组和Y组,而W组代谢物的浓度水平总体最低,其中,黄酮类化合物在P、W、Y组中分别占91.08%、60.32%和92.10%;酚酸类化合物分别占7.22%、35.72%和6.34%;木脂素和香豆素分别占1.25%、3.38%和1.19%;鞣质类分别占0.43%、0.58%和0.35%(图3-B)。前期研究也发现,紫色(0.18 mg/g)和黄色洋葱[(0.20±0.02) mg/g]中的总黄酮含量高于白色洋葱[(0.16±0.02) mg/g],与本研究结果类似。但白洋葱中酚酸含量明显高于紫洋葱和黄洋葱[14]。
酚酸和类黄酮具有多种生理功能。其中,酚酸不仅具有抗菌、抗突变、抑制人类免疫缺陷病毒等作用,还能抑制皮肤癌和肺癌[15];黄酮类化合物作为具有抗氧化特性的多酚类物质,除了抗氧化之外,还具有预防心脑血管疾病和保护肝脏的功能[16-17]。LI等[18]研究了洋葱皮中的酚类化合物,鉴定出34种酚类化合物,包括17种黄酮类化合物和17种非黄酮类酚类化合物,评估其抗氧化和抗神经炎症的能力,生物活性结果表明,洋葱中的黄酮类化合物具有明显的活性。值得注意的是,LACHMAN等[19]研究了3种彩色洋葱(紫红色-Carmen Karmen、黄色-Vsetana和白色-Ala),结果表明,紫红色-Carmen Karmen的多酚化合物含量最高,而白色-Ala的含量最低,与本研究结果基本一致。
2.3 PCA和OPLS-DA
PCA是一种用于无监督模式识别的多维数据统计分析方法。在本研究中,对含有QC组的样本(图4-A)进行PCA,作为对各组样本之间和样本内部代谢物差异程度的初步调查。结果表明,第一主成分(PC1)和第二主成分(PC2)的方差贡献率分别为46.43%和22.06%。其中,QC组聚类紧密,表明实验具有良好的重现性,同时,不同组间的成分呈现显著分离,表明3个品种洋葱的代谢组存在显著差异。
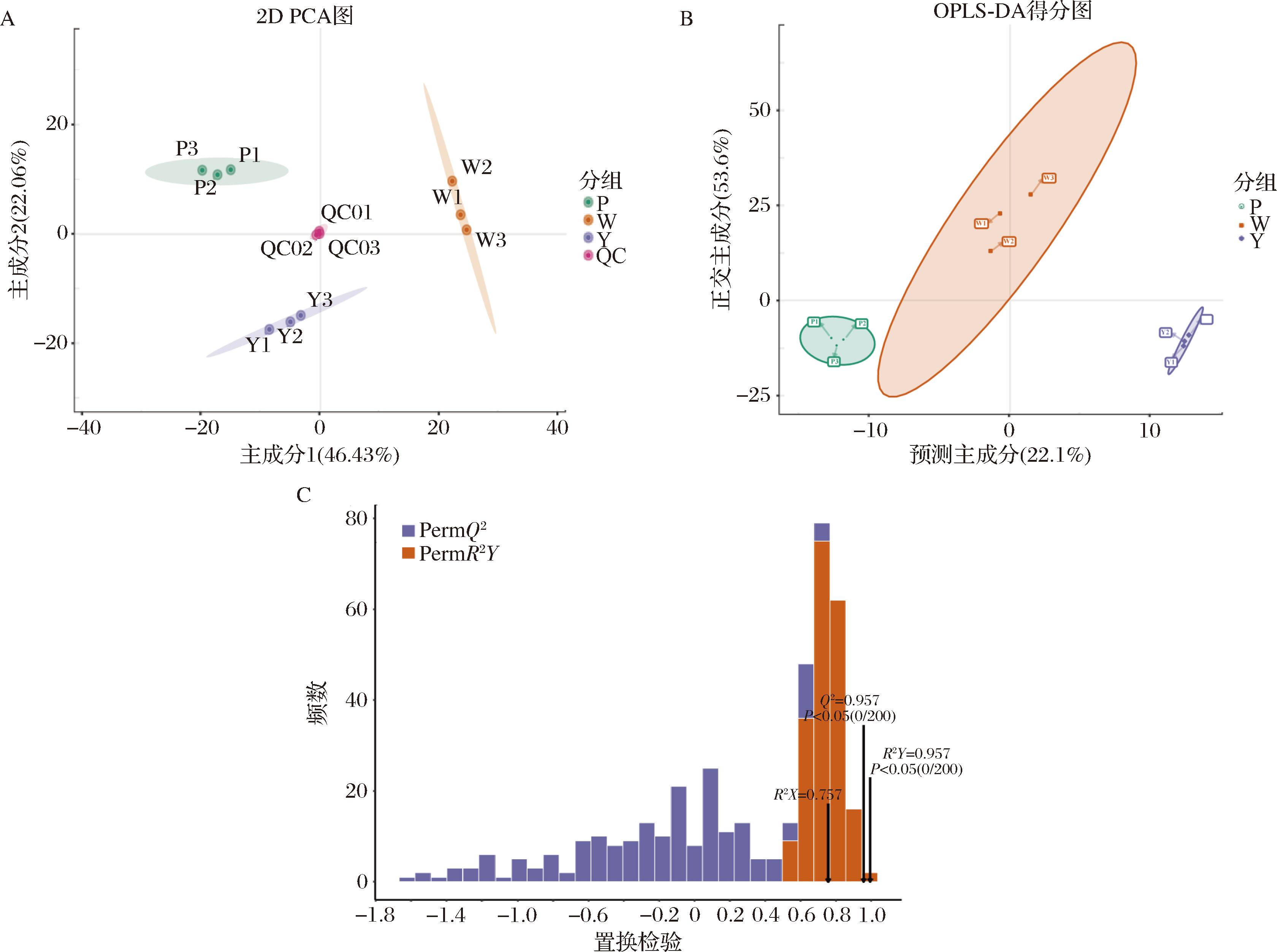
A-PCA;B-OPLS-DA得分图;C-OPLS-DA模型的验证图
图4 三种彩色洋葱样本的PCA、OPLS-DA得分图及OPLS-DA模型的验证图
Fig.4 PCA, OPLS-DA score plots and validation plots of OPLS-DA model for three colored onion samples
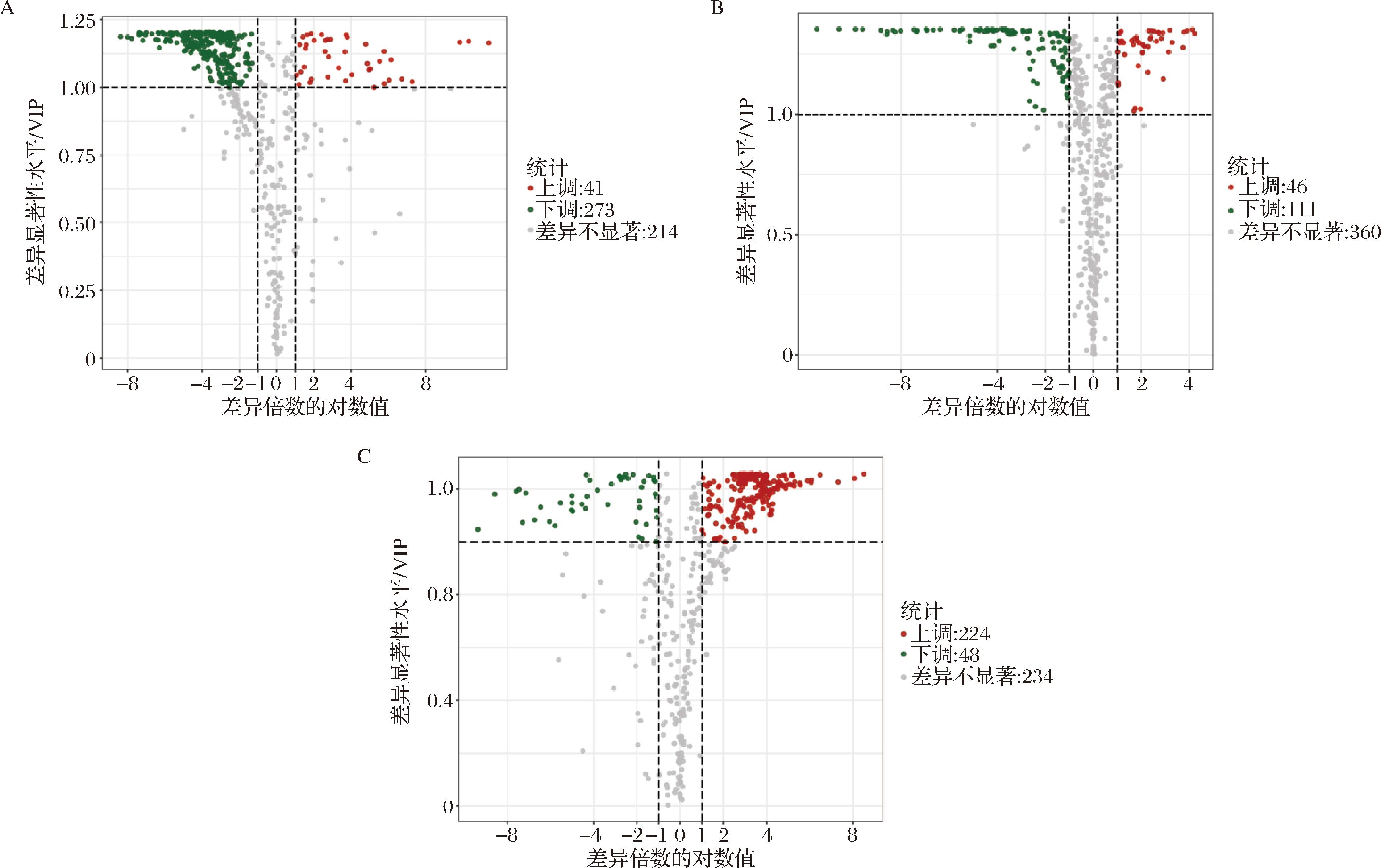
A-W_vs_P;B-Y_vs_P;C-Y_vs_W
图5 三种彩色洋葱组间代谢物差异火山图
Fig.5 Volcano plot of metabolite differences among three colored onion groups
为了进一步探索代谢物组成的差异,研究还采用了OPLS-DA方法。与PCA相比,OPLS-DA能更准确地消除无关差异,实现对差异变量的高效筛选[20]。图4-B为不同品种彩色洋葱OPLS-DA散点图,结果表明3个洋葱品种的样本点均实现了良好的分离,直观地表明其多酚代谢谱存在显著差异。同时,每个品种的所有3个生物重复都形成了紧凑的聚类,反映了组内极好的一致性。这些结果共同证实了不同洋葱品种之间存在着显著的多酚类代谢物差异。
根据OPLS-DA评价模型的预测参数R2X、R2Y和Q2(指标越接近1,模型的稳定性和可靠性越高),对3种有色洋葱的代谢差异模型进行了评价(图4-C)。结果表明,R2X=0.757,R2Y=0.957,Q2=0.957,每个模型的参数都高度趋近于1,表明模型非常稳定,可用于解释3个洋葱品种之间的代谢物变化。
2.4 彩色洋葱鳞茎多酚代谢物的数量及鉴定
在差异倍数≥2和≤0.5,VIP≥1、P<0.05的条件下筛选差异代谢物,并通过火山图展示结果(图5)。在W_vs_P、Y_vs_P和Y_vs_W的比较中,分别有314、157、272个差异代谢物,表明了不同洋葱品种之间在多酚代谢物组成和调控方面的显著差异,其中大多数差异代谢物属于类黄酮和酚酸。ESPINO等[21]研究了3个品种洋葱皮粉中的酚类化合物含量,3种洋葱均为酚类的主要来源,与本研究结果相似。有研究评估热超声处理对增强洋葱汁功能和生物活性特性的影响,结果显示,热超声处理后洋葱中的总酚含量、总类黄酮含量和抗氧化活性均显著增加,同时,研究证明其还有一定的抗癌(诱导结肠癌细胞中11.9%的凋亡细胞死亡)、抗高血压(抑制血管紧张素转换酶)和抗糖尿病(α-葡萄糖苷酶和α-淀粉酶抑制)作用[22]。这些结果可以帮助认识彩色洋葱中主要植物化学物的健康促进功能。
此外,为了系统分析多酚差异代谢物相对含量的变化规律,根据筛选标准对研究中发现的差异代谢物进行了分析,并绘制聚类热图(附图2)。结果显示,次生代谢物类别中共有115种差异代谢物(附表1),包括58种黄酮类、34种酚酸类、21种木脂素和香豆素类以及2种单宁酸类化合物。各组差异代谢物之间的关系用韦恩图表示(图6-A)。进一步通过K-均值聚类分析不同亚组中代谢物相对含量的变化趋势,并将其分为8个光谱类型(图6-B):图谱1、4、6显示,Y组中141个代谢物的累积量高于P组和W组;图谱2、7显示,W组中47个代谢物的累积量明显高于其他2组;图谱3、5、8显示,P组中193个代谢物的累积量高于W组和Y组。
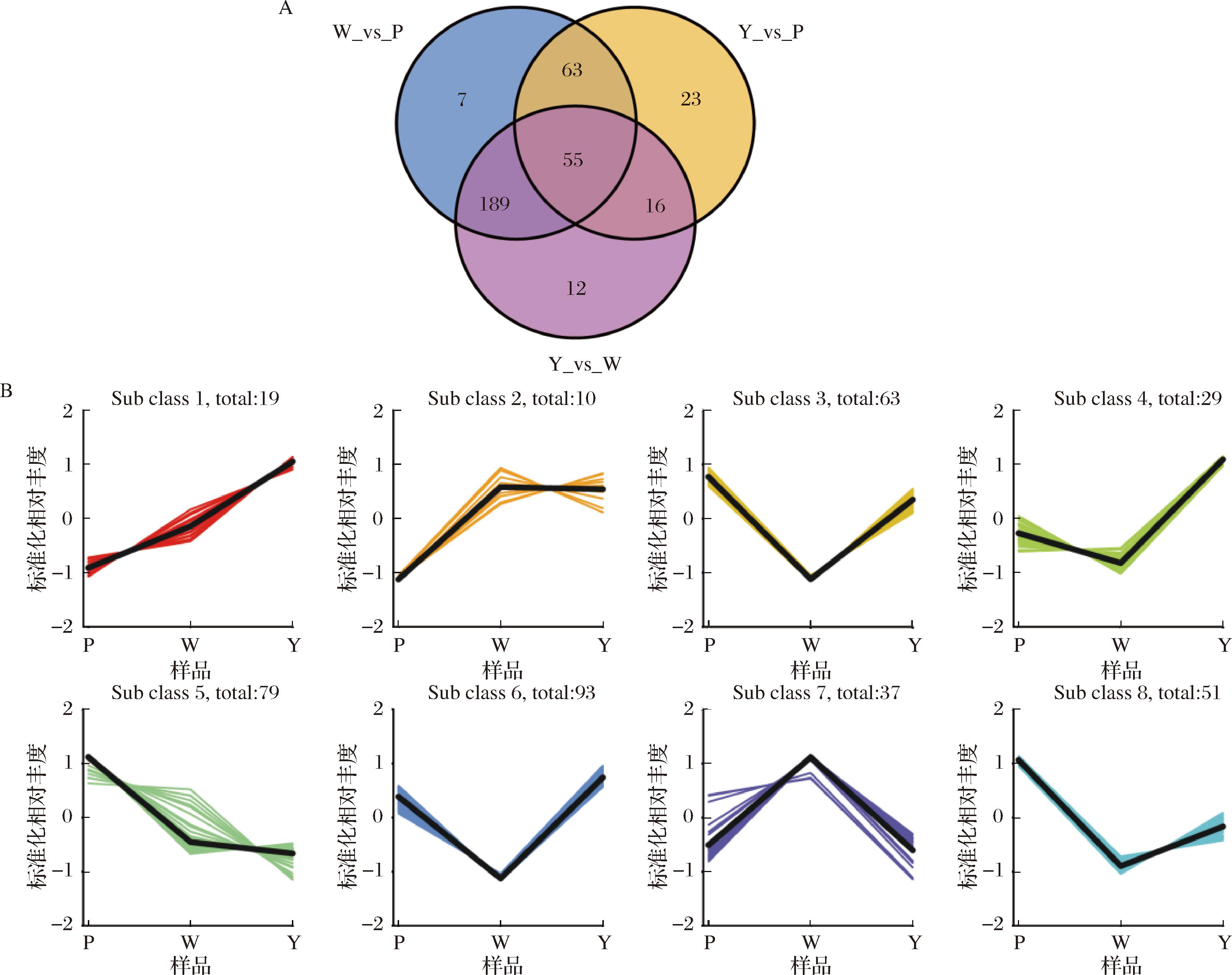
A-3种彩色洋葱的差异代谢物韦恩图;B-差异代谢物K均值聚类图
图6 三种彩色洋葱差异代谢物的韦恩图与K均值聚类分析
Fig.6 Venn diagram and k-means clustering analysis of differential metabolites in three colored onions
注:Sub class 代表相同变化趋势的代谢物类别编号;total 代表该类别代谢物数目。
与W组和Y组相比,P组的4种次生代谢物大多呈上调趋势。其中,除21种黄酮类化合物(3′,5,5′,7-四羟基黄烷酮-7-O-葡萄糖苷、3-异戊烯基-4,2′,4′-三羟基查尔酮、6′-O-对香豆酰基芦荟苦素等)、10种酚酸化合物[2-羟基苯酚-1-O-葡萄糖基-(6→1)-鼠李糖苷、5-没食子酰基-6-O-苯甲酰基葡萄糖、邻苯二甲酸丁基异丁酯等]、9种木脂素和香豆素(5′-甲氧基异落叶松脂素-9′-O-葡萄糖苷、7R,8S-赤式-3′、4,9,9′-四羟基-3-甲氧基-8-O-4′-新木脂素-7-O-吡喃葡萄糖苷等)外,其余代谢物的含量均显著高于W组和Y组。这一结果表明,与白色和黄色洋葱相比,紫色洋葱在抗氧化活性方面可能是更有利的原料选择,而前期对3种彩色洋葱体外抗氧化活性的检测结果也显示,紫色洋葱具有更好的抗氧化能力。
2.6 彩色洋葱鳞茎中差异代谢物的代谢途径分析
通过KEGG通路富集分析,进一步揭示了组间代谢通路的实质性变化。图7-A显示了基于KEGG数据库对3种洋葱差异显著代谢物的分类,结果表明,3个品种的78种差异代谢物中有16种富集在11个非重复KEGG通路中。
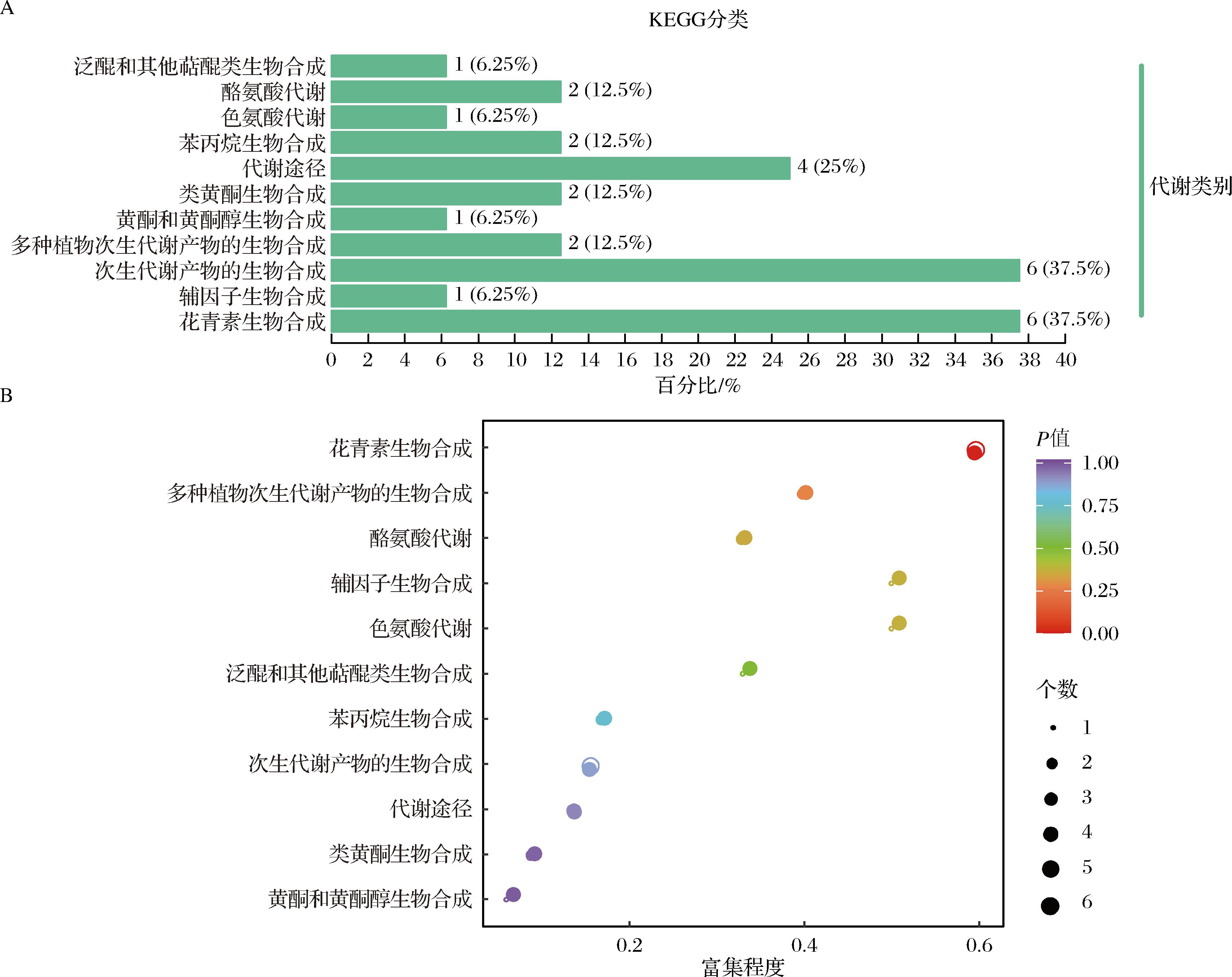
A-差异代谢物通路分类图;B-差异代谢物通路富集图
图7 三种彩色洋葱的差异代谢物通路分类图和差异代谢物通路富集图
Fig.7 Differential metabolite pathway classification map and differential metabolite pathway enrichment map of three colored onions
如图7-B所示,根据P值筛选出显著性最高的前11条代谢途径,其中花青素生物合成富集的代谢物数量最多,表明该途径是3种洋葱中主要的差异代谢物相关途径。花青素是植物中重要的次生代谢产物,其含量和组成决定了植物花和果实的颜色,这也与本研究的结果一致。花青素的生物合成是研究最广泛的次生代谢物途径之一,花青素苷的形成是甲基化等更复杂结构修饰的基础[23],虽然许多研究已经阐明了花青素合成的基本代谢途径,但该代谢途径非常复杂,涉及许多其他次生代谢途径,因此仍需进一步研究。
此外,各种植物次生代谢物的生物合成和酪氨酸代谢途径对3个不同洋葱品种之间的代谢差异也有重要影响。酪氨酸代谢的基本途径是由酪氨酸到生育酚、质醌和泛醌的合成途径,这3种代谢产物以及关键酶酪氨酸转氨酶和对羟基苯基丙酮酸二氧酶在植物体内无处不在,是植物生长发育必不可少的物质[24]。这些研究结果为解析洋葱品种间代谢差异的分子机制提供了一定参考依据。
3 结论
对3种彩色洋葱鳞茎中的多酚代谢物进行了系统的比较分析,共鉴定出528种多酚类代谢物,主要包括黄酮类、酚酸类、鞣质类、木脂素和香豆素等成分。多元统计分析表明多酚代谢物特征存在显著差异,能够实现对不同彩色洋葱的区分。在VIP≥1,差异倍数≥2和≤0.5条件下,得到了115种差异代谢物(1,3,6-三羟基-2,5,7-三甲氧基-9-蒽酮、1-O-阿魏酰奎宁酸、5′-甲氧基异落叶松脂醇-9′-O-葡萄糖苷等)。KEGG通路富集分析显示,花青素生物合成、各种植物次生代谢物生物合成和酪氨酸代谢3条通路是驱动品种差异的核心通路,其中紫色洋葱花青素通路显著富集,这与其色泽特征及多酚类物质积累特性相吻合。未来研究还可结合转录组学深入探究不同品种洋葱代谢差异的分子机制,为洋葱品质改良和理解多酚类物质生理活性奠定理论基础。
[1] TESHIKA J D, ZAKARIYYAH A M, ZAYNAB T, et al.Traditional and modern uses of onion bulb (Allium cepa L.):A systematic review[J].Critical Reviews in Food Science and Nutrition, 2019, 59(sup1):S39-S70.
[2] 曹颖, 张子毓, 戴杨帆, 等.响应面法优化洋葱中多酚的提取工艺研究[J].杭州师范大学学报(自然科学版), 2023, 22(1):52-57.CAO Y, ZHANG Z Y, DAI Y F, et al.Optimization of the extraction process of polyphenol from onion by response surface methodology[J].Journal of Hangzhou Normal University (Natural Science Edition), 2023, 22(1):52-57.
[3] 唐瑶, 陈洋, 曹婉鑫.多酚类化合物的分类、来源及功能研究进展[J].中国食物与营养, 2016, 22(3):32-34.TANG Y, CHEN Y, CAO W X.Research progress in classification, origin and function of polyphenols[J].Food and Nutrition in China, 2016, 22(3):32-34.
[4] 曹艳华, 程丽丽, 张小芳.响应面法优化洋葱多酚的提取工艺及抗氧化性研究[J].食品研究与开发, 2020, 41(12):164-170.CAO Y H, CHENG L L, ZHANG X F.Study on extraction of polyphenol from onion by response surface methods and antioxidant activity[J].Food Research and Development, 2020, 41(12):164-170.
[5] METRANI R, SINGH J, ACHARYA P, et al.Comparative metabolomics profiling of polyphenols, nutrients and antioxidant activities of two red onion (Allium cepa L.) cultivars[J].Plants, 2020, 9(9):1077.
[6] MITROV K, HRBEK V, SVOBODA P, et al.Antioxidant activity, S-alk(en)yl-l-cysteine sulfoxide and polyphenol content in onion (Allium cepa L.) cultivars are associated with their genetic background[J].Czech Journal of Food Sciences, 2016, 34(2):127-132.
K, HRBEK V, SVOBODA P, et al.Antioxidant activity, S-alk(en)yl-l-cysteine sulfoxide and polyphenol content in onion (Allium cepa L.) cultivars are associated with their genetic background[J].Czech Journal of Food Sciences, 2016, 34(2):127-132.
[7] 曾雷, 陈颖乐, 王颂, 等.基于UPLC-MS/MS广泛靶向代谢组学分析野生竹叶榕不同部位代谢物差异[J].亚热带植物科学, 2025, 54(2):144-157.ZENG L, CHEN Y L, WANG S, et al.Metabolite differences in different parts of wild Ficus stenophylla based on widely targeted metabolomics combined with UPLC-MS/MS[J].Subtropical Plant Science, 2025, 54(2):144-157.
[8] ARKORFUL E, YU Y, CHEN C S, et al.Untargeted metabolomic analysis using UPLC-MS/MS identifies metabolites involved in shoot growth and development in pruned tea plants (Camellia sinensis (L.) O.Kuntz)[J].Scientia Horticulturae, 2020, 264:109164.
[9] SUN Y L, YANG Y, ZHOU M C, et al.Widely targeted metabolic profiling reveals differences in polyphenolic metabolites during Rosa xanthina f.spontanea fruit development and ripening[J].Metabolites, 2022, 12(5):438.
[10] 王蓉, 曾文锦, 刘盼, 等.顶空固相微萃取结合气相色谱-质谱联用法对3种洋葱挥发性风味成分的分析[J].食品工业科技, 2022, 43(2):319-327.WANG R, ZENG W J, LIU P, et al.Analysis of volatile flavor components in three onion by headspace solid phase microextraction combined with gas chromatography-mass spectrometry[J].Science and Technology of Food Industry, 2022, 43(2):319-327.
[11] 景仁, 马驰.“酒泉洋葱”申请地理标志产品保护[N].酒泉日报, 2010-11-16.JING R, MA C.Jiuquan onions apply for geographical indication product protection [N].Jiuquan Daily, 2010-11-16.
[12] CHENG K Q, XIAO J Z, HE J Y, et al.Unraveling volatile metabolites in pigmented onion (Allium cepa L.) bulbs through HS-SPME/GC-MS-based metabolomics and machine learning[J].Frontiers in Nutrition, 2025, 12:1582576.
[13] JIN W G, ZHAO S B, CHEN X H, et al.Characterization of flavor volatiles in raw and cooked pigmented onion (Allium cepa L) bulbs:A comparative HS-GC-IMS fingerprinting study[J].Current Research in Food Science, 2024, 8:100781.
[14] DÜLGER ALTINER D, Y KM
KM
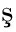 S, BOZGEYI\U0307K E, et al.Thermosonication as a novel processing technique to enhance phenolic content, amino acids, and health-promoting activities of white onion juice[J].ACS Omega, 2025, 10(23):25051-25067.
S, BOZGEYI\U0307K E, et al.Thermosonication as a novel processing technique to enhance phenolic content, amino acids, and health-promoting activities of white onion juice[J].ACS Omega, 2025, 10(23):25051-25067.
[15] ABOTALEB M, LISKOVA A, KUBATKA P, et al.Therapeutic potential of plant phenolic acids in the treatment of cancer[J].Biomolecules, 2020, 10(2):221.
[16] S NCHEZ M, ROMERO M, G
NCHEZ M, ROMERO M, G MEZ-GUZM
MEZ-GUZM N M, et al.Cardiovascular effects of flavonoids[J].Current Medicinal Chemistry, 2019, 26(39):6991-7034.
N M, et al.Cardiovascular effects of flavonoids[J].Current Medicinal Chemistry, 2019, 26(39):6991-7034.
[17] TAO H, LI L Y, HE Y Q, et al.Flavonoids in vegetables:Improvement of dietary flavonoids by metabolic engineering to promote health[J].Critical Reviews in Food Science and Nutrition, 2024, 64(11):3220-3234.
[18] LI Q L, WANG Y H, MAI Y X, et al.Health benefits of the flavonoids from onion:Constituents and their pronounced antioxidant and anti-neuroinflammatory capacities[J].Journal of Agricultural and Food Chemistry, 2020, 68(3):799-807.
[19] LACHMAN J, PRON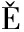 K D, HEJTM
K D, HEJTM NKOV
NKOV A, et al.Total polyphenol and main flavonoid antioxidants in different onion (Allium cepa L.) varieties[J].Horticultural Science, 2003, 30(4):142-147.
A, et al.Total polyphenol and main flavonoid antioxidants in different onion (Allium cepa L.) varieties[J].Horticultural Science, 2003, 30(4):142-147.
[20] KANG C D, ZHANG Y Y, ZHANG M Y, et al.Screening of specific quantitative peptides of beef by LC-MS/MS coupled with OPLS-DA[J].Food Chemistry, 2022, 387:132932.
[21] ESPINO N, GALIETTA G, VODANOVICH A, et al.Onion skin (Allium cepa L.) of three Landrace varieties produced in Uruguay:Minerals and fatty acids composition, phytochemical compounds, in vitro antioxidant and anti-inflammatory properties[J].Food Bioscience, 2025, 71:107112.
[22] KANEHISA M, FURUMICHI M, SATO Y, et al.KEGG for taxonomy-based analysis of pathways and genomes[J].Nucleic Acids Research, 2023, 51(D1):D587-D592.
[23] LIM I, HA J.Biosynthetic pathway of proanthocyanidins in major cash crops[J].Plants, 2021, 10(9):1792.
[24] SCHENCK C A, MAEDA H A.Tyrosine biosynthesis, metabolism, and catabolism in plants[J].Phytochemistry, 2018, 149:82-102.