青稞(Hordeum vulgare var. coeleste Linnaeus)属一年生草本植物,是大麦的一个亚型。因其颖果与稃体易分离而俗称“裸大麦”或“元麦”,在我国青藏高原地区承载着深厚的饮食文化内涵与传统医学价值[1]。研究显示,每100 g青稞含碳水化合物约60~75 g,蛋白质6.4~21 g,脂肪仅1.18~3.09 g,呈现典型的“三高两低”特点[2]。其中,β-葡聚糖含量高达5.25%~8.62%(质量分数),具有显著的降血脂、调节血糖等生理功能。青稞传统用于制作糌粑、青稞酒,现经深加工制成青稞茶。青稞茶富含多种生物活性成分,具有去油解腻、调节血糖的功效[3]。青稞茶的加工主要以干热加工为主,包括蒸煮、烘烤、焙炒以及微波处理。这些加工方式主要利用高温条件激发美拉德反应,一方面促使青稞在焙烤过程中生成独特的香气,另一方面其产生的热量会破坏青稞原本的细胞结构,使得黄酮类化合物、多糖、无机盐、氨基酸等营养成分更容易在茶汤中释放出来,从而赋予了青稞茶汤特殊的口感[4]。
研究显示,160 ℃烘烤处理可使青稞茶中游离总酚含量提高44.82%,结合总酚含量提高13.30%[5]。WANG等[6]发现,烘烤6.0 min的青稞茶β-葡聚糖释放量高、抗氧化活性低,烘烤9.0 min和12.0 min的青稞茶利于总糖、蛋白质、多酚、类黄酮和游离氨基酸溶出。然而,针对青稞茶热加工条件对其理化特性与感官风味的系统研究仍存在不足,尤其是缺乏对不同烘烤条件下营养成分保留率的精确量化分析,导致难以掌握营养物质在烘烤过程中的变化规律。其次,在不同烘烤温度和时间下,香气物质的种类、含量和比例变化尚不明确。此外,高温烘烤时美拉德反应可能产生潜在有害副产物,这也为青稞茶的品质和安全性带来挑战。因此,如何在保证青稞茶香气宜人的同时,尽量减少毒副产物的产生,是当前青稞茶加工领域亟待解决的关键问题。
本研究采用不同烘烤温度(170~190 ℃)与时间(5~15 min)双因子组合的实验设计,借助扫描电子显微镜、高效液相色谱及气相色谱-质谱联用等多技术手段,系统解析烘烤工艺对青稞微观结构和青稞茶活性成分保留、美拉德反应产物生成及感官风味组成的影响。明确兼具营养成分保留、风味品质提升与安全风险控制的最优烘烤条件,为优质青稞茶工业化生产提供理论依据与技术支撑。
1 材料与方法
1.1 材料与试剂
“藏青2000”青稞产地为西藏,由西藏农牧科学研究院提供,贮藏于4 ℃条件下备用。
福林酚、6-羟基-2,5,7,8-四甲基色烷-2-羧酸(Trolox)、2,4,6-三吡啶-S-三嗪(2,4,6-tripyridyl-S-triazine,TPTZ)、乙二醛、DNS试剂、苯酚(均为分析纯),天津索罗门生物科技有限公司;没食子酸(色谱纯),天津索罗门生物科技有限公司;碳酸钠、亚硝酸钠、氢氧化钠、儿茶素(catechin equivalent,CE)、DPPH、硫磺水杨酸、硼酸、浓盐酸、浓硫酸、六水氯化铁、乙酸钠(均为分析纯),天津市江天化工技术股份有限公司;L-抗坏血酸、磷酸二氢钠二水合物、磷酸氢二钠十二水合物(均为分析纯),天津百奥泰科技发展有限公司;甲醇、乙腈、5-羟甲基糠醛(均为色谱纯),凯玛特(天津)化工科技有限公司;甲基乙二醛(分析纯),安徽泽升科技有限公司。
1.2 仪器与设备
DHG-9140A电热鼓风干燥箱,安徽宁怀仪器有限公司;C40电烤箱,青岛多益智能电器有限公司;FD-1A-50+冷冻干燥机,博医康(天津)仪器有限公司;SU3800扫描电子显微镜、F-7000荧光分光光度计,日本日立公司;ES-J220电子分析天平,天津市德安特传感技术有限公司;DL-3021HR医用冷冻离心机,安徽中科都菱商用电器有限公司;Synergy HTX多功能酶标仪,美国伯腾仪器有限公司;SI-0246漩涡震荡仪,美国Scientific Industries公司;Agilent 1260高效液相色谱、8890-7010C/5977C三重四级杆气质联用仪,美国安捷伦科技有限公司;PENS3电子鼻,Schwerin Air sense Analytics公司。
1.3 实验方法
1.3.1 青稞样品预处理
仔细挑除青稞原料中的碎粒、泥沙和其他杂质,清水反复冲洗3次,彻底清除残留杂质。将洗净的青稞均匀平铺在托盘上,置于45 ℃的烘箱内干燥至含水率12%~14%(质量分数),达到工艺安全贮藏水分状态。
1.3.2 青稞的加工工艺
准确称取预处理后的青稞50 g,均匀平铺在边长30 cm的锡纸盒中,置于热风烘烤架上,设置温度分别为170、180、190 ℃,时间分别为5、10、15 min进行烘烤处理。烘烤结束后,将青稞转移至干燥的环境中冷却至室温,以备后续实验使用。
1.3.3 烘烤处理青稞微观结构分析
参考KARANAM等[7]的方法并稍作修改。使用双刃刀将烘烤处理后的青稞切成尺寸为8 mm×6 mm×6 mm的立方体,利用导电双面胶将样品固定在金属载物台上,并进行溅射镀金处理,利用扫描电子显微镜于10 kV加速电压下放大50倍和1 000倍观察样品微观结构并拍照。
1.3.4 青稞茶色度的测定
采用高稳定性台式分光测色仪对青稞茶的颜色进行测定。色差计算如公式(1)所示:
(1)
式中:L*表示明亮度,a*表示红绿值,b*表示黄蓝值;ΔL*、Δa*和Δb*分别表示样品测定值与标准值的差值;ΔE表示总色差值。
1.3.5 青稞茶基础成分测定
1.3.5.1 青稞活性成分浸提液的制备
参考SCHLÖRMANN等[8]的方法并适当修改。使用研磨机对烘烤后的青稞进行研磨并通过60目筛,将粉末冷冻干燥24 h放入干燥器中贮存备用。青稞粉与沸水按料液比1∶10(g∶mL)冲泡20 min,4 000×g室温离心5 min,取上清液,得到青稞茶提取液,常温下避光保存。
1.3.5.2 青稞茶生物活性成分的测定
参考TANG等[9]的方法并稍作修改。以没食子酸为标准品绘制标准曲线(Y=7.811 5X+0.084 5,R2=0.999 3)。样品总酚含量以没食子酸当量(gallic acid equivalent, GAE)表示,单位为mg GAE/g(每克样品干重所含的没食子酸当量毫克数)。
参考ZHANG等[10]的方法并略作修改。以儿茶素为标准品绘制标准曲线(Y=0.629 5X+0.045,R2=0.999 4),样品总黄酮含量以儿茶素当量表示,单位为mg CE/g(每克样品干重所含的儿茶素当量毫克数)。
1.3.5.3 青稞茶抗氧化活性的测定
参考TANG等[11]的方法并适当调整。以水溶性维生素E为标准品绘制标准曲线(Y=-0.002 1X+0.104 7,R2=0.999 9),DPPH自由基清除能力以水溶性维生素E当量(Trolox equivalent, TE)表示,单位为μmol TE/g(每克样品干重所含的Trolox 当量微摩尔数)。
参考TANG等[9]的方法并稍作修改。以抗坏血酸为标准品绘制标准曲线(Y=0.001 5X+0.073 7,R2=0.999 8),铁还原抗氧化能力以抗坏血酸当量(ascorbic acid equivalent, AAE)表示,单位为μmol AAE/g(每克样品干重所含的抗坏血酸当量微摩尔数)。
1.3.6 青稞茶美拉德反应产物的测定
1.3.6.1 青稞茶中乙二醛、甲基乙二醛含量测定
采用HPLC进行分析[12]。色谱条件:Agilent Zorbx AQ-C18色谱柱(柱长250 mm,内径4.6 mm,粒径5 μm);流动相A:含0.1%(体积分数)乙酸的水溶液,流动相B:含0.1%(体积分数)乙酸的甲醇溶液;流速0.8 mL/min;进样量10 μL;检测波长315 nm。梯度洗脱程序:0~2 min,95%(A)~5%(B);2~4 min,80%(A)~20%(B);4~7 min,40%(A)~60%(B);7~9 min,20%(A)~80%(B);14~17 min,100%(B);17~17.5 min,95%(A)~5%(B);17.5~20.5 min,95%(A)~5%(B)。
1.3.6.2 青稞茶中5-羟甲基糠醛、晚期糖基化终产物(advanced glycation end-products, AGEs)、类黑精含量测定
使用Agilent 1260 HPLC仪检测5-羟甲基糠醛[13]。色谱条件:Agilent Zorbx AQ-C18色谱柱(250 mm×4.6 mm×5 μm);流动相A:含0.1%(体积分数)乙酸的水溶液,流动相B:含0.1%(体积分数)乙酸的乙腈溶液;流速为1 mL/min;进样量20 μL;检测波长280 nm。梯度洗脱程序:0~2 min,5%(B);2~4 min,5%(A)~15%(B);4~12 min,15(A)~25%(B);12~25 min,25(A)~35%(B);25~28 min,35(A)~100%(B);28~30 min,100%(B);30~30.5 min,100%(A)~5%(B)。
参考QIN等[14]的研究以及PATRIGNANI等[15]的方法稍作修改。将青稞茶提取液用0.05 mol/L PBS(pH=7.4)稀释10倍。在激发波长345 nm、发射波长435 nm、狭缝宽度5 nm条件下记录AGEs荧光强度。激发波长350 nm、发射波长430 nm、狭缝宽度5 nm条件下记录类黑精荧光强度。结果均以任意单位(AU)/毫升表示。
1.3.7 青稞茶风味物质的测定
1.3.7.1 电子鼻的测定
采用PEN3便携式电子鼻对不同烘焙条件下青稞茶的挥发性香气进行分析[16],电子鼻传感器性能如表1所示。取5 mL不同处理的青稞茶提取液置于15 mL固相微萃取顶空进样瓶中,60 ℃恒温水浴摇床30 min。冷却至室温后,将进样针与平衡针插入密闭瓶采集180 s,取160~170 s数据分析挥发性成分相对含量。
表1 PENS3电子鼻传感器阵列及敏感物质
Table 1 PENS3 electronic nose sensor array and sensitive substances
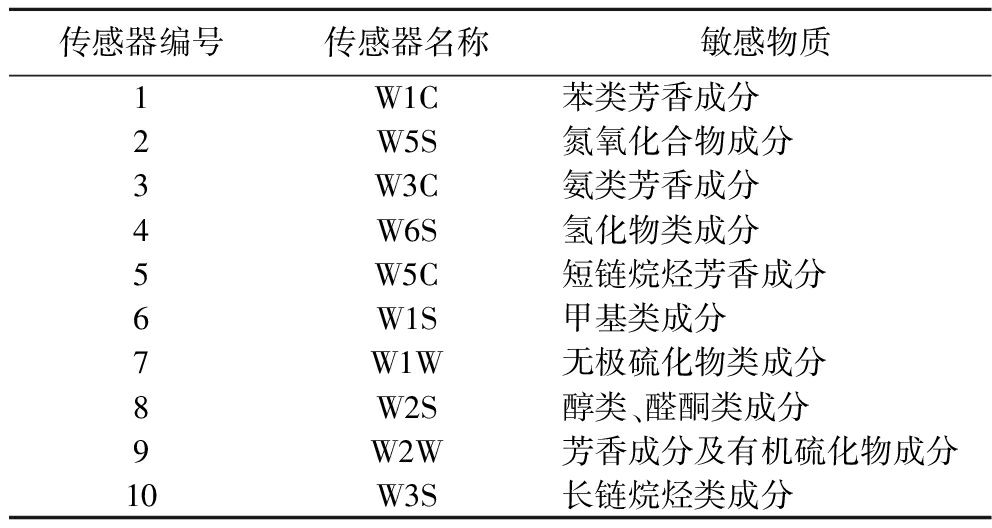
传感器编号传感器名称敏感物质1W1C苯类芳香成分2W5S氮氧化合物成分3W3C氨类芳香成分4W6S氢化物类成分5W5C短链烷烃芳香成分6W1S甲基类成分7W1W无极硫化物类成分8W2S醇类、醛酮类成分9W2W芳香成分及有机硫化物成分10W3S长链烷烃类成分
1.3.7.2 大体积顶空预浓缩-气相色谱-质谱的测定
参考WANG等[17]的方法稍作修改。采用大体积顶空预浓缩-气相色谱-质谱(large volume headspace preconcentration-gas chromatography-mass spectrometry,LVHP-GC-MS)联用系统对挥发性成分进行分析,该系统包括7650M、7200 CTS-C2和GC-MS,设置2种检测路径:M1(捕集温度为35 ℃,持续3 min;解吸温度为150 ℃,持续3 min;平衡温度为150 ℃,持续20 min)和M2(捕集温度为35 ℃,持续3 min;解吸温度为180 ℃,持续3 min;平衡温度为190 ℃,持续20 min),使用配备HP-5MS UI色谱柱的GC-MS系统进行分析。借助计算机化的NIST20质谱库与RTLPEST比对鉴定未知化合物,取匹配值在700~1 000(>80%可能性)的结果分析。
1.3.8 青稞茶的感官评价
参考对青稞银耳红曲茶的研究及GB/T 23776—2018《茶叶感官审评方法》确定产品品质[18],评议小组由7名熟悉掌握感官评价标准并通过培训的专业人员组成,具体的评分标准如表2所示。
表2 青稞茶感官评价标准
Table 2 Sensory evaluation criteria of highland barley tea

评价项目评分标准分值/分青稞外形(10%)表面金黄有光泽、形态胀裂且露出白芯8~10表面黄爽、形态膨胀略带裂缝5~7表面暗淡无光并发黑、形态皱缩1~4汤色(20%)金黄色澄清、透亮18~20黄色澄清、透亮15~17淡黄色澄清、欠透亮9~14褐色澄清、欠透亮5~8褐色浑浊1~4香气(30%)清香25~30焦香19~24淡香或微焦12~16微生或焦味8~11生味或糊味1~8口感(35%)鲜爽顺滑、回味甘甜29~35浓醇较爽口、略带有甜味21~28尚醇、有轻微涩感16~20入口稍苦涩,微生11~15苦涩,有明显生淀粉味1~10综合评价(5%)层次丰富,自然麦香与焦甜感完美交融5风味杂糅,烤香中裹挟青涩或微焦尾韵3~4焦苦难掩,焦糊味掩盖谷物本真风味1~2
1.4 数据分析
采用SPSS 2022、Excel 2019和Origin 2024对数据进行统计分析和处理,显著差异性分析采用ANOVA单因素方差分析。数据以“平均值±标准差”表示,LSD检验认为P<0.05差异有统计学意义。
2 结果与分析
2.1 不同烘烤处理对青稞微观组织结构的影响
图1对比了不同烘烤条件下青稞与未处理青稞(对照组)的微观结构变化。其中,对照组青稞谷粒结构致密、截面光滑,胚乳无空腔或裂缝形成(图1-a,Raw)。经烘烤处理后,胚乳呈现明显的热损伤特征(图1-a,A~I)。随着烘烤温度升高,青稞胚乳中出现带有空隙的大空腔,并且烘烤温度越高,空腔开口越大。这是因为胚乳受热而膨胀,温度过高时胚乳内部的水分及其他挥发性物质会迅速减少,胚乳收缩并形成空腔,这与SCHOEMAN等[19]的研究相似。随着烘烤时间的延长,青稞表面出现了疏松的结构和较大的裂缝,说明青稞皮层与胚乳之间的结合能力减弱,淀粉、蛋白质等成分逐渐暴露出来。如图1-b(A~I)所示,在1 000倍放大倍数下,可以更清楚地看到,在相同温度下烘烤的样品,其淀粉颗粒会随着烘烤时间的延长而变得肿胀、疏松且变形,但仍可辨别。这与热处理能够改变谷物的外观和结构相一致[20]。
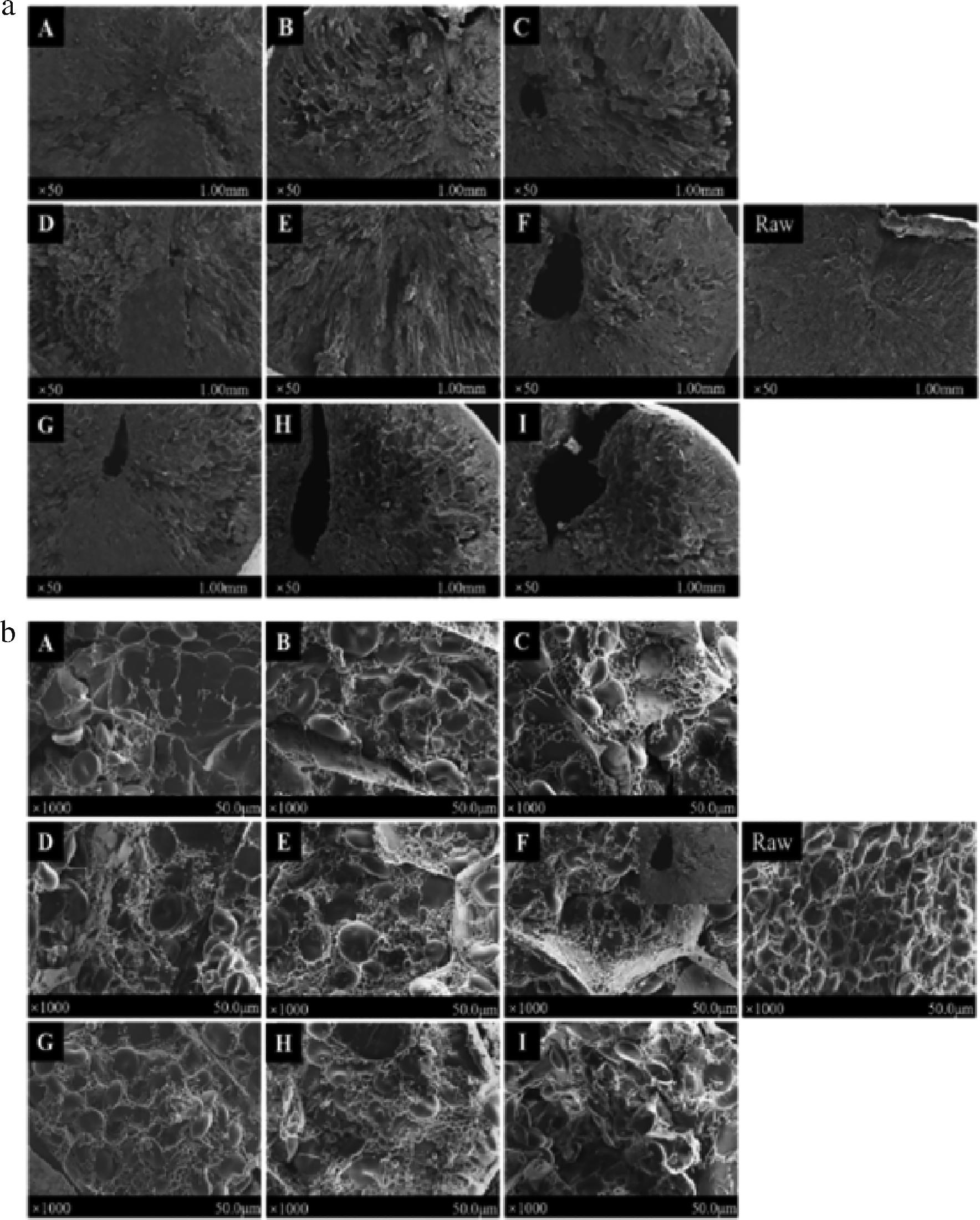
A-170 ℃ 5 min;B-170 ℃ 10 min;C-170 ℃ 15 min;D-180 ℃ 5 min;E-180 ℃ 10 min;F-180 ℃ 15 min;G-190 ℃ 5 min;H-190 ℃ 10 min;I-190 ℃ 15 min。
a-50倍;b-1 000倍
图1 不同烘烤处理青稞在50倍和1 000倍放大下的微观结构电镜图
Fig.1 Microstructure of highland barley from different roast under 50× and 1 000× magnifications of scanning electron microscope
2.2 不同烘烤处理对青稞茶色泽的影响
如图2所示,随着烘烤时间延长和烘烤温度的增加,青稞茶的颜色明显加深,L*(亮度)、a*(红绿值)、b*(黄蓝值)差异显著(P<0.05)。如表3所示,与对照样品相比,烘烤显著降低了青稞茶的L*值,从94.51±0.63(未经处理的青稞茶)降至63.27±0.09(190 ℃、5 min),这是由于青稞茶中花青素等酚类化合物的氧化降解和持续进行的美拉德反应所致[21]。烘烤温度190 ℃条件下,随着烘烤时间的延长,青稞茶的L*值下降越明显。当烘烤温度为170 ℃时,随着烘烤时间从5 min延长至15 min,青稞茶ΔE值从84.00±0.82升至89.74±0.04,表明颜色逐步加深,且变化幅度显著,符合美拉德反应和非酶褐变的累积效应。

图2 不同烘烤处理对青稞茶外观颜色的影响
Fig.2 Effects of different roasting treatments on the color of highland barley tea
表3 不同烘烤处理对青稞茶色泽参数的影响
Table 3 Effects of different roasting treatments on the color parameters of highland barley tea
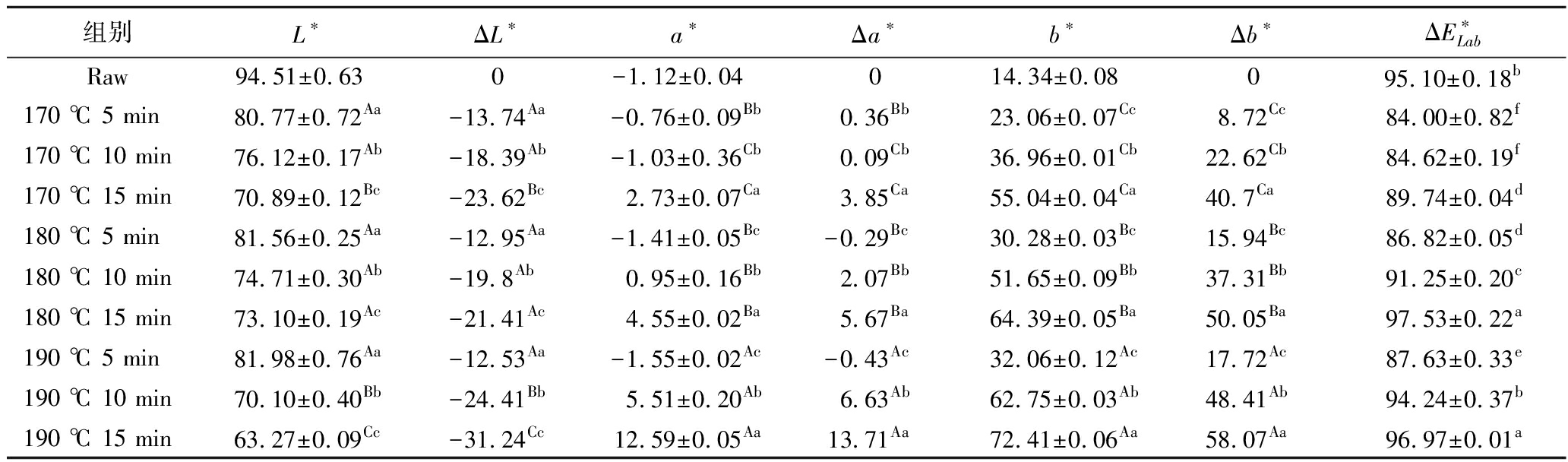
组别L∗ΔL∗a∗Δa∗b∗Δb∗ΔE∗LabRaw94.51±0.63 0-1.12±0.04 014.34±0.08 095.10±0.18b170 ℃ 5 min80.77±0.72Aa-13.74Aa-0.76±0.09Bb0.36Bb23.06±0.07Cc8.72Cc84.00±0.82f170 ℃ 10 min76.12±0.17Ab-18.39Ab-1.03±0.36Cb0.09Cb36.96±0.01Cb22.62Cb84.62±0.19f170 ℃ 15 min70.89±0.12Bc-23.62Bc2.73±0.07Ca3.85Ca55.04±0.04Ca40.7Ca89.74±0.04d180 ℃ 5 min81.56±0.25Aa-12.95Aa-1.41±0.05Bc-0.29Bc30.28±0.03Bc15.94Bc86.82±0.05d180 ℃ 10 min74.71±0.30Ab-19.8Ab0.95±0.16Bb2.07Bb51.65±0.09Bb37.31Bb91.25±0.20c180 ℃ 15 min73.10±0.19Ac-21.41Ac4.55±0.02Ba5.67Ba64.39±0.05Ba50.05Ba97.53±0.22a190 ℃ 5 min81.98±0.76Aa-12.53Aa-1.55±0.02Ac-0.43Ac32.06±0.12Ac17.72Ac87.63±0.33e190 ℃ 10 min70.10±0.40Bb-24.41Bb5.51±0.20Ab6.63Ab62.75±0.03Ab48.41Ab94.24±0.37b190 ℃ 15 min63.27±0.09Cc-31.24Cc12.59±0.05Aa13.71Aa72.41±0.06Aa58.07Aa96.97±0.01a
注:同一列中不同大写字母(A~C)表示相同烘烤时间下不同烘烤温度之间的差异具有统计学意义(P<0.05),不同小写字母(a~c)表示相同烘烤温度下不同烘烤时间之间的差异具有统计学意义(P<0.05)。
2.3 不同烘烤处理对青稞茶理化特性的影响
2.3.1 不同烘烤处理对青稞茶生物活性成分的影响
酚类物质是青稞抗氧化活性的主要功能成分,烘烤处理可通过释放结合态多酚显著增强其抗氧化活性[22]。如图3-a所示,随着烘烤时间延长,青稞茶总酚含量呈阶梯式增长(P<0.05)。烘烤温度170 ℃条件下,5 min时总酚含量为(3.47±0.02) mg GAE/g,10 min升至(4.06±0.01) mg GAE/g,15 min达(5.39±0.01) mg GAE/g。当烘烤时间为15 min时,170、180、190 ℃处理组的总酚含量分别为(5.39±0.01)、(5.68±0.02)、(5.71±0.13) mg GAE/g,其含量虽显著上升,但温度变化引起的增幅显著低于时间效应。原因可能是当温度超过170 ℃时,木质素-酚酸酯键断裂速率加快,释放出游离酚酸,与此同时,游离酚类在高温下也同步发生氧化降解,形成“释放-分解”动态平衡,导致温度单因素作用不显著[23]。
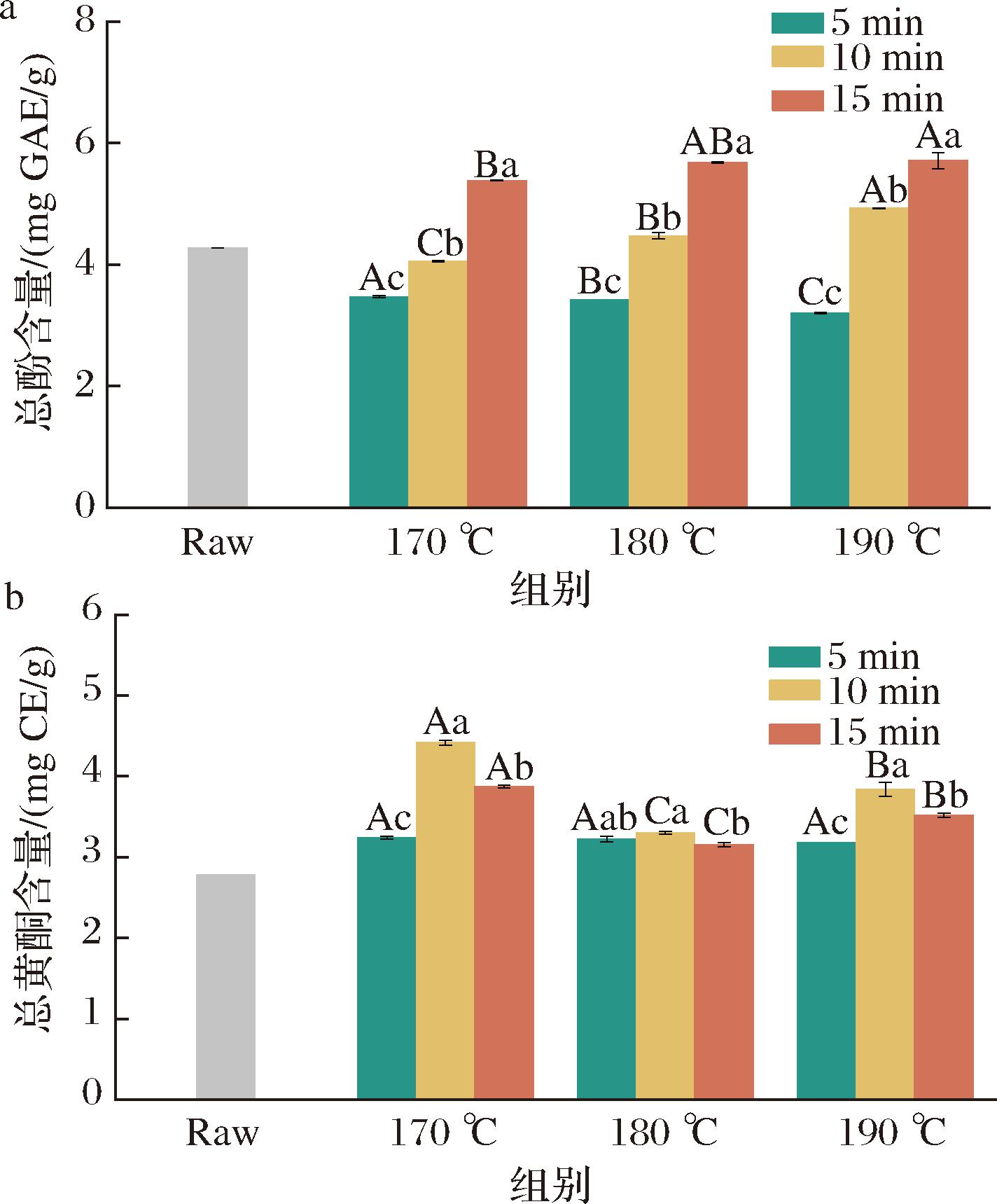
a-总酚含量;b-总黄酮含量
图3 不同烘烤处理对青稞茶生物活性成分的影响
Fig.3 Effects of different roasting treatments on bioactive ingredients of highland barley tea
注:大写字母(A~C)表示相同烘烤时间下不同烘烤温度之间的差异具有统计学意义(P<0.05);小写字母(a~c)表示相同烘烤温度下不同烘烤时间之间的差异具有统计学意义(P<0.05)(下同)。
由图3-b可知,总黄酮含量与烘烤温度和时间之间呈动态变化。与未经处理的青稞茶总黄酮含量(2.78 mg CE/g)相比,提高烘烤温度和延长烘烤时间有利于增加黄酮类化合物的释放量。这可能是由于烘烤热诱导细胞结构变化促进了黄酮类化合物的释放[24]。但随着烘烤时间的延长,总黄酮含量呈现出先增加后减少的趋势。170 ℃烘烤条件下,青稞茶中总黄酮含量5 min达(3.24±0.02) mg CE/g,10 min升至峰值(4.42±0.03) mg CE/g,15 min回落至(3.88±0.02) mg CE/g。这一现象与BABIKER等[25]研究烘烤对大麻籽中总黄酮影响的结果相似。而在180 ℃烘烤条件下,总黄酮含量随烘烤时间延长整体波动不大,这可能是由于在该温度下,黄酮的释放仍在进行,但热降解的影响已经开始显现。
2.3.2 不同烘烤处理对青稞茶抗氧化能力的影响
通过DPPH自由基清除能力和铁离子还原抗氧化能力(ferric reducing antioxidant power,FRAP)2种方法能够更全面地评估不同烘烤处理后青稞茶的抗氧化活性[26]。由图4可知,烘烤后的青稞茶DPPH自由基清除能力和铁还原抗氧化能力的变化趋势与总酚含量(图3-a)的变化趋势相似。在相同温度下,随着烘烤时间的延长,DPPH值呈上升趋势。在相同的烘烤时间条件下,随着烘烤温度的升高,美拉德反应加剧,因此,DPPH自由基清除能力也略有增强。与未经处理的青稞茶相比,升高温度显著提高了青稞茶的铁离子还原抗氧化能力。然而,在170~190 ℃的条件下,随着烘烤时间的延长,铁离子还原抗氧化能力并未受到显著影响,这可能是因为高温烘烤可能促使酚类物质发生氧化反应,生成醌类等氧化产物。醌类物质的还原电位与酚类不同,其电子转移能力相对较弱,使得在FRAP检测中,氧化后的酚类物质对铁离子还原抗氧化能力的提升效果不明显[27]。
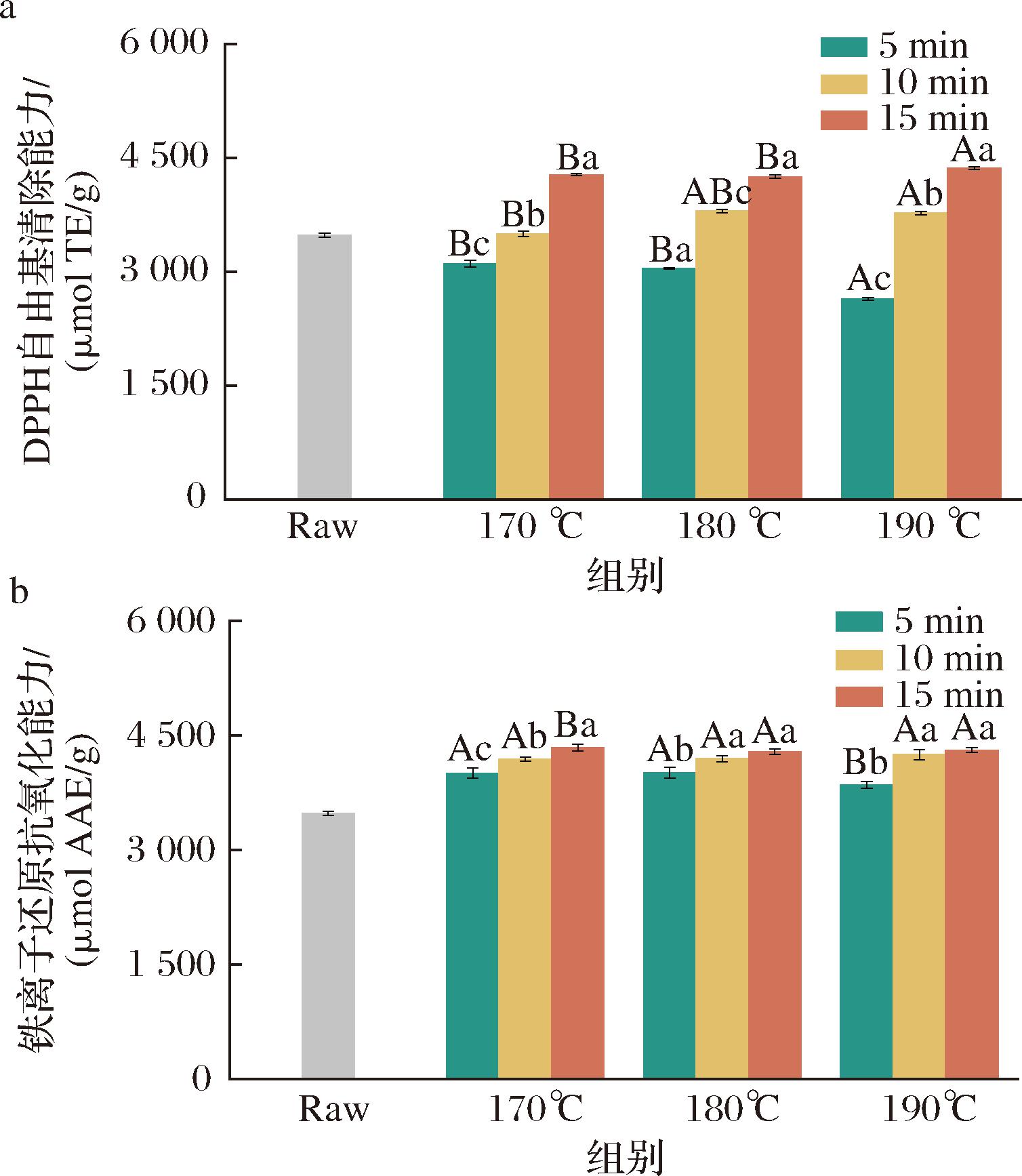
a-DPPH自由基清除能力;b-铁离子还原抗氧化能力
图4 不同烘烤处理对青稞茶抗氧化能力的影响
Fig.4 Effects of different roasting treatments on the antioxidant capacity of highland barley tea
2.3.3 不同烘烤处理对青稞茶美拉德反应产物含量的影响
美拉德反应作为食品热加工的核心化学过程,在赋予食品独特焦香风味的同时,也产生潜在的健康隐患。乙二醛和甲基乙二醛是具有高反应活性的醛类物质,可引起人体内氧化应激和炎症反应,是多种疾病的诱因[16]。如图5-a、5-b所示,随着烘烤温度升高和烘烤时间延长,青稞茶中乙二醛和甲基乙二醛的含量显著增加。在不同烘烤条件下,乙二醛的含量相对较低(1.59~4.13 μg/g),而甲基乙二醛的含量则为9.42~33.92 μg/g。当烘烤温度为170 ℃时,随烘烤时间延长,甲基乙二醛含量的变化相较于乙二醛含量的变化更为显著。可能是烘烤初期甲基乙二醛的生成速率快,从而迅速积累,而乙二醛的生成需更多中间步骤,其含量的增加相对滞后。此外,烘烤10 min后,乙二醛和甲基乙二醛含量增加速率随温度的升高先降低后上升,这或许是高温使美拉德反应加速,醛糖逆缩醛反应加剧,促使两者生成加快[28]。
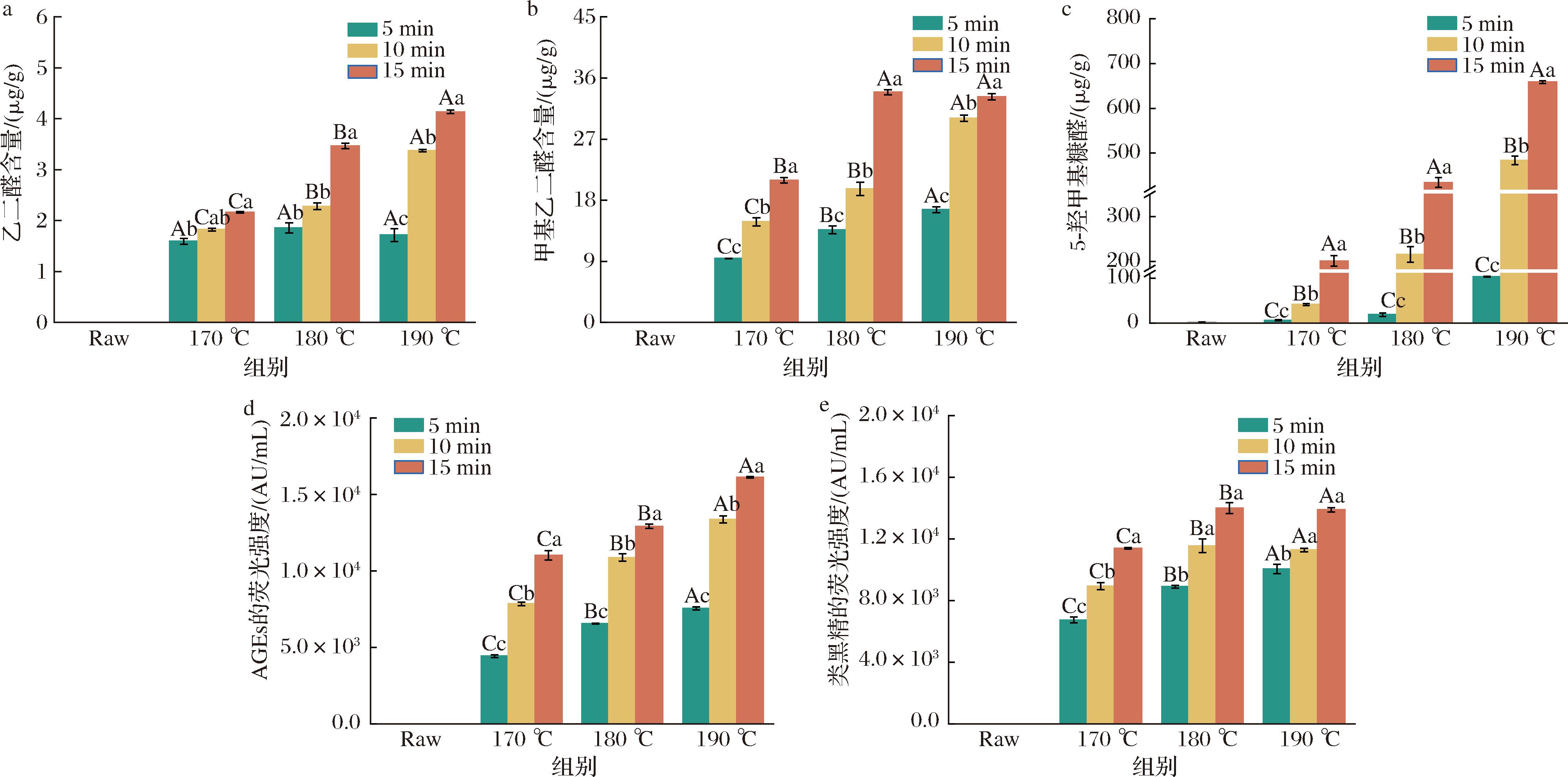
a-乙二醛含量;b-甲基乙二醛含量;c-5-羟甲基糠醛含量;d-AGEs荧光强度;e-类黑精荧光强度
图5 不同烘烤处理对青稞茶美拉德反应产物含量的影响
Fig.5 Effects of different roasting treatments on the contents of Maillard reaction products of highland barley tea
5-羟甲基糠醛是美拉德反应过程中的中间产物,而AGEs是该反应的最终产物。如图5-c所示,青稞茶中5-羟甲基糠醛含量呈阶梯式增长(P< 0.05)。170 ℃、15 min组的5-羟甲基糠醛含量为(201.43±11.93) μg/g,180 ℃、15 min组的5-羟甲基糠醛含量为(434.65±10.91) μg/g,190 ℃、15 min组的5-羟甲基糠醛含量为(658.35±3.19) μg/g。值得注意的是,未经处理的青稞茶中也检测到了5-羟甲基糠醛,其含量为2.44 μg/g。说明5-羟甲基糠醛含量的增加不仅是由热处理导致的,样品本身存在活性物质,在贮存过程中也会使5-羟甲基糠醛的含量略有增加。由图5-d可知,随着烘烤温度的升高以及烘烤时间的延长,青稞茶中AGEs的含量的变化趋势与乙二醛和甲基乙二醛变化趋势基本一致。
类黑精是由羰基与氨基经缩合聚合反应生成的深色大分子物质[29]。图5-e展示了经不同烘烤处理的青稞茶中类黑精的含量变化。随着烘烤温度的升高和时间的延长,类黑精含量的变化趋势与其他美拉德反应产物基本相似。但当烘烤时间控制在10 min和15 min时,与180 ℃处理组相比,190 ℃处理组的类黑精含量分别下降2.31%和0.83%,这可能是由于烘烤温度达180 ℃后焦糖化和碳化反应加剧,导致类黑精的降解。
2.4 不同烘烤处理对青稞茶感官风味的影响
2.4.1 不同烘烤处理对青稞茶挥发性成分的影响
图6呈现了不同烘烤处理下青稞茶的电子鼻雷达图。除对氮氧化物、醇醛酮类、长链烷烃敏感的传感器外,其他传感器变化微小,这显示电子鼻对青稞茶中香气成分感知有限。当烘烤5 min时,3个不同温度下青稞茶的无机硫化物香气物质差异极小,说明短时间烘烤时,提高温度不足以充分激发无机硫化物香气成分。此外,醇类、醛类和酮类物质随烘烤温度和时间增加呈先降后升趋势。总体来看,烘烤条件对青稞茶气味影响复杂,需精准调控。
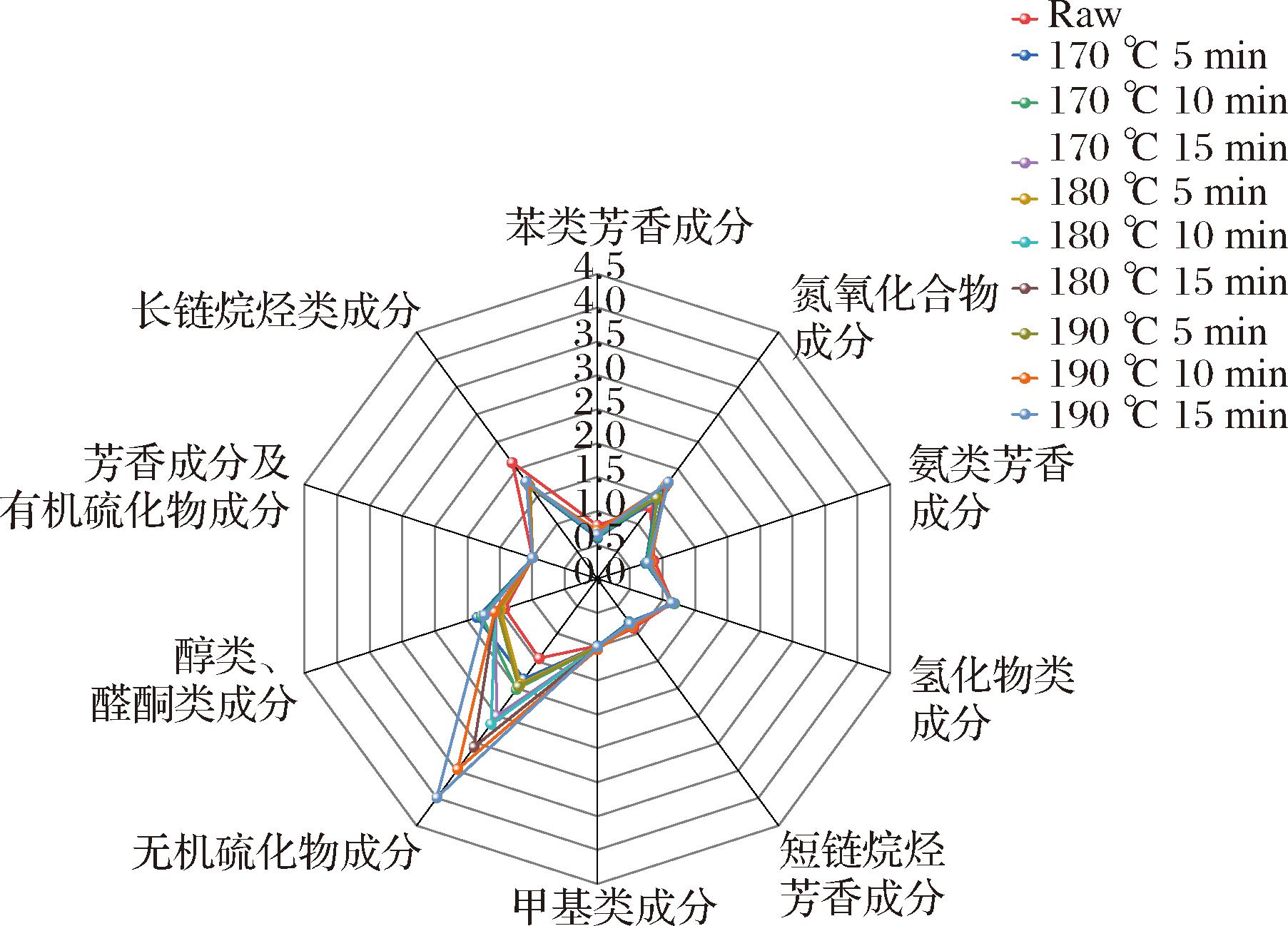
图6 不同烘烤处理对青稞茶气味的影响
Fig.6 Effects of different roasting treatments on the odor of highland barley tea
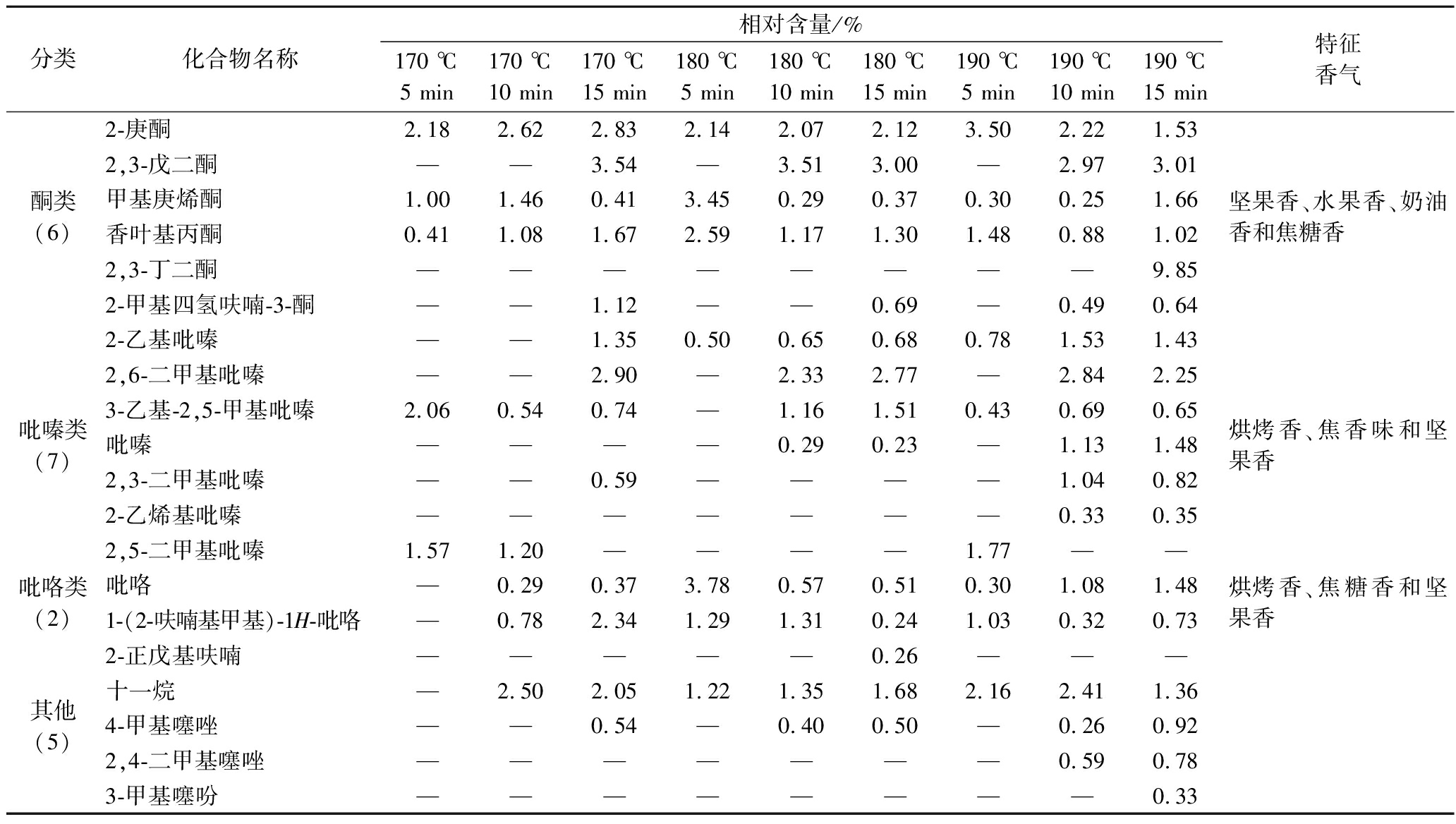
基于LVHP-GC-MS分析,青稞茶中共检测出40种特征性挥发性组分,涵盖七类化学物质:醇类(3种)、醛类(16种)、酮类(6种)、吡嗪类(7种)、吡咯类(2种)、有机酸(1种)及其他化合物(5种),与电子鼻分析结果相符。呋喃类化合物是青稞烘烤过程中产生焦糖香气的重要贡献物质,赋予青稞类似烤面包和烤饼干的香气。吡嗪类和吡咯类化合物是主要的含氮杂环化合物,其香气主要表现为坚果香、焦糖香以及宜人的花香[30]。由表4可知,异戊醛含量随温度升高而降低,这有可能是异戊醛在高温条件下容易发生氧化反应。此外,2, 6-二甲基吡嗪和吡嗪的香气特征被广泛描述为焦糊味,可能对人类的嗅觉体验产生负面影响。当温度较低且烘烤时间较短时青稞茶中不存在此类挥发性物质,因此,为保证青稞茶香气品质,需合理控制烘烤温度和时间。
表4 不同烘烤处理后青稞茶中主要香气物质的含量
Table 4 The content of the main aroma compounds in barley tea after different roasting treatments
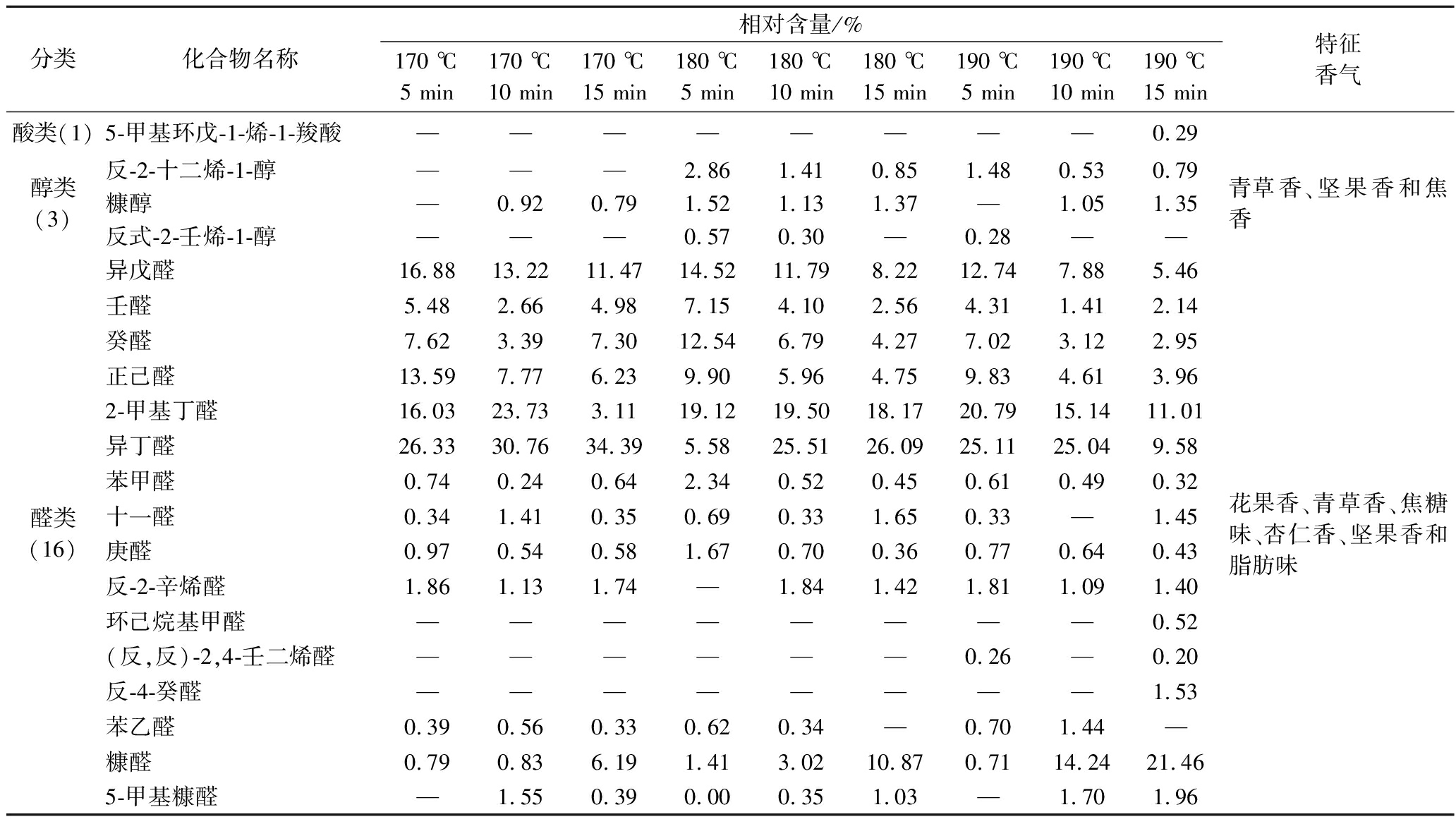
分类化合物名称相对含量/%170 ℃5 min170 ℃10 min170 ℃15 min180 ℃5 min180 ℃10 min180 ℃15 min190 ℃5 min190 ℃10 min190 ℃15 min特征香气酸类(1)5-甲基环戊-1-烯-1-羧酸————————0.29醇类(3)反-2-十二烯-1-醇———2.861.410.851.480.530.79糠醇—0.920.791.521.131.37—1.051.35反式-2-壬烯-1-醇———0.570.30—0.28——青草香、坚果香和焦香醛类(16)异戊醛16.8813.2211.4714.5211.798.2212.747.885.46壬醛5.482.664.987.154.102.564.311.412.14癸醛7.623.397.3012.546.794.277.023.122.95正己醛13.597.776.239.905.964.759.834.613.962-甲基丁醛16.0323.733.1119.1219.5018.1720.7915.1411.01异丁醛26.3330.7634.395.5825.5126.0925.1125.049.58苯甲醛0.740.240.642.340.520.450.610.490.32十一醛0.341.410.350.690.331.650.33—1.45庚醛0.970.540.581.670.700.360.770.640.43反-2-辛烯醛1.861.131.74—1.841.421.811.091.40环己烷基甲醛————————0.52(反,反)-2,4-壬二烯醛——————0.26—0.20反-4-癸醛————————1.53苯乙醛0.390.560.330.620.34—0.701.44—糠醛0.790.836.191.413.0210.870.7114.2421.465-甲基糠醛—1.550.390.000.351.03—1.701.96花果香、青草香、焦糖味、杏仁香、坚果香和脂肪味
续表4
分类化合物名称相对含量/%170 ℃5 min170 ℃10 min170 ℃15 min180 ℃5 min180 ℃10 min180 ℃15 min190 ℃5 min190 ℃10 min190 ℃15 min特征香气酮类(6)2-庚酮2.182.622.832.142.072.123.502.221.532,3-戊二酮——3.54—3.513.00—2.973.01甲基庚烯酮1.001.460.413.450.290.370.300.251.66香叶基丙酮0.411.081.672.591.171.301.480.881.022,3-丁二酮————————9.852-甲基四氢呋喃-3-酮——1.12——0.69—0.490.64坚果香、水果香、奶油香和焦糖香吡嗪类(7)2-乙基吡嗪——1.350.500.650.680.781.531.432,6-二甲基吡嗪——2.90—2.332.77—2.842.253-乙基-2,5-甲基吡嗪2.060.540.74—1.161.510.430.690.65吡嗪————0.290.23—1.131.482,3-二甲基吡嗪——0.59————1.040.822-乙烯基吡嗪———————0.330.352,5-二甲基吡嗪1.571.20————1.77——烘烤香、焦香味和坚果香吡咯类(2)吡咯—0.290.373.780.570.510.301.081.481-(2-呋喃基甲基)-1H-吡咯—0.782.341.291.310.241.030.320.73烘烤香、焦糖香和坚果香其他(5)2-正戊基呋喃—————0.26———十一烷—2.502.051.221.351.682.162.411.364-甲基噻唑——0.54—0.400.50—0.260.922,4-二甲基噻唑———————0.590.783-甲基噻吩————————0.33
注:—代表未检出。
2.4.2 不同烘烤处理对青稞茶的感官评价
对不同烘烤处理下青稞茶进行感官评价,总体评分如图7所示。当烘烤温度较低且时间短时,青稞茶的感官评价分数仅(66.93±0.44)分。这是由于烘烤程度过浅,致使青稞茶带有生面粉味,影响口感与整体评价。当温度升高至180 ℃烘烤15 min时,青稞茶的感官评分达到最高,为(75.21±0.44)分。然而,结合前文提及的美拉德反应产物含量,从食品安全角度出发,此工艺虽并非最佳烘烤工艺。当烘烤温度为170 ℃,烘烤时间为15 min时,青稞茶感官评分为(72.68±0.34)分,在香气、滋味和色泽等方面都得到了较好的评价。综合感官评价和食品安全等多方面因素,确定170 ℃、15 min为最佳烘烤条件。
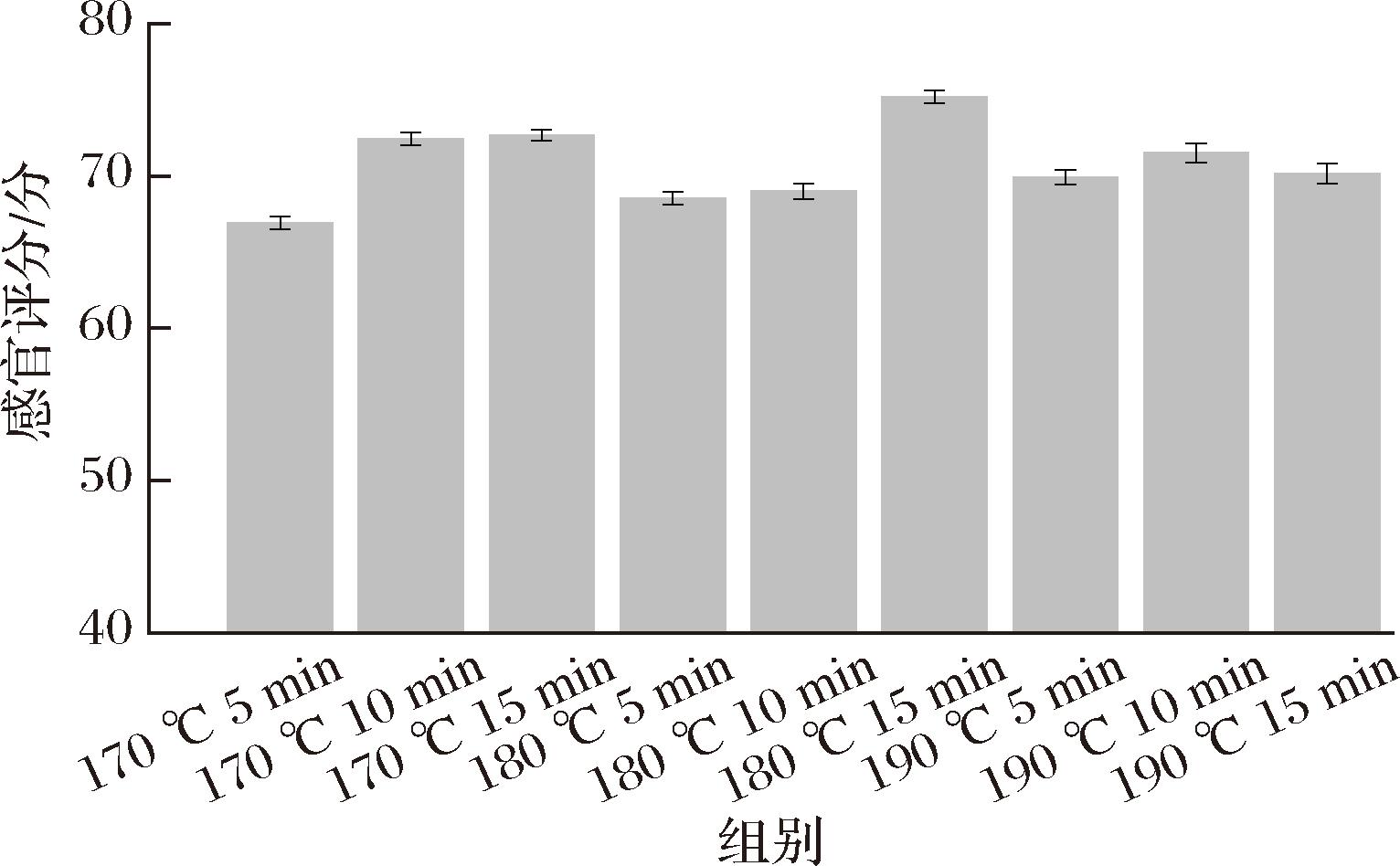
图7 不同烘烤处理青稞茶的感官评价
Fig.7 Sensory evaluation of highland barley tea with different roasting treatments
3 结论
本文以青稞为原料,系统研究了不同烘烤处理(170~190 ℃,5~15 min)对青稞茶理化特性、美拉德副产物生成及感官风味的影响。结果显示,170 ℃、10 min为青稞茶制备的最优烘烤工艺。在此条件下,青稞茶呈现出良好的品质特征,总酚保留率高达94.8%,总黄酮含量提升至1.64 mg CE/g,DPPH自由基清除能力与铁离子还原抗氧化能力分别达到(3.5±0.04) mmol TE/g和(4.19±0.24) mmol AAE/g。美拉德反应副产物相对较低,得到有效控制,降低了潜在的健康风险。感官评价综合得分达72.45±2.44(n=7)。微观结构分析进一步揭示了该条件下青稞细胞壁适度破裂,淀粉颗粒部分糊化,既促进了活性成分的溶出,又未引发纤维过度碳化,为功能成分释放与风味形成创造了有利条件。本研究初步阐明了不同烘烤工艺下青稞茶品质特性的差异,揭示了青稞茶在最优工艺下具有良好的理化特性、较低的健康风险和良好的感官风味,研究结果为青稞的综合利用与青稞茶的开发提供了理论依据。
[1] 邓婧, 马小涵, 赵天天, 等.青稞β-葡聚糖对淀粉体外消化性的影响[J].食品科学, 2018, 39(10):106-111.DENG J, MA X H, ZHAO T T, et al.Effect of highland barley β-glucan on starch digestibility in vitro[J].Food Science, 2018, 39(10):106-111.
[2] 范雨婷, 王可心, 张海霞, 等.发芽青稞营养成分及功能特性研究进展[J].食品工业科技, 2025, 46(2):403-411.FAN Y T, WANG K X, ZHANG H X, et al.Research progress on nutritional components and functional characteristics of sprouted highland barley[J].Science and Technology of Food Industry, 2025, 46(2):403-411.
[3] MITCHELL C A, VEROVSKAYA E V, CALERO-NIETO F J, et al.Stromal niche inflammation mediated by IL-1 signalling is a targetable driver of haematopoietic ageing[J].Nature Cell Biology, 2023, 25(1):30-41.
[4] SHARMA P, KOTARI S L.Barley:Impact of processing on physicochemical and thermal properties:A review[J].Food Reviews International, 2017, 33(4):359-381.
[5] 王犇. 不同热处理对青稞酚类物质和风味物质的影响规律及机理探究[D].无锡:江南大学, 2023.WANG B, Effects and mechanism of different thermal processing on phenolics and flavor substances of highland barley[D].Wuxi:Jiangnan University, 2023.
[6] WANG C, TIAN X Y, FANG S J, et al.Brewing characteristics, physicochemical constituents, and antioxidant activity of the infusions of colored highland barley roasted at different times[J].Journal of Cereal Science, 2023, 110:103639.
[7] KARANAM M, THEERTHA D P, KUMAR A, et al.Effect of hydrothermal treatment on physical and Semolina milling properties of barley[J].Journal of Food Engineering, 2020, 287:110142.
[8] SCHLÖRMANN W, ZETZMANN S, WIEGE B, et al.Impact of different roasting conditions on chemical composition, sensory quality and physicochemical properties of waxy-barley products[J].Food &Function, 2019, 10(9):5436-5445.
[9] TANG Y, ZHANG B, LI X H, et al.Bound phenolics of quinoa seeds released by acid, alkaline, and enzymatic treatments and their antioxidant and α-glucosidase and pancreatic lipase inhibitory effects[J].Journal of Agricultural and Food Chemistry, 2016, 64(8):1712-1719.
[10] ZHANG L H, ZHANG M, ADHIKARI B, et al.Salt reducing and saltiness perception enhancing strategy for shiitake (Lentinus edodes) bud using novel combined treatment of yeast extract and radio frequency[J].Food Chemistry, 2023, 402:134149.
[11] TANG Y, LI X H, ZHANG B, et al.Characterisation of phenolics, betanins and antioxidant activities in seeds of three Chenopodium quinoa Willd genotypes[J].Food Chemistry, 2015, 166:380-388.
[12] QIN R K, WU R L, SHI H N, et al.Formation of AGEs in fish cakes during air frying and other traditional heating methods[J].Food Chemistry, 2022, 391:133213.
[13] ZHAO F F, LI Y, LI C M, et al.Insight into the regulations of rice protein on the gluten-free bread matrix properties[J].Food Hydrocolloids, 2022, 131:107796.
[14] QIN W Y, PI J X, ZHANG G Y.The interaction between tea polyphenols and wheat gluten in dough formation and bread making[J].Food &Function, 2022, 13(24):12827-12835.
[15] PATRIGNANI M, BRANTSEN J F, AWIKA J M, et al.Application of a novel microwave energy treatment on brewers spent grain (BSG):Effect on its functionality and chemical characteristics[J].Food Chemistry, 2021, 346:128935.
[16] TANG Y, HUANG Y, LI M R, et al.Balancing Maillard reaction products formation and antioxidant activities for improved sensory quality and health benefit properties of pan baked buns[J].Food Research International, 2024, 195:114984.
[17] WANG Z F, DE JAGER L S, BEGLEY T, et al.Large volume headspace GC/MS analysis for the identification of volatile compounds relating to seafood decomposition[J].Food Science &Nutrition, 2022, 10(4):1195-1210.
[18] 张健明. 青稞银耳红曲发酵工艺、产品开发及其多糖免疫活性初步研究[D].成都:西华大学, 2016.ZHANG J M.Study on solid-state fermentation technology and products development and immunomodulatory activities of polysaccharides of highland barley and tremella monascus[D].Chengdu:Xihua University, 2016.
[19] SCHOEMAN L, MANLEY M.Oven and forced convection continuous tumble (FCCT) roasting:Effect on physicochemical, structural and functional properties of wheat grain[J].Food and Bioprocess Technology, 2019, 12(1):166-182.
[20] BAI Y P, ZHOU H M, ZHU K R, et al.Effect of thermal treatment on the physicochemical, ultrastructural and nutritional characteristics of whole grain highland barley[J].Food Chemistry, 2021, 346:128657.
[21] HUANG X T, FENG T T, CUI H P, et al.Analysis of the browning reaction in a sorbitol/glycine model:Formation and degradation of precursors, glucose and α-dicarbonyl compounds during heating[J].Food Research International, 2024, 177:113870.
[22] WANG B, NIE C, LI T T, et al.Effect of boiling and roasting on phenolic components and their bioaccessibilities of highland barley[J].Food Research International, 2022, 162:112137.
[23] ABDEL-AAL E M, RABALSKI I.Effect of baking on free and bound phenolic acids in wholegrain bakery products[J].Journal of Cereal Science, 2013, 57(3):312-318.
[24] GHAFOOR K, ALJUHAIMI F, ÖZCAN M M, et al.Effects of roasting on bioactive compounds, fatty acid, and mineral composition of chia seed and oil[J].Journal of Food Processing and Preservation, 2018, 42(10):jfpp.13710.
[25] BABIKER E E, USLU N, AL JUHAIMI F, et al.Effect of roasting on antioxidative properties, polyphenol profile and fatty acids composition of hemp (Cannabis sativa L.) seeds[J].LWT, 2021, 139:110537.
[26] YU M Y, GOUVINHAS I, ROCHA J, et al.Phytochemical and antioxidant analysis of medicinal and food plants towards bioactive food and pharmaceutical resources[J].Scientific Reports, 2021, 11:10041.
[27] SIAH S, KONCZAK I, WOOD J A, et al.Effects of roasting on phenolic composition and in vitro antioxidant capacity of Australian grown faba beans (Vicia faba L)[J].Plant Foods for Human Nutrition, 2014, 69(1):85-91.
[28] LIU J Y, GAN J, YU Y J, et al.Effect of laboratory-scale decoction on the antioxidative activity of Zhenjiang Aromatic Vinegar:The contribution of melanoidins[J].Journal of Functional Foods, 2016, 21:75-86.
[29] DHUA S, KHETO A, SINGH SHARANAGAT V, et al.Quality characteristics of sand, pan and microwave roasted pigmented wheat (Triticum aestivum)[J].Food Chemistry, 2021, 365:130372.
[30] WANG F, MA Y H, XIONG H Y, et al.The nonvolatile and volatile substances changes based on non-target metabonomics reveals the formation mechanism of Tsamba flavor before and after roasting of highland barley[J].Food Chemistry, 2025, 28:102524.