蚕蛹是蚕蛾科昆虫家蚕的蛹虫形态,在丝绸产业中作为一种主要副产物被获取。它也被称为小蜂、蝶元或蚕女[1]。在中国,蚕蛹因其营养价值高而被广泛作为食用昆虫。它是蛋白质、脂肪、矿物质和维生素的优质来源[2]。据研究报道,蚕蛹含有30%的脂肪与50%的蛋白质,是一种珍贵的动物蛋白资源[3]。同时,蚕蛹中的活性成分还具有多种药理作用,其蛋白质及水解肽能增强免疫力,并具有抗肿瘤和抗氧化功效[4]。因此,蚕蛹是一种富含多种有益人体营养素的健康食品,被认为兼具养生与滋补功效[5]。作为缫丝的粗加工产品,蚕蛹在加工过程中面临高温高湿环境,这为黄曲霉等产毒霉菌的生长创造了条件,其安全性受黄曲霉毒素(aflatoxin, AFT)污染的威胁[6]。
AFT是一类具有二氢呋喃香豆素结构的化合物,主要源于黄曲霉和寄生曲霉的次级代谢过程[7]。该类物质具有致癌、致畸及致突变作用,对人类构成严重威胁[8]。迄今为止,全球已鉴定出20余种不同类型的AFT,但从食品安全角度来看,以AFTB1、AFTB2、AFTG1和AFTG2最为常见[9]。AFTB1作为Ⅰ类致癌物,其在所有AFT中表现出最强的毒性[10]。为控制AFT污染,我国强制性标准GB 2761—2017《食品安全国家标准 食品中真菌毒素限量》限定了部分食品中AFTB1的含量,其最大允许值为0.5~20 μg/kg。
当前针对食品中AFT的定量分析工作,主要依赖于高效液相色谱技术[11](high performance liquid chromatography, HPLC)以及高效液质联用技术[12](high performance liquid chromatography-tandem mass spectrometry, HPLC-MS/MS)。由于此类毒素在食品中残留水平低且基质干扰严重,分析前通常必须借助样品前处理技术来完成净化和富集。为此,当前发展了多种前处理方法,如液液萃取[13-14]、固相萃取[15-16]、免疫亲和固相萃取[17]、免疫负载磁珠净化[18-19]以及QuEChERS技术[20-21]等。针对蚕蛹粉这类复杂基质,目前主要采用免疫亲和层析法进行处理[6],但该方法操作步骤较为繁琐且检测成本较高,难以满足高通量检测的需求。
超分子溶剂(supramolecular solvent, SUPRAS)是近年来发展的一种新型萃取技术,利用具有亲水基和疏水基的两亲性化合物[如长链烷基醇/烷基酸、四氢呋喃(tetrahydrofuran, THF)和水]作为萃取剂,在氢键、范德华力、疏水作用等分子间的非共价相互作用自组装形成纳米或者微米级胶束聚集体的溶剂体系来实现对污染物的提取,具有环境友好、原料廉价、制备简单、提取效率高等优点,克服了传统有机溶剂毒性强、环境不友好等缺点[22-23]。目前SUPRAS提取技术在真菌毒素应用方面应用较少,还仅限于小麦中AFTB1测定[24],针对蚕蛹粉中真菌毒素的检测应用还鲜见报道。由于小麦的主要成分为淀粉、蛋白质、脂肪等,其中与AFT极性相近且对检测干扰较大的蛋白质含量与脂肪仅占比约10%和1%[25],而蚕蛹中蛋白质含量与脂肪含量占比约55%和32%[1],基质更为复杂,干扰更大,因此制备去除蛋白质与脂肪干扰的SUPRAS萃取体系成为本研究的重要难点和挑战。盐析液液萃取法是向样品与萃取溶剂的混合液中引入无机盐,利用盐析效应驱动萃取相从混合物中分离[26]。这一方法在应用中表现出显著优势:过程简便快速、所需溶剂量少,且能实现高效的萃取。本实验以自主设计的SUPRAS为萃取剂,结合盐析辅助SUPRAS萃取作为前处理方式,构建了一种前处理快速、成本低廉的蚕蛹粉AFT检测体系,旨在为其高通量筛查提供可靠的技术支持。
1 材料与方法
1.1 材料与试剂
蚕蛹粉样品购于当地超市及网络平台销售。4种AFT标准物质(质量浓度均为100 μg/mL),青岛普瑞邦生物工程有限公司;0.22 μm 尼龙滤头,浙江月旭材料科技有限公司;乙酸铵(≥97%)、氯化铵(≥99.5%)、硫酸铵(≥99%)、亚硫酸铵一水合物(92%)、乙腈(色谱纯)、甲醇(色谱纯)、THF(色谱纯)、正戊醇(≥99%)、正己醇(≥99%)、正庚醇(≥99.5%)、正辛醇(≥99%)、正壬醇(≥98%)、正癸醇(≥98%)、正十一醇(97%)、正十二醇(≥98%)、正戊酸(≥99%)、正己酸(≥99%)、正庚酸(≥99%)、正辛酸(≥99%),德国Merck公司;实验用水为纯水仪自制的超纯水。
1.2 仪器与设备
ZORBAX RRHD Eclipse Plus C18色谱柱(100 mm×2.1 mm, 1.8 μm)、1260改型耐高压高效液相色谱仪、6470三重四极杆质谱仪,美国Agilent公司;XPR205DUE电子分析天平(精度0.000 1 g),瑞士Mettler Toledo仪器有限公司;Genius 3漩涡混合器,德国IKA公司;Sorvall St16高速离心机,美国Thermo公司;Simplicity超纯水仪,美国Millipore公司;DM2500光学显微镜,德国Leica公司。
1.3 实验方法
1.3.1 溶液制备
1.3.1.1 混合对照品溶液的制备
准确吸取100 μL AFT混合溶液标准物质于10 mL容量瓶,加入乙腈定容,配制成混合标准储备液(1.00 μg/mL),置于-20 ℃冰箱中低温保存。用空白基质溶液稀释储备液配制标准曲线工作溶液,使其质量浓度分别为0.1、0.5、1.0、5.0、10.0 ng/mL。
1.3.1.2 SUPRAS的制备
准确量取5.0 mL正庚醇和25.0 mL THF,迅速转移至50 mL离心管中,加入10.0 mL超纯水,涡旋5 min,以10 000 r/min离心10 min,移取上层有机相置于4 ℃下密封保存备用,同时收集下层饱和SUPRAS的水层用于蚕蛹粉中AFT的提取。
1.3.1.3 样品溶液的制备
称取0.50 g蚕蛹粉(精确至0.01 g),先后加入1.0 mL饱和SUPRAS的水溶液、1.2 mL SUPRAS和0.5 g硫酸铵,2 000 r/min涡旋5 min,10 000 r/min离心5 min,收集0.6 mL上清液并用甲醇水(体积比为1∶1)溶液定容至1 mL,过膜进样。
1.3.2 标准曲线的绘制
采用外标法绘制标准曲线:将5个浓度水平的4种AFT标准曲线工作液依次进样5 μL至超高效液相色谱-质谱(ultra-high performance liquid chromatography tandem mass spectrometry,UPLC-MS/MS)系统进行分析,系统自动计算出线性方程与相关系数。
1.3.3 色谱及质谱条件
色谱条件:流动相A:体积比1∶1的甲醇/乙腈混合液,流动相B:5 mmol/L乙酸铵溶液;以0.3 mL/min进行洗脱程序:0.0~1.0 min,30%~65% A;1.0~3.0 min,65% A;3.0~4.0 min,65%~95% A;4.0~5.0 min,95% A;5.0~5.6 min,95%~30% A;5.6~8.0 min,30% A;进样体积5 μL;柱温35 ℃。
质谱条件:毛细管正电压为3.5 kV;干燥气温度300 ℃;干燥气流速7 L/min;雾化器压力45 psi;鞘气温度:350 ℃;鞘气流速11 L/min;电离方式为电喷雾正离子电离(electron spray ionization, ESI+),采集模式为多反应监测;有关质谱参数详见表1。
表1 待测物的监测离子对及最佳质谱参数
Table 1 Selected transitions and optimized potentials of the target compounds
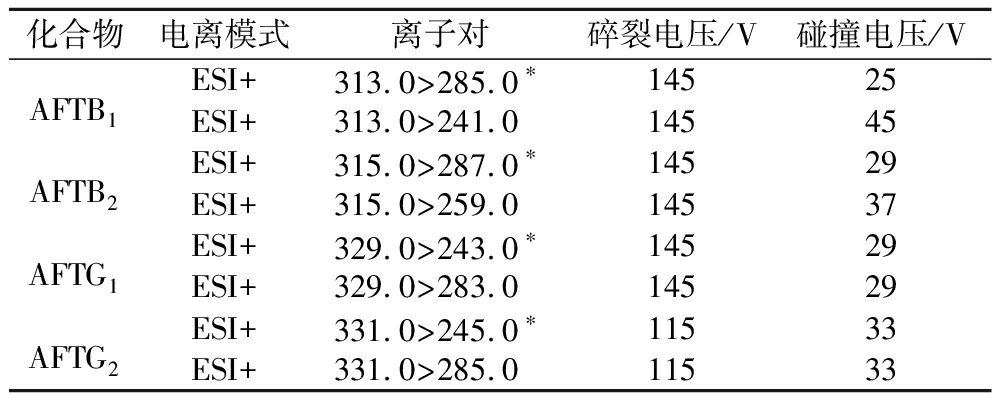
化合物电离模式离子对碎裂电压/V碰撞电压/VAFTB1ESI+313.0>285.0∗14525ESI+313.0>241.014545AFTB2ESI+315.0>287.0∗14529ESI+315.0>259.014537AFTG1ESI+329.0>243.0∗14529ESI+329.0>283.014529AFTG2ESI+331.0>245.0∗11533ESI+331.0>285.011533
*:定量离子对。
1.3.4 数据处理
目标物含量计算如公式(1)所示:
(1)
式中:Xi,测试样品中目标物含量,μg/kg;Ci,提取液中目标物的含量,ng/mL;V,提取液定容体积,mL;m,测试样品质量,g; f,稀释倍数。
1.3.5 基质效应
本研究通过相对响应值法评估基质效应,其计算基于空白溶液标准曲线斜率与基质标准曲线斜率的比值。基质效应(ME)的计算如公式(2)所示:
(2)
式中:k1和k2分别代表空白溶液与基质匹配标准曲线的斜率。
1.4 数据统计与分析
实验数据的处理与图表绘制在Origin 9.0软件中完成。统计分析采用SPSS 26.0软件进行,运用单因素方差分析比较组间差异,设定显著性水平α=0.05,当P<0.05时,则认为差异具有统计学意义。
2 结果与分析
2.1 SUPRAS的制备及萃取因子优化
2.1.1 烷基醇/酸的筛选
SUPRAS由于两亲性化合物的种类和含量不同,其结构和极性具备可调性,因此可以根据相似相溶原理,构建目标物质相似极性的SUPRAS来提高提取效率。因此,本研究考察了不同长链醇/酸所形成SUPRAS对AFT的提取能力。本实验选取12种常见长链醇/酸:正戊醇、正己醇、正庚醇、正辛醇、正壬醇、正癸醇、正十一醇、正十二醇、正戊酸、正己酸、正庚酸、正辛酸进行对比实验,结果见图1。结果显示,烷基醇的平均回收率高于烷基酸,这可能是因为AFT极性较弱,长链醇的极性更加与AFT相近,烷基酸极性过大影响了SUPRAS的萃取效率[27]。烷基链碳原子数在7(庚醇)时SUPRAS的萃取效率最高,且4种AFT均具有显著差异(P<0.05),其原因可能是庚醇组成的超分子在黏度及其与目标分析物之间的疏水相互作用达到了平衡[27],因此,本研究选取庚醇制备SUPRAS开展随后的实验研究。
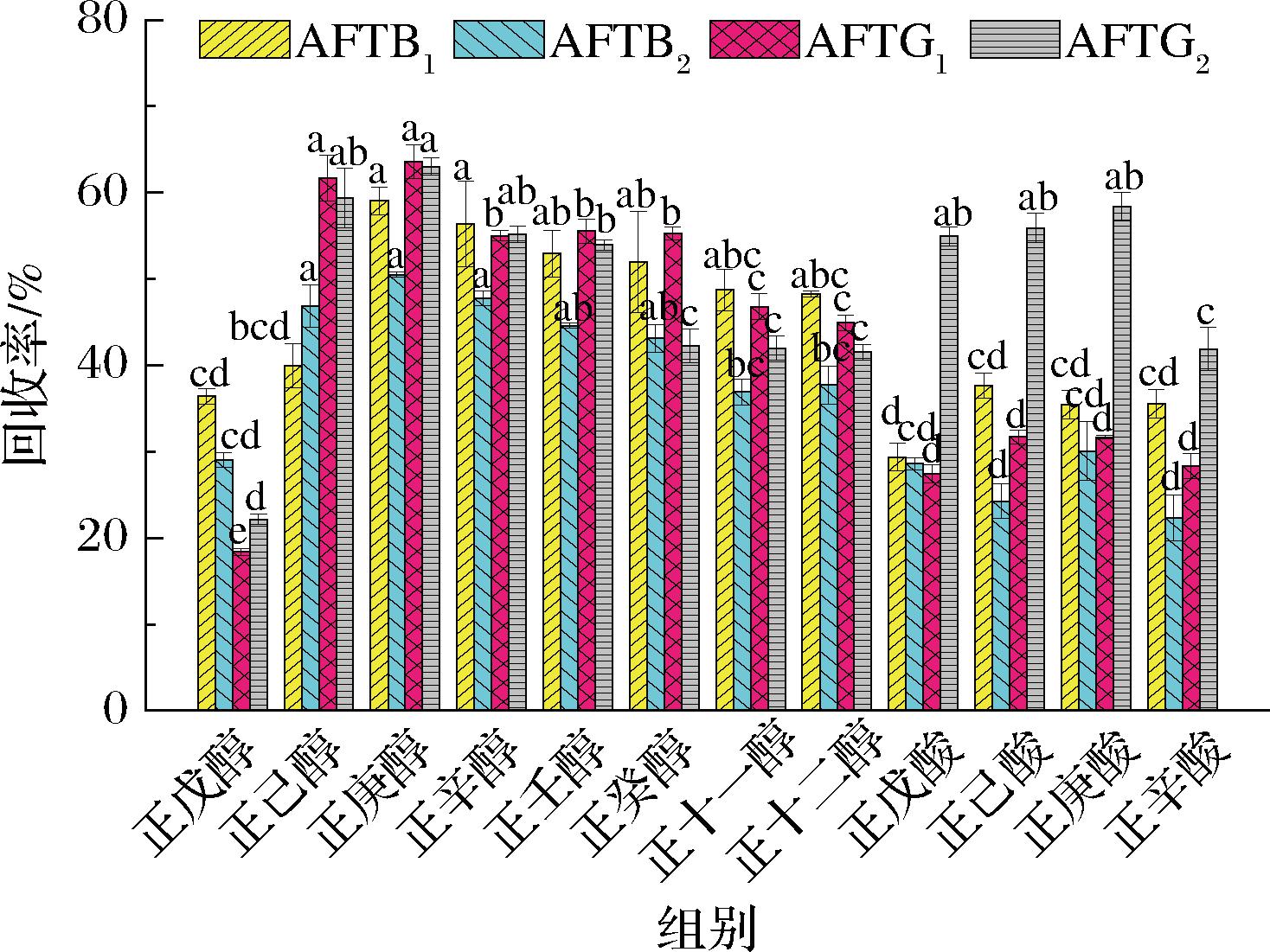
图1 烷基醇/酸类型筛选(n=3)
Fig.1 Screening of the optimal alkyl alcohol/acid type (n=3)
注:不同小写字母表示存在显著性差异(P<0.05)(下同)。
2.1.2 SUPRAS比例组成的筛选
SUPRAS一般由3种溶剂组成,在特定范围内形成SUPRAS,因此本研究绘制了庚醇、THF、水制备SUPRAS的相图。如图2所示,当THF的体积分数低于63.52%时可以构建超分子体系,本研究选取8个相位点比例的SUPRAS,用于筛选提取效率最高的体积比组成。结果见图3,实验结果显示THF的比例越高,4种AFT的回收率越高,其中对于AFTB1具有显著差异(P<0.05)。其原因可能在于高THF含量制备的SUPRAS其囊泡结构孔径更大,萃取效率更强[28],同时THF的低黏度属性也增强了传质效率[29]。因此,选取体积比为1∶5∶2用于后续实验。图4显示了采用放大倍数为400倍光学显微镜下SUPRAS的形貌,形貌与文献报道相近THF比例的光学图相似[27],可以看到大量囊泡聚集体结构。
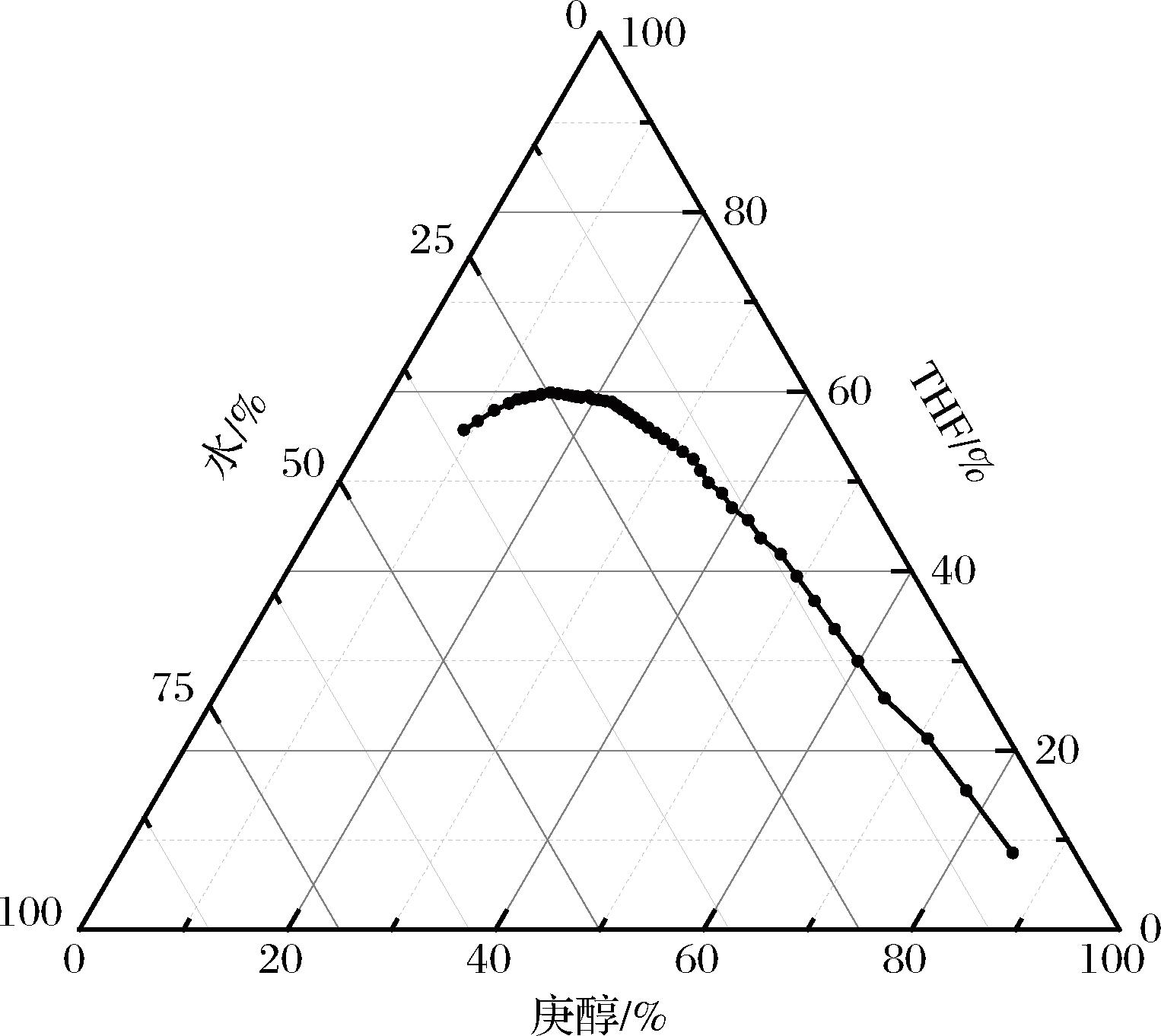
图2 庚醇/THF/水的相图
Fig.2 Phase diagram of heptanol/THF/water
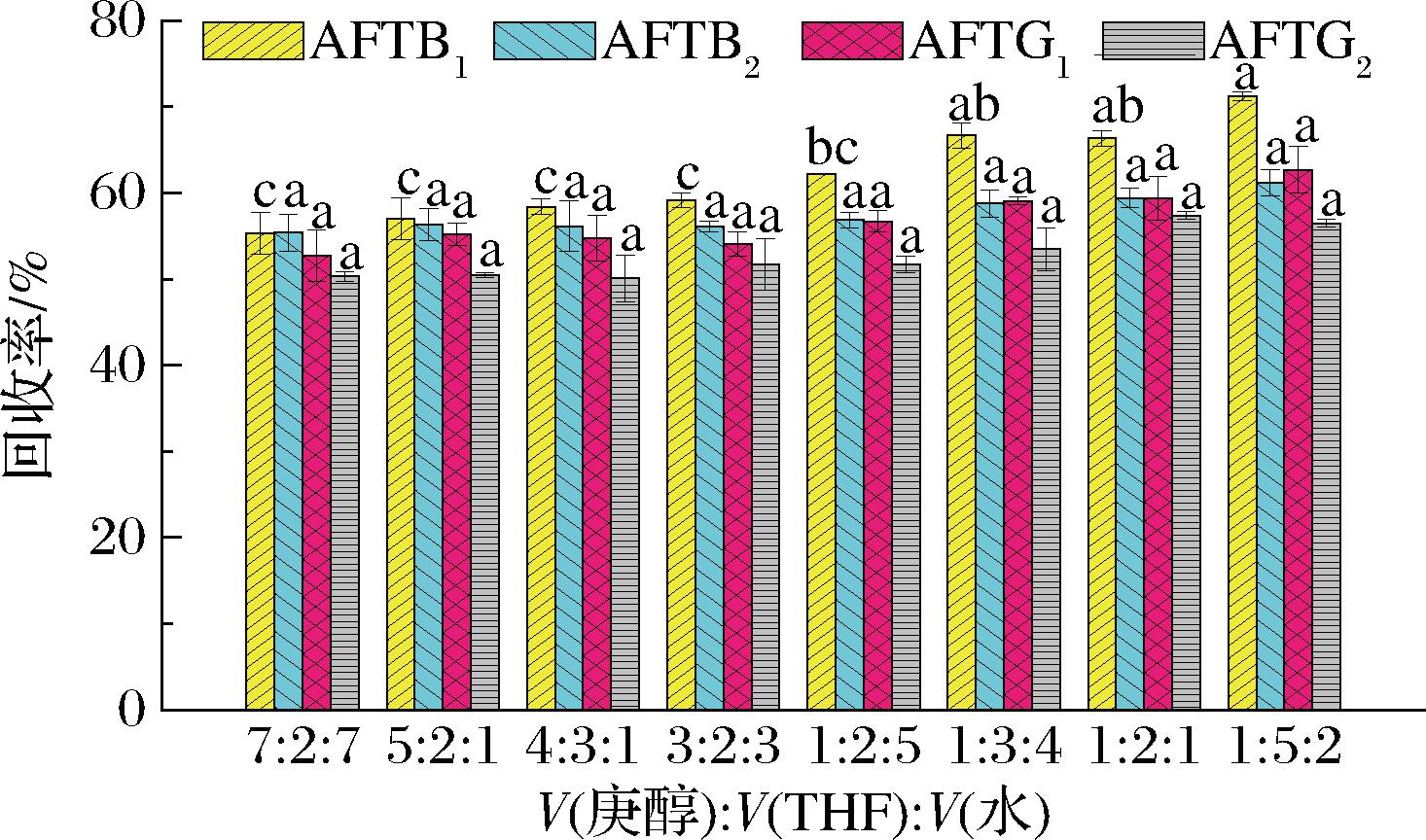
图3 庚醇/THF/水体积比的筛选
Fig.3 Screening of the optimal volume ratio of heptanol/THF/water
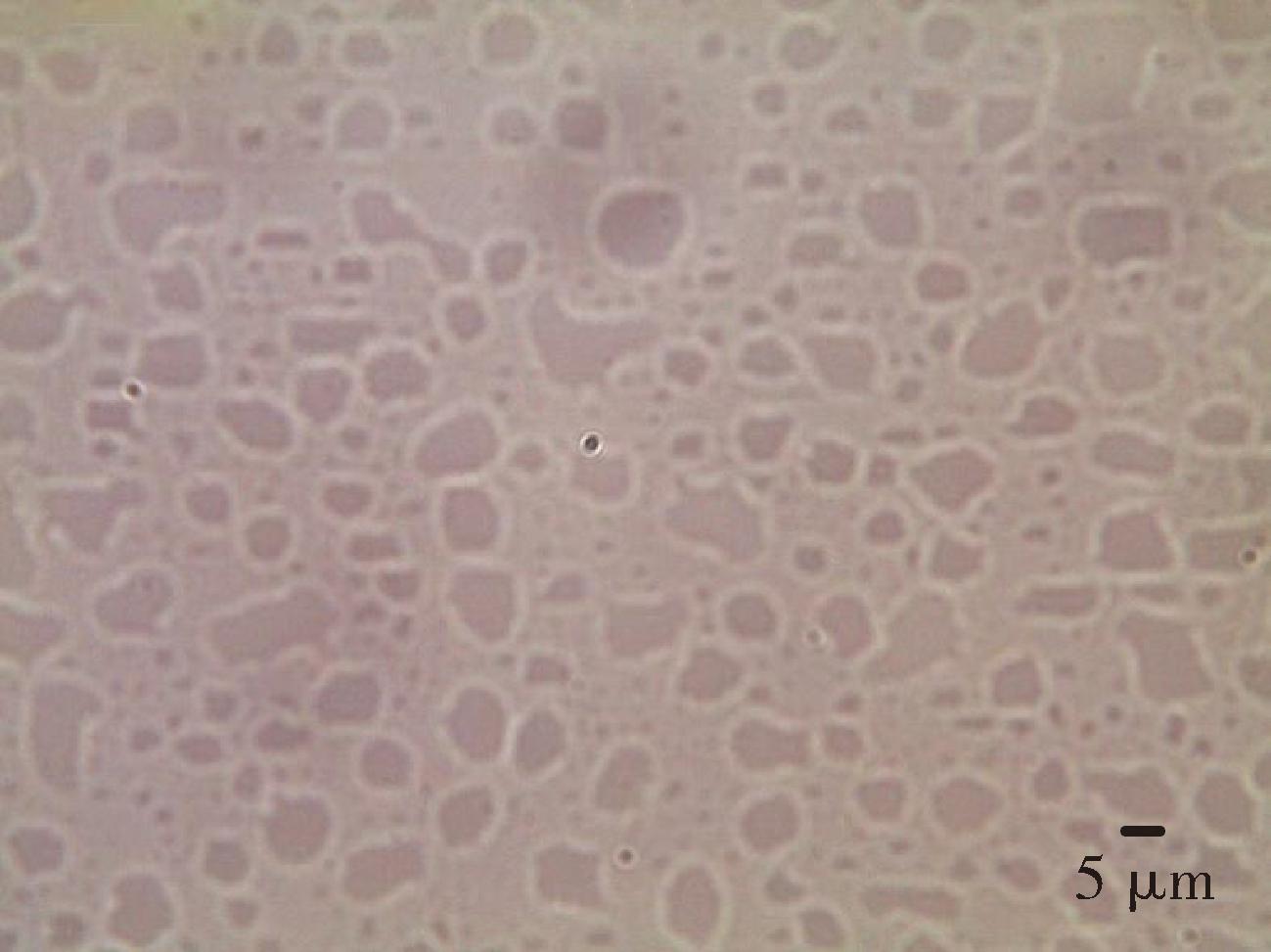
图4 SUPRAS的光学显微图像
Fig.4 Light microscope image of SUPRAS
2.1.3 盐析剂的类型筛选
在盐析液液萃取中,盐析剂的引入可以提高目标物萃取效率。但大量盐析剂的使用会造成萃取溶剂中盐析剂残留,降低目标物在质谱中的离子丰度,同时腐蚀和污染质谱硬件。为避免该缺陷,本研究为提高SUPRAS萃取效率,分别考察了4种对质谱相对友好的铵盐的提取效率,结果见图5。结果显示,硫酸铵与其他盐类对比具有显著差异(P<0.05),同时对比不加盐在AFTB2、AFTG1、AFTG2提取效率上也具有显著差异(P<0.05)。这可能是由于硫酸铵有更好的水溶解性和更强的盐析能力。因此,选取硫酸铵作为盐析助剂用于后续研究。
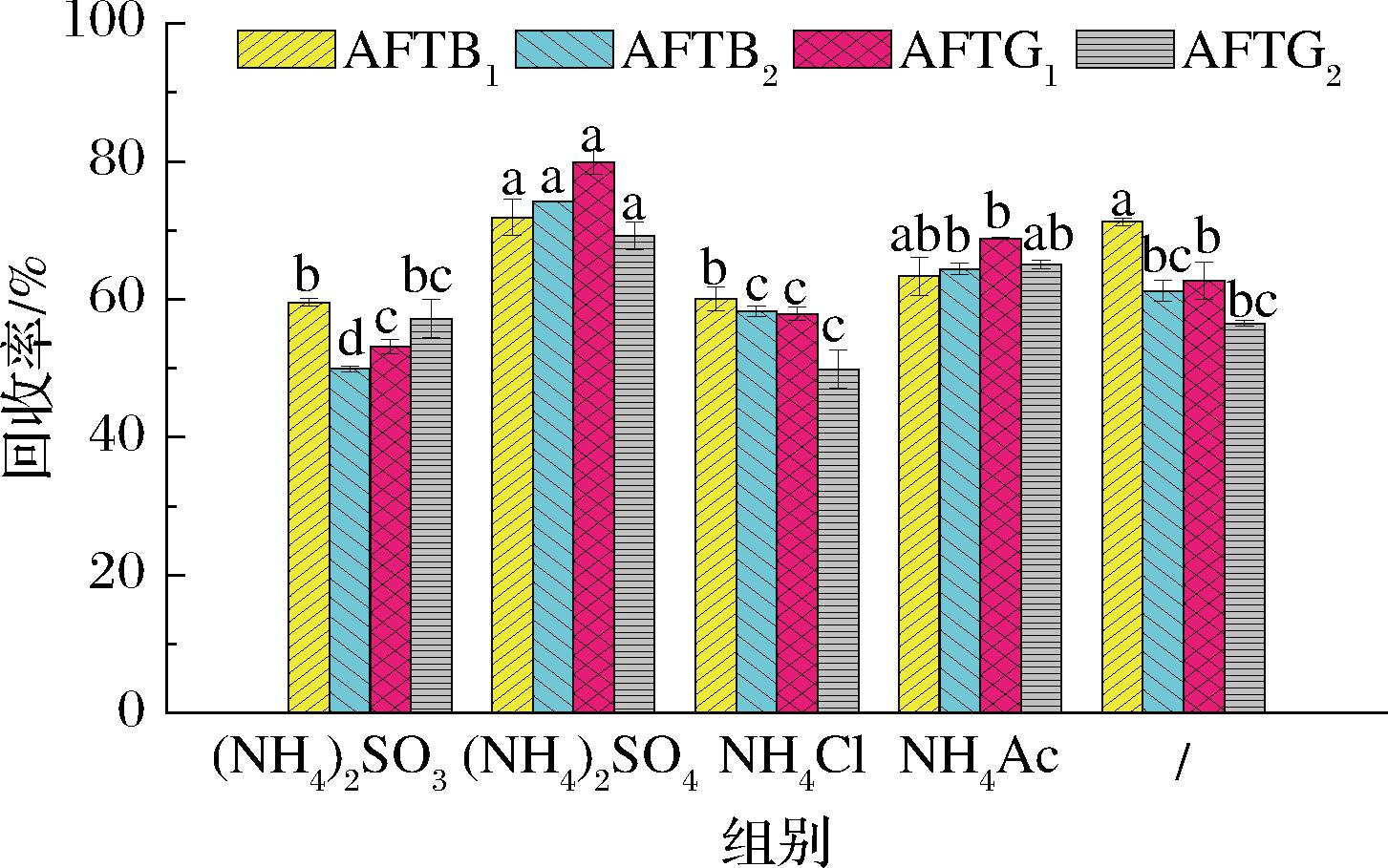
图5 盐种类筛选(n=3)
Fig.5 Screening of salt type (n=3)
注:“/”表示不加盐。
2.1.4 SUPRAS用量筛选
由于盐析剂的引入可以提高萃取效率,减少SUPRAS的使用量,但过低的SUPRAS体积会降低萃取效率。本研究筛选了SUPRAS的用量(0.4~1.6 mL)对目标物萃取效率的影响,结果见图6。SUPRAS体积用量为0.4 mL时,由于蚕蛹粉集中在两相交界处,易干扰上方SUPRAS溶剂的吸取,盐析后可吸取的SUPRAS较少,误差大,故舍去该用量数据,SUPRAS体积从0.8 mL增加至1.2 mL时,4种黄曲霉素毒素的回收率均有显著提升(P<0.05),继续增加体积萃取效率不再增加。故选取1.2 mL为最佳用量。
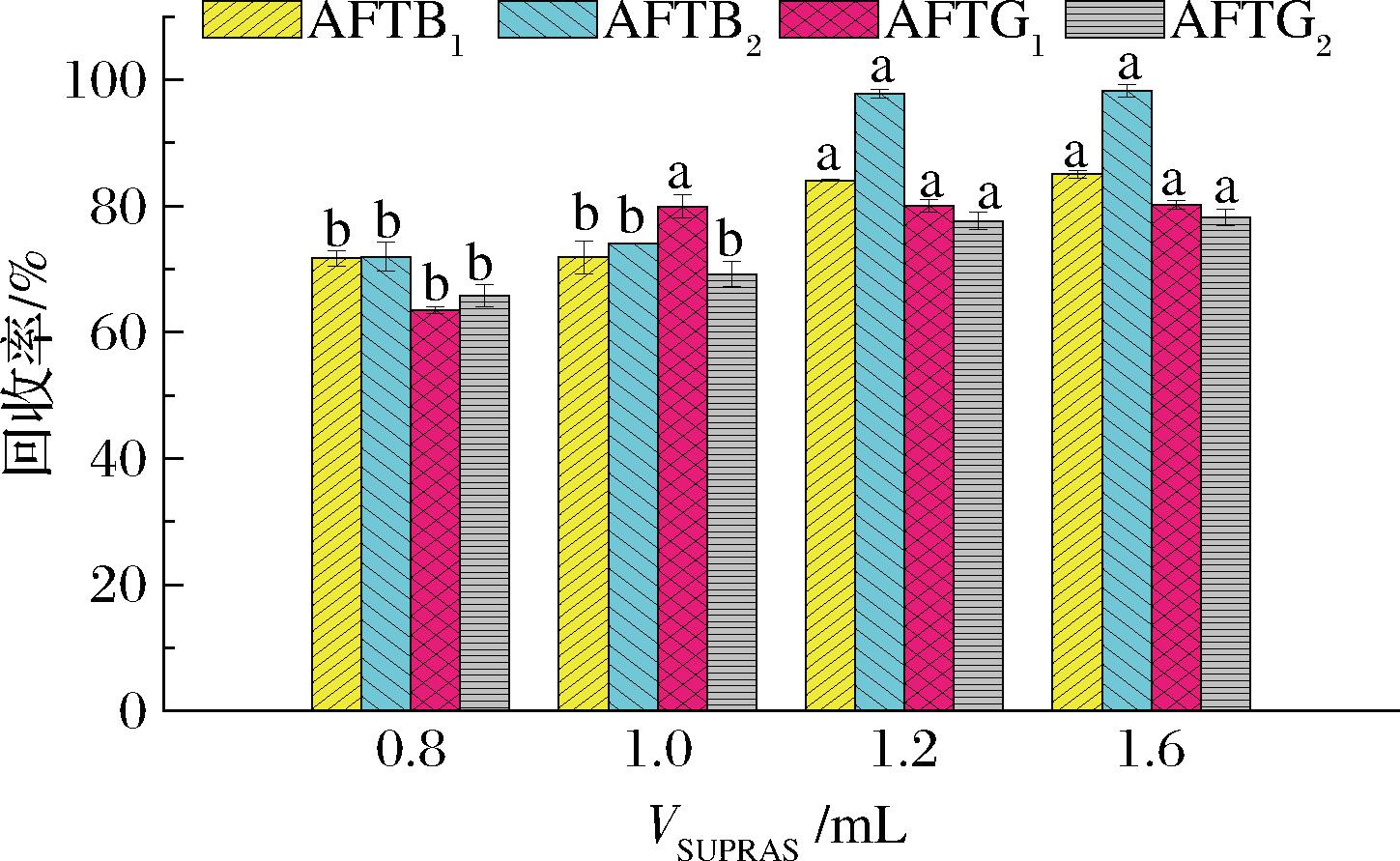
图6 SUPRAS体积筛选(n=3)
Fig.6 Screening of SUPRAS volume condition (n=3)
2.1.5 盐析剂的用量筛选
盐析剂的用量需要平衡盐析效果和干扰目标物电离程度。本研究考察了硫酸铵的用量(0.3、0.4、0.5、0.6、0.7 g)对4种AFT回收率的影响,结果见图7。研究表明:硫酸铵用量在考察范围内均完全溶解,且萃取溶剂澄清,吸取方便。AFT萃取效率随硫酸铵用量提高而提高明显(P<0.05),但当用量大于0.5 g,萃取效率反而有所下降。同时本研究考察了不同质量盐析剂(0.3、0.4、0.5、0.6、0.7 g)对质谱的抑制程度,以不加盐的基质空白溶液加标准物质测得的峰面积为基准响应,通过对比不同质量盐析剂得到的基质空白溶液加入相同浓度标准物质得到的响应,得到了不同质量盐析剂下目标物的响应率,结果见图8。结果发现不同质量硫酸铵对目标物的响应率为84.1%~104.2%,其中0.5 g较其他质量对目标物的响应率最高(95.5%~104.2%),但与其他质量条件下差异并不显著(P>0.05),表明本实验条件下不同硫酸铵用量对质谱的干扰并不严重,但0.5 g用量下质谱干扰最轻。因此,选取0.5 g为硫酸铵用量。
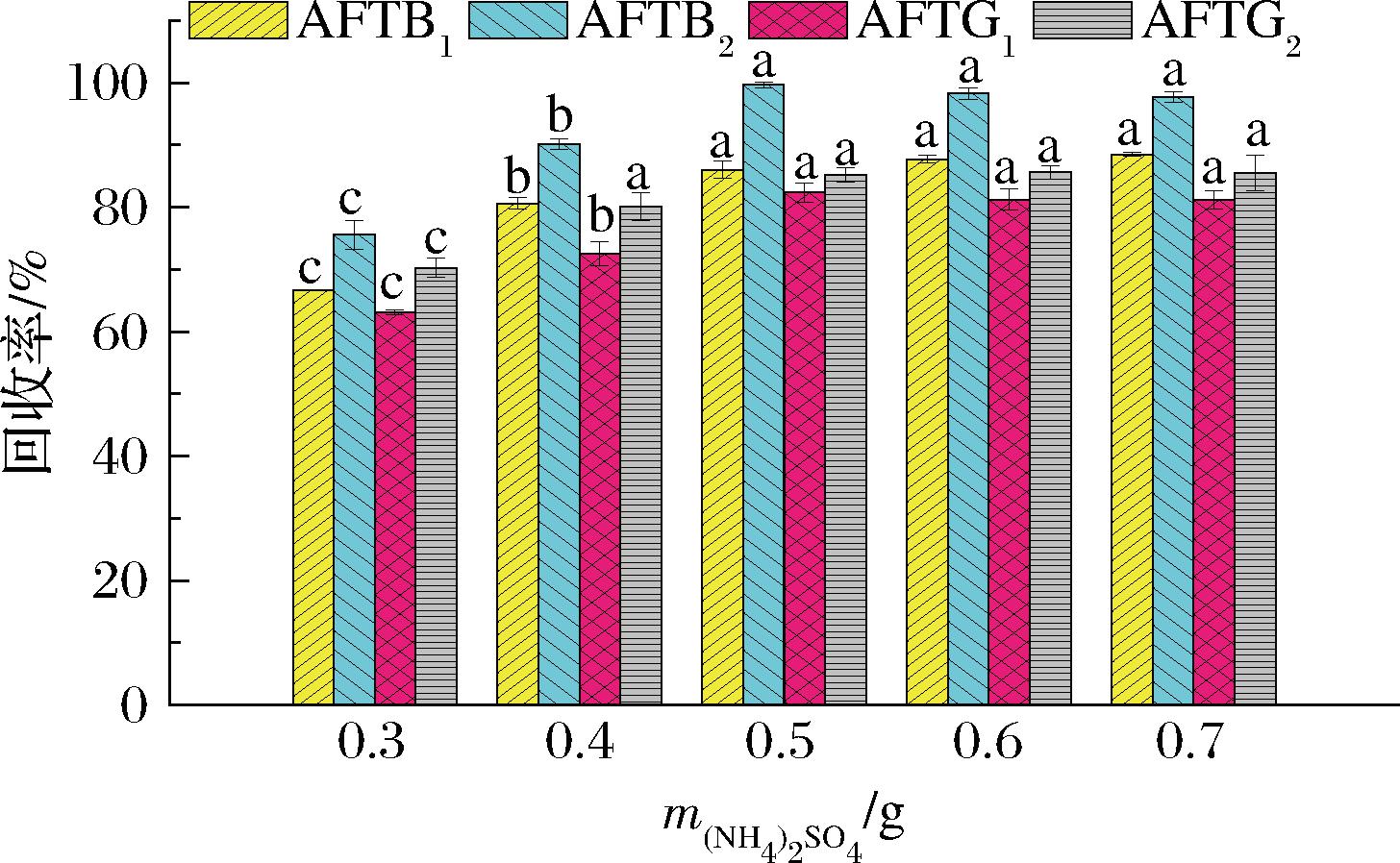
图7 硫酸铵质量筛选(n=3)
Fig.7 Quality screening of ammonium sulfate (n=3)
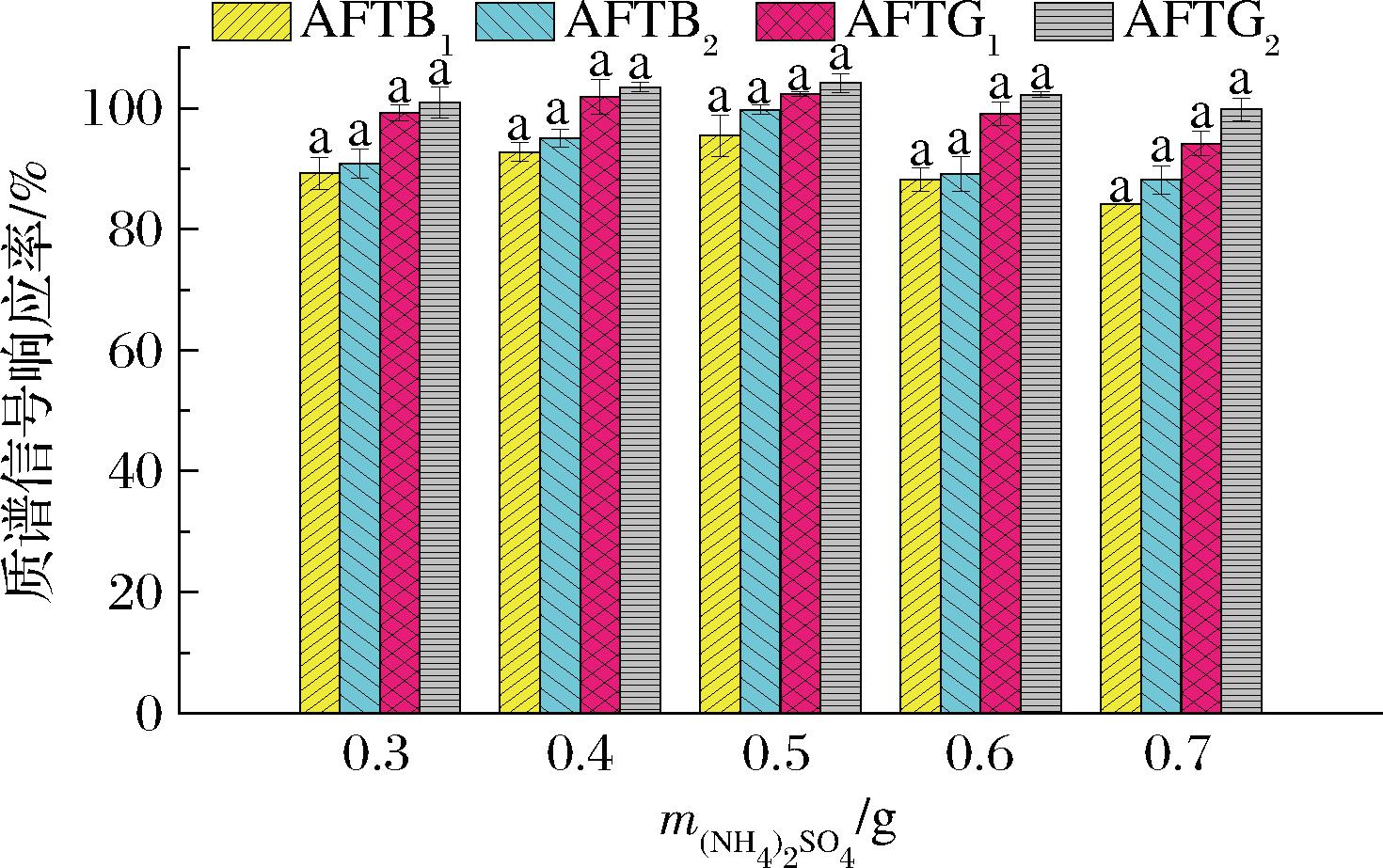
图8 硫酸铵质量对目标物质谱响应率比较
Fig.8 Comparison of the responsivity of the target substance with different amounts of ammonium sulfate
2.2 标准曲线、线性范围与检出限
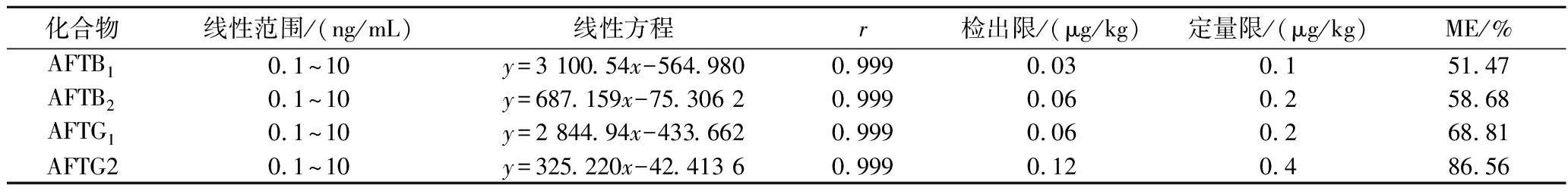
鉴于蚕蛹粉表现出较强的基质效应,本研究采用基质匹配标准曲线进行定量分析。经相对响应值法评估,4种AFT的基质效应为51.47%~86.56%,其中AFTB1、AFTB2和AFTG1均呈现显著的基质抑制效应。随后,将系列浓度的基质匹配标准工作液进样分析,在0.1~10 ng/mL范围内,4种AFTs均呈现良好线性,相关系数(r)均大于0.999(表2)。图9展示了质量浓度为5.0 ng/mL的混合标准溶液色谱图。基于信噪比S/N=3和S/N=10,分别计算得到方法的检出限与定量限,其范围分别为0.03~0.12 μg/kg和0.1~0.4 μg/kg,具体结果汇总于表2。
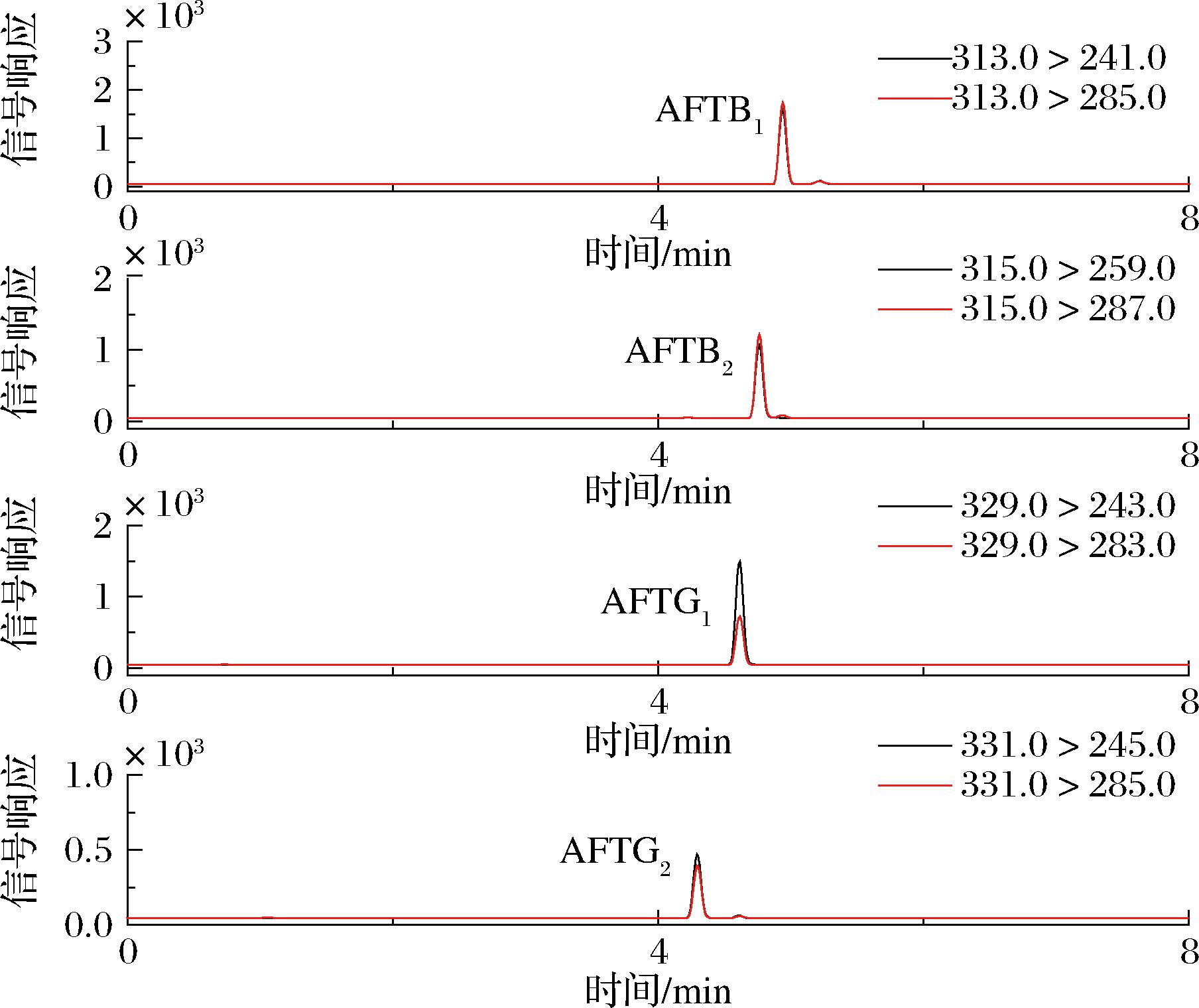
图9 AFT混合标准工作溶液的色谱图(5.0 ng/mL)
Fig.9 Chromatograms for mixed standard solution of AFTs (5.0 ng/mL)
表2 四种AFT的回归方程、线性范围、检出限与定量限
Table 2 Regression equations, linear ranges, limits of detection, and limits of quantitation of the four aflatoxins in silkworm pupae powder
化合物线性范围/(ng/mL)线性方程r检出限/(μg/kg)定量限/(μg/kg)ME/%AFTB10.1~10y=3 100.54x-564.9800.9990.030.151.47AFTB20.1~10y=687.159x-75.306 20.9990.060.258.68AFTG10.1~10y=2 844.94x-433.6620.9990.060.268.81AFTG20.1~10y=325.220x-42.413 60.9990.120.486.56
2.3 回收率与精密度实验
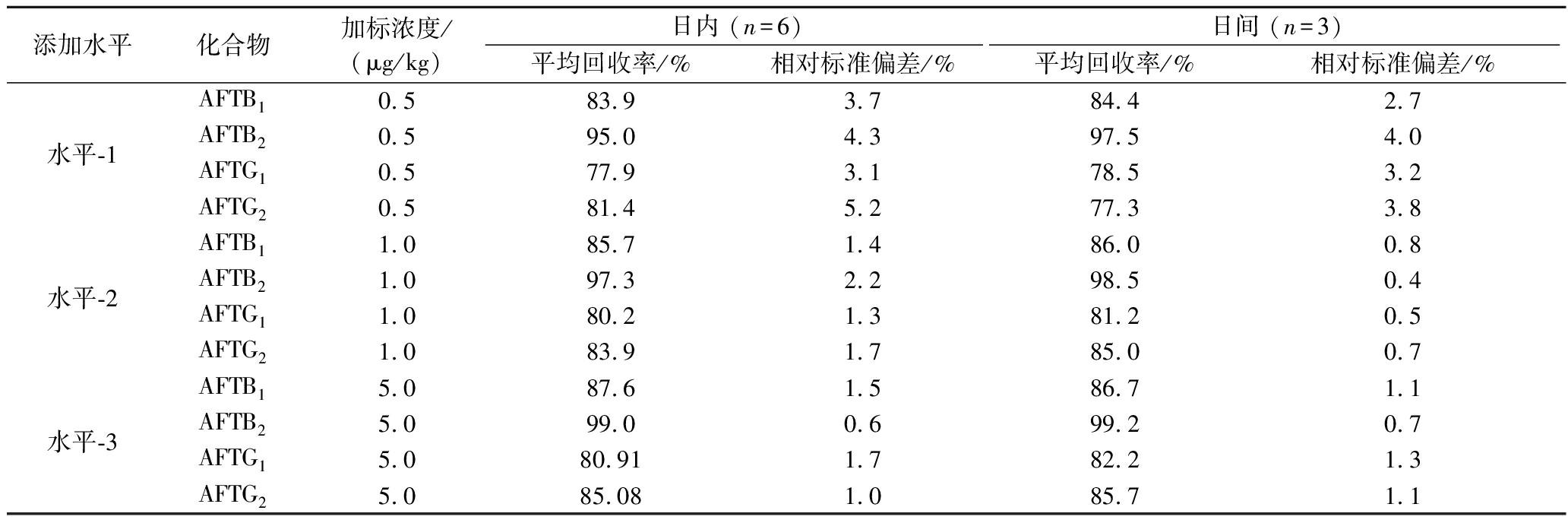
取0.5 g空白蚕蛹粉做加标回收实验,4种黄曲霉素毒素3个水平的加标浓度分别为0.5、1.0、5.0 μg/kg,平行6次实验,考察3个水平的回收率和日内精密度(n=6),并连续3 d平行实验,考察了日间精密度(n=3)。结果见表3,4种黄曲霉素毒素的平均回收率为77.3%~99.2%,日内相对标准偏差为0.6%~5.2%,日间相对标准偏差为0.4%~4.0%。
表3 蚕蛹粉中4种AFT的加标回收率和精密度(n=6 or 3)
Table 3 Recoveries and precisions of the four aflatoxins in silkworm pupae powder (n=6 or 3)
添加水平化合物加标浓度/(μg/kg)日内 (n=6)日间 (n=3)平均回收率/%相对标准偏差/%平均回收率/%相对标准偏差/%水平-1AFTB10.583.93.784.42.7AFTB20.595.04.397.54.0AFTG10.577.93.178.53.2AFTG20.581.45.277.33.8水平-2AFTB11.085.71.486.00.8AFTB21.097.32.298.50.4AFTG11.080.21.381.20.5AFTG21.083.91.785.00.7水平-3AFTB15.087.61.586.71.1AFTB25.099.00.699.20.7AFTG15.080.911.782.21.3AFTG25.085.081.085.71.1
2.4 与文献方法的比较
表4为本研究与文献方法的比较,由结果可见,较之文献或者国标方法,本研究取样量少,方便快捷,同时也大量节省有机溶剂使用量,非常适合大批次高通量的检测分析。
表4 本方法与其他测定蚕蛹粉中AFT方法的比较
Table 4 Assessment of this approach against other AFTs detection methods in silkworm pupae powder
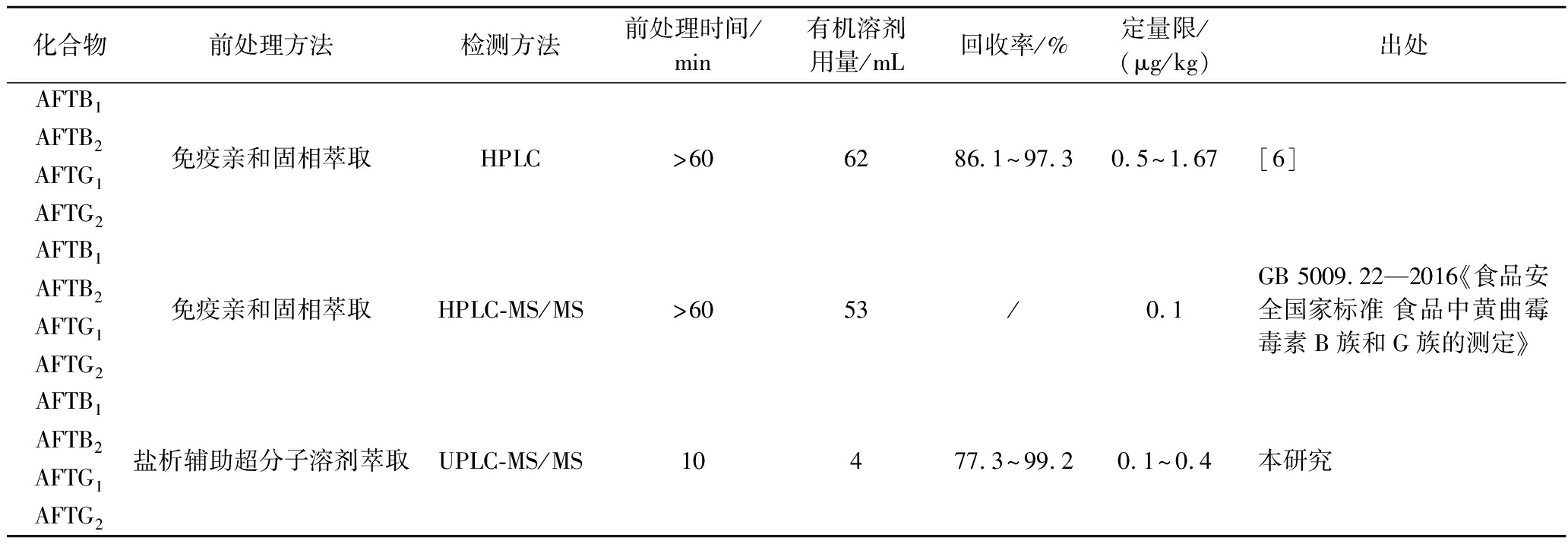
化合物前处理方法检测方法前处理时间/min有机溶剂用量/mL回收率/%定量限/(μg/kg)出处AFTB1AFTB2AFTG1AFTG2免疫亲和固相萃取HPLC>606286.1~97.30.5~1.67[6]AFTB1AFTB2AFTG1AFTG2免疫亲和固相萃取HPLC-MS/MS>6053/0.1GB 5009.22—2016《食品安全国家标准 食品中黄曲霉毒素B族和G族的测定》AFTB1AFTB2AFTG1AFTG2盐析辅助超分子溶剂萃取UPLC-MS/MS10477.3~99.20.1~0.4本研究
注:“/”表示无数据。
2.5 实际样品检测
购买随机抽取的市售蚕蛹粉样品10份,采用本研究建立的实验方法进行4种AFT检测,结果有1批次蚕蛹粉中检出AFTB1,检出率为10%,含量为11.08 μg/kg。由于蚕蛹粉中真菌毒素尚无国家标准,参照我国强制性标准GB 2761—2017《食品安全国家标准 食品中真菌毒素限量》规定,蚕蛹粉中的AFT污染需要引起重视。
3 结论与讨论
本研究开发了一种基于SUPRAS体系的新型盐析辅助液液萃取方法,结合UPLC-MS/MS技术用于了蚕蛹粉中AFT的快速检测,该方法首次将SUPRAS萃取和盐析液液结合应用,充分发挥了SUPRAS 极性可调节和盐析液液萃取高萃取效率的双重优势,同现有方法相比,本方法的检测灵敏度与现有技术相当,同时大幅缩减了有机溶剂消耗,并降低了成本、简化了操作流程,因而在蚕蛹粉的AFT大规模筛查中展现出极高的实际应用价值。
[1] 周亚西, 王点点, 段昊, 等.蚕蛹的功能活性及其在保健食品中的应用进展[J].食品安全质量检测学报, 2023, 14(15):241-251.ZHOU Y X, WANG D D, DUAN H, et al.Functional activity of silkworm pupae and its application progress in health food in China[J].Journal of Food Safety &Quality, 2023, 14(15):241-251.
[2] WU X L, HE K, VELICKOVIC T C, et al.Nutritional, functional, and allergenic properties of silkworm pupae[J].Food Science &Nutrition, 2021, 9(8):4655-4665.
[3] MENTANG F, MAITA M, USHIO H, et al.Efficacy of silkworm (Bombyx mori L.) chrysalis oil as a lipid source in adult Wistar rats[J].Food Chemistry, 2011, 127(3):899-904.
[4] GE S M, TONG X Y, GAO C F, et al.Kinetics of silkworm pupae protein extraction at different ultrasonic frequency and temperature:Effects on physicochemical properties, functional properties and oxidation resistance[J].Process Biochemistry, 2022, 122:36-52.
[5] CAI M, ZHANG Q, GUO P, et al.Comprehensive quality control of silkworm chrysalis using chemical fingerprints combined with antioxidant activity and acetylcholine content[J].Journal of Chromatography A, 2024, 1730:465168.
[6] 王东旭, 陈晓平.高效液相色谱法测定蚕蛹粉中的黄曲霉毒素含量[J].蚕业科学, 2020, 46(1):124-128.WANG D X, CHEN X P.Determination of aflatoxin content in silkworm Pupa powder by high-performance liquid chromatography[J].Acta Sericologica Sinica, 2020, 46(1):124-128.
[7] LOI M, LOGRIECO A F, PUSZTAHELYI T, et al.Advanced mycotoxin control and decontamination techniques in view of an increased aflatoxin risk in Europe due to climate change[J].Frontiers in Microbiology, 2023, 13:1085891.
[8] KUMAR P, MAHATO D K, KAMLE M, et al.Aflatoxins:A global concern for food safety, human health and their management[J].Frontiers in Microbiology, 2017, 7:2170.
[9] JALLOW A, XIE H L, TANG X Q, et al.Worldwide aflatoxin contamination of agricultural products and foods:From occurrence to control[J].Comprehensive Reviews in Food Science and Food Safety, 2021, 20(3):2332-2381.
[10] International Agency for Research on Cancer.Monographs on the Evaluation of Carcinogenic Risks to Humans[M].Lyon:IARC Press, 1993.
[11] 王蓓蓓, 陈琛, 李崇勇, 等.食品中黄曲霉毒素的前处理与检测方法进展[J].粮食与油脂, 2021, 34(11):1-5.WANG B B, CHEN C, LI C Y, et al.Advances in pretreatment and detection methods of aflatoxin in food[J].Cereals &Oils, 2021, 34(11):1-5.
[12] 张萍, 彭西甜, 冯钰锜.食品中黄曲霉毒素检测的样品前处理技术研究进展[J].分析科学学报, 2018, 34(2):274-280.ZHANG P, PENG X T, FENG Y Q.Research advances of sample preparation methods for detection of aflatoxin in food[J].Journal of Analytical Science, 2018, 34(2):274-280.
[13] DU B B, WANG P L, XIAO C, et al.Antibody-free colorimetric determination of total aflatoxins by mercury(II)-mediated aggregation of lysine-functionalized gold nanoparticles[J].Microchimica Acta, 2016, 183(4):1493-1500.
[14] 王东旭, 王新财, 王凤丽, 等.挥发性铵盐盐析辅助液液萃取结合超高效液相色谱-串联质谱法测定酱油中4种黄曲霉毒素[J].食品安全质量检测学报, 2022, 13(14):4634-4640.WANG D X, WANG X C, WANG F L, et al.Determination of 4 kinds of aflatoxins in soy sauce by volatile salting-out assisted liquid-liquid extraction combined with ultra performance liquid chromatography-tandem mass spectrometry[J].Journal of Food Safety & Quality, 2022, 13(14):4634-4640.
[15] 李丽, 吴宇, 王海波, 等.全自动免疫亲和固相萃取超高效液相色谱法测定粮油中黄曲霉毒素[J].中国粮油学报, 2020, 35(7):157-164.LI L, WU Y, WANG H B, et al.High throughput method for analysis of aflatoxins in cereals and oils using automated immunoaffinity cleaning up and ultra-high performance liquid chromatography[J].Journal of the Chinese Cereals and Oils Association, 2020, 35(7):157-164.
[16] 郝铖, 王思齐, 李腾飞, 等.分子印迹技术在黄曲霉毒素检测中的最新研究进展[J].分析试验室, 2022, 41(3):350-356.HAO C, WANG S Q, LI T F, et al.Recent research advances in aflatoxin detection by molecular imprinting technique[J].Chinese Journal of Analysis Laboratory, 2022, 41(3):350-356.
[17] MASSAROLO K C, MENDOZA J R, VERMA T, et al.Fate of aflatoxins in cornmeal during single-screw extrusion:A bioaccessibility approach[J].LWT, 2021, 138:110734.
[18] GUO L, SHAO Y N, DUAN H, et al.Magnetic quantum dot nanobead-based fluorescent immunochromatographic assay for the highly sensitive detection of aflatoxin B1 in dark soy sauce[J].Analytical Chemistry, 2019, 91(7):4727-4734.
[19] LIU Y, LI W, DING Z, et al.Three-dimensional ordered macroporous magnetic photonic crystal microspheres for enrichment and detection of mycotoxins (II):The application in liquid chromatography with fluorescence detector for mycotoxins[J].Journal of Chromatography A, 2019, 1604:460475.
[20] DONG X Q, ZOU B, ZHAO X Y, et al.Rapid qualitative and quantitative analysis of aflatoxin B1 in Pu-erh tea by liquid chromatography-isotope dilution tandem mass spectrometry coupled with the QuEChERS purification method[J].Analytical Methods, 2018, 10(39):4776-4783.
[21] HIDALGO-RUIZ J L, ROMERO-GONZ LEZ R, MART
LEZ R, MART NEZ VIDAL J L, et al.A rapid method for the determination of mycotoxins in edible vegetable oils by ultra-high performance liquid chromatography-tandem mass spectrometry[J].Food Chemistry, 2019, 288:22-28.
NEZ VIDAL J L, et al.A rapid method for the determination of mycotoxins in edible vegetable oils by ultra-high performance liquid chromatography-tandem mass spectrometry[J].Food Chemistry, 2019, 288:22-28.
[22] BALLESTEROS-G MEZ A, RUBIO S, PÉREZ-BENDITO D.Potential of supramolecular solvents for the extraction of contaminants in liquid foods[J].Journal of Chromatography A, 2009, 1216(3):530-539.
MEZ A, RUBIO S, PÉREZ-BENDITO D.Potential of supramolecular solvents for the extraction of contaminants in liquid foods[J].Journal of Chromatography A, 2009, 1216(3):530-539.
[23] 覃国顺, 吴丹, 龙欣琦, 等.超分子溶剂-微萃取技术在食品及环境污染物检测中的应用进展[J].食品安全质量检测学报, 2025, 16(14):128-138.QIN G S, WU D, LONG X Q, et al.Progress in the application of supramolecular solvent-microextraction technology in detection of food and environmental pollutants[J].Journal of Food Safety &Quality, 2025, 16(14):128-138.
[24] GARC A-FONSECA S, BALLESTEROS-G
A-FONSECA S, BALLESTEROS-G MEZ A, RUBIO S.Restricted access supramolecular solvents for sample treatment in enzyme-linked immuno-sorbent assay of mycotoxins in food[J].Analytica Chimica Acta, 2016, 935:129-135.
MEZ A, RUBIO S.Restricted access supramolecular solvents for sample treatment in enzyme-linked immuno-sorbent assay of mycotoxins in food[J].Analytica Chimica Acta, 2016, 935:129-135.
[25] 高慧宇, 王国栋, 赵佳, 等.近红外光谱测定小麦粉常规营养成分的模型优化[J].中国食物与营养, 2021, 27(5):30-34.GAO H Y, WANG G D, ZHAO J, et al.Model optimization for determination of common nutritional components in wheat flour using near infrared spectroscopy[J].Food and Nutrition in China, 2021, 27(5):30-34.
[26] WANG D X, WANG X C, HU Q J, et al.Salting-out assisted liquid-liquid extraction coupled to dispersive liquid-liquid microextraction for the determination of bisphenol A and six analogs (B, E, F, S, BADGE, BFDGE) in canned coffee drinks by ultra-performance liquid chromatography-tandem mass spectrometry[J].Food Analytical Methods, 2021, 14(3):441-452.
[27] BALLESTEROS-G MEZ A, RUBIO S.Environment-responsive alkanol-based supramolecular solvents:Characterization and potential as restricted access property and mixed-mode extractants[J].Analytical Chemistry, 2012, 84(1):342-349.
MEZ A, RUBIO S.Environment-responsive alkanol-based supramolecular solvents:Characterization and potential as restricted access property and mixed-mode extractants[J].Analytical Chemistry, 2012, 84(1):342-349.
[28] 叶钉利. 超分子溶剂的制备表征及其在中药活性成分提取中的应用[D].长春:长春工业大学, 2024.YE D L.Preparation, characterization and application of supramolecular solvents in the extraction of active components from traditional Chinese medicine [D].Changchun:Changchun University of Technology, 2024.
[29] S NCHEZ-VALLEJO C, BALLESTEROS-G
NCHEZ-VALLEJO C, BALLESTEROS-G MEZ A, RUBIO S.Tailoring composition and nanostructures in supramolecular solvents:Impact on the extraction efficiency of polyphenols from vegetal biomass[J].Separation and Purification Technology, 2022, 292:120991.
MEZ A, RUBIO S.Tailoring composition and nanostructures in supramolecular solvents:Impact on the extraction efficiency of polyphenols from vegetal biomass[J].Separation and Purification Technology, 2022, 292:120991.