随着全球对可持续发展需求的激增,生物制造正逐步取代高污染、高能耗的传统化学合成工艺,成为生产药物、精细化学品及可再生材料的核心策略。代谢工程通过重构微生物代谢网络,赋予细胞工厂定向合成目标产物的能力,而酶作为代谢通路的“分子工具”,其催化效率与功能多样性直接决定了生物制造的经济性与可行性。
细胞色素P450(cytochrome P450,CYP450)家族是自然界最庞大的酶类之一,具有高度催化多样性的血红素蛋白,其独特的氧化功能使其在代谢工程领域成为关键生物催化元件。这类酶能够介导多种底物的区域及立体选择性修饰(如羟基化、环氧化),在天然产物合成和药物代谢中具有重要应用潜力[1]。然而,CYP450在工业场景下面临多重瓶颈:其一,狭窄的底物谱系与低催化效率限制了其通用性;其二,酶蛋白在非生理条件下的稳定性不足,易受温度或有机溶剂影响而失活;其三,异源表达时与宿主代谢通路的适配性较差,导致辅因子供应失衡[2]。传统的酶工程方法虽可部分优化性能,但存在耗时长、成本高且难以靶向复杂催化网络等固有缺陷[3]。近年来,随着结构生物学、计算模拟和人工智能技术的突破,理性设计逐渐成为CYP450定向改造的核心手段。该策略通过解析酶的三维结构、底物结合模式及电子传递路径,结合分子动力学模拟和机器学习预测等方面进行工程化重构,从而高效实现催化活性、稳定性和底物适应性的协同优化[4-6]。理性设计不仅为代谢工程提供了高效生物制造工具,也为解析P450超家族的催化进化规律开辟了新路径。
1 CYP450酶
CYP450是血红素酶大家族,可催化各种化学反应,如羟基化反应、缩环反应、脱羧反应和反马氏加成等反应,如图1所示,除去传统的羟基化和缩环反应,一些非常规的催化反应更加全面地展现出CYP450酶多功能的一面,烯烃的反马氏氧化反应一直以来都是有机合成中的重要难题,它可以简化从烯烃到一些精细化学品和药物的有机合成路线,通过定向进化后得到新型CYP450工程酶aMOx,可以高效催化烯烃如苯乙烯的不对称反马氏氧化反应;P450酶催化的脱羧反应之前一直被认为只存在于药物合成和代谢过程中,P450过氧化物酶OleTJE被发现可以催化脂肪酸的氧化性脱羧合成一种十分重要的基础化工原料α烯烃[7-8]。
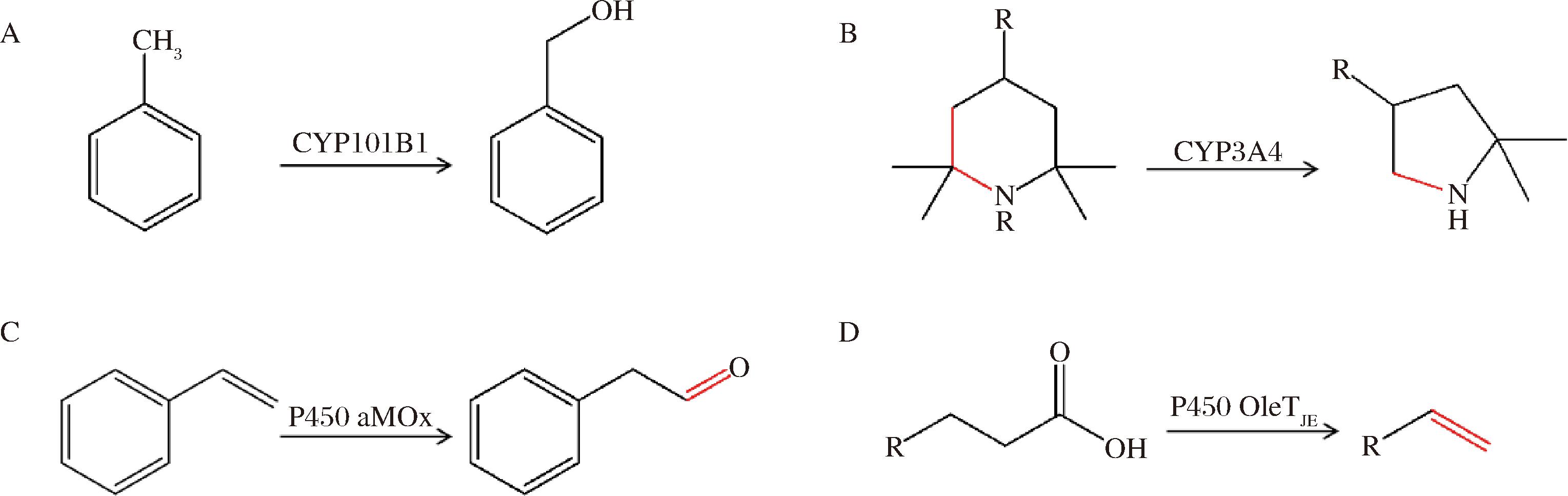
A-CYP101B1羟基化将甲苯催化生成苯甲醇;B-CYP3A4将2, 2, 6, 6-四甲基哌啶缩环生成2, 2-二甲基四氢吡咯;C-P450 aMOx将苯乙烯生成反马氏羰基化合物;D-P450 OleTJE将脂肪酸脱羧生成α烯烃
图1 P450的催化反应示意图
Fig.1 Schematic diagram of the catalytic reaction of P450
CYP450其名称源于大鼠肝脏微粒体中产生的亚铁-一氧化碳复合物在450 nm处具有最大吸光度值[1]。CYP超家族包括400多个基因家族的13 000个基因[9],其同一家族中的氨基酸序列显示40%的相似性,而给定亚家族中的氨基酸序列具有55%以上的相似性[10]。CYP命名委员会已为目前公认的CYP酶系统建立了命名法,其精确命名由CYP(细胞色素的正式缩写)、家族(数字)、亚家族(字母)和同工型(数字)按顺序书写,例如CYP1A1是CYP家族1亚家族和亚家族中的蛋白质1[9]。CYP450的结构相对保守,包含胞质结构域、跨膜结构域和辅基血红素。其催化机制以循环方式发生,主要分为Ⅰ型和Ⅱ型电子转移链[10]。CYP450能够利用分子氧对底物进行立体和区域选择性氧化,在催化过程中能够通过与还原伴侣蛋白的相互作用将电子从NADPH传递到血红素中心,激活氧分子,进而插入底物分子中完成氧化反应[9],这种催化机制使CYP450在生物体内的代谢过程中发挥着不可或缺的作用。作为典型的单加氧酶,P450 s的反应需要氧气和还原性辅因子的参与:首先,电子通过氧化还原伴侣从NAD(P)H传递至血红素铁以活化氧原子,随后1个氧原子插入底物中,而另1个氧原子则被还原为水。上述 P450单加氧酶催化的羟基化反应如下:
RH+O2+NADPH+H+→ROH+H2O+NADP+
氧化还原伴侣(redox partner proteins)是P450酶(几乎所有)催化过程中必需的。其中,NAD(P)H提供2个电子,氧化还原伴侣为了激活O2分子,将电子传递到亚铁血红素的反应中心。P450酶之所以被称为单加氧酶,是因为1个氧原子与底物结合形成环氧基或羟基等基团,与此同时另外1个氧原子结合形成了水分子。由于在温和条件下,如常压、常温和中性条件时,P450 酶能对惰性C—H键有效的催化以实现选择性羟基化,它们是环境友好的潜在生物催化剂并且获得了广泛的关注。图2为P450酶催化的羟基化反应,以简单介绍其催化机制。
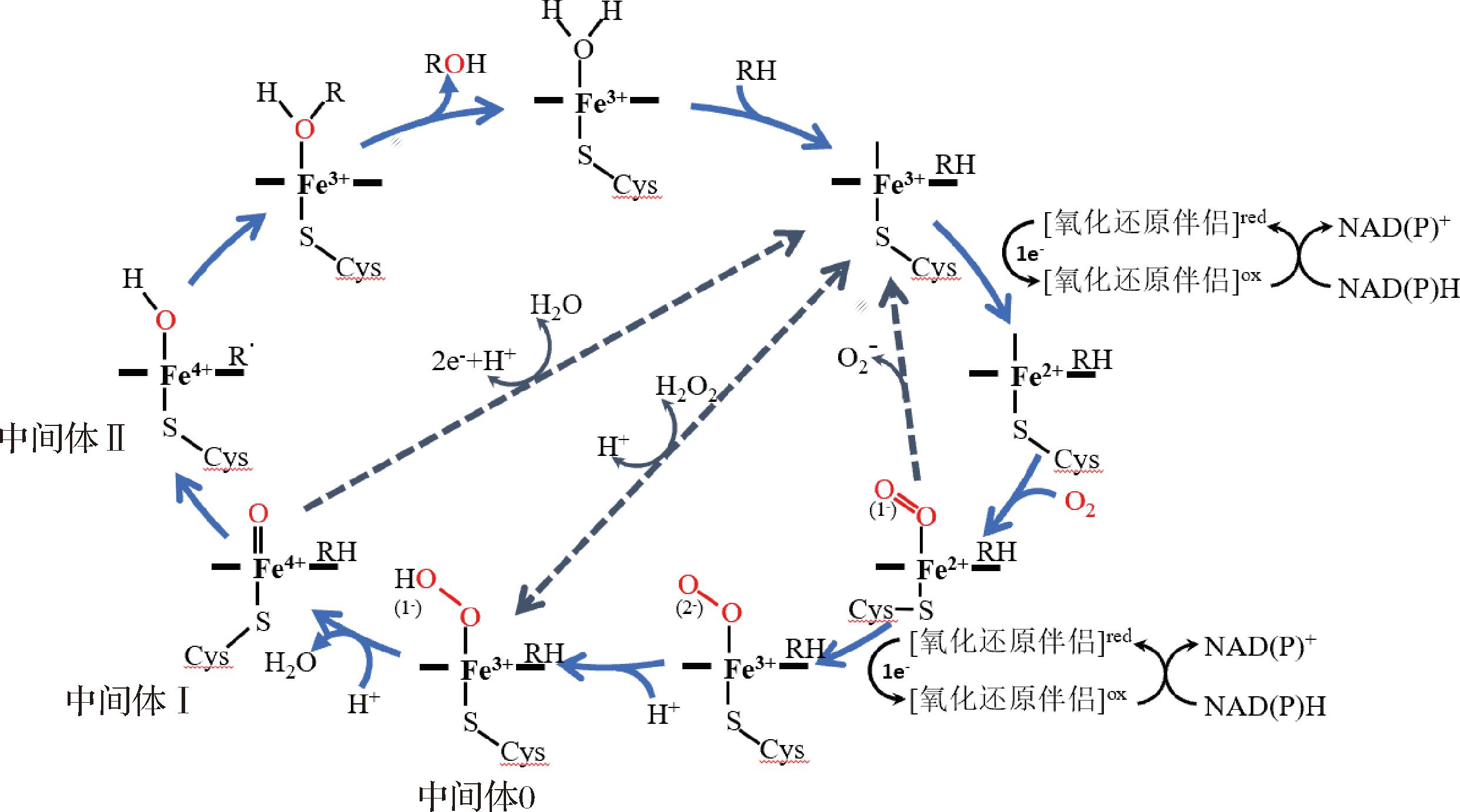
图2 P450的催化循环
Fig.2 Catalytic cycle of P450
2 理性设计策略在P450酶改造方面的优势
酶的理性设计通常依赖于生物信息学的方法,根据蛋白质的结构信息以及同源蛋白质的序列比较,理性选择氨基酸残基作为靶点,结合定点突变技术对关键氨基酸进行突变,筛选获得目标突变体,如图3所示。理性设计方法的出现,有效地改善了传统方法的诸多局限,减少了突变体库的数量。理性设计可高效快速地获得目标突变体,尤其是在酶的底物特异性改造方面,更能体现其优越性。与这些传统策略相比,理性设计的核心优势在于通过多尺度建模与逆向工程原理,在开发效率、经济性等方面有明显优势。
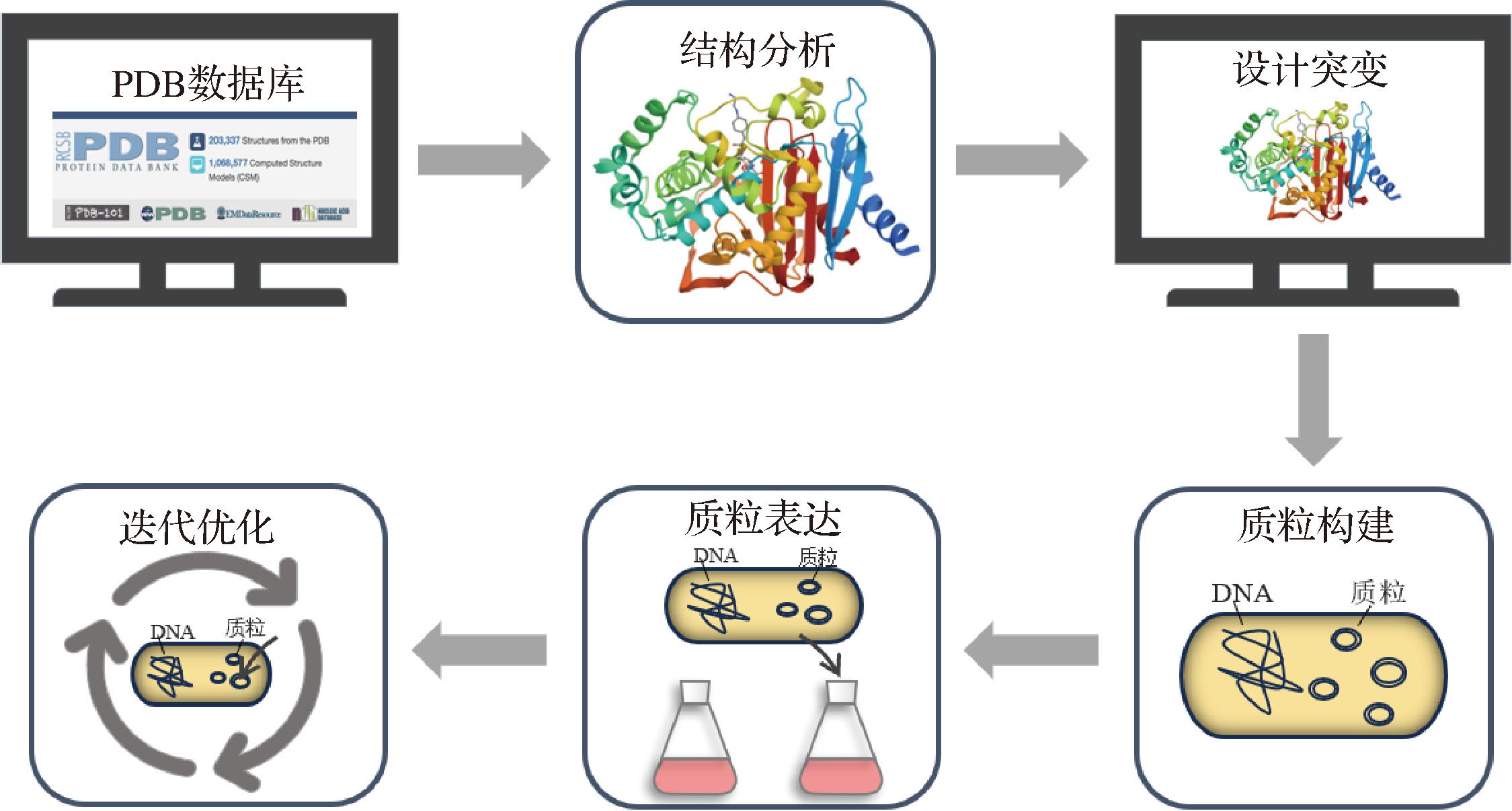
图3 理性设计传统策略
Fig.3 Rational design of traditional strategies
理性设计能够精准调控催化效率与选择性,通过解析酶的晶体结构和分子动力学模拟,精准识别底物结合口袋、配体通道及电子传递链的关键残基,进而设计突变以优化底物取向和电子传递效率,稳定底物结合口袋可减少水分子的干扰,提高偶联效率,从而降低副产物的生成[11]。
传统定向进化需依赖大量随机突变库,而理性设计能够减少对随机诱变的依赖。理性设计通过计算机辅助预测关键突变位点,显著缩短了优化周期,在细胞色素理性设计中,其核心策略是综合利用结构生物学、生物信息学和计算模拟技术,深入解析目标细胞色素的结构与功能关系。这使研究者能精准锁定影响目标性状的关键残基,高效引入少数最优突变,避免了传统方法中筛选海量随机突变体的巨大工作量。细胞色素的理性设计不仅显著缩短了优化周期并降低了成本,也充分展示了该策略作为蛋白质工程核心工具的效力[11]。
随着生物技术和分子生物学的飞速发展,CYP450的理性分析取得了突破性进展,同时在电子传递网络重构技术中取得重要突破。分子动力学模拟与深度学习技术在CYP450的理性设计中起着重要作用。Cytochrome P450 Engineering Database(CYPED)是一个广泛的数据库,整合了超过30万个P450酶序列以及41 000多个命名基因,该数据库不仅支持多序列比对,还能进行活性位点的预测,成为CYP450功能研究和工程改造的重要工具[12]。AlphaFold2是一种基于深度学习的蛋白质结构预测工具,在膜结合CYP450的结构建模中得到了应用,能够显著提高膜结合CYP450结构建模的准确性。通过结合CYPED与AlphaFold2,为深入理解催化机制及设计新型酶提供了有力的支持,能够更加高效地进行CYP450的理性设计,对开发和实际应用新型酶起到加速的作用[13]。
3 代谢工程中CYP450理性设计的应用案例
在代谢工程中,CYP450因其在生物合成中具有重要的催化作用,成为了优化天然产物合成过程的关键酶类。CYP450具有高度的底物特异性和丰富的催化反应种类,能够执行一系列重要的化学反应,这些反应常常是天然产物合成中的关键步骤(表1)。CYP450酶的理性设计通常在辅因子血红素周围进行改造,如图4所示,该蛋白质结构源于PDB数据库(Protein Data Bank),其PDB数据库配体名称为6HQG。由于CYP450的底物特异性和反应选择性受到其结构和活性位点的限制,如何通过理性设计来拓宽其底物范围,优化其催化效率,一直是代谢工程中的研究重点。
表1 CYP450理性设计的应用示例
Table 1 Example of an application for the rational design of CYP450
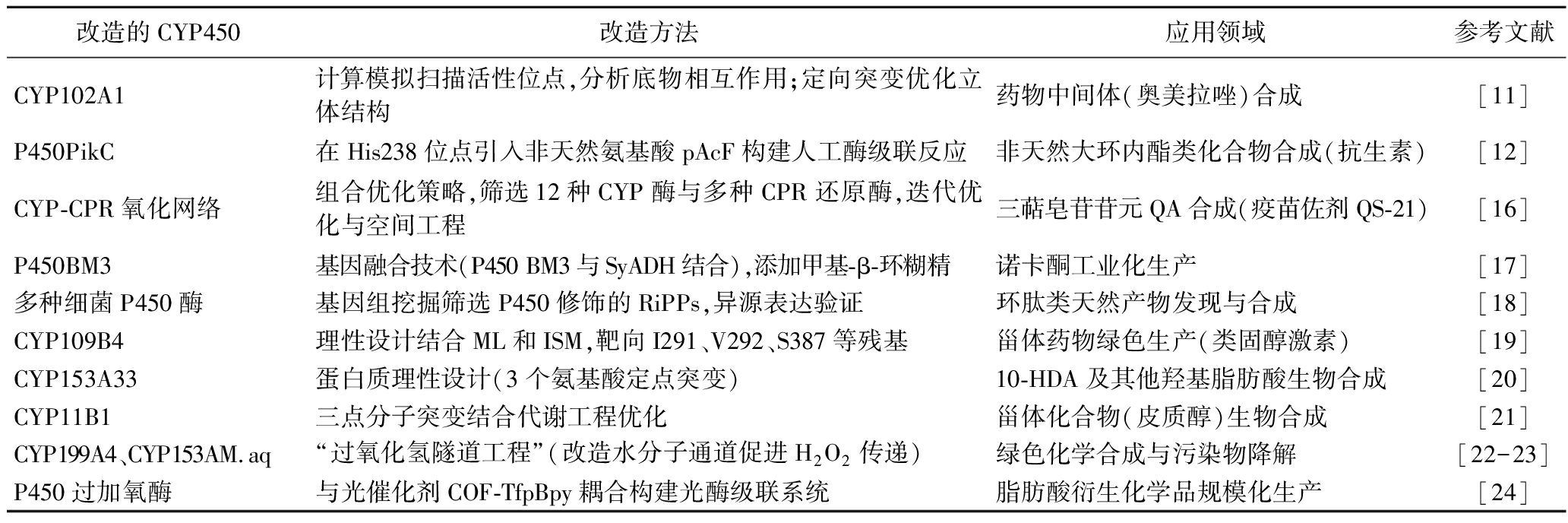
改造的CYP450改造方法应用领域参考文献CYP102A1计算模拟扫描活性位点,分析底物相互作用;定向突变优化立体结构药物中间体(奥美拉唑)合成[11]P450PikC在His238位点引入非天然氨基酸pAcF构建人工酶级联反应非天然大环内酯类化合物合成(抗生素)[12]CYP-CPR氧化网络组合优化策略,筛选12种CYP酶与多种CPR还原酶,迭代优化与空间工程三萜皂苷苷元QA合成(疫苗佐剂QS-21)[16]P450BM3 基因融合技术(P450 BM3与SyADH结合),添加甲基-β-环糊精诺卡酮工业化生产[17]多种细菌P450酶基因组挖掘筛选P450修饰的RiPPs,异源表达验证环肽类天然产物发现与合成[18]CYP109B4理性设计结合ML和ISM,靶向I291、V292、S387等残基甾体药物绿色生产(类固醇激素)[19]CYP153A33蛋白质理性设计(3个氨基酸定点突变)10-HDA及其他羟基脂肪酸生物合成[20]CYP11B1三点分子突变结合代谢工程优化甾体化合物(皮质醇)生物合成[21]CYP199A4、CYP153AM.aq“过氧化氢隧道工程”(改造水分子通道促进H2O2传递)绿色化学合成与污染物降解[22-23]P450过加氧酶与光催化剂COF-TfpBpy耦合构建光酶级联系统脂肪酸衍生化学品规模化生产[24]
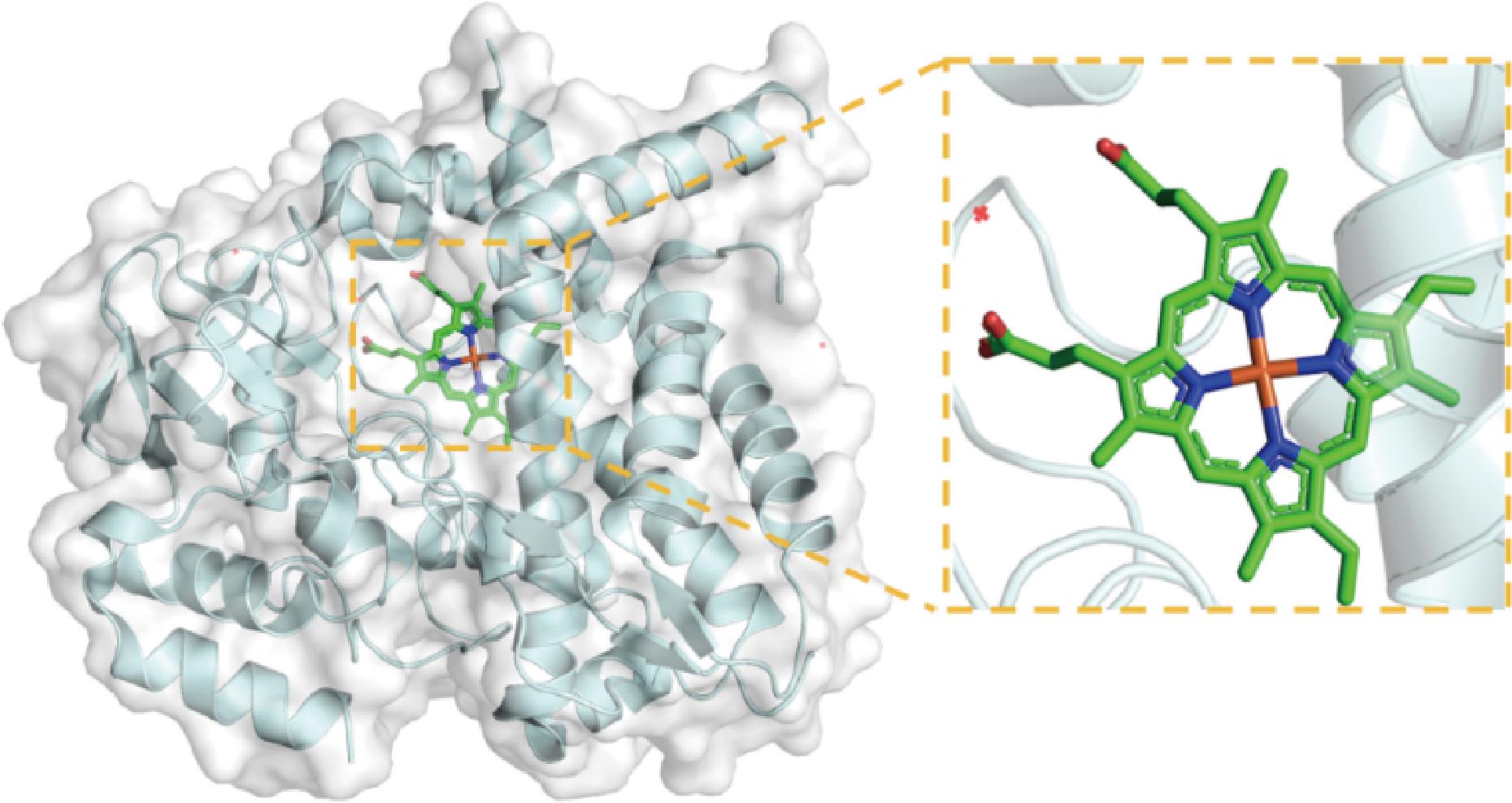
图4 CYP450 s的血红素辅因子
Fig.4 Heme cofactors of CYP450 s
3.1 天然产物高效合成
天然产物是生命体在特定环境下产生的化学小分子,通常具有复杂的分子结构。传统天然产物的获取方式往往面临产量低、资源有限和成本高等问题。CYP450在植物、微生物和动物体内,对甾体激素、萜类及黄酮等天然产物的合成中发挥重要作用,这些酶能够在温和条件下对复杂分子骨架进行精细的羟基化和环氧化等修饰,为天然产物的结构多样性和生物活性提供了基础。
工程组学的融合为天然产物的高效生物合成开辟了新路径。特别是在复杂代谢网络的重构与调控领域方面,多维度优化策略能够显著提升目标产物的合成效率,YANG等[14]采用组合优化策略成功构建了CYP-细胞色素P450还原酶 (cytochrome P450 reductase,CPR)氧化网络,在酿酒酵母中实现了三萜皂苷苷元奎诺酸(quillaic acid,QA)的高效合成,通过筛选12种CYP酶和多种CPR还原酶的组合以及迭代优化与空间工程,将QA的产量从21.3 mg/L提升至2.23 g/L,标志着微生物合成三萜皂苷进入克级生产阶段,同时副产物比例降低至14%以下,结果表明该策略在代谢通量精准调控方面具有借鉴意义,为皂苷类化合物的工业化生产奠定基础,若结合实时代谢监测与动态调控技术,可进一步增强酵母底盘的生产潜力。
近年来,合成生物学在酶工程领域的创新突破不断涌现,通过定向进化、非天然氨基酸整合等策略拓展天然产物的结构多样性。在重构酶催化功能与拓展底物谱方面,可以通过精准的蛋白质工程改造实现传统酶体系难以达到的催化效率,FISCHER等[12]将p-乙酰苯丙氨酸(p-acetylphenylalanine,pAcF)引入CYP450 PikC酶的His238位点,对底物特异性进行调控,使PikC酶能够催化无糖基的大环内酯底物的羟基化反应。这一突变使PikC的催化能力得到了显著增强,能够处理一些天然P450酶无法催化的底物,特别是突变体PikCH238pAcF与糖基转移酶BSGT-1的联用,成功合成了多种非天然的大环内酯类化合物,产率高达1.5 mmol/L。这种基于遗传密码扩展的策略,为突破天然酶进化限制提供了新方法。展现出天然产物合成的巨大潜力,使大环内酯类化合物的合成变得更加高效。
酶催化系统的模块化设计与能量代谢优化策略正在突破氧化还原反应的效率瓶颈,通过多酶协同组装与辅因子再生策略,为复杂生物催化过程的高效驱动建立新体系。KOKORIN等[15]通过基因融合技术将P450 BM3与来自 S.yanoikuyae 的ADH(SyADH)结合,构建了一种双功能酶,实现诺卡酮(+)-Nootkatone合成与辅因子再生的偶联。这种酶自供能系统的构建,为氧化还原反应的有关代谢提供了创新方法。融合酶在添加甲基-β-环糊精后能够使诺卡酮产量达到1 080 mg/L,较单独酶混合物提高1.7倍,是目前报道的最高水平之一。值得注意的是,甲基-β-环糊精的添加虽然能够提高产物产量,但其工业化应用的经济性需结合下游分离工艺综合考量。
环肽类天然产物的发现与结构解析一直是天然产物研究领域的重要方向,这类化合物主要通过核糖体合成和翻译后修饰肽(ribosomally synthesized and post-translationally modified peptides,RiPPs)生物合成途径产生。HU等[16]开发了一种基因组挖掘流程,通过系统筛选细菌中的P450酶修饰的RiPPs,异源表达验证后发现11种新型环肽分子,结构通过芳香氨基酸侧链交联形成刚性环状骨架。这项研究揭示了P450酶在天然产物多样性扩展中的潜力,后续研究应重点关注这些新型环肽的生物活性筛选及其生物合成途径的进化机制解析。
3.2 药物代谢合成
理性设计作为连接结构生物学与药物开发的桥梁,不仅优化了代谢酶的催化性能与选择性,还推动了绿色制药工艺与个性化治疗的发展。随着计算工具与合成生物学的进步,其在药物研发中的核心地位将愈发凸显。
通过精准调控酶的功能特性,能够为天然产物合成路径提供关键优化策略,酶蛋白结构与功能关系的深度解析为催化剂定向进化提供了全新视角。ZHANG等[17]展示了通过基因组挖掘和酶工程实现甾体药物的选择性羟基化,他们从细菌中筛选出了CYP109B4酶,并解析该酶与甾体底物的复合物晶体结构,为催化剂的优化提供了依据。分析了CYP109B4活性口袋中关键残基(如I291、V292、S387),结合理性设计、突变景观设计(mutation landscape,ML)和迭代饱和突变(iterative saturation mutation,ISM)方法,成功地将催化选择性从16β羟基化转变为15β羟基化。酶的工程化改造,可以精准调控甾体底物的区域和立体选择性,提供了一种新的绿色催化途径用于甾体药物的高效生产。这种方法不仅提升了甾体类药物的生产效率,还为类固醇激素的生物合成提供了可持续的方案。
在天然活性成分的高效生物合成中,酶工程技术的创新应用正不断突破传统化学转化的效率瓶颈。以蜂王浆核心功能物质10-羟基-2-癸烯酸(10-hydroxy-2-decenoic acid,10-HDA)为例,其不仅具有增强免疫力、抗肿瘤等多重功效,传统的方法提取效果差难以满足市场需求,亟需设计生物合成途径提升合成效率(图5)。李岩[18]针对10-HDA生物合成中的关键酶CYP153A33展开改造,通过计算机辅助筛选出3个关键氨基酸位点进行优化,其中M228L突变体催化反式-2-癸烯酸生成10-HDA的转化率提升至87%,产量较原始酶提高近4倍。研究表明,该突变可能通过调节酶分子与底物的结合方式强化催化效能,这一策略不仅为10-HDA的规模化制备提供了高效生物催化剂,也为其他功能性脂肪酸的绿色合成开辟了技术路径。
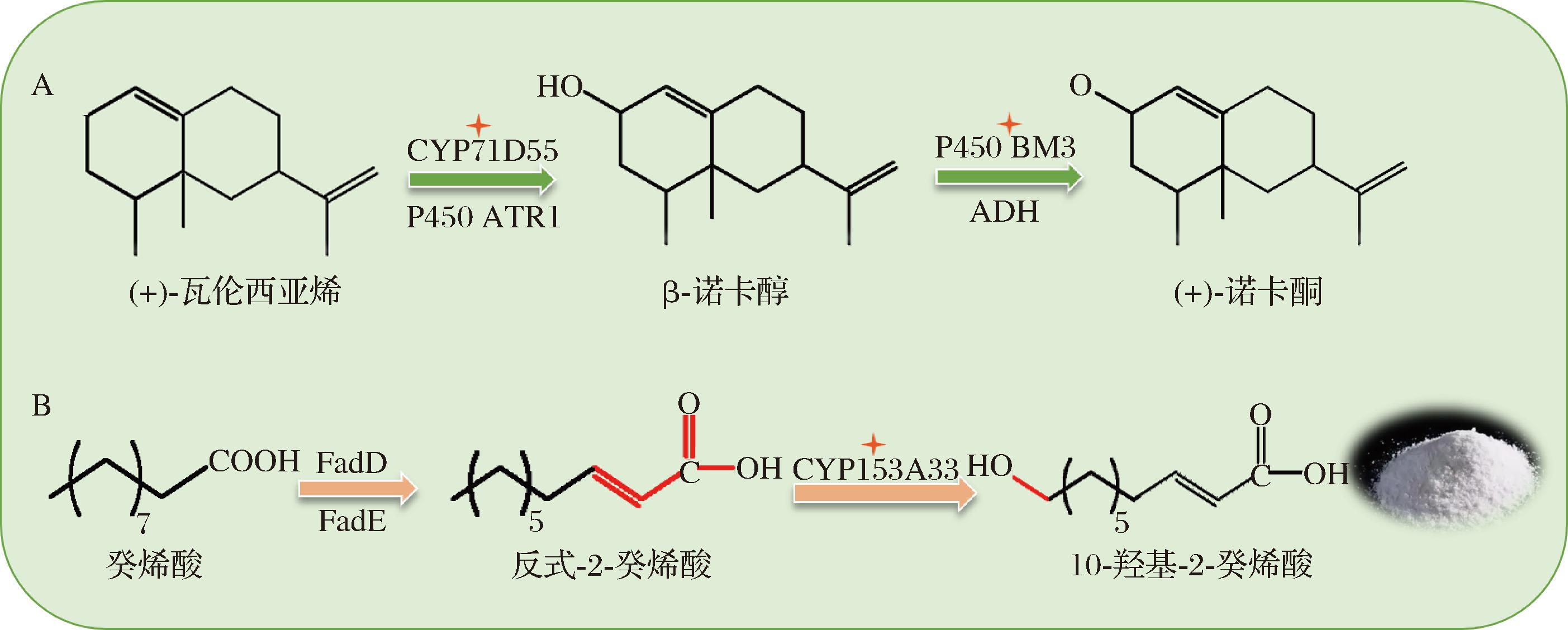
A-生物催化合成(+)-nootkatone;B-两步法催化癸酸合成10-HDA
图5 (+)-nootkatone和10-HDA的合成方法
Fig.5 Synthesis method of (+)-nootkatone and 10-HDA
生物催化剂的适配性改造为复杂药物分子的规模化生产注入了新动能。张岩峰[19]利用人源线粒体11β-羟化酶CYP11B1进行皮质醇的高效生物催化生产。通过优化代谢工程以及CYP11B1的分子改造,改善了酶的催化活性,最终通过三点突变(3 point mutation,M3)将皮质醇的产率提升至2 756.3 mg/(L/d),是已知最高产率的3.3倍,M3可能通过稳定血红素结合域增强了电子传递效率。成功构建人源线粒体酶在异源高效表达平台,突破性地解决了跨物种蛋白表达过程中酶活性维持与功能完整性的技术瓶颈。
3.3 环境污染物降解与绿色催化
在代谢工程领域,环境污染物降解和绿色催化成为研究的重点。传统的污染治理方式,往往面临成本高、效率低和二次污染等问题,而通过微生物、酶和代谢工程手段来降解环境污染物,不仅能提供高效、绿色的处理方法,还能将污染物转化为有价值的资源,助力生态修复和可持续发展。
酶工程与反应体系协同优化正成为提升氧化还原催化经济性的重要突破口,MA等[20]和丛志奇等[21]提出了一种创新的“过氧化氢隧道工程”策略,目的是优化CYP450催化反应中过氧化氢的利用效率,通过改造CYP450的水分子通道(如CYP199A4和CYP153AM.aq)促进H2O2进入血红素的活性中心,从而增强酶的催化活性。通过合理的结构改造,突变体的催化活性提升了15~183倍,同时使过氧化氢的消耗量减少了95%,提高了催化过程的经济性和环保性。尤其在C—H键氧化反应中,成功地将这一技术应用于P450BM3体系,通过双功能小分子的协同作用,提升了氧化反应的效率,为绿色化学合成提供了新的工具。
在合成生物学与清洁能源技术交叉创新的浪潮中,光能驱动与酶催化体系的深度融合正在重塑生物制造的能源利用方式。JIANG等[22]通过将光催化剂COF-TfpBpy介导的光合H2O2与P450过加氧酶的H2O2依赖性酶活相结合,建立了一个全新的人工光酶级联催化系统,在空气、水和光照条件下实现脂肪酸到1-烯烃和羟基脂肪酸的绿色转化,证明了该光生物炼制模型在生产脂肪酸衍生化学品方面的可放大性和应用潜力。体系展现的可放大性提示可以将其拓展到萜类、生物碱等高附加值化合物的合成领域,若能与代谢工程相结合构建细胞工厂,或许能实现从光能到化学品的全生物基转化路径。
CYP450在环境污染物降解和绿色化学合成中具有巨大的应用潜力。通过这些技术创新,CYP450在环境保护、农药降解和化学合成等领域展现了广阔的前景,为实现绿色可持续发展目标提供了有力支持。
4 总结
4.1 技术挑战
CYP450在异源宿主中的高效可溶表达面临严峻挑战,这主要源于其高度疏水的跨膜结构域、血红素辅基插入的复杂性以及对特定分子伴侣和氧化还原环境的需求,导致易形成无活性的包涵体,这种不可溶性不仅导致酶活性丧失或低下,也极大地阻碍了后续的蛋白纯化、结构解析、功能表征以及实际应用开发。张彭湃等[23]利用乳糖经β-半乳糖苷酶转化异乳糖的天然延迟诱导特性,显著降低肽链合成速率,为P450 BM3提供充分折叠时间,使可溶性表达比例提升至90%,活性蛋白产量较异丙基-β-D-硫代半乳糖苷提升3.13倍,并借乳糖的碳源属性缓解代谢负荷,使菌体生物量倍增。通过协同调控表达动力学与细胞微环境,攻克了复杂P450酶可溶表达的核心瓶颈。伴侣蛋白通常被认为通过辅助蛋白折叠提高可溶性表达,PENG等[24]探讨了通过共表达伴侣蛋白Prefoldin和P450 BM3,显著提升大肠杆菌中P450 BM3突变体催化吲哚生成靛蓝的效率,但Prefoldin并未直接解决P450 BM3突变体的可溶性表达问题,而是通过调节细胞代谢辅因子NADPH间接提高了催化效率,Prefoldin通过提高NADPH供应,解决了还原力不足的问题。通过工程化辅因子平衡而非仅聚焦酶本身性质,为优化依赖辅因子的生物催化过程提供了新策略。
尽管已经探索了多种策略来改善P450的可溶表达,例如使用融合标签、分子伴侣共表达、N端序列截短或修饰等方法,但其可溶表达效率、活性回收率及普适性问题仍未得到根本性解决。不同P450同工酶间存在显著差异,针对特定P450找到有效且高效的表达策略往往需要大量、繁琐的经验性优化工作。展望未来,突破可溶表达瓶颈的研究将向智能化利用AI辅助理性设计、机器学习预测关键突变,高效化和高通量化方向发展。深入利用多组学技术解析P450在异源宿主中的折叠失败机制,将为开发更精准的干预策略奠定坚实基础。系统梳理和深入剖析当前P450酶可溶表达的主要策略、技术瓶颈与优化方向,不仅具有重要的理论意义,也是推动其实际应用的关键前提。
膜结合型CYP450酶在微生物宿主中异源表达时,由于其膜结合特性,常常面临折叠困难,导致活性丧失的问题。此外,CYP450的反应依赖NADPH和血红素作为辅因子,但在异源宿主中,辅因子的再生能力有限,为解决这一问题,HU等[25]通过代谢工程引入亚铁血红素合成途径或优化氧化还原平衡,以提高辅因子的供应。
在CYP450酶的研究与应用中,催化选择性与稳定性之间存在一定的矛盾。在区域/立体选择性的精准控制方面,ZHANG等[17]在CYP109B4突变体通过残基替换(I291A/T317A)实现甾体底物羟基化位点的转换,但突变可能降低酶的热稳定性;对于非天然催化系统的兼容性,CHEN等[26]开发的H2O2驱动P450过加氧酶虽摆脱了辅因子依赖,但其催化效率受小分子助催化剂的稳定性和结合强度限制。
在数据驱动的设计中,功能数据的稀缺性是主要的难点,WANG等[27]发现深度学习模型(如P450Diffusion)需要大量高质量的结构-功能数据,但目前仅有约5%的植物CYP450完成了结构解析,导致生成序列的功能预测存在较大偏差。多目标优化存在复杂性的问题,在提升催化活性、稳定性和底物多样性的过程中,计算模型(如AlphaFold2)难以平衡多参数之间的冲突,因此需要开发多目标优化算法。
4.2 未来方向
人工智能与多组学的融合正引领生物工程和代谢工程领域的创新发展。在优化生成模型方面,扩散模型(如P450Diffusion)生成非天然P450酶序列,结合多组学数据(如结构组学和代谢组学)进行虚拟筛选,突破了天然酶序列空间的限制。WANG等[27]开发了P450Diffusion方法,成功设计出具有优异催化性能的新型P450酶。此外,结合微流控芯片与机器人技术能够实现突变体库的快速构建与筛选,提升了筛选通量,华大智造推出的MGIDS-1000高通量微流控液滴筛选平台,具有高通量、高精度、高灵敏度液滴筛选的特点。
动态调控宿主细胞的代谢网络对于优化代谢产物的合成至关重要。CRISPR-dCas9系统作为一种强大的基因调控工具,已被广泛应用于代谢工程中,能够催化酶的表达与辅因子再生途径耦合实现对代谢流的精确调控[28];利用CRISPR-dCas9系统动态调节宿主代谢流,实时匹配P450酶的表达需求与辅因子供应;在酵母中通过耦合NADPH再生途径与CYP表达模块,实现了对代谢流的精确调控[29]。此外,动态调控策略还被应用于代谢产物的优化合成,提升了产物的产量和质量。
在非天然催化系统的开发方面,董文锦等[30]探索了光/电驱动辅因子再生的方法,利用光敏剂或电极界面反应替代NADPH,构建无辅因子依赖的P450催化系统,适用于连续流生物反应器。光催化和酶的杂合系统为利用太阳能驱动生物酶催化提供了新案例,并为共价有机框架光催化剂提供了发展方向[22]。经过进一步优化,该系统有望成为一种绿色、高效、环境友好且成本效益高的油脂精细化学品合成方法。TIAN等[31]通过耦合硫化镍电催化剂和均相Rh分子催化剂,发现硫化镍作为协同质子耦合电子转移媒介体可促进Rh-H活性物种形成,巧妙模拟了酶催化NADP+还原的功能和机制,实现高活性、高选择性电催化NAD(P)H再生。该研究还建立了通过耦合质子还原电催化剂(硫化物或金属)和均相分子催化剂进行高效光电催化NAD(P)H再生的普适性策略,并验证了光电催化再生的NAD(P)H可用于氢化暗反应,为后续耦合酶催化暗反应、构建集成人工光合成体系奠定重要基础。
CYP450酶作为生物催化领域的重要支柱,其独特的氧化能力和底物多样性使其在药物合成、天然产物衍生和环境修复等方面具有广泛应用价值。但当前CYP450酶工程领域的核心挑战在于克服其固有的结构与功能复杂性所带来的限制,基于结构与机制的理性设计策略,常常因对酶的三维构象、动态变化及其与催化功能间复杂关联的理解尚不充分而受到限制;另一方面,尽管定向进化方法展现出强大的适应性进化能力,但在实际操作中往往遭遇高通量筛选通量不足这一关键瓶颈。因此,有效融合这2种策略的优势,并积极引入如人工智能预测、自动化实验平台等前沿技术,是突破当前困境、释放P450工程潜力的关键路径,还需深入剖析P450家族酶的活性口袋及电子转移链结构,关注其与底物结合作用过程中伴随的构象重排,对反应过渡态与中间体的能量分布进行精准预测。传统的理性设计手段虽然能够借助同源建模、底物对接以及量子化学计算来对关键氨基酸位点进行有针对性的突变,但由于P450在不同底物结构与反应路径间展现出巨大灵活性,这种静态的模拟往往难以反映其动态适应性,从而限制了工程化改造的深度与广度。
未来突破点在于深度整合半理性设计与机器学习驱动的计算预测,并结合高通量筛选技术。这种模式不仅能显著提升改造效率,更能针对性地解决P450催化中普遍存在的区域/立体选择性控制难题及异源表达中的稳定性问题。未来P450酶理性设计将向智能化、系统化和绿色化方向发展,突破天然酶的限制,推动生物制造在医药、能源与环境领域的规模化应用。
[1] GUENGERICH F P, WATERMAN M R, EGLI M. Recent structural insights into cytochrome P450 function[J]. Trends in Pharmacological Sciences, 2016, 37(8):625-640.
[2] URLACHER V B, GIRHARD M. Cytochrome P450 monooxygenases in biotechnology and synthetic biology[J]. Trends in Biotechnology, 2019, 37(8):882-897.
[3] ARNOLD F H. Innovation by evolution: Bringing new chemistry to life[J]. Biophysical Journal, 2022, 121(3):177a.
[4] POULOS T L. Heme enzyme structure and function[J]. Chemical Reviews, 2014, 114(7):3919-3962.
[5] GILLAM E M J. Engineering cytochrome p450 enzymes[J]. Chemical Research in Toxicology, 2008, 21(1):220-231.
[6] YANG K K, WU Z, ARNOLD F H. Machine learning-guided directed evolution for protein engineering [J]. Nat Methods. 2019,16(8):687-694. DOI:10.48550/arXiv.1811.10775.
[7] JIANG Y Y, LI S Y. Catalytic function and application of cytochrome P450 enzymes in biosynthesis and organic synthesis[J]. Chinese Journal of Organic Chemistry, 2018, 38(9):2307.
[8] 代萌. 工程化改造细胞色素P450催化合成苯甲醇衍生物及4-羟基异佛尔酮的研究[D]. 武汉: 湖北大学, 2024.DAI M. Study on the synthesis of benzyl alcohol derivatives and 4-hydroxyisophorone catalyzed by engineered cytochrome P450[D]. Wuhan: Hubei University, 2024.
[9] MANIKANDAN P, NAGINI S. Cytochrome P450 structure, function and clinical significance: A review[J]. Current Drug Targets, 2018, 19(1):38-54.
[10] GUENGERICH F P. Cytochrome P450 research and the journal of biological chemistry[J]. Journal of Biological Chemistry, 2019, 294(5):1671-1680.
[11] MENG S Q, JI Y, ZHU L L, et al. The molecular basis and enzyme engineering strategies for improvement of coupling efficiency in cytochrome P450s[J]. Biotechnology Advances, 2022, 61:108051.
[12] FISCHER M, KNOLL M, SIRIM D, et al. The Cytochrome P450 Engineering Database: A navigation and prediction tool for the cytochrome P450 protein family[J]. Bioinformatics, 2007, 23(15):2015-2017.
[13] SCHOTTLENDER G, PRIETO J M, CLEMENTE C, et al. Bacterial cytochrome P450s: A bioinformatics odyssey of substrate discovery[J]. Frontiers in Microbiology, 2024, 15:1343029.
[14] YANG J Z, LIU Y G, ZHONG D C, et al. Combinatorial optimization and spatial remodeling of CYPs to control product profile[J]. Metabolic Engineering, 2023, 80:119-129.
[15] KOKORIN A, URLACHER V B. Artificial fusions between P450 BM3 and an alcohol dehydrogenase for efficient (+)-nootkatone production[J]. ChemBioChem, 2022, 23(12): e202200065.
[16] HU Y L, YIN F Z, SHI J, et al. P450-modified ribosomally synthesized peptides with aromatic cross-links[J]. Journal of the American Chemical Society, 2023, 145(50):27325-27335.
[17] ZHANG X D, SHEN P P, ZHAO J, et al. Rationally controlling selective steroid hydroxylation via scaffold sampling of a P450 family[J]. ACS Catalysis, 2023, 13(2):1280-1289.
[18] 李岩. 生物合成10-HDA关键催化元件的筛选及P450酶理性设计的研究[D]. 济南: 齐鲁工业大学, 2021.LI Y. Screening of key catalytic elements of biosynthetic 10-HDA and rational design of P450 enzymes[D]. Jinan: Qilu University of Technology, 2021.
[19] 张岩峰. P450的分子改造及其在甾体生物合成中的应用[D]. 杭州: 浙江大学, 2023.ZHANG Y F. Molecular modification of P450 and its application in steroid biosynthesis[D]. Hangzhou: Zhejiang University, 2023.
[20] MA N N, CHEN Z F, CHEN J, et al. Dual-functional small molecules for generating an efficient cytochrome P450BM3 peroxygenase[J]. Angewandte Chemie (International Ed. in English), 2018, 57(26):7628-7633.
[21] 丛志奇, 陈杰, 马娜娜, 等. 一种激活酶催化反应的双功能小分子化合物及其应用: CN110128364B[P]. 2022-01-04.
[22] JIANG Y Y, LI P F, LI Z, et al. Photoenzymatic synthesis of 1-alkenes and hydroxyl fatty acids by cascading a COF photocatalyst and P450 peroxygenases[J]. Science Bulletin, 2024, 69(21):3350-3354.
[23] 张彭湃, 王松廷. 乳糖诱导剂促进P450 BM-3在大肠杆菌中可溶性表达的研究[J]. 工业微生物, 2016, 46(4):14-18.ZHANG P P, WANG S T. Enhanced soluble expression of cytochrome P450 BM-3 in E. coli by using lactose as inducer[J]. Industrial Microbiology, 2016, 46(4):14-18.
[24] PENG S Y, CHU Z M, LU J F, et al. Co-expression of prefoldin from hyperthermophilic Archaea Pyrococcus furiosus in Escherichia coli enhances the catalytic efficiency of modified cytochrome P450 BM3[J]. Progress in Biochemistry and Biophysics, 2017, 44(12):1125-1131.
[25] HU B D, YU H B, ZHOU J W, et al. Whole-cell P450 biocatalysis using engineered Escherichia coli with fine-tuned heme biosynthesis[J]. Advanced Science, 2023, 10(6):2205580.
[26] CHEN J, KONG F H, MA N N, et al. Peroxide-driven hydroxylation of small alkanes catalyzed by an artificial P450BM3 peroxygenase system[J]. ACS Catalysis, 2019, 9(8):7350-7355.
[27] WANG Q, LIU X N, ZHANG H J, et al. Cytochrome P450 enzyme design by constraining the catalytic pocket in a diffusion model[J]. Research, 2024, 7:413.
[28] 罗旻, 顾华. CRISPR-dCas9系统在基因表达调控中的最新研究进展[J]. 实验室研究与探索, 2016, 35(3):20-23.LUO M, GU H. The state of the art of CRISPR-dCas9 system on regulating level of gene expression[J]. Research and Exploration in Laboratory, 2016, 35(3):20-23.
[29] 陈永灿, 张建志, 司同. 酿酒酵母中基于CRISPR/dCas9的基因转录调控工具的开发与应用[J]. 生物技术通报, 2020, 36(4): 1-12.CHEN Y C, ZHANG J Z, SI T. Development and applications of CRISPR/dCas9-based gene transcriptional regulation tool in Saccharomyces cerevisiae[J]. Biotechnology Bulletin, 2020, 36(4):1-12.
[30] 董文锦, 陈夫山, 邓理, 等. 光催化NAD(P)H再生的研究进展[J]. 分子催化, 2022(3):274-286; I0004.DONG W J, CHEN F S, DENG L, et al. Recent advances on the photocatalytic regeneration of NAD(P)H[J]. Journal of Molecular Catalysis (China), 2022(3):274-286; I0004.
[31] TIAN S J, LONG G F, ZHOU P W, et al. A coupled system of Ni3S2 and Rh complex with biomimetic function for electrocatalytic 1, 4-NAD(P)H regeneration[J]. Journal of the American Chemical Society, 2024, 146(23):15730-15739.