挥发性硫醇是一类风味强度极高的硫化物,在众多食品和饮料的风味组成中起着关键作用。挥发性硫醇可根据分子质量大小被划分为低分子质量挥发性硫醇和高分子质量挥发性硫醇。低分子质量挥发性硫醇通常对食品风味具有显著的负面影响,部分高分子质量挥发性硫醇又被称为多官能团硫醇(polyfunctional thiols,PFTs)对产品的香气品质产生积极贡献。
啤酒中的PFTs主要来源于麦芽和啤酒花,以结合态和游离态2种方式存在。其中结合态的PFTs不具备香气特征,在酿造过程中,通过转移或生物转化生成游离态的PFTs。PFTs在结构上,除了含有巯基之外,还含有其他多种官能团(包括羟基、醛基、酮基、酯基)。按照官能团的差别,PFTs被划分为巯基醇、巯基醛、巯基酮和巯基酯。综合之前的研究,大部分巯基醛展现出奶酪和香葱气味,巯基酯则通常被描述为洋葱、大蒜、马铃薯和熟肉等气味特征[1-2]。在这些众多的PFTs中出现了一些有趣的物质,例如3-巯基己醇(3-sulfanylhexan-1-ol,3SH)、3-巯基己醇乙酸酯(3-sulfanylhexyl acetate,3SHA)、4-甲基-4-巯基-2-戊酮(4-methyl-4-sulfanylpentan-2-one,4MSP)等,表现出宜人的水果香气[1]。
本文重点介绍了啤酒中PFTs的存在形式、由结合态向游离态的释放机制以及相关的影响因素。
1 PFTs的存在
1.1 酒花中的游离PFTs
在酒花中检测到41种游离PFTs[3]。前人对这41种游离PFTs进行了嗅闻测试与感官特征分析,结果显示这些化合物普遍具有较低的嗅觉阈值,易于被嗅觉系统感知到(表1)。
表1 酒花中的PFTs风味属性与感官阈值[3-4]
Table 1 Flavour attributes and sensory thresholds of PFTs in hops

序号物质名称风味描述阈值/(ng/L)13-巯基丙醇乙酸酯烘烤的肉40 00021-巯基-3-丁醇乙酸酯洋葱、塑料33-巯基丁醇乙酸酯奶酪、洋葱43-巯基-2-甲基丙醇乙酸酯爆米花、烤坚果53-巯基-3-甲基丁醇乙酸酯胡椒、燃料5 30064-巯基-4-甲基-2-戊醇乙酸酯烤坚果、咖啡71-巯基-3-戊醇乙酸酯奶酪、百里香83-巯基-2-甲基丁醇乙酸酯煮熟的肉、烤肉93-巯基戊醇乙酸酯百香果、糖果103-巯基-2-乙基丙醇乙酸酯醋113-巯基己醇乙酸酯番石榴、葡萄柚5123-巯基-4-甲基戊醇乙酸酯柚子、大黄160133-巯基辛醇乙酸酯柠檬、胡萝卜143-巯基-1-丙醇爆米花、肉汤400 000153-巯基-1-丁醇汗、奶酪163-巯基-2-甲基丙醇肉汤、韭菜173-巯基-3-甲基丁醇硫磺、汗184-甲基-4-巯基-2-戊醇猫尿、黑加仑55191-巯基-3-戊醇蘑菇、荨麻203-巯基-2-甲基丁醇洋葱、胡椒213-巯基-1-戊醇羊毛、肉汤620223-巯基-2-甲基戊醇硫磺、煤气233-巯基己醇番石榴、大黄55243-巯基-2-丁基丙醇塑料,辛辣253-巯基-1-庚醇柠檬、柑橘35263-巯基-4-甲基戊醇大黄、柚子70273-巯基-1-辛醇枸杞、大黄283-巯基戊醛啤酒花、花香294-巯基-4-甲基-2-戊酮猫尿、黑加仑1.5303-巯基-2-乙基丙醛臭鼬、塑料311-巯基-3-戊酮矿物、奶酪323-巯基己醛花香、柠檬333-巯基庚醛柠檬、糖果343-巯基-2-丁基丙醛肉汤、塑料353-巯基辛醛柑橘、桃子362-巯基-1-乙醇煤气、工业污水2 000 000373-甲基-2-丁烯-1-硫醇咖啡、臭鼬2382-巯基乙基乙酸酯烧焦的木头40 000393-巯基-2-甲基丁-1-硫醇蘑菇、白果406-巯基-1-己醇蘑菇、花香414-巯基-4-甲基-1-戊醇咖喱、芹菜
2000年,研究人员在卡斯卡特啤酒花(Cascade)中分离出一种具有独特黑醋栗香气的物质,经鉴定,该物质为4MSP(29)[5]。这是PFTs首次作为果香风味物质在啤酒酿造领域被发现。REGLITZ等[6]在2017年开发了一种针对4MSP(29)具有极高灵敏度的检测方法,使用该方法对53组不同酒花样品进行了检测,实验结果表明美国产区的酒花4MSP(29)含量相比欧洲高的多。鉴于4MSP在不同啤酒花中含量的显著差异,它被视为区分啤酒花品种的重要风味物质之一[7]。3SH(23)是另一关注度较高的化合物,几乎在所有被检测的酒花样品中都可以找到。3SHA(11)是3SH的乙酸酯形式,相比3SH(23)具有更低的感官阈值(5 ng/L),在酒花中难寻其踪,主要通过酿造过程中的生物转化形成并最终存在于啤酒中[7]。4MSP(29)、3SH(23)和3SHA(11)是目前在啤酒领域关注度最高的3种PFTs。除此之外,对酒花香气组成起到特殊贡献的物质还包括:3-巯基-1-庚醇(25),被视为卡斯卡特啤酒花柠檬香味的主要贡献成分之一[8];3-巯基-4-甲基戊醇(26)和3-巯基-4-甲基戊醇乙酸酯(12),被视为是尼尔森苏维酒花(Nelson Sauvin)的特征性香气化合物,具有类似长相思葡萄酒的风味属性。在最新研究中,晚收的富良野美人酒花(Furano Beauty)中3-巯基-4-甲基戊醇(26)质量浓度高达615 μg/L,在目前已知的啤酒花中含量最高[9]。
1.2 PFTs前体的存在
在添加了酒花的麦汁中观察到一个有趣现象:在麦汁中,经过100 ℃加热处理后的PFTs含量显著高于90 ℃热处理后的含量;且在发酵早期PFTs的含量较酿造其他环节更高。这一结果表明:在酿造过程中有PFTs前体物质的存在,并能够通过非生物或生物转化实现PFTs的释放。
1.2.1 C-S共轭前体的存在
1998年,在葡萄中发现了2种能够释放出PFTs的C-S共轭物,分别为半胱酰氨化共轭前体和谷胱甘肽化共轭前体[10]。GROS等[11]推测该前体物质可能同样存在于啤酒花中,通过化学合成结合反相高效液相色谱-质谱的检测方法,最终确定了半胱酰氨化3-巯基己醇(3-S-cysteinylhexan-1-ol,Cys-3SH)的存在。在啤酒中,由结合态释放得到的3SH含量远高于原料中本身存在的游离态3SH的含量,占物质总量的99%以上,其中谷胱甘肽化3-巯基己醇(4-S-glutathionylhexan-1-ol,G-3SH)为原料中主要的前体形式[12]。而对于4MSP而言,游离态在酿造原料中为主要的存在形式,结合态仅占极少部分[13]。
在使用标记示踪G-3SH的代谢过程中,发现了2种二肽化合物:γ谷氨酰半胱氨酰-3SH(γGluCys-3SH)和半胱氨酸甘氨酸-3SH(CysGly-3SH),它们是G-3SH生物转化过程中的中间物质[14]。在麦芽中,CysGly-3SH的含量比啤酒花中更高[15]。在不同麦芽种类中,CysGly-3SH和γGluCys-3SH的含量最高可达10、11 μg/kg。其中,γGluCys-3SH只在特种大麦芽、黑麦麦芽、斯佩尔特小麦和小麦中发现[16]。在发酵过程中,二肽前体的含量和转化率受生物因素影响很大,这将在下一小节被详细说明。除了3SH和4MSP外,其他PFTs的二肽前体还尚未被研究。其他的PFTs,例如3-巯基-1-戊醇[16]、3-巯基-戊醛[17]、3-巯基-4-甲基戊醇[18-19]的C-S共轭前体在酒花中被检测到。在麦芽中,被报道过具有C-S共轭前体的硫醇种类包括:3-巯基-1-辛醇[8]、3-巯基-4-甲基戊醇[19]、3-巯基-1-戊醇[16,20]。其中谷胱甘肽化3-巯基-1-辛醇,仅在嫩麦芽中被检测到[8]。
1.2.2 其他潜在PFTs前体
然而,任何一种C-S共轭前体的转化效率与啤酒中最终的游离态PFTs含量之间均不存在直观的对应关系。研究人员针对硫醇化合物的理化性质及酿造过程中可能涉及到的生化反应过程进行了分析,通过试验证明了其他潜在PFTs前体的存在。使用液相色谱耦合傅立叶变换质谱在长相思葡萄汁中定性检测到了3-S-谷胱甘肽基己醛(3-S-gluthathionylhexanal)及其亚硫酸氢盐加合物,该物质在合成培养基中可释放出3SH,摩尔转化率可达0.4%[21]。另外,在添加了G-3SH的液体中,当铜离子质量浓度超过1.25 mg/L时,液相色谱质谱联用检测发现一种新型衍生物—4-S-(N-乙酰基-半胱氨酰基)-己-1-醇[3-S-(N-acetyl-cysteinyl)-hexan-1-ol]。在酵母参与生物转化的情况下,约有0.6%的3SH被释放出来[22]。此外,在采用一种名为三(2-羧乙基)膦[tris(2-carboxyethyl)phosphine,TCEP]的二硫键特异性还原剂处理过的酒花水和无酒花麦汁中,3SH浓度分别增加了8.9和9.9倍,4MSP则分别增加了2.1和5.1倍。而再次使用TCEP对发酵结束后的啤酒处理时,游离PFTs的释放量增益甚微[23]。发酵过程有效还原了大部分的二硫键结合态硫醇。鉴于PFTs的高反应活性,导致其极易被氧化形成分子内或分子间的二硫键。对啤酒中二硫键的特性及其转化机制进行进一步研究,或许可以帮助人们更好地理解PFTs的形成与释放过程。
2 C-S共轭前体的形成及向游离态的释放机制
前文提到,成品啤酒中游离硫醇的来源有2种:一种是从酒花直接转移而来,另一种是通过化学反应从前体中释放出来。截至目前,硫醇前体在酿造原料中的形成原因尚不明朗,据理论推测G-SH前体源自植物细胞体内的解毒和抗逆机制。这个过程在谷胱甘肽S-转移酶的作用下,将来源于脂质氧化和醇醛缩合代谢得到的不饱和醛酮与谷胱甘肽结合,生成谷胱甘肽共轭的硫醇前体[15]。形成的G-SH前体通过细胞内的酶系作用或外部的物化处理逐步转化分解释放出游离PFTs。
生物转化通常发生在啤酒酿造过程中的糖化和发酵这2个时期。糖化过程中,来自于谷物发芽产生的大量酶,在适宜的温度下行使催化作用。糖化过程中,G-3SH会被降解为CysGly-3SH[24]。随温度升高,游离PFTs的释放效率提升,但同样会导致风味物质的挥发。硫醇前驱物质在热端面临多个反应,首先位于啤酒花蛇麻腺结构中的前体物被释放于醪液中,而后被酶系作用实现游离硫醇的释放。温度达到80 ℃时麦芽中的酶将全部失活。但实验结果显示在酶失活后,伴随温度的上升,G-3SH在麦汁的含量仍在减少,CysGly-3SH的量在上升,此时非生物作用的影响占主导地位[24]。
发酵过程中PFTs的释放,主要通过细胞内的生物转化实现。酿酒酵母(Saccharomyces cerevisiae)作为发酵菌株,分解代谢Cys-SH释放PFTs的可能性早已被证实。最近,CHENOT等[20]发现拉格酵母(Saccharomyces pastorianus)具备强大的转化能力,约0.35%的G-SH在发酵过程中被转化成游离态[20]。由于这种生物转化的存在,一些本身游离硫醇含量较低的品种,例如萨兹(Saaz)酒花(PFTs含量较低,但却是G-3SH的重要来源),也具备了强大的芳香潜力。发酵过程中,可以通过调节pH、原麦汁浓度、发酵温度、发酵时间等参数调节微生物的生理活动,从而影响成品酒中PFTs的组成[20,25]。以3SH为例,如图1所示,参与硫醇前体转化和硫醇释放的酶系包含:γ-谷氨酰转肽酶(γ-glutamyl transpeptidase,γ-GT)、羧肽酶(carboxypeptidases)、β-裂解酶(β-lyase)以及实现醇酯转化所需要的乙酰化酶(acetyltransferase)。其中β-裂解酶不仅能够从半胱酰氨化前体中释放游离硫醇,还可以直接作用于二肽前体。
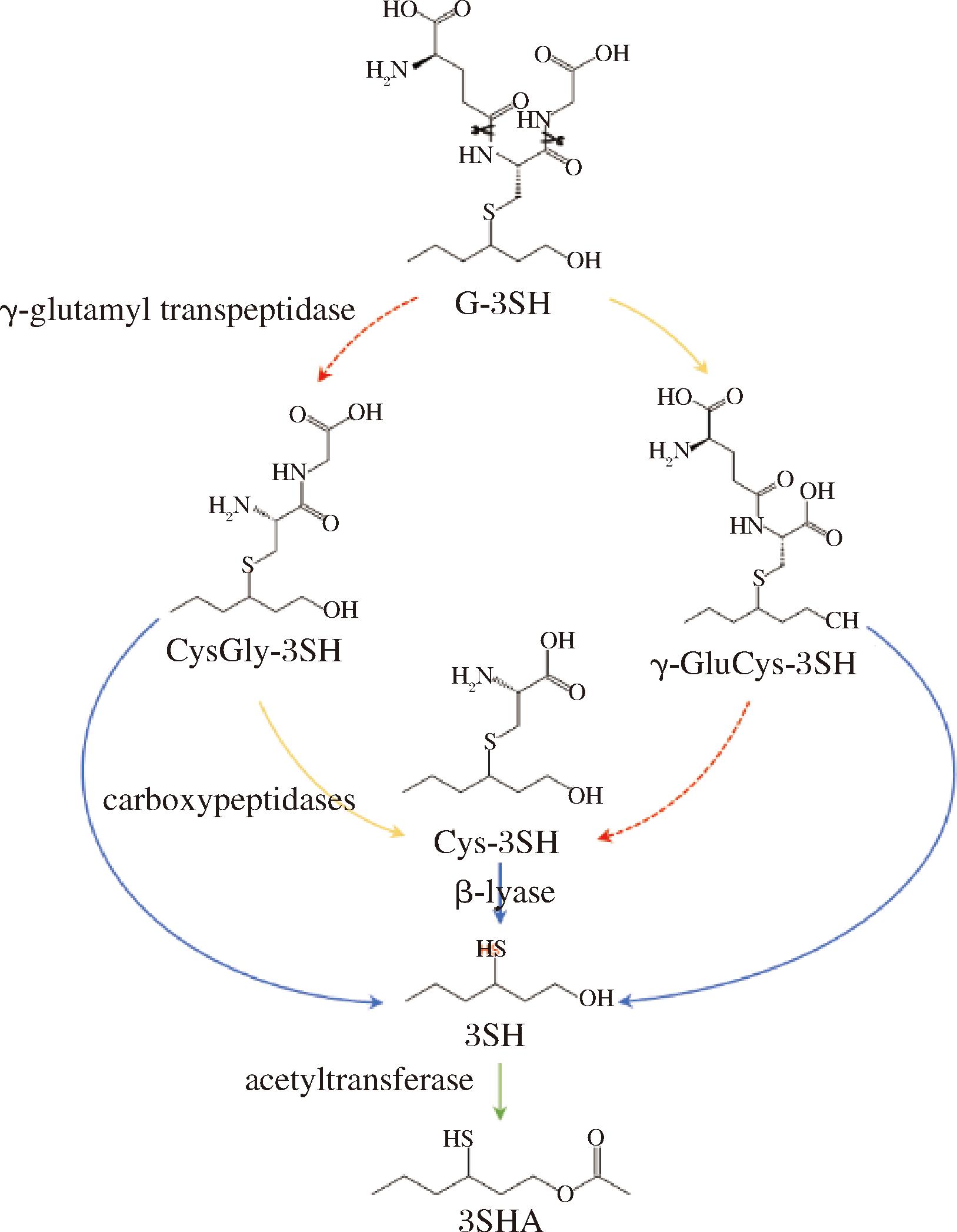
图1 结合态向游离态PFTs的释放机制[14]
Fig.1 The release mechanisms of polyfunctional thiols from bound to free states
注:图中γ-glutamyl transpeptidase、carboxypeptidases、β-lyase为PFTs释放过程中起催化作用的酶,对应的中文名称分别为γ-谷氨酰转肽酶、羧肽酶和β-裂解酶。
另外,一些细菌,例如:大肠杆菌(Escherichia coli),乳酸菌(Lactobacillus casei和Lactobacillus lactis)、金黄色葡萄球菌(Staphylococcus haemolyticus)和链球菌属的部分菌株和非酿酒酵母(例如:Eubacterium limosum)也具有从C-S共轭前体中释放游离硫醇的能力[14]。
采用基因敲除、RNA测序与实时荧光定量PCR等分子生物学手段,探究发酵过程中控制硫醇释放的基因序列以及生物反应发生的部位,结果如图2所示[26]。液泡或溶酶体是G-3SH代谢的关键场所。G-3SH通过OPT1p谷胱甘肽转运蛋白以主动运输的方式从外界进入细胞内。该转运过程与细胞膜上的另一转运蛋白Gex1p协同作用,共同维持细胞内谷胱甘肽前体的动态平衡。然而,Gex1基因的过表达可能导致三肽前体在细胞内外进行无效循环,从而影响分解代谢效率。此外,细胞膜上的二肽或三肽转运体Ptr2p在此过程中仅负责二肽硫醇前体的转运工作,不参与G-3SH的转运。G-3SH通过膜上的转运体YBT1p进入液泡内部,并刺激γ-谷氨酰转肽酶和羧肽酶相关基因的表达,从而实现其代谢转化。细胞质作为次要场所,通过谷胱甘肽降解替代途径将部分三肽前体分解为二肽或半胱酰氨化前体(图2)。生成的Cys-3SH在细胞质中被IRC7基因或STR3基因编码的β-裂解酶切断C-S共轭键释放出游离的3SH。IRC7基因和GAP1基因(用于编码一种泛氨基酸转运蛋白)是受到氮代谢抑制调节的,当氮源稀缺时,两者的表达得到上调,游离PFTs含量增加[26]。Cys-4MSP对IRC7p相比Cys-3SH更加敏感[27]。
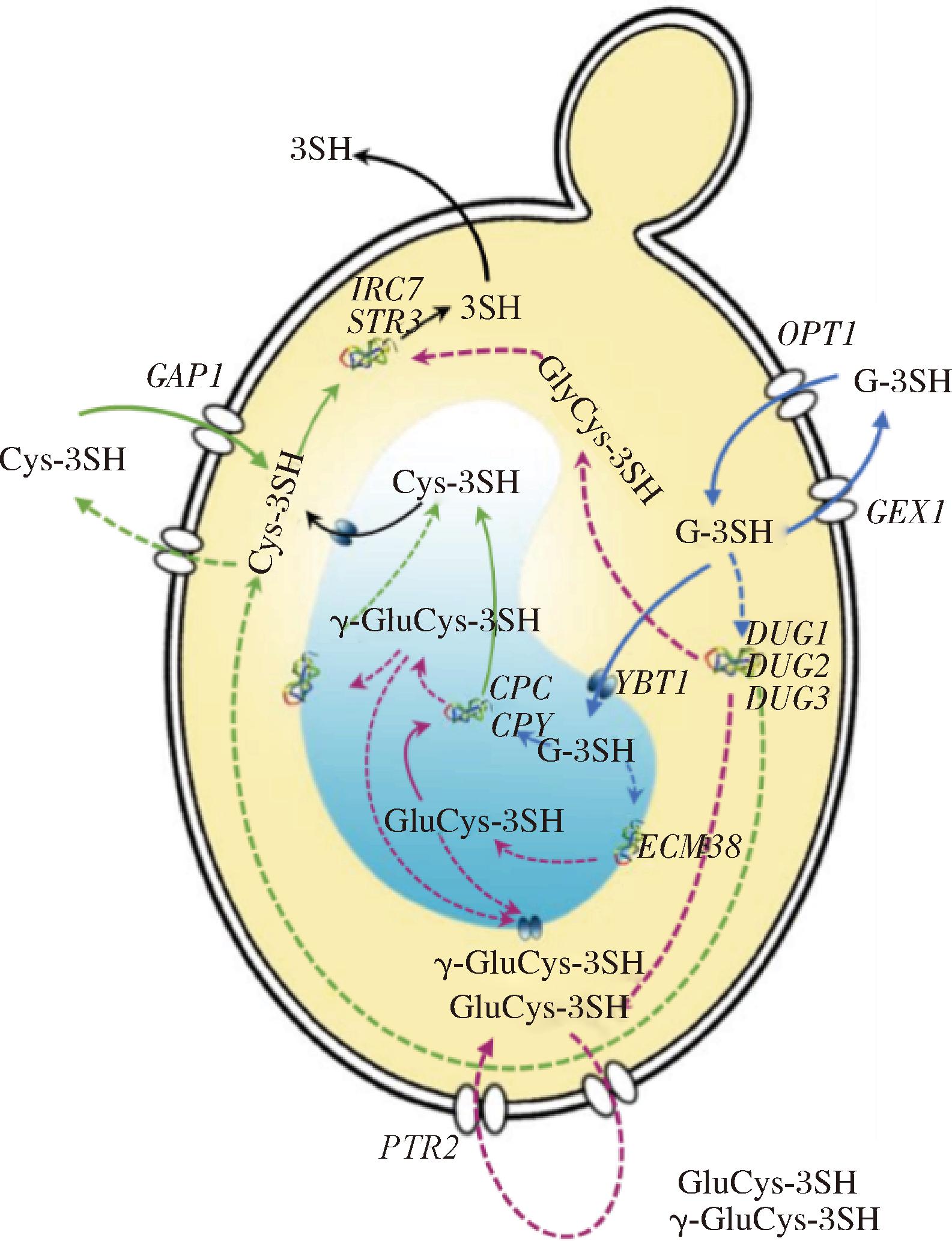
图2 酵母细胞内PFTs的释放过程[26]
Fig.2 The release process of polyfunctional thiols in yeast cells
注:OPT1编码一种谷胱甘肽转运蛋白;GEX1编码一种质子-谷胱甘肽反向转运蛋白。ECM38编码一种谷胱甘肽水解酶的前体蛋白。PTR2编码一种肽转运蛋白。GAP1编码一种一般氨基酸通透酶,参与多种氨基酸的跨膜转运。DUG1、DUG2和DUG3共同编码一个能够降解谷胱甘肽的蛋白复合物。YBT1编码一种属于ABC转运蛋白家族的膜转运蛋白。CPY与CPC在酵母细胞中编码液泡丝氨酸羧肽酶。IRC7和STR3为编码β-裂解酶的基因。
对比同批次啤酒花和啤酒中PFTs含量发现:4MSP在酒花中与啤酒中的含量呈线性相关。而对3SH而言,在假定酒花中游离硫醇向啤酒中的转化率为100%的情况下,最终啤酒中3SH的含量仍然大于这一数值[7]。这表明4MSP在啤酒中的含量主要由酒花中的游离硫醇含量决定,3SH含量则主要由前体物质的转化效率决定。G-3SH在酿造过程中的转化率低但在酿造原料中的含量高,Cys-3SH在原料中含量较少但释放效率高。含有羟基的硫醇在乙酰化酶的作用下同乙醇生成相应的乙酸酯。在成熟的啤酒可以检测到少量的3SHA,尽管含量很少(1~15 ng/L),由于其在啤酒介质中的阈值极低(5 ng/L),也会对啤酒风味产生重要的影响[11]。G-3SH相比其他前体中释放出来的3SH具有更高的酯化效率[25]。主发酵结束后的啤酒冷贮期是巯基酯释放到酒体中的关键阶段[20]。
3 影响PFTs及其对应前体的因素
对于酒花和麦芽这样的植物来说,各类化学反应伴随着它们的整个生长过程。植物生长过程和原料加工过程中的变量对硫醇在酿造原料中的存在起到关键作用。
3.1 铜离子
铜离子是一种公认的硫醇吸收剂,可与硫醇发生络合和氧化反应。研究发现,欧洲栽培的所有酒花品种中均未检出4MSP,这可能与欧洲地区广泛使用的铜基杀菌剂(如波尔多液,主要成分为CuSO4)有关[6]。为证明这一猜想,使用铜离子处理了啤酒花,与对照组(未接受铜离子处理)中4MSP的含量相比下降了25%,3SH则呈现出上升趋势[28]。这一差异表明了3SH与4MSP代谢合成过程中可能涉及的不同机制。铜离子作用于土壤与作用于植物叶面或酒花表面相比,作用于土壤对最终酒花中挥发性硫醇含量的影响更大[28]。在发酵过程中,铜离子会被酵母从麦汁中移除,此过程受到pH、酵母健康状况和酵母生长阶段的影响。这对于维持啤酒的风味稳定性具有重要意义。另外,根据这一特性,可以通过在成品啤酒中添加铜离子的方法,判断啤酒的某一风味特征是否源于PFTs。酿酒师们在选择多品种酒花混合投放时,应留意欧洲产区酒花中的铜离子残留可能对最终香气表达产生的交叉影响。
3.2 氮源
在酒花生长过程中,不同的施肥种类和方式导致酒花在质量和芳香潜力上具有差异。硫醇前体的浓度受氮肥种类和剂量的调节[29]。在植物生长早期和果实成熟晚期提升土壤中的氮含量,对硫醇前体在果实中的存在产生积极作用。一项研究报道称,施用硫肥会降低酒花中硝酸盐含量,而导致Cys-3SH和CysGly-3SH分别减少了19%和23%[30]。
氮在啤酒发酵过程中带来的影响是复杂的。在酿酒酵母内部,存在氮分解代谢物抑制(nitrogen catabolite repression,NCR)调节。在2009年,LUND等[31]在葡萄酒酿造实验中证实了Cys-SH的代谢会受NCR的控制。对比酵母浸出粉胨葡萄糖培养基和麦汁培养基中的发酵实验结果,发酵后酵母浸出粉胨葡萄糖培养基样品中游离挥发性硫醇的产量较麦汁培养基中更少。作者认为这可能与酵母浸出粉胨葡萄糖培养基中更高的游离氨基氮水平有关[25]。CHENOT等[20]测试了多种挥发性硫醇前体在不同氮含量条件下游离挥发性硫醇的释放情况,在低氮水平下更有利于从Cys-SH前体中释放出游离硫醇。然而,在实际酿造过程中,NCR具有意想不到的复杂性,这种复杂性主要体现在酵母菌种及不同生长阶段中基因调控的差异性。此外,NCR不仅与一般氨基酸控制途径相关联,还与其他不参与氮代谢的基因转录调控系统之间存在交互作用。
3.3 多酚
多酚可能干扰酵母细胞内硫醇前体向游离态的转化。部分酒花多酚(如单宁、黄烷醇等)可通过氧化聚合的方式与啤酒中的游离硫醇结合,降低液体中游离态硫醇含量。酒花多酚的种类与含量受到酒花品种、种植条件、收获时间等多种因素的影响[32]。值得注意的是,多酚作为天然抗氧化剂,可以防止硫醇被其他氧化剂所破坏[14]。
3.4 环境
种植区域对酒花中风味成分组成的影响已引起业内众多学者的关注。即使在同一品种的不同产区酒花中PFTs的含量也会表现出显著差异[33]。而同一产区,不同年份种植的同一种酒花在酿造过程中游离PFTs的释放潜力差异显著。在排除人为因素(例如:铜基杀菌剂的使用和施肥方式)的影响后,这种差异依然存在。上述证据共同指向一个关键影响因素:环境。众所周知,环境因素对植物生长及次生代谢产物的生成具有显著影响,具体包括但不限于温度、湿度、光照强度、水分供应、矿物质含量以及二氧化碳浓度[34]。葡萄叶片和果实在适度的环境胁迫下,Cys-3SH及G-3SH的含量会增加,而过度的环境胁迫则会抑制PFTs前体的积累。典型的环境胁迫包括干旱、缺氮、过度紫外线照射、低温胁迫和高温胁迫[22]。此外,反式-2-己烯醛(可在植物中与谷胱甘肽生成G-3SH)在植物生长发育过程中应对环境胁迫起重要作用[15]。
3.5 采收日期
在植物生长过程化学成分不断发生变化。RUBOTTOM等[35]连续3年对不同采收时间的卡斯卡特酒花样品进行了分析检测,结果发现伴随着收获期的增长,Cys-3SH浓度下降,游离3SH浓度上升。在晚收的富良野美人酒花(Furano Beauty),富良野奇迹(Furano Magical)和卡斯卡特酒花中3-巯基-4-甲基戊醇含量比常规采收时间的样品增长了数倍,而4MSP没有显示出含量与采收时间之间的相关性[9]。目前,晚收可能导致的问题(如酒花氧化发黄)是否会对啤酒质量产生不利的影响是需要关注的问题,这对后期将酒花收获日期的延后作为提升酒花风味的手段的合理性具有重要意义。
3.6 酒花加工
酒花加工过程涉及环境温度与湿度的变化。新鲜的酒花经干燥,含水量从70%~80%快速降至8%~12%,以便于贮存运输和制成酒花制品。酒花精油是热敏性物质,烘干会导致约15%~25%的损失[36]。干燥前后样品进行比较,发现伴随着干物质占比的上升,4MSP在此过程中多呈现上升趋势[6]。干燥后的酒花蓬松、易氧化,且酒花结构完整,使得存在于蛇麻腺中的香味物质转移率较低。最常用于提升酒花利用率的方法是通过研磨破损后压制得到颗粒。该过程对挥发性硫醇含量的影响很小。在贮存阶段,4MSP的回收率与贮存温度和时间呈反比,随两者数值的上升在酒花中的含量呈下降趋势[6]。
3.7 麦芽加工
麦芽在只提供挥发性硫醇的前体物质。在酿造过程中它依赖于原料和酵母中的酶系转化和化学水解实现游离挥发性硫醇的释放。基本的制麦工艺包括浸泡、发芽和干燥这3个步骤,在此基础上进行调整与延伸(例如烘烤、焙焦等),得到具有独特风味和结构的特种麦芽,用于满足啤酒在色、香、味、口感、泡持性方面的特殊要求。发芽过程会产生大量酶,大分子物质(例如淀粉、不溶性蛋白质和β-葡聚糖细胞壁等)被降解。对于基础麦芽来说,发芽过程对于最终麦芽物质组成起到决定性作用。在淡色麦芽中,发芽过程激活了内源酶,作用于G-3SH,使得CysGly-3SH含量与G-3SH含量呈正比。而γGluCys-3SH仅在特种麦芽中被检测到[16]。特种麦芽的制麦过程主要涉及美拉德反应、焦糖化反应和热解反应[37]。在色度为5~45 EBC的特种麦芽中,Cys-3SH的含量与CysGly-3SH的含量相关,前者可能由后者化学反应转化而来。烤制麦芽中没有发现任何种类的挥发性硫醇的前体物质,这与其过高的焙烧温度存在密切联系(130~230 ℃)[16]。
4 总结与展望
总的来说,提升成品啤酒中PFTs含量的方法主要可以从原料、发酵工艺调控及其他辅助手段3方面展开。原料优化:通过精准调控酒花关键生长期的氮素供给以促进硫醇前体生物合成;优选高PFTs含量的特色酒花品种(如西楚酒花、银河酒花、尼尔森苏维酒花等);适当推迟酒花采收时间;降低酒花和麦芽干燥时的温度。发酵工艺优化:运用基因工程技术选育高表达IRC7基因的酵母菌株,结合NCR机制调控提升前体转化效率;适当延长冷贮时间促进胞内硫醇释放;针对性实施酒花阶段投料策略(如煮沸末期/冷端添加)以定向调控硫醇组成。其他辅助手段:应用外源性酶直接解离结合态前体,并结合抗氧化剂稳定硫醇氧化还原态。此外,一些热带水果(如百香果、番石榴等)PFTs含量较高,添加其果汁可作为提升啤酒中PFTs含量的直接途径。上述策略整合了农业栽培技术、菌株代谢工程与酿造过程的控制,为提升啤酒中PFTs的含量提供了系统的方案。另外,在已去除酵母的啤酒中发现:前3个月内PFTs含量会呈现出上升趋势,陈酿一年后出现强烈降解,陈酿2年后的酒体中只有不到40%的游离PFTs[20]。鉴于其高反应活性,以硫醇类物质为主导香气的产品,应额外关注产品的抗氧化性能。
目前研究所揭示的由PFTs前体转化为游离态的释放机制,仅能解释啤酒中游离PFTs的一小部分来源。更多的前体物及可能涉及的生物代谢途径有待进一步探索。
[1] VERMEULEN C, COLLIN S.Synthesis and sensorial properties of mercaptoaldehydes[J].Journal of Agricultural and Food Chemistry, 2002, 50(20):5654-5659.
[2] VERMEULEN C, COLLIN S.Combinatorial synthesis and sensorial properties of 21 mercapto esters[J].Journal of Agricultural and Food Chemistry, 2003, 51(12):3618-3622.
[3] VERMEULEN C, GUYOT-DECLERCK C, COLLIN S.Combinatorial synthesis and sensorial properties of mercapto primary alcohols and analogues[J].Journal of Agricultural and Food Chemistry, 2003, 51(12):3623-3628.
[4] GROS J, NIZET S, COLLIN S.Occurrence of odorant polyfunctional thiols in the super alpha tomahawk hop cultivar.comparison with the thiol-rich nelson sauvin bitter variety[J].Journal of Agricultural and Food Chemistry, 2011, 59(16):8853-8865.
[5] STEINHAUS M, SCHIEBERLE P.Comparison of the most odor-active compounds in fresh and dried hop cones (Humulus lupulus L.variety spalter select) based on GC-olfactometry and odor dilution techniques[J].Journal of Agricultural and Food Chemistry, 2000, 48(5):1776-1783.
[6] REGLITZ K, STEINHAUS M.Quantitation of 4-methyl-4-sulfanylpentan-2-one (4MSP) in hops by a stable isotope dilution assay in combination with GC×GC-TOFMS:Method development and application to study the influence of variety, provenance, harvest year, and processing on 4MSP concentrations[J].Journal of Agricultural and Food Chemistry, 2017, 65(11):2364-2372.
[7] TAKAZUMI K, TAKOI K, KOIE K, et al.Quantitation method for polyfunctional thiols in hops (Humulus lupulus L.) and beer using specific extraction of thiols and gas chromatography-tandem mass spectrometry[J].Analytical Chemistry, 2017, 89(21):11598-11604.
[8] CHENOT C, ROBIETTE R, COLLIN S.First evidence of the glutathione S-conjugate of 3-sulfanylheptanol in green malt:Discrepancy with the ubiquitous 5- and 6-C analogues[J].Journal of the Institute of Brewing, 2022, 128(2):43-51.
[9] UEMOTO M, TAKOI K, TANIGAWA A, et al.Effect of “late harvest” of hops (Humulus lupulus L.) on the contents of volatile thiols in furano beauty, furano magical, and cascade varieties[J].Journal of Agricultural and Food Chemistry, 2022, 70(2):607-614.
[10] TOMINAGA T, PEYROT DES GACHONS C, DUBOURDIEU D.A new type of flavor precursors in Vitis vinifera L.cv.sauvignon Blanc:S-cysteine conjugates[J].Journal of Agricultural and Food Chemistry, 1998, 46(12):5215-5219.
[11] GROS J, PEETERS F, COLLIN S.Occurrence of odorant polyfunctional thiols in beers hopped with different cultivars.first evidence of an S-cysteine conjugate in hop (Humulus lupulus L.)[J].Journal of Agricultural and Food Chemistry, 2012, 60(32):7805-7816.
[12] CHENOT C, ROBIETTE R, COLLIN S.First evidence of the cysteine and glutathione conjugates of 3-sulfanylpentan-1-ol in hop (Humulus lupulus L.)[J].Journal of Agricultural and Food Chemistry, 2019, 67(14):4002-4010.
[13] ROLAND A, VIEL C, REILLON F, et al.First identification and quantification of glutathionylated and cysteinylated precursors of 3-mercaptohexan-1-ol and 4-methyl-4-mercaptopentan-2-one in hops (Humulus lupulus)[J].Flavour and Fragrance Journal, 2016, 31(6):455-463.
[14] BONNAFFOUX H, DELPECH S, RÉMOND E, et al.Revisiting the evaluation strategy of varietal thiol biogenesis[J].Food Chemistry, 2018, 268:126-133.
[15] HOLT S, CORDENTE A G, WILLIAMS S J, et al.Engineering Saccharomyces cerevisiae to release 3-mercaptohexan-1-ol during fermentation through overexpression of an S.cerevisiae gene, STR3, for improvement of wine aroma[J].Applied and Environmental Microbiology, 2011, 77(11):3626-3632.
[16] CHENOT C, COLLIN S, SUC L, et al.Unusual profile of thiol precursors in special malts:First evidence of chemical glutathione-/γGluCys- and CysGly-/cys- conversions[J].Journal of the American Society of Brewing Chemists, 2024, 82(1):15-22.
[17] CHENOT C, COLLIN S.Ability of the Mandarina Bavaria hop variety to release free odorant polyfunctional thiols in late-hopped beers[J].Journal of the Institute of Brewing, 2021, 127(2):140-148.
[18] CHENOT C, WILLEMART G, GROS J, et al.Ability of exogenous or wort endogenous enzymes to release free thiols from hop cysteinylated and glutathionylated S-conjugates[J].Journal of the American Society of Brewing Chemists, 2023, 81(1):33-44.
[19] KANKOLONGO CIBAKA M L, DECOURRI RE L, LORENZO-ALONSO C J, et al.3-sulfanyl-4-methylpentan-1-ol in dry-hopped beers:First evidence of glutathione S-conjugates in hop (Humulus lupulus L.)[J].Journal of Agricultural and Food Chemistry, 2016, 64(45):8572-8582.
RE L, LORENZO-ALONSO C J, et al.3-sulfanyl-4-methylpentan-1-ol in dry-hopped beers:First evidence of glutathione S-conjugates in hop (Humulus lupulus L.)[J].Journal of Agricultural and Food Chemistry, 2016, 64(45):8572-8582.
[20] CHENOT C, DONCK W, JANSSENS P, et al.Malt and hop as sources of thiol S-conjugates:Thiol-releasing property of lager yeast during fermentation[J].Journal of Agricultural and Food Chemistry, 2022, 70(10):3272-3279.
[21] MORIMOTO M, KISHIMOTO T, KOBAYASHI M, et al.Effects of Bordeaux mixture (copper sulfate) treatment on blackcurrant/Muscat-like odors in hops and beer[J].Journal of the American Society of Brewing Chemists, 2010, 68(1):30-33.
[22] CHRISFIELD B J, GUGINO B K, HOPFER H, et al.Effect of copper-based fungicide treatments on the quality of hop produced in the northeastern United States[J].Journal of the American Society of Brewing Chemists, 2022, 80(2):169-179.
[23] DOURNES G, SACHOT S, SUC L, et al.New light on the varietal thiols pathway during alcoholic fermentation:Role of 3- S-(N-acetyl-cysteinyl)-hexan-1-ol (NAC3SH)[J].Journal of Agricultural and Food Chemistry, 2023, 71 (9):4123-4131.
[24] CHENOT C, COLLIN S, SUC L, et al.Evidence of enzymatic and chemical interconversions of barley malt 3-sulfanylhexanol conjugates during mashing[J].Journal of Agricultural and Food Chemistry, 2023, 71(35):13107-13113.
[25] MOLITOR R W, FISCHBORN T, DAGAN L, et al.Examining how the fermentation medium influences thiol expression and its perceived aroma in commercial brewing yeast strains[J].Journal of Agricultural and Food Chemistry, 2023, 71(5):2493-2502.
[26] GROS J, TRAN T T H, COLLIN S.Enzymatic release of odourant polyfunctional thiols from cysteine conjugates in hop:Enzymatic release of hop thiols[J].Journal of the Institute of Brewing, 2013, 119(4):221-227.
[27] KISHIMOTO T, HISATSUNE Y, FUJITA A, et al.Presence of disulfide-bonded thiols in malt and hops as the precursors of thiols in beer[J].Journal of Agricultural and Food Chemistry, 2022, 70(41):13413-13418.
[28] DU EK M, JANDOVSK
EK M, JANDOVSK V.Variability in the levels of fungicide residues in final beer as they are influenced by various sequences of agrochemicals used for treatment on hops[J].Food Additives &Contaminants:Part A, 2023, 40(5):655-666.
V.Variability in the levels of fungicide residues in final beer as they are influenced by various sequences of agrochemicals used for treatment on hops[J].Food Additives &Contaminants:Part A, 2023, 40(5):655-666.
[29] GENT D H, BLOCK M, MASSIE S T, et al.Nitrogen and sulfur fertility practices:Influences on hop chemistry, aroma, and nitrate accumulation[J].Journal of the American Society of Brewing Chemists, 2024, 82(1):50-60.
[30] DEED N K, VAN VUUREN H J J, GARDNER R C.Effects of nitrogen catabolite repression and di-ammonium phosphate addition during wine fermentation by a commercial strain of S.cerevisiae[J].Applied Microbiology and Biotechnology, 2011, 89(5):1537-1549.
[31] LUND C M, NICOLAU L, GARDNER R C, et al.Effect of polyphenols on the perception of key aroma compounds from Sauvignon Blanc wine[J].Australian Journal of Grape and Wine Research, 2009, 15(1):18-26.
[32] 邵淑萍,杨朝霞,王剑锋,等.啤酒中多酚类物质研究进展[J].食品与发酵工业,2026,52(2):439-448.SHAO S P, YANG Z X, WANG J F, et al. Research progress on polyphenolic compounds in beer[J]. Food and Fermentation Industries, 2026,52(2):439-448.
[33] FORSTER A, GAHR A, SCHÜLL F, et al.The impact of climatic conditions on the biogenesis of various compounds in hops[J].Brewing Science, 2021, 74(12):160.
[34] FORSTER A, GAHR A, SCHÜLL F.The impact of diseases on the quality of hops for use in brewing beer[J].Brewing Science, 2023, 76(12):13.
[35] RUBOTTOM N, LAFONTAINE R, SHELLHAMMER H.Evaluating the impact of kilning temperature on hop quality in American deep bed dryers[J].Brewing Science, 2023, 75(11):98.
[36] RUBOTTOM L N, SHELLHAMMER T H.Evaluating the impact of high and low kilning temperatures on popular American aroma hops[J].Journal of the American Society of Brewing Chemists, 2024, 82(1):39-49.
[37] PRADO R, GASTL M, BECKER T.Influence of kilned specialty malt odorant markers on the aroma composition and sensory profile of beer[J].LWT, 2023, 173:114195.