桑叶(Morus alba L.)在我国种植历史悠久,兼具食用与药用价值。据《神农本草经》记载,桑叶甘、苦,寒。归肺、肝经,具有疏散风热,清肺润燥,平抑肝阳,清肝明目的功效[1]。现代研究通过体内外实验进一步证实了其生物活性,该作用可能源于1-脱氧野尻霉素(1-deoxynojirimycin,DNJ)等多种植物活性成分[2-3]。早在1993年,中国卫生部就将桑叶列入药食同源清单[4],为其在食品与医药领域的应用提供了重要依据。桑叶中富含丰富的对人体健康有益的生物活性成分,近年来,各国学者对桑叶开展了广泛研究。研究发现桑叶提取物包含黄酮、生物碱、植物甾醇、桑叶多糖等多种活性成分,这些成分共同作用,展现出降血压、降血脂、降血糖等多种生物活性[5-7]。其中DNJ作为从桑叶中分离得到的一种生物碱,是桑叶提取物中具有重要研究价值的成分之一,具有降血糖、降血脂、抗肥胖、降低胆固醇、抗病毒、抗炎症、抗癌症等功效。尤其值得关注的是,DNJ对α-淀粉酶、葡萄糖淀粉酶、蔗糖酶、异麦芽糖酶表现出很强的抑制潜力,能够有效的抑制餐后血糖的升高[8],这一特性使其在代谢性疾病干预领域具有重要的应用前景。
本文概述了桑叶中DNJ的提取方法,包括热提取、超声提取和微波提取等,探讨了不同提取方式对DNJ提取率的影响。桑叶中DNJ的检测主要是基于高效液相色谱(high performance liquid chromatography,HPLC),主要包括高效液相色谱-紫外检测(high performance liquid chromatography-ultraviolet absorption detector,HPLC-UV)、高效液相色谱-荧光检测(high performance liquid chromatography-fluorescence detector,HPLC-FLD)、高效液相色谱-蒸发光散射检测(high performance liquid chromatography-evaporative light-scattering detector,HPLC-ELSD)及液相色谱-串联质谱联用(liquid chromatography-tandem mass spectrometry,LC-MS/MS)、气相色谱-质谱联用(gaschromatography-mass spectrometry,GC-MS)等方法。本文亦对DNJ的功效及其机制进行了总结。本文旨在对DNJ的研究现状进行总结,探讨DNJ的最佳提取方式,测定方法以及对生物活性进行研究,为以后的研究提供一定的依据。
1 DNJ的提取
DNJ(C6H13NO4)是一种天然有机化合物,分子质量为163,分子结构式如图1所示。易溶于有机溶剂,常采用乙醇,酸,水等作为提取溶剂。DNJ的来源主要是植物和微生物,其中桑叶中DNJ含量最高。DNJ的化学合成方法复杂,产率低,难以提供大量供应。中国是桑产业大国,因此从桑叶中提取DNJ成为获取DNJ的主要方式。
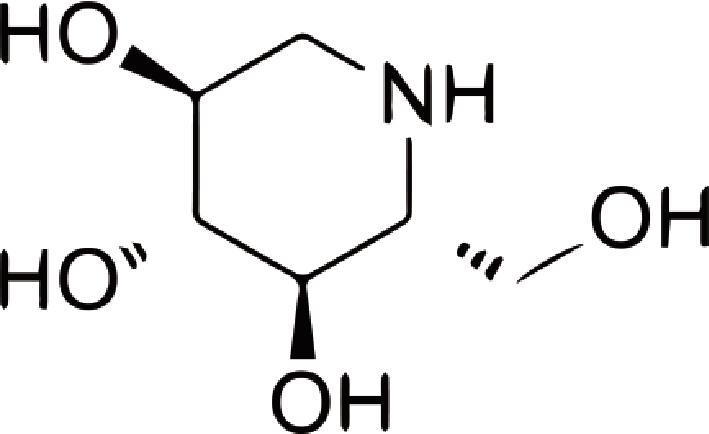
图1 DNJ结构图
Fig.1 Structure of DNJ
热萃取是传统的提取方式,该方法是通过加热从样品中提取目标成分。该方法萃取时间较长,萃取选择性较差。但因其萃取方式简单也得到广泛应用。超声辅助提取是利用超声产生的振动,粉碎,搅拌提取产物中的有效成分。与热萃取相比,该方法具有提取时间短、效率高、操作简便、提取液杂质少及目标成分易于分离纯化等优势。热萃取及超声辅助萃取为最常用的2种方法,其提取方法如表1、表2所示。
表1 热萃取方法
Table 1 Hot extraction method

提取温度/℃时间/h提取次数提取液料液比(g/mL)提取率文献79.21.461乙醇1∶9.8231.62 mg/g[9]801.2155%(体积分数)乙醇1∶122.56 mg/g[10]701250%(体积分数)乙醇-0.05 mol/L盐酸1∶60.59%[11]5521水1∶1001.48%[12]
表2 超声辅助萃取方法
Table 2 Ultrasonic assisted extraction methods

超声功率/W时间提取次数提取液料液比(g/mL)提取率文献15010 min265%(体积分数)乙醇1∶1501.069%[13]180260 s1乙醇7 mL/g0.8%[14]12520 min1—1∶400.091%[15]—20 min1氯化胆碱甘油和水1∶111 g/mL0.822 mg/g[16]
注:—表示该数据未见于相关文献(下同)。
回流提取是利用挥发性有机溶剂(如乙醇)从原料中提取活性成分的过程,操作简单,乙醇作为溶剂选择性溶解性好,可以高效提取目标物质。回流操作可以保持温度稳定,提高提取效率。提取过程中可以分离杂质,提高目标物的纯度。但是回流提取相对于超声辅助提取时间较长。陈博伦[17]采用回流法从桑叶中提取DNJ,系统考察了乙醇体积分数、回流温度和回流时间对DNJ得率的影响,并通过响应面法与多因素组合分析确定了最佳提取条件。研究发现,当回流温度为81 ℃、回流时间为1.7 h、乙醇体积分数为63%,料液比为1∶10(g∶mL)时,提取液中DNJ质量浓度可达35.6 mg/L,为最优提取工艺参数组合。
微波萃取是在微波反应器中利用适宜溶剂从原料中提取化学成分的过程。可提高萃取效率和产品纯度。与传统提取方法相比,微波萃取其有无可比拟的优势,选择性高、产率高、提取物纯度高、快速高效,节能,节省溶剂,污染小,质量稳定。LIU等[18]采用微波辅助法从桑叶中提取DNJ,并通过响应面优化获得最高得率。以水为提取溶剂,料液比为1∶80(g∶mL),当微波功率为600 W、处理时间为11.41 min时,DNJ提取率可达0.19%,为最优提取条件。
超临界流体萃取以处于温度和压力均高于其临界点的热力学状态的流体作为萃取剂,通过从液体或固体中提取特定组分以实现分离目的,利用超临界流体的溶解力和扩散速度较高的特点,对原料中的有用成分进行高效、温和、环保地提取。RAMYA等[19]采用超临界流体萃取法从桑叶中提取DNJ,以CO2为主要萃取剂、乙醇为共溶剂,确定最佳萃取条件为压力200 bar、温度50 ℃、萃取时间80 min,最终萃取率达13.41%。
DNJ的提取方式主要还是集中在热萃取以及超声辅助萃取上,热萃取提取时间较长,超声辅助萃取效率更高,回流萃取提取率相对较高,但是时间较长,微波萃取时间短,效率高,超临界流体萃取的方式更加环保,但是也比较耗费时间,表3将不同提取方法进行对比。结合上述内容,超声辅助萃取能够缩短提取时间,有较高的提取效率且设备成本较低易获得。
表3 不同提取方法对比
Table 3 Comparison of different extraction methods
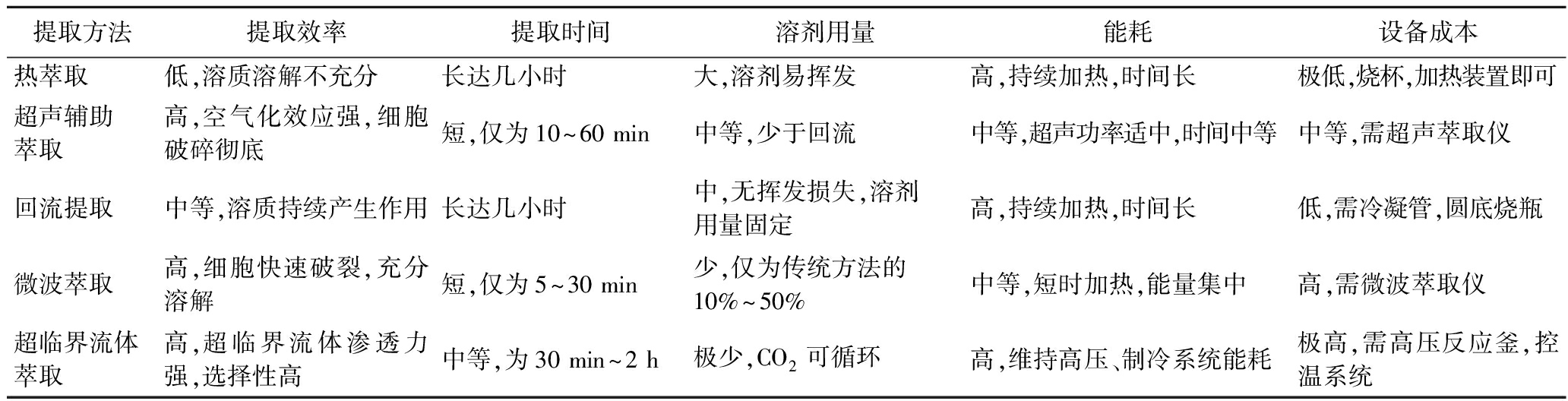
提取方法提取效率提取时间溶剂用量能耗设备成本热萃取低,溶质溶解不充分长达几小时大,溶剂易挥发高,持续加热,时间长极低,烧杯,加热装置即可超声辅助萃取高,空气化效应强,细胞破碎彻底短,仅为10~60 min中等,少于回流中等,超声功率适中,时间中等中等,需超声萃取仪回流提取中等,溶质持续产生作用长达几小时中,无挥发损失,溶剂用量固定高,持续加热,时间长低,需冷凝管,圆底烧瓶微波萃取高,细胞快速破裂,充分溶解短,仅为5~30 min少,仅为传统方法的10%~50%中等,短时加热,能量集中高,需微波萃取仪超临界流体萃取高,超临界流体渗透力强,选择性高中等,为30 min~2 h极少,CO2可循环高,维持高压、制冷系统能耗极高,需高压反应釜,控温系统
2 DNJ的测定
目前DNJ不仅在桑叶中发现,风信子、鸭拓草等植物,链霉菌,芽孢杆菌等细菌中也可分离出DNJ。2021年我国出版国标正式规定了桑叶提取物中DNJ的检测方法。目前对于DNJ的检测主要还是利用高效液相色谱法。
紫外吸收检测器(ultraviolet absorption detector,UV)是目前HPLC应用最广泛的检测器,灵敏度高,线性范围宽,紫外吸收检测要求待测样品有紫外-可见光吸收。由于DNJ不含生色团,因此使用紫外检测器测定时需要进行柱前衍生,氯甲酸9-芴甲基酯(9-fluorenylmethyl choroformate,FMOC-CL)作为衍生化试剂可以对DNJ进行衍生,衍生后的反应物有较强的紫外吸收,从而可以对DNJ含量进行检测。荧光检测器(fluorescence detector,FLD)是一种高灵敏度、高选择性的检测工具,适用于荧光化合物的检测,其灵敏度虽高于紫外检测器,但线性范围较窄,故常用于痕量分析。蒸发光散射检测器(evaporative light-scattering detector,ELSD)适用于检测挥发性低于流动相的组分,主要用于检测糖类、高级脂肪酸、磷脂、维生素、氨基酸、甘油三酯及甾体等,具有较好的通用型,但是其灵敏度比较低,尤其是有紫外吸收的组分。HPLC包括HPLC-FLD、HPLC-UV、HPLC-ELSD等检测器广泛应用于DNJ的检测。随着技术的发展,GC-MS联用,液相色谱-质谱联用(liquid chromatograph mass spectrometer,LC-MS)以及实时直接分析质谱(direct analysis in real time mass spectrometry,DART-MS)也被用于DNJ的定性分析以及定量检测。这些方法都具有其各自的优势,在DNJ检测中发挥重大作用。表4列举了DNJ的不同检测方法。
表4 DNJ检测方法
Table 4 DNJ detection methods
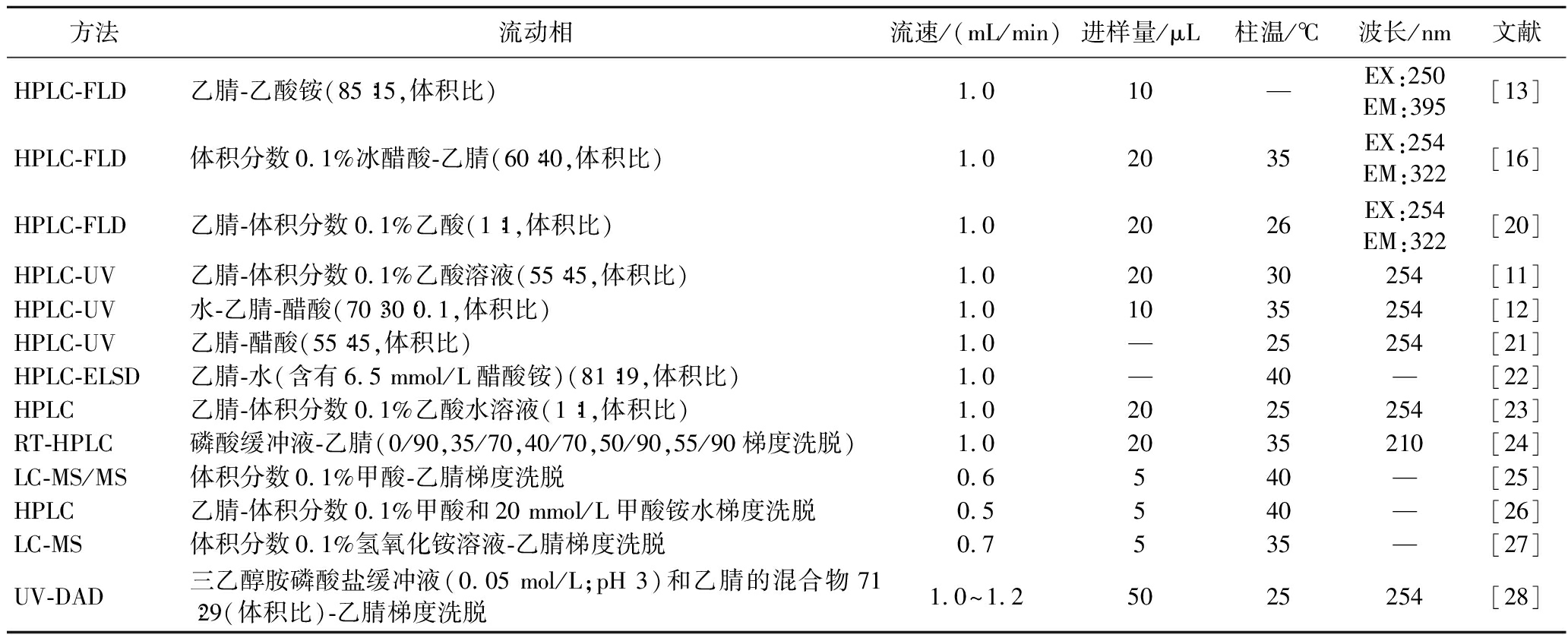
方法流动相流速/(mL/min)进样量/μL柱温/℃波长/nm文献HPLC-FLD乙腈-乙酸铵(85∶15,体积比)1.010—EX:250EM:395[13]HPLC-FLD体积分数0.1%冰醋酸-乙腈(60∶40,体积比)1.02035EX:254EM:322[16]HPLC-FLD乙腈-体积分数0.1%乙酸(1∶1,体积比)1.02026EX:254EM:322[20]HPLC-UV乙腈-体积分数0.1%乙酸溶液(55∶45,体积比)1.02030254[11]HPLC-UV水-乙腈-醋酸(70∶30∶0.1,体积比)1.01035254[12]HPLC-UV乙腈-醋酸(55∶45,体积比)1.0—25254[21]HPLC-ELSD乙腈-水(含有6.5 mmol/L醋酸铵)(81∶19,体积比)1.0—40—[22]HPLC乙腈-体积分数0.1%乙酸水溶液(1∶1,体积比)1.02025254[23]RT-HPLC磷酸缓冲液-乙腈(0/90,35/70,40/70,50/90,55/90梯度洗脱)1.02035210[24]LC-MS/MS体积分数0.1%甲酸-乙腈梯度洗脱0.6540—[25]HPLC乙腈-体积分数0.1%甲酸和20 mmol/L甲酸铵水梯度洗脱0.5540—[26]LC-MS体积分数0.1%氢氧化铵溶液-乙腈梯度洗脱0.7535—[27]UV-DAD三乙醇胺磷酸盐缓冲液(0.05 mol/L;pH 3)和乙腈的混合物71∶29(体积比)-乙腈梯度洗脱1.0~1.25025254[28]
表5列举了DNJ检测方法的对比。综合来看,LC-MS是检测DNJ较为优质的方法。在适用性方面,DNJ作为一种热稳定性较差的高极性生物碱,无需依赖样品的挥发性或热稳定性,即可通过LC-MS很好地适应其理化性质,可以检测各种形式的DNJ。在性能方面,LC-MS结合了液相色谱的强大分离能力与质谱的精确定性和定量优势。它具有极高的灵敏度,可以准确检测痕量的DNJ。LC-MS具有较强的定性能力,可以通过质谱提供的结构信息保证检测的特异性,有效避免其他组分的干扰。虽然LC-MS仪器相对昂贵,但考虑到其准确度高、适用性广、对复杂基质样品(如桑叶提取物和生物样品)检测DNJ有良好的处理能力,因此在DNJ测定中是更优的选择。
表5 检测方法对比
Table 5 Comparison of testing methods

检测方法原理优点缺点HPLC-UV基于待测物质紫外-可见光的吸收特性进行检测灵敏度高,线性范围宽,应用最广泛要求样品有紫外-可见光吸收,DNJ不含生色团,需要柱前衍生HPLC-FLD利用物质的荧光特性,通过检测荧光强度进行定量高灵敏度、高选择性,灵敏度高于紫外检测器线性范围较窄,仅适用于荧光化合物HPLC-ELSD检测挥发性低于流动相的组分,基于溶质颗粒对光的散射作用通用性较好灵敏度较低,尤其对于有紫外吸收的组分HPLC-PAD通过同时检测不同波长下的吸收值,获得物质的紫外光谱图可提供丰富的光谱信息,有助于定性分析灵敏度受限,低浓度样品信号弱GC-MS利用气相色谱分离组分,质谱进行定性和定量定性能力强,可提供化合物结构信息对样品挥发性和热稳定性要求高LC-MS液相色谱分离与质谱检测结合灵敏度高,定性定量准确,适用性广仪器成本较高DART-MS无需样品前处理,直接对样品进行离子化检测快速、无需复杂前处理可能存在基质干扰
3 DNJ生物活性及作用机制
3.1 降糖活性
目前,糖尿病已成为全球性的问题,其中2型糖尿病是最普遍的一种类型。2型糖尿病是通常是由于胰岛素抵抗或胰岛素分泌不足引起的[29]。目前治疗糖尿病的药物都有一定的副作用,导致体重增加、乳酸升高以及患心血管风险等问题[30],现如今已经发现许多降血糖作用的天然物质,包括黄酮类、多糖类、生物碱类等能起到有效的降糖作用。DNJ具有降糖作用,能够显著延缓多糖降解过程,可降低餐后血糖的峰值,稳定空腹血糖。并且DNJ还能够改善胰岛素抵抗。DNJ的降糖途径是通过多靶点、多途径实现的。在糖类代谢过程中,DNJ能够显著延缓多糖降解过程,这是其控制血糖的重要途径之一。食物中的多糖需经消化酶分解为单糖,然后才能被人体吸收,进而导致血糖升高。DNJ能够与相关糖苷酶结合,抑制这些酶的活性,减缓多糖分解为单糖的速度,从而降低餐后血糖的峰值,避免短时间内血糖急剧上升。
胰岛素抵抗是2型糖尿病的重要发病机制之一,DNJ在改善胰岛素抵抗方面发挥着关键作用。图2展示了胰岛素抵抗机制。REN等[31]探讨了DNJ对高脂和链脲佐菌素诱导的糖尿病前期小鼠的药用效果,对小鼠进行口服葡萄糖耐量实验以及胰岛素耐量实验,连续治疗10周。结果表明DNJ降低了糖尿病前期小鼠的血糖水平并改善了胰岛素敏感性。DNJ能够抑制NF-kB通路活性,降低TNF-α和IL-6的循环,TNF-α和IL-6等炎症因子可干扰胰岛素信号传导通路,引发胰岛素抵抗。DNJ降低这些炎症因子水平,从而抑制SCOS3的表达和TLR4/NF-κB信号通路,同时提高occludin的表达和p-IRS1(Tyr896)/IRS1值,以此来改善胰岛素抵抗。使机体对胰岛素的敏感性增强,更好地发挥胰岛素调节血糖的作用,稳定空腹血糖水平。
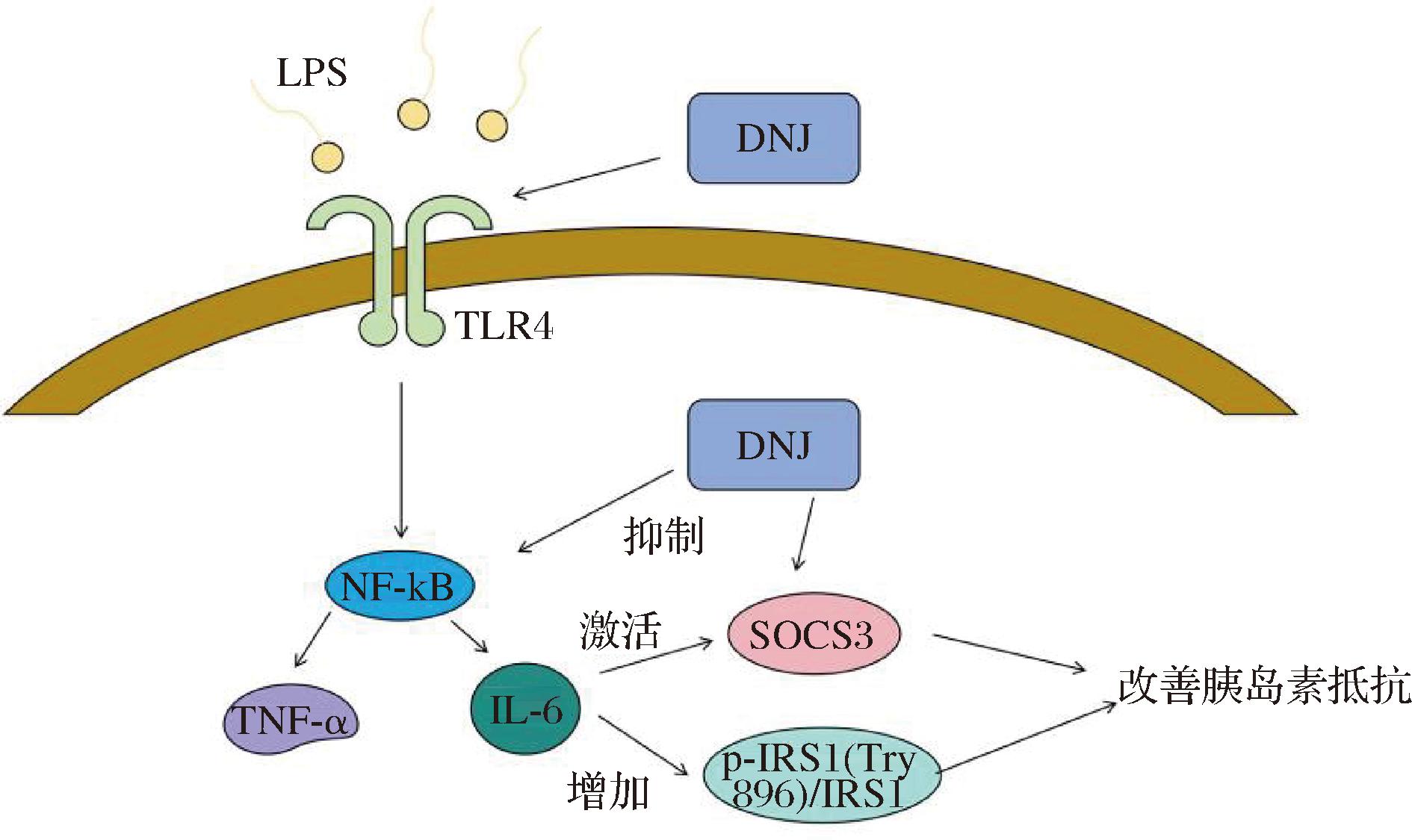
图2 DNJ改善胰岛素抵抗机制
Fig.2 Mechanism of DNJ improving insulin resistance
注:LPS:脂多糖(lipopolysaccharide);TLR4:Toll样受体4(Toll-like receptor 4);SOCS3:细胞信号转导抑制因子3(suppressor of cytokine signaling 3);IRS1:胰岛素受体底物(insulin receptor substrate);occludin:膜整合蛋白。
此外,DNJ对胰腺β细胞功能的调节也与其降糖作用密切相关。胰腺β细胞负责分泌胰岛素,高糖环境会导致胰腺β细胞功能障碍,影响胰岛素的正常分泌。LI等[32]探讨DNJ对β细胞影响的分子机制。DNJ处理显著恢复了高糖诱导的大鼠胰岛素瘤细胞(rat islet cell tumor cells,INS-1)功能障碍,DNJ对正常INS-1细胞无毒性。能够促进CCAAT /增强子结合蛋白α(CCAAT/enhancer binding protein alpha,CEBPA)蛋白表达,而CEBPA蛋白的过表达能够缓解高糖诱导的胰腺β细胞功能障碍。DNJ的治疗恢复了部分CEBPA引起的胰腺β细胞功能障碍。总之,DNJ可以通过促进CEBPA的表达来抑制高葡萄糖诱导的胰腺β细胞功能障碍,使得胰腺β细胞能够正常分泌胰岛素,从而降低血糖水平。TAKASU等[33]研究了氮杂糖在大鼠体内的吸收和器官分布情况,将大鼠分为3组,给予等摩尔量的DNJ,荞麦碱和2-O-α-d-galactopyranosyl-1-deoxynojirimycin(Gal-DNJ),在给药后240 min内从尾静脉阶段采血。对DNJ的药代动力学进行了研究,图3为DNJ在体内转运途径。DNJ在血浆中浓度最高,研究发现钠-葡萄糖共转运体(sodium-dependent glucose cotransporters,SGLT)介导了DNJ从肠道到血液的转运,以及SGLT和葡萄糖转运体(glucose transporter,GLUT)都参与了肝脏对DNJ的吸收。
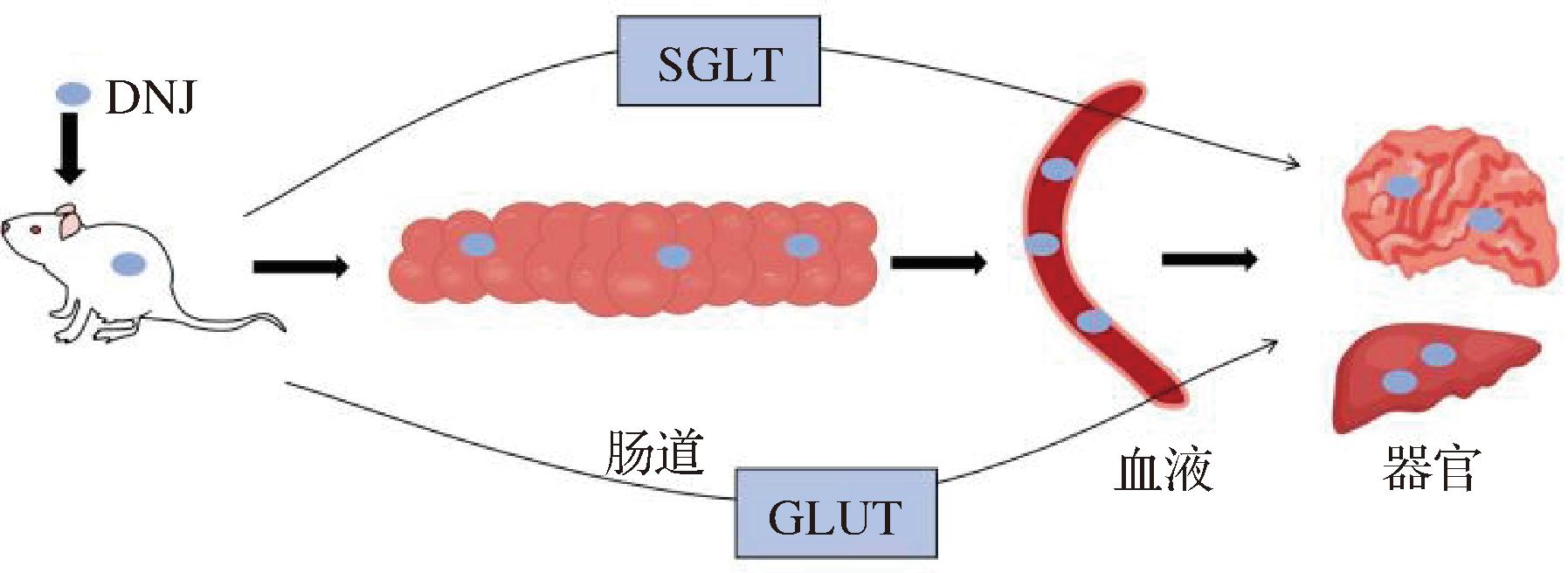
图3 体内DNJ转运途径
Fig.3 DNJ transport pathway in vivo
在降糖方面,多篇文献证实DNJ可以通过抑制α-葡萄糖苷酶活性延缓多糖降解;改善胰岛素抵抗,可通过抑制NF-κB通路、上调p-IRS1胰岛素传导信号;保护胰腺β细胞,促进CEBPA蛋白表达,进而缓解高糖诱导的胰腺β细胞功能障碍,维持胰岛素的正常分泌功能。目前,这些降糖机制均已通过细胞实验和动物模型验证,但仍存在一些问题。如不同研究中,DNJ的有效剂量差异较大,且与其他降糖药物的协同作用及其可能存在的相互影响作用尚不明确。未来将深入探究DNJ与其他活性成分的降糖协同作用,进一步挖掘DNJ在长期使用过程中的安全性及其对糖尿病并发症的预防作用。
3.2 抗肥胖
肥胖是世界上严重的健康挑战,摄入的热量过多会导致肥胖。肥胖症还会引发其他相关疾病比如糖尿病,高血压,高胆固醇等疾病。DNJ作为桑叶提取物,具有抗肥胖作用,能够增加肝脏对脂质的代谢以及控制体重[34]。DNJ可以减少正常大鼠的氧化应激和脂质过氧化,因此可以改善肥胖引起的不良反应[35]。
TSUDUKI等[35]对肥胖小鼠施用了桑叶DNJ,12周后降低了内脏脂肪重量和脂肪细胞大小。其作用机制是DNJ能够激活β氧化系统,抑制肝脏中的脂质积累并减少血浆三酰基甘油。β氧化系统的激活因子是脂联素,并且血浆脂联素随DNJ施用而升高。因此,DNJ通过增加脂联素来预防饮食引起的肥胖。
脂肪组织有3种分别为白色、棕色和米色脂肪组织。白色脂肪组织主要负责能量储存,白色脂肪细胞的分化和脂质代谢异常是肥胖的最直接原因[36]。棕色脂肪和米色脂肪是产热脂肪,可以通过促进解偶联呼吸来消耗能量,从而导致热量产生和体重减轻[37]。棕色脂肪ATP产生速率低且额外的能量不能以ATP的形式储存,以热量形式消散。而米色脂肪是啮齿动物的主要产热脂肪组织,因此,促进米色脂肪的形成是减轻体重的重要途径。
LI等[38]研究了DNJ对3T3-L1前脂肪细胞米色重塑的影响。结果发现DNJ能抑制白色前脂肪细胞分化过程中的脂肪生成,显著降低了AP2转录因子、PPARγ和Pref-1与脂肪生成相关转录因子的的表达,同时上调了UCP1、PRDM16和TMEM26等促进米色脂肪细胞形成的蛋白的表达,降低了脂质沉积。这些结果表明,DNJ可以抑制白色前脂肪细胞分化过程中的脂肪生成,并通过激活AMPK促进白色前脂肪细胞向米色脂肪细胞的转换,从而减轻体重以及抑制肥胖相关的病症。REN等[39]研究显示,低剂量DNJ和桑色素的联合应用不仅能通过抑制SOCS3表达、促进PPARγ和SOCS2表达增强改善胰岛素抵抗的功效,并且联合用药中的DNJ成分通过抑制CD36/Srebp1/Fas信号传导减少了脂肪生成。
DNJ通过多靶点,多途径在抗肥胖及相关代谢疾病干预中展现出显著效果。动物实验和细胞实验均证实,DNJ可以通过激活脂质β氧化系统;调控脂肪细胞表型转换以及协同增效减少脂肪生成,有效改善肥胖,预防和缓解肥胖及其相关健康问题。
3.3 抑制高血脂症
高血脂症是指血液中脂质水平异常升高的代谢疾病。可造成动脉粥硬化、冠心病等心血管疾病的风险。DNJ可以通过多种途径进行脂质调节。一方面,DNJ可以抑制肠道内脂肪吸收相关的关键酶活性或竞争性结合脂肪转运蛋白,减少肠道对甘油三酯和胆固醇的摄取和吸收,导致甘油三酯及胆固醇含量下降。另一方面,DNJ能够影响肝脏中脂质代谢酶相关活性,从而抑制内源性胆固醇合成,从源头上降低脂质在体内的蓄积。
LI等[40]通过构建高脂饮食(high-fat diet,HFD)诱导的小鼠模型,深入探究了DNJ在脂质代谢调节中的特异性作用。研究结果表明,DNJ能够特异性的预防HFD诱导的高胆固醇血症,并且发现具有性别特异性,能明显抑制HFD诱导的雌性小鼠的体重增加,降低血清胆固醇。同时DNJ能够显著改变雌性小鼠肠道微生物菌群结构。肠道微生物群有助于脂质代谢的性别特异性调节。DNJ能够增加相关具有缓解肥胖和糖尿病作用的有益菌属。此外,桑叶衍生的绿茶和红茶也具有降血脂的作用。ZHONG等[41]揭示了桑叶红茶,桑叶绿茶对HFD诱导的小鼠的降血脂作用,并且绿茶比红茶的降脂作用更优越。综上所述,DNJ通过多途径调节脂质代谢,其性别特异性和对肠道菌群的调节作用在预防高脂饮食诱导的高胆固醇血症方面为理解脂质代谢的复杂机制提供了新的视角。桑叶衍生茶的降脂作用也进一步拓展了DNJ和桑叶活性成分在代谢性疾病干预中的应用前景。
基于现有研究,DNJ通过调节脂质代谢,调节肠道菌群改善代谢环境,从而发挥显著的脂质调节作用。未来我们可以评估DNJ对高血脂症患者血清脂质指标的影响,明确安全剂量范围及适用人群,为临床应用提供依据。
3.4 心肌病
心肌病是由不同病因引起的心脏机械和电活动异常,表现为心室不当的肥厚或扩张。严重心肌病会引发心血管性死亡或进展性心力衰竭。心肌病的发生与很多因素有关,长期高血压、心力衰竭、心脏病、肥胖症、长期酗酒等都会增加患心肌病的风险[42-43]。
肥厚型心肌病(hypertrophic cardiomyopathy,HCM)一种常见的遗传性心肌病,是年轻人心源性猝死的主要原因,肥厚型心肌病会导致心肌异常增厚,从而使心脏更难正常工作。ZHUANG等[44]之前的研究为了解HCM的发病机制及寻找潜在治疗靶点提供了重要线索,他们表明HCM相关的变体导致线粒体功能障碍,DNJ通过靶向视萎缩蛋白1(optic atrophy type 1,OPA1)促进其寡聚化。OPA1的寡聚化状态对维持线粒体嵴的结构完整性和功能稳定性起着关键作用,DNJ通过促进其寡聚化,可有效推动线粒体嵴的重建,从而挽救受损的线粒体功能,为心肌细胞提供充足的能量支持。因此DNJ是线粒体肥厚型心肌病的潜在线粒体挽救剂。
脓毒性心肌病是脓毒症引起的心脏可逆性的功能障碍,病死率高,是导致脓毒症患者死亡的重要原因。JIANG等[45]针对DNJ介导脓毒性心肌病的生物活性机制开展了深入研究。研究发现,DNJ能够通过精准调节JAK2/STAT6信号通路来发挥作用。DNJ通过调节这一信号通路,可显著减少心肌细胞所遭受的氧化损伤,降低心肌细胞凋亡的发生率,同时减轻心肌组织的炎症反应,从多个方面缓解败血症诱导的心肌损伤,为脓毒性心肌病的治疗提供了新的思路和实验依据。
综上所述,DNJ在2种常见的心肌病中均展现出一定的治疗潜力,其针对不同类型心肌病的独特作用机制,为心肌病的精准治疗和新药研发奠定了重要的理论基础。
3.5 糖尿病心血管并发症
我国糖尿病患病率逐年增加,糖尿病患者心血管疾病的发病率和死亡率高,心血管疾病是T2DM患者的主要致死和致残病因。桑叶提取物主要包括DNJ,绿原酸,白藜芦醇,东莨若碱和黄氏甲苷。CAO等[46]研究桑叶提取物以及DNJ对小鼠的治疗效果。结果显示,桑叶提取物和DNJ能够显著改善心脏的功能,减少心肌纤维化。此外,DNJ还可降低活性氧和氧化应激水平,抑制TGF-β通路,阻止了α-SMA和Smad2/3以及胶原蛋白1和3的表达。DNJ作为桑叶提取物的主要活性成分,可保护糖尿病心肌并调节TGF β-Smad2/3通路。冠心病会导致血管狭窄或阻塞[47],动脉粥样硬化是导致冠心病的主要原因。DNJ能够减轻冠心病患者的动脉粥样硬化病变[48],改善心脏病患者的抗氧化和抗炎症特性以及血清脂质水平,且可以减少冠心病患者的一些副作用。DNJ作为α-葡萄糖苷酶抑制剂,可以降低餐后血糖,高血糖是导致脑血管心血管疾病的重要原因,DNJ通过对血糖进行控制从而减少心血管并发症的发生。
3.6 减轻肝损伤
肝损伤是指肝脏受到物理、病毒或化学等因素的损害,导致肝细胞变性或坏死,可引发肝硬化或肝癌等疾病。我国肝损伤发生率高于欧美国家,已成为不可忽视的问题。
非酒精性脂肪肝炎(non-alcoholic steatohepatitis,NASH)好发于超重肥胖类人群,非酒精性脂肪肝炎与肥胖、胰岛素抵抗、2型糖尿病、高血脂等代谢紊乱密切相关。ZHENG等[49]研究发现,DNJ可以调节肠道菌群失调来改善HFD诱导的小鼠NASH,通过小鼠实验结果表明,DNJ能显著调节HFD诱导的小鼠的葡萄糖耐受不良和高脂血症,减轻肝脂肪变性和全身性慢性炎症。
急性肝损伤是由于药物中毒、病毒感染、酒精摄入过多、免疫反应、放射性损伤等不同诱因造成的肝脏急性炎症性疾病,似肝细胞受到破坏,肝功能受损。YU等[50]探讨了桑叶提取物对D-半乳糖胺/脂多糖诱导的大鼠急性肝损伤的保肝作用。桑叶提取物主要包括DNJ,酚类化合物以及多糖。结果表明桑叶提取物表现出高抗氧化活性,并能够显著抑制细胞凋亡相关点样蛋白和Caspase-1的表达,抑制p38 MAPK和ERK1/2的磷酸化,具有较高的抗炎活性。通过减少氧化应激和炎症反应来保护大鼠以避免急性肝损伤。
3.7 抗氧化
氧化应激是机体应激遭受各种刺激时,体内氧化与抗氧化系统失衡,导致活性氧产生过多或者机体抗氧化能力不足,从而引起细胞和组织损伤的病理过程。桑叶DNJ在抗氧化能力方面具有显著功效。侯文玉等[51]研究了桑叶DNJ对肉兔抗氧化能力的影响,在基础饲料中添加一定量的DNJ,可以提高血清中的谷胱甘肽含量和超氧化物歧化酶活性,显著降低丙二醛含量。谷胱甘肽与谷胱甘肽过氧化物酶协同作用,能够清除自由基和过氧化物,保护细胞免受氧化损伤。DNJ可以显著提高血清谷胱甘肽过氧化物酶活性,对新西兰白兔的血清抗氧化能力有改善作用。此外桑叶DNJ由于其强大的抗氧化和抗炎活性,能够减轻冠心病患者的稳定型心绞痛。JIANG等[45]也证明了DNJ给药可抑制脓毒性心肌病中的心肌氧化应激、炎症和心肌细胞凋亡。
3.8 抗病毒
树突状细胞是登革病毒感染的关键靶细胞。研究表明,源于DNJ的亚氨基糖可通过抑制α- 葡萄糖苷酶Ⅱ,在登革病毒感染中诱导抗病毒活性。这些亚氨基糖已被证实可在未成熟树突状细胞中发挥抗病毒效应,以剂量依赖性方式抑制登革病毒感染的未成熟树突状细胞的病毒分泌[52]。
严重急性呼吸系统综合征冠状病毒2对人类健康构成重大挑战,DNJ可能对其具有抑制作用。MIGLANI等[53]研究了DNJ对严重急性呼吸系统综合征冠状病毒2关键蛋白酶的抑制作用。通过计算机模拟,基于分子力学技术的分子对接被用于筛选最佳对接抑制剂。研究发现,所获得的衍生物能够抑制严重急性呼吸系统综合征冠状病毒2的蛋白酶,表明DNJ可能通过抑制酶活性产生抗病毒作用。
DNJ表现出减轻心肌病、糖尿病心血管并发症和肝损伤的作用。在心肌病干预中,HCM侧重于线粒体功能修复,而脓毒性心肌病侧重于炎症与氧化应激抑制。预防和治疗糖尿病心血管并发症能保护心脏及调节新陈代谢。对肝损伤的保护依赖于肠道菌群调节与抗氧化抗炎协同作用。DNJ的抗氧化和抗炎活性是保护心脏与肝脏的共同基础,显示出对“炎症-氧化应激”网络的普遍调控力。因此DNJ在多系统疾病中的保护作用展现出广阔应用前景。
4 总结与展望
近年来,对桑叶的研究主要集中在DNJ、多糖和蛋白质等活性成分上。其中,DNJ作为关键的生物活性物质,在提取技术、定量分析、生物功效等领域引起了广泛关注。本文系统综述了DNJ的提取技术、测定方法和生物学功效的研究进展。DNJ萃取方法既涵盖传统的溶剂萃取方法(如乙醇萃取、盐酸萃取)也有新型辅助萃取技术(如超声辅助萃取、微波辅助萃取、超临界流体萃取等)。传统方法简单,但存在萃取周期长、效率低等缺点;尽管新的辅助技术可以显著提高提取率和产量,但它们面临着设备成本高和工业应用受限等问题。在定量分析领域,高效液相色谱法因其灵敏度高、分离度高、重现性好等优点,已成为DNJ含量测定的主流方法,为其质量控制和标准化研究提供了可靠的技术支持。在生物学功能研究中,DNJ表现出优异的降血糖活性,研究表明它可以通过延缓多糖降解、改善胰岛素抵抗、调节胰腺β细胞功能等多靶点机制发挥降血糖作用。此外,DNJ在调节脂质代谢、抑制高脂血症、干预肥胖进展和对抗病毒感染方面显示出显着的潜力,为糖尿病防治提供了理论基础。
然而,当前DNJ的提取方法仍存在提取时间长、效率低等局限性,因此需要开发更高效的提取方法以提高DNJ的得率和纯度。DNJ在食品、医药和保健品领域已有一定的研究,但在其他领域仍有很大的拓展空间。值得注意的是,现有DNJ功效研究仍局限于动物和细胞模型,缺乏人体实验数据。此外,深入研究DNJ的作用机制将为其应用奠定更坚实的科学基础。综上所述,DNJ是一种具有多元研究方向和应用潜力的天然化合物,深入挖掘其潜在价值将推动其在未来的广泛应用。
[1] 王梓欢, 田刚, 王莉, 等.桑叶活性成分的含量及其提取工艺研究进展[J].山东化工, 2020, 49(12):42-43; 45.WANG Z H, TIAN G, WANG L, et al.Research progress on the content of active components in mulberry leaves and its extraction technology[J].Shandong Chemical Industry, 2020, 49(12):42-43; 45.
[2] REN X X, XING Y, HE L Y, et al.Effect of 1-Deoxynojirimycin on insulin resistance in prediabetic mice based on next-generation sequencing and intestinal microbiota study[J].Journal of Ethnopharmacology, 2022, 289:115029.
[3] TANG C, BAO T T, ZHANG Q Q, et al.Clinical potential and mechanistic insights of mulberry (Morus alba L.) leaves in managing type 2 diabetes mellitus:Focusing on gut microbiota, inflammation, and metabolism[J].Journal of Ethnopharmacology, 2023, 306:116143.
[4] CHEN R H, ZHOU X, DENG Q F, et al.Extraction, structural characterization and biological activities of polysaccharides from mulberry leaves:A review[J].International Journal of Biological Macromolecules, 2024, 257:128669.
[5] MA G Q, CHAI X Y, HOU G G, et al.Phytochemistry, bioactivities and future prospects of mulberry leaves:A review[J].Food Chemistry, 2022, 372:131335.
[6] LI Y G, XU W Y, ZHANG F, et al.The gut microbiota-produced indole-3-propionic acid confers the antihyperlipidemic effect of mulberry-derived 1-deoxynojirimycin[J].mSystems, 2020, 5(5):e00313-e00320.
[7] DO H J, CHUNG J H, HWANG J W, et al.1-deoxynojirimycin isolated from Bacillus subtilis improves hepatic lipid metabolism and mitochondrial function in high-fat-fed mice[J].Food and Chemical Toxicology, 2015, 75:1-7.
[8] QIAO Y, ITO M, KIMURA T, et al.Inhibitory effect of Morus australis leaf extract and its component iminosugars on intestinal carbohydrate-digesting enzymes[J].Journal of Bioscience and Bioengineering, 2021, 132(3):226-233.
[9] TIAN G, YIN X F, PENG X M, et al.Response surface methodology optimized pilot plant extraction process of 1-deoxynojirimycin from mulberry leaves[J].Journal of Biobased Materials and Bioenergy, 2019, 13(2):207-213.
[10] WANG T, LI C Q, ZHANG H, et al.Response surface optimized extraction of 1-deoxynojirimycin from mulberry leaves (Morus alba L.) and preparative separation with resins[J].Molecules, 2014, 19(6):7040-7056.
[11] 吕志强, 李乔, 闫海龙, 等.正交实验优选桑籽中1-脱氧野尻霉素的提取工艺[J].中国当代医药, 2022, 29(4):45-49.LYU Z Q, LI Q, YAN H L, et al.Optimization of extraction technology of 1-deoxynojirimycin from mulberry seeds by orthogonal test[J].China Modern Medicine, 2022, 29(4):45-49.
[12] 冉晓燕, 何军.树脂富集桑皮中1-脱氧野尻霉素的工艺研究[J].贵州师范学院学报, 2013, 29(12):19-23.RAN X Y, HE J.Study on the enrichment of 1-Deoxynojirimycin from cortex Mori with resin column chromatography[J].Journal of Guizhou Normal College, 2013, 29(12):19-23.
[13] 伊丽则热·艾拜杜拉, 陈冰婷, 李德龙, 等.药桑不同部位中1-脱氧野尻霉素的提取工艺优化及含量测定分析[J].安徽农业科学, 2021, 49(11):178-181;204.ABAYDULA Yilzera, CHEN B T.LI D L, et al.Optimization of extraction technology and determination of 1-deoxynotahirymycin in different parts of mulberry[J].Journal of Anhui Agricultural Sciences, 2021, 49(11):178-181;204.
[14] VICHASILP C, NAKAGAWA K, SOOKWONG P, et al.Optimization of 1-deoxynojirimycin extraction from mulberry leaves by using response surface methodology[J].Bioscience, Biotechnology, and Biochemistry, 2009, 73(12):2684-2689.
[15] 花俊丽, 刘树兴, 陈素娟.超声波法提取1-脱氧野尻霉素[J].食品与生物技术学报, 2009, 28(6):845-849.HUA J L, LIU S X, CHEN S J.Study on ultrasonic extraction of 1-deoxynojirimycin (DNJ) from mulberry leaves[J].Journal of Food Science and Biotechnology, 2009, 28(6):845-849.
[16] 杨莉, 周鹏程, 白春莉, 等.桑枝皮中1-脱氧野尻霉素低共熔溶剂提取工艺研究[J].食品科技, 2025, 50(4):231-239.YANG L, ZHOU P C, BAI C L, et al.Research on the extraction technology of 1-deoxynojirimycin in mulberry bark with deep eutectic solvent[J].Food Science and Technology, 2025, 50(4):231-239.
[17] 陈博伦. 桑叶1-DNJ提取工艺优化及工艺过程安全评价[D].北京:北京石油化工学院, 2021.CHEN B L.Optimization of the pilot extractionprocess and process safety evaluationofmulberry leaf 1-DNJ[D].Beijing:Beijing Institute of Petrochemical Technology, 2021.
[18] LIU C, WANG C H, LIU J, et al.Optimization of microwave-assisted technology for extracting 1-deoxynojirimycin from mulberry tea by response surface methodology[J].Food Science and Technology Research, 2014, 20(3):599-605.
[19] RAMYA V, NIDONI U, HIREGOUDAR S, et al.Process optimization of supercritical carbon dioxide (SC-CO2) extraction parameters for extraction of deoxynojirimycin (1-DNJ) from mulberry (Morus alba L.) leaves[J].Journal of Applied and Natural Science, 2016, 8(1):405-411.
[20] ERUYGUR N, DURAL E.Determination of 1-Deoxynojirimycin by a developed and validated HPLC-FLD method and assessment of in-vitro antioxidant, α-Amylase and α-Glucosidase inhibitory activity in mulberry varieties from Turkey[J].Phytomedicine, 2019, 53:234-242.
[21] 丁俊男, 郑桂英, 张秀丽, 等.北方桑树中1-脱氧野尻霉素含量的测定[J].实验室研究与探索, 2012, 31(1):12-14, 45.DING J N, ZHENG G Y, ZHANG X L, et al.Determination of 1-DNJ content of northern mulberry varieties[J].Research and Exploration in Laboratory, 2012, 31(1):12-14, 45.
[22] KIMURA T, NAKAGAWA K, SAITO Y, et al.Simple and rapid determination of 1-deoxynojirimycin in mulberry leaves[J].BioFactors, 2004, 22(1-4):341-345.
[23] HU X Q, JIANG L, ZHANG J G, et al.Quantitative determination of 1-deoxynojirimycin in mulberry leaves from 132 varieties[J].Industrial Crops and Products, 2013, 49:782-784.
[24] YOSHIHASHI T, DOHTT, TUNGTRAKUL P, et al.Simple, selective, and rapid quantification of 1-deoxynojirimycin in mulberry leaf products by high-performance anion-exchange chromatography with pulsed amperometric detection[J].Journal of Food Science, 2010, 75(3):C246-C250.
[25] XU B, ZHANG D Y, LIU Z Y, et al.Rapid determination of 1-deoxynojirimycin in Morus alba L.leaves by direct analysis in real time (DART) mass spectrometry[J].Journal of Pharmaceutical and Biomedical Analysis, 2015, 114:447-454.
[26] BALAKUMARAN K, JANAGILI M, RAJANA N, et al.Development and validation of miglitol and its impurities by RP-HPLC and characterization using mass spectrometry techniques[J].Scientia Pharmaceutica, 2016, 84(4):654-670.
[27] HAN W L, CHEN X X, YU H M, et al.Seasonal variations of iminosugars in mulberry leaves detected by hydrophilic interaction chromatography coupled with tandem mass spectrometry[J].Food Chemistry, 2018, 251:110-114.
[28] ZHANG L, ZHOU Y R, MENG J, et al.Disperse solid-phase extraction cleanup for the determination of 1-deoxynojirimycin in mulberry leaves with ultraperformance liquid chromatography-tandem mass spectrometry[J].Journal of Food Quality, 2021, 2021(1):2274450.
[29] THAKUR K, ZHANG Y Y, MOCAN A, et al.1-Deoxynojirimycin, its potential for management of non-communicable metabolic diseases[J].Trends in Food Science &Technology, 2019, 89:88-99.
[30] DEMARSILIS A, REDDY N, BOUTARI C, et al.Pharmacotherapy of type 2 diabetes:An update and future directions[J].Metabolism, 2022, 137:155332.
[31] REN X X, XING Y, HE L Y, et al.Effect of 1-Deoxynojirimycin on insulin resistance in prediabetic mice based on next-generation sequencing and intestinal microbiota study[J].Journal of Ethnopharmacology, 2022, 289:115029.
[32] LI X Y, LIU S G, WANG S Q, et al.1-Deoxynojirimycin affects high glucose-induced pancreatic beta-cell dysfunction through regulating CEBPA expression and AMPK pathway[J].Biochemistry and Cell Biology, 2025, 103:1-12.
[33] TAKASU S, PARIDA I S, ITO J, et al.Intestinal absorption and tissue distribution of aza-sugars from mulberry leaves and evaluation of their transport by sugar transporters[J].Journal of Agricultural and Food Chemistry, 2020, 68(24):6656-6663.
[34] LI R L, WANG J, LIU J Y, et al.Mulberry leaf and its effects against obesity:A systematic review of phytochemistry, molecular mechanisms and applications[J].Phytomedicine, 2024, 128:155528.
[35] TSUDUKI T, KIKUCHI I, KIMURA T, et al.Intake of mulberry 1-deoxynojirimycin prevents diet-induced obesity through increases in adiponectin in mice[J].Food Chemistry, 2013, 139(1-4):16-23.
[36] RONKAINEN J, HUUSKO T J, SOININEN R, et al.Fat mass- and obesity-associated gene Fto affects the dietary response in mouse white adipose tissue[J].Scientific Reports, 2015, 5:9233.
[37] RAJAN S, GUPTA A, BEG M, et al.Adipocyte transdifferentiation and its molecular targets[J].Differentiation, 2014, 87(5):183-192.
[38] LI A N, CHEN J J, LI Q Q, et al.Alpha-glucosidase inhibitor 1-deoxynojirimycin promotes beige remodeling of 3T3-L1 preadipocytes via activating AMPK[J].Biochemical and Biophysical Research Communications, 2019, 509(4):1001-1007.
[39] REN X X, GUO Q F, JIANG H, et al.Combinational application of the natural products 1-deoxynojirimycin and morin ameliorates insulin resistance and lipid accumulation in prediabetic mice[J].Phytomedicine, 2023, 121:155106.
[40] LI Y G, ZHONG S, YU J Q, et al.The mulberry-derived 1-deoxynojirimycin (DNJ) inhibits high-fat diet (HFD)-induced hypercholesteremia and modulates the gut microbiota in a gender-specific manner[J].Journal of Functional Foods, 2019, 52:63-72.
[41] ZHONG S, YANG Y N, HUO J X, et al.Dissection of gut microbiota and metabolites reveals the hypolipidemic effect of green mulberry leaf tea/black mulberry leaf tea in mice[J].Journal of Functional Foods, 2023, 111:105906.
[42] HEYMANS S, LAKDAWALA N K, TSCHÖPE C, et al.Dilated cardiomyopathy:Causes, mechanisms, and current and future treatment approaches[J].The Lancet, 2023, 402(10406):998-1011.
[43] MARON B A, WANG R S, CARNETHON M R, et al.What causes hypertrophic cardiomyopathy?[J].The American Journal of Cardiology, 2022, 179:74-82.
[44] ZHUANG Q Q, GUO F F, FU L, et al.1-Deoxynojirimycin promotes cardiac function and rescues mitochondrial cristae in mitochondrial hypertrophic cardiomyopathy[J].The Journal of Clinical Investigation, 2023, 133(14):e164660.
[45] JIANG L Q, ZHANG L Y, YANG J C, et al.1-Deoxynojirimycin attenuates septic cardiomyopathy by regulating oxidative stress, apoptosis, and inflammation via the JAK2/STAT6 signaling pathway[J].Biomedicine &Pharmacotherapy, 2022, 155:113648.
[46] CAO Y, JIANG W, BAI H X, et al.Study on active components of mulberry leaf for the prevention and treatment of cardiovascular complications of diabetes[J].Journal of Functional Foods, 2021, 83:104549.
[47] LEE J Y, SUNWOO J S, KWON K Y, et al.Left ventricular ejection fraction predicts poststroke cardiovascular events and mortality in patients without atrial fibrillation and coronary heart disease[J].Korean Circulation Journal, 2018, 48(12):1148-1156.
[48] WANG Y T, YU Z W, JIANG J, et al.Mulberry leaf attenuates atherosclerotic lesions in patients with coronary heart disease possibly via 1-Deoxynojirimycin:A placebo-controlled, double-blind clinical trial[J].Journal of Food Biochemistry, 2021, 45(1):e13573.
[49] ZHENG J P, ZHU L, HU B F, et al.1-Deoxynojirimycin improves high fat diet-induced nonalcoholic steatohepatitis by restoring gut dysbiosis[J].The Journal of Nutritional Biochemistry, 2019, 71:16-26.
[50] YU Y F, CHEN Y H, SHI X P, et al.Hepatoprotective effects of different mulberry leaf extracts against acute liver injury in rats by alleviating oxidative stress and inflammatory response[J].Food &Function, 2022, 13(16):8593-8604.
[51] 侯文玉, 李少璁, 张文凤, 等.桑叶DNJ对肉兔生长性能、器官指数、抗氧化能力和肠道屏障功能的影响[J].饲料研究, 2024, 47(22):66-72.HOU W Y, LI S C, ZHANG W F, et al.Effects of mulberry leaf DNJ on growth performance, organ index, antioxidant capacity, and intestinal barrier function of meat rabbits[J].Feed Research, 2024, 47(22):66-72.
[52] PERERA N, BRUN J, ALONZI D S, et al.Antiviral effects of deoxynojirimycin (DNJ)-based iminosugars in dengue virus-infected primary dendritic cells[J].Antiviral Research, 2022, 199:105269.
[53] MIGLANI V, SHARMA P, KUMAR NARULA A.WITHDRAWN:Investigation of iminosugars as antiviral agents against SARS-CoV-2 main protease:Inhibitor design and optimization, molecular docking, and molecular dynamics studies to explore potential inhibitory effect of 1-deoxynojirmycin series[J].Current Computer-Aided Drug Design, 2025.