随着我国经济的迅猛发展,人们对动物源性食品的数量和质量的需求不断攀升,由畜禽及水生动物的肉、蛋、奶加工而成的食品已成为国民饮食结构的重要组成部分。然而,因兽药存在超量、超范围使用以及监管不力等情况,部分药物会残留在动物源性食品中,进而对食品安全构成威胁。兽药残留主要包含抗生素、抗寄生虫药、抗炎药、镇静剂以及具有促生长功效的药物[1]。这些药物随动物源性食品进入加工流程,在食物链中富集进入人体内,长期低剂量摄入可能造成健康损害。在众多种类兽药中,奶类、肉类等动物产品中残留的兽用抗生素可能引发人体过敏反应和促使耐药性病原体产生[2]。因此,研发全新的动物源性食品中抗生素残留物预处理方法与检测技术,实施严格的兽用抗生素残留监管,是保障动物源性食品质量安全、维护消费者健康的根本举措。近年来,国内外积极致力于发展检测动物源性食品中抗生素残留的技术,并已取得了大量研究成果。然而,考虑到动物源性食品的基质成分极为复杂,且富含多种干扰物质,亟须研发高效的前处理方法以及兼具高灵敏度和特异性的分析技术,实施严格的兽药残留监管。本文对动物源性抗生素残留现状和快速检测技术在畜禽产品抗生素残留检测领域的应用进展进行了综述,旨在为实现动物源性食品中抗生素残留的高效、便捷、精准检测提供参考。
1 动物源性食品中抗生素残留检测的特殊性
抗生素在动物源性食品和环境介质中的残留检测至关重要,但由于动物源性食品的复杂成分,与其他环境基质相比,检测动物源性食品中的抗生素残留有独特的挑战。动物源食品中的抗生素残留直接关系食品安全和人类健康,各国制定了最大残留限量(maximum residue limit,MRL)等标准,对检测灵敏度和方法有明确要求。而环境样品中的抗生素作为新兴污染物,浓度往往极低且种类繁杂,缺乏统一的强制限值,主要用于污染监测和风险评估。本文从样品前处理、检测技术、灵敏度与特异性3个方面对动物源性食品与环境样品中抗生素检测的核心差异进行了对比分析。
1.1 样品前处理方式差异
肉类、牛奶、鸡蛋和蜂蜜等动物源性食品因有高含量的蛋白质、脂质和其他大分子,会干扰分析过程,从而影响检测方法的灵敏度和准确性。因此,动物源食品基质复杂,需经过充分的提取和净化,避免干扰检测结果。对于动物源性食品提取通常采用有机溶剂萃取配合缓冲液以从组织中提取抗生素的方法,并可能加入螯合剂防止某些抗生素与基质结合[3]。高脂样品(如牛奶、蛋黄)则常需要排除脂质干扰,如加入正己烷去脂,酸沉淀蛋白以减少基质干扰[4]。净化过程,食品中多采用固相萃取(solid phase extraction,SPE)、凝胶净化或改良的QuEChERS方法去除杂质,对于特定药物类,还可使用免疫亲和柱专属净化,提高纯化效率。
环境水体和土壤中的抗生素浓度往往处于痕量水平,样品基质成分复杂且体积、质量大,因此前处理更强调富集浓缩。对于水样,通常取数百毫升到数升体积,通过SPE富集目标物,将水样调整至适宜的pH并加入螯合剂保持抗生素稳定后,过SPE小柱萃取抗生素,随后用少量有机溶剂洗脱[5]。这一过程可将样品浓缩数千倍以达到检出要求。土壤或沉积物样品则需要先提取释放抗生素,常用的方法包括加入缓冲溶液/有机溶剂混合体系振荡或超声提取,并辅以加热、微波或加压溶剂萃取等手段,以提升对吸附在土壤有机质和矿物表面的抗生素的提取效率。提取液往往含有大量干扰物质,需进一步经SPE、萃取液液分配等净化步骤。近年来,在环境样品前处理中出现微型化和自动化趋势,如引入固相微萃取(solid phase microextraction,SPME)、分散液液微萃取(dispersive liquid-liquid microextraction,DLLME)、中空纤维膜萃取等技术,以减少溶剂用量并适应现场快速富集的需求[6]。综上所述,环境样品前处理侧重于高倍富集和高选择性净化,以弥补基质复杂和靶向物含量极低的不足,而食品样品前处理强调提取回收率和基质净化的平衡,既要高效提取痕量残留,又要尽可能简化步骤提高通量。
1.2 常用检测技术差异
动物源性食品中抗生素残留检测一般采用“初筛-确证”的策略。初筛技术包括微生物法和免疫学方法等。微生物抑制法利用指示菌对抗生素敏感性的培养反应,在含样品的培养基上观察抑菌圈来判断残留。此类方法可一次性覆盖广谱抗菌物质,操作简单成本低,适合养殖场或屠宰场现场快速筛查,但仅能定性/半定量,且特异性不高[7]。免疫方法方面,酶联免疫吸附法(enzyme linked immunosorbent assay,ELISA)和胶体金试纸被广泛用于定量/定性筛检特定类别抗生素,具有灵敏度较高、操作简便和通量高等优点。但是,这些方法通常存在类物质交叉反应问题,只能针对某一类或某几种结构相近的药物,易出现假阳性或无法区分具体化合物的情况[8]。因此,当筛查检出阳性时,需采用确认分析。确证技术以色谱-质谱法为主,包括高效液相色谱-串联质谱(liquid chromatography-tandem mass spectrometry,LC-MS/MS)和GC-MS等。其中LC-MS/MS因适用范围广、灵敏度和特异性高,被认定为许多国家的兽药残留检测的“金标准”。此外,为提高食品中多残留检测效率,近年来还出现多残留联合检测技术和传感器技术。例如,光学、电化学生物传感器利用特异性识别元件实现抗生素快速检测,有望实现无需复杂前处理即可现场定量。
环境介质中的抗生素检测目前主要依赖仪器分析法,尤其是LC-MS/MS等高灵敏度手段进行多组分同时定量。由于环境中可能存在种类繁多的抗生素及其代谢转化产物,且难以确定具体目标物,因此检测方法趋向于广谱多残留分析。通常采用HPLC-MS技术同时检测数十种不同类别的抗生素。相比之下,免疫或生物学检测方法在环境领域应用较少。这是因为环境基质,尤其是污水、河水成分复杂,免疫法易受基质中天然物质干扰而降低特异性,且水环境中的抗生素含量远低于食品中残留,许多商业检测试剂盒在痕量水平难以有效工作[9]。总体来说,环境样品的抗生素检测技术更偏重于高灵敏多成分的分析仪器方法,以求在一次分析中覆盖尽可能多的化合物,并确保在超低浓度下可靠检出。不同的是,食品中的抗生素检测技术呈现“筛查面广-确证精准”的模式,先用快速方法大批量筛查可疑样品,再用高精度仪器法确认以满足监管需求。
1.3 技术灵敏度和特异性差异
食品中抗生素检测对灵敏度和特异性的要求由食品安全标准所驱动。灵敏度方面,分析方法的定量限一般需达到对应抗生素MRL的1/2或更低。多数兽药在食品中的MRL为几十到几百μg/kg量级;因此方法检出限通常需要达到亚ppb水平。例如,中国制定的标准方法(GB 31658.17—2021《食品安全国家标准 动物性食品中四环素类、磺胺类和喹诺酮类药物残留》)对四环素类、磺胺类和喹诺酮类检测的要求是各目标物的定量下限为1~5 μg/kg。对于禁用药物如氯霉素、硝基呋喃等,则要求方法最低检出限尽可能低以保证“不得检出”的法规限制。在特异性方面,色谱质谱法具有最高的选择性,利用保留时间和特征质谱离子对进行双重识别,大大降低了假阳性率。相比之下,免疫和微生物方法的特异性较低,ELISA等可能与结构类似药物交叉反应,从而测得“总量”而非单一组分。而微生物法只反映样品整体抑菌效应,无法指明是哪一种抗生素导致,也容易受样品pH或天然抑菌物质影响而出现误判。因此,在食品残留检测中,特异性较低的方法则用于初筛,特异性高的方法用于确证,二者结合保障既不漏检又不错判。
由于环境介质中的抗生素残留浓度通常比食品中低几个数量级,超高灵敏度是环境检测的首要要求。许多环境水样中抗生素只有ng/L级别,甚至更低。例如,有监测数据显示中国地表水、地下水中抗生素浓度大致在ppt水平,个别污染严重水域才达到近ppb水平。因此,环境分析方法往往需通过大量富集和高性能仪器来实现极低的检出限。实际监测中,为保证数据可靠,欧盟《水框架指令》中要求方法对大环内酯类抗生素的检测限需不高于0.09 μg/L,后来进一步降低至0.019 μg/L,以便评估其环境风险。目前很多实验室的LC-MS/MS方法在水中各抗生素的检出限已可达ng/L甚至更低水平[10]。特异性方面,由于环境基质成分复杂、多种污染物并存,仪器分析可能受到基质效应影响。为提高特异性和准确度,环境样品分析常采用内标法校正基质效应,并通过选择适当的质谱离子对或高分辨质谱筛选目标,提高对共存干扰物的区分能力。此外,环境中抗生素可能降解产生代谢物或产物,这些化合物结构类似且可能共存,对分析特异性提出了挑战。高分辨质谱可根据精确质荷比和谱库匹配识别出更多未知物,提升整体特异鉴别能力。综上,环境样品检测追求在痕量浓度下仍保持高度选择性,以确保在复杂基质中准确测定目标抗生素。
2 动物源性食品中抗生素残留快速检测技术概述
多国研究显示,动物源性食品中主要抗生素残留物为喹诺酮类、大环内酯类、β-内酰胺类、磺酰胺类、四环素、氨基糖苷类抗生素,抗生素残留问题仍然存在,需要引起重视[11]。近年来,动物源性食品中抗生素残留超标的现象频繁出现,已成为一个不容忽视的问题。为应对这一紧迫形势,我国农业农村部、国家卫生健康委员会以及国家市场监督管理总局相继出台多项规范与标准,对食品动物中禁用抗生素的种类及兽药残留的最大限量值作出了详细规定,与欧盟、美国MRL对比详细见表1。
表1 动物源性食品中主要抗生素MRL
Table 1 MRL of major antibiotics in animal-derived foods

抗生素种类中国美国欧盟恩诺沙星肉:100 μg/kg牛奶:禁用鸡蛋:10 μg/kg肉:禁用禁用于产奶动物禁用于产蛋鸡肉:100 μg/kg牛奶:100 μg/kg禁用于产蛋鸡氟苯尼考猪肉:300 μg/kg鸡肉:100 μg/kg鸡蛋:10 μg/kg牛、羊产乳期禁用肉:300 μg/kg未批准用于产奶奶牛未批准用于产蛋鸡肉:100 μg/kg禁用于产奶动物禁用于产蛋鸡四环素类肉:200 μg/kg牛奶:100 μg/kg鸡蛋:200 μg/kg肉:200 μg/kg牛奶:300 μg/kg禁用于产蛋鸡肉:100 μg/kg牛奶:100 μg/kg鸡蛋:200 μg/kg阿莫西林肉:50 μg/kg牛奶:4 μg/kg鸡蛋:4 μg/kg肉:10 μg/kg牛奶:10 μg/kg禁用于产蛋鸡肉:50 μg/kg牛奶:4 μg/kg禁用于产蛋鸡泰乐菌素肉:200 μg/kg牛奶:50 μg/kg鸡蛋:200 μg/kg肉:100 μg/kg牛奶:50 μg/kg禁用于产蛋鸡肉:100 μg/kg牛奶:50 μg/kg禁用于产蛋鸡林可霉素肉:100 μg/kg牛奶:150 μg/kg鸡蛋:50 μg/kg肉:100 μg/kg牛奶:150 μg/kg禁用于产蛋鸡肉:100 μg/kg牛奶:150 μg/kg禁用于产蛋鸡多西环素肉:100 μg/kg禁用于产奶动物禁用于产蛋鸡肉:100 μg/kg禁用于产奶动物禁用于产蛋鸡肉:100 μg/kg禁用于产奶动物禁用于产蛋鸡
传统检测动物源性食品中抗生素残留的方法主要为LC、GC、LC-MS、GC-MS等技术。这些方法虽精准可靠,但存在设备昂贵、操作复杂、耗时较长等问题,难以满足现场快速筛查和大量样本初筛的需求[12]。此外,LC-MS可能难以产生精确的定量结果,特别是在分析物浓度较低的情况下,这增加了假阴性结果的可能性[13]。近年来,随着纳米技术、材料科学、生物技术、传感技术的发展,免疫学分析技术、生物传感器技术等快速检测技术的发展,凭借简便、快速、灵敏、低成本以及适用于现场检测等优势,其迅速成为监控抗生素残留的研究热点之一。
3 免疫学技术
3.1 胶体金免疫层析法(gold colloid immunochromatography,GICA)
GICA是一种借助胶体金颗粒作为示踪标记物,结合抗原-抗体的特异性免疫反应以及毛细管层析作用,在固相膜上达成目标物快速定性或半定量检测的快速检测方法。检测时,样品溶液通过毛细作用在硝酸纤维素膜试纸条上流动。若样品中不含目标抗生素,金标抗体与T线抗原结合,呈现红色条带;若含目标抗生素,抗生素会与金标抗体结合,阻止其与T线抗原结合,导致T线不显色,原理图见图1[14]。该方法在动物临床疾病诊断和食品安全监测领域得到了广泛应用。GICA技术的发展主要在识别元件的改进和前处理方法的创新上,以应对复杂基质的挑战。在识别元件方面,研究者致力于制备高灵敏度和高特异性抗体。刘波等[15]采用活泼酯法偶联乳铁蛋白和牛血清白蛋白制备四环素类人工抗原,并制备出四环素类抗生素的广谱单克隆抗体,应用GICA成功研制四环素类抗生素检测试纸条,该方法对四环素、金霉素、土霉素、多西环素的IC50值分别为1.29、1.04、1.34、2.33 μg/kg,对多西环素检测限为40 μg/kg,检测时间约15 min。LI等[14]重新合成氧氟沙星半抗原,制备对氧氟沙星具有高灵敏度和亲和力的单克隆抗体,与洛美沙星、培氟沙星、环丙沙星和诺氟沙星的4种类似物的交叉反应性小于0.1%,亲和力高,特异性好。并且,建立的ELISA方法的IC50值为0.13 ng/mL,检出限为0.033 ng/mL,回收率为80%~120%,制备GICA试纸在3种肉制品中的目视检测限为1 ng/g。在前处理方面,集成化、快速化的样品前处理成为主要研究内容。HE等[16]开发了一种基于超声辅助固相萃取结合胶体金试纸的快速分析方法,测定孔雀石绿、氯霉素、氨基脲代谢物在常见水产品残留。在优化条件下,该方法的检出限为0.01~0.5 μg/kg,加标样品的相对标准偏差为0.99%~5.58%和1.6%~7.2%,加标回收率为84.2%~112.9%,平均检测时间仅需15 min。另外,GICA检测技术,由于其操作极为简便,无需专用仪器,检测结果可依据显色情况进行目视判读,故而适合在农场、屠宰场、农贸市场等场所开展现场快速检测工作,极大地提升了检测效率。但是,由于动物源性食品样品基质富含蛋白、脂肪等,容易干扰检测结果,导致假阳性或假阴性结果出现[17]。此外,目视试纸颜色变化仅能够粗略估计食品中残留物质范围,难以检测出微量存在的抗生素残留,不能成为定量检测技术。
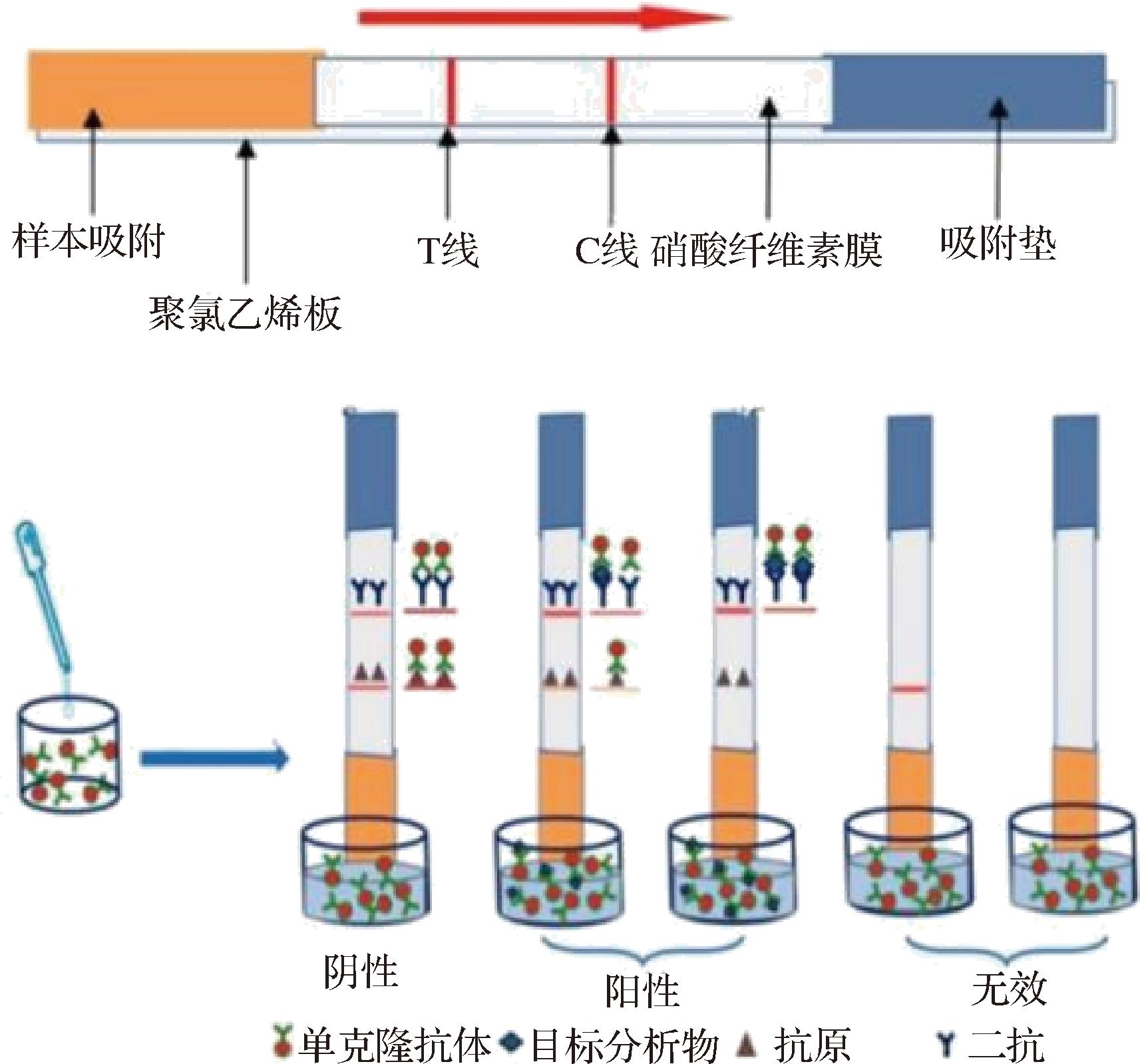
图1 胶体金免疫层析法检测原理
Fig.1 Detection principle of colloidal gold immunochromatography
3.2 ELISA
ELISA是检测动物源性食品抗生素残留应用最广泛的检测技术之一。其核心原理依赖于抗原-抗体的特异性免疫反应,并通过酶标记实现信号的放大与输出,从而完成对目标物的定量分析,原理图见图2[18]。近年来,该技术的发展主要体现在识别元件的创新(如纳米抗体、单克隆抗体、IgY抗体及广谱受体蛋白)和信号放大策略的优化上,旨在不断提升其灵敏度、特异性和检测通量。YANG等[19]通过构建恩诺沙星特异性纳米抗体-辣根过氧化物酶融合蛋白,开发了一种适用于牛奶及动物组织检测的高灵敏度竞争性ELISA方法。该方法IC50值为37.41 ng/mL,线性检测范围为10.89~244.34 ng/mL,检测限值达6.48 ng/mL,对结构类似物环丙沙星的交叉反应率仅4.66%,加标回收率为84.99%~107.72%,相对标准偏差低于10.70%。WU等[20]制备抗头孢氨苄单克隆抗体,成功构建了一种高灵敏度间接竞争性酶联免疫吸附法,其IC50值为1.83 μg/L,检出限和定量限分别为0.44~0.58 μg/kg和0.57~0.67 μg/kg,加标回收率为90.1%~103.6%。YADOUNG等[21]采用环丙沙星-牛血清白蛋白与诺氟沙星-牛血清白蛋白双半抗原混合免疫蛋鸡,经蛋黄纯化获得特异性IgY抗体。将该抗体引入间接竞争ELISA体系,方法验证表明,对恩诺沙星的IC50值为达0.05 μg/mL,对于鸡肉样品加标回收率为86.65%~112.71%,猪肉样品为84.24%~117.22%。在最近研究中,检测残留抗生素从针对单一化合物向多残留分析发展。殷萌琪[22]以能与β-内酰胺类抗生素特异性结合的青霉素结合蛋白(penicillin-binding proteins,PBPs)作为广谱识别材料,选取肺炎链球菌R6 pbp3片段作为模板,获得了N端截短但仍具备生物学活性的PBP3*蛋白。将纯化后的受体蛋白PBP3*直接固定在高吸附96孔聚乙烯反应板上,成功构建了用于检测牛奶中15种β-内酰胺类抗生素残留的直接竞争-酶标受体检测法。IC10值为0.28~100.30 ng/mL。在直接竞争-酶标受体检测法的基础上,结合酶促化学发光技术,使IC50值均降低至1/8~1/10。由于其具灵敏度高、特异性强、所需时间短、检测设备简便等优势被广泛应用在食品安全与质量检测。
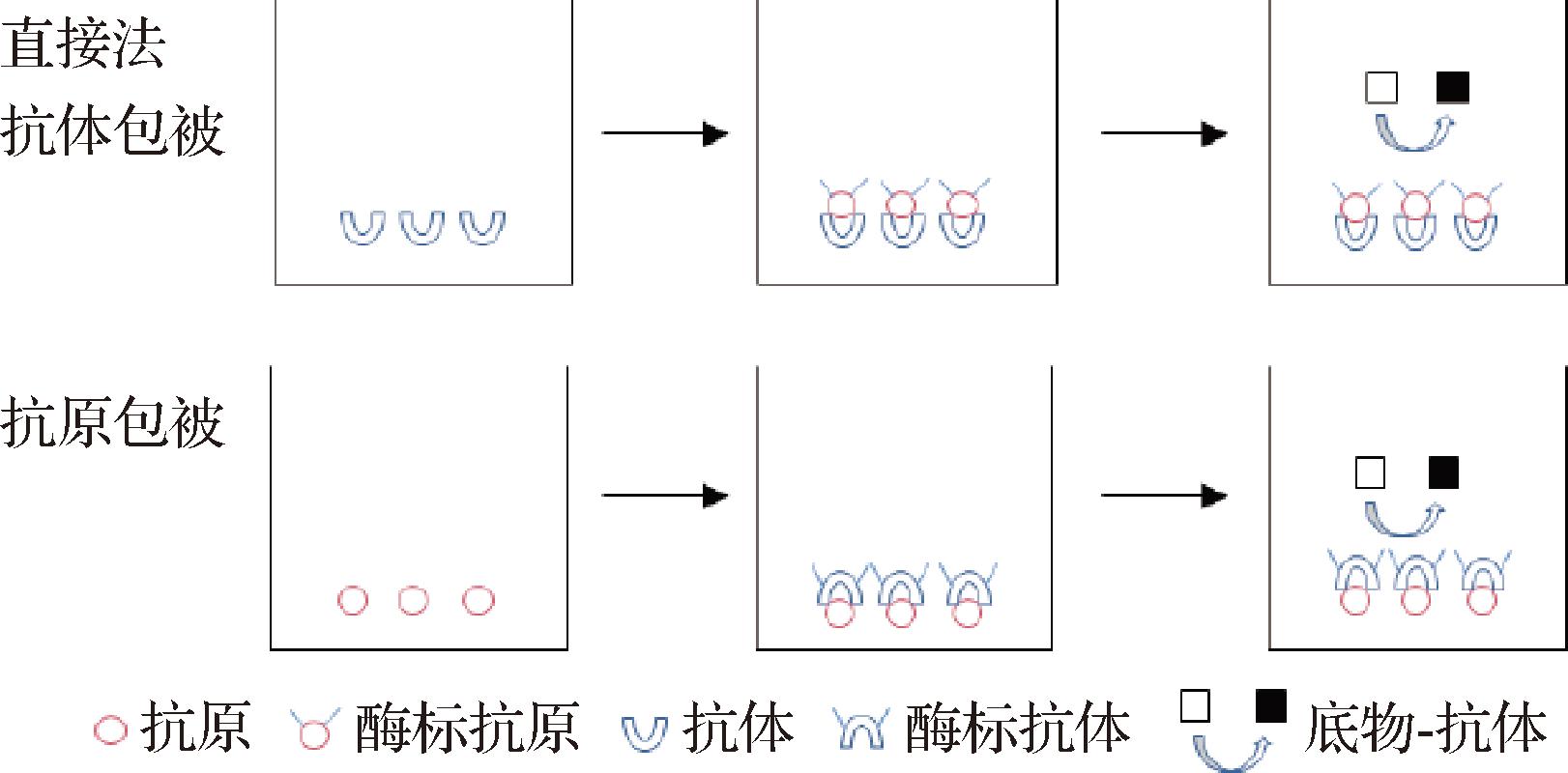
图2 ELISA检测原理
Fig.2 ELISA detection principle
虽然ELISA检测法具有多重优点,但ELISA检测法也存在一定的局限性。首先,尽管某些纳米材料能够改良ELISA检测法,ELISA检测法也存在交叉反应风险,对于结构相似的兽药或其代谢产物存在检测假阳性情况,影响检测结果。其次,酶活性易受温度、pH等环境因素影响,必须严格控制操作条件,若控制不当,酶活性会降低,从而影响检测结果的准确性[23]。
3.3 荧光偏振免疫分析法(fluorescence polarization immunoassay,FPIA)
FPIA是一种基于荧光偏振现象和免疫反应特异性相结合的均相免疫分析技术,其原理依赖于抗原-抗体结合前后分子体积的变化,游离态的小分子荧光标记物旋转速度快,偏振度低;而与抗体结合后,分子体积增大,旋转减慢,偏振度升高。通过测量偏振光信号的变化即可实现对目标物的定量分析,原理见图3[24]。FPIA无需分离洗涤步骤,操作简便、响应迅速,特别适用于小分子物质的快速检测。近年来,该技术在抗生素残留检测领域的进展主要体现在检测性能的优化、多残留分析能力的拓展以及检测效率的进一步提升。在提升检测性能方面,研究者致力于开发高性能的识别元件和荧光示踪剂。SHEN等[25]通过共价作用偶联恩诺沙星与牛血清白蛋白制备特异性多克隆抗体,并将氯乙酰胺部分共价连接荧光素合成恩诺沙星示踪剂,据此建立FPIA,该方法IC50值为21.49 ng/mL,检出限低至1.68 ng/mL;对结构类似物的交叉反应率均低于2%,猪肝与鸡肉样本的加标回收率为91.3%~112.9%,变异系数(coefficient of variation,CV)为5.13%。DUAN等[24]设计5种荧光素标记的红霉素示踪剂,并将代谢物与3种单克隆抗体配对使用,用于检测牛奶中的红霉素,该方法IC50值低至7.39 μg/L,检出限为14.08 μg/L,加标回收率达96.08%~107.77%,整个检测流程仅需5 min,显著优于传统方法。该团队在另一项研究中开发了一种均相双波长荧光偏振免疫分析法,实现食品中23种磺胺类药物与5种甲氧苄啶的高通量同步筛查,该方法对于牛奶中磺胺二甲嘧啶回收率为81.7%~97.2%,甲氧苄啶回收率为78.6%~103.6%,CV均小于18.9%,全流程检测时间仅需15 min[26]。FPIA作为抗生素快速检测方法,也存在明显局限性。首先,FPIA需要配备荧光偏振光路和检测器的特定仪器,高昂的投入并不适合小规模检测机构。其次,该方法的检测灵敏度依赖于特异性抗体和荧光示踪剂优劣,因此对于一些分子大、结构复杂的成分难以实现多残留物分析[23]。此外,由于动物源性食品基质成分复杂,样本中内源性荧光物质或光散射物质可能干扰偏振信号,必须通过SPE或稀释等预处理步骤才能确保检测精度。综上所述,尽管FPIA能提供快速检测方法,但以上技术瓶颈还需要探究新型检测方法攻克。
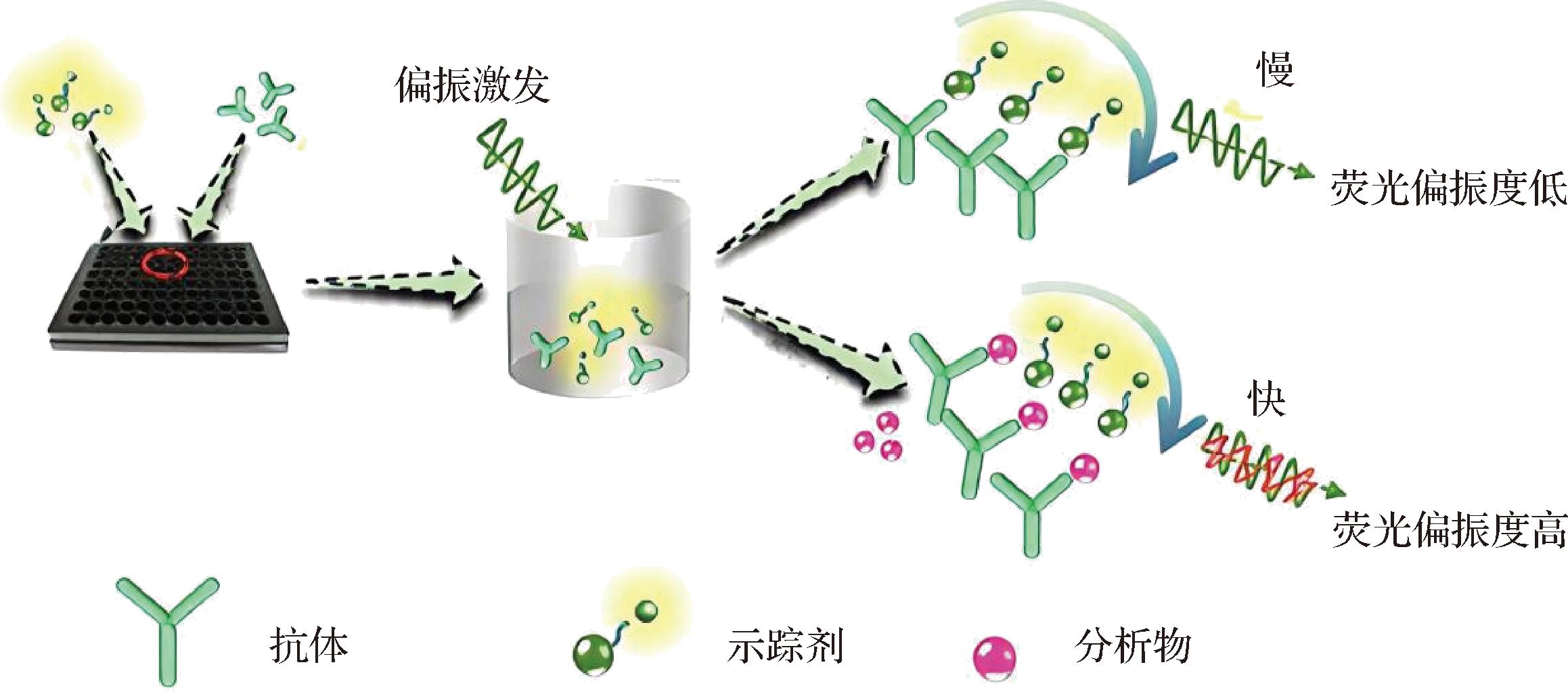
图3 荧光偏振免疫分析法原理
Fig.3 Principle of fluorescence polarization immunoassay
4 生物传感器技术
生物传感器是食品中抗生素残留检测领域的快速检测技术,主要由抗体、适配体(aptamer,Apt)、受体、酶、全细胞、分子印迹聚合物(molecular imprinted polymer,MIP)、金属有机框架(metal-organic frameworks,MOFs)材料等抗生素识别元件和可测量信号的传感器组成。如图4所示,该技术的核心原理是将特定抗原或抗体片段固定于相应传感器表面,借助抗原-抗体反应的高度特异性,以及标记物所提供的信号放大作用,实现对目标物的检测[27]。在结合过程中,抗原与抗体之间的相互作用会引起理化参数的改变,传感器可实时捕获这些变化并将其转换为可测信号,同时进行放大处理,从而显著提升检测的灵敏度和选择性。根据与抗生素残留物结合后产生响应信号种类,检测技术主要分为光学快速检测技术、电化学检测技术、压电传感技术等。
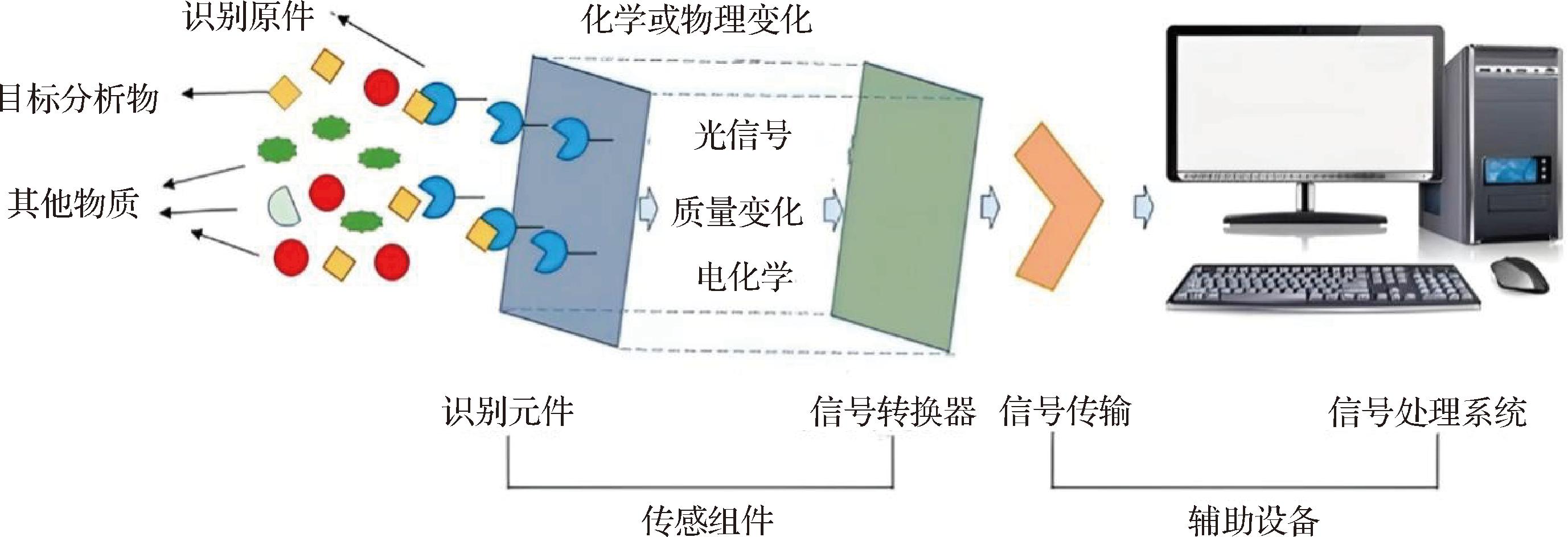
图4 生物传感器技术检测原理
Fig.4 Detection principle of biosensor technology
目前,因生物传感器灵敏度高、选择性强、操作简单、检测成本低、便携简单可开发成智能穿戴设备受研究者关注。
4.1 电化学传感器检测技术
电化学生物传感器技术检测抗生素残留的核心原理是利用生物识别元件对目标抗生素的特异性识别作用,结合信号转换器将这种生物识别转化为可定量的化学信号,从而实现对痕量抗生素的高灵敏、快速检测。根据识别元件种类可分为基于抗体、适配体、酶、受体蛋白、分子印迹聚合物等传感器[28]。电化学生物传感器具有灵敏度高、特异性强、操作简单、检测成本低等优势,在动物源性食品中痕量抗生素残留的监测中展现了较大的应用潜力。近年来,该技术的显著进展主要得益于新型纳米材料与复合结构的引入、分子识别元件的多样化以及固定化策略的创新,共同推动其在复杂食品基质中检测性能的不断提升。特别是随着近年来纳米材料的发展,其凭借高比表面积、优异导电性和催化活性,被广泛用于电极修饰以增强电子传递效率并放大检测信号,极大地提升了传感器灵敏度。ADANE等[29]基于热退火金银合金纳米多孔基体/还原氧化石墨烯/聚甘氨酸修饰玻碳电极的超灵敏传感器,实现对食品中甲硝唑的痕量检测,该传感器检出限为0.104 pmol/L,兼具优异稳定性与抗干扰性,相对标准偏差低于5%,在检测奶粉、猪肉、鸡肉样本中回收率达96.9%~101.4%。同时,识别元件与固定化策略的协同创新提高了传感器的选择性和稳定性。分子印迹聚合物(MIPs)和Apt的发展为解决传统生物分子易失活的问题提供了新路径。FU等[30]基于Cu2+掺杂共价有机框架的分子印迹电化学传感器,用于高选择性检测诺氟沙,通过Cu2+介导的共价键合策略,将诺氟沙星印迹层稳定锚定于玻碳电极表面,该传感器检出限为1.90 μg/kg,全脂、低脂、脱脂牛奶回收率为92.4%~99.0%,该设计首次融合共价有机框架导电改性与共价印迹层稳定化策略,为复杂基质中氟喹诺酮类残留检测提供了新检测方式。DING等[31]基于金纳米颗粒/适配体复合物(AuNPs-Apt)所开发的新型恩诺沙星适配体传感器对目标物恩诺沙星表现出高度特异性识别能力,检测限为0.05 μg/mL。电化学传感器因成本低、速度快、便携性好、灵敏度高,在抗生素残留检测领域展现出巨大潜力,但在实际应用中仍面临以下问题:首先,生物识别元件有时无法准确区分目标抗生素与其结构类似物导致假阳性或假阴性结果,而且抗体、酶、Apt固定化在电极表面后,其活性会随时间、温度变化或反复使用而逐渐下降,影响传感器的长期稳定性和使用寿命[32];其次,虽然纳米材料常被用于信号放大,但其放大效率、稳定性和重现性仍需优化,且可能引入新的干扰或复杂性。
4.2 压电传感器检测技术
压电传感器快速检测技术是利用压电效应,将目标分析物与传感器表面的相互作用直接转换为可测量的频率信号变化,具有实时响应、无标记、操作简便、高灵敏度等特点。在各类压电材料中,石英晶体微天平(quartz crystal microbalance,QCM)因其良好的稳定性和灵敏度成为研究热点。其原理是当目标物与固定在石英晶体金属表面的识别元件结合时,引起晶体表面质量增加,进而导致共振频率下降,通过监测该频率变化即可实现对目标物的定量检测。近年来,该技术的发展主要围绕敏感界面材料的创新与识别元件的多样化展开,显著提升了检测性能和适用范围。敏感界面材料的设计与复合纳米结构的引入是提升QCM性能的重要途径。通过修饰具有大比表面积和特定物理化学性质的纳米材料,可有效增强质量负载效应和信号响应。YANG等[33]开发金属有机框架(HKUST-1)和金纳米颗粒(AuNPs)的无标记即时检测QCM适配体传感平台,用于四环素的高灵敏分析,通过在QCM传感界面修饰HKUST-1与AuNPs复合结构,基于Au-S键合作用,将巯基化四环素适配体固定于AuNPs表面,实现超低检测限,四环素检测限为0.008 ng/mL。MUNAWAR等[34]开发了多壁碳纳米管/钨酸铋(MWCNTs/Bi2WO6)纳米复合材料作为QCM传感器涂层,用于高灵敏检测利福平,该材料由Bi2WO6纳米片包裹MWCNTs网络构成独特异质结构,将其修饰于QCM电极表面形成检测层,传感器对利福平表现出超敏响应,检测限为0.16 μmol/L,其对利福平的识别能力较结构类似干扰物提高3倍以上。识别元件的应用进一步提高了传感器的特异性。SHAHEEN等[35]合成MnO2-石墨相氮化碳(MnO2-GCN)纳米核/分子印迹聚合物,并将其覆在QCM传感器构建石英晶体表面构筑压电分子印迹传感器,该传感器由于分子印迹薄层的高吸附特性和良好的选择性,对氯霉素展现较高的特异性识别率,识别率达98%~99%。尽管压电传感器在抗生素残留检测中展现出良好的应用前景,其仍面临一些挑战,首先,实际样品中非特异性吸附可能影响频率响应的准确性;其次,传感器的重现性和长期稳定性仍需进一步提高;此外,复杂食品基质常常要求样品前处理步骤,以避免油脂、蛋白质等对晶体表面的污染。未来的研究可聚焦于开发抗污染能力强、稳定性高的新型界面材料与识别分子,推动QCM传感器从实验室走向现场实时检测。
4.3 光信号传感器检测技术
4.3.1 表面增强拉曼光谱(surface-enhanced Raman spectroscopy,SERS)技术
SERS技术是一种革命性的拉曼光谱技术,利用纳米结构金属基底的电磁场增强效应和化学增强效应,通过贵金属纳米结构产生的局域表面等离子体共振效应,将吸附在基底表面的痕量抗生素分子的拉曼信号显著放大105~106倍,通过特征拉曼指纹图谱实现高灵敏度、高特异性的定性和定量分析。SERS基底材料直接影响拉曼信号SERS效应的强弱程度。纳米金和纳米银是最为常见的SERS基底,它们能够通过与含硫化合物结合,实现目标物的无标记分析[36]。在增强基底材料的创新方面,研究者致力于构建具有更强、更均匀“热点”效应的纳米结构。单纯的纳米金或银颗粒虽常见,但其增强效果和稳定性有限。FAN等[37]新合成的Au-Ag纳米颗粒用5,5-二硫双-2-硝基苯甲酸或4-巯基苯甲酸等不同拉曼报告分子,然后与抗四环素单克隆抗体或抗青霉素受体偶联,形成2种SERS纳米探针。优化后,四环素和青霉素的检出限分别低至0.015 ng/mL和0.010 ng/mL,加标回收率为88.8%~111.3%,相对标准偏差低于16%。BI等[38]基于牛血清白蛋白修饰的γ-Al2O3/银纳米颗粒复合基底开发了一种高灵敏SERS检测方法。该基底对庆大霉素和妥布霉素的检出限分别为11.88 nmol/L和1.26 nmol/L。另一项研究应用银-金核壳纳米粒子构建的SERS传感器,结合化学计量学算法开发了罗非鱼中氯霉素残留的快速检测方法,该纳米传感器增强因子达2.67×106,显著放大拉曼信号,检出限为0.01 μg/kg[39]。值得注意的是,SERS还停留在实验室层面,尚未被认为公认的快速检测方法。主要原因是拉曼增强效应极易受纳米结构、样本与纳米颗粒模式因素影响,导致不同实验批次或检测位置的结果出现显著波动,重复性差[23]。此外,动物源性食品复杂基质食和复杂增强机制影响定量精度。因此,开发制备重复性高、抗污染能力强、且能用于复杂样品的标准化SERS基底,是推动该技术成为公认快速检测方法的关键。
4.3.2 表面等离子体共振(surface plasmon resonance,SPR)技术
SPR检测技术利用检测物质与传感器结合后,引起金属表面介电常数改变,继而通过监测反射光共振角度或者共振波长的变化对目标物进行定性定量分析,其核心原理是等离子体波与光波的共振耦合效应。识别元件的选取对SPR传感器的精准度有至关重要的影响。识别元件的创新是提升SPR选择性与灵敏度的重要途径,MIP、MOFs识别元件展现出了卓越的灵敏度,正逐步成为研究的热点。ÇELIK等[40]采用甲基丙烯酸羟乙酯-氧化石墨烯-N-甲基丙烯酰-l-苯丙氨酸复合物合成氨青霉素G分子印迹物聚修饰的SPR传感器,检测牛奶样品中痕量青霉素G。该传感器检测限低至0.063 nmol/L,其对青霉素G选择性显著优于同类抗生素,对氨苄西林的响应灵敏度分别是阿莫西林和氨苄西林的8.16倍和14.04倍。BAKHSHPOUR-YÜCEL等[41]通过微乳液聚合法合成了四环素分子印迹纳米颗粒,并将其修饰在SPR金芯片表面制成传感器。该传感器通过其表面的印迹纳米空腔实现对四环素分子的高选择性结合,用于牛奶中四环素分析的该传感器的检测限为0.45 mg/L。随着纳米科技的发展,人们发现二维材料(MXenes、GO、MoS2)、AuNPs、AgNPs等纳米材料具备SPR信号增强能力。纳米材料与二维材料的引入有效增强了SPR响应信号。通过构建具有局域场增强效应的纳米结构界面,可显著提高传感器的灵敏度。XU等[42]开发了一种高灵敏SPR传感器,通过金银纳米颗粒构建复合传感界面,对恩诺沙星和环丙沙星的检测限分别达0.97 ng/mL和0.70 ng/mL,在牛奶基质中回收率为96.18%~121.06%,对构建高灵敏SPR传感器具有较好的推动作用。此外,TAN等[43]基于MoS2修饰Au SPR芯片表面构建出高灵敏SPR传感器,通过间接竞争免疫法检测磺胺甲唑的方法,该方法对磺胺甲唑的检测灵敏度提高了24%,而单层石墨烯报告的SPR传感器的灵敏度只提高了6%,证明了增强型SPR生物传感器在检测抗生素方面表现出显著优势,为之后研究提供了较好的借鉴意义。尽管SPR技术具有实时、免标记的优势,但在抗生素残留检测中面临显著挑战:尽管SPR生物传感器在检测抗生素方面表现出显著优势,但对小分子抗生素灵敏度不足、高度依赖高质量且特异的识别元件、复杂样品基质干扰严重导致假信号和信噪比低、传感器稳定性有限、仪器成本高昂、操作复杂且难以现场应用,使其在灵敏度、特异性、抗干扰性、成本效益和实用性方面难以满足常规检测需求,尤其在大规模筛查和痕量检测领域难以替代色谱-质谱或成熟免疫学方法等技术[44-45]。
4.3.3 比色法
比色法通过抗生素诱导纳米材料存在状态改变或酶催化显色反应,引起溶液颜色肉眼可见的变化,实现对残留抗生素的快速、可视化检测。比色传感器因其操作简便,可开发成智能手机构建便携式即时传感器,备受研究者关注。
基于金属纳米颗粒聚集状态调控的比色传感策略因其高灵敏度与直观性被广泛采用。该策略主要利用抗生素分子与纳米颗粒表面修饰基团之间的特异性相互作用,诱导颗粒聚集或分散,进而引起表面等离子体共振吸收峰位移及溶液颜色变化。KIM等[46]本研究成功构建了酪蛋白水解肽功能化银纳米颗粒新型比色传感器,该传感器通过氨基糖苷类抗生素分子中胺基与纳米颗粒表面羟基、羧基的静电桥连作用触发特异性聚集,引起405 nm与520 nm双波长光谱响应及溶液显色变化,实现对目标物的可视化定量检测。其在自来水与乳清基质中链霉素检测限分别达98 nmol/L与56 nmol/L。WANG等[47]利用聚乙烯吡咯烷酮制备聚多巴胺包覆金纳米颗粒冻干粉末,该冻干粉具备优异的复溶性能,溶解后能维持原始光谱特性与单分散性,且可稳定贮存至少9个月,以易吸附于裸纳米金颗粒表面并引发假信号的卡那霉素为模型分析物,基于以上冻干粉末构建了无标记比色传感器,聚多巴胺涂层有效抑制了卡那霉素的非特异性吸附,显著降低假阳性风险,该传感器对卡那霉素的检出限达0.22 nmol/L,满足了牛奶残留检测要求。
抗生素残留物通过调控酶催化体系改变显色反应是比色检测的常用原理之一,因此选择特异性催化酶成为比色传感器主要研究内容之一。近年来,纳米酶催化比色法在抗生素残留检测中具有显著优势,其核心是通过人工模拟酶活性的纳米材料(如Fe3O4、CeO2、贵金属合金)催化显色反应,实现高灵敏、低成本、功能可设计和裁剪、长期贮存等优势广泛应用在比色传感器中[48]。纳米酶催化比色法的为构建高稳定、可设计的传感平台提供了新途径。YUE等[49]利用Au-Pd 双金属纳米颗粒、二茂铁(Fc)合成Au-Pd@Fc纳米酶,纳米酶催化3,3′,5,5′-四甲基联苯胺3,3′,5,5′-四甲基联苯胺(3,3′,5,5′-tetramethylbenzidine,TMB)发生显色反应,用于氨基糖苷类抗生素检测,该传感器检出限为0.0458 nmol/L。CHENG等[50]开发出类过氧化物酶活性的铁铜双金属纳米酶,用于诺氟沙星的快速检测,诺氟沙星吸附在带正电荷的纳米酶上,加剧催化TMB氧化显色,该方法检测限达0.386 μmol/L,并且可在1 min内完成食品基质中诺氟沙星的检测。ZOU等[51]开发具有类过氧化物酶活性多孔Co3O4纳米盘过氧化物酶模拟活性的比色传感器,用于中性条件下食品样品中卡那霉素的快速检测,该传感器对卡那霉素表现出高灵敏度,检测限57 μmol/L,当卡那霉素浓度超过0.5 μmol/L时,可通过裸眼识别明显的颜色变化进行半定量判断,该传感器能够在10 min内快速甄别卡那霉素残留是否超出允许限值,有效满足了食品中抗生素现场即时监测的需求。HOU等[52]使用微波消解法制备了铜铁双掺杂壳聚糖-肝素钠碳点纳米酶,其兼具过氧化物酶高活性与表面正电荷特性,可高效催化H2O2氧化ABTS产生绿色产物,构建了一种简单可靠的比色传感器,检测限11.6 ng/mL,用于氨苄西林的快速检测。值得注意的是,比色法传感器受限于显色反应的分子识别机制,如酶、纳米粒子对痕量抗生素的检测能力存在不足。未来工作应致力于开发抗干扰能力更强的功能化纳米材料、理性设计高活性与高选择性的纳米酶,并结合智能手机图像识别,推动比色传感器在实际样品现场检测中的可靠应用。
4.3.4 荧光法
荧光传感器是基于目标抗生素与荧光探针的特异性相互作用引起荧光信号变化,通过定量分析信号变化实现检测的技术。荧光传感检测性能主要依赖于荧光探针。近年来,纳米荧光探针在抗生素残留检测中具有高灵敏、低成本、快速响应等优势广泛应用在荧光传感器中。目前,碳点(Carbon Dots, CDs)、量子点、MOFs、上转换纳米粒子等纳米材料被应用于荧光传感器,以检测抗生素残留。在荧光探针的设计与构建方面,多色发射、比率型检测和多功能复合材料成为提升性能的关键策略。WANG等[53]开发了一种基于多色CDs的自参比荧光传感平台,用于甲硝唑及硝基咪唑类抗生素的高通量检测。通过水热法合成蓝、青、黄、红四色CDs(B/C/Y/R-CDs),发现青、红色CDs对甲硝唑呈现特异性相反响应,据此构建C-CD/R-CD双色荧光系统,实现甲硝唑浓度依赖的肉眼可视色变,结合智能手机成像与红绿反射强度比值分析,建立现场快检方法,检测时间小于5 min。SUN等[54]开发了一种基于碳量子点(carbon quantum dots,CQD)修饰双金属MOF(CQDx@Co/Mn-MOF)的荧光传感器,用于高选择性检测喹诺酮类抗生素诺氟沙星,以钴、锰为金属中心、1,3,5-三唑苯为配体构建MOF基底,通过CQDs复合显著增强传感性能,该传感器检测限低至0.70 μmol/L,较未修饰Co/Mn-MOF灵敏度提升5倍,具备超快响应、高选择性及稳定比例荧光信号,成功应用于鸡肉、牛肉和蜂蜜中诺氟沙星的痕量检测,回收率达97.5%~108.6%。在识别机制与信号转换方面,基于MOF的传感平台展现出优异的多目标物区分能力。WANG等[55]发现2,6-萘二羧酸配体的新型铕(Eu)基MOF材料BUC-88(该材料能对喹诺酮类和四环素类抗生素进行差异化荧光传感),对喹诺酮类表现出优异的选择性和高灵敏度,对检测限恩诺沙星、诺佛沙星、环丙沙星检出限分别为0.12、0.52、0.75 μmol/L,对盐酸四环类则具有超快响应、高选择性及超高灵敏度,检测限为0.08 μmol/L。由于动物源性食品中基质复杂导致荧光探针光谱信号易受基质环境干扰,未来应研发荧光检测配套前处理技术,并探索合成新型荧光纳米材料,从而提高灵敏度。
5 小结与展望
发展动物源性食品中抗生素残留快速检测技术是保障食品安全和公众健康的迫切需求。它能高效监控养殖用药、快速筛查流通环节,精准防范超标抗生素残留进入食物链,维护食品安全,并为监管部门提供强有力的现场执法工具,提升监管效能,维护消费者信心,是构建安全食品供应链的关键防线。本文对动物源性食品中抗生素残留快速检测技术的研究进展进行了归纳总结,详述了常用的快速检测技术的检测原理和应用效果。与传统的大型仪器相比,抗生素残留快检技术具备成本低、操作简便、短时间高通量检测等优势,备受研究者的广泛关注。但是,快速检测技术在实际应用中也存在诸多挑战。首要问题是灵敏度与特异性不足,难以在复杂食品基质干扰下精准识别痕量残留及结构类似物,进而导致假阴性或假阳性结果;其次,多残留同步检测能力弱,一次筛查通常仅覆盖少数几类抗生素,无法满足对养殖业中可能使用的多种抗生素全面监控的需求,多残留高通量快速检测技术发展相对不足,导致商业化应用滞后;此外,定量能力欠缺,多数现场方法仅能提供定性或半定量结果,难以满足精确执法和风险评估对残留浓度的要求;最后,部分技术存在成本高、生物试剂稳定性差、操作不够便捷以及样品前处理繁琐耗时等瓶颈,严重制约了其在大规模筛查和现场检测场景中的高效应用与推广。
综上所述,抗生素残留快速检测研发应更多关注以下4点:(1)基于生物工程技术对抗体、酶、适配体、受体蛋白等进行设计,开发新型生物识别元件的,提升稳定性与特异性,获得具有广泛特异性和对多种目标的高亲和力的识别元件[23]。(2)纳米材料作为关键的识别与信号转导增敏元件,对于检测性能而言尤为重要。需要进一步研发具备出色光学性能、导电性、类酶活性以及识别能力的纳米材料,提高生物试剂稳定性,降低生产成本并实现商业化应用水平。(3)设计智能传感设备与智能手机的结合,结合智能算法消减基质干扰,提高检测灵敏度和精确度。结合手机影像识别、手持式光谱仪和AI算法,推动检测设备向便携化、智能化发展,开发多残留高通量检测平台,提高检测效率。(4)简化前处理技术,针对不同基质样品配套前处理装置,减小非检测目标信号的干扰,有效提升抗基质干扰能力和检测精准度。
[1] MESFIN Y M, MITIKU B A, TAMRAT ADMASU H.Veterinary drug residues in food products of animal origin and their public health consequences:A review[J].Veterinary Medicine and Science, 2024, 10(6):e70049.
[2] APREJA M, SHARMA A, BALDA S, et al.Antibiotic residues in environment:Antimicrobial resistance development, ecological risks, and bioremediation[J].Environmental Science and Pollution Research, 2022, 29(3):3355-3371.
[3] ANGELES-HERNANDEZ J C, CONTRERAS CARO DEL CASTIUO D A, ESPINOSA-S NCHEZ A, et al.Multivariate approach to antimicrobial residue concentrations in animal-derived products:An analytical review[J].Veterinary Medicine and Science, 2025, 11(2):e70297.
NCHEZ A, et al.Multivariate approach to antimicrobial residue concentrations in animal-derived products:An analytical review[J].Veterinary Medicine and Science, 2025, 11(2):e70297.
[4] LIU Y W, LUO Y B, LI W X, et al.Current analytical strategies for the determination of quinolone residues in milk[J].Food Chemistry, 2024, 430:137072.
[5] KHATAEI M M, EPI S B H, LOOD R, et al.A review of green solvent extraction techniques and their use in antibiotic residue analysis[J].Journal of Pharmaceutical and Biomedical Analysis, 2022, 209:114487.
[6] KARIKALAN N, YAMUNA A, LEE T Y.Ultrasensitive detection of ineradicable and harmful antibiotic chloramphenicol residue in soil, water, and food samples[J].Analytica Chimica Acta, 2023, 1243:340841.
[7] WIDIASIH D A, PRATAMA R P, DRASTINI Y, et al.Rapid testing of antibiotic residues to increase food safety awareness of animal origin[J].Veterinary World, 2023:1177-1183.
[8] JANGULOVA A N, TARANOVA N A, DZANTIEV B B, et al.Multiplex immunochromatographic assay using a universal labeling reactant for determining antibiotic residues in milk[J].Veterinary World, 2024, 17(11):2527-2536.
[9] TUTS L, RASSCHAERT G, HEYNDRICKX M, et al.Detection of antibiotic residues in groundwater with a validated multiresidue UHPLC-MS/MS quantification method[J].Chemosphere, 2024, 352:141455.
[10] MAHMOUD R A, HADAD G M, ABDEL SALAM R A, et al.Optimization of a solid-phase extraction coupled with a high-performance liquid chromatography and diode array ultraviolet detection method for monitoring of different antibiotic class residues in water samples[J].Journal of AOAC International, 2024, 107(1):52-60.
[11] NIU C Y, YAN M L, YAO Z L, et al.Antibiotic residues in milk and dairy products in China:Occurrence and human health concerns[J].Environmental Science and Pollution Research, 2023, 30(53):113138-113150.
[12] LIU Z, LIU X, WU Q, et al.Application and development of signal amplification strategy in detection of antibiotic residues in food[J].Analyst, 2025, 150(11):2203-2225.
[13] FRIGOLI M, KRUPA M P, HOOYBERGHS G, et al.Electrochemical sensors for antibiotic detection:A focused review with a brief overview of commercial technologies[J].Sensors (Basel), 2024, 24(17):5576.
[14] LI X L, HUANG J, LI N, et al.Development of a colloidal gold immunochromatographic assay strip using a monoclonal antibody for the rapid detection of ofloxacin[J].Foods, 2024, 13(24):4137.
[15] 刘波, 华彦涛, 赵炫, 等.快速检测食品中四环素类抗生素残留的胶体金免疫层析方法[J/OL].现代食品科技, 2025.https://doi.org/10.13982/j.mfst.1673-9078.2026.2.1635.LIU B, HUA Y T, ZHAO X, et al.Colloidal gold immunochromatography assay for rapid detection of tetracycline antibiotic residues in food[J/OL].Modern Food Science and Technology, 2025.https://doi.org/10.13982/j.mfst.1673-9078.2026.2.1635.
[16] HE Z Y, ZHANG S E, CHEN Q Z, et al.Novel solid-phase extraction promotes simultaneous colloidal gold immunochromatographic assay of malachite green, leuco-malachite green, chloramphenicol, and semi-carbazone metabolites in aquatic products[J].Food Chemistry, 2025, 465:142118.
[17] JIANG H T, XU X X, SONG S S, et al.A monoclonal antibody-based colloidal gold immunochromatographic strip for the analysis of novobiocin in beef and chicken[J].Food Additives &Contaminants:Part A, 2022, 39(6):1053-1064.
[18] 刘书余, 郭亚文, 汤亚云, 等.禽组织和禽蛋中兽药残留快速检测技术研究进展[J].食品工业科技, 2023,44(15):482-491.LIU S Y, GUO Y W, TANG Y Y, et al.Research progress on rapid detection technology of veterinary drug residues in poultry tissues and eggs[J].Science and Technology of Food Industry, 2023, 44(15):482-491.
[19] YANG M, XU Q, GU K, et al.Development of a nanobody-horseradish peroxidase fusion-based competitive ELISA to rapidly and sensitively detect enrofloxacin residues in animal-derived foods[J].Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2025, 327:125309.
[20] WU S M, SHEN W, CHEN Y S, et al.Rapid determination of cephalexin in animal-derived food by an indirect competitive enzyme-linked immunosorbent assay[J].Analytical Letters, 2022, 55(17):2803-2816.
[21] YADOUNG S, ISHIMATSU R, XU Z L, et al.Development of IgY-based indirect competitive ELISA for the detection of fluoroquinolone residues in chicken and pork samples[J].Antibiotics, 2022,11(11):1512.
[22] 殷萌琪. α-玉米赤霉醇类化合物和β-内酰胺类抗生素的广谱快速检测方法研究[D].无锡:江南大学, 2020.YIN M Q.Study on broad-spectrum and rapid determination of α-zearalanol compounds and β-lactam antibiotics[D].Wuxi:Jiangnan University, 2020.
[23] DAI Q, TANG S S, DAI C S.Recent advances in pretreatment methods and detection techniques for veterinary drug residues in animal-derived foods[J].Metabolites, 2025,15(4):233.
[24] DUAN C F, ZHANG H Y, ZHANG Y J, et al.A robust homogeneous fluorescence polarization immunoassay for rapid determination of erythromycin in milk[J].Foods, 2023, 12(8):1581.
[25] SHEN X, CHEN J H, LV S W, et al.Fluorescence polarization immunoassay for determination of enrofloxacin in pork liver and chicken[J].Molecules, 2019, 24(24):4462.
[26] DUAN C F, ZHANG Y J, LI P P, et al.Dual-wavelength fluorescence polarization immunoassay for simultaneous detection of sulfonamides and antibacterial synergists in milk[J].Biosensors, 2022, 12(11):1053.
[27] LU N, CHEN J T, RAO Z K, et al.Recent advances of biosensors for detection of multiple antibiotics[J].Biosensors, 2023, 13(9):850.
[28] MADEJ M, KNIHNICKI P, PORADA R, et al.(bio)Electroanalysis of tetracyclines:Recent developments[J].Biosensors, 2025, 15(2):101.
[29] ADANE W D, CHANDRAVANSHI B S, TESSEMA M.A novel electrochemical sensor for the detection of metronidazole residues in food samples[J].Chemosphere, 2024, 359:142279.
[30] FU Y C, XIE Y, SHI H Z, et al.Molecularly imprinted electrochemical sensor based on metal-covalent organic framework for specifically recognizing norfloxacin from unpretreated milk[J].Food Chemistry, 2023, 429:136921.
[31] DING L Y, WANG P, XIAO B Q, et al.A novel sensing probe based on AuNPs-Apt for the detection of enrofloxacin[J].Nanotechnology, 2025, 36(4):045501.
[32] ZHENG A L T, TEO E Y L, YIU P H, et al.Recent advances in ultrasensitive electrochemical sensors and biosensors for determination of antibiotics in environment samples[J].Clean Technologies and Environmental Policy, 2025, 27(2):549-576.
[33] YANG Y K, YANG L Q, MA Y Y, et al.A novel metal-organic frameworks composite-based label-free point-of-care quartz crystal microbalance aptasensing platform for tetracycline detection[J].Food Chemistry, 2022, 392:133302.
[34] MUNAWAR A, SCHIRHAGL R, REHMAN A, et al.Facile in situ generation of bismuth tungstate nanosheet-multiwalled carbon nanotube composite as unconventional affinity material for quartz crystal microbalance detection of antibiotics[J].Journal of Hazardous Materials, 2019, 373:50-59.
[35] SHAHEEN A, IDREES F, BUTT F K, et al.Synthesis and integration of sea urchin-like MnO2-GCN nanocomposite with imprinted polymers for mass-sensitive detection of chloramphenicol in water[J].Composites Communications, 2025, 56:102357.
[36] 李方束, 张瑞婷, 程赞, 等.基于精准识别的农兽药残留快速检测技术研究进展[J].食品科学, 2025, 46(6):330-343.LI F S, ZHANG R T, CHENG Z, et al.Recent advances in rapid detection technologies based on precise recognition for pesticide and veterinary drug residues[J].Food Science, 2025, 46(6):330-343.
[37] FAN R Q, TANG S S, LUO S L, et al.Duplex surface enhanced Raman scattering-based lateral flow immunosensor for the low-level detection of antibiotic residues in milk[J].Molecules, 2020, 25(22):5249.
[38] BI S Y, YUAN Y, ZHANG F M, et al.A sensitive surface-enhanced Raman spectroscopy detection for gentamicin and tobramycin using γ-Al2O3-modified silver nanoparticles coated with bovine serum albumin as substrate[J].Talanta, 2023, 260:124635.
[39] YANG Z W, ZHU A F, ADADE S Y S, et al.Ag@Au core-shell nanoparticle-based surface-enhanced Raman scattering coupled with chemometrics for rapid determination of chloramphenicol residue in fish[J].Food Chemistry, 2024, 438:138026.
[40] ÇELIK O, SAYLAN Y, GÖKTÜRK I, et al.A surface plasmon resonance sensor with synthetic receptors decorated on graphene oxide for selective detection of benzylpenicillin[J].Talanta, 2023, 253:123939.
[41] BAKHSHPOUR-YÜCEL M, KÜÇÜK M, TÜMAY ÖZER E, et al.Nano-MIP based SPR sensor for tetracycline analysis in milk sample[J].Talanta Open, 2025, 11:100417.
[42] XU Q, YIN H T, ZHAO Z, et al.An Au-Ag@Au fiber surface plasmon resonance sensor for highly sensitive detection of fluoroquinolone residues[J].Analyst, 2025, 150(5):877-886.
[43] TAN J S, CHEN Y Y, HE J, et al.Two-dimensional material-enhanced surface plasmon resonance for antibiotic sensing[J].Journal of Hazardous Materials, 2023, 455:131644.
[44] CHEN T, CHENG G Y, AHMED S, et al.New methodologies in screening of antibiotic residues in animal-derived foods:Biosensors[J].Talanta, 2017, 175:435-442.
[45] ÉCIJA-ARENAS  , KIRCHNER E M, HIRSCH T, et al.Development of an aptamer-based SPR-biosensor for the determination of kanamycin residues in foods[J].Analytica Chimica Acta, 2021, 1169:338631.
, KIRCHNER E M, HIRSCH T, et al.Development of an aptamer-based SPR-biosensor for the determination of kanamycin residues in foods[J].Analytica Chimica Acta, 2021, 1169:338631.
[46] KIM D Y, SHARMA S K, RASOOL K, et al.Development of novel peptide-modified silver nanoparticle-based rapid biosensors for detecting aminoglycoside antibiotics[J].Journal of Agricultural and Food Chemistry, 2023, 71(34):12883-12898.
[47] WANG H Q, LIU X F, ZOU L Y, et al.Polymer-assisted Au@PDA nanoparticles lyophilized powder with high stability and low adsorption and its application in colorimetric biosensing[J].Analytica Chimica Acta, 2022, 1220:339995.
[48] SUN M, BAI X, FU X S, et al.Modification of Fe3O4 magnetic nanoparticles for antibiotic detection[J].Scientific Reports, 2025, 15:4751.
[49] YUE F L, HU M J, BAI M Y, et al.An exonuclease III-driven dual-mode aptasensor based on Au-Pd@Fc nanozyme and magnetic separation pretreatment for aminoglycoside antibiotics detection[J].Food Chemistry, 2024, 460:140480.
[50] CHENG C, HAN M, XIANG G, et al.Bimetallic iron-copper nanozyme for determination and degradation of norfloxacin in foods[J].Food Chemistry, 2024, 444:138667.
[51] ZOU W Y, WANG J J, YANG S Y, et al.Porous-nanozyme-based colorimetric sensor for rapid detection of kanamycin in foods under neutral condition[J].Journal of Food Science, 2023, 88(5):2009-2022.
[52] HOU L Q, WEI J Y, XIANG C, et al.A colorimetric sensor for the sensitive and rapid detection of ampicillin based on CS-Cu, Fe/HS nanozyme[J].Mikrochimica Acta, 2024, 192(1):36.
[53] WANG S J, WANG Y B, NING Y N, et al.Multicolor emissive carbon dot-based fluorometric analysis platform for rapid quantification and discrimination of nitroimidazole antibiotic residues[J].Talanta, 2024, 271:125679.
[54] SUN Y X, BAI X, LUO A P, et al.Ratiometric fluorescent sensor CQDx@Co/Mn-MOF for rapid and sensitive detection of quinolone antibiotics[J].Talanta, 2025, 293:128034.
[55] WANG C Y, WANG C C, ZHANG X W, et al.A new Eu-MOF for ratiometrically fluorescent detection toward quinolone antibiotics and selective detection toward tetracycline antibiotics[J].Chinese Chemical Letters, 2022, 33(3):1353-1357.