随着消费者对安全、健康和高质量食品的需求不断增加,食品包装材料与技术持续革新[1]。然而,当前超过90%的塑料包装基材源自不可再生的石油衍生物[2],其难以降解的特性导致了严重的环境污染问题[3]。根据国际自然保护联盟的数据,全球每年生产超过460万t塑料,塑料污染已成为威胁生态系统和人类健康的重大挑战。
为了应对这一挑战,全球开展可持续发展战略,中国通过在城市试点的“塑料极限顺序、零废物城市”和“海洋凋落物清洁行动”等创新举措[4],展现了国家层面对环境治理的重视和对发展绿色替代材料的迫切需求。在此背景下,开发环保、可降解的新型包装材料已成为科学研究的热点之一。生物基材料因其生物降解性、无毒性、低成本和易获取性等优势,展现出广阔的应用潜力。生物基材料,特别是基于蛋白质的材料,因其固有的生物降解性、无毒性、资源可再生性以及相对较低的成本等优势,展现出巨大的应用潜力,如图1所示,蛋白基薄膜的原料主要来源于植物蛋白和动物蛋白[5]。蛋白质是由氨基酸通过肽键连接而成的高分子聚合物,其分子间丰富的相互作用力(如离子键、氢键、二硫键、疏水作用)赋予了所成薄膜优异的氧气阻隔性能、良好的延展性和弹性,这些特性使得蛋白基薄膜能有效保护食品免受物理损伤、环境污染和质量退化[6-7],进而在食品包装、医药载体和组织工程等众多领域具备了广阔的应用前景。本文聚焦于蛋白基薄膜的研究进展,系统梳理了其原料来源、制备方法及应用领域,并深入分析了该领域所面临的挑战与未来发展方向,旨在为相关研究提供有益的参考和启发。
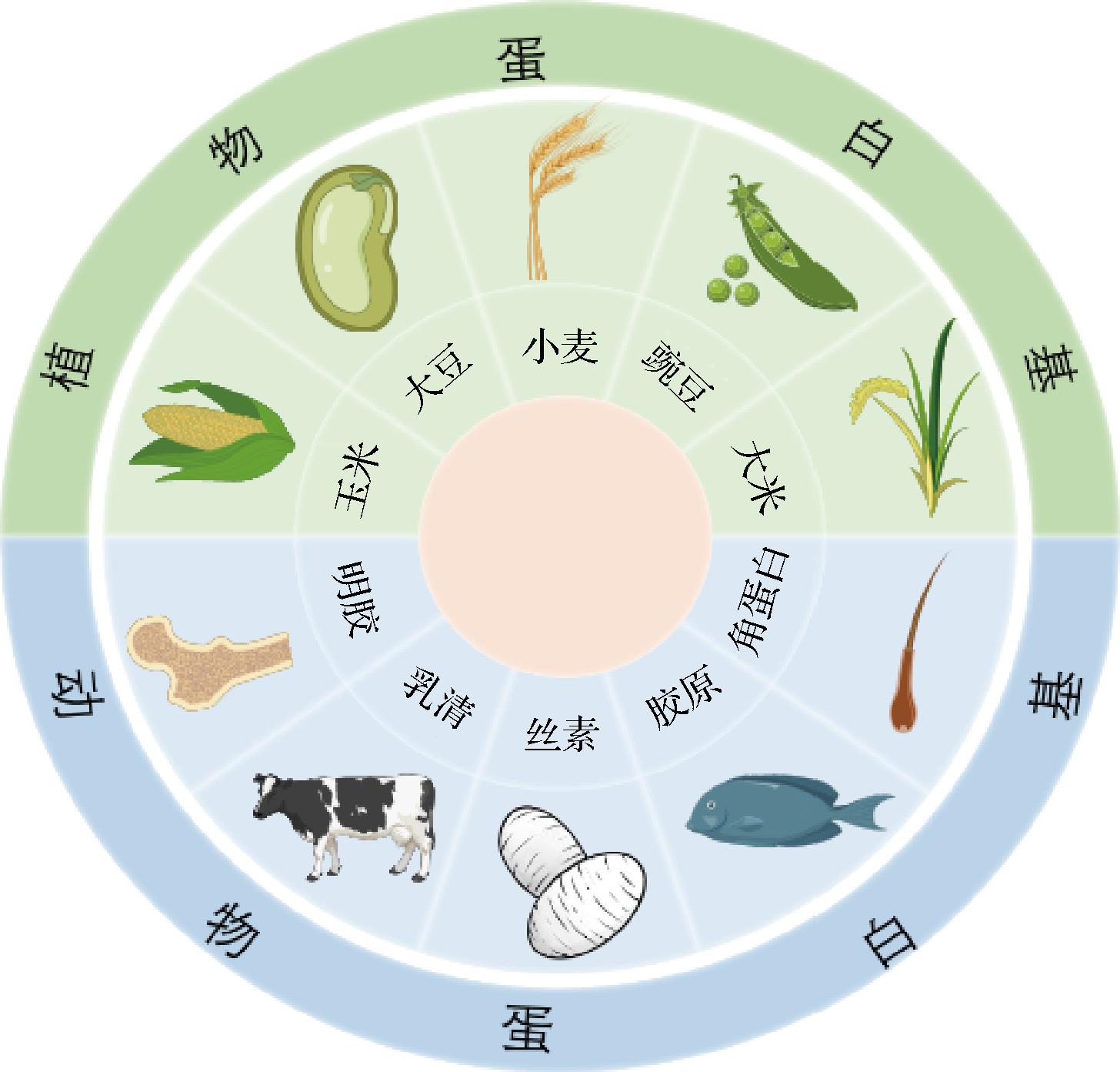
图1 蛋白基薄膜的主要来源
Fig.1 Sources of protein-based films
1 蛋白基薄膜原料的来源
1.1 明胶
明胶是胶原蛋白部分水解产生的生物聚合物,主要从肉类产品加工的副产品(如动物皮、肌腱和软骨)中提取[8],通过酸或碱的预处理,胶原蛋白的不溶性形式转化为可溶性形式,导致胶原链失去三股螺旋排列,从而在水中溶胀,水溶胀的胶原蛋白通过加热破坏了氢键和共价键,使得螺旋结构转变为卷曲结构进而得到明胶[9],I
 K等[10]将鸡皮明胶采用脱脂预处理后,依次经0.5 mol/L NaOH溶液碱处理(2 h)去除杂蛋白、0.9 mol/L HCl溶液酸处理(4 h, 25 ℃)打开胶原链,最后通过加热得到明胶。明胶因其优异的凝胶特性和可塑性,在食品包装领域得到了广泛应用[11]。尽管明胶基薄膜具有良好的成膜性能和生物相容性,但其在食品包装中的应用仍面临一些挑战,尤其是机械性能以及对水蒸气的阻隔性能较差。为解决这一问题,研究人员通过多种改性方法优化明胶薄膜的性能,拓展其应用范围,王浩等[12]以明胶(45 g/L)、海藻酸钠(5 g/L)和羧化壳聚糖(10 g/L)制备的三元共混薄膜中,三者混合形成大量氢键,使薄膜结构致密,从而显著降低水蒸气透过率,并保持较低含水量(19.51%)和溶解度(32.79%),具备作为食品内包装材料的潜力。
K等[10]将鸡皮明胶采用脱脂预处理后,依次经0.5 mol/L NaOH溶液碱处理(2 h)去除杂蛋白、0.9 mol/L HCl溶液酸处理(4 h, 25 ℃)打开胶原链,最后通过加热得到明胶。明胶因其优异的凝胶特性和可塑性,在食品包装领域得到了广泛应用[11]。尽管明胶基薄膜具有良好的成膜性能和生物相容性,但其在食品包装中的应用仍面临一些挑战,尤其是机械性能以及对水蒸气的阻隔性能较差。为解决这一问题,研究人员通过多种改性方法优化明胶薄膜的性能,拓展其应用范围,王浩等[12]以明胶(45 g/L)、海藻酸钠(5 g/L)和羧化壳聚糖(10 g/L)制备的三元共混薄膜中,三者混合形成大量氢键,使薄膜结构致密,从而显著降低水蒸气透过率,并保持较低含水量(19.51%)和溶解度(32.79%),具备作为食品内包装材料的潜力。
1.2 胶原蛋白(collagen, COL)
COL作为关键的功能性蛋白之一,在动物体内含量极高,主要存在于皮肤、肌腱和骨骼等组织和器官中[13],KAEWBANGKERD等[14]利用超声辅助提取肉鸡气管中的胶原蛋白;LI等[15]采用酸酶结合法在低温下从鱼鳔和牛跟腱中提取胶原蛋白。胶原蛋白具有独特的三重螺旋结构,由3条α链相互交织而成,赋予了胶原蛋白卓越的弹性和机械强度。这种结构特性使得胶原蛋白在不同组织中能够承受外部应力,同时维持组织的完整性和灵活性,帮助生物体在承受压力时恢复结构稳定性和功能完整性[16]。TEWELDE等[17]以亚麻籽多糖(flaxseed mucilage, FSM)为基础的生物膜,通过不同比例的弹性蛋白(elastin, ELN)胶原蛋白基质制备而成,FSM与ELN/COL之间发生了氢键和静电相互作用,与FSM膜相比,复合膜断裂伸长率从91.4%提高到188.6%,改善了FSM-ELN/COL生物膜的机械性,因此在食品包装和涂层方面具有潜在的应用前景。
1.3 丝素蛋白(fibroin, SF)
SF是一种由家蚕生产的天然高分子材料,丝素蛋白的生产流程基本上由脱胶、提取、透析、离心分离等过程组成[18],蚕丝脱胶是制备再生丝素蛋白的基础,研究人员不断致力于改进脱胶工艺,这通常需要试剂和有机溶剂才能获得更高质量的纯SF。KUMAR DAN等[19]通过从刺槐中分离的生物表面活性剂皂苷作为脱胶剂,研究了一种可持续、清洁且环境前景良好的桑蚕丝纤维蛋白提取技术;牛佳杰等[20]提出以Na2CO3和表面活性剂(十二烷基磺酸钠)的复合体系为脱胶剂,再结合超声处理的一体化天然蚕丝脱胶方案。丝素纤维经过脱胶处理后可以溶解在高浓度的盐溶液中,从而制成再生丝素蛋白溶液,这种溶液可以被加工成多种形式,如薄膜、粉末、水凝胶、纤维和多孔基质等[21]。丝素蛋白是一种具有优良生物相容性和可降解性的天然高分子材料,它所具备的低炎症反应以及促进感染伤口愈合的特性,使其在生物医学领域中获得了广泛的应用。
1.4 乳清分离蛋白(whey protein isolate, WPI)
WPI是通过乳清蛋白进一步加工而成的一种混合球状蛋白[22],主要由β-乳清白蛋白、α-乳清白蛋白、免疫球蛋白和牛血清白蛋白以及其他次要蛋白质构成,具有极高的营养价值[23]。此外,乳清分离蛋白还表现出良好的凝胶性、成膜性和氧气阻隔性能。然而,纯乳清分离蛋白膜因其亲水性质而导致薄膜的低机械性和高水蒸气渗透性能[24]。为了克服这些缺点,乳清蛋白常与其他大分子材料结合,实现不同材料性能的优势互补。DENG等[25]通过物理变性研究了不同变性程度的乳清分离蛋白、甘油和木质素制备的可生物降解薄膜的性能,发现在90 ℃下,WPI变性(蛋白质变性率为88.65%)引起的巯基暴露,促进了热交联和新分子间二硫键的形成,增强了薄膜基质的机械和屏障性能。
1.5 大豆分离蛋白(soybean protein isolate, SPI)
SPI是大豆油产业的一种副产品,主要由球蛋白组成,因其丰富的来源、良好的成膜性能和生物相容性而被广泛应用于食品工业[26]。然而,SPI的疏水中心含有大量疏水性氨基酸残基,使其在水溶液中形成疏水性内核和亲水性外壳的球状结构,导致由其制备而成的膜材料对水敏感,限制了应用范围[27]。为克服这一缺点,研究人员通过改变蛋白质分子的空间结构或与其他物质复配来提升其性能。胡文瑾等[28]利用无籽刺梨纳米纤维素(rosa sterilis cellulose-nanocrystalline cellulose,RSC-NCC)改善SPI薄膜性能,根据薄膜的扫描电镜图发现,SPI膜截面具有较多的裂纹,而RSC-NCC截面裂纹较少,这是由于RSC-NCC与蛋白质之间形成了致密、稳定和有序的网络结构,因此阻碍了水蒸汽和气体透过,RSC-NCC/SPI复合膜的水蒸气透过率、CO2透过率和氧气透过率比SPI膜分别降低了11.04%、5.63%和42.79%。大豆分离蛋白薄膜作为一种可再生、可降解且成本较低的材料,具有较高的市场潜力,但纯大豆分离蛋白薄膜的机械强度和韧性较差,耐水性较弱,在性能优化和大规模生产技术上仍需进一步突破。
1.6 玉米醇溶蛋白(Zein)
Zein作为一种天然高分子材料,因其独特的性能而备受关注,成为材料科学领域的研究热点[29]。它富含疏水性氨基酸(如谷氨酸和亮氨酸),但缺乏碱性和酸性氨基酸(特别是色氨酸和赖氨酸),这种氨基酸组成使玉米醇溶蛋白分子能够通过强二硫键和疏水键紧密连接,从而赋予膜材料良好的机械性能和阻隔特性[30]。然而,纯玉米醇溶蛋白膜存在着延展性差、易断裂等问题,限制了其在实际应用中的广泛使用。为解决这一问题,研究人员进行了多种改性尝试,TADELE等[31]以不同脂肪酸氯化物(六酰氯、十二酰氯和棕榈酰氯)对Zein进行了酯化,以改善其膜的形成和理化性能,其中十烷基氯改性Zein样品的拉伸强度比未改性的样品提高了500%。可见通过与其他可生物降解聚合物的结合,其机械强度和耐水性得到了显著提升,为可持续食品包装解决方案提供了广阔的应用前景。
1.7 豌豆分离蛋白(pea protein isolate, PPI)
PPI作为一种丰富的植物蛋白,在食品工业中备受青睐,这得益于其高产量、良好的成本效益以及易获取等优势[32]。豌豆蛋白被认为是一种低风险的过敏原,不仅具有平衡的氨基酸组成,还具备良好的分散性、稳定性、成膜性和凝胶特性[33]。PPI为球形结构,分子间交联度低,导致PPI薄膜的拉伸强度和疏水性较低,GAO等[34]用湿磨处理的PPI,并由湿磨PPI制备蛋白质膜,湿磨10 min后PPI的α-螺旋和β-转角分别增加到12.07%和31.37%,同时,色氨酸残留物暴露,这些变化增强了蛋白质之间和蛋白质-甘油的相互作用,因此所制备的薄膜接触角从56.48°至72.37°;拉伸强度由1.20 MPa提高至2.72 MPa;断裂伸长率由74.9%提高至166.8%,显著提升豌豆分离蛋白膜的机械性能。豌豆的种植需水量低且能固氮,生产碳排放比传统塑料低,可成为替代传统塑料的热门选择。
1.8 其他蛋白质
除了以上几种蛋白基材料以外,人们还从各种农副产品中提取出各种蛋白基材料,促进了生物基材料的发展,表1简要概括了几种生物基蛋白薄膜,以及它们的主要研究内容。
表1 蛋白基薄膜及主要研究内容
Table 1 Protein-based films and associated research focuses

蛋白基质研究内容参考文献面筋/麦谷蛋白评估不同酚类化合物存在对所得薄膜的物理化学、抗氧化和抗菌性能的影响[35]米糠蛋白探究不同pH条件下处理米糠蛋白对薄膜性能的影响[36]明胶/酪蛋白探究没食子酸对薄膜的热稳定性以及薄膜的表面特性的影响[37]羽扇豆分离蛋白探究氧化蔗糖对羽扇豆分离蛋白流延膜选定功能特性的影响[38]大米蛋白掺入不同纤维素纳米晶体和迷迭香提取物,探究对薄膜物理性能的影响[39]燕麦蛋白将天然燕麦蛋白改性后与羧甲基纤维素钠共同制备复合膜[40]茶多酚/卵白蛋白将茶多酚与卵白蛋白进行复合,加入壳聚糖制备茶多酚-卵白蛋白可食膜液应用于猪肉保鲜[41]花生分离蛋白利用静电纺丝技术制备负载茶多酚的花生分离蛋白-聚乳酸复合纳米纤维薄膜[42]
2 蛋白基薄膜的制备方法
蛋白基薄膜的制备涉及原料选择与处理、成膜工艺和改性技术3个核心环节。其中,原料选择是制备高性能薄膜的基础,原料需经过溶解和脱气等预处理,以制备均匀的成膜溶液。成膜工艺是决定薄膜结构和性能的关键,常用的方法包括溶液浇铸法、挤出法、静电纺丝法和3D打印法等。
2.1 溶液浇铸法
溶液浇铸法是制备薄膜最常用的方法之一[43]。如图2所示,其基本流程为:首先将生物基材料溶解于适当的溶剂中形成溶液,随后加入增塑剂(通常为甘油,用于增加薄膜的柔韧性),然后将制备好的薄膜溶液倒入模具中并进行干燥,最终得到薄膜。符建宁等[44]将丁香酚封装在金属有机框架IRMOF-3中,并将其与Zein基膜共混,通过溶液浇铸法制备了一种多功能包装膜,不仅具有良好的紫外线阻隔性能、抗氧化和抑菌性能,而且对丁香酚具有缓释的性能。ZAREIE等[45]通过溶液浇铸法制备了不同壳聚糖浓度的γ-氨基丁酸发酵大豆蛋白生物复合可食用薄膜;HADAVIFAR等[46]利用紫壳开心果提取副产物碳点和紫壳开心果花青素,通过溶液浇铸法与壳聚糖/大豆蛋白共混制备分离膜。溶液浇铸法制备过程相对简单、成本较低、操作条件宽松,且设备需求简单等优点,适合大规模生产。该方法可在大气环境及室温下进行,无需特殊环境条件。然而,溶液浇铸法也存在一些局限性,制备薄膜厚度的均匀性和精确控制能力较弱,容易受到基底材质和溶液性质的影响;其次,溶液浇铸法的成膜效率较低,尤其是在长时间干燥过程中,聚合物可能发生再结晶,从而影响薄膜的质量。综上所述,溶液浇铸法是一种低成本、工艺简单的薄膜制备技术,但在薄膜厚度精确控制、溶剂挥发性和成膜效率方面仍面临挑战。
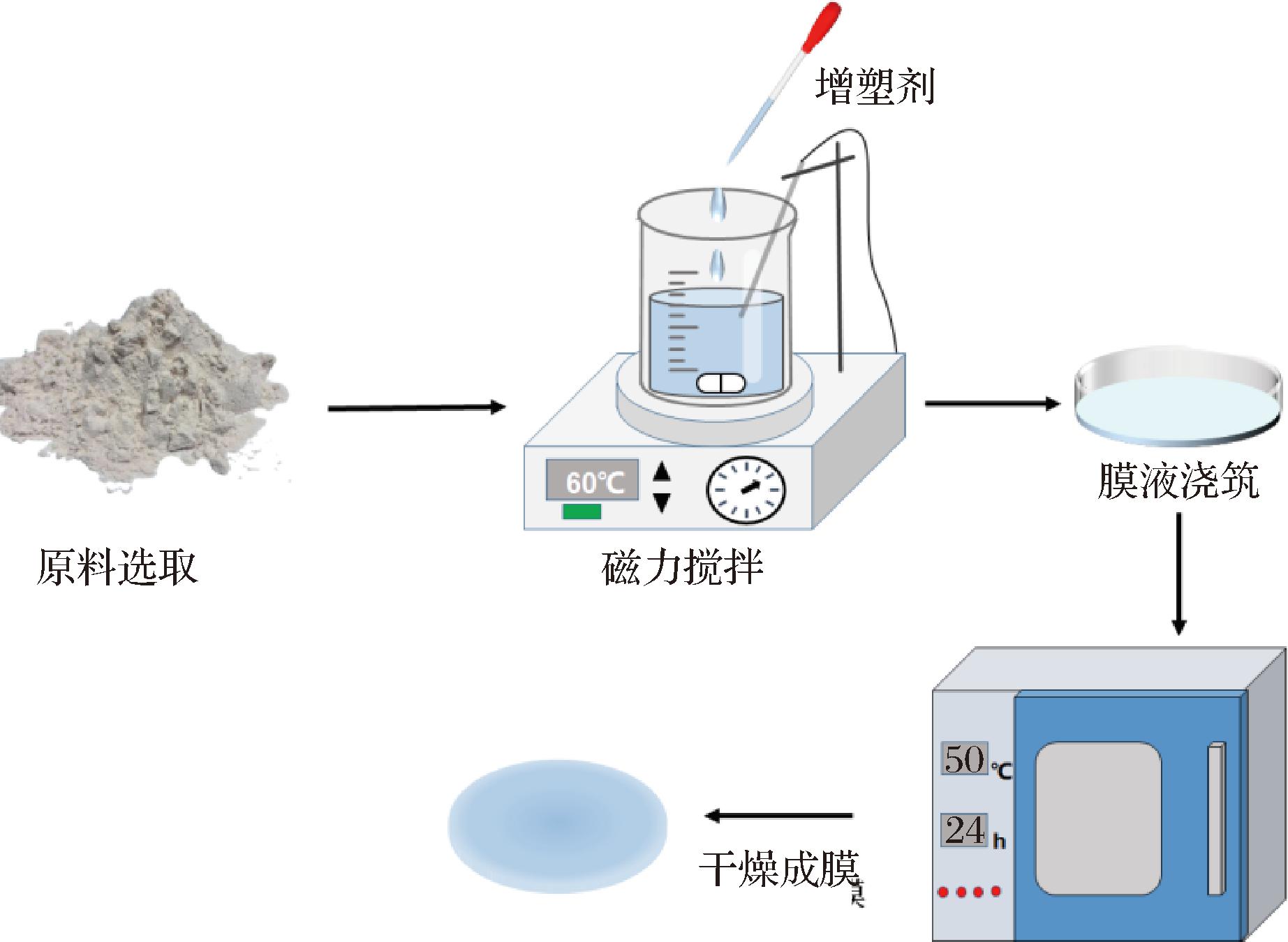
图2 溶液浇铸法制备薄膜的主要流程
Fig.2 Main steps in film preparation using solution casting
为突破上述瓶颈,未来研究可聚焦以下方向:采用低共熔溶剂(如氯化胆碱/甘油)等绿色溶剂来替代传统有毒溶剂,降低挥发性及毒性,实现薄膜制备的可持续发展。其次可以通过优化溶剂浇铸过程中的参数控制,进一步提高薄膜的均匀性以及成膜效率,如采用梯度干燥方法,分阶段调控温度、湿度或压力参数的智能干燥工艺,通过动态适配物料脱水过程中的物性变化,优化干燥效率与品质;开发真空-红外协同干燥体系,利用低压环境降低溶剂沸点,结合红外辐射精准供热,加速溶剂挥发,抑制结构变形与结晶风险;以及可以结合使用手术刀刮涂、狭缝涂布或结合高频振动辅助浇铸等方法实现对薄膜厚度的精准把控。
2.2 挤出法
挤出法是生产塑料薄膜的常用技术,相较于溶液浇铸法,它能更快速地制备薄膜并去除水分。其挤出过程中如图3所示,材料在挤出机中被加热,通过螺杆的推动形成连续的条带、薄片或管道,随后经过冷却、凝固和切割等步骤完成薄膜的制备。挤出法的优点在于其高效的连续生产能力、广泛的材料适用性以及较低的成本,特别适合大规模生产[47]。近年来,挤出法在生物基薄膜制备中得到了广泛应用。MASANABO等[48]通过挤出法制备了热塑性玉米淀粉-麦谷蛋白复合薄膜;YUAN等[49]则以虾壳废料蛋白和壳聚糖为基质,添加乌龙茶提取物、玉米须提取物和黑豆种皮提取物,通过挤出法开发出具有抗氧化和紫外线阻隔功能的可降解活性包装薄膜;HUNTRAKUL等[50]利用常规吹膜挤出法,将乙酰化木薯淀粉与豌豆分离蛋白混合,制备出可食用、可生物降解的包装薄膜。尽管挤出法具有高生产效率、成本低和环境友好等优点,但其在产品形状多样性、尺寸精度和设备成本方面仍存在一定的局限性。
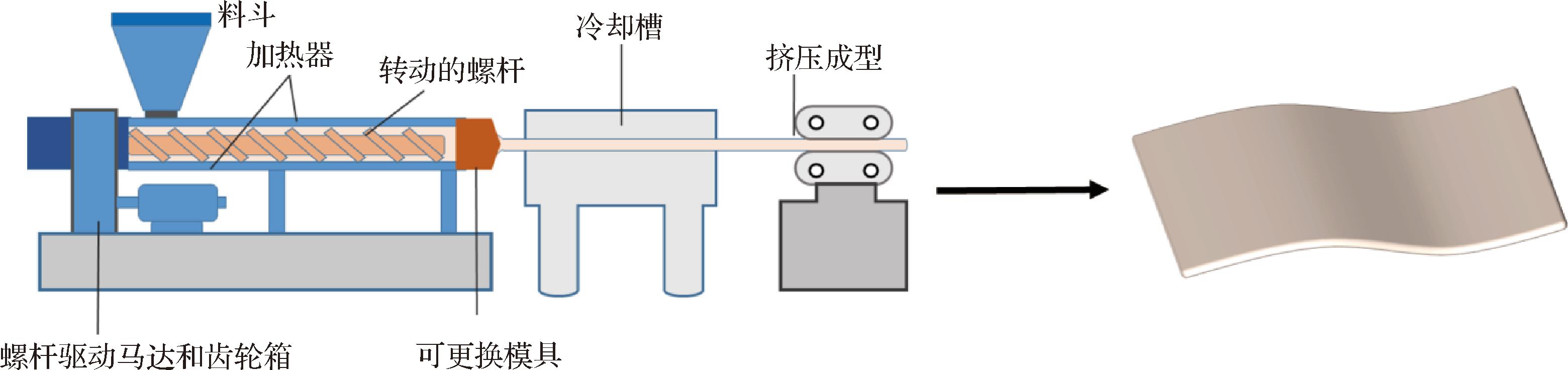
图3 利用挤压法制备薄膜
Fig.3 Thin film preparation using extrusion method
未来可以通过建立精确的温度和压力控制系统,实时监测和调整,确保热敏性蛋白基材料在加工过程中的稳定性控制,提高薄膜的均匀性和稳定性;设计微纳压印模具,实现抗菌/疏水等功能性表面图案薄膜的制备;开发可变径吹膜模头,支持立式袋、收缩膜等多形态包装的连续化生产;通过增加模具的流道设计,实现多层共挤薄膜,可使不同材料在挤出过程中更好地融合,提高薄膜的机械性能。
2.3 静电纺丝法
应用静电纺丝技术开发多功能性纳米纤维膜已成为食品包装保鲜发展的趋势,它不仅使膜材料附加值增高,也使膜材料的结构与功能产生进一步的变化。静电纺丝技术是液滴在静电场的作用下形成喷射,随着电场的作用力,溶液从针头喷出并拉长,形成细纤维(图4)。最终,这些细纤维被收集在接收板或其他接收装置上,形成一层纳米纤维膜[51]。在静电纺丝制备生物质食品包装膜的过程中,生物活性化合物可以均匀分布于聚合物纤维中,显著提升膜材料的性能。LIU等[52]利用静电纺丝技术将明胶、壳聚糖和3-苯基乳酸(phenyllactic acid, PLA)复合,制备出抗菌纳米纤维薄膜;WU等[53]采用静电纺丝技术制备了明胶/玉米蛋白纳米纤维薄膜,并负载肉桂醛和百里香酚,显著提升了薄膜的抗菌性能,并在草莓保鲜中表现出巨大潜力。此外,研究者还通过静电纺丝层层组装技术开发多层复合纤维膜,VALIZADEH等[54]以鼠尾草籽胶-明胶薄膜为外层,静电纺丝玉米醇溶蛋白-石榴花提取物为中间层,制备出生物基多层薄膜,随着中间层厚度的增加,薄膜的水溶性、水分含量和溶胀率降低,抗菌活性显著增强。JIANG等[55]通过静电纺丝层层组装技术将玉米醇溶蛋白-小麦面筋蛋白复合纤维膜与壳聚糖-明胶-百里香酚复合纤维膜进行物理组装,制备出双层复合纤维膜。静电纺丝技术生产的纳米纤维膜具有高比表面积,适用于催化、过滤等领域。其多孔结构有利于物质的吸附和扩散,在药物释放和传感器领域也有广泛应用。
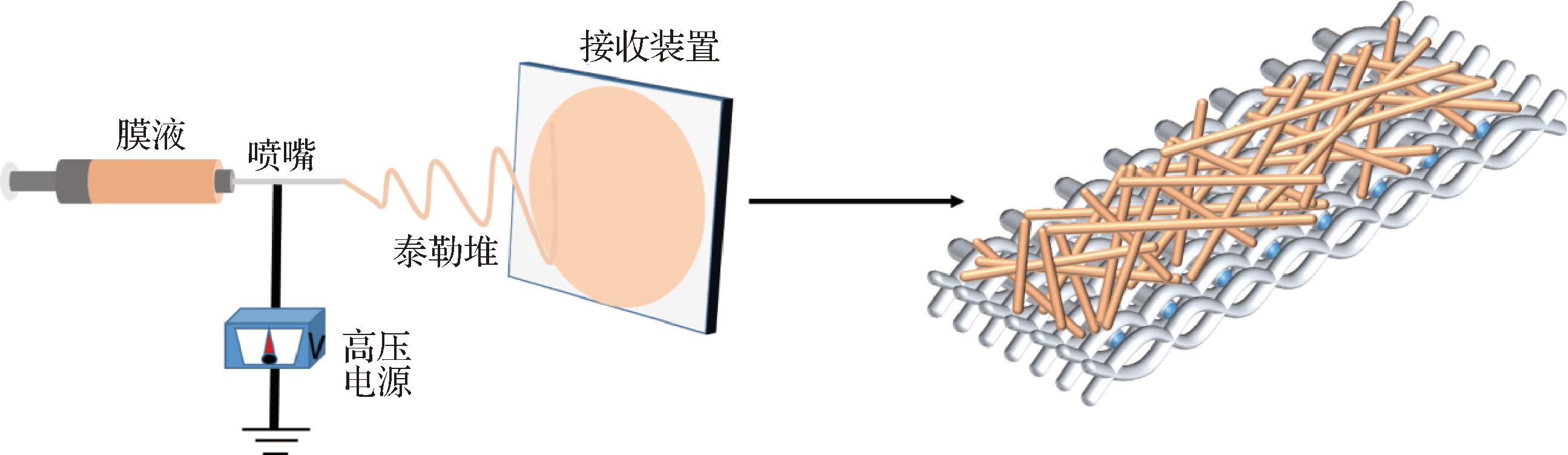
图4 利用静电纺丝技术制备薄膜
Fig.4 Fabrication of protein-based films via electrospinning
尽管电纺技术在功能性包装中的应用具有广泛的发展前景,但仍有一些挑战需要面对并引起更多关注和研究。开发绿色溶剂或无溶剂电纺对于更安全和可持续的静电纺丝至关重要,例如水基或生物来源的替代品,通过减少毒性和环境影响提供了环保选项;另一个挑战是一些天然聚合物不能直接电纺成纳米纤维,应加大对生物基材料的研究和应用,如一些可再生的天然高分子材料如纤维素、壳聚糖等;最重要的是,大多数研究仍处于实验室阶段,后续发展必须集中在高产量和工业化上,可以应用普通的多喷头电纺或无喷头电纺结合卷对卷收集系统,能够在广泛区域内连续制造纳米纤维,实现可扩展、高效和可靠的纳米纤维生产,满足各种工业应用的需求。
2.4 3D打印法
三维(3D)打印是一种新兴的制造技术,近年来在电池[56]、汽车[57]和医疗[58]等多个领域展现出巨大的应用潜力,它是一种基于计算机辅助设计模型的快速成型技术,通过“分层打印、逐层叠加”方式构建物体(图5),也被称为增材制造技术。与传统的溶液浇铸法相比,3D打印不仅能更快地构建薄膜,还能根据设计精确控制薄膜的形状、结构和孔隙率,从而优化活性化合物的释放,实现其最大利用率[59]。LEAW等[60]通过3D打印玉米淀粉-明胶可食用膜,优化了薄膜的物理、机械和抗菌性能;YAP等[61]利用甘油和藤黄提取物开发了3D打印明胶可食用薄膜,该薄膜具有低抗拉强度和高断裂伸长率的特点。此外,3D打印技术还被用于制备多层次薄膜,CHEN等[62]利用3D打印技术成功制备了一种双层活性膜,其中包含明胶-聚乙烯醇-碳点层和玉米淀粉-聚乙烯醇-肉桂精油层,这种薄膜不仅具有外部屏障功能,还能实现内部控释效果。3D打印技术在薄膜制备中展现了巨大的潜力,薄膜制备提供了结构创新与功能集成的新维度,尤其在定制化、功能集成和快速原型制作方面具有显著优势。
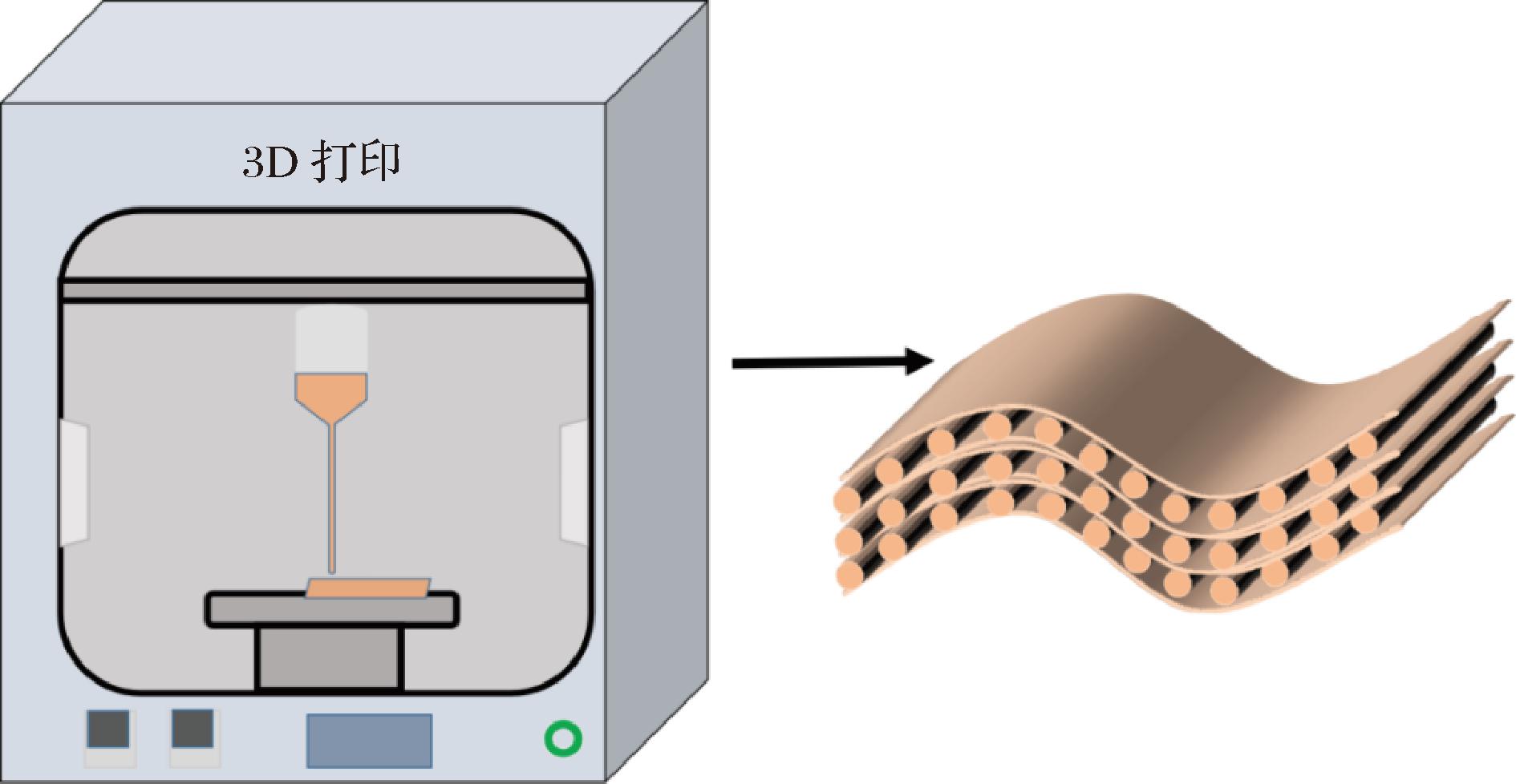
图5 利用3D打印法制备薄膜
Fig.5 Film fabrication via 3D printing
3D打印技术潜在的功能性墨水和基底种类广泛,目前符合食品行业监管标准的墨水选择有限,未来应继续促进可持续无毒、生物相容和可生物降解新墨水的开发;由于3D打印技术易于生产复杂的形状和结构,可以用来制备传感器、指示器和标签融入常规食品包装中,以创建安全且经济实惠的智能食品包装;与此同时,在提高打印可控性和打印效率方面可以采用多角度摄像头监控和多喷头系统,大大提高了生产效率,减少人工参与,并通过研发连续化卷对卷3D打印平台,突破单件生产效率瓶颈,让3D打印技术从实验室走向工业化。
2.5 蛋白基薄膜的改性技术
蛋白基薄膜作为一种绿色环保、可降解的材料,具有良好的生物相容性、可食用性、机械性能和气体阻隔性,然而,普遍蛋白基薄膜其水溶性、吸湿性、热稳定性差、机械强度不足等缺点。研究者们除了将蛋白基与其他物质复配以改善蛋白基薄膜的缺点外,还常采用各种改性技术提升蛋白基薄膜的性能。物理改性方法包括热处理、紫外辐照和高压均质化处理等,可以显著提升薄膜的机械性能和热稳定性。WANG等[63]研究了欧姆加热和传统加热对SPI薄膜的影响,经研究发现欧姆加热的SPI膜的机械性能和防水性能优于传统加热的SPI膜;CAO等[64]采用高压均质化处理SPI,处理后薄膜的接触角和吸水能力增加,表明薄膜疏水性增强,高压力处理导致薄膜不透明且呈黄色,从而减少了紫外线透过率;DE VARGAS等[65]通过紫外线处理明胶基薄膜,经紫外线处理2 h后显著降低了薄膜水溶性,且经紫外线暴露时间最长的薄膜,拉伸强度从1.56 MPa(对照)增加到2.85 MPa。化学改性方法如交联和接枝等,也被广泛用于改善薄膜的稳定性和功能特性。JIANG等[66]利用转谷氨酰胺酶对乳清浓缩蛋白和蛋清蛋白复合膜进行改性,显著提升了复合膜的机械强度、透光度和保鲜性能,成功延长了樱桃番茄的货架期;KIM等[67]通过诱导β-折叠结构的转变和引入共价键方法,有效控制了丝素蛋白膜的物理化学特性,获得了卓越的机械性能;ABDALRAZEQ等[68]利用微生物转谷氨酰胺酶对热变性乳清蛋白进行生物化学改性,酶促修饰将薄膜断裂伸长率从(10.4±4.9) MPa提高到(27.6±8.9) MPa,同时降低了拉伸强度和杨氏模量,从而使所得薄膜更具延展性。
单一改性方法往往难以同时解决蛋白膜的多项缺陷(如同时提升强度、阻水性和热稳定性),应深入研究物理、化学、生物等不同改性技术的协同效应与机制,建立“多技术联用”的优化策略,实现薄膜综合性能的协同跃升;未来研究应超越静态性能提升,致力于开发对湿度、温度、pH值或对功能物质具有持续缓释作用的智能响应蛋白基薄膜,以期利用改性技术将农业废弃物材料制成可堆肥和快速降解的包装,遵循零废物原则,让其变废为宝。
3 蛋白基薄膜的应用
3.1 蛋白基薄膜在食品包装中的应用
蛋白基薄膜凭借其出色的阻氧性能和可降解性,成为食品包装行业的热门选择。它们可用于新鲜果蔬、肉类、坚果等多种食品的包装,有效延长食品的货架期,减少浪费;还可以通过添加抗菌剂、抗氧化剂等功能性成分,开发出具有保鲜功能的活性包装材料。如一种pH响应性胶原蛋白纳米复合膜用来监测虾的新鲜度,该膜采用咖啡酸功能化修饰二维锂藻土纳米片,增强胶原蛋白与纳米片之间的相互作用,并利用姜黄素分子在碱性条件下的去质子化特性将其负载于纳米片表面,赋予薄膜抗氧化能力与pH响应功能,如图6所示,贮藏5 d后,虾显示出明显的变质迹象,相应地,薄膜指示标签的颜色逐渐从亮黄色变为红棕色,表明指示膜的pH值升高至碱性[69];GUO等[70]用酪蛋白和海藻酸钠作为底物的铸造方法,制备了含有沙门氏菌噬菌体SaTp-04的酪蛋白-海藻酸钠薄膜,该膜可使生鸡胸肉表面的沙门氏菌减少约6 lg CFU/cm2。此外,研究者通过将大球盖菇废料提取多糖与碳点作为活性物质掺入明胶基质,制备了具有增强阻隔性、机械性能、抗氧化及抗菌活性的生物基复合薄膜,其中,含3%碳点的复合膜对大肠杆菌和金黄色葡萄球菌的抑菌率分别为58.37%与70.25%[71]。WANG等[72]制备了含蓝莓花青素的大豆分离蛋白基可食用复合膜,蓝莓花青素能够均匀分布并与基体形成氢键,有效的增强了薄膜的机械性能,蓝莓花青素已被证明具有强大的清除自由基的能力,可以显著增强了薄膜的抗氧化特性。因此,这种薄膜在保鲜应用中可以很好地减缓蘑菇的新陈代谢。CHEN等[73]采用一种创新的方法,以丙烯酰胺/结冷胶复合水凝胶为内层结构,以豌豆蛋白/壳聚糖复合体系为外层结构,开发了一种具有pH敏感性和保鲜功能的双层水凝胶薄膜。
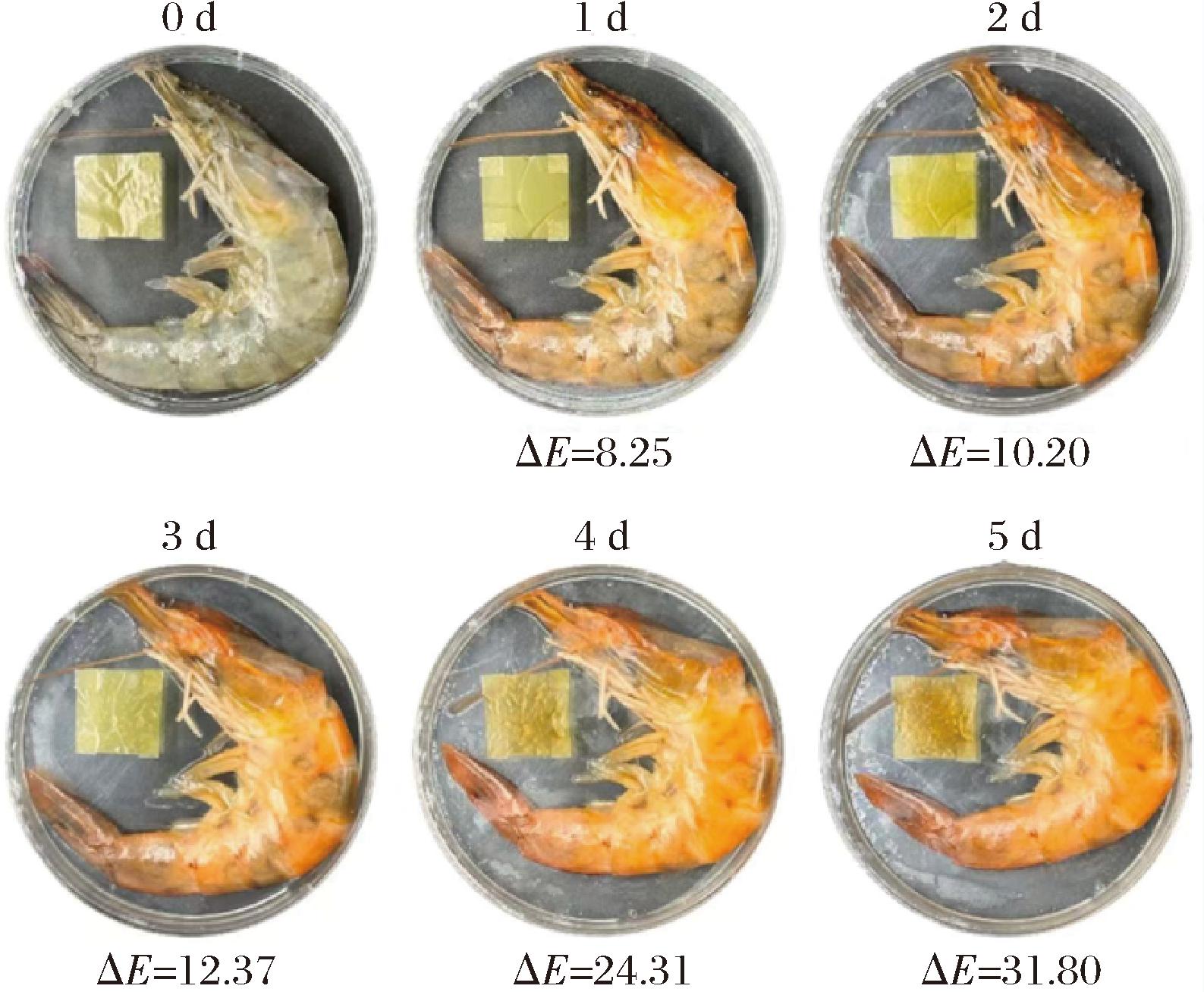
图6 pH响应性COL纳米复合膜在监测虾新鲜度中的应用
Fig.6 pH-responsive COL nanocomposite film for monitoring shrimp freshness
3.2 蛋白基薄膜在医药卫生中的应用
蛋白基薄膜因其良好的生物相容性和可控降解性,在医药领域被广泛应用于药物载体、伤口敷料和组织工程支架等方面。研究者通过将Mg2+掺入再生丝素蛋白(recycled silk fibroin protein, RSF)溶液中,开发出RSF/Mg2+复合膜(图7),复合薄膜具有优异的生物相容性,细胞毒性最小,溶血率低,并具有显著的抗氧化活性,有效抑制炎症环境中的细胞凋亡和氧化应激,有助于创造更有利的愈合微环境,在小鼠皮肤缺损模型中,RSF/Mg2+薄膜加速了伤口愈合,增强了表皮再生,改善了胶原沉积,并刺激了血管形成,突出了它们作为先进伤口敷料的潜力[74]。BYRAM等[75]利用甲酸将SF和丝胶蛋白(silk sericin, SS)混合,制备了具有抗菌活性和细胞兼容性的SF/SS薄膜,可以作为皮肤再生应用的生物材料候选者。SHAKOOR等[76]利用藻酸盐和鹰嘴豆蛋白作为基质,封装姜黄素,实现了在胃部pH值下的缓慢控释,为口服姜黄素提供了有效途径。XU等[77]通过调节WPI与海藻酸钠的比例,制备了负载白藜芦醇的口服速溶膜,改善了白藜芦醇的溶解性,展示了乳清蛋白在药物载体方面的潜力。
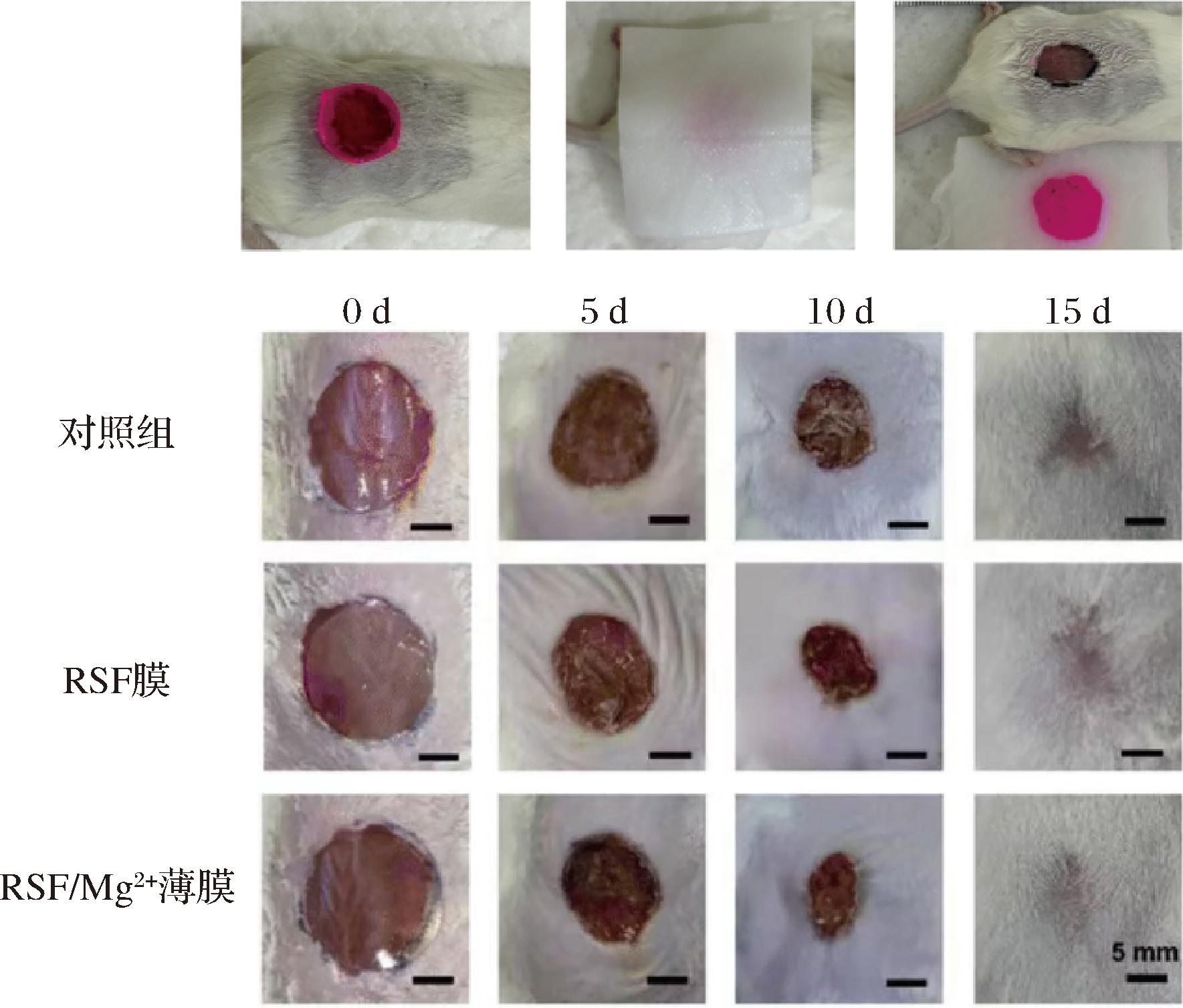
图7 再生丝素蛋白/镁离子薄膜在老鼠伤口敷料中应用
Fig.7 Application of RSF/Mg2+ film in rat wound dressing
3.3 蛋白基薄膜在环境保护中的应用
蛋白基薄膜可作为传统塑料薄膜的替代品,用于农业覆盖膜、可降解包装袋等产品,有效减少白色污染。通过功能化改性,还可开发出具有吸附重金属离子、降解有机污染物等功能的环境修复材料。如图8所示,研究者采用一种绿色无毒的方案,将SPI、壳聚糖、石墨烯、铁离子和植酸复合,制备出一种高灵敏度、阻燃且可降解的薄膜传感器,用于环境监测,其在68.1~194.3 ℃宽温域内响应/恢复时间为2.6 s/4.3 s,对火灾的3 s快速响应与145 s持续报警能力,为环保型火灾安全传感提供了新策略[78]。羽毛等废弃物的再利用也为蛋白基薄膜的开发提供了新思路,OCAK等[79]利用皮革修边和鸡毛废料提取的COL水解物和角蛋白,与壳聚糖复合,开发出可生物降解的三元薄膜,提高了废弃物的利用率。WEI等[80]通过将表面羟基化的高介电常数无机填料BaTiO3(HBT)作为散布的纳米颗粒嵌入到可生物降解的SPI基底中,制备了一系列基于SPI的纳米复合材料薄膜,这种薄膜具有高韧性、导电性、万次循环稳定性及可以在PBS环境降解性,其构建的穿戴传感器可无排斥监测人体关节运动,为绿色柔性电子提供新范式。综上所述,蛋白基薄膜凭借其多功能性和可持续性,在食品包装、医药卫生和环境保护等多个领域展现出巨大的应用潜力,为解决传统材料的局限性提供了新的思路和解决方案。
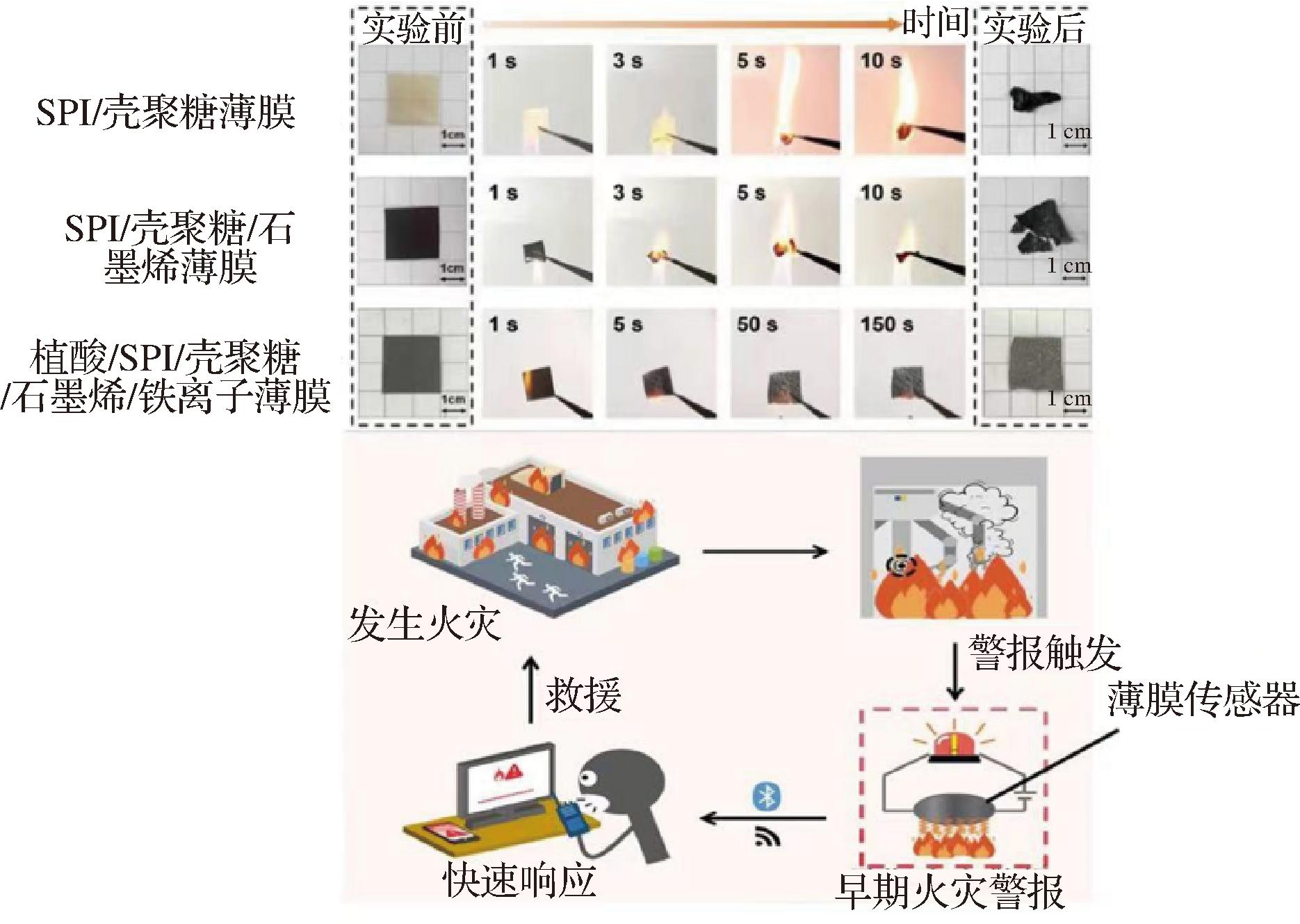
图8 植酸/SPI/壳聚糖/石墨烯/铁离子薄膜作为温度传感器中的应用
Fig.8 Application of phytic acid, SPI, chitosan, graphene, and ions film as a temperature sensor
4 结论
包装是防止物质外部环境污染的屏障。蛋白基薄膜作为一种环保且可降解的新型材料,在食品包装、医药卫生和环境保护等多个领域展现出广阔的应用前景。它利用蛋白质的生物活性和降解性来实现食品保护、延长保质期和环境保护等多个目标。近年来,通过持续优化其制备工艺和改性技术,蛋白基薄膜的性能得到了显著提升,为其实际应用提供了坚实基础。然而,该领域仍面临诸多挑战,例如如何进一步提高机械性能、降低生产成本以及实现规模化生产等问题亟待解决。
展望未来,随着材料科学、生物技术和纳米技术的不断进步,蛋白基薄膜的研究将朝着多功能化、智能化和绿色化方向迈进。通过开发新型蛋白质原料、优化复合改性技术以及探索先进的制备工艺,有望开发出性能更优异、功能更多样的蛋白基薄膜材料。同时,加强产学研合作,加速蛋白基薄膜的产业化进程,对于推动可持续发展目标的实现具有重要的现实意义。
[1] RAMAKANTH D, SINGH S, MAJI P K, et al.Advanced packaging for distribution and storage of COVID-19 vaccines:A review[J].Environmental Chemistry Letters, 2021, 19(5):3597-3608.
[2] PUSCASELU R, GUTT G, AMARIEI S.Rethinking the future of food packaging:Biobased edible films for powdered food and drinks[J].Molecules, 2019, 24(17):3136.
[3] RIBEIRO I S, MACIEL G M, BORTOLINI D G, et al.Sustainable innovations in edible films and coatings:An overview[J].Trends in Food Science &Technology, 2024, 143:104272.
[4] ZHOU X, XU B H.The SWOT analysis of China’s strategy for addressing marine plastic pollution in the context of global plastic treaty negotiations[J].Marine Pollution Bulletin, 2025, 213:117653.
[5] JIANG S, LI H Q, ZHANG L, et al.Generic Diagramming Platform (GDP):A comprehensive database of high-quality biomedical graphics[J].Nucleic Acids Research, 2025, 53(D1):D1670-D1676.
[6] TKACZEWSKA J.Peptides and protein hydrolysates as food preservatives and bioactive components of edible films and coatings-A review[J].Trends in Food Science &Technology, 2020, 106:298-311.
[7] JAFARZADEH S, JAFARI S M, SALEHABADI A, et al.Biodegradable green packaging with antimicrobial functions based on the bioactive compounds from tropical plants and their by-products[J].Trends in Food Science &Technology, 2020, 100:262-277.
[8] JANOWICZ M, GALUS S, SZULC K, et al.Investigation of the structure-forming potential of protein components in the reformulation of the composition of edible films[J].Materials, 2024, 17(4):937.
[9] FENG X, LIU T W, MA L, et al.A green extraction method for gelatin and its molecular mechanism[J].Food Hydrocolloids, 2022, 124:107344.
[10] I
 K Ç, PARLAK M E, K
K Ç, PARLAK M E, K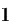 RAÇ DEMIREL F T, et al.Gelatin extraction from chicken skin by conventional and Ohmic heating methods and comparison with commercial halal gelatins[J].Food Hydrocolloids, 2024, 150:109694.
RAÇ DEMIREL F T, et al.Gelatin extraction from chicken skin by conventional and Ohmic heating methods and comparison with commercial halal gelatins[J].Food Hydrocolloids, 2024, 150:109694.
[11] LU Y N, LUO Q J, CHU Y C, et al.Application of gelatin in food packaging:A review[J].Polymers, 2022, 14(3):436.
[12] 王浩, 沙小梅, 李鑫, 等.鱼明胶基可食抗菌膜的制备及性能研究[J].食品与发酵工业, 2024, 50(21):175-182.WANG H, SHA X M, LI X, et al.Preparation and performance of fish gelatin-based edible antibacterial film[J].Food and Fermentation Industries, 2024, 50(21):175-182.
[13] GISBERT V G, BENAGLIA S, UHLIG M R, et al.High-speed nanomechanical mapping of the early stages of collagen growth by bimodal force microscopy[J].ACS Nano, 2021, 15(1):1850-1857.
[14] KAEWBANGKERD K, HAMZEH A, YONGSAWATDIGUL J.Ultrasound-assisted extraction of collagen from broiler chicken trachea and its biochemical characterization[J].Ultrasonics Sonochemistry, 2023, 95:106372.
[15] LI Y L, TIAN Y X, XIONG X, et al.Comparison of collagens extracted from swim bladder and bovine Achilles tendon[J].Materials Research Express, 2023, 10(5):055403.
[16] MILANI J M, TIRGARIAN B.An overview of edible protein-based packaging:Main sources, advantages, drawbacks, recent progressions and food applications[J].Journal of Packaging Technology and Research, 2020, 4(1):103-115.
[17] TEWELDE HAILU G, LEMESSA F, TESFAYE ALEMEA M.Development and characterization of flaxseed mucilage and elastin/collagen biofilms[J].Heliyon, 2024, 10(15):e35396.
[18] Y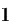 LD
LD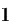 Z A, MUTLU
Z A, MUTLU ![]() N B, ACARTÜRK F.Evaluation of the effect of process parameters on the protein content of silk fibroin[J].Polymer Bulletin, 2023, 80(12):13181-13198.
N B, ACARTÜRK F.Evaluation of the effect of process parameters on the protein content of silk fibroin[J].Polymer Bulletin, 2023, 80(12):13181-13198.
[19] KUMAR DAN A, BISWAL B, DAS M, et al.Aqueous and chemical extraction of saponin of Acacia concinna (Willd.) dc:An effective bio-surfactant solution to extract silk fibroin from muga silk cocoons[J].Journal of Molecular Liquids, 2022, 360:119547.
[20] 牛佳杰, 寿万, 刘雍.超声协同SDS-Na2CO3提取丝素蛋白及高强韧纳米纤维膜的制备与细胞相容性研究[J].东华大学学报(自然科学版), 2024, 50(4):148-155.NIU J J, SHOU W, LIU Y.Ultrasonic co-extraction of silk fibroin with SDS-Na2CO3 and preparation/cytocompatibility of high-strength and tough nanofiber membranes[J].Journal of Donghua University(Natural Science), 2024, 50(4):148-155.
[21] WU X, WU X D, SHAO M, et al.Structural changes of Bombyx mori fibroin from silk gland to fiber as evidenced by Terahertz spectroscopy and other methods[J].International Journal of Biological Macromolecules, 2017, 102:1202-1210.
[22] KOH J, XU Z M, WICKER L.Blueberry pectin and increased anthocyanins stability under in vitro digestion[J].Food Chemistry, 2020, 302:125343.
[23] YIN X, WUSIGALE,CHENG H, et al.The mechanism of resveratrol stabilization and degradation by synergistic interactions between constituent proteins of whey protein[J].Food Research International, 2024, 188:114485.
[24] SUKYAI P, ANONGJANYA P, BUNYAHWUTHAKUL N, et al.Effect of cellulose nanocrystals from sugarcane bagasse on whey protein isolate-based films[J].Food Research International, 2018, 107:528-535.
[25] DENG Y H, KOLODJSKI S, LEWIS G, et al.Physical and functional characterization of whey protein-lignin biocomposite films for food packaging applications[J].Future Foods, 2025, 11:100554.
[26] XIE W Y, SONG F, WANG X L, et al.Development of copper phosphate nanoflowers on soy protein toward a superhydrophobic and self-cleaning film[J].ACS Sustainable Chemistry &Engineering, 2017, 5(1):869-875.
[27] LI D Z, LI X J, WU G C, et al.The characterization and stability of the soy protein isolate/1-Octacosanol nano complex[J].Food Chemistry, 2019, 297:124766.
[28] 胡文瑾, 陈相雨, 孙雪, 等.无籽刺梨纳米纤维特性及其对大豆分离蛋白膜性能的影响[J].食品与发酵工业, 2023, 49(6):105-110.HU W J, CHEN X Y, SUN X, et al.Properties of the nanocellulose from Rosa sterilis cellulose and their effects on properties of the soybean protein isolate film[J].Food and Fermentation Industries, 2023, 49(6):105-110.
[29] GAGLIARDI A, VOCI S, SALVATICI M C, et al.Brij-stabilized zein nanoparticles as potential drug carriers[J].Colloids and Surfaces B:Biointerfaces, 2021, 201:111647.
[30] ZHANG Y Y, XU M J, ZHANG X R, et al.Application of zein in gluten-free foods:A comprehensive review[J].Food Research International, 2022, 160:111722.
[31] TADELE D T, SHOREY R, MEKONNEN T H.Fatty acid modified zein films:Effect of fatty acid chain length on the processability and thermomechanical properties of modified zein films[J].Industrial Crops and Products, 2023, 192:116028.
[32] LU Z X, HE J F, ZHANG Y C, et al.Composition, physicochemical properties of pea protein and its application in functional foods[J].Critical Reviews in Food Science and Nutrition, 2020, 60(15):2593-2605.
[33] GE J, SUN C X, CORKE H, et al.The health benefits, functional properties, modifications, and applications of pea (Pisum sativum L.) protein:Current status, challenges, and perspectives[J].Comprehensive Reviews in Food Science and Food Safety, 2020, 19(4):1835-1876.
[34] GAO X P, DAI Y Y, CAO J, et al.Analysis of the effect mechanism of wet grinding on the film properties of pea protein isolate based on its structure changes[J].Innovative Food Science &Emerging Technologies, 2023, 89:103474.
[35] LIU X Y, XIE Y R, LI C, et al.Comparative studies on physicochemical properties of gluten-and glutenin-based films functionalized by polyphenols[J].Cereal Chemistry, 2022, 99(3):640-651.
[36] WANG N, SALEH A S M, GAO Y Z, et al.Effect of protein aggregates on properties and structure of rice bran protein-based film at different pH[J].Journal of Food Science and Technology, 2019, 56(11):5116-5127.
[37] BHATIA S, AL-HARRASI A, AL-AZRI M S, et al.Gallic acid crosslinked gelatin and casein based composite films for food packaging applications[J].Polymers, 2022, 14(19):4065.
[38] MAIDL M, ENGLBERGER H, ABBASNIA A, et al.Impact of oxidized sucrose as a bio-based crosslinker on thermoformable films made from lupin protein isolate (Lupinus angustifolius L.)[J].Journal of Applied Polymer Science, 2024, 141(42):e56109.
[39] LI J S, QIN X L, LIU X, et al.Enhanced mechanical, barrier and antioxidant properties of rice protein/sodium alginate-based films by incorporating cellulose nanocrystals and rosemary extract[J].Food Packaging and Shelf Life, 2022, 34:101000.
[40] 王亮亮, 韩苗苗, 曹崇江, 等.燕麦蛋白淀粉样聚集体-羧甲基纤维素钠复合膜的制备及性能[J].食品工业科技, 2025, 46(3):110-119.WANG L L, HAN M M, CAO C J, et al.Preparation and properties of oat protein amyloid aggregate-sodium carboxymethyl cellulose composite film[J].Science and Technology of Food Industry, 2025, 46(3):110-119.
[41] 杨乐, 刘丽莉, 丁玥, 等.茶多酚-卵白蛋白可食膜对冷鲜猪肉品质的影响及微生物生长模型的构建[J].食品与发酵工业, 2025, 51(6):103-111.YANG L, LIU L L, DING Y, et al.Effect of tea polyphenol-ovalbumin edible film on quality of chilled pork and construction of microbial growth model[J].Food and Fermentation Industries, 2025, 51(6):103-111.
[42] 姚飞, 陈复生, 郝明飞.负载茶多酚的花生分离蛋白-聚乳酸纳米纤维膜的制备及抗菌性能研究[J].食品工业科技, 2021, 42(13):247-252.YAO F, CHEN F S, HAO M F.Preparation and antibacterial properties of peanut protein isolate-polylactic acid nanofiber membrane loaded with tea polyphenols[J].Science and Technology of Food Industry, 2021, 42(13):247-252.
[43] BASTANTE C C, SILVA N H C S, CARDOSO L C, et al.Biobased films of nanocellulose and mango leaf extract for active food packaging:Supercritical impregnation versus solvent casting[J].Food Hydrocolloids, 2021, 117:106709.
[44] 符建宁, 韩昕苑, 贾白云, 等.玉米醇溶蛋白/丁香酚/IRMOF-3复合抗菌膜的制备与表征[J].食品与发酵工业, 2025, 51(8):203-210.FU J N, HAN X Y, JIA B Y, et al.Development and characterization of zein/eugenol/IRMOF-3 composite antimicrobial film[J].Food and Fermentation Industries, 2025, 51(8):203-210.
[45] ZAREIE Z, TABATABAEI YAZDI F, ALI MORTAZAVI S.Development and characterization of antioxidant and antimicrobial edible films based on chitosan and gamma-aminobutyric acid-rich fermented soy protein[J].Carbohydrate Polymers, 2020, 244:116491.
[46] HADAVIFAR S, ABEDI-FIROOZJAH R, BAHRAMIAN B, et al.Multifunctional performance of chitosan/soy protein isolation-based films impregnated carbon dots/anthocyanin derived from purple hull pistachio for tracking and extending the shelf life of fish[J].Food Hydrocolloids, 2025, 159:110678.
[47] MANGARAJ S, YADAV A, BAL L M, et al.Application of biodegradable polymers in food packaging industry:A comprehensive review[J].Journal of Packaging Technology and Research, 2019, 3(1):77-96.
[48] MASANABO M A, RAY S S, EMMAMBUX M N.Properties of thermoplastic maize starch-zein composite films prepared by extrusion process under alkaline conditions[J].International Journal of Biological Macromolecules, 2022, 208:443-452.
[49] YUAN G Q, JIA Y N, PAN Y X, et al.Preparation and characterization of shrimp shell waste protein-based films modified with oolong tea, corn silk and black soybean seed coat extracts[J].Polymer Testing, 2020, 81:106235.
[50] HUNTRAKUL K, YOKSAN R, SANE A, et al.Effects of pea protein on properties of cassava starch edible films produced by blown-film extrusion for oil packaging[J].Food Packaging and Shelf Life, 2020, 24:100480.
[51] XUE J J, WU T, DAI Y Q, et al.Electrospinning and electrospun nanofibers:Methods, materials, and applications[J].Chemical Reviews, 2019, 119(8):5298-5415.
[52] LIU Y N, WANG D B, SUN Z L, et al.Preparation and characterization of gelatin/chitosan/3-phenylacetic acid food-packaging nanofiber antibacterial films by electrospinning[J].International Journal of Biological Macromolecules, 2021, 169:161-170.
[53] WU X, LIU Z, HE S, et al.Development of an edible food packaging gelatin/zein based nanofiber film for the shelf-life extension of strawberries[J].Food Chemistry, 2023, 426:136652.
[54] VALIZADEH R, ZANDI M, GANJLOO A, et al.Bioactive multilayer film based on the sage seed gum-gelatin, TiO2 and electrospun zein fibers encapsulating pomegranate peel extract[J].International Journal of Biological Macromolecules, 2024, 283:137826.
[55] JIANG J, LIU Z Q, WANG Z M, et al.Physicochemical properties of protein-polysaccharide-polyphenol bilayer composite film prepared by electrospinning layer-by-layer assembly technology[J].Food Packaging and Shelf Life, 2025, 47:101441.
[56] MOTTAGHI M, PEARCE J M.A review of 3D printing batteries[J].Batteries, 2024, 10(3):110.
[57] DE SOUZA GONÇALVES P A, DE SOUSA G S BARROSO C, DE OLIVEIRA D M, et al.Transforming automotive polypropylene components into 3D printing filaments[J].Polymer Engineering &Science, 2025, 65(3):1166-1174.
[58] VERNON M J, MELA P, DILLEY R J, et al.3D printing of heart valves[J].Trends in Biotechnology, 2024, 42(5):612-630.
[59] GUO C F, ZHANG M, BHANDARI B.Model building and slicing in food 3D printing processes:A review[J].Comprehensive Reviews in Food Science and Food Safety, 2019, 18(4):1052-1069.
[60] LEAW Z E, KONG I, PUI L P.3D printed corn starch-gelatin film with glycerol and hawthorn berry (Crataegus pinnatifida) extract[J].Journal of Food Processing and Preservation, 2021, 45(9):e15752.
[61] YAP K L, KONG I, ABDUL KALAM SALEENA L, et al.3D printed gelatin film with Garcinia atroviridis extract[J].Journal of Food Science and Technology, 2022, 59(11):4341-4351.
[62] CHEN K, ZHANG M, BHANDARI B, et al.3D printed cinnamon essential oil/banana peel carbon dots loaded corn starch/gelatin bilayer film with enhanced functionality for food packaging application[J].Food Chemistry, 2024, 448:139176.
[63] WANG X, WANG W N, HU X H, et al.Structural and physical properties of soybean protein isolate films with ohmic heating treatment:Impacts of electric field[J].Innovative Food Science &Emerging Technologies, 2022, 82:103213.
[64] CAO Z, WANG H T, FENG T, et al.Advancing soy protein isolate-ulvan film physicochemical properties and antioxidant activities through strategic high-pressure homogenization technique[J].Industrial Crops and Products, 2024, 215:118704.
[65] DE VARGAS V H, MARCZAK L D F, FL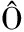 RES S H, et al.Morphology and functional properties of gelatin-based films modified by UV radiation and bacterial cellulose nanofibers[J].Journal of Food Process Engineering, 2023, 46(9):e14399.
RES S H, et al.Morphology and functional properties of gelatin-based films modified by UV radiation and bacterial cellulose nanofibers[J].Journal of Food Process Engineering, 2023, 46(9):e14399.
[66] JIANG S J, ZHANG J X, ZHANG M Y, et al.Characteristics of whey protein concentrate/egg white protein composite film modified by transglutaminase and its application on cherry tomatoes[J].Journal of Food Science, 2024, 89(12):9529-9542.
[67] KIM Y, YOON J, KIM J, et al.Multifunctional fructose-crosslinked fibroin film with a developed β-sheet structure for advanced food packaging[J].International Journal of Biological Macromolecules, 2025, 286:138370.
[68] ABDALRAZEQ M, AREF D, MARINIELLO L, et al.Microbial transglutaminase-mediated modification of heat-denatured whey proteins for the preparation of bio-based materials[J].Coatings, 2025, 15(1):66.
[69] SHI J B, SHENG L, CHEN M, et al.pH-responsive collagen nanocomposite films reinforced by curcumin-loaded iaponite nanoplatelets for dynamic visualization of shrimp freshness[J].Food Hydrocolloids, 2024, 157:110447.
[70] GUO P, ZHANG L, NING M G, et al.Characterization and release of caseinsodium alginate embedding phage edible film and the application in controlling of salmonella contamination in food[J].International Journal of Food Microbiology, 2025, 434:111137.
[71] WU J T, YAN Z L, SHAN P, et al.Characterization of gelatin-based composite films loaded with polysaccharide and carbon dots from Stropharia rugosoannulata and their application in pork fresh-keeping[J].International Journal of Biological Macromolecules, 2025, 297:139702.
[72] WANG X Y, GUO Y N, YUAN M, et al.Film-forming mechanism of blueberry anthocyanin-added soybean isolate protein-based biodegradable packaging film and its application in edible mushroom preservation[J].Food Packaging and Shelf Life, 2025, 49:101525.
[73] CHEN X H, JI W, NAN X J, et al.Preparation and characterization of Aronia melanocarpa/gellan gum/pea protein/chitosan bilayer films[J].Foods, 2022, 11(18):2835.
[74] CHEN Q L, WU K, YAO J R, et al.Adhesive silk fibroin/magnesium composite films and their application for removable wound dressing[J].Biomaterials Science, 2025, 13(1):287-298.
[75] BYRAM P K, MUKHERJEE M, RAHAMAN M, et al.Bioactive self-assembling silk fibroin-sericin films for skin tissue engineering[J].Biomedical Materials, 2024, 19(2):025009.
[76] SHAKOOR I F, PAMUNUWA G K, KARUNARATNE D N.Efficacy of alginate and chickpea protein polymeric matrices in encapsulating curcumin for improved stability, sustained release and bioaccessibility[J].Food Hydrocolloids for Health, 2023, 3:100119.
[77] XU Z Y, CHEN K W, KHAN M A, et al.Oral fast dissolving films made with alginate and whey protein for resveratrol delivery[J].Journal of Food Engineering, 2025, 385:112269.
[78] HAN X K, LU T Y, WANG H, et al.Phytic acid modified soy protein isolate/chitosan film:A multi-functional and degradable bio-based composite material for fire alarm sensor[J].Polymer Degradation and Stability, 2023, 216:110505.
[79] OCAK B.Collagen hydrolysate/chitosan/keratin-based ternary films from bio-wastes of the leather and poultry industries against plastic waste generation[J].Biomass Conversion and Biorefinery, 2024, 14(11):12397-12410.
[80] WEI Y Q, JIANG S C, LI X N, et al.“Green” flexible electronics:Biodegradable and mechanically strong soy protein-based nanocomposite films for human motion monitoring[J].ACS Applied Materials &Interfaces, 2021, 13(31):37617-37627.